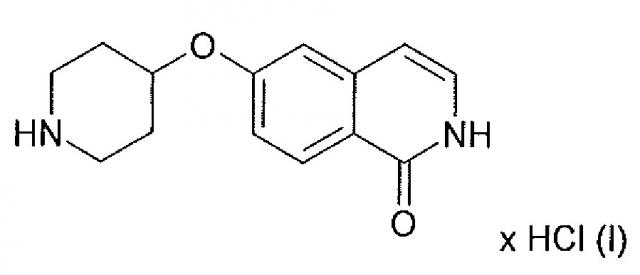
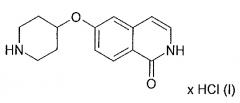
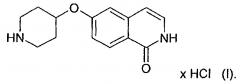
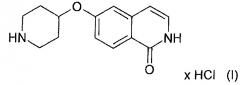
Кристаллические сольваты гидрохлорида 6-(пиперидин-4-илокси)-2н-изохинолин-1-oha
Иллюстрации
Показать всеИзобретение относится к органической химии, а именно к кристаллическому дигидрату гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она формулы (I) и твердой фармацевтической композиции на его основе. Технический результат: получен кристаллический дигидрат гидрохлорида формулы (I), обладающий лучшей стабильностью и гигроскопичностью, что предпочтительнее при получении лекарственного продукта на его основе. 3 н. и 13 з.п. ф-лы, 14 ил., 1 табл.
Реферат
Настоящее изобретение относится к новым кристаллическим сольватам гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она, к способам их получения и их применению, в частности, для приготовления лекарственных средств.
Соединение 6-(пиперидин-4-илокси)-2H-изохинолин-1-он известно в качестве фармацевтически активного соединения. 6-(Пиперидин-4-илокси)-2H-изохинолин-1-он описан в виде свободного основания в WO 2007/065916. WO2007/012421, WO2008/077550 и WO 2009/080335 описывают синтез 6-(пиперидин-4-илокси)-2H-изохинолин-1-она и его гидрохлорида, но они не содержат какие-либо данные о контролируемой, воспроизводимой процедуре кристаллизации. Описанное вещество получено только лиофилизацией.
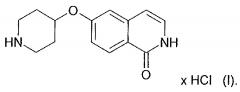
Соль хлористоводородной кислоты (HCl) 6-(пиперидин-4-илокси)-2H-изохинолин-1-она представляет собой соединение формулы (I)
.
Соединение формулы (I) может также существовать в таутомерной форме как 1-гидроксиизохинолин, и такой таутомер также является вариантом осуществления настоящего изобретения.
Сольваты являются соединениями, образованными в результате сольватации, которая представляет собой комбинацию молекул растворителя с молекулами или ионами растворенного вещества. Сольватация представляет собой взаимодействие растворенного вещества с растворителем, которое приводит к стабилизации частиц растворенного вещества в растворе. Сольватация может также относиться к сольватированному состоянию, где ион в растворе образует комплекс с молекулами растворителя. Растворитель производит растворение. Растворителями могут быть газы, жидкости или твердые вещества. Если растворителем является твердое вещество, тогда могут быть растворены газы, жидкости и твердые вещества. Примерами жидкости в твердом веществе являются, например, ртуть в золоте с образованием амальгамы. Сольваты и особенно твердые сольваты могут иметь различные и четко выраженные физические свойства, такие как различные профили растворимости, различная термодинамическая стабильность, различный режим кристаллизации, различная фильтрационная способность, различные температуры плавления и/или различные пики дифракции рентгеновских лучей. Различие в физических свойствах разных сольватов и их полиморфных форм является следствием различной ориентации и межмолекулярных взаимодействий соседних молекул в твердом веществе. Полиморфные формы соединений или сольватов можно различать по дифракции рентгеновских лучей и другими методами, такими как инфракрасная спектроскопия или рамановская спектроскопия, например.
Гидрат является сольватом, содержащим воду. Согласно изобретению термин "гидрат соединения (I)" включает все водные сольваты соединения (I), где вода присутствует в любом соотношении к соединению (I).
Однако, как признают специалисты в данной области, нельзя предугадать присутствие новых твердых сольватов известного химического соединения. Нельзя предусмотреть существование кристаллических фаз (гидраты или сольваты). Кроме того, нельзя определить условия, при которых имеет место кристаллизация для достижения конкретной формы и характеристики полиморфных форм и сольватов. Поскольку свойства, такие как растворимость и стабильность, и следовательно, пригодность к использованию и хранению каждого полиморфа и сольвата, могут изменяться, наличие существования полиморфов является важным для обеспечения фармацевтических препаратов с повышенной стабильностью при хранении или прогнозируемыми профилями растворимости.
Задача настоящего изобретения состояла в предоставлении новых твердых форм гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она (соединение (I)). В частности, задача изобретения состояла в предоставлении новых кристаллических твердых форм соединения (I). В частности, задача изобретения состояла в предоставлении новых кристаллических твердых форм соединения (I), которые имеют благоприятный профиль характеристик или являются пригодными для получения соединения. В частности, задача изобретения состояла в предоставлении новых кристаллических твердых форм соединения (I), имеющих такие благоприятные свойства, которые делают применение соединения (I) в качестве фармацевтически активного соединения более выгодным.
В частности, задача изобретения состояла в предоставлении новых кристаллических твердых форм соединения (I), имеющих благоприятные свойства относительно стабильности, растворимости, технологических свойств, гигроскопичности, текучести, фильтрационной способности или скорости кристаллизации.
Задачи изобретения были решены посредством следующих вариантов осуществления изобретения.
Один из вариантов осуществления настоящего изобретения относится к гидрату гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она. В одном из вариантов осуществления настоящего изобретения гидратом является дигидрат. Другой вариант осуществления настоящего изобретения относится к дигидрату гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она и полиморфу 2 и любой их смеси. Другой вариант осуществления настоящего изобретения относится к сольвату соединения (I) с органическим растворителем, особенно сольвату, выбранному из сольвата с метилацетатом, сольвата с 1,4-диоксаном или сольвата с ацетонитрилом.
В контексте настоящего изобретения, полиморф, полиморфная форма, сольват и т.д. всегда относится к полиморфу, полиморфной форме или сольвату гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она (I). Термины "полиморф", "форма" и "фаза" могут быть использованы в данном описании взаимозаменяемо. Безводные и свободные от растворителя формы, а также гидраты и сольваты с органическими растворителями настоящего изобретения были получены, как изложено в Примерах, представленных ниже.
Описание фигур
На фиг.1 представлена картина дифракции рентгеновских лучей дигидрата гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она, полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого высокого отражения]).
На фиг.2 представлена TGA термограмма дигидрата соединения (I).
На фиг.3 представлены DVS фазовые переходы и содержание воды как функция относительной влажности (25-40°C) дигидрата, который в течение периода сушки на начальной стадии до начала первого цикла сорбции превращался в фазу 2.
На фиг.4 представлена картина дифракции рентгеновских лучей полиморфа 2 соединения (I), полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.5 представлена картина дифракции рентгеновских лучей полиморфа 1 соединения (I), полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.6 представлена картина дифракции рентгеновских лучей полиморфа 3 соединения (I), полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.7 представлены фазовые переходы и содержание воды как функция относительной влажности при 25°C, начиная с фазы 3 (как определено из DVS и XRPD с разрешением по влажности).
На фиг.8 представлена картина дифракции рентгеновских лучей полиморфа 4 соединения (I), полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.9 представлена картина дифракции рентгеновских лучей сольвата соединения (I) с 1,4-диоксаном, полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.10 представлена картина дифракции рентгеновских лучей сольвата соединения (I) с ацетонитрилом, полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.11 представлена картина дифракции рентгеновских лучей сольвата соединения (I) с метилацетатом, полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% самого интенсивного отражения]).
На фиг.12 представлена картина дифракции рентгеновских лучей аморфной формы соединения (I), полученная в трансмиссионном режиме с CuKα1-излучением при комнатной температуре (ось x: дифракционный угол 2 тета (2θ) [°]; ось y: относительная интенсивность [% максимальной интенсивности аморфного кольца]).
На фиг.13 представлена DVS сорбция паров воды как функция относительной влажности дигидрата при 25°C.
На фиг.14 представлена DVS сорбция паров воды как функция относительной влажности аморфной формы соединения (I) при 25°C для сравнения с дигидратом.
Гидрат
Одним вариантом осуществления настоящего изобретения является кристаллический гидрат гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она (I). Другим вариантом осуществления настоящего изобретения является кристаллический гидрат соединения (I), где гидрат содержит приблизительно 10,5-12,5% воды (масс./масс). Другим вариантом осуществления настоящего изобретения является гидрат, где гидрат содержит 1,85-2,2 молекул воды на молекулу гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она (I). Другим вариантом осуществления настоящего изобретения является гидрат, где гидрат содержит 2 молекулы воды на молекулу гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она (I).
Кристаллический гидрат, содержащий 1,85-2,2 молекул воды на молекулу, в данном описании называют "дигидрат", и он является вариантом осуществления настоящего изобретения.
Другим вариантом осуществления настоящего изобретения является гидрат, содержание воды которого составляет 10,5-11,4% воды (масс./масс.). В другом варианте осуществления гидрат содержит приблизительно 1,85-2,0 молекулы воды. В другом варианте осуществления содержание воды в гидрате составляет 11,4% (масс./масс.). В другом варианте осуществления гидрат содержит 2,0 молекулы воды на молекулу (I). Хотя гидратная фаза обычно содержит приблизительно 10-12,5% воды, она может также включать более низкое содержание воды. Кристаллическая структура гидрата остается, даже если дигидрат сушат, и содержание оставшейся воды снижается до приблизительно 3%. Поглощение воды является обратимым процессом, если влажность в окружающей среде вновь увеличивается. Содержание воды в выделенном продукте зависит от условий сушки, используемых в течение обработки гидрата после кристаллизации.
В одном варианте осуществления изобретения дигидрат имеет свойство проявлять по меньшей мере характеристическое отражение рентгеновского излучения, фиксированное на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 7,7±0,2 градусах 2 тета.
В другом варианте осуществления изобретения дигидрат имеет свойство проявлять по меньшей мере характеристические отражения рентгеновского излучения, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 7,7 (сильное), 15,2 (сильное) и 16,8 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения дигидрат имеет свойство проявлять по меньшей мере характеристические отражения рентгеновского излучения, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 7,7 (сильное), 15,2 (сильное), 16,8 (среднее), 22,4 (сильное), 25,0 (сильное) и 26,6 (сильное) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения дигидрат имеет свойство проявлять по меньшей мере характеристические отражения рентгеновского излучения, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 7,7 (сильное), 15,2 (сильное), 16,8 (среднее), 18,4 (среднее), 20,4 (среднее), 22,4 (сильное), 25,0 (сильное), 26,6 (сильное) и 30,3 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения дигидрат может также характеризоваться картиной рентгеновской порошковой дифракции, по существу такой картиной, которая представлена на фиг.1, которая была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, показанные на фигуре, а также интенсивности отражений, указанные выше, не заданы заранее, а могут изменяться.
Дигидрат также может характеризоваться параметрами кристаллов, которые были определены посредством анализа монокристаллической структуры.
Было обнаружено, что дигидрат кристаллизуется в пространственной группе P-1, Z=2 с одной молекулой (I) и двумя молекулами воды в асимметричной единице. Данные измерений элементарной ячейки представлены в таблице 1.
| Таблица 1Параметры элементарной ячейки дигидрата соединения (I) при комнатной температуре | |
| Фаза | Дигидрат |
| Кристаллическая система | Триклинная |
| Пространственная группаСуммарная формула | P-1 ; Z=2C14H21ClN2O4 |
| Размеры ячейки | a=6,904 Å |
| b=9,907 Å | |
| c=12,256 Å | |
| α=107,60° | |
| β=96,70° | |
| γ=102,73° | |
| Объем ячейки V (1) | 764 Å3 |
| Плотность ρ (1) | 1,377 мг/м3 |
| (1) рассчитанный |
Молекулы воды в кристалле расположены в каналах, параллельных кристаллографической оси, и молекулы воды образуют водородные связи с анионом хлора, а также с катионом молекулы.
Дигидрат также может характеризоваться TGA-диаграммой, представленной на фиг.2. При нагревании дигидрата в сухой среде, значительная потеря массы начинается уже при слегка повышенной температуре и заканчивается при температуре приблизительно 110°C. В данном примере диаграмма показывает потерю массы 0,57 мг воды, соответствующую 10,8% масс. воды, которая означает, что данный образец потерял приблизительно 1,9 молей воды на моль соединения (I) при нагревании.
Содержание воды в дигидрате также можно определить другими способами, известными в данной области, такими как титрование по методу Карла Фишера.
Кроме того, дигидрат также может характеризоваться DVS (динамическая сорбция паров) изотермами сорбции и десорбции паров воды, измеренными при 25°C, как показано на фиг.3. До начала цикла сорбции образец дигидрата обрабатывают сухим газообразным азотом, что приводит к переходу в фазу 2, как показано посредством XRPD с разрешением по влажности. Как показано на фиг.3, изотермы сорбции и десорбции являются почти одинаковыми. В сорбционном цикле, содержание воды в образце быстро увеличивается, когда фазу 2 выдерживают в среде с относительными влажностями, составляющими значения между 1 и 20%, и содержание воды остается почти постоянным, составляющим значения между 20 и 95%. В десорбционном цикле содержание воды остается почти постоянным, когда дигидрат выдерживают в среде с относительной влажностью между 95% и 20%. Потеря массы начинается при значении относительной влажности, составляющем ниже 20%, и становится существенной при значении ниже 10%, особенно ниже 5%. Изменение массы при низкой относительной влажности полностью обращается, и, когда влажность увеличивается вновь, регидратация происходит быстро с небольшими образцами. Однако для объемных образцов регидратация сверхсухих образцов может происходить значительно дольше, и регидратация может потребовать нескольких дней. Почти идентичные изотермы сорбции и десорбции воды наблюдают при 40°C.
В зависимости от условий окружающей среды и хранения дигидрата, особенно если влажность составляет ниже приблизительно 10%, особенно ниже приблизительно 5%, дигидрат может частично или полностью трансформироваться в полиморф 2. Степень превращения зависит от влажности, размера образца и продолжительности воздействия сухой среды. Таким образом, в другом варианте, изобретение относится к дигидрату, содержащему количество полиморфа 2, составляющее диапазон от 1% до 99%, особенно диапазон от 1 до 10%. В контексте данного определения, любое количество другого полиморфа рассчитывают относительно количества дигидрата.
Анализ XRPD во влажной камере обнаруживает, что при достаточно низкой относительной влажности (2%), и когда образец почти полностью дегидратирован, происходит переход в фазу 2. Для измерения относительную влажность (r.h.) в камере вначале линейно снижают от 50% до 2% в течение 6 часов, поддерживают на уровне 2% в течение 6 часов, затем повторяют цикл дважды между 2% и 95% влажности в течение 6 часов (выдерживание образца при 95% и 2% влажности в течение 6 часов), и, наконец, повышают влажность до 50% в течение 7 часов. Обратимый переход для гидрата в фазу 2 наблюдают при 2% r.h., переход обратно в дигидрат протекает в промежутке между 8 и 10% r.h. Когда регулируемую по влажности XRPD осуществляют при 25 и 40°C, получают идентичные в значительной степени результаты.
С другой стороны, XRPD с разрешением по температуре показывает, что указанная потеря воды сопровождается или за ней следует переход к фазе 3, причем начало перехода наблюдается при приблизительно 90°C.
На основании полученных данных следует, что дигидрат является стабильным при температуре ниже 90°C и, следовательно, при комнатной температуре. Поэтому, по сравнению с другими описанными безводными полиморфами, дигидрат, в частности, является наиболее подходящим, когда желательна высокая стабильность. Он является единственным дигидратом, который может храниться при относительных влажностях, составляющих диапазон между 20 и 95% при различных температурах окружающей среды ниже 90°C, которые являются обычными условиями хранения, без риска перехода в другую описанную кристаллическую фазу. Даже если его подвергают воздействию очень сухой среды, возможная потеря воды является обратимой, и потерянная вода набирается обратно, как только соединение вновь находится в среде с обычными условиями влажности. Поэтому дигидрат является подходящим, в частности, для приготовления лекарственных средств и фармацевтических композиций с улучшенной стабильностью.
Кроме того, соответствующий аморфный материал является гигроскопичным, и содержание воды изменяется намного значительнее в зависимости от относительной влажности по сравнению с дигидратом. Это поглощение воды и вариабельность в содержании воды затрудняет точную дозировку в процессе получения лекарственного продукта. В противоположность, было доказано, что дигидрат является стабильным в течение более чем двух лет при обычных условиях хранения (не обнаруживаемое разложение при 25°C/65% относительной влажности). Таким образом, кристаллический дигидрат является предпочтительной твердой формой для получения лекарственного продукта.
Кроме того, дигидрат также может быть охарактеризован посредством его DVS (динамическая сорбция паров) изотерм сорбции и десорбции водяных паров, полученных при 25°C, как показано на фиг.13. Подобным образом, является возможным сравнение с характеристикой аморфного соединения (I) посредством его DVS (динамическая сорбция паров) изотерм сорбции и десорбции водяных паров, полученных при 25°C, показанных на фиг.14. Оказалось поразительным и неожиданным, что дигидрат принадлежит к редкому классу стехиометрических гидратов, т.е. дигидрат сохраняет довольно постоянное содержание воды, когда его подвергают воздействию относительных влажностей в широком диапазоне. Это свойство является благоприятным, например, когда активный фармацевтический ингредиент сушат после кристаллизации или взвешивают в процессе получения лекарственной формы, а также в течение хранения твердой лекарственной формы.
Как уже упоминали, аморфный материал является гигроскопичным, и содержание воды в нем доводится до относительной влажности окружающей среды (фиг.13). Стабильная (молекулярная) масса этого материала достигается только тогда, когда по стечению обстоятельств содержание воды соответствует равновесному содержанию воды при относительной влажности окружающей среды, в которой выдерживают образец. Кроме того, многие ключевые свойства аморфного материала изменяются с содержанием в нем воды, такие как подвижность молекул, скорость растворения и тенденция к переходу в другие твердые фазы. Таким образом, гигроскопичный аморфный материал следует рассматривать как неблагоприятный для пероральных твердых лекарственных форм. Неожиданным оказалось, что близкородственный дигидрат является подходящим в качестве твердого вещества для получения лекарственного продукта из-за его благоприятных свойств и стабильности.
Полиморф 2
Другой аспект настоящего изобретения относится к полиморфу 2 соединения (I), который имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при
8,1 (среднее),
15,8 (сильное) и
16,5 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом аспекте полиморф 2 имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 8,1 (среднее), 15,8 (сильное), 16,5 (среднее), 17,7 (среднее), 19,6 (среднее), 20,8 (среднее), 22,2 (среднее), 25,0 (среднее), 26,6 (среднее) и 30,5 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения полиморф 2 может также характеризоваться картиной дифракции рентгеновских лучей, по существу такой картиной, как представленная на фиг.4. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Полиморф 2 может также характеризоваться DVS сорбцией водяных паров, где он переходит в дигидрат, и изотермами десорбции, где он переходит обратно в форму 2. Для дальнейших деталей см. описание дигидрата и фиг.3.
Полиморф 2 не получается прямо при кристаллизации из раствора. Обычно он образуется при температуре окружающей среды или при 40°C в условиях воздействия на дигидрат достаточно низкой относительной влажности (предпочтительно менее чем 5%, более предпочтительно менее чем 2%), и превращается обратно в дигидрат, когда полиморф 2 подвергают воздействию увеличивающейся влажности, предпочтительно при относительной влажности выше приблизительно 10%. Соответственно, полиморф 2 является особенно пригодным в случае необходимости получения дигидрата.
В зависимости от условий окружающей среды и хранения полиморфа 2, особенно если влажность повышается выше приблизительно 10%, полиморф 2 частично или полностью превращается в дигидрат, и, таким образом, образец может содержать дигидрат в диапазоне от 0,1% до 100%.
В следующем аспекте изобретение относится к полиморфам 1, 3 и 4 соединения (I), которые отличаются от полиморфа 2, могут быть получены прямо из соединения (I), и которые затем могут быть превращены в дигидрат.
В одном аспекте три безводных полиморфа характеризуются проявлением по меньшей мере характеристических отражений, фиксированных на рентгеновской порошковой дифрактограмме с использованием CuKα1-излучения, при
1) 15,4 градусах 2 тета и в любом из диапазонов, выбранных из
2) 16,6-16,8 и
3) 21,5-21,7 градусов 2 тета ± 0,2 градуса 2 тета.
Полиморф 1
Другой аспект настоящего изобретения относится к полиморфу 1 гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она, который имеет по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме (XRPD) при использовании CuKα1-излучения, при
4,5 (среднее),
15,4 (сильное),
16,8 (сильное),
21,7 (среднее) и
24,7 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом аспекте полиморф 1 имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 4,5 (среднее), 15,4 (сильное), 16,8 (сильное), 19,8 (слабое), 21,7 (среднее), 22,5 (сильное), 22,8 (сильное), 24,7 (среднее) и 27,3 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения полиморф 1 может также характеризоваться картиной дифракции рентгеновских лучей, такой как картина, представленная на фиг.5. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Полиморф 1 может также характеризоваться параметрами плавления, такими как температура плавления, определенная посредством DSC. При нагревании фаза 1 начинает плавиться приблизительно при 300°C с предшествующим и сопровождающим химическим разложением. Никакого превращения в другую кристаллическую фазу не наблюдают до плавления.
Выдерживание в условиях повышенной влажности вызывает превращение в дигидрат, определенное посредством XRPD с регулируемой влажностью среды, выполненной при 25°C. Относительную влажность в камере вначале поддерживают при 2% в течение 6 часов, затем линейно повышают до 95% в течение 19 часов, поддерживают при 95% в течение 6 часов, линейно уменьшают до 2% в течение 19 часов и поддерживают при 2% в течение дополнительных 10 часов. Фаза 1 превращается в дигидрат после приблизительно 15 мин при 95%, который, в свою очередь, превращается в фазу 2 после приблизительно 40 мин при 2% r.h. Кроме того, хранение фазы 1 при 20°C и 75% относительной влажности приводит к полному превращению в дигидрат в течение 3 недель. Скорость превращения коррелирует с относительной влажностью.
Эксперименты по созреванию кристаллов с суспензиями, исходя из смеси фаз (см. эксперименты по созреванию), указывают на то, что в диапазоне температур от 0 до 40°C фаза 1 представляет собой только метастабильный полиморф.
Таким образом, полиморф 1 может быть использован в получении дигидрата и также в получении полиморфа 2.
Полиморф 3
Другой аспект настоящего изобретения относится к полиморфу 3 гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она, который имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при
4,5 (среднее),
15,4 (сильное),
16,7 (сильное),
21,7 (сильное) и
25,5 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом аспекте полиморф 3 имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 4,5 (среднее), 15,4 (сильное), 16,7 (сильное), 21,7 (сильное), 22,0 (среднее), 22,3 (среднее) и 25,5 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
Полиморф 3 может также характеризоваться картиной дифракции рентгеновских лучей, будучи по существу такой, как картина, представленная на фиг.6. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться, и представляют собой другой вариант осуществления изобретения.
Полиморф 3 может также характеризоваться параметрами плавления, такими как температура плавления, определенная посредством DSC. При нагревании фаза 3 начинает плавиться приблизительно при 300°C с предшествующим и сопровождающим химическим разложением. Никакого превращения в другую кристаллическую фазу не наблюдают при низкой влажности до плавления.
Выдерживание в условиях повышенной влажности вызывает превращение в дигидрат, определенное посредством XRPD с регулируемой влажностью среды, выполненной при 25°C. Относительную влажность (r.h.) в камере вначале линейно снижают от 50% до 2% за 6 часов, поддерживают на уровне при 2% в течение 6 часов, затем линейно повышают до 95% в течение 12 часов, поддерживают при 95% в течение 6 часов, линейно уменьшают до 2% за 12 часов и поддерживают при 2% в течение дополнительных 6 часов. В результате фаза 3 превращается в гидрат после приблизительно 30 мин при 95%, который, в свою очередь, превращается в фазу 2 после приблизительно 30 мин при 2% r.h.
Кроме того, фаза 3 может также характеризоваться DVS (динамическая сорбция паров) изотермами сорбции и десорбции водяных паров, полученными при 25°C. (Фиг.7). На фигуре показано в соответствии XRPD с регулируемой влажностью, описанной выше, что фаза 3 сохраняется при увеличивающейся влажности и превращается в дигидрат при выше приблизительно 80% относительной влажности (цикл 1, сорбция). При уменьшающейся влажности дигидрат превращается обратно при низкой влажности (ниже приблизительно 10% r.h.) в фазу 2 (цикл 1, десорбция). Затем фаза 2 превращается в дигидрат при увеличивающейся влажности, и приблизительно с такой же изотермой он превращается обратно при уменьшающейся влажности в полиморф 2 (цикл 2, см. также фиг.3).
Соответствующие фигуры, показывающие DVS, характеризующие превращения фазы 1 и фазы 4 в дигидрат, который затем превращается обратно в фазу 2, являются похожими.
Кроме того, хранение фазы 3 при 20°C и 75% относительной влажности приводит к полному превращению в дигидрат в течение 3 недель. Скорость превращения коррелирует с относительной влажностью. При суспендировании в воде, полное превращение в дигидрат наблюдают почти немедленно (<10 мин).
Кроме того, эксперименты по созреванию с суспензиями, исходя из смеси фаз в сухих органических растворителях (см. Примеры), указывают на то, что в диапазоне температур от 0 до 40°C, фаза 3 является самой стабильной безводной фазой. Полученные данные показывают, что полиморф 3 при комнатной температуре или при примерно комнатной температуре является самой стабильной фазой при низкой относительной влажности (менее чем приблизительно 10% относительной влажности).
Полиморф 3 можно легко получить кристаллизацией из различных свободных от воды растворителей при повышенных температурах, и он является, таким образом, подходящим для выделения и очистки сырого соединения (I).
Полиморф 4
Настоящее изобретение также относится к полиморфу 4 гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она, который имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при
15,4 (среднее),
16,7 (среднее),
21,5 (сильное) и
30,7 (слабое) градусах 2 тета ± 0,2 градуса 2 тета.
В другом аспекте полиморф 4 имеет свойство проявлять по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 15,4 (среднее), 16,7 (среднее), 16,9 (среднее), 21,5 (сильное), 21,9 (слабое), 22,4 (среднее), 23,2 (слабое), 27,6 (слабое) и 30,7 (слабое) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения полиморф 4 может также характеризоваться картиной дифракции рентгеновских лучей, такой как картина, представленная на фиг.8. Дифрактограмма была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Полиморф 4 может также характеризоваться параметрами плавления, такими как температура плавления, определенная посредством DSC (дифференциальная сканирующая калориметрия). При нагревании фаза 4 начинает расплавляться при приблизительно 300°C с предшествующим и сопровождающим химическим разложением. Никакого превращения в другую кристаллическую фазу 1, 2 или 3 не наблюдают до плавления.
Выдерживание в условиях повышенной влажности вызывает превращение в дигидрат, определенное посредством XRPD с регулированием влажности. Вначале влажность линейно снижают от 50% до 2% за 6 часов, поддерживают при 2% в течение 6 часов, затем линейно повышают до 95% в течение 12 часов, поддерживают при 95% в течение 6 часов, линейно уменьшают до 2% за 12 часов и поддерживают при 2% в течение дополнительных 6 часов. В результате фаза 4 превращается в дигидрат после приблизительно 15 мин при 95%, который, в свою очередь, превращается в фазу 2 после приблизительно 20 мин при 2% r.h.
Полиморф 4 может также характеризоваться DVS (динамическая сорбция паров) изотермами сорбции и десорбции водяных паров. Характер сорбции/десорбции полиморфа 4 подобен характеру, изображенному на фиг.7 для полиморфа 3.
Кроме того, хранение фазы 4 при 20°C и 75% относительной влажности вызывает полное превращение в дигидрат в течение 3 недель. Скорость превращения явно коррелирует с относительной влажностью.
Эксперименты по созреванию с суспензиями, исходя из смеси фаз в сухих органических растворителях, указывают на то, что в диапазоне температур от 0 до 40°C фаза 4 является только метастабильной фазой.
Сольваты
Кроме того, настоящее изобретение относится к сольвату гидрохлорида 6-(пиперидин-4-илокси)-2H-изохинолин-1-она с 1,4-диоксаном, сольвату с метилацетатом и сольвату с ацетонитрилом.
Сольват с 1,4-диоксаном согласно изобретению демонстрирует характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 15,1 (сильное) и 22,5 (сильное) градусах 2 тета ± 0,2 градуса 2 тета.
В другом аспекте сольват с 1,4-диоксаном имеет по меньшей мере характеристические отражения рентгеновских лучей, фиксированные на рентгеновской порошковой дифрактограмме при использовании CuKα1-излучения, при 15,1 (сильное), 19,7 (среднее), 20,3 (среднее), 21,6 (среднее), 22,5 (сильное), 23,8 (среднее), 24,9 (среднее) и 30,2 (среднее) градусах 2 тета ± 0,2 градуса 2 тета.
В другом варианте осуществления изобретения сольват с 1,4-диоксаном может также характеризоваться картиной дифракции рентгеновских лучей, такой, как картина, представленная на фиг.9. Картина была получена при использовании CuKα1-излучения в трансмиссионном режиме, где интенсивности отражений, изображенные на фигуре, а также интенсивности отражений, установленные выше, не являются необходимым предварительным условием, а могут изменяться.
Согласно порошковой дифракции рентгеновских лучей с разрешением по температуре, DSC и TGA, сольват с 1,4-диоксаном обнаруживает потерю массы, составляющую 16,6%, при термогравиметрическом анализе, главным образом, в диапазоне температур от 80 до 120°C, по сравнению с ожидаемой потерей массы 16,6% для полусольвата и 23,9% для одного молярного эквивалента диоксана. В указанном диапазоне температур, наблюдают превращение в фазу 3, определенное посредством XRPD. Таким образом, сольват является относительно стабильным.
Таким образом, следующий аспект настоящего изобретения относится к применению сольвата с 1,4-диоксаном для получ