Конъюгаты для доставки полинуклеотидов in vivo, содержащие чувствительные к ферментативному расщеплению связи
Иллюстрации
Показать всеИзобретение относится к соединениям для обратимой модификации амфипатического мембраноактивного полиамина и полимеру для доставки полинуклеотида в клетку in vivo. Амфипатические мембраноактивные полиамины обратимо модифицированы поддающимися ферментативному отщеплению дипептидными амидобензилкарбонатными маскирующими агентами. Указанная модификация приводит к маскированию мембранной активности полимера, а обратимость обеспечивает чувствительность к физиологическим условиям. Обратимо модифицированные полиамины (динамичные поликонъюгаты, или КДП) также ковалентно связаны с полинуклеотидом РНКи или вводятся совместно с направленным конъюгатом полинуклеотид РНКи-нацеливающая молекула. 4 н. и 13 з.п. ф-лы, 15 табл., 4 ил., 16 пр.
Реферат
УРОВЕНЬ ТЕХНИКИ
Доставка полинуклеотидов и других по существу не проникающих через клеточные мембраны соединений в живую клетку в значительной степени ограничена сложной системой клеточных мембран. Лекарственные средства, используемые в антисмысловой, РНКи и генной терапии, представляют собой относительно большие гидрофильные полимеры и часто несут сильный отрицательный заряд. Обе указанные физические характеристики значительно ограничивают возможность их непосредственную диффузию через клеточную мембрану. По этой причине основным ограничением для доставки полинуклеотида является доставка указанного полинуклеотида через клеточную мембрану в цитоплазму или ядро клетки.
Один способ, который используется для in vivo доставки малой нуклеиновой кислоты, заключатся в присоединении нуклеиновой кислоты либо к малой нацеливающей молекуле, либо к липиду или стеролу. Несмотря на то, что при использовании указанных конъюгатов наблюдается некоторая доставка и активность, необходимая для этих методов очень высокая доза нуклеиновой кислоты делает их непрактичными.
Также было разработано множество реагентов трансфекции, которые обеспечивали достаточно эффективную доставку полинуклеотидов в клетки в vitro. Однако доставка полинуклеотидов in vivo с использованием указанных реагентов трансфекции является сложной и признана неэффективной из-за токсичности, нежелательных взаимодействий с компонентами сыворотки и слабым направленным действием in vivo. Реагенты трансфекции, которые хорошо работают в vitro, катионные полимеры и липиды, как правило, образуют большие катионные электростатические частицы и дестабилизируют клеточные мембраны. Положительный заряд реагентов трансфекции в vitro облегчает связывание с нуклеиновой кислотой через взаимодействия между зарядами (электростатические), что приводит, к образованию комплекса нуклеиновая кислота/реагент трансфекции. Положительный заряд также является полезным для неспецифического связывания носителя с клеткой и для слияния с мембраной, ее дестабилизации или разрушения. Дестабилизация мембран облегчает доставку по существу не проникающего через клеточные мембраны полинуклеотида через клеточную мембрану. Хотя указанные свойства облегчают перенос нуклеиновой кислоты в vitro, они обуславливают токсичность и обеспечивают неэффективное направленное действие in vivo. Катионный заряд приводит к взаимодействию с компонентами сыворотки, которое вызывает дестабилизацию взаимодействия полинуклеотид-реагент трансфекции, плохую биодоступность и слабое нацеливание. Мембранная активность реагентов трансфекции, которая может являться эффективной в vitro, часто вызывает токсичность in vivo.
Для доставки in vivo носитель (нуклеиновая кислота и связанный агент доставки) должен быть маленьким, менее 100 нм в диаметре, предпочтительно, менее 50 нм. Еще более маленькие комплексы, менее 20 нм или менее 10 нм, были бы более применимыми. Носители для доставки размером более 100 нм имеют очень слабый доступ к клеткам, отличным от клеток кровеносных сосудов, in vivo. Комплексы, образованные за счет электростатических взаимодействий, склонны агрегировать или распадаться под воздействием физиологических концентраций солей или компонентов сыворотки. Кроме того, катионный заряд на носителях для доставки in vivo приводит к нежелательным взаимодействиям с компонентами сыворотки и, таким образом, слабой биодоступности. Интересно, что сильный отрицательный заряд также может ингибировать нацеливание (targeting) in vivo, препятствуя взаимодействию, необходимому для направленного действия, т.е. связыванию нацеливающих лигандов с клеточными рецепторами. Таким образом, для распределения и направленного действия in vivo являются желаемыми почти нейтральные носители. В отсутствие тонкой регуляции разрушающая или дестабилизирующая мембраны активность вызывает токсичность при использовании in vivo. Баланс между токсичностью носителя и доставкой нуклеиновой кислоты легче достигается в vitro, чем in vivo..
Согласно публикации патента США 20080152661, Розема и др. (Rozema et al.) предложили способ обратимой регуляции разрушающей мембраны активности мембраноактивного полиамина с использованием модификации с помощью дизамещенного малеинового ангидрида. Малеаматные связи, образованные путем проведения реакции между малеиновым ангидридом и амином, являются рН-лабильными в диапазоне рН, подходящем для доставки in vivo. Указанный процесс позволял использовать мембраноактивные полимеры для доставки in vivo или нуклеиновых кислот. Согласно настоящему изобретению предложены модифицированные мембраноактивные полимеры, содержащие дипептид-амидобензилкарбаматные связи. Дипептид-амидобензилкарбаматные связи (связывающие фрагменты) являются обратимыми и физиологически чувствительными. В отличие от рН-лабильных малеаматных связей, образованных путем модификации дизамещенным малеиновым ангидридом, присоединение модифицирующих полимер агентов, описанных в настоящей заявке, приводит к образованию расщепляемых ферментами связей, которые являются более стабильными при циркуляции in vivo.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно предпочтительному варианту реализации настоящего изобретения описаны маскирующие агенты для обратимой модификации и ингибирования мембранной активности амфипатического мембраноактивного полиамина, содержащие: стерический стабилизатор или нацеливающий лиганд, присоединенный к дипептид-амидобензилкарбонату, который называются в настоящей заявке дипептидными маскирующими агентами или расщепляемыми протеазы маскирующими агентами. Дипептидные маскирующие агенты имеют общую форму:
R-A1A2-амидобензилкарбонат,
где R представляет собой стерический стабилизатор или нацеливающий лиганд. А1 представляет собой аминокислоту, и А2 представляет собой аминокислоту. Реакция маскирующего агента с полимерным амином приводит к получению карбаматной связи. Маскирующий агент является стабильным до расщепления дипептида in vivo эндогенной протеазой, что приводит, соответственно, к отщеплению стерического стабилизатора или нацеливающего лиганда от полиамина. После ферментативного расщепления за дипептидом (между А и амидобензилом) амидобензилкарбамат претерпевает спонтанную перестройку, которая приводит к регенерации полимерного амина. Предпочтительно R является нейтральным. Более предпочтительно, R является незаряженным. Предпочтительный стерический стабилизатор представляет собой полиэтиленгликоль (PEG). Нацеливающий лиганд может быть выбран из перечня, включающего гаптены, такие как дигоксигенин, витамин, такой как биотин, антитело, моноклональное антитело и лиганд рецептора клеточной поверхности. Нацеливающий лиганд может быть связан с дипептидом через линкер, такой как PEG-линкер. Предпочтительный лиганд рецептора клеточной поверхности представляет собой лиганд рецептора асиалогликопротеина (ASGPr). Предпочтительный лиганд ASGPr представляет собой N-ацетилгалактозамин (NAG). Предпочтительный дипептид состоит из гидрофобной аминокислоты, связанной с гидрофильной незаряженной аминокислотой амидной связью. Предпочтительная амидобензильная группа представляет собой п-амидобензильную группу.
Предпочтительный карбонат представляет собой активированный амин-реактивный карбонат.
Согласно предпочтительному варианту реализации изобретения изобретение относится к композиции для доставки полинуклеотида интерферирующей РНК (РНКи) в клетку in vivo, содержащей: маскированный амфипатический мембраноактивный полиамин (полимер доставки), где указанный полиамин маскирован путем обратимой модификации дипептидными маскирующими агентами, описанными в настоящей заявке, и полинуклеотид РНКи. Полимер доставки может быть ковалентно связан с полинуклеотидом РНКи. Предпочтительная связь для ковалентного присоединения полимера доставки к полинуклеотиду РНКи представляет собой чувствительную к физиологическим условиям ковалентную связь. Согласно одному варианту реализации изобретения указанная связь является ортогональной по отношению к связи дипептидного маскирующего агента. Альтернативно, полимер доставки не является ковалентно связанным с полинуклеотидом РНКи, и полинуклеотид РНКи ковалентно связан с направленной молекулой.
Согласно предпочтительному варианту реализации настоящего изобретения описана композиция, содержащая: амфипатический мембраноактивный полиамин, ковалентно связанный с: a) множеством нацеливающих лигандов или пространственных стабилизаторов дипептид-амидобензилкарбаматными связями; и b) одним или более полинуклеотидами через одну или более обратимых связей. Согласно одному варианту реализации изобретения дипептид-амидобензилкарбаматная связь является ортогональной по отношению к обратимой ковалентной связи полинуклеотида. Конъюгат полинуклеотид-полимер вводят млекопитающему в фармацевтически приемлемом носителе или разбавителе.
Согласно предпочтительному варианту реализации настоящего изобретения описана композиция, содержащая: а) амфипатический мембраноактивный полиамин, ковалентно связанный со множеством нацеливающих лигандов или пространственных стабилизаторов дипептид-амидобензилкарбаматными связями; и b) полинуклеотид РНКи, ковалентно связанный с нацеливающей группой, выбранной из перечня, состоящего из: гидрофобной группы, содержащей 20, или более, атомов углерода и галактозного кластера. Согласно указанному варианту реализации изобретения полинуклеотид РНКи не является ковалентно связанным с модифицированным амфипатическим мембраноактивным полиамином. Конъюгат модифицированного полиамина и нацеленной на полинуклеотид РНКи группы синтезируются раздельно и могут поставляться в отдельных контейнерах или одном контейнере. Конъюгат модифицированного полиамина и нацеленной на полинуклеотид РНКи группы вводят млекопитающему совместно или раздельно в фармацевтически приемлемых носителях или разбавителях.
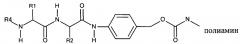
Предпочтительный дипептидный маскирующий агент содержит расщепляемое протеазой (пептидазой) амин-реактивное карбонатное производное дипептид-п-амидобензила. В расщепляемых протеазами маскирующих агентах согласно изобретению используется дипептид, соединенный с активированным амидобензилом карбонатным фрагментом. Нацеливающий лиганд или стерический стабилизатор присоединен к амино-концу дипептида. Активированный амидобензилом карбонатный фрагмент присоединен к карбокси-концу дипептида. Расщепляемые протеазами линкеры, подходящие для применения согласно изобретению, имеют следующую общую структуру:
где R4 содержит нацеливающий лиганд или стерический стабилизатор, R3 содержит амин-реактивный карбонатный фрагмент, и R1 и R2 представляют собой боковые цепи аминокислот. Предпочтительный активированный карбонат представляет собой пара-нитрофенол. Однако другие амин-реактивные карбонаты, известные в данной области техники, можно легко использовать вместо пара-нитрофенола. Реакция активированного карбоната с амином приводит к связыванию нацеливающего лиганда или стерического стабилизатора с мембраноактивным полиамином через поддающуюся расщеплению пептидазой дипептид-амидобензилкарбаматную связь. Ферментативное расщепление дипептида между аминокислотой и амидобензильной группой приводит к удалению R4 от полимера и возбуждает реакцию элиминации, которая приводит к регенерации полимерного амина.
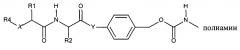
Дипептидные маскирующие агенты согласно изобретению применимы для обратимой модификации/ингибирования амфипатических мембраноактивных полиаминов. Ковалентная связь образуется в результате реакции активированного карбоната дипептидного маскирующего агента с полимерным амином, в частности, первичной аминогруппой. Таким образом, согласно настоящему изобретению предложен конъюгат, содержащий дипептид-амидобензилкарбонатный маскирующий агент, описанный в настоящей заявке, и амфипатический мембраноактивный полиамин:
Соединения согласно настоящему изобретению, в целом, могут быть получены с использованием методов, известных специалисту в области органической или медицинской химии. Дополнительные объекты, признаки и преимущества согласно изобретению будут очевидны из следующего подробного описания при его совместном рассмотрении с сопутствующими графическими материалами.
КРАТКОЕ ОПИСАНИЕ ФИГУР.
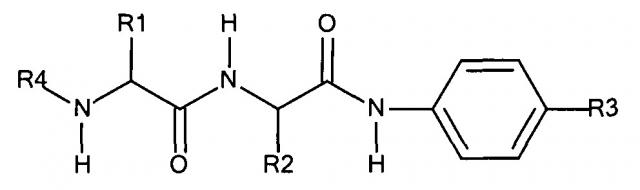
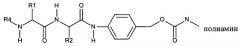
ФИГ.1. Изображение, показывающее структуру дипептидного маскирующего агента, где:
R1 и R2 представляют собой R-группы аминокислот,
R4 представляет собой нацеливающий лиганд стерического стабилизатора,
Х представляет собой -NH-, -О- или -СН2-,
Y представляет собой -NH- или -O-
R5 находится в положении 2, 4 или 6 и представляет собой -CH2-O-C(O)-O-Z, где Z представляет собой карбонат, и
R6 независимо представляет собой водород, алкил или галогенид в каждом из положений 2, 3, 4, 5 или 6, за исключением положения, занимаемого R5.
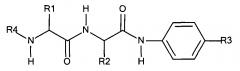
ФИГ.2. Изображение, показывающее структуру дипептидного маскирующего агента, связанного с полиамином, где: R1 и R2 представляют собой R-группы аминокислот, R4 представляет собой нацеливающий лиганд стерического стабилизатора, Х представляет собой -NH-, -О- или -СН2-, и Y представляет собой -NH- или -О-.
ФИГ.3. Изображение, показывающее структуры различных дипептидных маскирующих агентов.
ФИГ.4. График, показывающий время циркуляции полимеров, модифицированных дипептидными маскирующими агентами, по сравнению с двумя различными маскирующими агентами на основе малеинового ангидрида.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Описаны маскирующие агенты, применимые для обратимой модификации и ингибирования амфипатических мембраноактивных полиаминов, и доставки полимеров, образованных путем модификации полиамина дипептидными маскирующими агентами. Расщепляемые пептидазам связи являются устойчивыми к гидролизу в отсутствие фермента, электрически нейтральными и обеспечивают повышенную стабильность КДП (конъюгатов для доставки полинуклеотидов) при хранении и при циркуляции in vivo. Улучшенное (удлиненное) время полужизни при циркуляции расширяет возможности для лиганд-опосредованного накопления в ткани, такой как опухолевая ткань. Полимеры доставки особенно полезны для доставки полинуклеотидов РНКи in vivo. Доставка полинуклеотидов РНКи in vivo применима для терапевтического ингибирования (нокдауна) экспрессии гена.
Дипептидные маскирующие агенты имеют общую форму:
R-A1A2-амидобензилкарбонат,
где R представляет собой стерический стабилизатор или нацеливающий лиганд, А1 представляет собой аминокислоту, А2 представляет собой аминокислоту, и карбонат представляет собой активированный амин-реактивный карбонат. R предпочтительно является незаряженным. Реакция маскирующего агента карбоната с полимерным амином приводит к образованию карбаматной связи. Маскирующий агент является стабильным до расщепления дипептида эндогенной протеазой in vivo, что приводит, соответственно, к отщеплению стерического стабилизатора или нацеливающего лиганда от полиамина. После ферментативного расщепления за дипептидом (между А2 и амидобензилом), амидобензилкарбамат подвергается спонтанной перестройке, которая приводит к регенерации полимерного амина. Предпочтительный стерический стабилизатор представляет собой полиэтиленгликоль (PEG). Предпочтительный нацеливающий лиганд для доставки в печень представляет собой лиганд ASGPr. Предпочтительный лиганд ASGPr представляет собой N-ацетилгалактозамин (NAG). Предпочтительная амидобензильная группа представляет собой п-амидобензильную группу.
Дипептиды дипептидных маскирующих агентов, обозначенные как А1А2 (или АА), представляют собой димеры аминокислот, соединенных амидными связями. Аминокислоты, включая α- и β-аминокислоты, хорошо известны в области биологии и химии и представляют собой молекулы, содержащие аминогруппу, карбоксильную группу и боковую цепь, которая различается у разных аминокислот. Предпочтительная аминокислота представляет собой α-аминокислоту, имеющую общую формулу H2NCHRCOOH, где R представляет собой органический заместитель. Предпочтительная α-аминокислота представляет собой незаряженную природную аминокислоту. В предпочтительном дипептиде А1 представляет собой гидрофобную аминокислоту, и А2 представляет собой незаряженную гидрофильную аминокислоту. Предпочтительная гидрофобная аминокислота представляет собой фенилаланин, валин, изолейцин, лейцин, аланин или триптофан. Предпочтительная незаряженная гидрофильная аминокислота представляет собой аспарагин, глутамин или цитруллин. Более предпочтительная гидрофобная аминокислота представляет собой фенилаланин или валин. Более предпочтительная незаряженная гидрофильная аминокислота представляет собой цитруллин. Несмотря на то, что дипептиды являются предпочтительными, возможно включение дополнительной аминокислоты между А1 и R. Также возможно использовать одну аминокислоту вместо дипептида путем исключения аминокислоты А1. Любые природные аминокислоты, применимые согласно изобретению, в настоящей заявке обозначены обычными аббревиатурами. Несмотря на то, что могут использоваться заряженные аминокислоты, предпочтительно, чтобы маскирующий агент был незаряженным.
Согласно предпочтительному варианту реализации изобретения амфипатический мембраноактивный полиамин обратимо модифицирован путем проведения реакции с дипептид-амидобензилкарбонатным маскирующим агентом согласно изобретению с получением не обладающего мембранной активностью полимера доставки. Дипептидные маскирующие агенты могут защищать полимер от неспецифических взаимодействий, повышать время циркуляции в кровотоке, усиливать специфические взаимодействия, подавлять токсичность или изменять заряд полимера.
Обратимо маскированные полимеры согласно изобретению включают следующую структуру:
где:
Х представляет собой -NH-, -О- или -СН2-
Y представляет собой -NH- или -O-
R1 предпочтительно представляет собой
-(СН2)k-фенил (k представляет собой 1, 2, 3, 4, 5, 6; k=1, фенилаланин),
-СН-(СН3)2 (валин),
-СН2-СН-(СН3)2 (лейцин),
-СН(СН3)-СН2-СН3 (изолейцин),
-СН3 (аланин),
-(СН2)2-СООН (глутаминовая кислота),
или
R2 предпочтительно представляет собой
водород (глицин)
-(СН2)3-NH-С(O)-NH2 (цитруллин),
-(CH2)4-N-(CH3)2 (лизин(СН3)2),
-(CH2)k -C(O)-NH2; (k представляет собой 1, 2, 3, 4, 5, 6),
-CH2-C(O)-NH2 (аспарагин),
-(CH2)2-C(O)-NH2 (глутамин),
-CH2-C(O)-NR1R2 (амид аспарагиновой кислоты),
-(CH2)2-C(O)-NR1R2 (амид глутаминовой кислоты),
-CH2-C(O)-OR1 (эфир аспарагиновой кислоты) или
-(CH2)2-C(O)-OR1 (эфир глутаминовой кислоты),
R1 и R2 представляют собой алкильные группы
R4 включает полиэтиленгликоль или нацеливающий лиганд; и
полиамин представляет собой амфипатический мембраноактивный полиамин.
Несмотря на то, что на структуре, приведенной выше, показан один дипептидный маскирующий агент, связанный с полимером, при осуществлении настоящего изобретения от 50% до 90%, или более, полимерных аминов модифицированы дипептидными маскирующими агентами.
Согласно предпочтительному варианту реализации изобретения обратимо маскированный полимер согласно изобретению включают структуру:
где R1, R2, R4 и полиамин являются такими, как описано выше.
Обратимо маскированные полимеры согласно изобретению образованы путем проведения реакции между дипептидными маскирующими агентами согласно изобретению и аминами полимера. Дипептидные маскирующие агенты согласно изобретению имеют следующую структуру:
где:
X, Y, R1, R2, и R4 являются такими, как описано выше
R5 находится в положении 2, 4 или 6 и представляет собой -CH2-O-C(O)-O-Z, где Z представляет собой
- Галогенид,
,
,
или
; и
R6 независимо представляет собой водород, алкил, -(СН2)n-СН3 (где n=0-4), -(СН2)-(СН3)2 или галогенид в каждом из положений 2, 3, 4, 5 или 6, за исключением положения, занимаемого R5.
Согласно предпочтительному варианту реализации изобретения Х представляет собой -NH-, Y представляет собой -NH-, R4 является незаряженным, R5 находится в положении 4, и R6 представляет собой водород, как показано на следующей схеме:
.
Согласно другому варианту реализации изобретения R4 представляет собой:
R-(O-CH2-CH2)s-O-Y1-, где
R представляет собой водород, метил или этил; и s представляет собой целое число от 1 до 150,
и Y1 представляет собой линкер, выбранный из перечня, включающего:
-O-Y2-NH-C(O)-(CH2)2-C(O)-, где Y2 представляет собой
-(СН2)3-
-C(O)-N-(CH2-CH2-O)p-CH2-CH2- (p представляет собой целое число от 1 до 20), и
-О-.
Нацеливающий лиганд может быть выбран из перечня, включающего гаптен, витамин, антитело, моноклональное антитело и лиганд рецептора клеточной поверхности. Нацеливающий лиганд может быть связан с дипептидом через линкер, такой как PEG-линкер.
Неограничивающие примеры мембраноактивных полимеров, подходящих для применения согласно изобретению, были ранее описаны в публикациях патентов США 20080152661, 20090023890, 20080287630, и 20110207799. Подходящий амфипатический мембраноактивный полиамин также может представлять собой маленький пептид, такой как пептид мелитина.
Полимерные амины обратимо модифицировали с использованием расщепляемых ферментами линкеров, описанных в настоящей заявке. Амин является обратимо модифицированным, если расщепление модифицирующей группы приводит к восстановлению амина. Реакция маскирующего агента на основе активированного карбоната с полимерным амином приводит к связыванию нацеливающего лиганда или стерического стабилизатора с полимером через поддающуюся расщеплению пептидазой дипептид-амидобензильную карбаматную связь, как показано далее:
R1 включает нацеливающий лиганд (содержащий или не содержащий защитные группы) или PEG,
R2 представляет собой амфипатический мембраноактивный полиамин,
АА представляет собой дипептид (содержащий или не содержащий защитные группы), и
Z представляет собой амин-реактивный карбонат.
Защитные группы можно использовать в ходе синтеза дипептидных маскирующих агентов. В случае присутствия защитных групп, их можно удалять до или после модификации амфипатического мембраноактивного полиамина.
Обратимая модификация достаточного процента полимерных аминов дипептидными маскирующими агентами ингибирует мембранную активность мембраноактивного полиамина. Модификация полимерных аминов дипептидными маскирующими агентами также предпочтительно приводит к нейтрализации заряда амина. Дипептид-амидобензилкарбаматная связь чувствительна к расщеплению протеазой (или пептидазой). В присутствии протеазы анилидная связь расщепляется, что приводит к образованию промежуточного соединения, которое сразу подвергается реакции 1,6-элиминации с высвобождением свободного полимера:
На приведенной выше схеме реакции АА представляет собой дипептид, R1 содержит нацеливающий лиганд или стерический стабилизатор, и R2 представляет собой амфипатический мембраноактивный полиамин. Важно, что свободный полимер является немодифицированным и, таким образом, мембранная активность восстанавливается.
В маскированном состоянии обратимо маскированный мембраноактивный полиамин не обладает разрушающей мембраны активностью. Может требоваться обратимая модификация дипептидными маскирующими агентами более чем 50%, более чем 55%, более чем 60%, более чем 65%, более чем 70%, более чем 75%, более чем 80% или более чем 90% аминов на полиамине для ингибирования мембранной активности и обеспечения функции нацеливания на клетки, т.е. образования обратимо маскированного мембраноактивного полимера (полимера доставки).
Настоящее изобретение также обеспечивает способ доставки биологически активного вещества в клетки. Более конкретно, настоящее изобретение относится к соединениям, композициям и способам, применимым для доставки полинуклеотидов РНКи в клетки млекопитающих in vivo.
Согласно одному варианту реализации изобретения полинуклеотид РНКи связан с полимером доставки согласно изобретению чувствительной к физиологическим условиям ковалентной связью. Благодаря использованию чувствительной к физиологическим условиям связи полинуклеотид можно отщеплять от полимера, высвобождая указанный полинуклеотид для его участия в функциональных взаимодействиях с клеточными компонентами.
Изобретение включает систему доставки конъюгата, имеющую следующую общую структуру:
где N представляет собой полинуклеотид РНКи, L1 представляет собой чувствительную к физиологическим условиям ковалентную связь, P представляет собой амфипатический мембраноактивный полиамин, М1 представляет собой нацеливающий лиганд, связанный с Р дипептид-амидобензилкарбаматной связью, и М2 представляет собой стерический стабилизатор, связанный с P дипептид-амидобензилкарбаматной связью, каждый из y и z представляет собой целое число,, большее или равное нулю, при условии, что y+z имеет значение больше 50%, больше чем 60%, больше 70%, больше 80% или больше 90% первичных аминов на полиамине P, как определено на основе количества аминов на P в отсутствие любых маскирующих агентов. В немодифицированном состоянии P представляет собой мембраноактивный полиамин. Полимер доставки не является мембраноактивным. Обратимая модификация первичных аминов P путем присоединения М1 и/или М2 приводит к обратимому ингибированию или инактивации мембранной активности Р. Показано, что некоторые маленькие амфипатические мембраноактивные полиамины, такие как пептид мелитина, содержат только 3-5 первичных аминов. Предполагается, что изменение процента аминов отражает изменение процента аминов в популяции полимеров. При расщеплении М1 и М2 амины полиамина перестраиваются, что приводит, соответственно, к возвращению P в его немодифицированное мембраноактивное состояние.
Согласно другому варианту реализации изобретения полинуклеотид РНКи вводят совместно с полимером доставки согласно изобретению in vivo. Таким образом, изобретение включает композиции, которые имеют следующую общую структуру:
плюс N-T,
где N представляет собой полинуклеотид РНКи, Т представляет собой нацеливающую группу, P представляет собой амфипатический мембраноактивный полиамин, М1 представляет собой нацеливающий лиганд, связанный с P дипептид-амидобензилкарбаматной связью, и М2 представляет собой стерический стабилизатор, связанный с P дипептид-амидобензилкарбаматной связью. Каждый из y и z представляет собой целое число, большее или равное нулю, при условии, что y+z имеет значение больше 50%, больше 60%, больше 70%, больше 80% или больше 90% первичных аминов на полиамине P, как определено на основе количества аминов на Р в отсутствие любых маскирующих агентов. В немодифицированном состоянии Р представляет собой мембраноактивный полиамин. Полимер доставки M1y-P-M2z не является мембраноактивным. Обратимая модификация первичных аминов Р путем присоединения М1 и/или М2 приводит к обратимому ингибированию или инактивации мембранной активности Р. Показано, что некоторые маленькие амфипатические мембраноактивные полиамины, такие как пептид мелитина, содержат только 3-5 первичных аминов. Таким образом, предполагается, что изменение процента аминов отражает изменение процента аминов в популяции полимеров. При расщеплении М1 и М2 амины полиамина регенерируют, что приводит, соответственно, к возвращению Р в его немодифицированное мембраноактивное состояние. N связывается с Т через ковалентную связь с образованием конъюгата полинуклеотид РНКи-нацеливающая группа с использованием стандартных способов, известных в данной области техники. Предпочтительная ковалентная связь представляет собой чувствительную к физиологическим условиям ковалентную связь. N-T. Полимер доставки и N-T синтезируются или производятся раздельно. Т и N не являются напрямую или не напрямую ковалентно связанными с Р, М1 или М2. Электростатическое или гидрофобное соединение полинуклеотида или конъюгата полинуклеотида с маскированным или немаскированным полимером не является необходимым для доставки полинуклеотида в печень in vivo. Маскированный полимер и конъюгат полинуклеотида могут поставляться в одном контейнере или в отдельных контейнерах. Их можно объединять до введения, вводить совместно или вводить раздельно.
Для доставки в гепатоциты, независимо от того, является ли полинуклеотид РНКи связанным с полимером доставки через ковалентную связь или его вводят совместно с полимером доставки, у имеет значение больше 50% и до 100% первичных аминов на полимере Р. z, таким образом, имеет значение, больше или равное нулю процентов (0%), но меньше чем 50% первичных аминов на полимере Р.
В случае доставки к опухолевым клеткам печени z может иметь значение вплоть до 100% первичных аминов на полимере Р. Согласно предпочтительному варианту реализации изобретения для доставки к опухолевым клеткам z имеет значение более 50%, более 60%, более 70%, более 80% или более 90% первичных аминов на полиамине Р, и y равен нулю.
Мембраноактивные полиамины способны разрушать плазматические мембраны или лизосомальные/эндоцитозные мембраны. Указанная мембранная активность является существенным свойством для доставки в клетки полинуклеотида. Однако мембранная активность обуславливает токсичность при введении полимера in vivo. Полиамины также легко взаимодействуют со многими анионными компонентами in vivo, что обуславливает нежелательное биораспределение. Таким образом, обратимое маскирование мембранной активности полиамина является существенным для применения in vivo.
Маскирование осуществляют путем обратимого присоединения описанных дипептидных маскирующих агентов к мембраноактивному полиамину с образованием обратимо маскированного мембраноактивного полимера, т.е. полимера доставки. Помимо ингибирования мембранной активности, маскирующие агенты защищают полимер от неспецифических взаимодействий, снижают взаимодействия с компонентами сыворотки, нейтрализуют полиамин, снижая положительный заряд и приводя к образованию почти нейтрально заряженного полимера, повышают время циркуляции в кровотоке и/или обеспечивают клеточно-специфичные взаимодействия, т.е. направленность.
Существенным признаком маскирующих агентов является то, что при агрегации они ингибируют мембранную активность полимера. Маскирующие агенты могут защищать полимер от неспецифических взаимодействий (снижать взаимодействия с компонентами сыворотки, повышать время циркуляции в кровотоке). Мембраноактивный полиамин является мембраноактивным в немодифицированном (немаскированном) состоянии и не обладает мембранной активностью (является инактивированным) в модифицированном (маскированном) состоянии. Для достижения желаемой степени инактивации достаточное количество маскирующих агентов должно быть связано с полимером. Желаемая степень модификации полимера путем присоединения маскирующего агента (агентов) легко определяется с использованием подходящих тестов активности полимера. Например, если полимер в конкретном тесте обладает мембранной активностью, с указанным полимером связывают количество маскирующих агентов, достаточное для достижения желаемой степени ингибирования мембранной активности в указанном анализе. Маскирование требует модификации ≥50%, ≥60%, ≥70%, ≥80% или ≥90% первичных аминогрупп на популяции полимера, что определяют на основе количества первичных аминов на полимере в отсутствие любых маскирующих агентов. Также предпочтительной характеристикой маскирующих агентов является то, что их присоединение к полимеру снижает положительный заряд полимера, приводя, соответственно, к образованию более нейтрального полимера доставки. Желательно, чтобы маскированный полимер оставался растворимым в воде.
Мембраноактивный полиамин может быть конъюгирован с маскирующими агентами в присутствии избытка маскирующих агентов. Указанный избыток маскирующего агента может быть удален от конъюгированного полимера доставки до введения указанного полимер доставки.
В настоящей заявке «стерический стабилизатор» представляет собой неионный гидрофильный полимер (природный, синтетический или неприродный), который предотвращает или ингибирует внутримолекулярные или межмолекулярные взаимодействия полимера, к которому он присоединен, в отличие от полимера, не содержащего стерический стабилизатор. Стерический стабилизатор препятствует вовлечению полимера, к которому он присоединен, в электростатические взаимодействия. Электростатическое взаимодействие представляет собой нековалентное связывание двух или более веществ благодаря силам притяжения между положительными и отрицательными зарядами. Стерические стабилизаторы могут ингибировать взаимодействие с компонентами крови и, таким образом, ингибировать опсонизацию, фагоцитоз и захват ретикулоэндотелиальной системой. Стерические стабилизаторы, таким образом, могут повышать время циркуляции в кровотоке молекул, к которым они присоединены. Стерические стабилизаторы также могут предотвращать агрегацию полимера. Предпочтительный стерический стабилизатор представляет собой полиэтиленгликоль (PEG) или производное PEG. В настоящей заявке предпочтительный PEG может содержать примерно 1-500 или 2-25 этиленгликолиевых мономеров. В настоящей заявке средняя молекулярная масса предпочтительного PEG может также составлять примерно 85-20,000 Дальтон (Да), примерно 85-1000 Да. В настоящей заявке стерические стабилизаторы предотвращают или ингибируют внутримолекулярные или межмолекулярные взаимодействия полимера, к которому они присоединены, в водном растворе, по сравнению с полимером, не содержащим стерический стабилизатор.
«Нацеливающие лиганды» улучшают фармакокинетические свойства или биораспределение конъюгата, к которому они присоединены, для улучшения клеточно- или тканеспецифического распределения и клеточно-специфического захвата конъюгата. Для ясности, В настоящей заявке термин «нацеливающий лиганд» применяется для обозначения нацеливающего лиганда, который присоединен к дипептидному маскирующему агенту, и «нацеливающая группа» представляет собой нацеливающий лиганд, который связан с полинуклеотидом РНКи в конъюгате полинуклеотид РНКи-нацеливающая группа. Нацеливающие лиганды усиливают связывание молекулы с клеткой-мишенью. Таким образом, нацеливающие лиганды могут улучшать фармакокинетические свойства или биораспределение конъюгата, к которому они присоединены, обеспечивая улучшение клеточного распределения и клеточного захвата указанного конъюгата. Связывание нацеливающего лиганда с клеткой или клеточным рецептором может вызывать эндоцитоз. Нацеливающие лиганды могут являться моновалентными, бивалентными, тривалентными, тетравалентными или иметь бол