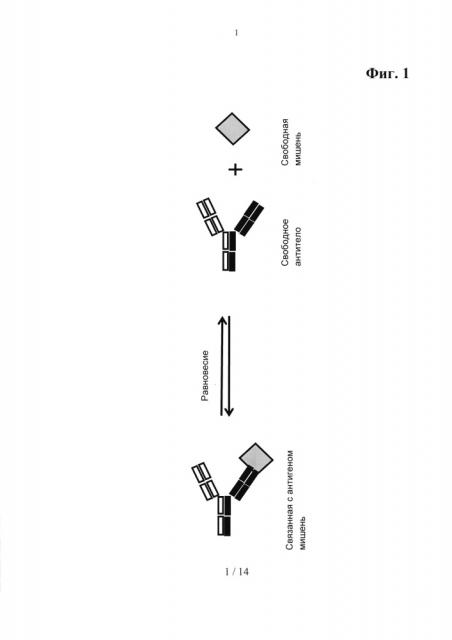
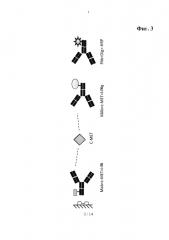
Способ детекции партнера по связыванию мультиспецифического связывающего агента
Иллюстрации
Показать всеГруппа изобретений относится к области химии и представляет собой способ иммуноферментного анализа. Предложен способ детекции свободного антигена биоспецифического антитела в образце, в котором антиген, подлежащий определению, может быть специфически связан с первым сайтом связывания биоспецифического антитела, включающий этап инкубации образца, содержащего свободный антиген и биоспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой. Заявленная группа изобретений позволяет эффективно определить наличие/концентрацию свободного антигена биоспецифического антитела в образце. 2 н. и 7 з.п. ф-лы, 13 ил., 9 пр.
Реферат
Данное изобретение относится к способу детекции/определения свободного, т.е. не входящего в состав комплекса, партнера по связыванию мультиспецифического связывающего агента, который может специфически связываться с мультиспецифическим связывающим агентом в образце, при этом перед детекцией свободного партнера по связыванию из образца элиминируют партнер по связыванию, связанный с мультиспецифическим связывающим агентом. Подвергшийся элиминации мультиспецифический связывающий агент может использоваться для детекции/определения партнера по связыванию, входящего в состав комплекса.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Стандартный твердофазный иммуноферментный анализ с использованием антител включает образование комплекса между антителом, адсорбированным/иммобилизованным на твердой фазе (захватывающее антитело), антигеном и антителом, распознающим другой эпитоп антигена, конъюгированным с ферментом или детектируемой меткой (меченое антитело). В анализе происходит образование «сэндвича»: твердая фаза/захватывающее антитело/антиген/меченое антитело. В реакции, катализируемой в анализе сэндвич-типа, активность фермента, конъюгированного с антителом, пропорциональна концентрации антигена в инкубационной среде. Исследования с использованием антиидиотипических антител упоминаются, например, в патентах US 5,219,730; WO 87/002778; ЕР 0139389 и ЕР 0170302. Wadhwa, Μ., et al. (J. Immunol. Methods 278 (2003) 1-17) предложили способ детекции, измерения и характеризации нежелательных антител, образование которых вызывают терапевтически активные биопрепараты. Способ получения антиидиотипических антител описан в ЕР 1917854.
Chen, Y.-P., et al. (Clin. Vac. Immunol. 14 (2007) 720-725) предложили способ быстрой детекции поверхностного антигена вируса гепатита В методом агглютинации, опосредованной биспецифическим диателом, направленным против человеческих эритроцитов и поверхностного антигена вируса гепатита В. Porter, R., et al. предложили электроактивную систему для иммунологического анализа (EASI assay, от англ. electro-active system of immuno-assay), в котором применяются электроды с самособирающимся монослоем (Biosensors Bioelec. 16 (2001) 9-12). Иммуноферментный анализ для определения человеческого фактора некроза опухоли-альфа (hTNF-alpha) с применением биспецифических антител к hTNF-alpha и пероксидазе хрена разработан Berkova, Ν., et al. (Biotechnol. Appl. Biochem. 23 (1996) 163-171). EP 0 962 771 описывает детектирующее устройство и способ его работы. Reinhartz, H.W., et al. (Analyst 121 (1996) 767-771) предложили биспецифическое мультивалентное антитело, охарактеризованное методом изучения непосредственного взаимодействия биомолекул в режиме реального времени, для проведения непрямого конкурентного (ингибиторного) иммуноферментного анализа. Получение биспецифических антител химическим методом описано Doppalapudi, V.R., et al. (Proc. Natl. Acad. Sci. 107 (2010) 22611-22616).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данной заявке предложен способ детекции наличия или определения концентрации свободного, т.е. не входящего в состав комплекса партнера по связыванию в образце, где партнер по связыванию может быть специфически связан по меньшей мере с одной связывающей детерминантой мультиспецифического связывающего агента, т.е. с первой связывающей детерминантой.
Было обнаружено, что перед определением концентрации свободного партнера по связыванию предпочтительно элиминировать из образца партнер по связыванию, который специфически связан с мультиспецифическим связывающим агентом, т.е. комплекс партнер по связыванию-мультиспецифический связывающий агент.
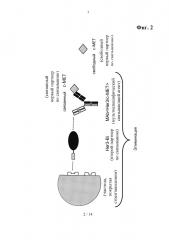
Согласно способам, предложенным в данной заявке, элиминация мультиспецифического связывающего агента осуществляется путем инкубации образца либо с партнером по связыванию, т.е. со вторым партнером по связыванию, который может быть специфически связан с другой, т.е. со второй связывающей детерминантой мультиспецифического связывающего агента, которая не связывается с партнером по связыванию, подлежащим определению, т.е. с первым партнером по связыванию, либо с моноспецифическим связывающим агентом, который специфически связывается с одной связывающей детерминантой мультиспецифического связывающего агента, при этом моноспецифический связывающий агент специфически связывается со связывающей детерминантой мультиспецифического связывающего агента, которая не связывается с партнером по связыванию, подлежащим определению (см. Фиг. 2).
Один аспект данного описания относится к способу определения in vitro наличия и/или концентрации (первого) антигена биспецифического антитела в образце, где антиген, подлежащий определению, может быть специфически связан с первой связывающей детерминантой биспецифического антитела и причем антиген находится в комплексе с биспецифическим антителом (комплекс антиген-биспецифическое антитело), включающему этап:
- инкубации образца, содержащего антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- детекции комплекса антиген-биспецифическое антитело-антиидиотипическое антитело и таким образом, определения наличия и/или концентрации антигена биспецифического антитела.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- инкубации комплекса, образованного на первом этапе, с антителом, которое специфически связывается с эпитопом антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения наличия и/или концентрации антигена биспецифического антитела в образце.
В одном воплощении способ предназначен для определения наличия и/или концентрации антигена биспецифического антитела, находящегося в комплексе с биспецифическим антителом.
В одном воплощении способ включает следующие этапы:
- получение образца, содержащего антиген и биспецифическое антитело, где по меньшей мере 90% антигена находится в комплексе с биспецифичским антителом,
- инкубацию образца, содержащего антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- инкубацию комплекса, образованного на первом этапе, с антителом, которое специфически связывается с эпитопом антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения наличия и/или концентрации антигена биспецифического антитела в образце.
В одном воплощении способ включает следующие этапы:
- инкубацию образца, содержащего антиген и биспецифическое антитело, с таким количеством биспецифического антитела, чтобы в образце по меньшей мере 90% антигена находилось в составе комплекса с биспецифическим антителом,
- инкубацию образца, содержащего антиген, находящийся в комплексе с биспецифическим антителом, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- инкубацию комплекса, образованного на предыдущем этапе, с антителом, которое специфически связывается с эпитопом антигена, отличным от эпитопа, связанного с биспецифическим антителом и таким образом определения наличия и/или концентрации антигена биспецифического антитела в образце.
В одном воплощении концентрация биспецифического антитела составляет приблизительно от 1 мкг/мл до 10 мкг/мл, предпочтительно приблизительно 1,5 мкг/мл.
В одном воплощении коцентрация биспецифического антитела составляет 1 мг/мл образца.
В одном воплощении по меньшей мере 95% антигена находится в комплексе с биспецифическим антителом. В одном воплощении по меньшей мере 98% антигена находится в комплексе с биспецифическим антителом.
Один аспект данного описания представляет собой способ определения in vitro концентрации связанного с антителом (первого) антигена биспецифического антитела в образце, причем антиген может быть специфически связан с первой связывающей детерминантой биспецифического антитела, включающий этапы:
- инкубации первой аликвоты образца, содержащего антиген и биспецифическое антитело, с таким количеством биспецифического антитела, чтобы в образце по меньшей мере 90% антигена находилось в комплексе с биспецифическим антителом,
- инкубации образца, содержащего антиген, находящийся в комплексе с биспецифическим антителом, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- инкубации комплекса, образованного на предыдущем этапе, с антителом, которое специфически связывается с эпитопом антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения наличия и/или концентрации антигена биспецифического антитела в образце и таким образом определения общей концентрации антигена, присутствующего в образце,
- инкубации второй аликвоты образца, содержащего антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, при этом антиидиотипическое антитело связано с твердой фазой, и
- инкубации образованного комплекса с антителом, которое специфически связывается с эпитопом антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения концентрации свободного антигена биспецифического антитела, присутствующего в образце, и
- определения концентрации связанного с антителом антигена биспецифического антитела по разнице между общей концентрацией антигена, присутствующего в образце, и концентрацией свободного антигена, присутствующего в образце.
В одном воплощении концентрация биспецифического антитела составляет приблизительно от 1 мкг/мл до 10 мкг/мл, предпочтительно приблизительно 1,5 мкг/мл.
В одном воплощении концентрация биспецифического антитела составляет 1 мг/мл образца.
Один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации партнера по связыванию (антигена, мишени, аналита), который может быть специфически связан с первой связывающей детерминантой мультиспецифического связывающего агента, причем фракцию партнера по связыванию, связанного с мультиспецифическим связывающим агентом, присутствующую в образце, элиминируют перед определением партнера по связыванию путем инкубации образца со вторым партнером по связыванию, который может специфически связываться со второй связывающей детерминантой мультиспецифического связывающего агента, или с моноспецифическим связывающим агентом, специфически связывающимся со второй связывающей детерминантой мультиспецифического связывающего агента.
В одном воплощении партнер по связыванию, подлежащий определению, является партнером по связыванию, не входящим в состав комплекса, или свободным партнером по связыванию.
Таким образом, один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации (первого) партнера по связыванию мультиспецифического связывающего агента, причем партнер по связыванию может быть специфически связан с первой связывающей детерминантой мультиспецифического связывающего агента, включающий этап:
- инкубации образца, содержащего (первый) партнер по связыванию и мультиспецифический связывающий агент, со вторым партнером по связыванию, который может быть специфически связан со второй связывающей детерминантой мультиспецифического связывающего агента, отличной от первой связывающей детерминанты.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего (первый) партнер по связыванию и мультиспецифический связывающий агент, с моноспецифическим связывающим агентом, который специфически связывается со второй связывающей детерминантой мультиспецифического связывающего агента, отличной от первой связывающей детерминанты, и
- определения концентрации (свободного первого) партнера по связыванию в образце, из которого элиминирован мультиспецифический связывающий агент.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего (первый) партнер по связыванию и мультиспецифический связывающий агент, с моноспецифическим связывающим агентом, который специфически связывается со второй связывающей детерминантой мультиспецифического связывающего агента, отличной от первой связывающей детерминанты,
- элиминации из образца комплекса моноспецифический связывающий агент-мультиспецифический связывающий агент перед определением наличия или концентрации свободного партнера по связыванию, и
- определения концентрации (свободного первого) партнера по связыванию в образце, из которого элиминирован мультиспецифический связывающий агент.
При инкубации со вторым партнером по связыванию, который может специфически связываться со второй связывающей детерминантой мультиспецифического связывающего агента, из образца элиминируют мультиспецифический связывающий агент. Одновременно из образца также удаляют комплексы (первый) партнер по связыванию-мультиспецифический связывающий агент.
В одном воплощении мультиспецифический связывающий агент выбран из антитела, химерного полипептида, содержащего антитело или фрагмент антитела и полипептид, не являющийся антителом, химерного полипептида, содержащего антитело или фрагмент антитела и растворимый рецептор, или химерного полипептида, содержащего антитело или фрагмент антитела и пептидную связывающую молекулу.
В одном воплощении мультиспецифический связывающий агент представляет собой антитело. В одном воплощении антитело представляет собой биспецифическое антитело или триспецифическое антитело, или тетраспецифическое антитело, или пентаспецифическое антитело, или гексаспецифическое антитело. В одном воплощении антитело представляет собой биспецифическое антитело.
В одном воплощении моноспецифический связывающий агент представляет собой антиидиотипическое антитело.
В одном воплощении связывающая детерминанта представляет собой сайт связывания или пару вариабельных доменов тяжелой цепи антитела и легкой цепи антитела.
В одном воплощении второй партнер по связыванию или моноспецифический связывающий агент связан с твердой фазой.
В одном воплощении второй партнер по связыванию биотинилирован, а поверхность твердой фазы покрыта стрептавидином. В одном воплощении твердая фаза представляет собой покрытые стрептавидином парамагнитные частицы или покрытые стрептавидином гранулы сефарозы.
Один аспект данного описания представляет собой способ иммунологического определения наличия и/или концентрации партнера по связыванию мультиспецифического связывающего агента в образце с помощью иммунологического анализа, в котором мультиспецифический связывающий агент элиминирован из образца перед определением партнера по связыванию.
В одном воплощении всех аспектов данного описания партнер по связыванию представляет собой свободный партнер по связыванию, т.е. партнер по связыванию, который не связан или не находится в комплексе с мультиспецифическим связывающим агентом.
В одном воплощении второй партнер по связыванию представляет собой биотинилированный второй партнер по связыванию и конъюгирован с твердой фазой при помощи стрептавидина.
В одном воплощении способов данного описания второй партнер по связыванию представляет собой смесь, содержащую по меньшей мере два вторых партнера по связыванию, у которых различаются сайты, по которым они конъюгированы с твердой фазой. В одном воплощении сайт представляет собой аминокислотную позицию в аминокислотной последовательности второго партнера по связыванию.
В одном воплощении первый партнер по связыванию представляет собой полипептид.
В одном воплощении второй партнер по связыванию представляет собой полипептид.
В одном воплощении конъюгацию полипептида с его партнером по конъюгации осуществляют путем химического связывания по N-концевым и/или ε-аминогруппам (лизина), ε-аминогруппам различных лизинов, карбоксильным, сульфгидрильным, гидроксильным и/или фенольным функциональным группам аминокислотного скелета полипептида и/или спиртовым группам углеводных компонентов полипептида.
В одном воплощении второй партнер по связыванию представляет собой смесь, содержащую второй партнер по связыванию, конъюгированный с твердой фазой по меньшей мере через две различные аминогруппы. Такое присоединение через различные аминогруппы может осуществляться путем ацилирования на первом этапе части ε-аминогрупп при помощи химических защитных агентов, например, путем введения цитраконильных групп. На втором этапе конъюгирование осуществляется через оставшиеся аминогруппы. Впоследствии цитраконильные группы удаляют, а партнер по связыванию конъюгируют с твердой фазой через оставшиеся свободные аминогруппы, т.е. полученный партнер по связыванию конъюгируют с твердой фазой через аминогруппы, которые не были защищены цитраконильными группами. Подходящие химические защитные агенты образуют связи с незащищенными аминогруппами боковых цепей, которые являются менее стабильными и отличаются связей, образующихся на N-конце. Известно множество химических защитных агентов (см., например, ЕР 0651761). В одном воплощении химические защитные агенты включают циклические ангидриды дикарбоновых кислот, такие как ангидрид малеиновой или цитраконовой кислот.
В одном воплощении второй партнер по связыванию конъюгируют с твердой фазой при помощи пассивной адсорбции. Пассивная адсорбция описана, например Butler, J.Ε., "Solid Phases in Immunoassay" (1996) 205-225 и Diamandis, E.P., and Christopoulos, Т.К. (Editors), "Immunoassay" (1996) Academic Press (San Diego).
В одном воплощении второй партнер по связыванию конъюгирован (иммобилизован) при помощи специфически связывающейся пары. В одном воплощении такая связывающаяся пара (первый компонент/второй компонент) выбрана из стрептавидина или авидина/биотина, антитела/антигена (см., например, Hermanson, G.T., et al., Bioconjugate Techniques, Academic Press (1996)), лектина/полисахарида, стероида/стероид-связывающего белка, гормона/рецептора гормона, фермента/субстрата, IgG/белка А и/или G и т.д. В одном воплощении второй партнер по связыванию конъюгирован с биотином, а иммобилизация осуществляется через иммобилизованный авидин или стрептавидин.
Один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации (первого) антигена мультиспецифического антитела в образце, в котором антиген, подлежащий определению, может быть специфически связан с первой связывающей детерминантой мультиспецифического антитела, включающий этап:
- инкубации образца, содержащего мультиспецифическое антитело, (первый) антиген, связанный с мультиспецифическим антителом, и свободный (первый) антиген, со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, отличной от первой связывающей детерминанты.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего мультиспецифическое антитело, (первый) антиген, связанный с мультиспецифическим антителом, и свободный (первый) антиген, со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, отличной от первой связывающей детерминанты, и
- определения концентрации (первого) антигена в образце, из которого элиминировано мультиспецифическое антитело.
В одном воплощении способ включает этапы:
- инкубации образца, содержащего (первый) антиген и мультиспецифическое антитело, со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, отличной от первой связывающей детерминанты,
- элиминации комплекса второй антиген-мультиспецифическое антитело из образца перед определением наличия или концентрации свободного антигена, и
- определения концентрации (первого) антигена в образце, из которого элиминировано мультиспецифическое антитело.
При инкубации со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, мультиспецифическое антитело удаляют из образца. Одновременно из образца также удаляют комплексы (первый) антиген-мультиспецифическое антитело.
В одном воплощении образец содержит мультиспецифическое антитело, свободный (первый) антиген и комплексы мультиспецифическое антитело-антиген, и осуществляют детекцию свободного (первого) антигена мультиспецифического антитела.
В одном воплощении второй антиген конъюгирован с парамагнитной частицей.
В одном воплощении второй антиген конъюгирован с твердой фазой.
В одном воплощении второй антиген биотинилирован, а поверхность твердой фазы покрыта стрептавидином. В одном воплощении твердая фаза представляет собой покрытые стрептавдином парамагнитные частицы или покрытые стрептавидином гранулы сефарозы.
В одном воплощении связывающая детерминанта представляет собой сайт связывания. В одном воплощении сайт связывания представляет собой пару вариабельных доменов тяжелой цепи антитела и легкой цепи антитела.
В одном воплощении способ включает следующие этапы:
- инкубацию образца, содержащего мультиспецифическое антитело, связанный с мультиспецифическим антителом (первый) антиген и свободный (первый) антиген, со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, отличной от первой связывающей детерминанты, для образования комплекса второй антиген-мультиспецифическое антитело, и
- удаление из образца комплекса второй антиген-мультиспецифическое антитело.
В одном воплощении комплекс второй антиген-мультиспецифическое антитело представляет собой смесь комплекса второй антиген-мультиспецифическое антитело и комплекса второй антиген-мультиспецифическое антитело-(первый) антиген.
В одном воплощении способ включает следующие этапы:
- инкубацию образца, содержащего (первый) антиген и мультиспецифическое антитело, со вторым антигеном, который может быть специфически связан со второй связывающей детерминантой мультиспецифического антитела, отличной от первой связывающей детерминанты, для образования комплекса второй антиген-мультиспецифическое антитело,
- удаление из образца комплекса второй антиген-мультиспецифическое антитело, и
- определение концентрации (первого) антигена в образце, из которого элиминировано мультиспецифическое-антитело.
В одном воплощении определение концентрации (первого) антигена включает следующие этапы:
- инкубацию образца, из которого элиминировано мультиспецифическое антитело, с захватывающим антителом, которое специфически связывается с (первым) антигеном, для образования комплекса захватывающее антитело-(первый) антиген, и
- установление зависимости между образованием комплекса захватывающее антитело-(первый) антиген и концентрацией в образце (первого) антигена.
В одном воплощении определение концентрации (первого) антигена включает следующие этапы:
- инкубацию образца, из которого элиминировано мультиспецифическое антитело, с захватывающим антителом, которое специфически связывается с (первым) антигеном, для образования комплекса захватывающее антитело-(первый) антиген,
- инкубацию комплекса захватывающее антитело-(первый) антиген с меченым антителом, где захватывающее антитело и меченое антитело связываются с неперекрывающимися эпитопами (первого) антигена, и
- установление зависимости между образованием комплекса захватывающее антитело-(первый) антиген-меченое антитело и концентрацией в образце антигена.
В одном воплощении определение концентрации (первого) антигена включает следующие этапы:
- инкубацию образца, из которого элиминировано мультиспецифическое антитело, с захватывающим антителом, которое специфически связывается с (первым) антигеном, для образования комплекса захватывающее антитело-(первый) антиген,
- инкубацию комплекса захватывающее антитело-(первый) антиген с меченым антителом, при которой захватывающее антитело и меченое антитело связываются с неперекрывающимися эпитопами (первого) антигена,
- инкубацию комплекса захватывающее антитело-(первый) антиген-меченое антитело с детектирующим антителом, содержащим детектируемую метку, где детектирующее антитело специфически связывается с эпитопом меченого антитела, находящимся за пределами вариабельных доменов меченого антитела, и
- установление зависимости между образованием комплекса захватывающее антитело-(первый) антиген-меченое антитело и концентрацией в образце (первого) антигена.
В одном воплощении мультиспецифическое антитело представляет собой биспецифическое антитело, которое имеет первую связывающую детерминанту, которая специфически связывается с первым антигеном или первым эпитопом антигена, и которое имеет вторую связывающую детерминанту, которая специфически связывается со вторым антигеном или вторым эпитопом антигена.
В одном воплощении первый антиген и второй антиген представляют собой один и тот же антиген, и первая связывающая детерминанта связывается с первым эпитопом антигена, а вторая связывающая детерминанта связывается со вторым эпитопом антигена, причем второй эпитоп представляет собой эпитоп, не перекрывающийся с первым эпитопом, а связывание первой связывающей детерминанты не препятствует связыванию второй связывающей детерминанты.
В одном воплощении способ включает этап:
- элиминации из образца образованного комплекса перед определением наличия или концентрации (первого) антигена.
Один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации (первого) антигена мультиспецифического антитела в образце, где антиген, подлежащий определению, может быть специфически связан с первой связывающей детерминантой мультиспецифического антитела, включающий этап:
- инкубации образца, содержащего (первый) антиген, с комплексом биспецифического антитела и второго антигена или с комплексом биспецифического антитела и антиидиотипического антитела, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты.
В одном воплощении второй антиген представляет собой меченый второй антиген. В одном воплощении второй антиген иммобилизован на твердой фазе при помощи специфически связывающейся пары. В одном воплощении специфически связывающаяся пара представляет собой биотин и стрептавидин.
В одном воплощении способ включает в качестве второго этапа:
- инкубацию комплекса, образованного на первом этапе, с антителом, которое специфически связывается с эпитопом первого антигена, отличным от эпитопа, связанного с биспецифическим антителом.
Один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации (первого) антигена биспецифического антитела в образце, в котором антиген, подлежащий определению, может быть специфически связан с первой связывающей детерминантой биспецифического антитела, включающий этап:
- инкубации образца, содержащего (первый) антиген, с биспецифическим антителом и вторым антигеном или с биспецифическим антителом и антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, где второй антиген или антиидиотипическое антитело связаны с твердой фазой.
В одном воплощении способ включает в качестве второго этапа:
- инкубацию комплекса, образованного на первом этапе, с антителом, которое специфически связывается с эпитопом первого антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения в образце концентрации (первого) антигена биспецифического антитела.
Один аспект данного описания представляет собой способ определения in vitro наличия и/или концентрации (первого) антигена биспецифического антитела в образце, находящегося в комплексе с биспецифическим антителом (комплекс первый антиген-биспецифическое антитело), где антиген, подлежащий определению, может быть специфически связан с первой связывающей детерминантой биспецифического антитела, включающий этап:
- инкубации образца, содержащего (первый) антиген и биспецифическое антитело, с антиидиотипическим антителом, которое специфически связывается со второй связывающей детерминантой биспецифического антитела, отличной от первой связывающей детерминанты, где антиидиотипическое антитело связано с твердой фазой.
В одном воплощении способ включает в качестве второго этапа:
- инкубацию комплекса, образованного на первом этапе, с антителом, которое специфически связывается с эпитопом первого антигена, отличным от эпитопа, связанного с биспецифическим антителом, и таким образом определения в образце концентрации (первого) антигена биспецифического антитела, находящегося в комплексе с биспецифическим антителом (комплекс первый антиген-биспецифическое антитело).
В одном воплощении способ включает этап:
- элиминации образованного комплекса из образца перед определением наличия или концентрации (первого) антигена.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В данном документе описан способ предварительной обработки образца in vitro для детекции "свободного и/или общего партнера по связыванию" мультиспецифических связывающих агентов, таких как биспецифические антитела/лекарственные средства, в образцах для доклинических и клинических исследований.
Было обнаружено, что перед детекцией свободного партнера по связыванию предпочтительно осуществлять элиминацию из образца мультиспецифического связывающего агента.
Было обнаружено, что для перевода общего партнера по связыванию, присутствующего в образце, в соответствующий комплекс предпочтительно инкубировать образец с мультиспецифическим связывающим агентом.
Было обнаружено, что предпочтительно осуществлять захват мультиспецифического связывающего агента с помощью антиидиотипического антитела.
В данном документе описано применение второго партнера по связыванию, который может специфически связываться со второй связывающей детерминантой терапевтически активного мультиспецифического антитела при определении уровня (свободного первого) антигена, который может быть но не является связанным с первой связывающей детерминантой терапевтически активного мультиспецифического антитела. Второй антиген применяют для элиминации из образца мультиспецифического антитела и комплексов мультиспецифическое антитело-антиген, подлежащий определению.
Таким образом, в данном документе описан способ детекции in vitro свободного (первого) партнера по связыванию (антигена, мишени, аналита) мультиспецифического связывающего агента, который может быть специфически связан с первой связывающей детерминантой мультиспецифического связывающего агента, где мультиспецифический связывающий агент элиминирован из образца перед определением свободного партнера по связыванию путем инкубации образца со вторым партнером по связыванию, который может быть специфически связан со второй связывающей детерминантой мультиспецифического связывающего агента, отличной от первой связывающей детерминанты, и таким образом элиминации из образца мультиспецифического связывающего агента и комплексов мультиспецифический связывающий агент-(первый) партнер по связыванию.
Ниже способ по данному описанию проиллюстрирован на примере мультиспецифического антитела, специфически связывающегося с множеством антигенов или эпитопов того же антигена, как воплощения мультиспецифического связывающего агента и (первого) антигена, который может быть специфически связан с первой связывающей детерминантой мультиспецифического антитела, как воплощения (первого) партнера по связыванию.
Термин "антитело" здесь используется в широком смысле и охватывает антитела с различной структурой, включая моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител, при условии, что они проявляют желаемую антигенсвязывающую активность, но не ограничивается ими.
В некоторых воплощениях антитело представляет собой мультиспецифическое антитело, например, биспецифическое антитело. Мультиспецифические антитела представляют собой моноклональные антитела, имеющие связывающие детерминанты по меньшей мере для двух различных сайтов. В некоторых воплощениях одна из связывающих детерминант предназначена для первого антигена, а другая - для отличающегося второго антигена. В некоторых воплощениях биспецифические антитела могут связывать два различных эпитопа одного и того же антигена. Биспецифические антитела могут быть созданы в виде полноразмерных антител или фрагментов антител. В одном воплощении антитело представляет собой биспецифическое антитело, которое специфически связывается с первым и вторым антигеном. В одном воплощении биспецифическое антитело имеет i) первую связывающую детерминанту, которая специфически связывается с первым антигеном или первым эпитопом антигена, и ii) вторую связывающую детерминанту, которая специфически связывается со вторым антигеном или вторым эпитопом того же самого антигена. В одном воплощении второй эпитоп того же самого антигена представляет собой неперекрывающийся эпитоп.
Мультиспецифические антитела описаны в WO 2009/080251, WO 2009/080252, WO 2009/080253, WO 2009/080254, WO 2010/112193, WO 2010/115589, WO 2010/136172, WO 2010/145792 или WO 2010/145793.
Фрагмент антитела" обозначает молекулу, отличную от интактного антитела, содержащую часть интактного антитела, которая связывается с антигеном, связывающимся с интактным антителом. Примеры фрагментов антител включают Fv, Fab, Fabʹ, Fabʹ-SH, F(abʹ)2, диатела, линейные антитела, молекулы одноцепочечных антител (например, scFv) и мультиспецифические антитела, образованные из фрагментов антител, но не ограничиваются ими.
"Класс" антитела обозначает тип константного домена или константного участка его тяжелой цепи. Существует пять основных классов антител: IgA, IgD, IgE, IgG и IgM, и некоторые из них можно подразделить на подклассы (изотипы), например, IgG1, lgG2, lgG3, lgG4, IgA1 и IgA2. Константные домены тяжелых цепей, соответствующие различным классам иммуноглобулинов, обозначаются α, δ, ε, γ и μ, соответственно.
Термин "свободный антиген" обозначает антиген, который может быть специфически связан со связывающей детерминантой антитела, но в данный момент не связан с данной связывающей детерминантой. В одном воплощении свободный антиген представляет собой антиген, не связанный с антителом, или антиген, не находящийся в комплексе с антителом.
Термин "Fc-фрагмент" здесь использу