Применение ингибитора ароматазы для лечения гипогонадизма и родственных заболеваний
Иллюстрации
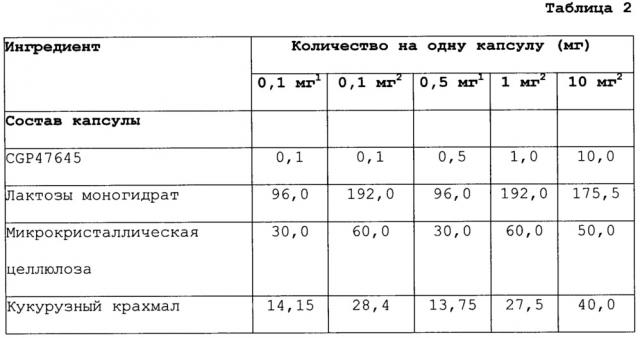
Показать всеГруппа изобретений относится к медицине, а именно к эндокринологии, и может быть использована для лечения гипогонадизма. Способ по изобретению включает введение пациентам мужского пола с уровнем общего тестостерона в сыворотке ниже 400 нг/дл 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила в дозе 0,001-1,0 мг еженедельно. Композиция по изобретению включает фармацевтическую композицию и инструкции по введению. Использование изобретения позволяет повысить уровень тестостерона у указанных пациентов. 3 н. и 16 з.п. ф-лы, 2 табл., 5 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Это изобретение относится к способу повышения уровней тестостерона и лечению гипогонадизма и родственных заболеваний с помощью ингибитора ароматазы 4,4’-[фтор-(1Н-1,2,4-триазол-1- ил)метилен]бисбензонитрила. Кроме того, настоящее изобретение относится к способу повышения уровней тестостерона и лечения гипогонадизма и родственных заболеваний с помощью ингибитора ароматазы 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила при конкретном режиме дозирования. Изобретение также относится к фармацевтическим композициям, включающим указанный ингибитор ароматазы 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрил, необязательно, в комбинации с другими активными ингредиентами. Кроме того, настоящее изобретение относится к фармацевтическим наборам, включающим указанные фармацевтические композиции вместе с инструкциями по их применению.
УРОВЕНЬ ТЕХНИКИ
Фермент ароматаза (CYP 19) в высокой степени экспрессирует в жировой ткани, где этот фермент превращает тестостерон в эстрадиол. У страдающего полнотой или ожирением человека избыток жировой ткани объясняют избыточной активностью ароматазы, которая, в свою очередь, приводит к более высоким уровням эстрадиола, как у мужчин, так и у женщин. У страдающих полнотой или ожирением мужчин относительный избыток эстрадиола может возвращаться в гипоталамо-гипофизарную систему, подавляя секрецию гонадотропина и, в силу этого, подавляя продукцию тестикулярного тестостерона, а также сперматогенез. Таким образом, тяжелая степень ожирения связана с относительным дефицитом андрогена у мужчин. Это состояние могут называть ОНН, или гипогонадотропным гипогонадизмом при ожирении, или гипогонадотропным гипогонадизмом у мужчин, страдающих ожирением.
Согласно данным Национального исследования здоровья населения и просвещения в области питания США, за период 1999-2002 годы 27,5% мужчин старше 20 лет в США имели индекс массы тела (BMI) выше 30 кг/м2. Ожидается, что частота случаев ожирения будет продолжать увеличиваться и в США, и в развитых и развивающихся странах по всему миру. При одном исследовании 160 мужчин, которым было рекомендовано терапевтическое или хирургическое лечение ожирения, гипогонадотропный гипогонадизм присутствовал суммарно у 36% пациентов. В этом исследовании, частота случаев гипогонадотропного гипогонадизма возрастала линейно с 7,4% для пациентов с величиной BMI 30-35 кг/м2 до 59,2% для пациентов с величиной BMI выше 50 кг/м2 [Hofstra, et al., 2008]. Исходя из частоты случаев ожирения можно приблизительно оценить, что вследствие гипогонадотропного гипогонадизма могут иметь андрогенный дефицит до 1,5 миллиона мужчин в США и 1 миллион мужчин в Европе.
Многочисленные последствия дефицита тестостерона включают симптомы пониженного либидо, уменьшения спонтанных эрекций, пониженной фертильности, потери волосяного покрова и снижения потребности в бритье, низкой минеральной плотности костной ткани, повышенного риска переломов, уменьшения мышечной массы и мышечной силы и повышения утомляемости мышц [Bhasin, et al., 2006]. Кроме того, более поздние исследования показали, что дефицит тестостерона у пожилых мужчин и мужчин, страдающих ожирением, связан также с метаболическими нарушениями, включающими резистентность к инсулину, непереносимость глюкозы и липидные нарушения, что способствует повышенной частоте возникновения метаболического синдрома и, вероятно, повышает риск возникновения сердечно-сосудистого заболевания. В одном исследовании, до 15% мужчин, страдающих диабетом, имели очевидный гипогонадизм (тестостерон <300 нг/дл или <8 нмоль/л) и до 50% имели уровень тестостерона в нижнем диапазоне нормальных значений (<12 нмоль/л или <450 нг/дл) [Kapoor, et al., 2006 and 2007]. Была установлена взаимосвязь между низкими уровнями тестостерона и факторами риска возникновения различных сердечно-сосудистых заболеваний. Недавние эпидемиологические исследования также обнаружили зависимость между смертностью от сердечно-сосудистых заболеваний и низким уровнем тестостерона [Maggio et al., 2009].
Рекомендации по лечению гипогонадизма у мужчин разработаны несколькими организациями, включающими Общество эндокринологов США, которое заявляет, что "для мужчин с симптоматикой андрогенного дефицита, которые имеют низкие уровни тестостерона, рекомендуется терапия тестостероном, для того чтобы вызвать и поддерживать у пациентов вторичные половые признаки и улучшить их половую функцию, хорошее самочувствие, увеличить мышечную массу и мышечную силу и минеральную плотность костной ткани" [Bhasin, et al., 2006]. Заместительная терапия тестостероном обычно рекомендуется в форме внутримышечного или трансдермального введения в качестве стандартного лечения мужчин с документально подтвержденным гипогонадизмом (тестостерон <300 нг/дл, сопровождаемый симптомами низкого уровня тестостерона), и эта терапия может нормализовать либидо, мышечную массу и мышечную силу [Bhasin, et al., 2006]. Кроме того, заместительная терапия тестостероном улучшает состояние резистентности к инсулину у мужчин с гипогонадизмом [Naharci, et al.,. 2007].
Помимо полноты и ожирения и связанной с ними избыточной активностью ароматазы, другие причины гипогонадизма у мужчин включают первичную тестикулярную недостаточность, которая может быть обусловлена внутренними нарушениями в организме или может быть приобретенной в результате травмы, инфекции и химиотерапии или лучевой терапии, и вторичную недостаточность с угнетением гонадотропинов, которая может быть следствием стресса, сопутствующих заболеваний или гипоталамо-гипофизарных расстройств.
Применяемые в настоящее время при дефиците тестостерона терапии представляют собой ограниченный выбор. Большинство гипогонадных мужчин подвергают лечению путем внутримышечных инъекций тестостерона каждые 2-4 недели, что обычно требует визита в медицинское учреждение к лечащему врачу. Некоторые мужчины выбирают тестостероновые гели или пластыри, которые обычно применяют ежедневно. Мужчины с гипогонадотропным гипогонадизмом, желающие восстановить фертильность, могут быть подвергнуты лечению путем внутримышечных или подкожных инъекций хорионического гонадотропного гормона (HCG) или гонадотропинов. При заместительной терапии тестостероном возникает ряд осложнений, которые могут включать гинекомастию в результате избыточного превращения экзогенного тестостерона в эстрадиол, инфертильность в результате подавления гонадотропинов, перемены настроения вследствие подъема и падения уровня тестостерона после внутримышечных инъекций, и раздражение в месте инъекции или месте применения лекарственной формы. Избыток тестостерона может приводить к полицитемии (эритроцитозу), гипертрофии предстательной железы, приступам апноэ во сне и ухудшению состояния при сердечной недостаточности, а также к агрессивности. Общество эндокринологов США рекомендует "воздерживаться от проведения терапии тестостероном в случае пациентов с раком грудной железы или раком предстательной железы, с пальпируемым узлом в предстательной железе или ее уплотнением или с уровнем простатического специфического антигена большим чем 3 нг/мл, без дополнительного урологического обследования, с эритроцитозом (гематокрит >50%), с повышенной вязкостью крови, с нелечеными приступами обструктивного апноэ во время сна, с тяжелыми симптомами со стороны нижних мочевыводящих путей, с количеством баллов по Международной шкале симптомов нарушения простаты (IPSS) [Barry, et al., 1992] большим чем 19, или с сердечной недостаточностью III или IV степени", и обращает внимание на то, что "мужчины, получающие лечение тестостероном, должны подвергаться постоянному контролю на основе стандартизированного плана" [Bhasin, et al., 2006].
Пероральная андрогенная терапия обычно противопоказана в связи с пресистемными воздействиями на печень, которые значительно снижают липопротеин высокой плотности (HDL), повышают тромбообразующие факторы и часто вызывают нарушения функции печени. Эти воздействия андрогенов на печень также ограничивают в настоящее время клиническое применение селективных модуляторов андрогенового рецептора (SARM).
Некоторые имеющиеся в продаже ингибиторы ароматазы также были испытаны на эффективность при лечении гипогонадных мужчин в ряде небольших исследований с целью подтверждения правильности такого подхода. Летрозол, вводимый в дозах 2,5 мг еженедельно, повышал общее содержание тестостерона до области нормальных значений, подавлял общий эстрадиол и повышал содержание лютеинизирующего гормона (LH) и фолликулостимулирующего гормона (FSH) у 12 мужчин, страдающих гипогонадотропным гипогонадизмом [de Boer, et al., 2005, Loves, et al., 2008]. При этом фиксированном интервале дозирования, уровень свободного тестостерона возрастал выше области нормальных значений у приблизительно половины пациентов. Другие исследователи оценили воздействия ингибиторов ароматазы (летрозола [de Boer, et al., 2005, Lapauw, et al., 2009, Loves, et al., 2008], CGS 20267 [Trunet, et al., 1993] и анастрозола [Medras, et al., 2007]) при исследованиях в отсутствие контрольных групп.
Одним существенным недостатком всех проводимых до настоящего времени клинических исследований является то, что используемые в исследованиях ингибиторы ароматазы анастрозол и летрозол создавались для лечения гормонально зависимых типов рака, таких как рак молочной железы у женщин в постклимактерическом периоде, и, вероятно, поэтому они не являются оптимальными для лечения гипогонадизма у пациентов мужского пола, в частности, с точки зрения оптимальных доз и режима дозирования и возможных побочных эффектов. В настоящее время, дозы и режимы дозирования, опробованные при клинических испытаниях, составляют 2,5 мг или 1 мг соответствующего ингибитора ароматазы еженедельно при лечении гипогонадизма, что соответствует дозам, применяемым при адъювантном лечении женщин в постклимактерическом периоде на ранней стадии рака молочной железы с положительной реакцией на рецептор гормона, но не является схемой лечения, оптимизированной для гипогонадизма.
И, действительно, фармакокинетические и фармакодинамические исследования доступных ингибиторов ароматазы на мужчинах с гипогонадизмом показали, что, например, летрозол при еженедельной дозе 2,5 мг приводил в результате к избыточным уровням свободного тестостерона у приблизительно половины пациентов [Loves, et al., 2008]. К настоящему времени еще не проводились исследования с целью всесторонней оценки воздействия ингибиторов ароматазы на уровни тестостерона и способов реального достижения нормализации уровней тестостерона у мужчин с гипогонадизмом.
Таким образом, необходимы оптимизированные схемы лечения, обеспечивающие облегчение связанных с дефицитом тестостерона симптомов гипогонадизма с минимальными побочными эффектами. Создание ингибитора ароматазы, специально предназначенного для пациентов мужского пола с пониженными уровнями тестостерона, позволило бы использовать новый подход для недостаточно целенаправленного в настоящее время лечения этого заболевания.
Помимо клинически опробованных нестероидных ингибиторов ароматазы анастрозола, летрозола и фадрозола, которые рекомендованы для лечения гормонально зависимого рака молочной железы путем ежедневного введения доз в миллиграммовом диапазоне, в патентах и в научной литературе описаны некоторые другие ингибиторы ароматазы. Одним из этих соединений является ингибитор ароматазы 4,4'-[фтор-(1Н-1,2,4-триазол-1- ил)метилен]бисбензонитрил, также известный как 4-[а-4-цианофенил)-а-фтор-1-(1,2,4-триазолил)метил]бензонитрил или CGP47645, впервые описанный в 1992 году [патентные документы ЕР 490 816 и US 5637605], имеющий следующую структурную формулу
Ингибитор CGP47645 представляет собой фторпроизводное летрозола с пролонгированным периодом действия. Предварительные in-vitro и in-vivo эксперименты с этим соединением на крысах и обезьянах показали одинаковую в 10 раз более высокую активность ингибирования ароматазы по сравнению с летрозолом, и продемонстрировали возможность применения схемы лечения с некаждодневным дозированием. Введение раз в неделю 3 мг/кг CGP47645 рассматривали как эффективную дозу, позволяющую достигать медикаментозной стерилизации взрослых самцов крыс [Batzl-Hartraann et al., 1994]. Был сделан вывод, что период полувыведения CGP47645 является достаточно длительным для поддержания эффективности эндокринного действия, подобного эффекту овариэктомии, при схеме дозирования один раз в неделю [Bhatnagar et al., 1996]. Однако дополнительные исследования этого лекарственного соединения не проводились, а потенциальная возможность его применения для лечения гормонально-зависимых типов рака или других заболеваний, таких как эндометриоз, никогда не исследовалась.
В настоящее время, в США и большинстве других стран не существует схем перорального фармакологического лечения, опробованных для лечения гипогонадизма и/или дефицита тестостерона у страдающих ожирением пациентов мужского пола. Как изложено выше, на данный момент, инъекции тестостерона, хорионического гонадотропного гормона (HCG) или гонадотропина являются единственным вариантом выбора для этих пациентов. Поэтому, для этой группы людей в медицине существует важная неудовлетворенная на данный момент потребность в разработке фармакологического лечения, которое облегчало бы связанные с дефицитом тестостерона расстройства и симптомы.
В частности, была бы чрезвычайно востребована пероральная терапия, которая нормализует общий тестостерон, но значительно не увеличивает местное воздействие андрогенов на печень. Кроме того, было бы желательно иметь в наличии схему лечения, которая позволяет достигать более физиологического замещения тестостерона.
В результате обсуждения всех проблем и неблагоприятных факторов, связанных с известными на настоящий момент вариантами лечения гипогонадизма и дефицита тестостерона у пациентов мужского пола, в частности, гипогонадотропного гипогонадизма у страдающих ожирением или полнотой мужчин, было бы весьма полезно создать новый вариант лечения, у которого отсутствуют упомянутые выше недостатки и который реально приводит к облегчению или, по меньшей мере, улучшению состояния этих пациентов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соответственно, в первом аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона.
В одном варианте осуществления, указанный пациент мужского пола страдает полнотой или ожирением.
Во втором аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения гипогонадизма у пациента мужского пола.
В третьем аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения гипогонадизма у страдающего полнотой или ожирением пациента мужского пола.
В четвертом аспекте, настоящее изобретение относится к соединению 4,4’-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения гипогонадотропного гипогонадизма у пациента мужского пола.
В дополнительном аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения гипогонадотропного гипогонадизма у страдающего полнотой или ожирением пациента мужского пола.
В дополнительном аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для повышения, предпочтительно для нормализации уровней тестостерона у пациента мужского пола с гипогонадизмом или гипогонадотропным гипогонадизмом, предпочтительно у страдающего полнотой или ожирением пациента мужского пола с гипогонадизмом или гипогонадотропным гипогонадизмом.
В дополнительном аспекте, настоящее изобретение относится к соединению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, которое применяют для лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона, где соединение приготавливают в форме, включающей от приблизительно 0,0005 мг до приблизительно 5,0 мг, предпочтительно от приблизительно 0,0005 мг до приблизительно 2,0 мг 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила в одной дозе, и соединение вводят в соответствии с режимом дозирования, характеризующимся периодичностью дозирования от приблизительно одного раза в день до приблизительно одного раза каждые 60 дней.
В дополнительном аспекте, настоящее изобретение относится к применению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила для приготовления лекарственного средства для лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона.
В дополнительном аспекте, настоящее изобретение относится к применению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила для приготовления лекарственного средства для повышения предпочтительно нормализации уровней тестостерона у страдающего полнотой или ожирением пациента мужского пола с гипогонадотропным гипогонадизмом.
Дополнительный аспект настоящего изобретения относится к применению 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила для приготовления лекарственного средства для лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона, где соединение приготавливают в форме, включающей от приблизительно 0,0005 мг до приблизительно 5,0 мг, предпочтительно от приблизительно 0,0005 мг до приблизительно 2,0 мг 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила в одной дозе, и соединение вводят в соответствии с режимом дозирования, характеризующимся периодичностью дозирования от приблизительно одного раза в день до приблизительно одного раза каждые 60 дней.
В дополнительном аспекте, настоящее изобретение относится к пероральной фармацевтической композиции, включающей от приблизительно 0,0005 мг до приблизительно 5,0 мг, предпочтительно от приблизительно 0,0005 мг до приблизительно 2,0 мг 4,4’-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила в одной дозе, необязательно, в комбинации с одним или более фармацевтически приемлемыми вспомогательными веществами.
Согласно дополнительному аспекту изобретения, предлагается фармацевтический набор, включающий (i) такую фармацевтическую композицию, включающую 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрил, необязательно, в комбинации с одним или более фармацевтически приемлемыми вспомогательными веществами; вместе с (ii) инструкциями по применению указанной фармацевтической композиции для лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона, в частности, для лечения гипогонадизма у пациента мужского пола, предпочтительно страдающего полнотой или ожирением пациента мужского пола.
В дополнительном аспекте, настоящее изобретение относится к способу лечения пациента мужского пола, нуждающегося в повышении уровней тестостерона, включающему введение указанному пациенту эффективного количества 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)-метилен]бисбензонитрила.
Согласно дополнительному аспекту изобретения, предлагается способ лечения гипогонадизма, включающий введение пациенту мужского пола, если он в этом нуждается, эффективного количества 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрила.
Доза может составлять от приблизительно 0,0005 мг до приблизительно 5,0 мг, предпочтительно от приблизительно 0,0005 мг до приблизительно 2,0 мг, и может вводиться при режиме дозирования, характеризующемся периодичностью дозирования от приблизительно одного раза в день до приблизительно одного раза каждые 60 дней.
УСЛОВНЫЕ СОКРАЩЕНИЯ
В тексте заявки на изобретение далее будут использоваться следующие условные сокращения :
| АЕ | побочный эффект |
| ANC0VA | ковариационный анализ |
| AUC | площадь под кривой зависимости концентрации от времени |
| ВА | биодоступность |
| BE | биоэквивалентность |
| BMD | минеральная плотность костной ткани |
| BMI | индекс массы тела |
| EOS | окончание исследования |
| FDA | Управление по контролю за продуктами питания и |
| лекарственными средствами США | |
| GCP | надлежащая клиническая практика |
| GnRH | гонадотропин-рилизинг гормон |
| НОМА-IR | гомеостатическая модель оценки резистентности к инсулину |
| HRQoL | обусловленное здоровьем качество жизни |
| i.v. | внутривенный (внутривенно) |
| LH | лютеинизирующий гормон |
| LLN | нижняя граница нормы |
| LL0Q | нижний предел количественных колебаний |
| мл | миллилитр (миллилитры) |
| mm Hg | миллиметры ртутного столба |
| NCS | клинически незначимый |
| NOAEL | уровень, при котором не обнаруживается побочное |
| действие | |
| NTEL | уровень, при котором отсутствует токсическое действие |
| o.d. или q.d. | один раз в день |
| р. о. | внутрь/через рот/перорально |
PD фармакодинамика
| рН | отрицательный логарифм концентрации ионов водорода |
РК фармакокинетика
| SAE | серьезный побочный эффект |
| SOP | стандартная методика работы |
| TBD | подлежит определению |
| ULN | верхняя граница нормы |
ОПРЕДЕЛЕНИЯ
В тесте этого описания и пунктах формулы изобретения, которые следуют далее, следующие термины имеют следующие значения, если явным образом не указано иначе.
Используемые в изобретении термины "включающий" и "содержащий" имеют открытое неограничивающее значение.
Когда для соединений, солей и других подобных веществ применяют форму множественного числа, то в этом случае она также включает в себя соединение, соль или другое подобное вещество в единственном числе.
Используемые в изобретении формы слов в единственном числе и такие выражения, как "по меньшей мере, один" и "один или более", являются взаимозаменяемыми.
Используемый в изобретении термин "или" обычно включает в себя "и/или", если из контекста однозначно не явствует иное.
Кроме того, перечисление в тексте изобретения области числовых значений путем указания конечных значений для этой области включает все числа, находящиеся внутри этой области (например, область числовых значений 1-5 включает 1, 1,5, 2, 2,75, 3, 3,80, 4, 5, и так далее).
Термин "ингибитор ароматазы" обозначает соединение, которое предотвращает образование эстрогенов из их метаболических предшественников путем ингибирования фермента ароматазы.
Используемый в изобретении термин "соединение" относится к 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрилу, также известному, как 4-[α-4-цианофенил)-α-фтор-1-(1,2,4-триазолил)метил]бензонитрил или CGP47645, впервые описанному в 1992 году в патентных документах ЕР 490 816 и US 5637605, содержание которых приводится в описании этого изобретения путем ссылки на них.
Соединение 4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрил представляет собой кристаллическое соединение с четкой эндотермой плавления при 169,5°С. Кристаллический порошок негигроскопичен и плохо растворим в воде.
4,4'-[фтор-(1Н-1,2,4-триазол-1-ил)метилен]бисбензонитрил (CGP47645) является высоко специфичным и эффективным ингибитором ароматазы, который, как было упомянуто выше, характеризуется более продолжительным периодом полувыведения у людей, чем периодом полураспада летрозола (Femara®), выпускаемого промышленностью ингибитора ароматазы, по отношению к которому ингибитор CGP47645 является структурно родственным. In vitro эксперименты с человеческой плацентарной микросомальной ароматазой продемонстрировали величину IС50=6 нМ. Пероральное введение CGP47645 крысам давало величину периода полувыведения ТЧ 75 часов. Воздействие, выражаемое как AUC, было пропорцианальным величине вводимой дозы. В двух различных ароматаза-зависимых экспериментальных моделях ингибирования вызванной андростендионом гипертрофии шейки матки у крыс и ингибирования вызванного с помощью DMBA роста опухоли молочной железы у крыс, величина ED50 составляла 0,003 мг/кг и 0,01 мг/кг соответственно. Эти результаты позволили сделать вывод о том, что активность CGP47645 в качестве ингибитора ароматазы приблизительно в 10 раз выше активности летрозола.
Следует иметь в виду, что используемый в изобретении термин "соединение" охватывает все без исключения изомеры (например, энантиомеры, стереоизомеры, диастереомеры, ротомеры, таутомеры) или любую смесь изомеров, пролекарства и любые фармацевтически приемлемые соли присоединения указанного соединения, если не заявлено иное.
Термин "уровень тестостерона" в контексте настоящего изобретения относится либо к уровню общего тестостерона, либо к уровню свободного тестостерона, измеренных в сыворотке крови. В одном варианте осуществления, термин "уровень тестостерона" относится к уровню общего тестостерона в сыворотке крови. "Общий тестостерон" включает тестостерон, который связан с глобулином, связывающим половые гормоны (SHBG), и, в силу этого, он не является биодоступным, и тестостерон, который либо является свободным, либо слабосвязанным с другими белками (не-SHBG-связанный). Уровни свободного или биодоступного тестостерона могут быть вычислены из уровней общего тестостерона и SHBG. Предпочтительно уровни тестостерона определять утром, между 6 и 12 часами, в качестве "утренних уровней тестостерона". Уровни тестостерона и SHBG могут быть определены с помощью простых анализов крови, проводимых в лаборатории.
Термин "пациент мужского пола, нуждающийся в повышении уровней тестостерона" обозначает особь мужского пола, имеющую уровни общего тестостерона в сыворотке ниже 450 нг/дл или ниже 12 нмоль/л. В одном варианте осуществления, термин "пациент мужского пола, нуждающийся в повышении уровней тестостерона" обозначает особь мужского пола, имеющую уровни общего тестостерона в сыворотке ниже 400 нг/дл или ниже 350 нг/дл, или ниже 10 нмоль/л. В одном варианте осуществления, термин "пациент мужского пола, нуждающийся в повышении уровней тестостерона" обозначает особь мужского пола, имеющую уровни общего тестостерона в сыворотке ниже 300 нг/дл или ниже 8 нмоль/л.
В другом варианте осуществления, термин "пациент мужского пола, нуждающийся в повышении уровней тестостерона" обозначает особь мужского пола, имеющую, вне зависимости от уровней тестостерона, повышенные уровни общего эстрадиола в сыворотке (и/или повышенные уровни общего эстрона и/или сульфата эстрона и/или эстриола в сыворотке). Повышенные уровни эстрадиола в контексте настоящего изобретения означают уровни эстрадиола, которые выше верхней границы нормы (ULN) при соответствующем стандартизированном анализе.
Используемый в изобретении термин "страдающий полнотой пациент" относится к пациенту с индексом массы тела (BMI), равным или большим чем 25 кг/м2 и меньшим чем 30 кг/м2, рассчитанным из данных по массе тела и росту пациента.
Используемый в изобретении термин "страдающий ожирением пациент" относится к пациенту с индексом массы тела (BMI), равным или большим чем 30 кг/м2, рассчитанным из данных по массе тела и росту пациента.
Индекс массы тела (BMI), показатель, который сравнивает массу и рост, на основе которого людей относят к страдающим полнотой (предшествующей ожирению стадии), когда их BMI составляет от 25 кг/м2 до 30 кг/м2, и к страдающим ожирением, когда их BMI больше чем 30 кг/м2.
Используемый в изобретении термин "гипогонадизм" относится к субъектам, имеющим уровень общего тестостерона меньше чем 400 нг/дл, в конкретных вариантах осуществления, меньше чем 350 нг/дл, и в дополнительных вариантах осуществления, меньше чем 300 нг/дл. В качестве варианта, термин "гипогонадизм" относится к субъектам, имеющим уровень общего тестостерона меньше чем 12 нмоль/л, в конкретных вариантах осуществления, меньше чем 10 нмоль/л, и в дополнительных вариантах осуществления, меньше чем 8 нмоль/л. В одном варианте осуществления, термин "гипогонадизм" относится к особи мужского пола, имеющей утренние уровни общего тестостерона ниже 300 нг/дл или ниже 8 нмоль/л.
Термин "гипогонадотропный пациент" относится к пациенту с неприемлемо низкими уровнями гонадотропинов. В частности, пациент с "неприемлемо низкими уровнями гонадотропинов" определяется как пациент с (i) уровнями лютеинизирующего гормона (LH) ≤ ULN при соответствующем стандартизированном анализе, (ii) с уровнями фолликулстимулирующего гормона (FSH) ≤ ULN, и (iii) с уровнем эстрадиола внутри или выше области нормальных значений (определяемых как ≥ LLN при стандартизированном анализе).
В другом варианте осуществления, "гипогонадотропный пациент" может иметь определенные выше "неприемлемо низкие уровни гонадотропинов" и нормальную гипоталамическую/гипофизарную функцию, в том числе (i) уровни пролактина в области нормальных значений, (ii) уровни тиреостимулирующего гормона (TSH) в области нормальных значений и (iii) уровни ферритина в области нормальных значений.
Термин "гипогонадотропный гипогонадизм" или "пациент с гипогонадотропным гипогонадизмом" относится к субъекту мужского пола, страдающему от определенного в описании изобретения гипогонадизма и являющемуся гипогонадотропным, в соответствии с приведенным в описании изобретения определением.
Термин "ожирение при гипогонадотропном гипогонадизме" или "страдающий ожирением гипогонадотропный пациент мужского пола с гипогонадизмом" или "гипогонадотропный гипогонадизм у страдающих ожирением мужчин" относится к субъекту мужского пола, страдающему определенным в описании изобретения ожирением, страдающему определенным в описании изобретения гипогонадизмом и являющемуся гипогонадотропным в соответствии с приведенным в описании изобретения определением. В одном варианте осуществления, такой пациент определяется как субъект, удовлетворяющий следующим критериям: (а) имеющий индекс массы тела (BMI) ≥30 кг/м2, (b) имеющий утренний уровень общего тестостерона в сыворотке ниже 400 нг/дл, предпочтительно ниже 350 нг/дл и более предпочтительно ниже 300 нг/дл, и (с) имеющий неприемлемо низкий уровень гонадотропинов, определенный выше в описании изобретения, и (d) имеющий нормальную гипоталамическую/гипофизарную функцию, определенную выше в описании изобретения.
Термин "полнота при гипогонадотропном гипогонадизме" или "страдающий полнотой гипогонадотропный пациент мужского пола с гипогонадизмом" или "гипогонадотропный гипогонадизм у страдающих полнотой мужчин" относится к субъекту мужского пола, страдающему определенной в описании изобретения полнотой, страдающему определенным в описании изобретения гипогонадизмом и являющемуся гипогонадотропным в соответствии с приведенным в описании изобретения определением. В одном варианте осуществления, такой пациент определяется как субъект, удовлетворяющий следующим критериям: (а) имеющий индекс массы тела (BMI), равный или больший чем 25 кг/м2 и меньший чем 30 кг/м2, (b) имеющий утренний уровень общего тестостерона в сыворотке ниже 400 нг/дл, предпочтительно ниже 350 нг/дл и более предпочтительно ниже 300 нг/дл, и (с) имеющий неприемлемо низкий уровень гонадотропинов, определенный выше в описании изобретения, и (d) имеющий нормальную гипоталамическую/гипофизарную функцию, определенную выше в описании изобретения.
Используемый в изобретении термин "нормализация уровней тестостерона" означает повышение уровней общего тестостерона в сыворотке, предпочтительно уровней утреннего общего тестостерона в сыворотке, до более чем 300 нг/дл или более чем 8 нмоль/л. В одном варианте осуществления, термин означает повышение уровней общего тестостерона в сыворотке, предпочтительно уровней утреннего общего тестостерона в сыворотке, до более чем 400 нг/дл, до более чем 450 нг/дл или до более чем 8 нмоль/л.
Используемый в изобретении термин "повышение уровней тестостерона" означает повышение уровня утреннего общего тестостерона в сыворотке после введения соединения согласно изобретению по меньшей мере на 10% по сравнению с уровнем тестостерона до введения соединения. В конкретных вариантах осуществления, термин "повышение уровней тестостерона" означает повышение уровня утреннего общего тестостерона в сыворотке после введения терапевтически эффективного количества соединения пациенту мужского пола согласно изобретению по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70% или даже выше, по сравнению с уровнем тестостерона до введения соединения.
Термин "лечение гипогонадизма" относится к лечению заболевания гипогонадизмом, где заболевание определяется так, как в водной части описания изобретения. В одном аспекте, термин "лечение гипогонадизма" включает лечение пациентов с пониженными уровнями тестостерона в сыворотке.
Используемый в изобретении термин "режим дозирования, характеризующийся периодичностью дозирования от приблизительно одного раза в день до приблизительно одного раза каждые 60 дней" относится к режиму дозирования, при котором активное соединение может вводиться один раз каждый 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 21, 26, 27, 28, 29, 30 .., 35, 42, 49, 56, 57, 58, 59, 60 дней. Этот термин включает, например, режимы дозирования, характеризующиеся (i) периодичностью дозирования от приблизительно одного раза в день до приблизительно одного раза каждые 60 дней, (ii) периодичностью дозирования от приблизительно одного раза каждые 2 дня до приблизительно одного раза каждые 40 дней или 6 недель, (iii) периодичностью дозирования от приблизительно одного раза каждые 5 дней до приблизительно одного раза в месяц или приблизительно одного раза каждые 4 недели или приблизительно одного раза каждые 30 дней, (iv) периодичностью дозирования от приблизительно одного раза в неделю или приблизительно одного раза каждые 7 дней до приблизительно одного раза каждые 3 недели или приблизительно одного раза каждые 20 дней, или (ν) периодичностью дозирования от приблизительно одного раза в неделю или приблизительно одного раза каждые 7 дней до приблизительно одного раза в две недели или одного раза каждые 10 дней.
В этом контексте, термин "приблизительно" может иметь значение от "плюс/минус 1 день" для режима дозирования один раз каждые 3 дня до "плюс/минус 10 дней" для режима дозирования один раз каждые 60 дней. Режим дозирования "приблизительно один раз каждые 3 дня" относится к режиму дозирования одной дозы, вводимой каждые 3 дня плюс/минус 1 день; режим дозирования "прибл