Лечение воспалительных повреждений при розацеа с помощью ивермектина
Иллюстрации
Показать всеИзобретение относится к области дерматологии и представляет собой способ лечения воспалительных повреждений при розацеа у нуждающегося в этом индивидуума, включающий местное введение один раз в сутки на область кожи, затронутую воспалительными повреждениями при розацеа, фармацевтической композиции, содержащей от 0,5% до 1,5% по массе ивермектина и фармацевтически приемлемый носитель, где уже через 2 недели после исходного введения фармацевтической композиции наблюдают значительное снижение количества воспалительных повреждений. Изобретение обеспечивает значительное сокращение количества воспалительных поражений при розацеа уже через две недели после исходного нанесения, а также более эффективное лечение, статистически значимую ремиссию и уменьшение побочных реакций кожи. 2 н. и 13 з.п. ф-лы, 5 пр., 8 табл., 13 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0002] По настоящей заявке испрашивается приоритет на основании патентной заявки США с регистрационным № 14/209927, поданной 13 марта 2014 года, имеющей право на приоритет в соответствии с 35 U.S.C. § 119(e) по предварительной патентной заявке США № 61/843540, поданной 8 июля 2013 года, предварительной патентной заявке США № 61/919208 поданной 20 декабря 2013 года, и предварительной патентной заявке США № 61/927717, поданной 15 января 2014 года, описание каждой из которых, таким образом, включено в настоящее описание посредством ссылки в полном объеме.
УРОВЕНЬ ТЕХНИКИ
[0003] Розацеа является широко распространенным хроническим воспалительным состоянием кожи, оцениваемым как поражающее 16 миллионов американцев.1-2 Розацеа является распространенным хроническим и прогрессирующим воспалительным заболеванием с особенностями кожи, отличающимися покраснением и гиперемией, эритемой лица, папулами, пустулами, телеангиэктазией и, иногда, поражениями глаз, известными как глазная розацеа. В тяжелых случаях, в частности у мужчин, может образовываться ринофима, или луковичное увеличение носа. Розацеа развивается в течение нескольких лет с периодами обострений, запускаемых различными стимулами, такими как изменения температуры, алкоголь, острая пища, инсоляция и эмоциональные факторы.
[0004] Распространенность розацеа в европейской популяции находится в диапазоне от 0,09 до 22% с пиковым возрастом дебюта от 25 до 70 лет, и розацеа гораздо более распространена среди людей с белой кожей. Чаще она поражает женщин, хотя состояние, как правило, является более тяжелым у мужчин. Сообщают о распространенности семейных случаев розацеа.
[0005] Определены четыре подтипа розацеа по степени первичных признаков, таких как вазомоторная гиперемия, постоянная эритема, папулы и пустулы, телеангиэктазы (Wilkin J et al., JAAD, 2002, 46: 584-587). Эритематозно-телеангиэктатическая розацеа (ETR), в основном, отличается вазомоторной гиперемией и постоянной центральной эритемой лица. Как правило, телеангиэктазы наблюдают, но они не являются необходимыми для диагностики этого подтипа. Центральная эритема лица, ощущение жжения и шершавость, шелушение кожи также являются симптомами, о которых иногда сообщают. Гиперемию, как единственный симптом в анамнезе, как правило, обнаруживают у людей с эритематозно-телеангиэктатической розацеа.
[0006] Папулопустулезная розацеа (PPR) отличается постоянной центральной эритемой лица и транзиторным появлением папул и/или пустул в центре лица. Однако папулы и пустулы также могут возникать в периорифициальных областях, т.е. вокруг рта, носа и глаз. Папулопустулезный подтип похож на обыкновенные угри, но отсутствуют комедоны. Розацеа и угри могут сосуществовать у одного пациента, в случае чего комедоны также могут присутствовать вместе с папулами и пустулами, наводящими на мысль о розацеа. Люди с папулопустулезной розацеа иногда жалуются на ощущение жжения. Этот подтип часто наблюдают до или одновременно с ETR (включая наличие телеангиэктазов). Телеангиэктазы могут быть маскированы постоянной эритемой и папулами и пустулами, но они становятся более видимыми после успешного лечения, скрывающего эти признаки. Папулопустулезная розацеа (PPR) является подтипом воспалительных повреждений, ассоциированных со значительным психологическим расстройством.3 Обнаружено, что недостатки кожи лица значительно ухудшают связанное со здоровьем качество жизни, наряду со страхом негативной оценки со стороны других людей.4 Кроме того, PPR отличается наличием воспалительных инфильтратов, сопровождающих покраснения, наряду с повышенным иммунным ответом, включающим нейтрофильную инфильтрацию и повышенную экспрессию гена ИЛ-8 (Steinhoff et al. JInvestig Dermatol Symp Proc 2011; 15:2-11)
[0007] Фиматозная розацеа отличается утолщением кожи, узловыми образованиями с шероховатой поверхностью и отеком. Как правило, она, главным образом, поражает нос, но фиматозная розацеа также может затрагивать другие области, такие как подбородок, лоб, щеки и уши. У пациентов с этим подтипом иногда наблюдают выступающие, увеличенные фолликулы в пораженных областях, а также телеангиэктазы. Этот подтип часто возникает до или одновременно с ETR или PPR (включая наличие постоянной эритемы, телеангиэктазов, папул и пустул). В случае ринофимы эти дополнительные признаки могут быть особенно выраженными в области носа.
[0008] При глазной розацеа (или офтальмической розацеа) проявляются симптомы, ограниченные областью глаз, с блефаритом, конъюнктивитом и кератитом. Диагноз глазной розацеа необходимо рассматривать, когда у пациента присутствует один или несколько из следующих глазных признаков и симптомов: слезящиеся или красные глаза (гиперемия конъюнктивы век), ощущение чужеродного тела, жжения, сухости или зуда в глазах, чувствительность к свету, нечеткое зрение, конъюнктивальные телеангиэктазы или телеангиэктазы края века или эритема века и периокулярной области.
[0009] Патогенез розацеа еще не полностью понятен. Ее этиология является мультифакториальной. В дополнение к экзогенным факторам (включая УФ-излучение, жару и алкоголь), она может являться вторичной по отношению к паразитарной инвазии (в частности, клещей Demodex folliculorum).5-6 Такие факторы активируют нейроваскулярные и/или иммунные ответы и, таким образом, воспалительные каскады. Периодические обострения могут способствовать хронизации розацеа, т.к. они ассоциированы с длительной вазодилатацией, периваскулярным воспалением, отеком и воздействием цитокинов и клеточных инфильтратов. В некоторых исследованиях PPR наблюдали более высокую плотность клещей по сравнению с контролями (Forton et al., Br JDermatol 1993; 128(6):650-9; Karincaoglu et al., JDermatol 2004; 31(8):618-26). Кожа, пораженная розацеа, высокочувствительна и склонна к раздражению.7
[0010] Лечение розацеа является сложным, и в настоящее время наиболее используемые способы терапии включают пероральные антибиотики (тетрациклин или его производные, метронидазол и макролиды) и пероральные ретиноиды. В настоящее время существует лишь несколько вариантов терапии воспалительных повреждений при розацеа и не так много альтернатив с высокой эффективностью и введением дозы один раз в сутки. В недавно опубликованном обзоре Cochrane отмечено, что неясно, что является более эффективным, в то время как некоторые данные подтверждают эффективность местного введения метронидазола, азелаиновой кислоты и субантимикробной дозы доксициклина в лечение розацеа от умеренной до тяжелой.8 В национальном исследовании индивидуумов, в настоящее время принимающих лекарственные средства против розацеа, 46% пациентов ранее меняли лекарственные средства, как правило, по причине отсутствия улучшения.9 При использовании некоторых общепринятых способов лечения отмечают медленное и неполное лечение и короткий безрецидивный период.
[0011] Ивермектин является антипаразитарным лекарственным производным из семейства макроциклических лактонов, одобренным для использования на человеке для лечения и химиопрофилактики онхоцеркоза и стронгилоидоза с 1996 года в США и 1988 года во Франции. Кроме того, во Франции он одобрен для лечения чесотки у человека. Пероральный ивермектин при демодикозе человека и животного являлся эффективным в уменьшении Demodex folliculorum и улучшении демодикоза. Кроме того, при пероральном введении ивермектина в комбинации с последующим еженедельным местным нанесением перметрина демонстрировал эффективность лечения у пациента с хроническим розацеа-подобным демодикозом (14).
[0012] В патенте США № 5952372 описывают способ лечения розацеа у людей, включающий пероральное или местное введение ивермектина. Однако в соответствии с патентом США № 5952372 в результате эффекта кожного барьера можно ожидать, что для местного введения ивермектина потребуется его введение один или два раза в сутки в течение четырех недель для достижения достаточного проникновения в фолликулы и эффективной акарицидной активности. В нем дополнительно описывают, что после осуществления ивермектином его акарицидной активности в отношении организмов Demodex folliculorum в коже воспалительные ответы на них начинают уменьшаться, но остатки мертвых клещей все равно вызывают некоторую гиперемию и образование повреждений, пока процессы очищения организма не удалят их, что занимает от шести до восьми недель. В нем предлагают использовать общепринятые лекарственные средства против розацеа, такие как пероральный тетрациклин и местный метронидазол, для супрессии ранних обострений и обеспечения раннего клинического ответа в течение начальной фазы введения ивермектина. Патент США № 5952372 не содержит конкретного описания местного лечения PPR.
[0013] В патенте США № 6133310 и патенте США № 8415311 также описывают способ лечения розацеа посредством местного использования ивермектина. Однако они не содержат конкретное описание лечения воспалительных повреждений при розацеа или PPR.
[0014] Таким образом, существует потребность в лечении воспалительных повреждений при розацеа посредством местного введения один раз в сутки с более ранним появлением значимой эффективности и более длительным периодом времени до рецидива, чем в случае доступных в настоящее время способов лечения, для обеспечения безопасной, более быстрой и длительной ремиссии и лучшего соблюдения пациентом схемы лечения для тех, кто нуждается в таком лечении. Такая потребность удовлетворяется настоящим изобретением.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0015] В настоящее время показано, что местное введение от 0,5 до 1,5% по массе ивермектина обеспечивает более быстрое уменьшение воспалительных повреждений при розацеа, а также более длительный безрецидивный период по сравнению с доступными в настоящее время способами лечения, такими как местное лечение 0,75% по массе метронидазола.
[0016] В одном общем аспекте варианты осуществления настоящего изобретения относятся к способу лечения воспалительных повреждений при розацеа у нуждающегося в этом индивидуума, включающему местное введение фармацевтической композиции, содержащей от 0,5% до 1,5% по массе ивермектина и фармацевтически приемлемый носитель, один раз в сутки на область кожи, затронутую воспалительными повреждениями при розацеа, где уже через 2 недели после исходного введения фармацевтической композиции наблюдают значительное снижение количества воспалительных повреждений.
[0017] В другом общем аспекте настоящее изобретение относится к способу лечения воспалительных повреждений при розацеа у нуждающегося в этом индивидуума, включающему местное введение один раз в сутки на область кожи, затронутую воспалительными повреждениями, фармацевтической композиции, содержащей 1% по массе ивермектина и фармацевтически приемлемый носитель, где уже через 2 недели после исходного введения фармацевтической композиции индивидууму наблюдают значительное снижение количества воспалительных повреждений и достигают равновесной концентрации ивермектина в плазме индивидуума, где равновесная концентрация имеет среднюю Cmax ивермектина 2,10±1,04 нг/мл с диапазоном 0,69-4,02 нг/мл, и среднюю AUC0-24ч 36,14±15,56 нг⋅ч/мл с диапазоном 13,69-75,16 нг⋅ч/мл.
[0018] В предпочтительном варианте осуществления настоящего изобретения до начала лечения индивидуум имеет папулопустулезную розацеа от умеренной до тяжелой.
[0019] В другом предпочтительном варианте осуществления настоящего изобретения индивидуум имеет по меньшей мере 10, предпочтительно - по меньшей мере 12, и более предпочтительно - по меньшей мере 15 воспалительных повреждений при розацеа до начала лечения.
[0020] Согласно вариантам осуществления настоящего изобретения местное введение ивермектина один раз в сутки значительно превосходит местное введения метронидазола дважды в сутки при лечении воспалительных повреждений при розацеа.
[0021] Другие аспекты, признаки и преимущества изобретения будут очевидны из следующего описания, включающего подробное описание изобретения и его предпочтительных вариантов осуществления и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0022] Изложенное выше краткое описание, а также следующее подробное описание изобретения будут более понятны при прочтении в комбинации с прилагаемыми чертежами. В целях иллюстрирования изобретения на чертежах представлены варианты осуществления, являющиеся предпочтительными в настоящее время. Однако следует понимать, что изобретение не ограничено конкретными вариантами осуществления, представленными на чертежах.
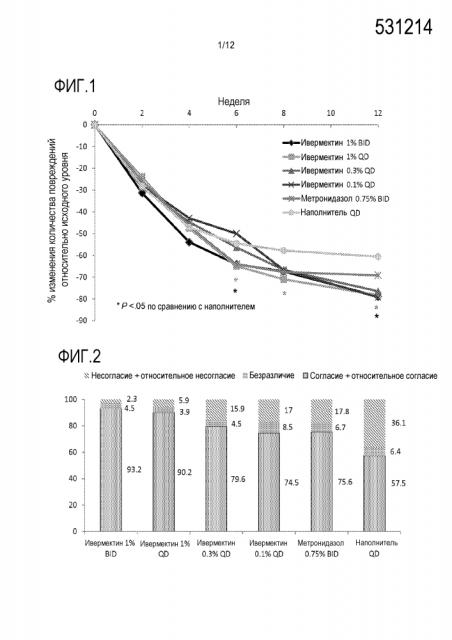
[0023] На фигуре 1 показан средний процент изменения количества повреждений относительно базового уровня (выборка ITT-LOCF) в исследовании диапазона доз после различного местного лечения;
[0024] На фигуре 2 проиллюстрирован ответ индивидуума до утверждения "продукт улучшил мою розацеа" после различного местного лечения (наблюдения ITT);
[0025] На фигуре 3 показано распределение индивидуумов в 2 клинических исследованиях безопасности и эффективности местного лечения ивермектином;
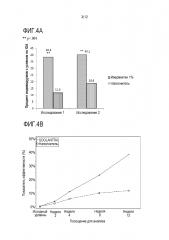
[0026] На фигуре 4 представлены пропорции индивидуумов, достигших положительного результата в IGA ("чистая" или "почти чистая"): (A) на неделе 12 в исследованиях 1 и 2; (B) на неделях 2, 4, 8 и 12 в исследовании 1; и (C)) на неделях 2, 4, 8 и 12 в исследовании 2, где SOOLANTRA является кремом с 1% ивермектина;
[0027] На фигуре 5 показано изменение количества воспалительных повреждений относительно базового уровня (ITT-LOCF): (A) среднее абсолютное изменение (± стандартная ошибка) в исследовании 1; (B) среднее абсолютное изменение (± стандартная ошибка) в исследовании 2; (C) медиана процента изменения в исследовании 1; и (D) медиана процента изменения в исследовании 2, где SOOLANTRA является кремом с 1% ивермектина;
[0028] На фигуре 6 представлена оценка индивидуумами улучшения розацеа в (A) исследовании 1 и (B) исследовании 2 на неделе 12;
[0029] Фигура 7 представляет собой фотографии пациента на исходном уровне и неделе 12 (стандартное освещение);
[0030] На фигуре 8 показано распределение индивидуумов в клиническом исследовании, в котором сравнивали местное лечение ивермектином и метронидазолом;
[0031] На фигуре 9 показан средний процент изменения количества воспалительных повреждений относительно базового уровня (ITT-LOCF) после местного лечения ивермектином и метронидазолом, * p<0,05, ** p<0,001;
[0032] На фигуре 10 показан показатель эффективности на основе IGA "чистая" или "почти чистая" после местного лечения ивермектином и метронидазолом, * p<0,05, ** p<0,001;
[0033] На фигуре 11 представлена оценка индивидуумами улучшения розацеа после местного лечения ивермектином и метронидазолом;
[0034] На фигуре 12 показано время до первого рецидива, определенного как первое повторение IGA≥2 после успешного лечения ивермектином (CD5024) и метронидазолом; и
[0035] На фигуре 13 показаны общие средние концентрации ивермектина в плазме (± SD, при N=15).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0036] В уровне техники и на всем протяжении описания цитируют или описывают различные публикации, статьи и патенты; каждая из этих ссылок включена в настоящее описание в качестве ссылки в полном объеме. Обсуждение документов, актов, материалов, устройств, статей или т.п., включенных в настоящее описание, представлено в целях обеспечения контекста для настоящего изобретения. Такое обсуждение не является признанием того, что любой или все из этих объектов образуют часть предшествующего уровня техники в отношении любых описываемых или заявленных изобретений.
[0037] Если не указано иначе, все технические и научные термины, используемые в настоящем описании, обладают тем же значением, которое, как правило, понятно специалисту в области, к которой это изобретение относится. В противном случае, конкретные термины, используемые в настоящем описании, обладают значениями, приведенными в описании. Все патенты, опубликованные патентные заявки и публикации, процитированные в настоящем описании, включены в качестве ссылки так, как если бы они были полностью приведены в настоящем описании. Необходимо отметить, что, как применяют в настоящем описании и прилагаемой формуле изобретения, формы в единственном числе включают ссылки на множественное число, если контекст четко не указывает на иное.
[0038] Ивермектин является членом класса авермектинов, которые, как показано в иммунофармакологических исследованиях, проявляют противовоспалительные эффекты посредством ингибирования липополисахарид-индуцированной продукции воспалительных цитокинов, таких как фактор некроза опухоли и интерлейкин (ИЛ)-1b, одновременно повышающе регулируя противовоспалительный цитокин ИЛ-1010. Он является полусинтетическим производным, выделенным при ферментации Streptomyces avermitilis, принадлежащим к авермектиновому семейству макроциклических лактонов. Ивермектин является смесью, содержащей 5-0-деметил-22,23-дигидроавермектин A1a и 5-0-деметил-25-де(1-метилпропил)-25-(1-метилэтил)-22,23-дигидроавермектин A1a, как правило, обозначаемый как 22,23-дигидроавермектин B1a и B1b или H2B1a и H2B1b, соответственно. Соответствующими эмпирическими формулами H2B1a и H2B1b являются C48H74O14 и C47H72O14 с молекулярными массами 875,10 и 861,07, соответственно.
[0039] Ивермектин является производным макроциклического лактона, считают, что его терапевтический эффект, главным образом, является результатом его противовоспалительных свойств, аналогичных таковым других макролидов.11-12 Сообщают, что авермектин проявляет противовоспалительные эффекты посредством ингибирования липополисахарид-индуцированной продукции воспалительных цитокинов. В дополнение к его противовоспалительному механизму действия ивермектин обладает антипаразитарными свойствами. Его предшественник авермектин является антипаразитарным средством, имеющим значение в сельском хозяйстве, впервые выделенным в 1974 году.13 Некоторые исследования подтверждают роль ивермектина в эффективном пероральном лечении кожного демодикоза (в комбинации с кремом с перметрином для местного использования) и чесотки, а также местном лечении педикулеза.14-16 Ивермектин вызывает гибель паразитов, главным образом, посредством селективного связывания с высокой аффинностью с глутамат-зависимыми хлоридными каналами, происходящего в нервных и мышечных клетках беспозвоночных. Это приводит к прерыванию нервных импульсов, вызывая паралич и гибель организмов-паразитов. Известно, что ивермектин действует на клещей Demodex при локализованном и генерализованном демодикозе у животных и людей.
[0040] В случае настоящего изобретения проводили исследования для оценки эффективности и безопасности ивермектина в лечении воспалительных повреждений при розацеа, такой как папулопустулезная розацеа (PPR).
[0041] Обнаруживали, что уже через 2 недели после исходного местного введения индивидууму фармацевтической композиции, содержащей от 0,5 до 1,5% (масс./масс.) ивермектина, наблюдали значимое снижение количества воспалительных повреждений.
[0042] Как применяют в настоящем описании, "значимое снижение" относится к снижению, являющемуся статистически значимым, не только в результате случайности, имеющему значение p 0,05 или меньше. "Значимое снижение" может иметь значение p менее 0,05, 0,04, 0,03, 0,01, 0,005, 0,001 и т.д. Как применяют в настоящем описании, "количество воспалительных повреждений" относится к количеству воспалительных повреждений, ассоциированных с розацеа или PPR. Воспалительные повреждения могут являться папулами и/или пустулами. Папула является небольшим, твердым возвышением менее одного сантиметра в диаметре, и пустула является небольшим, ограниченным возвышением кожи, содержащим желтовато-белый экссудат.
[0043] Повреждения могут являться, например, папулами и/или пустулами любого размера (небольшого или большого). Например, через две недели после исходного введения наблюдали медиану снижения количества воспалительных повреждений приблизительно 30% (p<0,001) и 27,3% (p<0,01) у пациентов, которых лечили ивермектином, в двух отдельных клинических исследованиях с использованием способов по настоящему изобретению. Эти снижения являются статистически значимыми, т.к. они имели значения p менее 0,01 или даже менее 0,001.
[0044] Это раннее появление значимой эффективности является неожиданным при сравнении с общепринятыми способами лечения. Например, значимые различия лечения наблюдали только с недели 4 или недели 8 в двух исследованиях фазы III для местного лечения умеренной PPR с использованием 15% азелаиновой кислоты дважды в сутки (Thiboutot et al., 2003, J. Am Acad Dermatol, 48 (6): 836-845), в то время как не наблюдали статистически значимых различий в отношении медианы количества воспалительных повреждений или медианы процента изменения количества воспалительных повреждений в любой момент оценки в течение исследования (P>0,29) местного лечения PPR от умеренной до тяжелой с использованием 0,75% или 1,0% метронидазола один раз в сутки (Dahl et al., 2001, J. Am Acad Dermatol, 45 (5): 723-730).
[0045] Это раннее появление значимой эффективности также является неожиданным с учетом существовавшей ранее идеи о том, что ожидают, что для местного лечения ивермектином потребуется введение один или два раза в сутки в течение четырех недель для достижения достаточного проникновения в фолликулы и эффективной акарицидной активности; и что после осуществления ивермектином его акарицидной активности в отношении организмов Demodex folliculorum в коже остатки мертвых клещей все еще вызывают некоторую гиперемию и образование повреждений, пока процессы очищения организма не удалят их, что занимает от шести до восьми недель; и что предлагают использовать общепринятые лекарственные средства против розацеа, такие как пероральный тетрациклин и местный метронидазол, для супрессии ранних обострений и обеспечения раннего клинического ответа в течение начальной фазы введения ивермектина (см., например, патент США № 5952372).
[0046] Кроме того, в случае настоящего изобретения обнаружено, что после повторного местного введения фармацевтической композиции, содержащей от 0,5 до 1,5% (масс./масс.) ивермектина и фармацевтически приемлемый носитель, концентрации ивермектина в плазме постепенно повышались до достижения плато или равновесного состояния. Также обнаружено, что повторное местное введение приводит к гораздо большему конечному времени полувыведения ивермектина в организме индивидуума, чем в случае перорально вводимого ивермектина, что свидетельствует о том, что лимитирующим скорость этапом в снижении концентрации ивермектина в плазме является медленное и постоянное высвобождение ивермектина из места введения на коже в кровоток, а не скорость выведения ивермектина из кровотока, т.е. явление "высвобождения с постоянной скоростью" (Toutain et al., 2004, J. Vet. Pharmacol. Therap. 27: 427-439). Неожиданно, несмотря на этот лимитирующий скорость фактор медленного и постоянного высвобождения ивермектина из кожи в кровоток, не наблюдали дополнительного накопления ивермектина в кровотоке после длительного местного лечения 0,5-1,5% (масс./масс.) ивермектином. Таким образом, местное лечение по варианту осуществления настоящего изобретения является безопасным, и его можно осуществлять так долго, как это необходимо без возникновения каких-либо угроз безопасности.
[0047] Параллельные клинические исследования в настоящем изобретении также показали, что способы по вариантам осуществления настоящего изобретения приводят к большему снижению количества воспалительных повреждений, а также большему времени до рецидивирования воспалительных повреждений, чем в случае общепринятого местного лечения, такого как лечение с использованием метронидазола. Кроме того, способы по вариантам осуществления настоящего изобретения также приводят к менее частым побочным эффектам со стороны кожи, чем в случае общепринятых способов местного лечения.
[0048] Не желая быть связанными теорией, полагают, что механизм действия ивермектина при лечении воспалительных повреждений при розацеа может быть связан с противовоспалительными эффектами ивермектина, а также гибелью клещей Demodex, которые, как сообщают, являются фактором воспаления кожи. Т.к. ивермектин обладает противовоспалительной и антипаразитарной активностями, лечение воспалительных повреждений ивермектином представляет собой инновационную терапию, направленную на эти важные патогенетические факторы при розацеа, таким образом, новым дополнением к существующему арсеналу лечения.
[0049] По варианту осуществления настоящего изобретения способ лечения воспалительных повреждений при розацеа у нуждающегося в этом индивидуума включает местное введение один раз в сутки на область кожи, затронутую воспалительными повреждениями при розацеа фармацевтической композиции, содержащей от 0,5% до 1,5% по массе ивермектина и фармацевтически приемлемый носитель, где уже через 2 недели после исходного введения фармацевтической композиции наблюдают значительное снижение количества воспалительных повреждений.
[0050] Как применяют в настоящем описании, "фармацевтически приемлемый носитель" относится к фармацевтически приемлемому наполнителю или дилюенту, содержащему эксципиенты и вспомогательные средства, облегчающие переработку активных соединений в препараты, которые можно использовать фармацевтически.
[0051] Фармацевтические композиции по изобретению подходят для лечения кожи. Они могут находиться в жидкой, пастообразной или твердой форме, и более конкретно, в форме мазей, кремов, молочка, помад, порошков, пропитанных подушечек, синтетических детергентов, влажных салфеток, растворов, гелей, спреев, пенок, суспензий, лосьонов, косметических карандашей, шампуней или моющих основ. Они также могут находиться в форме суспензий микросфер или наносфер или липидных или полимерных везикул или полимерных патчей и гидрогелей для контролируемого высвобождения. Эти композиции для местного использования могут находиться в безводной форме, в водной форме или в форме эмульсии.
[0052] В одном из вариантов осуществления настоящего изобретения фармацевтическая композиция, составляемая в виде эмульсии, фармацевтической эмульсии для местного использования, содержит ивермектин и один или несколько других ингредиентов, выбранных из группы, состоящей из: масляной фазы, содержащей диметикон, циклометикон, изопропилпальмитат и/или изопропилмиристат, масляной фазы, дополнительно содержащей жирные вещества, выбранные из группы, состоящей из цетилового спирта, цетостеарилового спирта, стеарилового спирта, пальмитостеариновой кислоты, стеариновой кислоты и самоэмульгирующегося воска; по меньшей мере одного поверхностно-активного вещества-эмульгатора, выбранного из группы, состоящей из глицерил/PEG100-стеарата, сорбитан моностеарата, сорбитан пальмитата, стеарета-20, стеарета-2, стеарета-21 и цетеарета-20; смеси растворителей и/или средств, усиливающих проникновение, выбранных из группы, состоящей из пропиленгликоля, олеилового спирта, феноксиэтанола и глицерил триацетата; одного или нескольких гелеобразующих средств, выбранных из группы, состоящей из карбомеров, гелеобразующих средств на основе целлюлозы, ксантановой камеди, силикатов магния алюминия, за исключением силиката магния алюминия/диоксида титана/диоксида кремния, гуаровой камеди, полиакриламидов и модифицированных крахмалов; и воды.
[0053] В предпочтительном варианте осуществления настоящего изобретения фармацевтическая композиция содержит приблизительно 1% (масс./масс.) ивермектина и фармацевтически приемлемый носитель.
[0054] В другом предпочтительном варианте осуществления настоящего изобретения фармацевтическая композиция содержит приблизительно 1% (масс./масс.) ивермектина и один или несколько неактивных ингредиентов, выбранных из группы, состоящей из карбомера, такого как сополимер карбомер типа B; цетилового спирта; моногидрата лимонной кислоты; диметикона 20 Cst; эдетата динатрия; глицерина; изопропилпальмитата; метилпарабена; олеилового спирта; феноксиэтанола; полиоксил-20-цетостеарилового эфира; пропиленгликоля; пропилпарабена; очищенной воды; гидроксида натрия; сорбитан моностеарата и стеарилового спирта.
[0055] Как применяют в настоящем описании, термин "индивидуум" означает любое животное, предпочтительно - млекопитающее, наиболее предпочтительно - человека, которому будут вводить или вводят соединения или составы для местного использования по вариантам осуществления изобретения. Предпочтительно, индивидуум нуждается или является объектом наблюдения или эксперимента, лечения или профилактики воспалительных повреждений при розацеа или папулопустулезной розацеа.
[0056] Как известно специалистам в этой области, "выборка пациентов, которым назначено лечение" или "ITT-выборка" относится ко всем индивидуумам, случайным образом отобранным в клиническое исследования и которым вводят исследуемое лекарственное средство. "ITT-LOCF" относится к ITT-выборке при использовании способа переноса данных последнего наблюдения (LOCF), стандартного способа обработки недостающих данных, с помощью которого приписывают или заполняют значения на основе существующих данных. "ITT-MI" относится к ITT-выборке при использовании способа многократного заполнения (MI) на основе всех данных, доступных в модели, другого способа обработки данных, известного специалистам в этой области. "Протокольная выборка" или "PP-выборка" относится к индивидуумам из ITT-выборки в клиническом исследовании, не имевшим значительных отклонений от протокола исследований.
[0057] Как применяют в настоящем описании, термин "воспалительные повреждения при розацеа" включают любой тип повреждений кожи, ассоциированный с воспалительной фазой розацеа. Примеры "воспалительных повреждений при розацеа" включают папулы и пустулы различного размера, ассоциированные с розацеа. В предпочтительном варианте осуществления настоящего изобретения воспалительные повреждения при розацеа включают воспалительные повреждения при папулопустулезной розацеа (PPR), более предпочтительно, воспалительные повреждения при PPR от умеренной до тяжелой.
[0058] В одном из вариантов осуществления термин "лечение" относится к улучшению, профилактике или реверсированию заболевания или нарушения или по меньшей мере одного его видимого симптома. В другом варианте осуществления термин "лечение" относится к улучшению, профилактике или реверсированию по меньшей мере одного измеряемого физического параметра, относящегося к заболеванию или нарушению, подвергаемого лечению, не обязательно видимого у млекопитающего или млекопитающему. В еще одном варианте осуществления термин "лечение" относится к ингибированию или замедлению прогрессирования заболевания или нарушения, физическому, например, стабилизации видимого симптома, физиологическому, например, стабилизации физического параметра, или и тому, и другому. В еще одном варианте осуществления термин "лечение" относится к задержке дебюта заболевания или нарушения.
[0059] Успех лечения воспалительных повреждений при розацеа или PPR можно измерять известными в этой области способами, такими как измерение снижения количества воспалительных повреждений по отношению к исходному уровню до начала лечения, улучшения баллов общей оценки исследователем (IGA) по отношению к исходному уровню или снижения и количества воспалительных повреждений, и баллов IGA.
[0060] Баллы IGA определяет обученный медицинский персонал, оценивающий состояние кожи пациента с использованием общей оценки исследователем состояния кожи. Как правило, при такой общей оценке определяют значение степени розацеа, проявляемой кожей. В дополнение к оценке, осуществляемой медицинским персоналом, участие и наблюдения пациентом состояния своей кожи и ответы на различные вопросы (например, ощущение жжения) также играют роль в определении заданных баллов IGA. Например, баллы IGA в случае розацеа (таблица 1) могут находиться в диапазоне, например, от 0 (чистая) до 1 (почти чистая), до 2 (слабая), до 3 (умеренная), до 4 (тяжелая), включая значения между этими числовыми категориями, такие как 1,5, 2,6, 3,4 и т.д. (например, интервалы 0,1).
[0061]
| Таблица 1Общая оценка тяжести розацеа исследователем | ||
| Степень | Баллы | Клиническое описание |
| Чистая | 0 | Отсутствие воспалительных повреждений, отсутствие эритемы |
| Почти чистая | 1 | Очень мало небольших папул/пустул, наличие очень слабой эритемы |
| Слабая | 2 | Мало небольших папул/пустул, слабая эритема |
| Умеренная | 3 | Несколько небольших или больших папул/пустул, умеренная эритема |
| Тяжелая | 4 | Многочисленные небольшие и/или большие папулы/пустулы, тяжелая эритема |
[0062] В свете настоящего описания область кожи, затронутую воспалительными повреждениями при розацеа или папулопустулезной розацеа, можно определять с использованием любых диагностических признаков или средств, известных в этой области, и можно лечить способами по вариантам осуществления настоящего изобретения. Пациенты могут иметь папулопустулезную розацеа на разных стадиях от слабой до тяжелой.
[0063] В предпочтительном варианте осуществления пациент имеет папулопустулезную розацеа от умеренной до тяжелой. Как применяют в настоящем описании, пациент, имеющий "папулопустулезную розацеа от умеренной до тяжелой", имеет, по меньшей мере, умеренную эритему лица и по меньшей мере 10 папулопустулезных повреждений до начала лечения. Например, пациент может иметь IGA розацеа 3 или 4 и по меньшей мере 10, 12, 15, 20, 25 или больше папулопустулезных повреждений до начала лечения.
[0064] По вариантам осуществления настоящего изобретения воспалительные повреждения при розацеа или папулопустулезной розацеа лечат посредством местного введения на пораженную область кожи фармацевтической композиции, содержащей ивермектин и фармацевтически приемлемый носитель, и лечение приводит к снижению количества воспалительных повреждений при розацеа с исходного количества повреждений (до начала лечения) по меньшей мере на 1-100 повреждений или более, например, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 35, 40, 50, 60, 70, 80, 90 или 100 повреждений или более. По вариантам осуществления настоящего изобретения после лечения наблюдают снижение количества воспалительных повреждений по меньшей мере приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%. В зависимости от количества воспалительных повреждений и других факторов, таких как состояние пациента, лечение можно продолжать столько, сколько потребуется, например, от 4 до 12 недель.
[0065] По другим вариантам осуществления настоящего изобретения лечение снижает баллы IGA у подвергнутого лечению индивидуума. Как применяют в настоящем описании, "показатель эффективности" в клиническом исследовании относится к процентной доле индивидуумов в исследовании, имеющих IGA 0 ("чистая") или 1 ("почти чистая") после лечения.
[0066] По вариантам осуществления настоящего изобретения после исходного успешного лечения ивермектином, т.е. до IGA 0 или 1, до рецидивирования, т.е. до IGA 2 или выше, проходит больше времени по сравнению с общепринятыми способами лечения, такими как местное лечение 0,75% по массе метронидазолом. Например, лечение