Производные триазолкарбоксамида
Иллюстрации
Показать всеИзобретение относится к соединениям формулы
или их фармацевтически приемлемым солям присоединения кислоты. В формуле I R1 обозначает фенил или пиридинил, возможно замещенный галогеном, низшим алкилом, низшим алкокси, низшим алкилом, замещенным галогеном, и низшим алкокси, замещенным галогеном; X1 представляет собой -N= или СН; X2 представляет собой CR2 или =N-; X3 представляет собой -N= или СН; при условии, что только два из X1, X2 или X3 являются азотом; где представляет собой триазоловую группу, выбранную из , или ; R2 представляет собой водород или низший алкил; Z представляет собой связь, -О- или -СН2-. Соединения изобретения обладают аффинностью к рецепторам, ассоциированным со следовыми аминами (TAAR). Изобретение также относится к фармацевтическим композициям и к применению соединения для изготовления лекарственных средств. Технический результат: получены новые соединения формулы I, обладающие высокой аффинностью к рецепторам, ассоциированным со следовыми аминами (TAAR), особенно к TAAR1. 4 н. и 8 з.п. ф-лы, 1 табл., 36 пр.
Реферат
Данное изобретение относится к соединениям формулы
где
R1 обозначает фенил или пиридинил, возможно замещенный галогеном, низшим алкилом, низшим алкокси, низшим алкилом, замещенным галогеном, и низшим алкокси, замещенным галогеном;
X1 представляет собой -N= или СН;
X2 представляет собой CR2 или =N-;
X3 представляет собой -N= или СН;
при условии, что только два из X1, X2 или X3 являются азотом;
где представляет собой триазоловую группу, выбранную среди
R2 представляет собой водород или низший алкил; Z представляет собой связь, -О- или -СН2-;
или к его фармацевтически приемлемым солям присоединения кислоты.
Изобретение включает все рацемические смеси, все их соответствующие энантиомеры и/или оптические изомеры. Кроме того, все таутомерные формы соединений формулы I также входят в объем данного изобретения.
Было обнаружено, что соединения формул I обладают высокой аффинностью к рецепторам, ассоциированным со следовыми аминами (trace amine associated receptors, TAAR), особенно к TAAR1.
Соединения могут быть использованы для лечения депрессии, тревожных расстройств, биполярного расстройства, синдрома дефицита внимания с гиперактивностью (ADHD), нарушений, связанные со стрессом, психотических расстройств, таких как шизофрения, неврологических заболеваний, таких как болезнь Паркинсона, нейродегенеративных нарушений, таких как болезнь Альцгеймера, эпилепсии, мигрени, гипертензии, злоупотребления психоактивными веществами, метаболических нарушений, такие как расстройство пищевого поведения, диабета, диабетических осложнений, ожирения, дислипидемии, нарушений потребления и усвоения энергии, нарушений и неправильного функционирования температурного гомеостаза организма, нарушений сна и циркадных ритмов и сердечно-сосудистых заболеваний.
Некоторые из физиологических эффектов (т.е. сердечно-сосудистые эффекты, гипотония, седативный эффект), которые были описаны для соединений, которые могут связываться с адренергическими рецепторами (WO 02/076950, WO 97/12874 или ЕР 0717037), могут рассматриваться как нежелательные побочные эффекты в случае лекарственных препаратов, направленных на лечение заболеваний центральной нервной системы, описанных выше. Поэтому желательно получить медикаменты, имеющие селективность в отношении рецептора TAAR1 по сравнению с адренергическими рецепторами. Объекты данного изобретения демонстрируют селективность в отношении рецептора TAAR1 по сравнению с адренергическими рецепторами, в частности хорошую селективность по сравнению с человеческими и крысиными адренергическими рецепторами альфа1 и альфа2.
Классические биогенные амины (серотонин, норадреналин, адреналин, дофамин, гистамин) играют важную роль нейромедиаторов в центральной и периферической нервной системе [1]. Их синтез и хранение, а также их деградация и обратный захват после освобождения сильно регулируется. Нарушение баланса в уровнях биогенных аминов, как известно, ответственно за измененное функционирование мозга при многих патологических состояниях [2-5]. Второй класс эндогенных аминных соединений, так называемых следовых аминов (trace amines, ТА), значительно перекрывается с классическими биогенными аминами в плане структуры, метаболизма и субклеточной локализации. ТА включают п-тирамин, β-фенилэтиламин, триптамин и октопамин, и они присутствуют в нервной системе млекопитающих в целом на более низких уровнях, чем классические биогенные амины [6].
Нарушение их регуляции было связано с различными психиатрическими заболеваниями, такими как шизофрения и депрессия [7], а также с другими состояниями, такими как синдром дефицита внимания и гиперактивность, мигрень, болезнь Паркинсона, злоупотребление психоактивными веществами и расстройства пищевого поведения [8, 9].
В течение долгого времени ТА-специфические рецепторы были только гипотезой, основанной на анатомически дискретных высокоаффинных сайтах связывания ТА в ЦНС человека и других млекопитающих [10, 11]. Соответственно, считалось, что фармакологические эффекты ТА опосредуются через известный механизм классических биогенных аминов, либо за счет их освобождения, подавления их обратного захвата, либо за счет "перекрестной реакции" с их рецепторными системами [9, 12, 13]. Эта точка зрения существенно изменилась в последнее время благодаря открытию нескольких членов нового семейства GPCR, рецепторов, ассоциированных со следовыми аминами (TAAR) [7, 14]. У человека есть 9 генов TAAR (в том числе 3 псевдогена), а у мышей 16 генов (в том числе 1 псевдоген). Гены TAAR не содержат интроны (с одним исключением, TAAR2 содержит один интрон) и расположены рядом друг с другом в одном и том же хромосомном сегменте. Филогенетическое родство генов рецепторов, в соответствии с углубленным сравнением фармакофорного сходства GPCR и фармакологическими данными, подтверждает, что эти рецепторы образуют три различных подсемейства [7, 14]. TAAR1 находится в первом подклассе из четырех генов (TAAR1-4), высоко консервативных у человека и грызунов. ТА активируют TAAR1 с помощью Ga. Было показано, что нарушение регуляции ТА вносит свой вклад в этиологию различных заболеваний, таких как депрессия, психоз, синдром дефицита внимания с гиперактивностью, злоупотребление психоактивными веществами, болезнь Паркинсона, мигрень, расстройства пищевого поведения, нарушения обмена веществ, и, таким образом, лиганды TAAR1 имеют высокий потенциал для лечения этих заболеваний.
Таким образом, существует большой интерес к повышению уровня знаний о рецепторах, ассоциированных со следовыми аминами.
Список используемой литературы:
1 Deutch, A.Y. and Roth, R.H. (1999) Neurotransmitters. In Fundamental Neuroscience (2nd edn) (Zigmond, M.J., Bloom, F.E., Landis, S.C., Roberts, J.L, and Squire, L.R., eds.), pp. 193-234, Academic Press;
2 Wong, M.L. and Licinio, J. (2001) Research and treatment approaches to depression. Nat. Rev. Neurosci. 2, 343-351;
3 Carlsson, A. et al. (2001) Interactions between monoamines, glutamate, and GABA in schizophrenia: new evidence. Annu. Rev. Pharmacol. Toxicol. 41, 237-260;
4 Tuite, P. and Riss, J. (2003) Recent developments in the pharmacological treatment of Parkinson's disease. Expert Opin. Investig. Drugs 12, 1335-1352,
5 Castellanos, F.X. and Tannock, R. (2002) Neuroscience of attention-deficit/hyperactivity disorder: the search for endophenotypes. Nat. Rev. Neurosci. 3, 617-628;
6 Usdin, Earl; Sandler, Merton; Editors. Psychopharmacology Series, Vol. 1: Trace Amines and the Brain. [Proceedings of a Study Group at the 14th Annual Meeting of the American College of Neuropsychoparmacology, San Juan, Puerto Rico] (1976);
7 Lindemann, L. and Hoener, M. (2005) A renaissance in trace amines inspired by a novel GPCR family. Trends in Pharmacol. Sci. 26, 274-281;
8 Branchek, T.A. and Blackburn, T.P. (2003) Trace amine receptors as targets for novel therapeutics: legend, myth and fact. Curr. Opin. Pharmacol. 3, 90-97;
9 Premont, R.T. et al. (2001) Following the trace of elusive amines. Proc. Natl. Acad. Sci. U.S.A. 98, 9474-9475;
10 Mousseau, D.D. and Butterworth, R.F. (1995) A high-affinity [3H] tryptamine binding site in human brain. Prog. Brain Res. 106, 285-291;
11 McCormack, J.K. et al. (1986) Autoradiographic localization of tryptamine binding sites in the rat and dog central nervous system. J. Neurosci. 6, 94-101;
12 Dyck, L.E. (1989) Release of some endogenous trace amines from rat striatal slices in the presence and absence of a monoamine oxidase inhibitor. Life Sci. 44, 1149-1156;
13 Parker, E.M. and Cubeddu, L.X. (1988) Comparative effects of amphetamine, phenylethylamine and related drugs on dopamine efflux, dopamine uptake and mazindol binding. J. Pharmacol. Exp.Ther. 245, 199-210;
14 Lindemann, L. et al. (2005) Trace amine associated receptors form structurally and functionally distinct subfamilies of novel G protein-coupled receptors. Genomics 85, 372-385.
Объектами данного изобретения являются новые соединения формулы I и их фармацевтически приемлемые соли, их применение для производства лекарственных средств для лечения заболеваний, связанных с биологической функцией рецепторов, ассоциированных со следовыми аминами, их производство, а также лекарственные средства на основе соединения согласно изобретению для лечения или профилактики заболеваний, таких как депрессия, тревожные расстройства, биполярное расстройство, синдром дефицита внимания с гиперактивностью, расстройства, вызванные стрессом, психотические расстройства, такие как шизофрения, неврологические заболевания, такие как болезнь Паркинсона, нейродегенеративные заболевания, такие как болезнь Альцгеймера, эпилепсия, мигрень, злоупотребление психоактивными веществами и метаболические нарушения, такие как расстройство пищевого поведения, диабет, диабетические осложнения, ожирение, дислипидемия, нарушение потребления и усвоения энергии, нарушение и неправильное функционирование температурного гомеостаза организма, нарушение сна и циркадных ритмов и сердечно-сосудистые заболевания.
Предпочтительными показаниями для применения соединений данного изобретения являются депрессия, психоз, болезнь Паркинсона, беспокойство и синдром дефицита внимания с гиперактивностью (ADHD) и диабет.
Используемый в данном документе термин "низший алкил" обозначает группу с прямой или разветвленной цепью, содержащую от одного до семи атомов углерода, например, метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и т.п. Предпочтительными алкил-группами являются группы, содержащие от 1 до 4 атомов углерода.
Используемый в данном документе термин "низший алкил, замещенный галогеном" обозначает алкильную группу, определенную выше, в которой по меньшей мере один атом водорода замещен атомом галогена.
Используемый в данном документе термин "низший алкокси" означает группу, в которой алкильный остаток является таким, как определено выше, и присоединен через атом кислорода.
Термин "галоген" означает хлор, йод, фтор и бром.
Используемый в данном документе термин "низший алкокси, замещенный галогеном" обозначает алкокси-группу, определенную выше, в которой по меньшей мере один атом водорода замещен атомом галогена.
Термин "фармацевтически приемлемые соли присоединения кислоты" охватывает соли неорганических и органических кислот, таких как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п.
Одним из воплощений данного изобретения являются соединения формулы IA
R1 обозначает фенил или пиридинил, возможно замещенный галогеном, низшим алкилом, низшим алкокси, низшим алкилом, замещенным галогеном, и низшим алкокси, замещенным галогеном;
R2 представляет собой водород или низший алкил;
Z представляет собой связь, -О- или -СН2-;
или их фармацевтически приемлемые соли присоединения кислоты,
например, следующие соединения:
(S)-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамид
(S)-5-метил-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(4-хлорфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(R)-5-метил-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамид
(R)-N-(4-(морфолин-2-ил)фенил)-2-фенил-2H-1,2,3-триазол-4-карбоксамид
(S)-2-(4-фторфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-2-(4-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(3-фторфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(3-хлорфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-2-(3-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-2-(4-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(4-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-2-п-толил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
(S)-2-(4-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(4-этоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-2-м-толил-2Н-1,2,3-триазол-4-карбоксамид гидрохлорид
(S)-N-(4-(морфолин-2-ил)фенил)-2-(3-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(3-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(S)-2-(3-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид
(RS)-2-фенил-N-(4-(пирролидин-3-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид или
2-фенил-N-(4-(пиперидин-3-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамид.
Другим воплощением данного изобретения являются соединения формулы IB
где
R1 обозначает фенил или пиридинил, возможно замещенный галогеном, низшим алкилом, низшим алкокси, низшим алкилом, замещенным галогеном, и низшим алкокси, замещенным галогеном;
Z представляет собой связь, -О- или -СН2-;
или их фармацевтически приемлемые соли присоединения кислоты, например, следующие соединения:
(S)-1-(4-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-1-(4-фторфенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-1-(3-фторфенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-1-(4-(трифторметокси)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-1-п-толил-1Н-1,2,3-триазол-4-карбоксамид гидрохлорид
(S)-1-(4-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-1-(4-этоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-1-м-толил-1Н-1,2,3-триазол-4-карбоксамид гидрохлорид
(S)-1-(3-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-1-(3-этоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-N-(4-(морфолин-2-ил)фенил)-1-(3-(трифторметокси)фенил)-1Н-1,2,3-триазол-4-карбоксамид
(S)-1-(3-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид или
(RS)-1-(4-(дифторметокси)фенил)-N-(4-(пирролидин-3-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамид.
Другим воплощением изобретения являются соединения формулы IC
где
R1 обозначает фенил или пиридинил, возможно замещенный галогеном, низшим алкилом, низшим алкокси, низшим алкилом, замещенным галогеном, и низшим алкокси, замещенным галогеном;
Z представляет собой связь, -О- или -СН2-;
или их фармацевтически приемлемые соли присоединения кислоты, например, следующее соединение:
(S)-1-(4-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,4-триазол-3-карбоксамид.
Данные соединения формулы I и их фармацевтически приемлемые соли могут быть получены способами, известными в данной области, например, способами, описанными ниже, которые включают
а) отщепление N-защитной группы от соединений формулы
с образованием соединения формулы
где определения даны выше, и,
при необходимости, превращение полученных соединений в фармацевтически приемлемые соли присоединения кислоты.
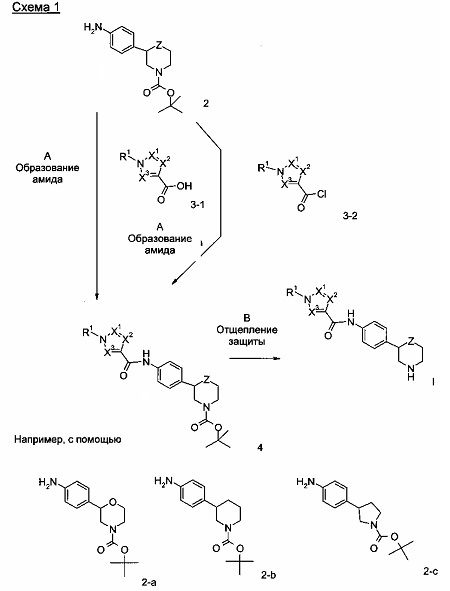
Получение соединений формулы I данного изобретения может быть проведено с использованием последовательных или конвергентных путей синтеза. Синтез соединений данного изобретения показан на следующей схеме 1 и в описании 36 конкретных примеров. Навыки, необходимые для проведения реакций и очистки полученных продуктов, известны специалистам в данной области. Заместители и индексы, используемые в последующем описании процессов, имеют значения, данные здесь ранее, если не указано иное.
Более подробно, соединения формулы I могут быть получены с помощью способов, приведенных ниже, способов, приведенных в примерах, или аналогичных способов. Подходящие условия реакции для отдельных реакционных этапов известны специалисту в данной области. Последовательность реакций не ограничена тем, что показано на схеме 1, тем не менее, в зависимости от исходных материалов и их соответствующей реакционной активности последовательность реакционных этапов может быть свободно изменена. Исходные материалы либо коммерчески доступны, либо могут быть получены способами, аналогичными способам, приведенным ниже, способами, описанными в ссылках, приведенных в описании или в примерах, или способами, известными в данной области.
Общие процедуры:
Заместители являются такими, как описано выше.
Этап А: формирование амида может быть достигнуто путем реакции сочетания между амином 2 и кислотным соединением хлорида 3-2 в галогенированных растворителях, таких как дихлорметан или 1,2-дихлорэтан, или эфирных растворителях, таких как диэтиловый эфир, диоксан, THF, DME или ТВМЕ, в присутствии органического основания, такого как триэтиламин или N,N-диизопропилэтиламин. Примеры соответствующих аминов 2 включают N-защищенные производные морфолина, такие как 2-а [CAS 1002726-96-6], производные пиперидина, такие как 2-b [CAS 875798-79-1], производные пирролидина, такие как 2-е [CAS 908334-28-1]. Предпочтительными условиями являются триэтиламин в THF при комнатной температуре в течение 18 часов.
Если необходимо, ацилхлоридное соединение 3-2 может быть получено in situ из соответствующей карбоновой кислоты 3-1 путем обработки оксалилхлоридом или 1-хлор-N,N,2-триметилпропениламином в галогенированных растворителях, таких как дихлорметан или 1,2-дихлорэтан, или эфирных растворителях, таких как диэтиловый эфир, диоксан, THF, DME или ТВМЕ, в присутствии катализатора, такого как DMF.
Предпочтительные условия: дихлорметан, при комнатной температуре в течение 1 часа.
Альтернативно, образование амида может быть осуществлено путем реакции сочетания между амином 2 и карбоновыми кислотами 3-1 в присутствии сочетающего реагента, такого как DCC, EDC, TBTU, HBTU или HATU, в присутствии органического основания, такого как триэтиламин, N,N-диизопропилэтиламин или N-метилморфолин, в галогенированных растворителях, таких как DMF, дихлорметан или 1,2-дихлорэтан, или эфирных растворителях, таких как диэтиловый эфир, диоксан, THF, DME или ТВМЕ.
Предпочтительные условия: BTU с N-метилморфолином в DMF при 60°С в течение 18 часов.
Этап В: Удаление N-концевой защитной группы ВОС может быть осуществлено с помощью минеральных кислот, таких как HCl, H2SO4 или H3PO4, или органических кислот, таких как CF3COOH, CHCl2COOH, НОАс или п-толуолсульфоновая кислота, в растворителях, таких как CH2Cl2, CHCl3, THF, диоксан, МеОН, EtOH или H2O, при температуре от 0 до 80°С.
Предпочтительные условия: HCl в диоксане при 60°С в течение 1-20 ч.
Выделение и очистка соединений
Выделение и очистка соединений и промежуточных продуктов, описанных в данном документе, могут быть осуществлены, если нужно, с помощью любой подходящей процедуры разделения или очистки, такой как, например, фильтрация, экстракция, кристаллизация, колоночная хроматография, тонкослойная хроматография, толстослойная хроматография, препаративная жидкостная хроматография низкого или высокого давления или сочетание этих процедур. Конкретные иллюстрации пригодных процедур разделения и выделения можно получить по ссылке на препараты и примеры, приведенные ниже. Тем не менее, конечно, также можно использовать другие эквивалентные процедуры разделения или выделения. Рацемические смеси хиральных соединений формулы I могут быть разделены с помощью хиральной HPLC.
Соли соединений формулы I
Соединения формулы I являются базовыми и могут быть превращены в соответствующую соль присоединения кислоты. Превращение осуществляют путем обработки по меньшей мере стехиометрическим количеством соответствующей кислоты, такой как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., и органическими кислотами, такими как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п. Как правило, свободное основание растворяют в инертном органическом растворителе, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол и т.п., и добавляют кислоту в аналогичном растворителе. Температуру поддерживают между 0°С и 50°С. Полученная соль самопроизвольно выпадает в осадок или может быть выделена из раствора с помощью менее полярного растворителя.
Соли присоединения кислоты основных соединений формулы I могут быть превращены в соответствующие свободные основания обработкой по меньшей мере стехиометрическим эквивалентом подходящего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и т.п.
Пример 1
(S)-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамид гидрохлорид
а) Получение (S)-трет-бутил 2-(4-(2-фенил-2Н-1,2,3-триазол-4-карбоксамидо)фенил)морфолин-4-карбоксилата:
В круглодонном сосуде объемом 25 мл 2-фенил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 13306-99-5) (59,8 мг, 316 мкмоль, экв: 1,1), (S)-трет-бутил 2-(4-аминофенил)морфолин-4-карбоксилат (80 мг, 287 мкмоль, экв: 1,00), N-метилморфолин (87,2 мг, 94,8 мкл, 862 мкмоль, экв: 3) и HBTU (164 мг, 431 мкмоль, экв: 1,5) объединяли с DMF (2 мл), получая желтый раствор. Реакционную смесь перемешивали при 60°С. Смесь выливали в воду (10 мл) и дважды экстрагировали с помощью EtOAc. Органические слои промывали NaHCO3, концентрированным соляным раствором, высушивали над MgSO4, фильтровали и концентрировали in vacuo, получая коричневую сырьевую смесь. Смесь разводили эфиром, перемешивали в течение 15 минут и суспензию фильтровали. Полученное твердое вещество промывали несколько раз эфиром, получая нужное соединение в виде светло-желтого твердого вещества (35 мг, 27,1%).
MS (ISP): 394,0 ([М+Н]+-изобутен).
b) (S)-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамид гидрохлорид: к раствору (S)-трет-бутил-2-(4-(2-фенил-2Н-1,2,3-триазол-4-карбоксамидо)фенил)морфолин-4-карбоксилата (30 мг, 66,7 мкмоль, экв: 1,00) в диоксане (2 мл) добавляли 4 М HCl в диоксане (250 мкл, 1,00 ммоль, экв: 15). Реакционную смесь перемешивали при 60°С в течение 48 часов. К смеси добавляли 2 мл диэтилового эфира и перемешивали в течение 15 минут при комнатной температуре. Смесь фильтровали и концентрировали под высоким вакуумом, получая ожидаемую соль HCl в виде светло-желтого твердого вещества (24 мг, 93,2%). MS (ISP): 350,3([М+Н]+).
Получение (S)-трет-бутил 2-(4-аминоФенил)морфолин-4-карбоксилата:
Этап а) (S)-2-(4-бромФенил)морфолин:
2,27 г (RS)-2-(4-бром-фенил)-морфолина (CAS-1131220-82-0) отделяли на колонке Chiralpak IA HPLC (8×32 см) с помощью смеси н-гептан/этанол (1:11) + 0,1% DEA.
(S)-2-(4-бром-фенил)-морфолин: фракции собирали с 7,6 мин до 9,4 мин. Выход 0,97 г (42,9%) с 97,4% ее
(R)-2-(4-бром-фенил)-морфолин: фракции собирали с 9,8 мин до 13,9 мин Выход 0,99 г (43,6%) с 97,4% ее
Этап b) (S)-трет-бутил 2-(4-бромфенил)морфолин-4-карбоксилат:
(S)-2-(4-бром-фенил)-морфолина (36,3 г, 150 ммоль) и N,N-диизопропилэтиламина (23,3 г, 31,4 мл, 180 ммоль) в THF (360 мл) обрабатывали дитретбутилдикарбонатом (39,3 г, 180 ммоль). Реакционную смесь перемешивали в течение 17 ч при комнатной температуре, концентрировали in vacuo, разводили этилацетатом, промывали 1М лимонной кислотой (2×100 мл), высушивали над сульфатом магния, фильтровали и концентрировали in vacuo. Сырьевой материал кристаллизовали из гексана, получая 47,1 г (92%) (S)-трет-бутил-2-(4-бромфенил)морфолин-4-карбоксилата в виде тведого вещества белого цвета сжетоватым оттенком. MS (ISP): 344,1 ([М+Н]+).
Этап с) (S)-трет-бутил 2-(4-(диФенилметиленамино)фенил)морфолин-4-карбоксилат:
(S)-трет-бутил-2-(4-бромфенил)морфолин-4-карбоксилат (47 г, 137 ммоль), дифенилметанимин (29,9 г, 27,6 м, 165 ммоль), BINAP (6,41 г, 10,3 ммоль) и Pd2(dba)3 (3,14 г, 3,43 ммоль) растворяли в атмосфере аргона в сухом и деаэрированном толуоле (940 мл) и обрабатывали третбутоксидом натрия (18,5 г, 192 ммоль). Темно-коричневую смесь перемешивали при 90°С в течение 18 ч. Желтую/коричневую реакционную смесь разводили толуолом (700 мл), охлаждали до комнатной температуры и экстрагировали дважды водой. Органический слой отделяли, высушивали над сульфатом магния и концентрировали in vacuo. Сырьевой продукт разводили в 300 мл гексана, перемешивали в течение 1 ч и отфильтровывали, получая оранжевое твердое вещество (68 г), которое очищали путем колоночной хроматографии (1,3 кг силикагеля, 20% этил ацетат/гептан). Объединенные и концентрированные фракции суспендировали в гексане, перемешивали в течение 17 ч, отфильтровывали и высушивали под высоким вакуумом, получая выход 54,1 г (89%) желтого твердого вещества. MS (ISP): 443,3 ([М+Н]+).
Этап d) (S)-трет-бутил 2-(4-аминоФенил)морфолин-4-карбоксилат:
Суспензию (S)-трет-бутил-2-(4-(дифенилметиленамино)фенил)морфолин-4-карбоксилата (54,1 г, 122 ммоль), аммония формата (116 г, 1,83 моль) и 5% Pd/C (6,5 г, 3,06 ммоль) в метаноле (930 мл) перемешивали при 60°С в течение 2 ч. Реакционную смесь фильтровали и концентрировали. Осадок растворяли в этилацетате и воде. Органическую фазу экстрагировали дважды 0,5 М HCl. Объединенные водные фазы защелачивали с помощью 2 М NaOH и экстрагировали дважды DCM. Органические фазы высушивали над сульфатом магния, фильтровали и высушивали in vacuo, получая 31,95 г твердого вещества белого цвета с желтоватым оттенком. MS (ISP): 279,1 ([М+Н]+).
Пример 2
(S)-5-метил-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично этапу а) примера 1, используя 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 22300-56-7) вместо 2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты.
Этап b): к раствору (S)-трет-бутил-2-(4-(5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоксамидо)фенил)морфолин-4-карбоксилата (106 мг, 229 мкмоль, экв: 1,00) в диоксане (298 мкл) добавляли 4 М HCl в диоксане (858 мкл, 3,43 ммоль, экв: 15). Реакционную смесь перемешивали при 60°С в течение ночи. К смеси добавляли 2 мл диоксана и перемешивали в течение 15 минут при комнатной температуре. Смесь фильтровали и концентрировали под высоким вакуумом, получая ожидаемую соль HCl в виде белого твердого вещества (82 мг, 90%)
Белое твердое вещество. MS (ISP): 364,4 ([М+Н]+).
Пример 3
(S)-1-(4-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(4-(дифторметокси)фенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1096995-13-9) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 416,1 ([М+Н]+).
Пример 4
(S)-1-(4-фторфенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(4-фторфенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 214541-35-2) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 368,0 ([М+Н]+).
Пример 5
(S)-1-(3-фторфенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(3-фторфенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 944905-84-4) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Светло-желтое твердое вещество. MS (ISP): 368,0 ([M+H]+).
Пример 6
(S)-2-(4-хлорфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-хлорофенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 89522-59-8) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Светло-желтое твердое вещество. MS (ISP): 384,2 ([М+Н]+).
Пример 7
(R)-5-метил-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 22300-56-7) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты и (R)-трет-бутил-2-(4-аминофенил)морфолин-4-карбоксилат вместо (S)-трет-бутил-2-(4-аминофенил)морфолин-4-карбоксилата на этапе а).
Светло-желтое твердое вещество. MS (ISP): 364,1 ([М+Н]+).
Пример 8
(R)-N-(4-(морфолин-2-ил)фенил)-2-фенил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-фенил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 13306-99-5) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты и (R)-трет-бутил-2-(4-аминофенил)морфолин-4-карбоксилат вместо (S)-трет-бутил-2-(4-аминофенил)морфолин-4-карбоксилата на этапе а).
Желтое твердое вещество. MS (ISP): 350,3 ([М+Н]+).
Пример 9
(S)-2-(4-фторфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-фторфенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 833-60-3) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 368,2 ([М+Н]+).
Пример 10
(S)-N-(4-(морфолин-2-ил)фенил)-2-(4-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1368530-38-4) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Светло-желтое твердое вещество. MS (ISP): 418,3 ([М+Н]+).
Пример 11
(S)-2-(3-фторфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(3-фторфенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 833-54-5) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 368,2 ([М+Н]+).
Пример 12
(S)-2-(3-хлорфенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(3-хлорофенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 90839-69-3) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Твердое вещество белого цвета с желтоватым оттенком. MS (ISP): 384,2 ([М+Н]+).
Пример 13
(S)-N-(4-(морфолин-2-ил)фенил)-2-(3-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(3-(трифторметил)фенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1368509-73-2) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 418,3 ([М+Н]+).
Пример 14
(S)-N-(4-(морфолин-2-ил)фенил)-1-(4-(трифторметокси)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(4-(трифторметокси)фенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1338653-72-7) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Светло-желтое твердое вещество. MS (ISP): 434,3 ([М+Н]+).
Пример 15
(S)-N-(4-(морфолин-2-ил)фенил)-2-(4-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоновую кислоту вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 434,3 ([М+Н]+).
Получение 2-(4-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоновой кислоты:
Этап а) этил 2-(4-(трифторметокси)Фенил)-2Н-1,2,3-триазол-4-карбоксилат:
Этил-2Н-1,2,3-триазол-4-карбоксилат (CAS 1084802-21-0) (250 мг, 1,77 ммоль, экв: 1,00), 4-(трифторметокси)фенилборную кислоту (730 мг, 3,54 ммоль, экв: 2) и ацетат меди (644 мг, 3,54 ммоль, экв: 2) растворяли в DMA (8,86 мл). Затем добавляли пиридин (560 мг, 572 мкл, 7,09 ммоль, экв: 4) и реакционную смесь перемешивали при комнатной температуре в течение 48 часов. К реакционной смеси добавляли воду и этилацетат. Органический слой отделяли, промывали насыщенным раствором соли, высушивали над MgSO4 и выпаривали. Сырьевой материал очищали путем флэш-хроматографии с силикагелем, получая белое твердое вещество (129 мг, 24%). MS (ISP): 302,1 ([М+Н]+).
Этап b) 2-(4-(трифторметокси)Фенил)-2Н-1,2,3-триазол-4-карбоновая кислота:
К раствору этил 2-(4-(трифторметокси)фенил)-2Н-1,2,3-триазол-4-карбоксилата (127 мг, 422 мкмоль, экв: 1,00) в THF (5 мл) и МеОН (1,00 мл) добавляли 1М LiOH (843 мкл, 843 мкмоль, экв: 2). Смесь перемешивали в течение ночи. К осадку добавляли воду и 1 N HCl (рН:1), эту водную фазу экстрагировали два раза этилацетатом, полученные органические слои объединяли и промывали насыщенным раствором соли, затем высушивали над MgSO4, фильтровали и концентрировали, получая нужное соединение (94 мг, 81,6%) в виде белого твердого вещества.
Пример 16
(S)-2-(4-(дифторметокси)фенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 15, используя 4-(дифторметокси)фенилборную кислоту вместо 4-(трифторметокси)фенилборной кислоты на этапе а).
Светло-желтое твердое вещество. MS (ISP): 416,3 ([М+Н]+).
Пример 17
(S)-N-(4-(морфолин-2-ил)фенил)-1-п-толил-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-п-толил-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 113934-31-9) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 364,2 ([М+Н]+).
Пример 18
(S)-N-(4-(морфолин-2-ил)фенил)-2-п-толил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-п-толил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 69059-60-5) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 364,2 ([М+Н]+).
Пример 19
(S)-1-(4-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(4-метоксифенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 4916-13-6) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 380,3 ([М+Н]+).
Пример 20
(S)-2-(4-метоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-метоксифенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 90946-76-2) вместо 5- метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 380,2 ([М+Н]+).
Пример 21
(S)-1-(4-этоксифенил)-N-(4-(морфолин-2-ил)фенил)-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-(4-этоксифенил)-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1042534-41-7) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 394,2 ([М+Н]+).
Пример 22
(S)-2-(4-этоксифенил)-N-(4-(морфолин-2-ил)фенил)-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-(4-этоксифенил)-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1368754-17-9) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 394,2 ([М+Н]+).
Пример 23
(S)-N-(4-(морфолин-2-ил)фенил)-2-м-толил-2Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 2-м-толил-2Н-1,2,3-триазол-4-карбоновую кислоту (CAS 1042655-56-0) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Белое твердое вещество. MS (ISP): 364,3 ([М+Н]+).
Пример 24
(S)-N-(4-(морфолин-2-ил)фенил)-1-м-толил-1Н-1,2,3-триазол-4-карбоксамида гидрохлорид
Названное соединение получали аналогично примеру 2, используя 1-м-толил-1Н-1,2,3-триазол-4-карбоновую кислоту (CAS 944901-55-7) вместо 5-метил-2-фенил-2Н-1,2,3-триазол-4-карбоновой кислоты на этапе а).
Бе