Анализы определения антител, специфичных к терапевтическим антителам против ige, и их применение при анафилаксии
Иллюстрации
Показать всеИзобретение относится к биохимии. Предложены способы обнаружения человеческого антитела изотипа IgE против омализумаба. Также рассмотрены наборы, способы идентификации пациента, имеющего риск анафилактической реакции на омализумаб, и способ лечения пациента, имеющего IgE-опосредованное нарушение. Данное изобретение позволяет своевременно обнаруживать аллергические реакции на омализумаб и может найти применение в терапии и предупреждении развития анафилаксии. 9 н. и 43 з.п. ф-лы, 27 ил., 7 табл., 7 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет по предварительной заявке США № 61/255052, поданной 26 октября 2009 года, включенной в настоящий документ в полном объеме путем ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение, главным образом, относится к области способов и реагентов для определения антител изотипа IgE против лекарственного средства к терапевтическим антителам против IgE, и способов оценки риска анафилаксии.
УРОВЕНЬ ТЕХНИКИ
IgE является членом семейства иммуноглобулинов, опосредующим аллергические ответы, такие как астма, пищевые аллергии, гиперчувствительность 1 типа и хорошо известный синусит, возникающие под влиянием множества факторов. B-клетки, или B-лимфоциты, секретируют и экспрессируют IgE на своей поверхности. IgE связывается с B-клетками (а также моноцитами, эозинофилами и тромбоцитами) через их Fc-область с низкоаффинным рецептором IgE, известным как FcεRII. После воздействия аллергена на млекопитающее, B-клетки, несущие поверхностное антитело IgE, специфичное к антигену, "активируются" и развиваются в IgE-секретирующие плазматические клетки. Затем получаемые специфичные к аллергену IgE циркулируют в кровотоке и связываются с поверхностью тучных клеток в тканях и базофилов в крови посредством высокоаффинного рецептора, также известного как FcεRI. Таким образом, тучные клетки и базофилы покрываются к аллергену. Последующее воздействие аллергена вызывает перекрестное сшивание FcεRI базофила и тучной клетки, приводящее к дегрануляции данных клеток и высвобождению гистамина, лейкотриенов и факторов активации тромбоцитов, хемотактических факторов эозинофилов и нейтрофилов и цитокинов IL-3, IL-4, IL-5 и GM-CSF, ответственных за клиническую гиперчувствительность и анафилаксию.
Антагонисты, блокирующие образование IgE-рецепторного комплекса, применимы в качестве терапевтических средств для предотвращения аллергического ответа. Разработано несколько терапевтических средств антител против IgE. Данные антитела против IgE блокируют связывание IgE с высокоаффинным рецептором FcεRI, обнаруженном на базофилах и тучных клетках, и, таким образом, предотвращают высвобождение гистамина и других анафилактических факторов, приводящее к патологическому состоянию.
Сообщают, что анафилаксия возникает у пациентов после получения антител против IgE, таких как омализумаб (например, Xolair®). Анафилаксия является острой системной (мультисистемной) и очень тяжелой аллергической реакцией гиперчувствительности 1 типа. Она вызвана дегрануляцией тучных клеток и базофилов и опосредована IgE. В течение 2006 года у 124 из 57269 (приблизительно 0,2%) пациентов с астмой возникала анафилаксия после введения омализумаба. В то время как не сообщали о смертельных случаях анафилаксии в результате введения омализумаба, некоторые случаи являлись тяжелыми и потенциально опасными для жизни. По этой причине FDA рекомендует наблюдать пациентов, получающих омализумаб, в кабинете врача в течение периода времени после введения омализумаба, и медицинские работники, вводящие омализумаб, должны быть готовы к оказанию помощи при анафилаксии, которая может являться опасной для жизни. Шестьдесят процентов приведенных случаев (124) имели место после первых двух доз омализумаба. Таким образом, возможно, что реакцию у пациентов вызывают уже существующие антитела, распознающие эпитоп на омализумабе, в отличие от реакции против лекарственного средства, развивающейся после введения лекарственного средства. Т.к. анафилаксия связана с антителом изотипа IgE, существует необходимость разработки анализа для определения и количественного определения у пациента IgE, специфичного к терапевтическому антителу против IgE, для оценки риска анафилаксии, предпочтительно, до лечения таким антителом против IgE и идентификации пациентов с высоким риском.
Все цитируемые в данном документе ссылки, включая патентные заявки и публикации, в полном объеме включены путем ссылки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном из аспектов изобретение относится к способам определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, включающим этапы: a) приведения образца, который может содержать антитело против лекарственного средства, в контакт с мутантным терапевтическим антителом, содержащим по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где относительная аффинность связывания мутантного терапевтического антитела с IgE (такого как IgE человека) составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с IgE; и b) определения связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В некоторых вариантах осуществления относительная аффинность связывания мутантного терапевтического антитела составляет приблизительно 7,5% или менее, приблизительно 5% или менее, приблизительно 2,5% или менее, приблизительно 2,0% или менее, приблизительно 1,5% или менее, приблизительно 1% или менее, приблизительно 0,9% или менее, приблизительно 0,8% или менее, приблизительно 0,7% или менее, приблизительно 0,5% или менее, приблизительно 0,25% или менее, приблизительно 0,1% или менее от относительной аффинности связывания терапевтического антитела против IgE.
В другом аспекте изобретение относится к способам определения антител изотипа IgE против лекарственного средства, связывающихся с терапевтическим антителом против IgE, в образце, включающим этапы: a) приведения образца, который может содержать антитела против лекарственного средства, в контакт с мутантным терапевтическим антителом, обладающим по меньшей мере одной мутацией аминокислоты терапевтического антитела против IgE, где активность мутантного терапевтического антитела по отношению к IgE (такого как IgE человека) составляет приблизительно 10% или менее от активности терапевтического антитела против IgE по отношению к IgE; и b) определения связывания антител против лекарственного средства с мутантным терапевтическим антителом.
В некоторых вариантах осуществления активность мутантного терапевтического антитела составляет приблизительно 7,5% или менее, приблизительно 5% или менее, приблизительно 2,5% или менее, приблизительно 2,0% или менее, приблизительно 1,5% или менее, приблизительно 1% или менее, приблизительно 0,9% или менее, приблизительно 0,8% или менее, приблизительно 0,7% или менее, приблизительно 0,5% или менее, приблизительно 0,25% или менее, приблизительно 0,1% или менее от активности терапевтического антитела против IgE.
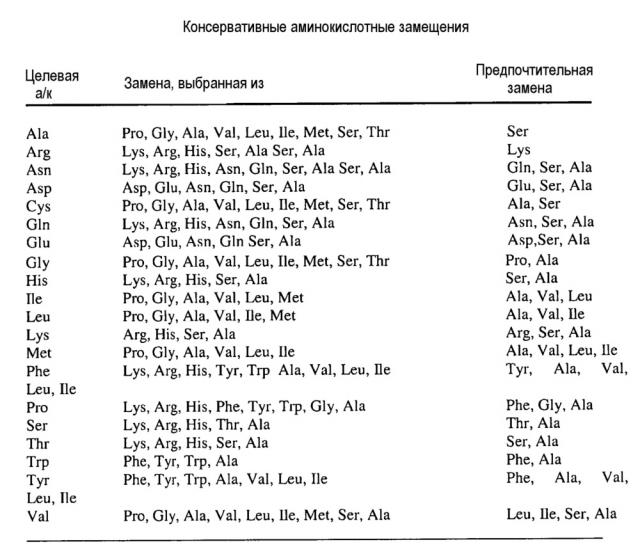
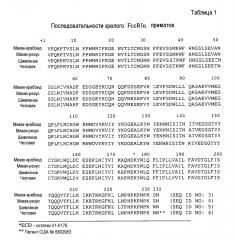
Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит одну, две, три, четыре, пять или шесть мутаций аминокислот в последовательностях CDR тяжелой и/или легкой цепи терапевтического антитела против IgE. В некоторых вариантах осуществления терапевтическое антитело против IgE является омализумабом, и мутантное терапевтическое антитело содержит одну, две или три мутации аминокислот в первой CDR легкой цепи омализумаба. В некоторых вариантах осуществления терапевтическое антитело против IgE является омализумабом, и мутантное терапевтическое антитело содержит замену аминокислоты в положении 34 (Asp) легкой цепи (SEQ ID NO:1) омализумаба. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит аминокислотную последовательность тяжелой цепи SEQ ID NO:2 и аминокислотную последовательность легкой цепи SEQ ID NO:1, где заменяют аминокислоты в положениях 30 (Asp) и 34 (Asp) или положениях 32 (Asp) и 34 (Asp) легкой цепи. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит аминокислотную последовательность тяжелой цепи SEQ ID NO:2 и аминокислотную последовательность легкой цепи SEQ ID NO:1, где в легкой цепи заменяют аминокислоту D (Asp) в положениях 30, 32 и 34. В некоторых вариантах осуществления аминокислоту Asp заменяют на Ala. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит аминокислотную последовательность тяжелой цепи SEQ ID NO:2 и аминокислотную последовательность легкой цепи SEQ ID NO:1 с заменами аминокислот Asp на Ala в положениях 30, 32 и 34 легкой цепи. В некоторых вариантах осуществления терапевтическое антитело против IgE является омализумабом, и мутантное терапевтическое антитело содержит одну, две или три мутации аминокислот в третьей CDR тяжелой цепи омализумаба. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит аминокислотную последовательность тяжелой цепи SEQ ID NO:2 и аминокислотную последовательность легкой цепи SEQ ID NO:1, где заменяют аминокислоты в положениях 101 (His), 105 (His) и 107 (His) тяжелой цепи (SEQ ID NO:2). В некоторых вариантах осуществления аминокислоту His заменяют на Ala. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит аминокислотную последовательность тяжелой цепи SEQ ID NO:2 с заменами аминокислот His на Ala в положениях 101, 105 и 107 тяжелой цепи и аминокислотную последовательность легкой цепи SEQ ID NO:1.
В некоторых вариантах осуществления мутантное терапевтическое антитело иммобилизируют или фиксируют на поверхности. В некоторых вариантах осуществления мутантное терапевтическое антитело напрямую иммобилизируют на поверхности. В некоторых вариантах осуществления мутантное терапевтическое антитело конъюгируют с меткой и иммобилизируют или фиксируют на поверхности средством фиксации, специфически связывающимся с меткой, где средство фиксации иммобилизируют на поверхности. В некоторых вариантах осуществления метка является биотином, и средство фиксации является стрептавидином. В некоторых вариантах осуществления метка является дигоксигенином, и средство фиксации является антителом против дигоксигенина.
В некоторых вариантах осуществления образец приводят в контакт с мутантным терапевтическим антителом, которое иммобилизируют или фиксируют на поверхности. В некоторых вариантах осуществления образец приводят в контакт с мутантным терапевтическим антителом до фиксации мутантного терапевтического антитела на поверхности. В некоторых вариантах осуществления мутантное терапевтическое антитело фиксируют на поверхности после приведения образца в контакт с мутантным терапевтическим антителом и до определения связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В некоторых вариантах осуществления связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют средством детекции. В некоторых вариантах осуществления средство детекции является полипептидом FcεRIα, связывающимся с Fc-областью IgE. Можно применять любые полипептиды FcεRIα, предоставляемые в настоящем документе. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα, слитый с константной областью IgG. В некоторых вариантах осуществления метят полипептид FcεRIα. В некоторых вариантах осуществления метка выбрана из группы, состоящей из биотина, дигоксигенина, рутения, радиоактивной метки, фотолюминесцентной метки, хемилюминесцентной метки, флуоресцентной метки, электрохемилюминесцентной метки и ферментной метки. В некоторых вариантах осуществления полипептид FcεRIα метят биотином, и связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют посредством стрептавидина-HRP. В некоторых вариантах осуществления полипептид FcεRIα метят дигоксигенином, и связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют посредством конъюгированного с HRP антитела против дигоксигенина. В некоторых вариантах осуществления полипептид FcεRIα метят рутением, и связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют анализом электрохемилюминесценции.
В некоторых вариантах осуществления образец содержит сыворотку или плазму человека. В некоторых вариантах осуществления образец содержит терапевтическое антитело против IgE. В некоторых вариантах осуществления образец не содержит терапевтическое антитело против IgE. В некоторых вариантах осуществления сыворотка или плазма содержит омализумаб. В других вариантах осуществления сыворотка или плазма не содержит омализумаб.
В некоторых вариантах осуществления способы дополнительно включают этап сравнения связывания антител против лекарственного средства с мутантным терапевтическим антителом с референсным значением. В некоторых вариантах осуществления референсное значение представляет собой определяемое связывание между мутантным терапевтическим антителом и контрольным антителом. В некоторых вариантах осуществления контрольное антитело является антителом положительного контроля, связывающимся и с терапевтическим антителом против IgE, и с мутантным терапевтическим антителом со схожей аффинностью. В некоторых вариантах осуществления антитело положительного контроля содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:7, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:8. В некоторых вариантах осуществления антитело положительного контроля дополнительно содержит константные области тяжелой цепи и легкой цепи IgE человека.
В другом аспекте изобретение также относится к наборам для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, содержащим (a) мутантное терапевтическое антитело, содержащее по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где относительная аффинность связывания мутантного терапевтического антитела с IgE (такого как IgE человека) составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с IgE; и b) средство детекции, связывающееся с Fc-областью IgE. Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления средство детекции является полипептидом FcεRIα. В набор можно включать любые полипептиды FcεRIα, предоставляемые в настоящем документе. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα, слитый с константной областью IgG. В некоторых вариантах осуществления метят полипептид FcεRIα (например, метят биотином, дигоксигенином, рутением и т.д.). В некоторых вариантах осуществления набор дополнительно содержит стрептавидин-HRP или Amdex SA-HRP. В некоторых вариантах осуществления набор дополнительно содержит конъюгированное с HRP антитело против дигоксигенина для определения меченного дигоксигенином полипептида FcεRIα. В некоторых вариантах осуществления набор дополнительно содержит антитело положительного контроля, связывающееся и с терапевтическим антителом против IgE, и с мутантным терапевтическим антителом со схожей аффинностью. В некоторых вариантах осуществления антитело положительного контроля содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:7, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:8. В некоторых вариантах осуществления антитело положительного контроля дополнительно содержит константные области тяжелой цепи и легкой цепи IgE человека.
В другом аспекте изобретение также относится к наборам для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, содержащим a) мутантное терапевтическое антитело, обладающее по меньшей мере одной мутацией аминокислоты терапевтического антитела против IgE, где активность мутантного терапевтического антитела по отношению к IgE (такого как IgE человека) составляет приблизительно 10% или менее от активности терапевтического антитела против IgE по отношению к IgE; и b) средство детекции, связывающееся с Fc-областью IgE. Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления средство детекции является полипептидом FcεRIα. В набор можно включать любые полипептиды FcεRIα, предоставляемые в настоящем документе. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα, слитый с константной областью IgG. В некоторых вариантах осуществления метят полипептид FcεRIα (например, метят биотином, дигоксигенином, рутением и т.д.). В некоторых вариантах осуществления набор дополнительно содержит стрептавидин-HRP или Amdex SA-HRP. В некоторых вариантах осуществления набор дополнительно содержит конъюгированное с HRP антитело против дигоксигенина для определения меченного дигоксигенином полипептида FcεRIα. В некоторых вариантах осуществления набор дополнительно содержит антитело положительного контроля, связывающееся и с терапевтическим антителом против IgE, и с мутантным терапевтическим антителом со схожей аффинностью. В некоторых вариантах осуществления антитело положительного контроля содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:7, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, представленную в SEQ ID NO:8. В некоторых вариантах осуществления антитело положительного контроля дополнительно содержит константные области тяжелой цепи и легкой цепи IgE человека.
В другом аспекте изобретение также относится к способам определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, включающим этапы: (a) приведения образца, который может содержать антитело против лекарственного средства, в контакт с (i) мутантным терапевтическим антителом и (ii) полипептидом FcεRIα, связывающимся с Fc-областью IgE человека, где мутантное терапевтическое антитело содержит по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека; (b) фиксацию мутантного терапевтического антитела на поверхности; и (c) определение связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В некоторых вариантах осуществления избыточное количество полипептида FcεRIα приводят в контакт с образцом на этапе (a). В некоторых вариантах осуществления по меньшей мере приблизительно 2-кратный, по меньшей мере приблизительно 3-кратный, по меньшей мере приблизительно 4-кратный, по меньшей мере приблизительно 5-кратный, по меньшей мере приблизительно 6-кратный, по меньшей мере приблизительно 7-кратный, по меньшей мере приблизительно 8-кратный, по меньшей мере приблизительно 9-кратный или по меньшей мере приблизительно 10-кратный избыток полипептида FcεRIα приводят в контакт с образцом на этапе (a). Можно применять любые полипептиды FcεRIα, предоставляемые в настоящем документе. В некоторых вариантах осуществления полипептид FcεRIα содержит внеклеточный домен субъединицы FcεRIα. Полипептид FcεRIα можно метить или не метить.
Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления мутантное терапевтическое антитело метят и фиксируют на поверхности средством фиксации, специфически связывающимся с меткой. В некоторых вариантах осуществления метка является биотином, и поверхность покрывают стрептавидином. В некоторых вариантах осуществления связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют посредством меченого антитела против IgE человека. В некоторых вариантах осуществления метят полипептид FcεRIα и определяют связывание антитела против лекарственного средства с мутантным терапевтическим антителом средством детекции, специфически связывающимся с меткой на полипептиде FcεRIα. В некоторых вариантах осуществления полипептид FcεRIα метят дигоксигенином, и связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют конъюгированным с HRP антителом против дигоксигенина. В некоторых вариантах осуществления полипептид FcεRIα метят рутением, и связывание антитела против лекарственного средства с мутантным терапевтическим антителом определяют анализом электрохемилюминесценции.
В другом аспекте изобретение также относится к наборам для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, содержащим: (a) мутантное терапевтическое антитело, содержащее по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с IgE человека; и (b) полипептид FcεRIα, связывающийся с Fc-областью IgE человека. Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. Можно применять любой полипептид FcεRIα, описываемый в настоящем документе. В некоторых вариантах осуществления в наборе предоставляют избыточное количество полипептида FcεRIα. В некоторых вариантах осуществления метят полипептид FcεRIα. В некоторых вариантах осуществления набор дополнительно содержит средство детекции, специфически связывающееся с меткой на полипептиде FcεRIα. В некоторых вариантах осуществления набор дополнительно содержит антитело против IgE человека. В некоторых вариантах осуществления метят антитело против IgE человека.
В другом аспекте изобретение также относится к способам определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, включающим этапы: (a) преинкубации образца, который может содержать антитело против лекарственного средства, с избыточным количеством полипептида FcεRIα, связывающегося с Fc-областью IgE человека; (b) инкубации преинкубированного на этапе (a) образца с терапевтическим антителом против IgE или мутантным терапевтическим антителом, содержащим по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека снижена по сравнению с относительной аффинностью связывания терапевтического антитела против IgE с указанным IgE человека; и (c) определения связывания антитела против лекарственного средства с терапевтическим антителом против IgE или мутантным терапевтическим антителом.
Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления мутантное терапевтическое антитело содержит по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека.
В некоторых вариантах осуществления по меньшей мере приблизительно 2-кратный, по меньшей мере приблизительно 3-кратный, по меньшей мере приблизительно 4-кратный, по меньшей мере приблизительно 5-кратный, по меньшей мере приблизительно 6-кратный, по меньшей мере приблизительно 7-кратный, по меньшей мере приблизительно 8-кратный, по меньшей мере приблизительно 9-кратный или по меньшей мере приблизительно 10-кратный избыток полипептида FcεRIα преинкубируют с образцом на этапе (a). Можно применять любые полипептиды FcεRIα, предоставляемые в настоящем документе.
В некоторых вариантах осуществления терапевтическое антитело против IgE или мутантное терапевтическое антитело фиксируют на поверхности до или после инкубации с образцом на этапе (b). В некоторых вариантах осуществления терапевтическое антитело против IgE или мутантное терапевтическое антитело напрямую иммобилизируют на поверхности до инкубации с образцом на этапе (b).
В некоторых вариантах осуществления терапевтическое антитело против IgE или мутантное терапевтическое антитело метят и фиксируют на поверхности иммобилизированным средством фиксации, специфически связывающимся с меткой. В некоторых вариантах осуществления терапевтическое антитело против IgE или мутантное терапевтическое антитело метят биотином и фиксируют на покрытой стрептавидином поверхности.
В некоторых вариантах осуществления связывание антитела против лекарственного средства с терапевтическим антителом или мутантным терапевтическим антителом определяют посредством конъюгированного с HRP антитела против IgE человека. В некоторых вариантах осуществления метят полипептид FcεRIα и определяют связывание антитела против лекарственного средства с терапевтическим антителом против IgE или мутантным терапевтическим антителом посредством определения метки. В некоторых вариантах осуществления полипептид FcεRIα метят дигоксигенином и определяют связывание антитела против лекарственного средства с терапевтическим антителом или мутантным терапевтическим антителом посредством конъюгированного с HRP антитела против дигоксигенина. В некоторых вариантах осуществления полипептид FcεRIα метят рутением и определяют связывание антитела против лекарственного средства с терапевтическим антителом против IgE или мутантным терапевтическим антителом анализом электрохемилюминесценции.
В другом аспекте изобретение также относится к наборам для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, содержащим: (a) терапевтическое антитело против IgE или его мутантное терапевтическое антитело, где мутантное терапевтическое антитело содержит по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где относительная аффинность связывания мутантного терапевтического антитела с IgE человека снижена по сравнению с относительной аффинностью связывания терапевтического антитела против IgE с IgE человека; и (b) полипептид FcεRIα, связывающийся с Fc-областью IgE человека. Можно применять любые мутантные терапевтические антитела, предоставляемые в настоящем документе. В некоторых вариантах осуществления набор дополнительно содержит антитело против IgE человека. В некоторых вариантах осуществления метят антитело против IgE человека. Можно применять любой полипептид FcεRIα, предоставляемый в настоящем документе. В некоторых вариантах осуществления метят полипептид FcεRIα. В некоторых вариантах осуществления набор дополнительно содержит средство детекции, специфически связывающееся с меткой на полипептиде FcεRIα.
В другом аспекте изобретение относится к способам идентификации пациента, имеющего риск анафилактической реакции на терапевтическое антитело против IgE, включающим этапы: (a) приведения образца от пациента в контакт с мутантным терапевтическим антителом, содержащим по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека; и (b) определения связывания антитела изотипа IgE против лекарственного средства с мутантным терапевтическим антителом, где наличие и/или уровень антитела против лекарственного средства в образце свидетельствует о том, что пациент обладает риском анафилактической реакции на терапевтическое антитело против IgE.
В другом аспекте изобретение относится к способам идентификации пациента, имеющего риск анафилактической реакции на терапевтическое антитело против IgE, включающим этапы: (a) приведения образца от пациента в контакт с мутантным терапевтическим антителом, содержащим по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, где активность мутантного терапевтического антитела по отношению к IgE человека составляет приблизительно 10% или менее от активности терапевтического антитела против IgE по отношению к указанному IgE человека; и (b) определения связывания антитела изотипа IgE против лекарственного средства с мутантным терапевтическим антителом, где наличие и/или уровень антитела против лекарственного средства в образце свидетельствует о том, что пациент обладает риском анафилактической реакции на терапевтическое антитело против IgE.
В другом аспекте изобретение относится к способам идентификации пациента, имеющего риск анафилактической реакции на терапевтическое антитело против IgE, включающим этапы: (a) приведения образца от пациента в контакт с (i) мутантным терапевтическим антителом и (ii) полипептидом FcεRIα, связывающимся с Fc-областью IgE человека, где мутантное терапевтическое антитело содержит по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека; (b) фиксации мутантного терапевтического антитела на поверхности; и (c) определения связывания антитела изотипа IgE против лекарственного средства с мутантным терапевтическим антителом, где наличие и/или уровень антитела против лекарственного средства в образце свидетельствует о том, что пациент обладает риском анафилактической реакции на терапевтическое антитело против IgE.
В другом аспекте изобретение относится к способам идентификации пациента, имеющего риск анафилактической реакции на терапевтическое антитело против IgE, включающим этапы: (a) преинкубации образца от пациента с избыточным количеством полипептида FcεRIα, связывающегося с Fc-областью IgE человека; (b) инкубации преинкубированного на этапе (a) образца с терапевтическим антителом против IgE или мутантным терапевтическим антителом, содержащим по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека снижена по сравнению с относительной аффинностью связывания терапевтического антитела против IgE с указанным IgE человека; и (c) определения связывания антитела изотипа IgE против лекарственного средства с терапевтическим антителом против IgE или мутантным терапевтическим антителом, где наличие и/или уровень антитела против лекарственного средства в образце свидетельствует о том, что пациент обладает риском анафилактической реакции на терапевтическое антитело против IgE.
В другом аспекте изобретение относится к способам лечения пациента, обладающего IgE-опосредованным нарушением, включающим этапы: (a) определения уровня антитела изотипа IgE против лекарственного средства к терапевтическому антителу против IgE в образце от пациента; (b) введения эффективного количества терапевтического антитела против IgE пациенту, если уровень антитела против лекарственного средства в образце не свидетельствует о том, что пациент обладает риском анафилактической реакции на терапевтическое антитело против IgE. Уровень антитела против лекарственного средства можно определять любыми способами, предоставляемыми в настоящем документе.
В другом аспекте изобретение относится к применению мутантного терапевтического антитела, содержащего по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE в получении набора для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE в образце, где определение включает этапы: (a) приведения образца, который может содержать антитело против лекарственного средства, в контакт с мутантным терапевтическим антителом, где относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека; и (b) определения связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В другом аспекте изобретение относится к применению мутантного терапевтического антитела, содержащего по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, в получении набора для определения антител изотипа IgE против лекарственного средства, связывающихся с терапевтическим антителом против IgE, в образце, где определение включает этапы: (a) приведения образца который может содержать антитело против лекарственного средства, в контакт с мутантным терапевтическим антителом, где активность мутантного терапевтического антитела по отношению к IgE человека составляет приблизительно 10% или менее от активности терапевтического антитела против IgE по отношению к указанному IgE человека; и (b) определения связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В другом аспекте изобретение относится к применению (i) мутантного терапевтического антитела и (ii) полипептида FcεRIα, связывающегося с Fc-областью IgE человека, в получении набора для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, где определение включает этапы: (a) приведения образца, который может содержать антитело против лекарственного средства, в контакт с (i) мутантным терапевтическим антителом и (ii) полипептидом FcεRIα, где мутантное терапевтическое антитело содержит по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека составляет приблизительно 10% или менее от относительной аффинности связывания терапевтического антитела против IgE с указанным IgE человека; (b) фиксации мутантного терапевтического антитела на поверхности; и (c) определения связывания антитела против лекарственного средства с мутантным терапевтическим антителом.
В другом аспекте изобретение относится к применению (i) терапевтического антитела против IgE или мутантного терапевтического антитела, содержащего по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, и (ii) полипептида FcεRIα, связывающегося с Fc-областью IgE человека, в получении набора для определения антитела изотипа IgE против лекарственного средства, связывающегося с терапевтическим антителом против IgE, в образце, где определение включает этапы: (a) преинкубации образца, который может содержать антитело против лекарственного средства, с избыточным количеством полипептида FcεRIα; (b) инкубации преинкубированного на этапе (a) образца с терапевтическим антителом против IgE или мутантным терапевтическим антителом, и относительная аффинность связывания мутантного терапевтического антитела с IgE человека снижена по сравнению с относительной аффинностью связывания терапевтического антитела против IgE с указанным IgE человека; и (c) определения связывания антитела против лекарственного средства с терапевтическим антителом против IgE или мутантным терапевтическим антителом.
В другом аспекте изобретение относится к применению мутантного терапевтического антитела, содержащего по меньшей мере одну мутацию аминокислоты терапевтического антитела против IgE, в получении набора для идентификации пациента, имеющего риск анафилактической