Жидкая композиция длительно действующих инсулина и инсулинотропного пептида
Иллюстрации
Показать всеГруппа изобретений относится к области фармакологии и медицины и касается жидкой композиции, содержащей комбинацию длительно действующего инсулина в форме, в которой инсулин связан с Fc-областью иммуноглобулина и инсулинотропного пептида, который находится в форме, в которой пептид связан с Fc-областью иммуноглобулина. Композиция не содержит альбумина, а стабилизатор содержит буфер, сахарный спирт, неионное поверхностно-активное вещество и изотонический агент. Заявлен также способ получения жидкой композиции. Группа изобретений обеспечивает превосходную стабильность при хранении композиции, содержащей конъюгат инсулина и конъюгат инсулинотропного пептида в высокой концентрации без риска заражения вирусами. 2 н. и 31 з.п. ф-лы, 4 пр., 7 табл.,4 ил.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к жидкой композиции комбинации длительно действующих инсулина и инсулинотропного пептида, содержащей инсулин и инсулинотропный пептид, являющиеся физиологически активными пептидами, и не содержащий альбумина стабилизатор, который содержит буфер, сахарный спирт, неионное поверхностно-активное вещество и изотонический агент; и к способу получения жидкой композиции.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Инсулин представляет собой пептид, секретируемый бета-клетками поджелудочной железы, и в организме он играет центральную роль в контроле уровней глюкозы в крови. Если количество секретируемого инсулина в организме недостаточно или если секретируемый инсулин функционирует неправильно, уровень глюкозы в крови будет повышен, приводя к метаболическому заболеванию, называемому диабетом. При неправильной секреции инсулина или его неправильном функционировании в организме уровень глюкозы в крови нерегулируемо повышается, и этот тип диабета называют диабетом II типа. Диабет I типа развивается, когда поджелудочная железа не вырабатывает достаточно инсулина для регуляции повышения уровня глюкозы в крови. Диабет II типа обычно лечат посредством введения пероральных гипогликемических агентов, состоящих, главным образом, из химических соединений, и иногда некоторым пациентам можно вводить инсулин. С другой стороны, для лечения диабета I типа введение инсулина необходимо.
Широко применяемое лечение инсулином представляет собой инъекции инсулина до и после приема пищи. В настоящее время инсулин доступен в композиции для парентеральных инъекций, его вводят главным образом подкожно, и, в зависимости от продолжительности лечения, способ введения может быть другим. Введение инсулина посредством инъекции более эффективно снижает уровень глюкозы в крови по сравнению с пероральным лекарственным средством, и его можно безопасно применять в обстоятельствах, при которых пероральное лекарственное средство не может быть использовано. Кроме того, парентеральные инъекции инсулина не имеют ограничений по дозе, тем не менее, поскольку их необходимо проводить регулярно три раза в сутки, они обладают такими недостатками, как вызывание отвращения к иглам, сложный способ введения, симптомы гипогликемии и увеличение массы тела из-за длительного введения инсулина. В частности, увеличение массы тела повышает риск развития сердечнососудистых заболеваний и может нарушать регуляторную функцию организма относительно уровня глюкозы в крови. В то же время было предпринято множество попыток максимизировать терапевтический эффект инсулинового пептидного лекарственного средства посредством поддержания высокого уровня лекарственного средства в крови на протяжении длительного периода времени после введения лекарственного средства в организм. В результате был разработан, произведен и выведен на рынок длительно действующий инсулин. Примеры такого длительно действующего лекарственного средства включают лантус (инсулин гларгин; Sanofi Aventis) и левемир (инсулин детемир; Novo Nordisk). В отличие от инсулина «нейтральный протамин Хагедорна» (NPH) длительно действующие лекарственные средства имеют меньший риск гипогликемии в состоянии сонливости. В частности, левемир уменьшает степень увеличения массы тела. Тем не менее способ введения, включающий одну или две инъекции в сутки, все еще имеет недостатки.
В то же время, глюкагоноподобный пептид-1 (GLP-1), являющийся разновидностью инсулинотропного пептида, представляет собой инкретиновый гормон, секретируемый L-клетками подвздошной и толстой кишки. Основной функцией GLP-1 является повышение секреции инсулина для развития глюкозозависимой секреции инсулина в организме, предотвращая таким образом гипогликемию. Благодаря этому эффекту, GLP-1 можно использовать для лечения диабета 2 типа. Тем не менее, поскольку период полувыведения GLP-1 из сыворотки составляет всего 2 минуты, возможности разработки лекарственного средства на его основе ограничены. Поэтому был разработан и произведен новый агонист GLP-1, называемый эксендином-4. Эксендин-4 представляет собой агонист GLP-1, образующийся в слюнной железе ящерицы-ядозуба. Кроме того, эксендин-4 устойчив к дипептидилпептидазе-4 (DPP-IV) и обладает более высокой физиологической активностью, чем GLP-1. Таким образом, период полувыведения эксендина-4 из организма составляет от 2 до 4 часов, что намного больше, чем у GLP-1 (патент США, регистрационный № US 5424286). Тем не менее достаточной продолжительности физиологической активности лекарственного средства нельзя добиться только повышением устойчивости к DPPIV. Например, доступный в настоящее время эксендин-4 (эксенатид) необходимо вводить пациенту два раза в сутки инъекцией, и он все еще имеет недостатки, вызывая тошноту и рвоту.
Поэтому в качестве способа одновременного поддержания активности белкового лекарственного средства и улучшения его стабильности в организме для решения описанных выше проблем авторы настоящего изобретения ранее предложили разработку длительно действующего белкового конъюгата посредством связывания известного физиологически активного полипептида и Fc-области иммуноглобулина ковалентной связью с использованием непептидильного полимера в качестве линкера (корейский патент, регистрационный №10-0725315). В частности, ранее было подтверждено, что как длительно действующий конъюгат инсулина, так и длительно действующий конъюгат эксендина-4 имеют существенно увеличенную продолжительность сохранения in vivo (корейский патент, регистрационный №10-1058290 и публикация №10-2011-0134210). Тем не менее введение терапевтически эффективного количества инсулина или эксендина-4 для поддержания стабильного уровня глюкозы в крови может приводить к увеличению массы тела или симптомам тошноты и рвоты. Поэтому существует выраженная потребность в разработке терапевтического способа, позволяющего снизить дозу лекарственного средства и частоту введения, обеспечивая в то же время превосходный терапевтический эффект в отношении диабета.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая проблема
С учетом данного предшествующего уровня техники при попытке обеспечить стабильную жидкую композицию комбинации длительно действующего конъюгата инсулина и длительно действующего конъюгата инсулинотропного пептида, которая позволяла бы хранить комбинацию двух конъюгатов на протяжении длительного периода времени без риска заражения вирусами, авторы настоящего изобретения повысили стабильность комбинации двух конъюгатов с использованием стабилизатора, содержащего буфер, сахарный спирт, хлорид натрия в качестве изотонического агента и неионное поверхностно-активное вещество, и разработали экономически выгодную и стабильную жидкую композицию, в чем и заключается настоящее изобретение.
Техническое решение
Одной задачей настоящего изобретения является обеспечение жидкой композиции комбинации длительно действующих инсулина и инсулинотропного пептида, содержащей инсулин и инсулинотропный пептид, являющиеся физиологически активными пептидами, и не содержащий альбумина стабилизатор, который содержит буфер, сахарный спирт, неионное поверхностно-активное вещество и изотонический агент.
Другой задачей настоящего изобретения является обеспечение способа получения жидкой композиции.
Другой задачей настоящего изобретения является обеспечение фармацевтической композиции для предотвращения или лечения диабета, содержащей инсулин и инсулинотропный пептид.
Другой задачей настоящего изобретения является обеспечение способа лечения диабета, включающего введение композиции субъекту с диабетом.
Полезные эффекты
Комбинация длительно действующего конъюгата инсулина и длительно действующего конъюгата инсулинотропного пептида демонстрирует отличный терапевтический эффект для лечения диабета. Кроме того, жидкая композиция комбинации длительно действующего конъюгата инсулина и длительно действующего конъюгата инсулинотропного пептида по настоящему изобретению содержит стабилизатор, содержащий буфер, сахарный спирт, изотонический агент и неионное поверхностно-активное вещество, но не содержит человеческого сывороточного альбумина и других потенциально токсичных для организма факторов, и, таким образом, риск инфицирования вирусами отсутствует. Кроме того, жидкая композиция обеспечивает превосходную стабильность при хранении для длительно действующего конъюгата инсулина и длительно действующего конъюгата инсулинотропного пептида, имеющих увеличенную молекулярную массу и увеличенную продолжительность сохранения in vivo по сравнению с нативной формой, поскольку они состоят из инсулина или инсулинотропного пептида и Fc-области иммуноглобулина. В частности, согласно настоящему изобретению предложена стабильная жидкая композиция комбинации длительно действующего конъюгата инсулина и длительно действующего конъюгата инсулинотропного пептида. Такая жидкая композиция по настоящему изобретению представляет собой простую композицию, обеспечивающую превосходную стабильность при хранении и, таким образом, более выгодную с экономической точки зрения по сравнению с композициями, полученными с использованием других стабилизаторов и лиофильной сушки. Кроме того, настоящая жидкая композиция позволяет сохранять активность белка в организме на протяжении более длительного периода по сравнению с другими обычными композициями инсулина и инсулинотропного пептида, и, таким образом, она может быть использована как эффективная композиция лекарственного средства.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
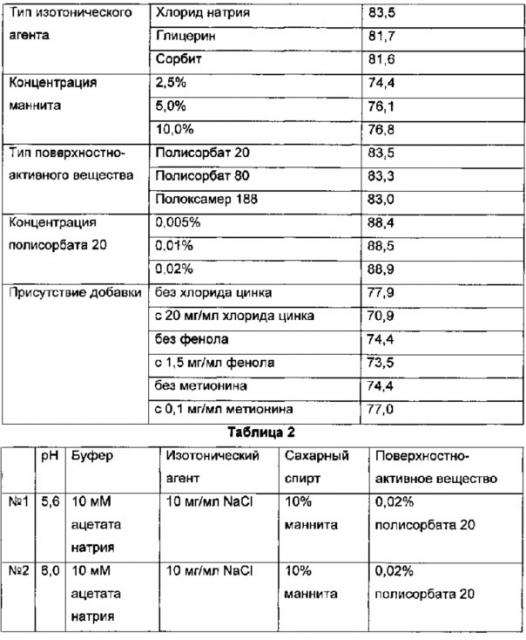
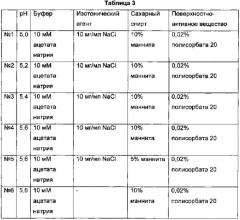
На Фиг. 1 показаны результаты мониторинга преципитации для композиций длительно действующего конъюгата инсулинотропного пептида, полученного в композициях по Таблице 3, при 40°C в течение 1 недели.
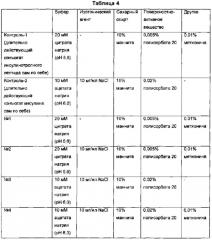
На Фиг. 2 показаны результаты IE-HPLC (ионообменная высокоэффективная жидкостная хроматография) - анализа длительно действующих конъюгата инсулина и конъюгата инсулинотропного пептида, которые получали в композициях по Таблице 4 и хранили при 40°C в течение 4 недель.
На Фиг. 3 показаны результаты PH-HPLC (высокоэффективная жидкостная хроматография с обращенной фазой) - анализа длительно действующих конъюгата инсулина и конъюгата инсулинотропного пептида, которые получали в композициях по Таблице 4 и хранили при 40°C в течение 4 недель.
На Фиг. 4 показаны результаты мониторинга преципитации белка в каждой из комбинированных композиций, имеющих разный состав, по сравнению с раздельной композицией.
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В качестве одного аспекта настоящего изобретения предложена жидкая композиция длительно действующих инсулина и инсулинотропного пептида, содержащая инсулин и инсулинотропный пептид, являющиеся физиологически активными пептидами, и не содержащий альбумина стабилизатор, который содержит буфер, сахарный спирт, неионное поверхностно-активное вещество и изотонический агент. Жидкая композиция по настоящему изобретению характеризуется тем, что инсулин и инсулинотропный пептид вводят совместно.
Инсулин может быть представлен в жидкой композиции в форме фармацевтически эффективного количества длительно действующего конъюгата инсулина, где инсулин связан с Fc-областью иммуноглобулина. Инсулинотропный пептид может быть представлен в жидкой композиции в форме фармацевтически эффективного количества длительно действующего конъюгата инсулинотропного пептида, где инсулинотропный пептид связан с Fc-областью иммуноглобулина.
При использовании здесь «длительно действующий конъюгат инсулина» относится к конъюгату, где физиологически активный инсулин, включая производное, вариант, предшественник и фрагмент, связан с Fc-областью иммуноглобулина, и он может относиться к конъюгату с увеличенной продолжительностью сохранения физиологической активности in vivo по сравнению с нативным инсулином. При использовании здесь длительно действующий конъюгат инсулина относится к инсулину, связанному с Fc-областью иммуноглобулина через непептидильный линкер или пептидильный линкер. При использовании здесь «длительно действующий конъюгат инсулинотропного пептида» относится к конъюгату, где физиологически активный инсулинотропный пептид, включая производное, вариант, предшественник и фрагмент, связан с Fc-областью иммуноглобулина, и он может относиться к конъюгату с увеличенной продолжительностью сохранения физиологической активности in vivo по сравнению с нативным инсулинотропным пептидом.
При использовании здесь длительно действующий конъюгат инсулинотропного пептида относится к инсулинотропному пептиду, связанному с Fc-областью иммуноглобулина через непептидильный линкер или пептидный линкер.
При использовании здесь термин «длительно действующий» относится к увеличению продолжительности сохранения физиологической активности по сравнению с нативным пептидом. Термин «конъюгат» относится к форме пептида, где инсулин или инсулинотропный пептид связан с Fc-областью иммуноглобулина.
Длительно действующий конъюгат инсулина или конъюгат инсулинотропного пептида по настоящему изобретению имеет увеличенную продолжительность сохранения эффекта по сравнению с нативным инсулином или инсулинотропным пептидом. Тип длительно действующего конъюгата инсулина или конъюгата инсулинотропного пептида включает, без ограничения, форму инсулина или инсулинотропного пептида, полученную посредством модификации, замены, добавления или делеции аминокислот нативного инсулина или инсулинотропного пептида, конъюгат, где инсулин или инсулинотропный пептид связан с биоразлагаемым полимером, таким как ПЭГ (полиэтиленгликоль), конъюгат, где инсулин или инсулинотропный пептид связан с белком с большой продолжительностью сохранения, таким как альбумин или иммуноглобулин, конъюгат, где инсулин или инсулинотропный пептид связан с жирной кислотой, обладающей аффинностью связывания с альбумином в организме, или форму инсулина или инсулинотропного пептида, помещенную в биоразлагаемую наночастицу.
Длительно действующий конъюгат инсулина или инсулинотропного пептида, используемый в настоящем изобретении, получают посредством соединения синтезированного инсулина или инсулинотропного пептида с Fc-областью иммуноглобулина. Способ соединения этих двух компонентов может представлять собой поперечное связывание инсулина или инсулинотропного пептида и Fc-области иммуноглобулина через непептидильный полимер или получение слитого белка, в котором инсулин или инсулинотропный пептид и Fc-область иммуноглобулина соединены посредством генетической рекомбинации.
При использовании здесь «инсулин» относится к пептиду, секретируемому поджелудочной железой в ответ на повышенные уровни глюкозы в крови в организме для поглощения глюкозы в печени, мышцах или жировой ткани и ее превращения в гликоген и для прекращения использования жира в качестве источника энергии и, таким образом, функционирующему, контролируя уровень глюкозы в крови. Этот пептид включает нативный инсулин, базальный инсулин и их агонисты, предшественники, производные, фрагменты и варианты.
При использовании здесь «нативный инсулин» представляет собой гормон, секретируемый поджелудочной железой для стимуляции поглощения глюкозы и ингибирования распада жира в клетках и, таким образом, функционирующему, контролируя уровень глюкозы в крови. Инсулин образуется при процессинге его предшественника, проинсулина, не обладающего функцией регуляции уровня глюкозы в крови. Аминокислотные последовательности инсулина представляют собой следующее.
Альфа-цепь:
Gly-Ile-Val-Glu-Gln-Cys-Cys-Thr-Ser-Ile-Cys-Ser-Leu-Tyr-Gln-Leu-Glu-Asn-Tyr-Cys-Asn (SEQ ID NO: 1).
Бета-цепь:
Phe-Val-Asn-Gln-His-Leu-Cys-Gly-Ser-His-Leu-Val-Glu-Ala-Leu-Tyr-Leu-Val-Cys-Gly-Glu-Arg-Gly-Phe-Phe-Tyr-Thr-Pro-Lys-Thr (SEQ ID NO: 2).
При использовании здесь «базальный инсулин» относится к пептиду, регулирующему нормальные изменения уровня глюкозы в крови в течение каждого дня, и примеры такого пептида включают левемир, лантус и деглюдек. При использовании здесь «агонист инсулина» относится к соединению, связывающему собственный рецептор инсулина, демонстрируя такую же биологическую активность, как инсулин, независимо от структурного отличия от инсулина. При использовании здесь «вариант инсулина» относится к пептиду, имеющему одно или более чем одно отличие аминокислотной последовательности от нативного инсулина, обладающему функцией регуляции уровня глюкозы в крови в организме. Производное инсулина может быть получено посредством одного из замены, добавления, делеции и модификации некоторых аминокислот нативного инсулина или их комбинации. При использовании здесь «производное инсулина» относится к пептиду с по меньшей мере 80%-й гомологией аминокислотной последовательности нативному инсулину, где некоторые группы аминокислотных остатков могут быть химически замещены (например, альфа-метилирование, альфа-гидроксилирование), удалены (например, дезаминирование) или модифицированы (например, N-метилирование), обладающему функцией регуляции уровня глюкозы в крови в организме. При использовании здесь «фрагмент инсулина» относится к фрагменту, где одна или более чем одна аминокислота добавлена или удалена на N-конце или С-конце нативного инсулина, где могут быть добавлены аминокислоты, не встречающиеся в природе (например, аминокислота D-типа). Фрагмент инсулина обладает функцией регуляции уровня глюкозы в крови в организме.
Каждый из способов получения агонистов, производных, фрагментов и вариантов инсулина можно применять по отдельности или в комбинации. Например, объем настоящего изобретения включает пептид, где одна или более аминокислотных последовательностей отличаются от соответствующих последовательностей нативного пептида и N-концевой аминокислотный остаток дезаминирован, обладающий, в то же время, функцией регуляции уровня глюкозы в крови в организме.
Инсулин, используемый в настоящем изобретении, может быть получен посредством рекомбинантной технологии или синтезирован посредством твердофазного синтеза. Кроме того, инсулин, используемый в настоящем изобретении, может быть связан с непептидильным полимером. Такой непептидильный полимер может быть использован в настоящем изобретении в качестве линкера. Соединение инсулина с непептидильным полимером в качестве линкера позволяет улучшить стабильность инсулина, сохраняя в то же время его активность. Применение методики генетической рекомбинации позволяет использовать в качестве линкера пептид.
При использовании здесь «непептидильный полимер» относится к биологически совместимому полимеру, состоящему из одной или более повторяющихся единиц, связанных друг с другом ковалентной связью любого типа, но не пептидной связью. В настоящем изобретении «непептидильный полимер» может быть использован взаимозаменяемо с «непептидильным линкером».
Непептидный полимер, который может быть использован в настоящем изобретении, может быть выбран из группы, состоящей из биоразлагаемых полимеров, таких как полиэтиленгликоль, полипропиленгликоль, сополимеры этиленгликоля и пропиленгликоля, полиоксиэтилированные полиолы, поливиниловый спирт, полисахариды, декстран, поливинилэтиловый эфир, полимолочная кислота (PLA) и сополимер молочной и гликолевой кислот (PLGA); липидных полимеров; хитинов; гиалуроновой кислоты; и их комбинации. Предпочтительно в качестве непептидильного полимера используют полиэтиленгликоль. Объем настоящего изобретения также включает их производные, хорошо известные в данной области, и производные, которые могут быть легко получены с применением методик, доступных в данной области техники.
Пептидильный линкер, используемый в слитом белке, полученном обычной методикой внутрирамочного слияния, имеет ограничение, состоящее в том, что в организме он может легко расщепляться протеазой, и, таким образом, он не может в достаточной степени увеличить период полувыведения активного лекарственного средства из сыворотки, так, как при использовании носителя. Тем не менее в настоящем изобретении при использовании полимера, устойчивого к протеазе, можно поддерживать период полувыведения пептида из сыворотки, сходный с периодом полувыведения при использовании носителя. Поэтому непептидильный полимер, который можно использовать в настоящем изобретении, включает непептидильные полимеры любого типа, при условии, что они обладают указанной выше функцией, то есть устойчивы к протеазе. Молекулярная масса непептидильного полимера составляет от 1 до 100 кДа и предпочтительно от 1 до 20 кДа. Кроме того, непептидильный полимер по настоящему изобретению, связанный с Fc-областью иммуноглобулина, может представлять собой один тип полимеров или комбинацию разных типов полимеров.
Непептидильный полимер, используемый в настоящем изобретении, может иметь функциональную группу, которая может быть связана с Fc-областью иммуноглобулина и белковым лекарственным средством. Функциональные группы на обоих концах непептидильного полимера предпочтительно выбраны из группы, состоящей из реакционноспособной альдегидной группы, пропиональдегидной группы, бутиральдегидной группы, малеимидной группы и сукцинимидного производного. Сукцинимидное производное может представлять собой сукцинимидилпропионат, гидроксисукцинимидил, сукцинимидилкарбоксиметил или сукцинимидилкарбонат. В частности, когда непептидильный полимер имеет реакционноспособные альдегидные группы на обоих концах, это может минимизировать неспецифическое связывание и может делать эффективным связывание непептидильного полимера с физиологически активным полипептидом и иммуноглобулином на каждом конце. Конечный продукт, полученный посредством восстановительного алкилирования альдегидной связи, намного стабильнее продуктов, связанных амидной связью. Альдегидная функциональная группа селективно связывается с N-концом при низком pH и образует ковалентную связь с лизиновым остатком при высоком pH, например при pH 9,0.
Функциональные группы на двух концах непептидильного полимера могут быть одинаковыми или разными. Например, непептидильный полимер может иметь малеимидную группу на одном конце и альдегидную группу, пропиональдегидную группу или бутиральдегидную группу на другом конце. При использовании полиэтиленгликоля с гидроксигруппами на обоих концах в качестве непептидильного полимера гидроксигруппа может быть активирована с образованием различных функциональных групп известными химическими реакциями, или для получения длительно действующего конъюгата инсулина по настоящему изобретению может быть использован имеющийся в продаже полиэтиленгликоль с модифицированной функциональной группой.
Предпочтительно, непептидильный полимер может быть связан с N-концом бета-цепи инсулина.
Инсулин по настоящему изобретению может быть модифицирован с использованием непептидильного полимера.
При разработке длительно действующего конъюгата инсулина с использованием фрагмента иммуноглобулина, если физиологически активный полипептид модифицирован с использованием ПЭГ для увеличения продолжительности сохранения лекарственного средства без вызывания гипогликемии, это может снижать титр. Тем не менее снижение титра становится преимуществом длительно действующего конъюгата инсулина, и, таким образом, инсулин, модифицированный с использованием ПЭГ, может быть связан с Fc-областью иммуноглобулина через непептидильный полимер. Тип непептидильного полимера, который может быть использован при модифицировании инсулина, является таким же, как описано выше, и предпочтительно представляет собой полиэтиленгликоль (PEG, ПЭГ). В ПЭГ-модифицированном инсулине ПЭГ селективно связан с N-концом альфа-цепи инсулина или с определенным лизиновым остатком бета-цепи. ПЭГ, используемый для модифицирования инсулина, предпочтительно содержит на конце альдегидную группу или сукцинильную группу и более предпочтительно сукцинильную группу.
Способ получения и эффект длительно действующего конъюгата инсулина по настоящему изобретению раскрыты в публикациях корейских патентов №№10-2011-0134210, 10-2011-0134209 и 10-2011-0111267. Руководствуясь этими ссылками, специалисты в данной области могут получить длительно действующий конъюгат инсулина, используемый в настоящем изобретении. Кроме того, авторы настоящего изобретения ранее предложили способ получения длительно действующего конъюгата инсулина посредством моноПЭГилирования N-конца Fc-области иммуноглобулина и аналогичной модификации первого фенилаланина бета-цепи инсулина.
При использовании здесь «инсулинотропный пептид» относится к пептиду, обладающему функцией секреции инсулина, и он может стимулировать синтез или экспрессию инсулина в β-клетках поджелудочной железы. Инсулинотропный пептид предпочтительно представляет собой, без ограничения, глюкагоноподобный пептид-1 (GLP-1), GLP-2, эксендин-3 или эксендин-4. Инсулинотропный пептид включает нативный инсулинотропный пептид, а также его предшественники, агонисты, производные, фрагменты и варианты.
Производное инсулинотропного пептида по настоящему изобретению может относиться к производному, полученному посредством удаления N-концевой аминогруппы (или аминной группы) инсулинотропного пептида (то есть дезаминогистидильному производному); производному, полученному посредством замещения аминогруппы инсулинотропного пептида гидроксильной группой (то есть бета-гидроксиимидазопропионильному производному); производному, полученному посредством модификации аминогруппы инсулинотропного пептида двумя метильными группами (то есть диметилгистидильному производному); производному, полученному посредством замещения N-концевой аминогруппы инсулинотропного пептида карбоксильной группой (то есть бета-карбоксиимидазопропионильному производному); или производному, полученному посредством устранения положительного заряда аминогруппы инсулинотропного пептида удалением альфа-углерода N-концевого гистидинового остатка, оставляя только имидазоацетильную группу (имидазоацетильному производному). Кроме того, объем настоящего изобретения включает производные с другими формами модифицированной N-концевой аминогруппы.
В настоящем изобретении производное инсулинотропного пептида предпочтительно представляет собой производное, полученное посредством химической модификации N-концевой аминогруппы или аминокислотного остатка эксендина-4 и более предпочтительно производное эксендина-4, где альфа аминогруппа или альфа-углеродная группа при альфа-углероде гистидинового остатка, являющегося первым аминокислотным остатком на N-конце эксендина-4, замещена или удалена. Еще более предпочтительно производное инсулинотропного пептида представляет собой дезаминогистидилэксендин-4 (DA-эксендин-4), полученный посредством удаления N-концевой аминогруппы эксендина-4; бетагидроксиимидазопропионилэксендин-4 (HY-эксендин-4), полученный посредством замещения эксендина-4 гидроксильной группой или карбоксильной группой; бета-карбоксиимидазопропионилэксендин-4 (CX-эксендин-4); диметилгистидилэксендин-4 (DM-эксендин-4), полученный посредством модификации эксендина-4 двумя метильными группами; или имидазоацетилэксендин-4 (CA-эксендин-4), полученный посредством удаления альфа-углерода N-концевого гистидинового остатка.
GLP-1 представляет собой гормон, секретируемый тонкой кишкой и обычно функционирующий, стимулируя биосинтез и секрецию инсулина, подавляя секрецию глюкагона и стимулируя поглощение глюкозы клетками. В тонкой кишке предшественник глюкагона расщепляется на три пептида, представляющих собой глюкагон, GLP-1 и GLP-2. Здесь GLP-1 относится к GLP-1 (1-37), не обладающему функцией секреции инсулина, но активируемому при его процессинге с образованием формы GLP-1 (7-37). Аминокислотная последовательность GLP-1 (7-37) представляет собой следующее.
GLP-1 (7-37):
HAEGT FTSDV SSYLE GQAAK EFIAW LVKGR G (SEQ ID NO: 3).
При использовании здесь «производное GLP-1» относится к пептиду, последовательность которого по меньшей мере на 80% гомологична нативному GLP-1, и который может быть представлен в химически модифицированной форме, демонстрируя в то же время по меньшей мере такую же или улучшенную активность секреции инсулина. При использовании здесь «фрагмент GLP-1» относится к форме пептида, где одна или более чем одна аминокислота на N-конце или С-конце нативного GLP-1 добавлена или удалена, где добавленная аминокислота может представлять собой аминокислоту, не встречающуюся в природе (например, аминокислоту D-типа). При использовании здесь термин «длительно действующий конъюгат инсулинотропного пептида» относится к пептиду, имеющему увеличенную продолжительность сохранения эффектов по сравнению с нативным инсулинотропным пептидом. Длительно действующий конъюгат инсулинотропного пептида может быть представлен в форме, где аминокислота нативного инсулинотропного пептида модифицирована, заменена, добавлена или удалена; в форме конъюгата, где инсулин связан с биоразлагаемым полимером, таким как ПЭГ; в форме конъюгата, где инсулин связан с белком с большой продолжительностью сохранения, таким как альбумин, иммуноглобулин и их фрагменты; в форме конъюгата, где инсулинотропный пептид связан с жирной кислотой, обладающей аффинностью связывания с альбумином в организме, или в форме инсулинотропного пептида, помещенной в биоразлагаемые наночастицы; но тип длительно действующего конъюгата инсулинотропного пептида не ограничен настоящим изобретением.
При использовании здесь «вариант GLP-1» относится к пептиду, аминокислотные последовательности которого имеют одно или более чем одно отличие от нативного GLP-1, обладающему функцией секреции инсулина.
Эксендин-3 и эксендин-4 представляют собой инсулинотропные пептиды, состоящие из 39 аминокислот, последовательность которых на 53% гомологична GLP-1. Аминокислотные последовательности эксендина-3 и эксендина-4 представляют собой следующее.
Эксендин-3:
HSDGT FTSDL SKQME EEAVR LFIEW LKNGG PSSGA PPPS (SEQ ID NO: 4).
Эксендин-4:
HGEGT FTSDL SKQME EEAVR LFIEW LKNGG PSSGA PPPS (SEQ ID NO: 5).
Агонист эксендина относится к веществу, имеющему такую же биологическую активность, как эксендин, связываясь с рецептором эксендина in vivo, независимо от его структурного сходства с эксендином. Производное эксендина относится к пептиду с по меньшей мере 80%-й гомологией последовательности нативному эксендину, где некоторые группы аминокислотных остатков могут быть химически замещены (например, альфа-метилирование, альфа-гидроксилирование), удалены (например, дезаминирование) или модифицированы (например, N-метилирование), и такое производное эксендина обладает функцией секреции инсулина.
Фрагмент эксендина относится к форме пептида, где одна или более чем одна аминокислота добавлена или удалена на N-конце или С-конце нативного эксендина, где могут быть добавлены аминокислоты, не встречающиеся в природе (например, аминокислота D-типа), и такой фрагмент эксендина обладает функцией секреции инсулина.
Вариант эксендина представляет собой пептид, аминокислотные последовательности которого имеют одно или более чем одно отличие от нативного эксендина, обладающий функцией секреции инсулина. Вариант эксендина включает пептид, полученный посредством замены 12-й аминокислоты эксендина, лизина, серином или аргинином. Способы получения такого агониста, производного, фрагмента и варианта эксендина можно применять по отдельности или в комбинации. Например, инсулинотропный пептид включает инсулинотропный пептид, аминокислотные последовательности которого имеют одно или более чем одно отличие от нативного пептида, и N-концевой аминокислотный остаток которого дезаминирован. Нативный инсулинотропный пептид и модифицированный инсулинотропный пептид, используемые в настоящем изобретении, могут быть синтезированы посредством твердофазного синтеза. Кроме того, большинство нативных пептидов, включая нативный инсулинотропный пептид, могут быть получены рекомбинантным способом.
Длительно действующий конъюгат инсулинотропного пептида, используемый в настоящем изобретении, имеет форму инсулинотропного пептида, связанного с фрагментом имуноглоублина, таким как Fc иммуноглобулина, через непептидильный линкер или пептидильный линкер с применением методики генетической рекомбинации. Непептидильный линкер является таким же, как описано выше. Длительно действующий конъюгат инсулинотропного пептида получают с использованием фрагмента иммуноглобулина, как в случае с длительно действующим конъюгатом инсулина. Длительно действующий конъюгат инсулинотропного пептида поддерживает физиологическую активность существующего инсулинотропного пептида, такую как стимуляция синтеза и секреции инсулина, подавление аппетита, индуцирование уменьшения массы тела, повышение чувствительности бета-клеток к глюкозе в сыворотке, стимуляция пролиферации бета-клеток, задержка опорожнения желудка и подавление глюкагона, и он также имеет увеличенную продолжительность сохранения эффектов in vivo, благодаря увеличенному периоду полувыведения инсулинотропного пептида из сыворотки. Поэтому длительно действующий конъюгат инсулинотропного пептида эффективен в лечении диабета и ожирения.
Для получения длительно действующего конъюгата инсулинотропного пептида, использованного в настоящем изобретении, можно воспользоваться следующими ссылками: корейский патент, регистрационный №10-0725315, публикация корейского патента №10-2009-0008151 и корейский патент, регистрационный №10-1058290. Руководствуясь этими ссылками, специалисты в данной области могут получить длительно действующий конъюгат инсулинотропного пептида, используемый в настоящем изобретении.
Кроме того, авторы настоящего изобретения ранее разработали способ получения длительно действующего конъюгата эксендина-4 сначала присоединением ПЭГ к лизиновому (Lys) остатку имидазоацетилэксендина-4 (СА эксендина-4) и связыванием ПЭГ-модифицированного эксендина-4 с Fc иммуноглобулина.
Инсулин и инсулинотропный пептид, используемые в настоящем изобретении, связаны с носителем через непептидильный полимер, используемый в качестве линкера. Носитель, который может быть использован в настоящем изобретении, может быть выбран из группы, состоящей из Fc-области иммуноглобулина, альбумина, трансферрина и ПЭГ, и предпочтительно представляет собой Fc-область иммуноглобулина.
Длительно действующий конъюгат инсулина и длительно действующий конъюгат инсулинотропного пептида по настоящему изобретению имеют инсулин или инсулинотропный пептид, связанные с Fc-областью иммуноглобулина через непептидильный линкер, и обладают продолжительностью сохранения и стабильностью. В настоящем изобретении Fc иммуноглобулина может быть использована взаимозаменяемо с фрагментом иммуноглобулина.
Кроме того, поскольку Fc-область иммуноглобулина имеет относительно небольшую молекулярную массу по сравнению с полноразмерной молекулой иммуноглобулина, ее применение может быть полезным для получения и очистки конъюгата, а также для получения высокого выхода. Кроме того, Fc-область иммуноглобулина не содержит Fab-фрагмента, являющегося очень неоднородным из-за различий аминокислотных последовательностей в соответствии с подклассами антител, и, таким образом, можно ожидать, что Fc-область иммуноглобулина обладает большей однородностью и менее антигенна.
При использовании здесь «Fc-область иммуноглобулина» относится к белку, содержащему константную область 2 тяжелой цепи (СН2) и константную область 3 тяжелой цепи (СН3) иммуноглобулина, исключая вариабельные области тяжелой и легкой цепей, константную область 1 тяжелой цепи (СН1) и константную область 1 легкой цепи (CL1) иммуноглобулина. Она может дополнительно содержать шарнирную область при константной области тяжелой цепи. Кроме того, Fc-область иммуноглобулина по настоящему изобретению может содержать всю Fc-область или ее часть, включая константную область 1 тяжелой цепи (СН1) и/или константную область 1 легкой цепи (CL1), за исключением вариабельных областей тяжелой и легкой цепей, при условии, что она обладает физиологической