Способ изготовления биосенсорной структуры
Иллюстрации
Показать всеИзобретение относится к технологии изготовления сенсорных структур на основе твердотельного полупроводника и функционального органического покрытия и может быть использовано при создании ферментных биосенсоров на основе полевых транзисторов или структур «электролит-диэлектрик-полупроводник». Способ изготовления биосенсорной структуры включает модификацию полупроводникового электрохимического преобразователя для создания эффективного отрицательного электростатического заряда, а также послойную адсорбцию слоя поликатионных молекул полимера и слоя полианионных молекул фермента из их водного раствора. При этом используют пластину монокристаллического кремния с электронным типом проводимости, а его модификацию производят путем кипячения полупроводниковой пластины в перекисно-аммиачном растворе NH4OH/H2O2/H2O=1/1/4, а в процессе адсорбции молекул фермента, либо предварительно непосредственно перед процессом адсорбции, на поверхность структуры «n-Si/SiO2/полиэтиленимин» осуществляют освещение структуры со стороны раствора с интенсивностью, достаточной для изменения плотности заряда поверхности полупроводниковой структуры за время адсорбции. Техническим результатом изобретения является увеличение чувствительности к аналиту из-за увеличения количества молекул в монослое фермента на модифицированной поверхности полупроводникового преобразователя. 2 з.п. ф-лы, 4 ил., 3 табл.
Реферат
Область техники
Изобретение относится к технологии изготовления сенсорных структур на основе твердотельного полупроводника и функционального органического покрытия и может быть использовано при создании ферментных биосенсоров на основе полевых транзисторов или структур «электролит-диэлектрик-полупроводник», обеспечивая высокую чувствительность и избирательность биосенсора.
Уровень техники
Основными требованиями к сенсорным структурам, использующим в качестве чувствительного слоя молекулы фермента на поверхности электрохимического преобразователя, являются сохранение биокаталитической активности закрепленных молекул фермента и достижение как можно большего количества молекул фермента на единицу площади поверхности электрохимического преобразователя, что приводит к увеличению чувствительности к аналиту. Основными методами закрепления молекул фермента на поверхности твердой подложки являются физическая адсорбция из раствора, микрокапсулирование, включение и ковалентное связывание [Эггинс Б. Химические и биологические сенсоры. – М.: Техносфера, 2005. 336 с.]. При создании ферментативного слоя наиболее надежным и чаще используемым в лабораторных исследованиях является метод ковалентного связывания, но наиболее простым и используемым в крупномасштабных промышленных процессах является метод физической адсорбции. Кроме того, физическую адсорбцию обеспечивает широко распространенный метод послойной адсорбции, который обусловлен электростатическими взаимодействиями между слоями полиэлектролитов и подложкой и позволяет поочередно наносить слои противоположно заряженных полиэлектролитов из раствора на твердую подложку [Iler, R.K. Multilayers of colloidal particles // J. Colloid. Interf. Sci., 1966, 21, p. 569; Decher, G. Fuzzy nanoassemblies: toward layered polymeric multicomposites // Science, 1997, V. 277, P.1232–1237]. Так как молекулы фермента обладают эффективным зарядом в растворе, то с помощью подобной последовательной адсорбции можно создавать многослойные полиэлектролитные структуры, которые могут быть использованы в качестве чувствительных покрытий биосенсоров и при которых может быть достигнута значительная концентрация фермента на поверхности электрохимического преобразователя при многократном повторении циклов адсорбции. Очевидно, что необходимость многократного повторения циклов адсорбции для повышения количества закрепленных на поверхности подложки молекул фермента является недостатком.
Известен способ получения многослойных функциональных тонких пленок на твердом носителе (см. патент на изобретение US 6020175A, МПК C12N11/00). В этом патенте описаны мультислойные функциональные тонкие пленки, формируемые на твердотельных подложках, и метод их получения. Пленки на подложках содержат слои функциональных молекул, смешанные с полимерными ионами (полиэлектролитами), в комбинации с множественными слоями полиэлектролитов без функциональных молекул. Минимальное количество слоев в пленке равно двум. Способ получения таких пленок осуществляют следующим образом: твердотельную подложку, имеющую электрический заряд, погружают в раствор смеси функциональных молекул и примешанного полиэлектролита, имеющего электрический заряд, противоположный заряду твердотельной подложки, затем подложку с полученным первым слоем (состоящим из смеси функциональных молекул с полиэлектролитом) погружают в раствор полиэлектролита (без функциональных молекул), имеющего электрический заряд, противоположный заряду полиэлектролита в первом полученном слое. Так формируют второй слой - слой полиэлектролита без функциональных молекул. Процедуру получения двух указанных слоев можно повторять требуемое число раз. Также пленки могут быть получены путем погружения твердотельной подложки в раствор полиэлектролита, имеющего электрический заряд, противоположный заряду подложки, с последующим погружением подложки в раствор функциональных молекул и примешанного полиэлектролита, имеющих суммарный электрический заряд, противоположный заряду раствора полимера, и повторением, по крайней мере, один раз процедуры последовательного погружения подложки в растворы. В качестве функциональных молекул могут быть использованы белки, пигменты или красители. Данный способ позволяет избавиться от проблемы ассоциации молекул фермента, например глюкозооксидазы, в водном растворе, но также требует большого количества повторений циклов адсорбции.
Известен способ получения тонкопленочного материала, содержащего функциональные компоненты (см. патент РФ 2326898, МПК C08J5/18). Тонкопленочный материал, содержащий функциональные компоненты и молекулы полиэлектролитов, сформирован на поверхности подложки и выполнен в виде слоя или слоев полиионных комплексов функциональных компонентов, связанных со слоем или слоями полиэлектролитов, при этом количество функциональных компонентов в полиионном комплексе больше 1. Функциональными компонентами являются коллоидные частицы. Способ получения тонкопленочного материала включает проведение процедуры чередующейся послойной адсорбции на подложку компонентов из водной фазы. При этом в водной фазе предварительно формируют полиионные комплексы, включающие молекулы поликатионов или поликатиона, полианионов или полианиона и функциональные компоненты в количестве более 1, создавая стехиометрический избыток катионных или анионных групп полиэлектролитов и функциональных компонентов и обеспечивая отличие от нуля суммарного электростатического заряда катионных и анионных групп таких комплексов. Данный способ является экономически эффективнее предыдущего, т.к. за одно погружение подложки за счет адсорбции комплекса функциональных компонентов возможно нанести такое количество молекул фермента, которое в предыдущем способе достигается лишь при многократном повторении процедуры адсорбции. Но при применении этого способа в отношении ферментов преимущество метода может стать недостатком из-за необходимости формирования в растворе полиионных комплексов, что может привести к снижению биокаталитической активности фермента при закреплении на подложке в составе такого комплекса.
Известен способ изготовления ультратонкого полимерного покрытия, образованного противоположно заряженными полиэлектролитами (см. патент на изобретение РФ 2333231, МПК C09D201/02, B05D1/36). Способ изготовления такого покрытия включает нанесение полиэлектролитных слоев на твердую подложку произвольной формы за счет физической сорбции, главным образом, посредством электростатических взаимодействий, а также размещение одного или нескольких слоев полиэлектролитных капсул, содержащих фермент, между полиэлектролитными слоями. В результате достигается увеличение числа молекул на единицу площади подложки, а сами молекулы не контактируют с полиэлектролитной оболочкой, оставаясь в нативном состоянии. Таким образом, в указанном способе необходима дополнительная операция капсулирования фермента, а размещение капсул дополнительно между полиэлектролитными слоями затрудняет доступ субстрата к ферменту, находящемуся в слое, далеком от границы раздела полиионное покрытие – раствор аналита.
Таким образом, у всех указанных выше способов есть недостатки. Все известные способы подразумевают увеличение числа молекул фермента, необходимое для повышения чувствительности, только за счет увеличения числа слоев фермента в мультислойном покрытии, либо за счет процедуры капсулирования. Однако сам процесс капсулирования состоит из множества процедур, например, таких как центрифугирование и обработка в ультразвуковой ванне, которые приводят к изменениям свойств (например, конформации) молекул фермента. Многослойность и наличие буферных прослоек между слоями фермента приводит к высокому расходу фермента и сложным диффузионным механизмам переноса (доставки) субстрата к ферменту, а также к затруднению диффузии продуктов ферментативной реакции в раствор. Как следствие, применение вышеуказанных способов для создания ферментативных слоев с высокой чувствительностью к субстрату может оказаться неэффективным в случае использования сенсорной структуры «полупроводник — функциональное органическое покрытие», где для детектирования ферментативной реакции прибегают к методам регистрации электрохимического импеданса. Поэтому для увеличения числа закрепленных молекул фермента в сенсорных структурах «полупроводник — функциональное органическое покрытие» необходимо использование иных подходов.
Необходимо также отметить значимость интерфейсного (буферного) слоя, который может быть как слоем поликатионных молекул полимерного материала, так и слоем полианионных молекул. Дело в том, что в случае одинакового по знаку заряда подложки и молекул фермента адсорбция за счет электростатических взаимодействий невозможна, поэтому необходимы предварительная либо специальная химическая обработка, либо нанесение на поверхность подложки полимерного покрытия, эффективный заряд которого в растворе по знаку противоположен знаку заряда подложки. Второй способ предпочтительнее, так как позволяет изменить не только знак заряда подложки, но и изменить ее параметры, например механические свойства, морфологию и др. Например, шероховатость и толщина интерфейсного (буферного) слоя на поверхности планарной подложки (например, поверхности монокристаллического кремния) существенно влияют на адсорбцию молекул фермента. Оптимальным считается случай, когда после нанесения интерфейсного (буферного) слоя шероховатость поверхности меняется на 10-25 % по сравнению с поверхностью «чистого» кремния. Добиться такого результата можно путем изменения pH, ионной силы раствора, его солености и т.д.
Известен способ изготовления тонкопленочного органического покрытия (см. патент на изобретение РФ 2529216 C1, МПК C09D201/00) из катионного полиэлектролита, который включает модификацию подложки, приготовление водного раствора катионного полиэлектролита с адсорбцией полиэлектролита на подложку, промывку, сушку подложки с осажденным слоем. В качестве подложки используют монокристаллический кремний с шероховатостью, меньшей или сравнимой с толщиной получаемого покрытия. Для создания отрицательного электростатического заряда модифицируют подложку в растворе щелочи, перекиси водорода и воды при 75°С в течение 15 мин. Во время адсорбции осуществляют освещение подложки со стороны раствора светом с интенсивностью в диапазоне 2-8 мВт/см2 и с длинами волн из области собственного поглощения кремния. В результате, при помощи освещения подложки во время нанесения интерфейсного (буферного) слоя можно добиться требуемого изменения шероховатости поверхности, а также добиться равномерного распределения поверхностного потенциала. Техническим результатом этого способа является получение более однородного и менее шероховатого покрытия за счет изменения конформации полиионных соединений, обладающих достаточно высокой гибкостью полимерной цепи, состоящей из значительного количества звеньев (указанные в описании полиэлектролиты имели количество звеньев от 600 до 2150). При этом покрытие получается более плотным за счет «распрямления» полимернной молекулы на планарной твердотельной подложке. Описание способа не содержит информации о воздействии освещения на адсорбцию из раствора молекул фермента, имеющих строение, отличающееся от строения линейного, слаборазветвленного полимера, и не обладающих достаточной гибкостью.
Наиболее близким к предлагаемому изобретению является способ получения одно- или многослойных пленочных элементов путем послойной адсорбции, заключающийся в осаждении из раствора на заряженные подложки полиионных молекул, то есть полимерных молекул, обладающих эффективным зарядом в растворе (см. патент на изобретение US 5208111, МПК B32B7/04). Способ включает модификацию подложки таким образом, чтобы по всей площади поверхности подложки располагались отрицательно заряженные ионы или ионизируемые отрицательно заряженные соединения, приготовление водного раствора поликатионных молекул, адсорбцию поликатионных молекул на подложку, промывку в деионизованной воде и сушку подложки с осажденным слоем в потоке сухого воздуха. Заряд первого органического слоя противоположен заряду подложки. Для осаждения следующего слоя подложку помещают в раствор с молекулами, обладающими зарядом, противоположным заряду последнего осажденного слоя. Если одним или несколькими слоями в таких многослойных полиэлектролитных покрытиях являются размещенные между слоями полиэлектролитов молекулы фермента, имеющие соответствующий электрический заряд, то такие многослойные полиэлектролитные структуры могут быть использованы в качестве чувствительных покрытий биосенсоров.
Однако данный способ не учитывает специфику формирования эффективного заряда полупроводниковой подложки, рассматривая только заряд OH-групп на поверхности диоксида кремния после модификации кремниевой подложки, и тем более не учитываются факторы влияния на знак заряда поверхностных электронных состояний на границах раздела Si/SiO2 и SiO2/полиэлектролит. Также в этом способе предусмотрено увеличение количества адсорбированных молекул определенного сорта на единицу площади только за счет изменения количества нанесенных слоев, причем между слоями молекул фермента должен адсорбироваться монослой молекул, имеющих противоположный заряд.
Задача изобретения и технический результат
Задачей изобретения является разработка относительно простого способа повышения содержания молекул в монослое фермента, нанесенного из раствора на модифицированную поверхность полупроводникового электрохимического преобразователя, без увеличения концентрации молекул фермента в растворе и увеличения числа циклов адсорбции.
Техническим результатом изобретения является увеличение чувствительности к аналиту из-за увеличения количества молекул в монослое фермента на модифицированной поверхности полупроводникового преобразователя.
Сущность изобретения
Указанный технический результат достигается тем, что способ изготовления биосенсорной структуры включает модификацию подложки для создания эффективного отрицательного электростатического заряда, приготовление и адсорбцию из водного раствора слоя поликатионных молекул на подложку, приготовление и адсорбцию из водного раствора слоя полианионных молекул фермента, промывку в деионизованной воде и сушку подложки в потоке сухого воздуха после нанесения каждого слоя, согласно решению в качестве подложки используют монокристаллический кремний с электронным типом проводимости со слоем туннельно прозрачного для электронов диоксида кремния, для приготовления водного раствора поликатионных молекул используют полиэтиленимин, для приготовления водного раствора полианионных молекул фермента используют глюкозооксидазу, а во время адсорбции полианионных молекул фермента на подложку осуществляют освещение подложки со стороны раствора белым светом с интенсивностью, достаточной для установившегося во времени изменения плотности заряда поверхности структуры Si/SiO2/ПЭИ за время адсорбции молекул фермента.
Описание чертежей
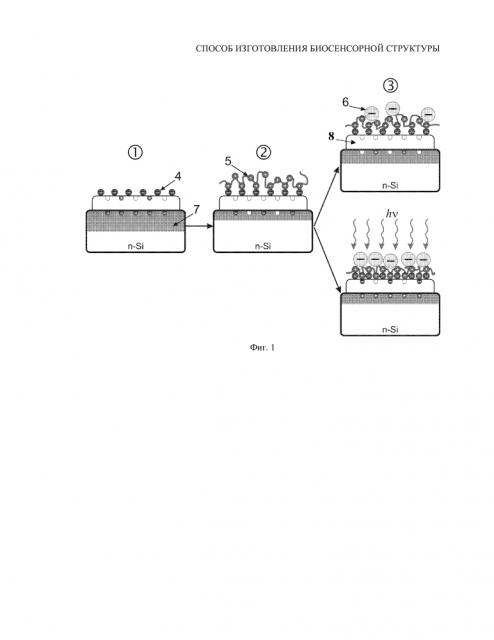
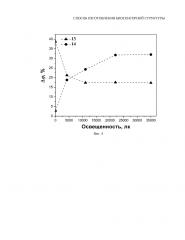
Заявляемое изобретение поясняется чертежами 1-4. На фиг. 1 показана схема, иллюстрирующая сущность заявляемого изобретения: 1 – этап предварительной подготовки поверхности кремния, 2 – этап нанесения слоя поликатионных молекул, 3 – этап нанесения молекул фермента способом-аналогом (вверху) и предлагаемым способом (внизу). При проведении этапов происходят процессы: активация отрицательно заряженных OH-групп на поверхности кремния (4) после проведения этапа 1; образование на поверхности положительного заряда за счет адсорбции молекул катионного полиэлектролита полиэтиленимина (ПЭИ) (5) после проведения этапа 2; частичная компенсация положительного заряда поверхности зарядом полианионных молекул фермента глюкозооксидазы (6). 7 – область пространственного заряда (ОПЗ), ширина которой меняется на этапах 1-3 в зависимости от процессов 4-6. 8 – туннельно тонкий слой SiO2. На фиг. 2-3 приведены по два изображения, полученных с помощью атомно-силовой микроскопии (АСМ), поверхностей n-Si (Фиг. 2) и p-Si (Фиг. 3) после нанесения слоя молекул глюкозооксидазы (GOx) в темноте (9, 11) и при освещении пластины кремния со стороны раствора белым светом (22000 лк) во время нанесения глюкозооксидазы (10, 12). На фиг. 4 показаны кривые изменения поверхностного потенциала после нанесения слоя GOx (Δφ=φПЭИ-φGOx) от уровня освещенности при освещении со стороны раствора пластины кремния с дырочным (13) и электронным (14) типом проводимости. Концентрации полиэтиленимина и глюкозооксидазы в растворе для получения образцов составляли соответственно 1-3 мг/мл и 0,5 мг/мл.
Подробное описание изобретения
Предлагаемый способ реализуется в три этапа следующим образом. Сначала проводят стадию предварительной подготовки поверхности монокристаллического кремния со слоем естественного окисла для удаления органических и неорганических загрязнений и создания однородного отрицательного заряда на поверхности благодаря активизации отрицательно заряженных ОН-групп на поверхности оксида. Предварительная подготовка кремниевых пластин включает перекисно-аммиачную обработку (кипячение при 75°С в течение 10-15 минут в растворе NH4OH/H2O2/H2O в объемном соотношении 1/1/4 соответственно). После кипячения в перекисно-аммиачном растворе подложки тщательно промываются в деионизованной воде с удельным сопротивлением 18 МΩ·см в течение 20 минут и сушатся в потоке сухого воздуха.
Следующим этапом является нанесение из водного раствора слоя поликатионных молекул на очищенную кремневую пластину, благодаря которому происходит закрепление молекул фермента методом послойной адсорбции. Для этого приготавливают водный раствор катионного полиэлектролита, например полиэтиленимина (ПЭИ) концентрацией 1-3 мг/мл. В приготовленный раствор погружают очищенную на предыдущем этапе пластину монокристаллического кремния на 10-15 минут. Этого времени достаточно для адсорбции одного сплошного монослоя полиэлектролитных молекул. Далее пластина кремния промывается в деионизованной воде в течение 10 минут для удаления тех молекул, которые адсорбировались на поверхности кремниевой пластины не из-за электростатического взаимодействия, и сушится в потоке сухого воздуха.
Следующим этапом является нанесение слоя полианионных молекул фермента, например глюкозооксидазы (GOx). Заявленный технический результат достигается за счет того, что на данном этапе полупроводниковую подложку, на которую предварительно нанесли слой поликатионных молекул, освещают монохромным или полихромным («белым») светом с длинами волн из области собственного поглощения полупроводника.
Дело в том, что при поглощении кванта света с энергией больше ширины запрещенной зоны в полупроводнике генерируются электронно-дырочные пары. При этом толщина приповерхностного слоя, в котором происходит максимальное поглощение энергии квантов, зависит как от длины волны (λ), так и от материала. Например, для кремния при воздействии монохромным излучением с длиной волны 700 нм глубина поглощения составляет 5,7 мкм, а для 400 нм – 0,11 мкм [Green, M.A. Short communication: Optical properties of intrinsic silicon at 300 K / M.A. Green, M.J. Keevers // Progress in photovoltaics: research and appl, 1995, Vol. 3, P. 189–192].
В случае отсутствия воздействия излучений и электрических полей полупроводник, как правило, в целом электронейтрален, поскольку заряд на поверхностных электронных состояниях (ПЭС) приводит к перераспределению свободных носителей заряда в приповерхностной области полупроводника, в результате чего у поверхности (границы) образуется область пространственного заряда (ОПЗ) [Шалимова, К.В. Физика полупроводников / К.В. Шалимова. - М.: Энергоатомиздат, 1985. - 392 с.]. В равновесных условиях заряд в ОПЗ равен по модулю и противоположен по знаку заряду ПЭС. Как правило, на поверхности полупроводника n-типа преобладают отрицательно заряженные ПЭС, и это приводит к обеднению приповерхностного слоя основными носителями заряда (электронами) и изгибу энергетических зон вверх на величину qφS, где q – заряд электрона по модулю, φS – поверхностный потенциал. Для полупроводников с дырочным типом проводимости преобладание донорных (положительно заряженных) ПЭС приводит к обеднению основными носителями заряда приповерхностного слоя и изгибу зон вниз.
Нанесение катионного полиэлектролита, например полиэтиленимина, приводит к появлению положительного поверхностного заряда на поверхности структуры. В результате чего у кремния с дырочным типом проводимости происходит увеличение изгиба зон, а у кремния с электронным типом проводимости изгиб зон уменьшается.
При погружении пластины n-Si/SiO2 с покрытием ПЭИ в водный раствор, содержащий, например, GOx, отрицательно заряженные молекулы GOx адсорбируются и удерживаются на поверхности слоя ПЭИ во многом благодаря электростатическому притяжению, обусловленному положительным зарядом ПЭИ. При адсорбции GOx на поверхности подложки образуется дополнительный отрицательный заряд. Поэтому для установления равновесия часть электронов с отрицательно заряженных ПЭС на границе раздела n-Si/SiO2 уходит в объем полупроводника, что, в свою очередь, уменьшает ОПЗ.
В случае освещения структуры n-Si/SiO2/ПЭИ происходит выпрямление энергетических зон за счет генерации электронно-дырочных пар и разделения их полем ОПЗ. Поле ОПЗ заставляет электроны двигаться от границы раздела n-Si/SiO2 в объем полупроводника, в результате чего заряд поверхностных электронных состояний на границе раздела n-Si/SiO2 уменьшается и может стать положительным или нейтральным. Это приводит к увеличению эффективного положительного заряда вблизи поверхности n-Si/SiO2/ПЭИ. Таким образом, при адсорбции GOx на освещаемую структуру эффективный положительный заряд, образуемый зарядами ПЭИ и ПЭС, больше, чем при темновом нанесении. Это приводит к увеличению количества адсорбированных молекул GOx по сравнению с темновой адсорбцией (фиг.1, 2). В соответствии с формулой Михаэлиса-Ментен увеличение количества адсорбированных молекул фермента приводит к увеличению скорости ферментативной реакции:
(1),
где ν – скорость ферментативной реакции, k и KM – константы, [E0] – концентрация фермента, [S] – концентрация субстрата.
Поскольку скорость ферментативной реакции - это мера каталитической активности фермента, то чувствительность биосенсора зависит от скорости ферментативной реакции, в частности от концентрации фермента на поверхности полупроводникового преобразователя.
Кроме того, если после выключения освещения неравновесные носители заряда рекомбинируют не сразу, а по истечении значительного промежутка времени (не менее часа), т.е. созданный при освещении эффективный поверхностный потенциал все это время не изменяется или изменяется незначительно, то можно говорить «об эффекте памяти» [Рывкин, С.М. Фотоэлектрические явления в полупроводниках. - М.: «Физматгиз», 1963, 496 с.]. Этот эффект возможен, если в процессе генерации носителей заряда при освещении неравновесные («световые») носители заряда не только разделяются внутренним электрическим полем ОПЗ, но и туннелируют через потенциальный барьер и разделяются пространственно плохо проводящим слоем (диэлектриком). В структуре Si/SiO2 такой барьер складывается из потенциального барьера на границе Si/SiO2, зависящего от заряда ПЭС, и туннельно тонкого слоя оксида кремния. Процесс туннелирования электронов через SiO2 активируется только в структуре Si/SiO2/ПЭИ, т.е. в присутствии на его поверхности положительно заряженного ПЭИ. Осаждение ПЭИ приводит к перераспределению зарядов на границах раздела Si/SiO2 и SiO2/ПЭИ и, соответственно, уменьшению потенциального барьера на границе Si/SiO2. Освещением генерируются электронно-дырочные пары, но при этом концентрация основных носителей заряда в приповерхностной области полупроводника увеличивается весьма незначительно по сравнению с темновой, а концентрация дырок (неосновных носителей заряда) возрастает на несколько порядков. Таким образом, если после нанесения ПЭИ структура Si/SiO2/ПЭИ приобретает поверхностный положительный потенциала за счет нескомпенсированного заряда ПЭИ, то при освещении потенциальный барьер понижается, что облегчает туннелирование электронов к ПЭИ и полностью компенсирует заряд ПЭИ. Если освещать структуру Si/SiO2/ПЭИ далее (при «нулевых электрических полях в структуре), то перезарядка ПЭС и ловушек в оксиде будет зависеть только от вероятности захвата электронов и дырок, а вероятность захвата возрастает с увеличением концентрации свободных носителей заряда. Освещение генерирует электроны и дырки парами, но при этом концентрация основных носителей заряда в приповерхностной области полупроводника увеличивается весьма незначительно по сравнению с темновой, а концентрация дырок (неосновных носителей заряда) возрастает на несколько порядков. Поэтому вероятность захвата дырок увеличивается на несколько порядков и все ПЭС и ловушки в оксиде могут захватить дырки и стать нейтральными (положительный заряд ловушек уже гораздо менее вероятен ввиду появления препятствующего этому электрическому полю).
Если не наносить следующий слой полиионного покрытия, то будем наблюдать «эффект памяти» после выключения света, так как вероятность туннелирования электронов с границы SiO2/ПЭИ обратно в n-Si весьма мала из-за достаточно большой концентрации электронов в объеме полупроводника (дырки в объеме полупроводника рекомбинировали после выключения света) и «нулевого» заряда ПЭС. То есть электрические поля в структуре Si/SiO2/ПЭИ скомпенсированы, а SiO2 пространственно разделяет заряды.
Если сразу после освещения Si/SiO2/ПЭИ начать адсорбцию глюкозооксидазы, то количество адсорбированных полианионных молекул будет больше за счет перезарядки ловушек и поверхностных электронных состояний (ПЭС), так как произойдет нейтрализация их отрицательного заряда при длительном освещении. Таким образом, используя в качестве подложки предварительно освещенные структуры с «эффектом памяти», можно ожидать увеличения количества адсорбированных на них молекул GOx по сравнению с темновой адсорбцией без предварительного освещения подложки.
В случае освещения структуры p-Si/SiO2/ПЭИ поле ОПЗ направлено в противоположную сторону полю, создаваемому неравновесными носителями заряда, что заставляет электроны двигаться к границе раздела p-Si/SiO2, и в итоге приводит к уменьшению эффективного положительного заряда структуры p-Si/SiO2/ПЭИ вблизи границы раздела ПЭИ- субстрат. Это приводит к уменьшению количества адсорбированных полианионных молекул фермента GOx по сравнению с темновой адсорбцией (фиг.3).
Исходя из вышесказанного, заявленный технический результат достигается только при использовании пластин монокристаллического кремния с электронным типом проводимости.
В качестве сведений, подтверждающих возможность осуществления заявленного способа с достижением указанного технического результата, приводим нижеследующие примеры осуществления предлагаемого изобретения.
Примеры осуществления изобретения
Пример 1
Использовались пластины монокристаллического кремния p-типа (100). Подложки обрабатывались в течение 10 минут в перекисно-аммиачном растворе со следующим соотношением компонент: 1 доля NH4OH, 1 доля H2O2, 4 доли H2O при 75° С. Толщина диоксида кремния после перекисно-аммиачной обработки составляет 2,0 нм. Для измерения толщин SiO2 использовался эллипсометр «Эллипс - 1000 АСГ» (Россия). Определяемые значения толщин SiO2 усреднялись не менее чем по 3 измерениям на различных участках каждого образца, при этом максимальный разброс значений был менее 1 Å. В качестве катионного полиэлектролита использовали полиэтиленимин (-C2H5N-)х с молекулярной массой 25 кДа. Полиэтиленимин растворялся в деионизованной воде до концентрации 1 мг/мл. Далее подложка погружалась в раствор полиэтиленимина. Время адсорбции - 10 минут. После адсорбции поликатионных молекул полиэтиленимина образцы промывались 20 минут в деионизованной воде с удельным сопротивлением 18 МΩ·см и сушились в потоке сухого воздуха. Для адсорбции полианионных молекул фермента структуру p-Si/SiO2/ПЭИ погружали в водный раствор фермента глюкозооксидазы (GOx) концентрацией 0,5 мг/мл. Время адсорбции - 10 минут. Всего было получено 5 образцов, которые отличались между собой режимом нанесения слоя GOx, нанесенным как в темноте, так и при варьировании величины освещенности (при 4200 лк, 11000 лк, 22000 лк, 35000 лк). После адсорбции образцы промывались 20 минут в деионизованной воде с удельным сопротивлением 18 МΩ·см и сушились в потоке сухого воздуха.
Для характеризации образцов измеряли морфологию поверхности и электрический поверхностный потенциал чистой поверхности p-Si, после нанесения слоя полиэтиленимина и после нанесения GOx. Электрический потенциал измерялся методом Кельвин-зондовой силовой микроскопии (КЗСМ) при помощи станции NTEGRA Spectra (г. Зеленоград, Россия). Использовался кантилевер HA_NC/Pt серии ETALON с платиновым покрытием. В полуконтактном режиме сканировались участки поверхности одинаковой площади и определялись средняя шероховатость, средний потенциал и их дисперсия. По АСМ сканам (Фиг.3) определялось среднее значение количества адсорбированных молекул GOx, исходя из известных параметров молекулы GOx, а также с учетом ограничений метода измерения [J. Aue´ and J. Th. M. De Hosson, Influence of atomic force microscope tip–sample interaction on the study of scaling behavior // Appl. Phys. Lett. 1997, Vol. 71(10), p. 1347–1349; A. Makky et al. Piezoelectric tuning fork probe for atomic force microscopy imaging and specific recognition force spectroscopy of an enzyme and its ligand // J. Mol. Recognit. 2013, 26, p. 521–531]. Было получено, что после нанесения молекул GOx на поверхность p-Si способом-аналогом поверхностная концентрация молекул составляет 45 шт./мкм2, а при нанесении предлагаемым способом - 4 шт./мкм2.
По сканам, полученным в режиме КЗСМ, определялись значения среднего поверхностного потенциала для каждого скана и относительные изменения среднего потенциала поверхности Δφ после нанесения слоя GOx на поверхность структуры p- Si/SiO2/ПЭИ при помощи следующей формулы:
(2),
где φПЭИ и φGOx - значения среднего поверхностного потенциала после нанесения слоя ПЭИ и слоя GOx соответственно.
Полученные значения Δφ для образцов с разными условиями нанесения GOx показаны на фиг. 4 (кривая 13).
Выводы о количестве и распределении по поверхности молекул GOx основаны на том, что в растворе каждая молекула GOx приобретает примерно одинаковый отрицательный заряд. Наличие отрицательного заряда приводит к уменьшению суммарного поверхностного потенциала на значение, пропорциональное количеству молекул фермента на отсканированном участке. Следовательно, большее количество адсорбированных молекул на участке той же площади приводит к большему значению Δφ.
Таким образом, из фиг. 4 следует, что с увеличением интенсивности освещения в процессе нанесения GOx в случае использования пластины p-Si происходит уменьшение Δφ, что свидетельствует об уменьшении количества адсорбированных молекул фермента. Следовательно, это при прочих равных условиях приведет к уменьшению чувствительности сенсорной структуры при проведении ферментативной реакции. Это предположение подтверждается при проведении ферментативной реакции окисления глюкозы, при котором детектировалось изменение силы тока, протекающего по поверхности полупроводниковой пластины (таблица 1).
Таблица 1. Изменение силы тока ΔI при проведении ферментативной реакции окисления глюкозы с использованием растворов глюкозы концентрацией 1-20 мМ в случае использования пластины p-Si
| Концентрация глюкозы, мМ | ΔI, μA | |
| Способ аналог | Предлагаемый способ (освещенность 22000 лк) | |
| 1 | 0,32 | 0,30 |
| 10 | 0,78 | 0,52 |
| 20 | 1,05 | 0,62 |
Таким образом, в случае использования пластины p-Si количество адсорбированных молекул фермента на поверхности полупроводникового преобразователя при освещении уменьшается, то есть при использовании в качестве электронного преобразователя p-Si технический результат не достигается.
Пример 2
Использовались пластины монокристаллического кремния n-типа (100). Предварительная обработка подложек, подготовка полиэлектролитных растворов, этапы адсорбции слоя поликатионных молекул и слоя полианионных молекул фермента, промывки и сушки совпадают с Примером 1. Также совпадает способ характеризации с помощью методов АСМ и КЗСМ. Было получено, что после нанесения молекул GOx на поверхность n-Si способом-аналогом поверхностная концентрация молекул составляет 60 шт./мкм2, а при нанесении предлагаемым способом - 253 шт./мкм2. Результаты измерений методом КЗСМ показаны на фиг. 4 (кривая 14).
Таким образом, из фиг. 4 следует, что с увеличением интенсивности освещения в процессе нанесения GOx в случае использования пластины n-Si происходит увеличение Δφ (начиная с освещенности 22000 лк Δφ не меняется), что свидетельствует об увеличении количества молекул фермента. Следовательно, это при прочих равных условиях должно привести к увеличению чувствительности сенсорной структуры при проведении ферментативной реакции. Это предположение подтверждается при проведении ферментативной реакции окисления глюкозы, при котором детектировалось изменение силы тока, протекающего по поверхности полупроводниковой пластины (таблица 2).
Таблица 2. Изменение силы тока ΔI при проведении ферментативной реакции окисления глюкозы с использованием растворов глюкозы концентрацией 1-20 мМ в случае использования пластины n-Si
| Концентрация глюкозы, мМ | ΔI, μA | |
| Способ аналог | Предлагаемый способ (освещенность 22000 лк) | |
| 1 | 9,10 | 11,06 |
| 10 | 26,74 | 38,12 |
| 20 | 52,22 | 75,41 |
Таким образом, в случае использования пластины n-Si количество молекул глюкозооксидазы, адсорбированных на поверхности полупроводникового преобразователя, увеличивается при освещении во время адсорбции более чем в 4 раза. При этом относительное изменение среднего потенциала поверхности Δφ после нанесения слоя GOx зависит от уровня освещенности во время адсорбции, но рост Δφ прекращается после достижения значений освещенности 22000 лк и более (см. фиг.4), что свидетельствует о достижении предельного заполнения молекулами фермента поверхности преобразователя при указанной освещенности. Увеличение ΔI при использовании предлагаемого способа для изготовления сенсорной структуры свидетельствует об увеличении чувствительности сенсора к аналиту (на 21 % при малых концентрациях (1 мМ) глюкозы в растворе и на 42-45 % при значительных концентрациях (10-20 мМ) глюкозы в растворе).
Пример 3
Использовались пластины монокристаллического кремния n-типа (100). Предварительная обработка подложек, подготовка полиэлектролитных растворов, этапы адсорбции слоя поликатионных молекул и слоя полианионных молекул фермента, промывки и сушки совпадают с Примером 1 за тем лишь исключением, что освещение кремниевой подложки светом проводят предварительно непосредственно перед процессом адсорбции слоя полианионных молекул фермента, но после этапа нанесения слоя поликатионных молекул. Освещение проводят с интенсивнос