Способ получения бензоксазепиновых соединений
Иллюстрации
Показать всеИзобретение относится к способам получения соединения формулы (I):
. Технический результат: разработан способ получения соединения GDC-0032, являющегося ингибитором PI3K, который может быть использован для получения соединения формулы I в промышленном масштабе, где осуществлен специальный выбор реакций, комбинация которых привела к снижению массы используемых реактивов при одновременном исключении вредных и опасных реактивов. 3 н. и 5 з.п. ф-лы, 37 пр.
Реферат
Перекрестная ссылка на родственные заявки
Данная заявка, не являющаяся предварительной, поданная согласно 37 Свода федеральных правил (CFR) §1.53(b), претендует на приоритет согласно 35 Свода законов США (USC) §119(e) в соответствии с предварительной заявкой на патент США №61/779619, поданной 13 марта 2013 года, содержание которой включено в настоящее описание полностью посредством ссылки на нее.
Область изобретения
Изобретение относится к способам получения ингибитора PI3K соединения GDC-0032.
Предшествующий уровень техники
Фосфоинозитид-3-киназы (PI3K от phosphoinositide 3-kinases) представляют собой липидкиназы, которые фосфорилируют липиды по 3-гидроксильному остатку инозитольного кольца (Whitman et al (1988) Nature, 332: 664). 3-Фосфорилированные фосфолипиды (PIP3s от 3-phosphorylated phospholipids), синтезированные PI3-киназами, действуют в качестве вторичных мессенджеров, вовлекающих киназы с липид-связывающими доменами (включая плекстрин-гомологичные (РН от plekstrin homology) области), такие как Akt и фосфоинозитид-зависимая киназа-1 (PDK1 от phosphoinositide-dependent kinase-1). Связывание Akt с мембранными PIP3s вызывает транслокацию Akt к клеточной мембране, приводя в контакт Akt с PDK1, который ответственен за активацию Akt. Опухоль-супрессорная фосфатаза, PTEN, дефосфорилирует PIP3 и поэтому действует в качестве отрицательного регулятора активации Akt. PI3-киназы Akt и PDK1 имеют большое значение в регуляции многих клеточных процессов, включая регуляцию клеточного цикла, пролиферацию, продолжительность существования, апоптоз и подвижность, и являются важными компонентами молекулярных механизмов заболеваний, таких как рак, диабет и иммунное воспаление (Vivanco et al (2002) Nature Rev. Cancer 2: 489; Phillips et al (1998) Cancer 83: 41).
Основной изоформой PI3-киназы при раке является PI3-киназа класса I, p110 α (альфа) (US 5824492; US 5846824; US 6274327). Другие изоформы участвуют в сердечно-сосудистых и иммуновоспалительных заболеваниях (Workman Р (2004) Biochem Soc Trans 32: 393-396; Patel et al (2004) Proceedings of the American Association of Cancer Research (Abstract LB-247) 95th Annual Meeting, March 27-31, Orlando, Florida, USA; Ahmadi K and Waterfield MD (2004) Encyclopedia of Biological Chemistry (Lennarz W J, Lane M D eds) Elsevier/Academic Press). Путь PI3 киназа/Akt/PTEN является привлекательной мишенью для разработки противораковых лекарственных средств, поскольку ожидается, что такие модулирующие или ингибирующие агенты будут ингибировать пролиферацию, изменять подавление апоптоза и преодолевать сопротивляемость к цитотоксическим средствам в раковых клетках (Folkes et al (2008) J. Med. Chem. 51: 5522-5532; Yaguchi et al (2006) Jour, of the Nat. Cancer Inst. 98(8): 545-556). Сигнальный путь PI3K-PTEN-AKT дерегулируется при большом числе раковых заболеваний (Samuels Y, Wang Z, Bardellil A et al. High frequency of mutations of the PIK3CA gene in human cancers. (2004) Science; 304 (5670): 554; Carpten J, Faber AL, Horn C. "A transforming mutation in the pleckstrin homology domain of AKT1 in cancer" (2007) Nature; 448: 439-444).
GDC-0032, также известный как 2-(4-(2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-9-ил)-1H-пиразол-1-ил)-2-метилпропанамид, оказывает сильное действие на PI3K (WO 2011/036280; US 8242104) и исследуется на пациентах с местно-распространенными или метастатическими солидными опухолями.
Сущность изобретения
Изобретение относится к способам получения PI3K ингибитора I (GDC-0032), называемого 2-(4-(2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-9-ил)-1H-пиразол-1-ил)-2-метилпропанамид, имеющего структуру:
и его стереоизомеров, геометрических изомеров, таутомеров и фармацевтически приемлемых солей.
Другой аспект изобретения включает новые промежуточные соединения, полезные для получения GDC-0032 и имеющие структуры:
и
Определения
Термин "хиральный" относится к молекулам, которые обладают свойством неналожения зеркального изображения партнера, тогда как термин "ахиральный" относится к молекулам, которые являются налагающимися на зеркальное изображение их партнера.
Термин "стереоизомер" относится к соединениям, которые имеют одинаковый химический состав, но отличаются расположением атомов или групп в пространстве.
"Диастереомер" относится к стереоизомеру с двумя или более центрами хиральности, и чьи молекулы не являются зеркальными изображениями друг друга. Диастереомеры имеют разные физические свойства, например, температуры плавления, температуры кипения, спектральные свойства и реакционные способности. Смеси диастереомеров можно разделить в ходе аналитических методик с высоким разрешением, таких как электрофорез и хроматография.
"Энантиомеры" относятся к двум стереоизомерам соединения, которые являются неналагающимися зеркальными изображениями друг друга.
Стереохимические определения и обозначения, используемые в данном документе, как правило применяют согласно S.P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; и Eliel, E. and Wilen, S., "Stereochemistry of Organic Compounds", John Wiley & Sons, Inc., New York, 1994. Соединения по изобретению могут содержать центры асимметрии или хиральные центры, и, следовательно, существуют в разных стереоизомерных формах. Предполагается, что все стереоизомерные формы соединений по изобретению, включая, но не ограничиваясь этим, диастереомеры, энантиомеры и атропоизомеры, а также их смеси, такие как рацемические смеси, являются частью настоящего изобретения. Многие органические соединения существуют в оптически активных формах, т.е. они обладают способностью вращать плоскость плоскополяризованного света. При описании оптически активного соединения приставки D и L, или R и S, используют для обозначения абсолютной конфигурации молекулы относительно ее хирального центра(ов). Приставки d и I или (+) и (-) используют для обозначения знака направления вращения плоскополяризованного света соединением, так (-) или I означает, что соединение является левовращающим. Соединение с приставкой (+) или d является правовращающим. Для приведенной химической структуры эти стереоизомеры являются одинаковыми за исключением того, что они представляют собой зеркальные изображения друг друга. Также конкретный стереоизомер может называться энантиомером, и смесь таких изомеров часто называется энантиомерной смесью. Смесь 50:50 энантиомеров называется рацемической смесью или рацемат, которая может встречаться, когда отсутствует стереоселективность или стереоспецифичность в химической реакции или способе. Термины "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомерных соединений без оптической активности.
Термин "таутомер" или "таутомерная форма" относится к структурным изомерам разных энергий, которые являются взаимопревращаемыми при переходе через низкоэнергетический барьер. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения в ходе перемещения протона, такие как кето-енольные и имин-енаминовые изомеризации. Валентные таутомеры включают взаимопревращения в ходе перегруппировки некоторых из связывающих электронов.
Фраза "фармацевтически приемлемая соль", как используется в данном документе, относится к фармацевтически приемлемым органическим или неорганическим солям соединения по изобретению. Примерные соли включают, но не ограничиваются этим, сульфат, цитрат, ацетат, оксалат, хлорид, бромид, иодид, нитрат, бисульфат, фосфат, кислый фосфат, изоникотинат, лактат, салицилат, кислый цитрат, тартрат, олеат, таннат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат "мезилат", этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Фармацевтически приемлемая соль может содержать включение другой молекулы, такой как ион ацетата, ион сукцината или другой противоион. Противоион может представлять собой органическую или неорганическую группировку, которая стабилизирует заряд в исходном соединении. Кроме того, фармацевтически приемлемая соль может иметь более чем один заряженный атом в своей структуре. В тех случаях, когда многочисленные заряженные атомы являются частью фармацевтически приемлемой соли, они могут содержать многочисленные противоионы. Следовательно, фармацевтически приемлемая соль может иметь один или более заряженных атомов и/или один или более чем один противоион.
Если соединение по изобретению представляет собой основание, то требуемую фармацевтически приемлемую соль можно получить любым подходящим способом, применимым в данной области техники, например, обработкой свободного основания неорганической кислотой, такой как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, метансульфоновая кислота, фосфорная кислота и подобные, или органической кислотой, такой как уксусная кислота, малеиновая кислота, янтарная кислота, миндальная кислота, фумаровая кислота, малоновая кислота, пировиноградная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота, пиранозидильная кислота, такая как глюкуроновая кислота или галактуроновая кислота, альфа-гидроксикислота, такая как лимонная кислота или винная кислота, аминокислота, такая как аспарагиновая кислота или глутаминовая кислота, ароматическая кислота, такая как бензойная кислота или коричная кислота, сульфоновая кислота, такая как п-толуолсульфоновая кислота или этансульфоновая кислота, или подобные.
Если соединение по изобретению представляет собой кислоту, то требуемую фармацевтически приемлемую соль можно получить любым подходящим способом, например, обработкой свободной кислоты неорганическим или органическим основанием, таким как амин (первичный, вторичный или третичный), гидроксид щелочного металла или гидроксид щелочноземельного металла, или подобные. Иллюстративные примеры подходящих солей включают, но не ограничиваются этим, органические соли, полученные из аминокислот, таких как глицин и аргинин, аммиака, первичных, вторичных и третичных аминов и циклических аминов, таких как пиперидин, морфолин и пиперазин, и неорганические соли, полученные из натрия, кальция, калия, магния, марганца, железа, меди, цинка, алюминия и лития.
"Сольват" относится к ассоциации или комплексу одной или более молекул растворителя и соединения по изобретению. Примеры растворителей, которые образуют сольваты, включают, но не ограничиваются этим, воду, изопропанол, этанол, метанол, ДМСО, этилацетат, уксусную кислоту и этаноламин. Термин "гидрат" относится к комплексу, где молекулой растворителя является вода.
Фраза "фармацевтически приемлемая соль", как используется в данном документе, относится к фармацевтически приемлемым органическим или неорганическим солям соединения по изобретению. Примерные соли включают, но не ограничиваются этим, сульфат, цитрат, ацетат, оксалат, хлорид, бромид, иодид, нитрат, бисульфат, фосфат, кислый фосфат, изоникотинат, лактат, салицилат, кислый цитрат, тартрат, олеат, таннат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат "мезилат", этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Фармацевтически приемлемая соль может содержать включение другой молекулы, такой как ион ацетата, ион сукцината или другой противоион. Противоион может представлять собой органическую или неорганическую группировку, которая стабилизирует заряд в исходном соединении. Кроме того, фармацевтически приемлемая соль может иметь более чем один заряженный атом в своей структуре. В тех случаях, когда многочисленные заряженные атомы являются частью фармацевтически приемлемой соли, они могут содержать многочисленные противоионы. Следовательно, фармацевтически приемлемая соль может иметь один или более заряженных атомов и/или один или более чем один противоион.
Получение GDC-0032
Настоящее изобретение включает процессы, способы, реактивы и промежуточные соединения для синтеза GDC-0032, формулы I, низкомолекулярного ингибитора PI3K и mTOR, (Roche RG7604, CAS рег. №1282512-48-4), который имеет структуру:
и может быть назван: 2-(4-(2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-9-ил)-1H-пиразол-1-ил)-2-метилпропанамид (US 8242104; WO 2011/036280, которые явным образом включены посредством ссылки). Как используется в данном документе, GDC-0032 включает все стереоизомеры, геометрические изомеры, таутомеры и фармацевтически приемлемые соли.
Соединения по изобретению могут содержать центры асимметрии или хиральные центры, и, следовательно, существуют в разных стереоизомерных формах. Предполагается, что все стереоизомерные формы соединений по изобретению, включая, но не ограничиваясь этим, диастереомеры, энантиомеры и атропоизомеры, а также их смеси, такие как рацемические смеси, являются частью настоящего изобретения. Кроме того, настоящее изобретение охватывает все геометрические и позиционные изомеры. В структурах, показанных в данном документе, где стереохимия конкретного хирального атома не определена, все стереоизомеры предусмотрены и включены в качестве соединений по изобретению. Когда стереохимия обозначена цельным клином или пунктирной линией, изображающей конкретную конфигурацию, тогда этот стереоизомер таким образом установлен и определен.
Соединения по изобретению могут существовать в несольватированных, а также сольватированных формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и подобные, и предполагается, что изобретение охватывает как сольватированные, так и несольватированные формы.
Соединения по изобретению могут также существовать в разных таутомерных формах, и все такие формы находятся в объеме данного изобретения. Термин "таутомер" или "таутомерная форма" относится к структурным изомерам разных энергий, которые являются взаимопревращаемыми при переходе через низкоэнергетический барьер. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения в ходе перемещения протона, такие как кето-енольные и имин-енаминовые изомеризации. Валентные таутомеры включают взаимопревращения в ходе перегруппировки некоторых из связывающих электронов.
Соединения по изобретению также включают изотопно-меченые соединения, которые являются такими же как те, что перечислены в данном документе, за исключением того факта, что один или более атомов заменены атомом, имеющим атомную массу или массовое число, отличающееся от атомной массы или массового числа, обычно находящегося в природе. Все изотопы конкретного атома или элемента, как указано, находятся в объеме соединений по изобретению, и их использования. Примерные изотопы, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, хлора и йода, такие как 2H, 3H, 11C, 13C, 14С, 13N, 15N, 15O, 17O, 18O, 32P, 33P, 35S, 18F, 36Cl, 123I и 125I. Конкретные изотопно-меченые соединения по настоящему изобретению (например, меченные 3Н и 14С) полезны в анализах распределения в тканях соединения и/или субстрата. Меченные тритием (3Н) и углеродом-14 (14С) изотопы полезны из-за легкости их получения и обнаружения. Кроме того, замещение тяжелыми изотопами, такими как дейтерий (т.е. 2Н), может давать определенные терапевтические преимущества, возникающие вследствие большей метаболической устойчивости (например, увеличенный in vivo период полураспада или уменьшенные требования к дозировке) и, следовательно, может быть предпочтительно при некоторых обстоятельствах. Позитронно-активные изотопы, такие как 15O, 13N, 11С и 18F, полезны для изучений позитронно-эмиссионной томографии (ПЭТ), чтобы проверить степень занятости рецептора субстратом. Изотопно-меченые соединения по настоящему изобретению как правило можно получить, соблюдая способы, аналогичные тем, что раскрыты в разделе примеры, приведенном ниже в данном документе, замещая изотопно-меченым реагентом неизотопно-меченый реагент.
Исходные вещества и реактивы для получения GDC-0032 как правило есть в наличии у поставщиков, таких как Sigma-Aldrich Chemical (Milwaukee, WI), или их легко получают, используя способы, хорошо известные квалифицированным специалистам в данной области техники (например получают способами, в общем описанными у Louis F. Fieser and Mary Fieser, Reagents for Organic Synthesis, v. 1-19, Wiley, N.Y. (1967-1999 ed.), или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая приложения (также доступные через электронную базу данных Бейльштейн).
Следующие схемы 1-15 иллюстрируют химические реакции, способы, методику синтеза GDC-0032, формулы I, и конкретные промежуточные соединения и реактивы.
Схема 1:
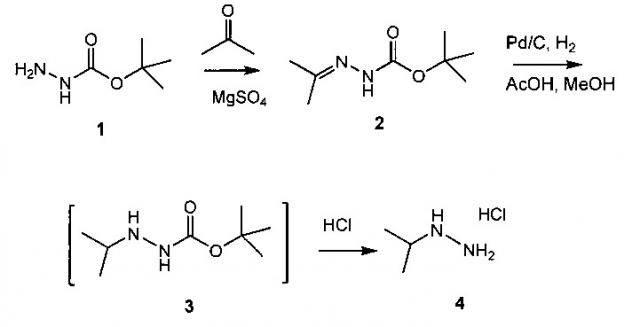
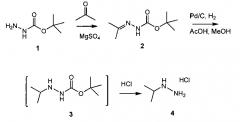
Схема 1 демонстрирует синтез промежуточного изопропилгидразина гидрохлорида 4 из Boc-гидразина 1. Конденсация 1 с ацетоном и сульфатом магния давала Boc-гидразон, трет-бутил 2-(пропан-2-илиден)гидразинкарбоксилат 2 (пример 1). Катализируемое палладием гидрирование 2 в уксусной кислоте и метаноле давало Boc-изопропил-гидразин 3 (пример 2), который обрабатывали в реакционной смеси газообразным хлороводородом, получая 4 (пример 3).
Альтернативно, двойную связь в 2 можно восстановить гидридным реагентом, таким как цианоборгидрид натрия (пример 2).
Схема 2:
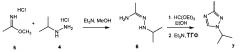
Схема 2 демонстрирует синтез 1-изопропил-3-метил-1Н-1,2,4-триазола 7 из метилацетимидата гидрохлорида 5 и изопропилгидразина гидрохлорида 4. Реакция 5 и 4 в триэтиламине и метаноле с последующей циклизацией продукта конденсации, N'-изопропилацетогидразонамида 6 (пример 4), с триэтилортоформиатом (триэтоксиметаном) давала 7 (пример 5). Альтернативно, 4 и ацетамидин можно подвергнуть взаимодействию с получением 6.
Или 4 можно подвергнуть взаимодействию с ацетонитрилом и кислотой с образованием соответствующей соли 6.
Схема 3:
Схема 3 демонстрирует синтез промежуточного соединения, 2-хлор-N-метокси-N-метилацетамида 10. Реакция 2-хлорацетилхлорида 8 и N,O-диметилгидроксиламина гидрохлорида 9 в водном карбонате калия и метил-трет-бутиловом эфире (МТБЭ) давала 10 (пример 6).
Схема 4:
Схема 4 демонстрирует синтез промежуточного 4-бром-2-фторбензимидамида гидрохлорида 12, образующегося в ходе реакции 4-бром-2-фторбензонитрила 11 с гексаметилдисилазидом лития (LiHMDS) в тетрагидрофуране (пример 7). Альтернативно, 11 обрабатывают хлороводородом в спирте, таком как этанол, с образованием имидата, этил 4-бром-2-фторбензимидата гидрохлорида, затем аммиаком в спирте, таком как этанол, с образованием 12 (пример 7).
Схема 5:
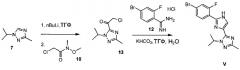
Схема 5 демонстрирует синтез 5-(2-(4-бром-2-фторфенил)-1Н-имидазол-4-ил)-1-изопропил-3-метил-1Н-1,2,4-триазола V из 1-изопропил-3-метил-1Н-1,2,4-триазола 7. Депротонирование 7 с н-бутиллитием и ацилирование с 2-хлор-N-метокси-N-метилацетамидом 10 давало промежуточный 2-хлор-1-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)этанон 13 (пример 8). В ходе циклизации 13 с 4-бром-2-фторбензимидамида гидрохлоридом 12 и гидрокарбонатом калия в воде и ТГФ (тетрагидрофуране) образовывался имидазол V (пример 9).
Схема 6:
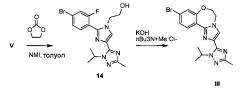
Схема 6 демонстрирует синтез 9-бром-2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепина III из V. Алкилирование имидазольного азота V 2-гидроксиэтилирующим реагентом, таким как 1,3-диоксолан-2-он, давало 2-(2-(4-бром-2-фторфенил)-4-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-1Н-имидазол-1-ил)этанол 14 (пример 10). Циклизация 14 с водным основным реагентом, таким как метилтрибутиламмония хлорид, в водном гидроксиде калия, давало III, который может кристаллизоваться из этанола и воды (пример 11).
Схема 7:
Схема 7 демонстрирует синтез этил 2-(4-бром-1H-пиразол-1-ил)-2-метилпропионата IV, исходя из 2-бром-2-метилпропионовой кислоты 15. Алкилирование пиразола с 15 давало 2-метил-2-(1H-пиразол-1-ил)пропионовую кислоту 16 (пример 12). Этерификация 16 с серной кислотой в этаноле давала этил 2-метил-2-(1H-пиразол-1-ил)пропионат 17 (пример 13). Региоспецифическое бромирование 17 с N-бромсукцинимидом (NBS) давало IV (пример 14). Альтернативно, 16 обрабатывали в реакционной смеси бромирующим реагентом, таким как 1,3-дибром-5,5-диметилгидантоин (ДБДМГ), получая 2-(4-бром-1Н-пиразол-1-ил)-2-метилпропионовую кислоту, которую этерифицировали, получая IV, где R представляет собой этил. Также можно получить другие эфиры, такие как метиловый, изопропиловый, или любой алкиловый, бензиловый или ариловый эфир.
Схема 8:
г
Схема 8 демонстрирует альтернативный синтез этил 2-(4-бром-1Н-пиразол-1-ил)-2-метилпропионата IV, исходя из этил 2-бром-2-метилпропионата 18. Алкилирование пиразола с 18 в присутствии основания, такого как трет-бутилат натрия или карбонат цезия, давало смесь этил 2-метил-2-(1H-пиразол-1-ил)пропионата 17 и этил 2-метил-3-(1H-пиразол-1-ил)пропионата 19. Бромирование смеси 1,3-дибром-5,5-диметилимидазолидин-2,4-дионом (ДБДМГ) давало смесь, содержащую IV, этил 3-(4-бром-1H-пиразол-1-ил)-2-метилпропионат 20 и 4-бром-1Н-пиразол 21, которую обрабатывали сильным основанием в безводных условиях, таких как гексаметилдисилазид лития в тетрагидрофуране. Подкисление хлористоводородной кислотой давало IV.
Схема 9:
Схема 9 демонстрирует синтез 2-(4-(2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-9-ил)-1H-пиразол-1-ил)-2-метилпропанамида, GDC-0032, I из этил 2-(4-бром-1H-пиразол-1-ил)-2-метилпропионата IV (регистрационный номер CAS: 1040377-17-0, WO 2008/088881) и 9-бром-2-(1-изопропил-3-метил-1H-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепина III (регистрационный номер CAS: 1282514-63-9, US 2012/0245144, US 8242104). Также кроме этилового можно использовать другие эфиры, которые могут гидролизоваться с водным основанием, такие как метиловый, изопропиловый, или любой алкиловый, бензиловый или ариловый эфир. При однореакторном борилировании Мияура / Сузуки, система Бухвальда, этил 2-(4-бром-1H-пиразол-1-ил)-2-метилпропионат IV подвергают взаимодействию с 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксаборолан), CAS рег. №73183-34-3, также называемым B2PiN2, и палладиевым катализатором, таким как XPhos (2-дициклогексилфосфино-2',4',6'-триизопропилбифенил, CAS рег. №564483-18-7), с солью, такой как ацетат калия, в растворителе, таком как этанол, приблизительно при 75°C с образованием промежуточного этил 2-метил-2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразол-1-ил)пропионата 22 (пример 15, регистрационный номер CAS: 1201657-32-0, US 8242104, US 8263633, WO 2009/150240).
Промежуточное соединение 22 может быть выделено или подвергнуто взаимодействию в реакционной смеси (один реактор) с III с образованием 23.
Целый ряд низковалентных Pd(II) и Pd(0) палладиевых катализаторов можно использовать на стадии сочетания Сузуки с образованием 23 (пример 16) из 22 и III, включая PdCl2(PPh3)2, Pd(t-Bu)3, PdCl2 dppf CH2Cl2, Pd(PPh3)4, Pd(OAc)/PPh3, Cl2Pd[(Pet3)]2, Pd(DIPHOS)2, Cl2Pd(Bipy), [PdCl(Ph2PCH2PPh2)]2, Cl2Pd[P(o-толил)3]2, Pd2(dba)3/P(o-толил)3, Pd2(dba)/P(фурил)3, Cl2Pd(фурил)3]2, Cl2Pd(PMePh2)2, Cl2Pd[P(4-F-Ph)3]2, Cl2Pd[P(C6F6)3]2, Cl2Pd[P(2-COOH-Ph)(Ph)2]2, Cl2Pd[P(4-COOH-Ph)(Ph)2]2, и инкапсулированные катализаторы Pd EnCat™ 30, Pd EnCat™ TPP30 и Pd(II)EnCat™ BINAP30 (US 2004/0254066).
Эфирную группу 23 омыляют водным основным реагентом, таким как гидроксид лития, получая 2-(4-(2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-9-ил)-1H-пиразол-1-ил)-2-метилпропионовую кислоту II (пример 17). Промежуточное соединение 23 можно выделить или дополнительно подвергнуть взаимодействию в реакционной смеси с водным основным реагентом с образованием II. Карбоксильную группу II активируют с ацил-активирующим реагентом, таким как ди(1Н-имидазол-1-ил)метанон (карбонилдиимидазол, CDI) или N,N,N',N'-тетраметил-O-(7-азабензотриазол-1-ил)урония гексафторфосфат (HATU), и затем подвергают взаимодействию со спиртовым раствором аммиака, таким как аммиак, растворенный в метаноле, этаноле или изопропаноле, водным гидроксидом аммония, водным хлоридом аммония или аммиаком, растворенным в ТГФ, получая I (пример 18).
Целый ряд твердых адсорбирующих акцепторов палладия можно использовать, чтобы удалить палладий после стадии сочетания Сузуки с образованием соединения I. Примерные воплощения акцепторов палладия включают FLORISIL®, SILIABOND®Thiol и SILIABOND® Thiourea. Другие акцепторы палладия включают силикагель, стекло с контролируемым размером пор (TosoHaas) и дериватизированный слабосшитый полистирол QUADRAPURE™ АЕА, QUADRAPURE™ IMDAZ, QUADRAPURE™ МРА, QUADRAPURE™ TU (Reaxa Ltd., Sigma-Aldrich Chemical Co.).
Схема 10:
Схема 10 демонстрирует синтез 9-бром-2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепина III из 4-бром-2-фторбензонитрила 11. Присоединение гидроксиламина к нитрилу 11 давало 4-бром-2-фтор-N-гидроксибензимидамид 24. Присоединение по Михаэлю 24 к этилпропиолату давало этил 3-(4-бром-2-фторбензимидамидоокси)акрилат 25. Нагревание 25 в высококипящем растворителе, таком как толуол, ксилол, этилбензол или дифенилоксид, давало циклизованный имидазол, этил 2-(4-бром-2-фторфенил)-1Н-имидазол-4-карбоксилат 26, наряду с побочным продуктом пиримидина, 2-(4-бром-2-фторфенил)пиримидин-4-олом. Альтернативно, 25 может циклизоваться до 26 с каталитическими кислотами Льюиса, такими как соли Cu(I) или Cu(II). Алкилирование 26 с 2-гидроксиэтилирующим реагентом, таким как 1,3-диоксолан-2-он, в основании, таком как N-метилимидазол или карбонат цезия, давало этил 2-(4-бром-2-фторфенил)-1-(2-гидроксиэтил)-1H-имидазол-4-карбоксилат 27. Кольцевая циклизация 27 с водным основным реагентом, таким как гидроксид калия, гидроксид лития и метилтрибутиламмония гидрохлорид, давала 9-бром-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-2-карбоновую кислоту 28. Присоединение ацетамидина к 28 с трифенилфосфином давало 9-бром-N-(1-иминоэтил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-2-карбоксамид 29. Кольцевая циклизация 29 с изопропилгидразина гидрохлоридом 4 в уксусной кислоте давала 9-бром-2-(1-изопропил-3-метил-1Н-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин III.
Альтернативно, 28 можно подвергнуть взаимодействию с N'-изопропилацетогидразонамидом 6, получая III (Схема 12).
Схема 11:
Схема 11 демонстрирует синтез 5-(2-(4-бром-2-фторфенил)-1Н-имидазол-4-ил)-1-изопропил-3-метил-1Н-1,2,4-триазола V из 4-бром-2-фторбензимидамида гидрохлорида 12. 3-Хлор-2-оксопропионовую кислоту и 12 подвергают взаимодействию с основанием, получая 2-(4-бром-2-фторфенил)-1Н-имидазол-4-карбоновую кислоту 30. Альтернативно, 3-бром-2-оксопропионовую кислоту можно подвергнуть взаимодействию с 12, получая 30. Реакция 30 с N'-изопропилацетогидразонамидом 6 и связующим реагентом HBTU (N,N,N',N'-тетраметил-O-(1Н-бензотриазол-1-ил)урония гексафторфосфат, О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат, CAS рег. №94790-37-1) в ДМФА дает промежуточное соединение, 2-(4-бром-2-фторфенил)-N-(1-(2-изопропилгидразинил)этилиден)-1Н-имидазол-4-карбоксамид 31, который не обязательно выделять, и он циклизуется при нагревании, что дает V.
Альтернативно, 5-(2-(4-хлор-2-фторфенил)-1H-имидазол-4-ил)-1-изопропил-3-метил-1Н-1,2,4-триазол 44, вариант V с хлором, можно получить из 4-хлор-2-фторбензонитрила 38 (Схема 15).
Схема 12:
Схема 12 демонстрирует альтернативный синтез 9-бром-2-(1-изопропил-3-метил-1H-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепина III из 4-бром-2-фторбензонитрила 11. Алкилирование 11 с трет-бутил 2-гидроксиэтилкарбаматом дает трет-бутил 2-(5-бром-2-цианофенокси)этилкарбамат 32. Циклизация 32 при кислотных условиях, таких как хлористоводородная кислота в этаноле, дает 8-бром-3,4-дигидробензо[f][1,4]оксазепин-5(2Н)-имин 33. Следует отметить, что 33 имеет альтернативную таутомерную форму, когда двойная связь находится внутри кольца оксазепина. Образование имидазольного кольца происходит в ходе реакции 3-бром-2-оксопропионовой кислоты (X = Br, R = ОН) или другой 3-гало-2-оксопропионовой кислоты, или эфира (R = алкил), и 33, что дает 9-бром-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-2-карбоновую кислоту 28. Связывание 28 с N'-изопропилацетогидразонамидом 6 и связующим реагентом, таким как HBTU, HATU или CDI, в ДМФА дает промежуточное соединение, 9-бром-N-(1-(2-изопропилгидразинил)этилиден)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин-2-карбоксамид 34, который не обязательно выделять, и из него образуется 9-бром-2-(1-изопропил-3-метил-1H-1,2,4-триазол-5-ил)-5,6-дигидробензо[f]имидазо[1,2-d][1,4]оксазепин III при нагревании.
Альтернативно, N'-изопропилацетогидразонамид 6 используют в виде моногидрохлорида, который следует выделить при реакционных условиях с подходящим основанием, таким как K2CO3.
Схема 13:
Схема 13 демонстрирует альтернативный синтез 8-бром-3,4-дигидробензо[f][1,4]оксазепин-5(2Н)-имина 33 из 4-бром-2-фторбензонитрила 11. Реакция 11 с метилатом натрия в метаноле дает метил 4-бром-2-фторбензимидат 35. Алкилирование 35 с 2-аминоэтанолом дает 4-бром-2-фтор-N-(2-гидроксиэтил)бензимидамид 36 с последующей циклизацией до 33.
Схема 14:
Схема 14 демонстрирует другой альтернативный синтез 8-бром-3,4-дигидробензо[f][1,4]оксазепин-5(2Н)-имина 33 из 4-бром-2-фторбензонитрила 11. В ходе реакции 11 с 2-аминоэтанолом и трет-бутилатом калия замещается фтор, что дает 2-(2-аминоэтокси)-4-бромбензонитрила гидрохлорид 37. Замыкание кольца 37 с триметилалюминием давало 33. Альтернативно, можно использовать другие триалкилалюминиевые реагенты или алкоголяты магния, такие как этилат магния (диэтоксид магния, CAS рег. №2414-98-4), чтобы циклизовать 37 до 33.
Схема 15:
Схема 15 демонстрирует синтез 5-(2-(4-хлор-2-фторфенил)-1Н-имидазол-4-ил)-1-изопропил-3-метил-1Н-1,2,4-триазола 44 из 4-хлор-2-фторбензонитрила 38. Присоединение гидроксиламина к нитрилу 38 давало 4-хлор-2-фтор-N-гидроксибензимидамид 39. Присоединение по Михаэлю 39 к этилпропиолату давало этил 3-(4-хлор-2-фторбензимидамидоокси)акрилат 40. Нагревание 40 в дифенилоксиде давало циклизованный имидазол, этил 2-(4-хлор-2-фторфенил)-1H-имидазол-4-карбоксилат 41. Омыление эфира 41 с водным гидроксидом натрия в тетрагидрофуране давало 2-(4-хлор-2-фторфенил)-1Н-имидазол-4-карбоновую кислоту 42. Реакция 42 с N'-изопропилацетогидразонамидом 6 и связующим реагентом HBTU в ДМФА дает промежуточное соединение, 2-(4-хлор-2-фторфенил)-N-(1-(2-изопропилгидразинил)этилиден)-1Н-имидазол-4-карбоксамид 43, который циклизуется при нагревании с образованием 44.
Лекарственные препараты
GDC-0032, формулы I, можно изготовить в соответствии с общепринятой фармацевтической практикой для применения в терапевтическом сочетании для терапевтического лечения (включая профилактическое лечение) гиперпролиферативных заболеваний у млекопитающих, включая людей. Согласно изобретению предложена фармацевтическая композиция, включающая GDC-0032 в сочетании с одним или более чем одним фармацевтически приемлемым носителем, скользящем веществом, разбавителем или эксципиентом.
Подходящие носители, разбавители, скользящие вещества и эксципиенты хорошо известны квалифицированным специалистам в данной области техники и включают вещества, такие как углеводы, воски, водорастворимые и/или разбухающие полимеры, гидрофильные или гидрофобные вещества, желатин, масла, растворители, вода и подобные.
Препараты можно получить, используя традиционные процедуры растворения и перемешивания. Соединение по настоящему изобретению обычно входит в состав фармацевтических лекарственных форм, обеспечивая тем самым легко регулируемую дозировку лекарства и соблюдение пациентом предписанного режима.
Фармацевтическая композиция (или препарат) для применения может быть упакован разными способами в зависимости от способа, используемого для введения лекарства. Как правило, изделие для распространения включает контейнер с вложенным в него фармацевтическим препаратом в подходящей форме. Подходящие контейнеры хорошо известны квалифицированным специалистам в данной области техники и включают материалы, такие как флаконы (пластиковые и стеклянные), пакетики, ампулы, пластиковые пакеты, металлические цилиндры и подобные. Также контейнер может включать устройство контроля первого вскрытия, чтобы предотвратить неосторожный доступ к содержимому упаковки. Кроме того, на контейнер наносится этикета, которая описывает содержимое контейнера. Также этикета может включать соответствующие предупреждения.
Фармацевтические препараты соединений по настоящему изобретению можно получить для разных способов и типов введения с фармацевтически приемлемыми разбавителями, носителями, экципиентами, скользящими веществами или стабилизаторами (Remington's Pharmaceutical Sciences (1995) 18th edition, Mack Publ. Co., Easton, PA) в форме лиофилизированного препарата, полученного размолом порошка или водного раствора. Препарат можно производить, смешивая при температуре окружающей среды при соответствующем pH и при требуемой степени чистоты с физиологически приемлемыми носителями, т.е. носителями, которые нетоксичны к реципиентам при используемых дозах и концентрациях. pH препарата в основном зависит от конкретного применения и концентрации соединения, но может изменяться от приблизительно 3 до приблизительно 8.
Фармацевтический препарат предпочтительно является стерильным. В частности, препараты, используемые для введения in vivo, должны быть стерильными. Такую стерилизацию легко выполнить в ходе фильтрации через стерилизующие фильтрующие мембраны.
Фармацевтический препарат как правило можно хранить в виде твердой композиции, таблетки, пилюли, капсулы, лиофилизированного препарата или в виде водного раствора.
Фармацевтические препараты по изобретению дозируют и вводят до известной степени, т.е. количества, концентрации, режимы, курс, наполнители и способ введения согласуются с надлежащей медицинской практикой. Рассматриваемые в этой связи факторы включают конкретное заболевание, подвергаемое лечению, клиническое состояние отдельного пациента, причину заболевания, место доставки лекарства, способ введения, планирование введения и другие факторы, известные врачам.
Приемлемые разбавители, носители, эксципиенты и стабилизаторы не токсичны для реципиентов при используемых дозах и концентрациях, и включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид, бензетония хлорид; фенол, бутил, этанол или бензиловый спирт; алкилпарабены, такие как метил или пропилпарабен; катехол; резорцин; циклогексанол; 3-пентанол и м-крезол); низкомолекулярные (менее чем приблизительно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахара, т