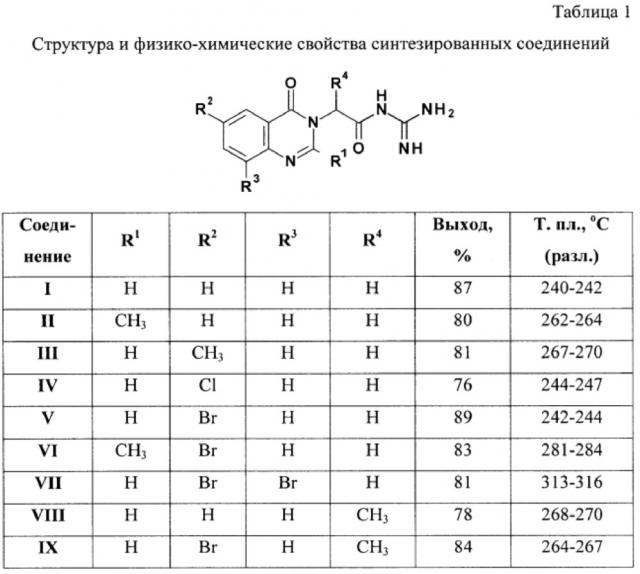
Производные хиназолин-4(3н)-она, ингибирующие натрий-водородный обмен
Иллюстрации
Показать всеИзобретение относится к новым производным хиназолин-4(3H)-она общей формулы
где R1=Н или СН3; R2=Н, СН3, Сl или Br; R3=Н или Вr; R4=Н или СН3, которые обладают ингибиторной активностью в отношении натрий-водородного обменника первой изоформы. В экспериментах in vitro на тромбоцитах кролика соединения демонстрируют величину ингибиторной концентрации IС50 в диапазоне 1×10-8-1×10-12 моль/л и значительно превосходят препарат сравнения зонипорид. Новые производные хиназолин-4(3H)-она могут найти применение при разработке эффективных и безопасных нейро- и кардиопротекторных лекарственных средств, реализующих свои лечебные эффекты посредством влияния на натрий-водородный обмен. 4 табл., 2 пр.
Реферат
Изобретение относится к области фармакологии, к новым средствам, обладающим способностью ингибировать натрий-водородный обмен.
Патобиохимический каскад ишемического повреждения миокарда, нервной ткани представляет собой серию многочисленных взаимосвязанных процессов. В первую очередь, это метаболические нарушения, которые вызывают дисбаланс между процессами гликолиза и окисления глюкозы, приводящие к внутриклеточному накоплению лактата и ацидозу. Понижение рН способствует активации Na+/H+ обменника (NHE) [Orlowski J., Grinstein S. Na+/H+ exchangers // Compr. Physiol. - 2011. - Vol.1. - No. 4. - P. 2083-2100], а дефицит энергии нарушает работу наиболее энергозависимого фермента натрий-калий-АТФазы. Последствием этих процессов является избыточное проникновение в клетку ионов натрия с последующей активацией реверсивного тока кальция, усилению поступления внеклеточного Са2+ в клетку и высвобождению внутриклеточного Са2+ из депо. Перегрузка кальцием клетки активизирует различные ферментные системы, приводит к образованию свободных радикалов, повышает синтез NO, способствует цитотоксическому отеку, развитию оксидантного стресса, что, в конечном итоге, способствует гибели клетки по некротическому или апоптотическому путям. Несмотря на обилие механизмов, приводящих к перегрузке кальцием и гибели клетки, NHE первой изоформы (NHE-1) является одним из основных факторов регуляции гомеостаза в условиях ишемии/реперфузии [Fliegel L. Molecular biology of the myocardial Na+/H+ exchanger // J. Mol. Cell. Cardiol. - 2008. - Vol. 44. - No. 2. - P. 228-237].
NHE-1 принимает участие во многих патологических процессах центральной нервной и сердечно-сосудистой систем: ишемически-реперфузионом повреждении миокарда и головного мозга [Спасов А.А., Муравьева В.Ю., Гурова Н.А., Чепляева Н.И., Резников Е.В., Анисимова В.А. Нейропротекторные свойства нового ингибитора Na+/H+-обменника соединения РУ-1355 на модели фокальной ишемии у крыс // Эксперим. клинич. фармакол. - 2016. - Т. 79. - №4. - С. 3-7; Karmazyn М. NHE-1: still а viable therapeutic target // Rev. Bras. Cir. Cardiovasc. - 2013. - No. 61. - P. 7-82], нарушении ритма [Ayoub I.M., Kolarova J.D. Zoniporide preserves left ventricular compliance during ventricular fibrillation and minimizes postresuscitation myocardial dysfunction through benefits on energy metabolism // Crit. Care Med. - 2007. - Vol. 35. - No. 10. - P. 2329-2336] и развитии гипертрофии сердца, сердечной недостаточности [Wakabayashi S., Hisamitsu Т., Nakamura T.Y. Regulation of the cardiac Na+/H+ exchanger in health and disease // J. Mol. Cell. Cardiol. - 2013. - Vol. 61. - No. 1. - P. 68-76], эндотелиальной дисфункции, болезни Альцгеймера [ R., U.H., K. The Na+/H+ exchanger modulates long-term potentiation in rat hippocampal slices //Naunyn Schmiedebergs Arch. Pharmacol. - 2009. - Vol. 379. - No. 3. - P. 233-239] и эпилепсии [Verma V., Bali A., Singh N. Implications of sodium hydrogen exchangers in various brain diseases // J. Basic. Clin. Physiol. Pharmacol. - 2015. - Vol. 26. - No. 5. - P. 417-426].
В настоящее время актуальным направлением является поиск и исследование ингибиторов NHE-1 в качестве потенциальных цитопротекторов, защищающих клетки от ишемического и реперфузионного повреждения. При анализе химической структуры известных ингибиторов NHE-1 выявлено, что большинство из них содержат гуанидиновую группу. Ингибиторы NHE-1 найдены среди производных пиразина (амилорид, DMA, EIPA, MIBA); бензоилгуанидинов (HOE-642, HOE-694, EMD-96785); моноциклических производных гуанидина - производных метакрилоилгуанидина (S1611, S3226); бициклических производных гуанидина: производных индолоилгуанидина (SM-20220) и хинолина (зонипорид) [Orlowski J., Grinstein S. Na+/H+ exchangers // Compr. Physiol. - 2011. - Vol. 1. - No. 4. - P. 2083-2100]. Показана NHE-1-ингибирующая активность у ряда производных бензимидазолов [Патент РФ №2518740. Средство, ингибирующее Na+/Н+-обмен, и дигидрохлорид 2-(3,4-метилендиоксифенил)-9-морфолиноэтилимидазо[1,2-a]бензимидазола // Спасов А.А., Анисимова В.А., Гурова Н.А., Тимофеева А.С., Федорчук В.Ю., Минкин В.И. - Опубл. 10.06.2014. - Бюлл. Изобр. - 2014. - №16; Zhang R., Lei L., Xu Y. Benzimidazol-2-yl or benzimidazol-2-ylthiomethyl benzoylguanidines as novel Na+/H+ exchanger inhibitors, synthesis and protection against ischemic-reperfusion injury // Bioorg. Med. Chem. Lett. - 2007. - Vol. 17. - No. 9. - P. 2430-2433] и аминобензимидазолов [Патент РФ №2518741. Средство, ингибирующее Na+/H+-обмен, и галогениды 1-диалкиламиноэтил-3-[замещенный(дизамещенный)фенацил]-2-аминобензимидазолия // Анисимова В.А., Спасов А.А., Гурова Н.А., Толпыгин И.Е., Тимофеева А.С., Федорчук В.Ю., Петров В.И., Минкин В.И. - Опубл. 10.06.2014. - Бюлл. Изобр. - 2014. - №16]. Согласно базе данных [Thomson Reuters Integrity, 2011], известно 481 соединение, проявляющее NHE-ингибирующую активность, которые находятся на различных стадиях доклинических и клинических исследований. В качестве возможных терапевтических групп они рекомендованы для лечения стенокардии, нарушений ритма сердечных сокращений, нарушений мозгового кровотока и сердечной недостаточности.
В настоящее время наиболее активным для селективного фармакологического ингибирования NHE-1 считается производное бензоилгуанидина - зонипорид - [1-(хинолин-5-ил)-5-циклопропил-1Н-пиразол-4-карбонил]гуанидина гидрохлорид моногидрат. В исследованиях на тромбоцитах кролика данный препарат подавлял NHE-1-зависимое набухание тромбоцитов; на изолированном сердце по Лангендорфу и in vivo уменьшал размер инфаркта, ослаблял постреперфузионную сократительную дисфункцию, а также снижал частоту и продолжительность желудочковых фибрилляций [Tracey W.R., Allen М.С., Frazier D.E. Zoniporide: a potent and selective inhibitor of the human sodium-hydrogen exchanger isoform 1 (NHE-1) // Cardiovasc. Drug Rev. - 2003. - No. 21. - P. 17-32]. Нейропротекторные эффекты зонипорида связаны с ингибированием так называемого глутамат-кальциевого каскада как in vitro, так и in vivo при моделировании фокального ишемического повреждения [Lee В.К., Lee D.H., Park S. Effects of KR-33028, a novel Na+/H+ exchanger-1 inhibitor, on glutamate-induced neuronal cell death and ischemia-induced cerebral infarct // Brain Res. - 2009. - Vol. 1248. - No. 6. - P. 22-30]. В настоящее время проводятся клинические испытания препарата фирмой Pfizer у больных с инфарктом миокарда, заболеваниями коронарных сосудов и атеросклерозом.
Поиск, изучение и создание новых цитопротекторных средств является актуальной задачей в решении проблемы улучшения прогноза сердечно-сосудистых заболеваний. Используемые в России кардио- и нейропротекторы имеют недостаточно высокую клиническую эффективность. Поиск и изучение соединений с NHE-1-ингибирующими свойствами позволит создать препараты патогенетической терапии ишемического повреждения тканей [Спасов А.А., Гурова Н.А., Харитонова М.В. Структура и биологическая роль NHE-1. Фармакологическая регуляция активности // Эксперим. клинич. фармакол. - 2013. - Т. 76. - №1. - С. 43-48; Madonna R., De Caterina R. Sodium-hydrogen exchangers (NHE) in human cardiovascular diseases: interfering strategies and their therapeutic applications // Vascul. Pharmacol. - 2013. - Vol. 59. - No. 5-6. - P. 127-130].
Целью изобретения является разработка новых высокоактивных и низкотоксичных ингибиторов натрий-водородного обмена для создания на их основе эффективных и безопасных нейро- и кардиопротекторных лекарственных средств.
Сущность изобретения заключается в синтезе и использовании в качестве ингибиторов натрий-водородного обмена новых производных хиназолин-4(3H)-она, содержащих фрагменты N-ацетилгуанидина в качестве заместителей при атоме азота N3 хиназолиновой гетероциклической системы. Синтез целевых соединений был осуществлен путем аминирования сложных эфиров 2-[ханазолин-3(4H)-ил]уксусной или пропионовой кислоты, содержащих различные заместители в положениях 2, 6 и 8 хиназолин-4(3H)-она, гуанидином-основанием, получаемым in situ из соответствующего гидрохлорида в среде безводного метилового спирта в присутствии калия гидроксида.
Представленные ниже примеры иллюстрируют сущность предлагаемого изобретения.
Пример 1. N-[2-Метил-6-бромхиназолин-3(4H)-ил]ацетилгуанидин (соединение VI).
А. Метиловый эфир 2-ацетиламинобензойной кислоты. К раствору 25,0 мл (0,193 моль) метилового эфира антраниловой кислоты и 20,0 мл (0,247 моль) безводного пиридина в 100 мл безводного 1,2-дихлорэтана, охлаждаемому на ледяной бане, при интенсивном перемешивании добавляют в течение 15 мин 25,0 мл (0,265 моль) уксусного ангидрида. Перемешивают при охлаждении еще 15 мин и оставляют на ночь при комнатной температуре. Реакционную массу последовательно промывают 100 мл воды, 100 мл 1 М хлористоводородной кислоты, 100 мл воды, сушат сульфатом магния, фильтруют и упаривают на роторном испарителе при температуре 70-80°С в вакууме водоструйного насоса. Охлаждают, закристаллизовавшийся остаток сушат на воздухе в течение суток при комнатной температуре и получают 36,6 г (98%) белого кристаллического вещества, Т. пл. 98-100°С, которое используют далее без дополнительной очистки.
Б. Метиловый эфир 5-бром-2-ацетиламинобензойной кислоты. К перемешиваемому раствору 15,0 г (0,078 моль) метилового эфира 2-ацетиламинобензойной кислоты в 100 мл безводного диметилформамида добавляют при комнатной температуре в один прием 14,2 г (0,082 моль) N-бромсукцинимида, перемешивают 1 ч и оставляют на сутки в защищенном от света месте. Реакционную массу выливают в 500 мл ледяной воды, через 15 мин образовавшийся осадок отфильтровывают, промывают на фильтре 3 раза по 50 мл воды, сушат на воздухе в течение суток при комнатной температуре и получают 19,9 г (94%) белого игольчатого кристаллического вещества, Т. пл. 132,5-134°С.
Спектр ЯМР 1Н, δ, м. д. (ДМСO-D6): 2,12 с (3Н, СН3); 3,87 с (3Н, СН3); 7,69-7,74 м (1Н, Н3); 7,95 т (1Н, 4 Гц, Н6); 8,17-8,21 м (1Н, Н4); 10,38 уш. с (1Н, NH).
Спектр ЯМР 13С, δ, м. д. (ДMCO-D6): 27,86; 55,94; 117,79; 123,02; 126,53; 135,87; 139,64; 142,34; 169,58; 171,83.
В. 2-Метил-6-бромхиназолин-4(3H)-он. Смесь 15,0 г (0,055 моль) метилового эфира 5-бром-2-ацетиламинобензойной кислоты и 50 мл концентрированного гидроксида аммония нагревают в стальном герметичном сосуде на кипящей водяной бане в течение 8 ч при периодическом перемешивании и оставляют на ночь при комнатной температуре. Образовавшийся осадок отфильтровывают, промывают на фильтре 2 раза по 10 мл холодной воды, сушат на воздухе в течение суток и получают 7,3 г (55%) белого кристаллического вещества, Т. пл. 298-302°С.
Спектр ЯМР 1Н, δ, м. д. (ДМСО-D6): 2,33 с (3Н, СН3); 7,47 д (1H, 4 Гц, Н8); 7,84 д (1Н, 4 Гц, Н7); 8,12 с (1Н, Н5); 11,85 уш. с (1Н, NH).
Спектр ЯМР 13С, δ, м. д. (ДМСО-D6): 24,84; 121,41; 125,73; 131,18; 132,27; 140,26; 151,32; 158,42; 163,94.
Г. Бензиловый эфир [2-метил-6-бромхиназолин-3(4H)-ил]уксусной кислоты. 3,0 г (0,013 моль) 2-метил-6-бромхиназолин-4(3H)-она и 4,0 г (0,029 моль) безводного карбоната калия перемешивают в 40 мл безводного диметилформамида при температуре 80-85°С в течение 15 мин, добавляют раствор 3,0 г (0,013 моль) бензилового эфира бромуксусной кислоты в 10 мл диметилформамида и перемешивают при той же температуре 1 ч. Реакционную массу охлаждают, фильтруют, фильтрат упаривают на роторном испарителе при остаточном давлении 10 мм рт. ст. при температуре бани 90-95°С, остаток охлаждают, растирают с 25 мл воды, фильтруют, промывают на фильтре 2 раза по 10 мл холодной воды, сушат на воздухе в течение суток и кристаллизуют из 100 мл изопропилового спирта. Получают 3,0 г (62%) золотисто-желтых игольчатых кристаллов, Т. пл. 158,5-160,5°С.
Спектр ЯМР 1Н, δ, м. д. (ДМСО-D6): 2,51 с (3Н, СН3); 5,00 с (2Н, СН2); 5,22 с (2Н, СН2); 7,30-7,42 м (5Н, фенил); 7,56 д (1Н, 4 Гц, Н8); 7,95 д (1Н, 4 Гц, Н7); 8,16 с (1Н, Н5).
Спектр ЯМР 13С, δ, м. д. (ДМСО-D6): 26,21; 49,06; 70,16; 122,31; 124,38; 131,36; 131,61; 131,63; 131,85; 132,53; 138,83; 141,01; 145,39; 158,90; 163,39; 171,22.
Д. N-[2-Метил-6-бромхиназолин-3(4H)-ил]ацетилгуанидин (соединение VI). К кипящему раствору 2,50 г (6,46 ммоль) бензилового эфира [2-метил-6-бромхиназолин-3(4H)-ил]уксусной кислоты и 0,75 г (7,85 ммоль) гуанидина гидрохлорида в 50 мл безводного метилового спирта добавляют в один прием 0,55 г (8,84 ммоль) гранулированного калия гидроксида и кипятят в течение 30 мин. Горячий раствор фильтруют, отделяя образовавшийся осадок калия хлорида, фильтрат охлаждают и выдерживают в течение суток при комнатной температуре. Выделившийся осадок отфильтровывают, промывают 2 раза по 10 мл холодного метилового спирта, 10 мл диэтилового эфира, сушат на воздухе в течение суток при комнатной температуре и получают 1,8 г (83%) белого кристаллического вещества, Т. пл. 281-284°С (разл.).
Спектр ЯМР 1Н, δ, м. д. (ДMCO-D6): 2,46 с (3Н, СН3); 4,47 с (2Н, СН2); 7,51 д (1Н, 8 Гц, Н8); 7,60 уш. с (4Н, NH); 7,88 д (1Н, 8 Гц, Н7); 8,13 с (1Н, Н5).
Спектр ЯМР 13С, δ, м. д. (ДМСО-D6): 23,24; 47,76; 118,44; 121,86; 128,56; 129,20; 137,14; 146,53; 156,98; 159,13; 160,22; 170,91.
Остальные соединения получают аналогично. Выход и физико-химические свойства веществ представлены в табл. 1, спектральные характеристики - в табл. 2 и 3.
Пример 2. Изучение влияния новых производных хиназолина на активность Na+/H+-обменника (ингибиторование NHE-1). Изучение влияния соединений на активность Nа+/Н+-обменника проведено in vitro на тромбоцитах кролика, на мембране которых активно экспрессируют NHE-1, по методу [Rosskopf D., Morgenstern Е., Scholz W. Rapid determination of the elevated Na+/Н+ exchanger in platelets of patients with essential hypertension using an optical swelling assay // J. Hypertens. - 1991. - No. 9. - P. 231-238; Kusumoto K., Igata H., Abe A. In vitro and in vivo pharmacology of a structurally novel Na+/H+ exchanger inhibitor, T-162559 // Brit. J. Pharmacol. - 2002. - No. 135. - P. 1995-2003]. Образцы крови забирали из краевой вены уха кролика в пробирку, содержащие 3,8% цитрата натрия, в соотношении 1:10. Для получения плазмы, богатой тромбоцитами (ПБогТ), кровь центрифугировали при 1000 об/мин в течение 12 мин. Для проведения калибровки использовали ПБогТ с ЭДТА и раствор Кребса (NaCl - 120 мМ, КСl - 4,8 мМ, КН2РO4 - 1,2 мМ, MgSO4 - 2,5 мМ, NaHCO3 - 25 мМ, СаСl2 - 2,6 мМ, глюкоза - 5,4 мМ, рН - 7,4). В контрольной серии экспериментов к 200 мкл ПБогТ для снижения внутриклеточного рН добавляли 600 мкл раствора пропионата натрия (в ммоль/л: пропионат натрия -135, HEPES - 20, СаСl2 - 1, MgCl2 - 1, глюкоза - 10; рН 6,7; температура 37°С). При этом происходила активация Na+/H+-обменника и увеличение притока натрия, связанное с выделением цитозольного, ведущее к отеку (сферуляции), тромбоцита в результате аккумуляции воды в цитоплазме. Наблюдалось облегчение светопропускания. Для контроля изменения светопропускания в условиях физиологического значения рН использовали раствор Кребса (600 мкл). Изменения формы тромбоцитов регистрировали по изменению уровня светопропускания с помощью лазерного агрегометра «БИОЛА-220 ЛА» (Россия). При изучении новых соединений и препарата сравнения зонипорида (SIGMA, США) 10 мкл вещества добавляли в кювету с ПБогТ (200 мкл) за 3-5 мин до добавления раствора пропионата натрия, инкубировали при температуре 37°С и постоянном перемешивании с помощью магнитной мешалки (1000 об/мин). Исследования проводили в диапазоне концентраций 1×10-8-1×10-12 М. Для исследуемых веществ и препарата сравнения экспериментально определяли величины IС50 с использованием метода регрессионного анализа зависимости между lg концентрации и процентом ингибирования активности обменника в программе Microsoft Excel (пакет Office ХР, Microsoft, США). В экспериментах были использованы кролики-самцы (n=15) весом 2,5-3,5 кг (Филиал «Электрогорский» ФГБУ НЦБМТ РАН, ветеринарное свидетельство 250 №0380791 от 14.01.2013 г.). Результаты исследований представлены в табл. 4.
Исследования проведены в соответствии с применимыми требованиями ГОСТ ИСО/МЭК 17025-2009, ГОСТ Р ИСО 5725-2002 и ГОСТ 33044-2014 «Межгосударственный стандарт. Принципы надлежащей лабораторной практики» (введен в действие Приказом Росстандарта от 20.11.2014 г. №1700-ст) с соблюдением «Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях» [Directive 2010/63/EU of the European Parliament and of the Council of 22 September 2010 on the protection of animals used for scientific purposes. - Official Journal. - L 276, 20.10.2010. - P. 33-79] (revising Directive 86/609/EEC). Все эксперименты были одобрены локальным Этическим комитетом (протокол №126-2011 от 02 февраля 2011 г.).
Как следует из данных табл. 4, наиболее активные соединения VI и VII по своей способности ингибировать NHE-1 in vitro соответственно в 3250 и 8500 раз превосходят препарат сравнения.
Таким образом, результаты исследований свидетельствуют о том, что на основе новых производных хиназолина, содержащих гуанидиновые фрагменты, возможно создание новых, более эффективных и безопасных нейро- и кардиопротекторных лекарственных средств, реализующих свои лечебные эффекты посредством влияния на натрий-водородный обмен.
Производные хиназолин-4(3H)-она общей формулы
где R1=Н или СН3; R2=Н, СН3, Cl или Br; R3=Н или Br; R4=Н или СН3,
ингибирующие натрий-водородный обмен.