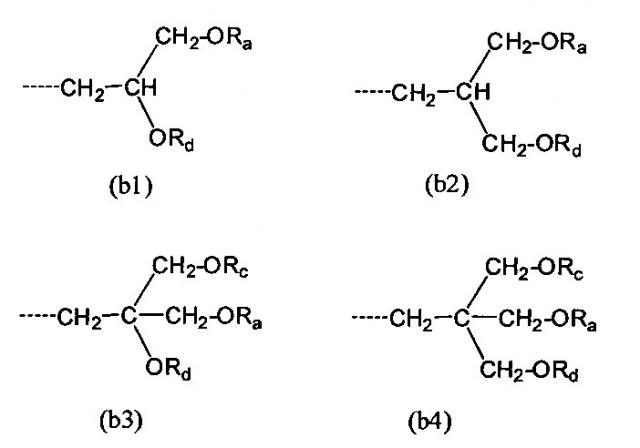
Нацеливающие аминокислотные липиды
Иллюстрации
Показать всеИзобретение относится к системе носителя, включающей соединение формулы I, и включает этер-липиды, конъюгированные с одним или более биоактивными лигандами, которые размещаются на поверхности системы носителя, для применения в нацеленной доставке и/или системах антигенного дисплея. Необязательно, один или более дополнительных биоактивных агентов могут быть инкапсулированы или встроены в, или присоединены к, или адсорбированы на системе носителя. Также предложены соединения формулы I, где Y представляет собой О, N, S или ковалентную связь, S1, S2, S3 представляют собой независимо друг от друга ковалентную связь или группу спейсера, Х1, Х2, Х3 представляют независимо друг от друга Н или нацеливающий лиганд, или антигенный лиганд, или терапевтический лиганд, или диагностический лиганд, или их комбинацию, L представляет собой группу формулы (а), где пунктирная линия представляет собой связь с N, R1 представляет собой Н, R1' представляет собой Н, R2 представляет собой Н, R2' представляет собой Н или группу формулы -ORd или -СН2- ORd, R3 представляет собой Н или группу формулы -(CH2)2-ORe или -(CH2)3-ORe, Ra, Rd, Re представляют независимо друг от друга неразветвленный или разветвленный С(10-22)алкил, С(10-22)алкенил или С(10-22)алкинил, m равен 1, 2 или 3, при условии, что по крайней мере один из R1, R1', R2, R2', R3 не является Н, и по крайней мере один из Х1, Х2, Х3 представляет собой указанную группу лиганда. 4 н. и 11 з.п. ф-лы, 1 табл., 2 ил., 22 пр.
Реферат
Область изобретения
Настоящее изобретение является направленным на системы носителя, которые включают этер-липиды, конъюгированные с одним или более биоактивными лигандами (которые размещаются на поверхности системы носителя), для применения в нацеленных системах доставки и/или в системах дисплея антигена, где системы носителя могут включать один или более дополнительных биоактивных агентов. Настоящее изобретение также является направленным на способы их получения и их применение для медицинских показаний, таких как нацеленная доставка указанных биоактивных агентов к специфическим тканям или клеткам и системы дисплея антигена, для изучения, диагностики и лечения симптомов, состояний и заболеваний, которые являются чувствительными к указанным биоактивным агентам.
Предпосылки создания изобретения
Молекулярное узнавание, такое как имеет место между рецептором и лигандом, антигеном и антителом, ДНК и белком, сахаром и лектином, РНК и рибосомой и т.д., представляет собой важный принцип, который лежит в основе многих биологических систем и является применимым к множеству искусственно созданных биологических систем для применения с медицинской целью, как, например, в синтетических (микро- или нано-) системах на основе частиц, включая полимерные шарики, везикулярные липиды, микроэмульсии и тому подобное. Один важный пример применения на основе молекулярного узнавания представляет собой применение нацеленной доставки диагностических или терапевтических соединений, таких как противовирусные, химиотерапевтические или радиофармацевтические препараты, к специфическим сайтам, что позволяет преодолевать ограничения, которые ассоциируются с неспецифической доставкой (такие как время выведения in vivo, потенциальная токсичность, проблемы, связанные с транспортом через мембраны агента и подобные им) и, таким образом, значительно повышают их эффективность таких соединений. Были использованы разнообразные стратегии на основе узнавания для улучшения доставки соединений во внутриклеточное содержимое целевой клетки (то есть к специфическим компартментам клетки) для оказания влияния на ее биологическую активность, в частности, доставка с помощью специфических транспортеров, которая предусматривает применение биологических или синтетических носителей, таких как вирусные векторы, катионные полимеры, такие как полилизин, полиаргинин и подобные им (смотри, например, WO 79/00515, WO 98/52614), липидные носители, а также различные другие конъюгатные системы.
Один широко используемый подход предусматривает применение липидных везикул в качестве синтетических носителей, например липосом или мицелл, которые были подвергнуты интенсивному усовершенствованию и исследованию в качестве векторов для доставки лекарственных средств благодаря их способности снижать системное воздействие биоактивного агента, преодолевая, таким образом, проблемы, которые ассоциируются с разложением, растворимостью и т.д., и обеспечивая удлинение периода времени циркуляции в русле крови. Активно нацеленная доставка биоактивного агента предусматривает дериватизацию липидов в составе липидных везикул (либо до, либо после формирования везикул) с нацеливающим лигандом, который является предназначенным для направления (или нацеливания) везикулы на специфические типы клеток, такие как раковые клетки или клетки, которые являются специфическими для определенных тканей и органов, такие как гепатоциты, после in vivo введения (смотри, например, US 6316024 и US 6214388; Allen и др., Biochim. Biophys. Acta, 1237: 99-108 (1995); Blume и др., Biochim. Biophys. Acta, 1149: 180-184 (1993)). Это может сопровождаться использованием рецепторов, которые сверхэкспрессируются в клетках специфического типа, включающих, например, рецептор фолиевой кислоты (FR) (который сверхэкспрессируется в разнообразных неопластических тканях, включая опухоли молочной железы, яичника, шейки матки, колоректальные, ренальные и назофарингеальные опухоли), трансферриновый рецептор (TfR) (который сверхэкспрессируется на метастатических и устойчивых к лекарственным средствам клетках большинства карцином, сарком, а также некоторых лимфом и лейкемий), рецептор эпидермального фактора роста (EGFR) (который сверхэкспрессируется при анапластическом раке щитовидной железы и молочной железы, легочной и колоректальной опухоли), рецептор сосудистого эндотелиального фактора роста 1 и 2 (VEGFR-1/2) (который экспрессируется на высоком уровне на эндотелиальных клетках в опухолевых новообразованных сосудах), рецептор метастатина (который сверхэкспрессируется при аденопапиллярной злокачественной опухоли щитовидной железы), ErbB семейство рецепторов тирозинкиназ (которые сверхэкспрессируются при большом подмножестве видов рака молочной железы), рецептор эпидермального фактора роста (Her2/neu) (который сверхэкспрессируется при раке молочной железы), рецептор тирозинкиназы-18 (c-Kit) (который сверхэкспрессируется при саркоматоидных ренальных карциномах), HGF рецептор c-Met (который сверхэкспрессируется при аденокарциноме пищевода), CXCR4 и CCR7 (которые сверхэкспрессируются при раке молочной железы), рецептор эндотелина А (который сверхэкспрессируется при раке предстательной железы), рецептор дельта, активируемый пролифератором пероксисом (PPAR-delta) (который сверхэкспрессируется при большинстве случае колоректального рака), PDGFR А (который сверхэкспрессируется в карциномах яичника), BAG-1 (который сверхэкспрессируется при различных видах рака легких), рецептор растворимого типа II TGF бета (который сверхэкспрессируется при раке поджелудочной железы), асиалогликопротеиновый рецептор (который сверхэкспрессируется на гепатоцитах), рецептор avβ3 интегрина (который сверхэкспрессируется в растущей сосудистой системе опухоли), легумаин (группа CD цистеинпротеазы, которая является обогащенной в ткани солидных опухолей и сверхэкспрессируется на ТАМ, ассоциированных с опухолью макрофагах), и т.д.
Любой агент, который специфически связывается с таким специфическим рецептором клетки или ткани, которые подвергаются обработке или анализу, может присоединяться к липидной везикуле и функционировать в качестве нацеливающего или рецепторного лиганда. В типичном случае такие нацеливающие лиганды присоединяют к липиду или к поверхности липидной везикулы с помощью линкера с длинной цепью (например, полимерного). К примеру, конъюгаты на основе фолиевой кислоты использовали для обеспечения подхода нацеленной доставки терапевтического соединения, полезного для лечения и/или диагностики заболевания, что позволяло снизить необходимую дозу терапевтических соединений (смотри, например, WO 02/094185, US 6335434, WO 99/66063, US 5416016). Кроме того, применение конъюгатов на основе галактозы и галактозамина для транспорта экзогенных соединений через клеточные мембраны может обеспечивать подход нацеленной доставки при лечении заболеваний печени, таких как инфекция HBV и HCV или гепатоклеточная карцинома, одновременно позволяя снизить требуемую дозу терапевтических соединений, которая является необходимой для лечения (смотри, например, US 6030954).
Другой важный пример применения на основе молекулярного узнавания представляет собой применение систем дисплея антигена, которые вовлекают презентацию как "собственных, так и "чужеродных" белков (антигенов) иммунной системе для достижения активации, модуляции или толерантности Т-клеток. Взаимодействия рецептора и лиганда в системах презентации антигена, которые осуществляют свой вклад в желаемый иммунный ответ или его отсутствие, являются комплексным и сложным для оценки, и подвергается воздействию со стороны различных параметров, таких как концентрации лигандов, присутствие корецепторов, аффинность связывания лиганд-рецептор и состояние поверхности. Таким образом, широко используемый подход вовлекает применение существующих в природе клеток человека (или их частей), первичная функция которых состоит в процессинге и презентации антигена. Однако в то время как системы на основе живых клеток могут быть оптимальными для имитации взаимодействия между клетками и для достижения желаемой индукции толерантности или иммунного ответа, они являются зависимыми от регулируемой экспрессии поверхностных молекул, включая возможную экспрессию дополнительных "костимуляторных" и/или адгезионных молекул на их поверхностной мембране при достаточном терапевтическом уровне. Известные в настоящее время искусственные системы колеблются от генетически сконструированных субклеточных везикул, презентирующих антиген, которые на своей поверхности несут молекулы, необходимые для презентации антигена и активации или ингибирования Т-лимфоцитов, (WO 03/039594) до систем презентации антигена, в основе которых лежит биоразлагаемые микросферы, имеющие размер клетки (WO 07/087341).
Является понятным, что указанные выше системы узнавания все еще имеют недостатки, а также все еще существует потребность в области техники в многофункциональных и эффективных системах на основе искусственного носителя для применений, которые основываются на молекулярном узнавании, таких как нацеленная доставка или презентация антигена, включая простые и экономичные способы их получения.
Настоящая заявка обеспечивает конъюгаты, которые включают этер-липиды, содержащие один или более ковалентно присоединенных биоактивных лигандов, а также различные системы носителя, которые включают такие конъюгаты (и которые необязательно включают один или более биоактивных агентов), позволяющие преодолевать описанные выше ограничения.
Краткое изложение сущности изобретения
Настоящее изобретение является направленным на системы носителя, которые включают этер-липиды, конъюгированные с одним или более биоактивными лигандами, для применения в нацеленной доставке и/или системах антигенного дисплея. Один или более биоактивных лигандов являются ковалентно присоединенными к этер-липидам общей формулы I и размещаются на поверхности системы носителя. Необязательно, по крайней мере, один биоактивный агент может быть инкапсулированным или встроенным в, или присоединенным к, или адсорбированным на поверхности системы носителя.
Таким образом, в одном аспекте изобретение является направленным на систему липидного носителя в форме везикулы, такую как липосома или мицелла, которые включают, по крайней мере, один конъюгат липид-лиганд формулы I, необязательно в смеси с дополнительными со-липидами. По крайней мере, один конъюгат липид-лиганд включает, по крайней мере, один этер-липид, который является связанным, по крайней мере, с одним биоактивным лигандом, таким как антигенный лиганд, целевой лиганд, терапевтический или диагностический лиганд. Необязательно, по крайней мере, один дополнительный биоактивный агент является инкапсулированным или встроенным во внутреннюю область или двойной слой (мембраны) или присоединенным к, или адсорбированным на поверхности везикулы. В некоторых воплощениях везикула представляет собой липосому или мицеллу. В другом аспекте изобретение является направленным на систему носителя на основе наночастиц в форме частиц, покрытых липидом, которые имеют внутренние полости или твердое ядро, где частица является покрытой с помощью, по крайней мере, одного конъюгата липид-лиганд формулы I, необязательно, в смеси с дополнительными со-липидами. По крайней мере, один конъюгат липид-лиганд формулы I включает, по крайней мере, один этер-липид, который является связанным, по крайней мере, с одним биоактивным лигандом, таким как антигенный лиганд, целевой лиганд, терапевтический лиганд или диагностический лиганд.
В некоторых воплощениях материал наночастиц представляет собой покрытую липидом наночастицу или наносферу. Необязательно, по крайней мере, один дополнительный биоактивный агент является инкапсулированным во внутренней полости, или встроенным, или диспергированным в твердом ядре.
В другом аспекте изобретение также является направленным на конъюгаты липид-лиганд в соответствии с формулой I сами по себе, которые включают этер-липид, характеризующийся, по крайней мере, двумя цепями связанного с этером углеводорода и головной группой, которая имеет короткую аминокислоту с неразветвленной цепью, которая содержит вплоть до 6 атомов углерода и вплоть до трех сайтов слияния, к которым может быть ковалентно присоединен, по крайней мере, один биоактивный лиганд.
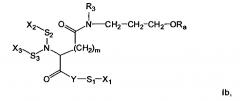
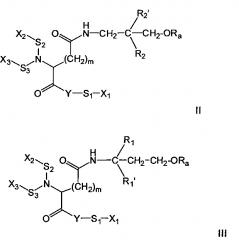
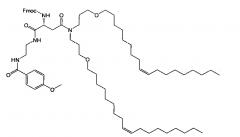
Конъюгаты липид-лиганд относятся к соединению общей формулы I
где Y представляет собой О, N, S или ковалентную связь, S1, S2, S3 представляют собой независимо друг от друга ковалентную связь или группу спейсера,
X1, Х2, Х3 представляют независимо друг от друга Н или группу лиганда, L представляет собой группу формулы (а)
где пунктирная линия представляет собой связь с N,
R1 представляет собой Н или группу формулы -(CH2)2-ORb1,
R1' представляет собой Н или группу формулы -(CH2)2-ORb2,
R2 представляет собой Н или группу формулы -СН2-ORc,
R2' представляет собой Н или группу формулы -ORd or -CH2-ORd,
R3 представляет собой Н или группу формулы -(CH2)2-ORe или
-(CH2)3-ORe,
Ra, Rb1, Rb2, Rc, Rd, Re представляют независимо друг от друга насыщенную или ненасыщенную, разветвленную или неразветвленную углеводородную цепь,
m равно1, 2 или 3,
при условии, что, по крайней мере, один из R1, R1', R2, R2', R3 не является Н и, по крайней мере, один из Х1, Х2, Х3 представляет собой группу лиганда.
В специфических воплощениях группа лиганда представляет собой нацеливающий лиганд, или антигенный лиганд, или терапевтический лиганд, или диагностический лиганд.
Предпочтительно, нацеливающий лиганд представляет собой производную птероевой кислоты, пептид или его производную, полипептид, белок или углевод, а антигенный лиганд представляет собой пептид, белок или углевод.
В дополнительном аспекте изобретение также является направленным на применения систем носителя в соответствии с изобретением в качестве системы доставки лекарственного средства, диагностической системы или системы антигенного дисплея. Также обеспечиваются наборы для получения систем носителя, которые содержат липиды в соответствии с изобретением, и фармацевтические композиции, содержащие такие системы носителя.
В других аспектах настоящее изобретение является также направленным на способы для лечения или диагностики заболевания, которые включают введение эффективного количества системы носителя в соответствии с изобретением.
В дополнительных аспектах настоящее изобретение также является направленным на способы модулирования иммунного ответа, которые включают введение эффективного количества системы носителя в соответствии с изобретением.
Другие аспекты изобретения включают способы для транспорта биологически активного соединения через мембрану и/или способы доставки биологически активного соединения в клетку при использовании системы носителя в соответствии с изобретением.
Чертежи
Фигура 1. Клеточное поглощение RGD нацеленной липосомы (которая включает 5% DMA-RGD) по сравнению с ненацеленной липосомой (которая не содержит DMA-RGD).
Фигура 2. Эксперименты по нацеливанию на легумаин при использовании декорированных RR11a липосом (MS 15-4) по сравнению с контрольными липосомами (MS 15-0) в соответствии с Примером 20:
Подробное описание изобретения
Настоящее изобретение обеспечивает системы носителя, которые включают, по крайней мере, один этер-липид и, по крайней мере, один биоактивный лиганд, конъюгированный с указанным этер-липидом с образованием конъюгата липид-лиганд в соответствии с изобретением. Любая система носителя, которая может быть состоять из или быть покрыта с помощью конъюгатов липид-лиганд общей формулы I, необязательно, в комбинации с другими соединениями липидного матрикса (или со-липидами), может действовать как система носителя в соответствии с настоящим изобретением. Типично, система носителя в соответствии с изобретением основывается на материале микрочастиц или наночастиц различной формы и различных размеров, таких как пузырьки или сферы с внутренней полостью, частицы с твердым ядром, палочковидные, кубические, частицы в виде кластеров и тому подобное. В некоторых воплощениях система носителя в соответствии с изобретением представляет собой систему на основе липидного носителя такую, как липосома, мицелла, где конъюгат липид-лиганд, необязательно, вместе с другими матриксными липидами, формирует липидную стенку везикулы. В других воплощениях система носителя в соответствии с изобретением представляет собой систему носителя на основе наночастиц, таких как наночастицы, наносферы, нанокластеры, нанотрубочки, полимерные гранулы и тому подобное, где конъюгат липид-лиганд адсорбируется, необязательно, вместе с другими матриксными липидами, в качестве покрытия на поверхности системы носителя на основе наночастиц. В зависимости от природы и предназначенного применил системы носителя в соответствии с изобретением, один или более биоактивных агентов могут быть инкапсулированы или встроены в, или присоединены к, или адсорбированы на поверхности системы носителя.
Как используется в данной заявке, термин "биоактивный" относится к способности вызывать биологический ответ, который предполагается в клетке, ткани, системе и/или у субъекта (включая человека). Термин "биологический ответ" относится к физиологической реакции клетки на стимул и, таким образом, может представлять собой любой клеточный, неврологический, химический, воспалительный, иммунологический или патологический биологический ответ, процесс или реакцию у субъекта. Ответ, процесс или реакция может быть химической, клеточной, неврологической, физиологической или подобной им. Таким образом, термин "биоактивный лиганд», или "биоактивная группа лиганда", или просто "лиганд", или "группа лиганда", как используется в данной заявке, относится к лиганду, который вызывает такой биологический ответ и который используется для ковалентного присоединения к этер-липиду общей формулы I либо непосредственно, либо с помощью группы спейсера (при использовании стандартных методик химического слияния). Биоактивный лиганд может представлять собой нацеливающий лиганд, антигенный лиганд, терапевтический лиганд или диагностический лиганд.
Термин "биоактивный агент" или просто "агент", как используется в данной заявке, относится к любому синтетическому или существующему в природе соединению (в свободной форме, форме соли, или в растворенной форме, или в гидратированной форме), который обладает биологической активностью, такому как нацеливающий агент, антигенный агент, терапевтический агент или диагностический агент, предпочтительно терапевтический агент или диагностический агент. При этом является понятным, что определения различных групп биоактивных агентов и групп биоактивных лигандов могут перекрываться.
Таким образом, выражение "нацеливающий" используется в сочетании с "агентом" или "лигандом" (для применения в системах нацеленной доставки) и относится к соединению, которое является способным к взаимодействию с комплементарным связывающим остатком в желательном положении и/или при определенных условиях. Например, комплементарные связывающие остатки могут представлять собой лиганды и анти-лиганды (например, стрептавидин и биотин, белок А или G и Fc участок иммуноглобулинов), лиганды и рецепторы (например, лиганды на основе малых молекул и их рецепторы, или взаимодействия сахар-лектин), пептиды, которые получены из фагового дисплея, комплементарные нуклеиновые кислоты (например, ДНК гибриды, РНК гибриды, ДНК/РНК гибриды, и т.д.) и аптамеры. Другие типичные комплементарные связывающие остатки включают, но без ограничения таковыми, остатки, которые демонстрируют комплементарные заряды, гидрофобность, образование водородной связи, ковалентное связывание, Ван дер Ваальсовы силы, реактивные взаимодействия, электростатические взаимодействия, магнитные взаимодействия и подобные им.
"Нацеливающий лиганд" или "нацеливающий агент", который является специфическим для определенного рецептора (рецепторный агент или лиганд), относится к любому соединению, которое представляет собой специфический партнер связывания пары специфического связывания, в которой другой партнер связывания представляет собой рецептор. Рецептор может быть присоединенным к клеточной мембране или поверхности, или может находится в растворенной форме и может присутствовать внутриклеточно и/или за пределами клетки у субъекта, предпочтительно у субъекта, который представляет собой человека, например, человека или животное. Примеры рецептора включают, но без ограничения таковыми, мембранные рецепторы, растворимые рецепторы, клонированные или рекомбинантные рецепторы, семейство CD цистеинпротеазы и другие протеазы, а также другие ферменты, гормональные рецепторы, рецепторы лекарственного средства, рецепторы трансмиттера, аутакоидные рецепторы, цитокиновые рецепторы, антитела, фрагменты антител, сконструированные антитела, миметики антител, единицы молекулярного узнавания, адгезионные молекулы, агглютинины, интегрины и селектины. Типично, связывающая аффинность рецепторного лиганда для этого рецептора может составлять, по крайней мере, 10-5 М, предпочтительно 10-7 М и более, например, от приблизительно 10-8 М до приблизительно 10-12 М. Примеры рецепторного агента или лиганда включают, но без ограничения таковыми, пептид или полипептид, включая их производные, такие как аза-пептидные производные или производные, содержащие частично или только D-аминокислоты, гликопептид и тому подобное, белок, включая гликобелок или фосфобелок, углевод, гликолипид, фосфолипид, олигонуклеотид, полинуклеотид, аптамеры, шпигельмеры, витамины (например, витамин В9 или фолиевую кислоту, витамин В12), антигены и их фрагменты, гаптены, агонисты рецепторов, частичные агонисты, смешанные агонисты, антагонисты, наркотики, хемокины, гормоны (например, LH, FSH, TRH, TSH, АСТН, CRH, PRH, MRH, MSH, глюкагон и пролактин; трансферрин, лактоферрин; ангиотензин, гистамин; инсулин, лектины), трансмиттеры, аутокоиды; ростовые факторы (например, PDGF, VEGF, EGF, TGFα, TBFβ, GM-CSF, G-CSF, M-CSF, FGF, IGF, бомбезины, тромбопоэтин, эритропоэтин, онкостатин и эндотелии 1), цитокины, включая интерлейкины (например, интерлейкины от 1 до 15), лимфокины и клеточные сигнальные молекулы, такие как факторы некроза опухоли (например, факторы некроза опухоли α и β) и интерфероны (например, интерфероны α, β и γ), простетические группы, коэнзимы, кофакторы, регуляторные факторы или любые другие существующие в природе или синтетические органические молекулы, которые специфически связываются с рецепторами, включая фрагменты, аналоги и любые другие их производные, которые сохраняют те же свойства связывания. Выбор рецепторного агента или лиганды для применения в настоящем изобретении будет определяться природой заболевания, состояния или инфекции, которые подвергаются анализу и/или лечению. Предпочтительные рецепторные агенты или лиганды включают витамины (например, фолиевую кислоту или ее фрагменты), производную птероевой кислоты, пептиды, включая их производные, такие как аза-пептидные производные, белки и углеводы. Наиболее предпочтительными являются производные птероила и пептидов, в частности, производны аза-пептидов.
Термин "птероил" или "птероевая кислота", как используется в данной заявке, представляет собой конденсированный пиримидиновый гетероцикл, который является связанным с остатком аминобензоила. Как используется в данной заявке термин "конденсированный пиримидиновый гетероцикл" включает пиримидин, слитый с дополнительным 5- или 6-членным гетероциклом, что приводит к получению птеридинового или пирролпиримидинового бицикла. Конъюгация группы птероила с одним или более реактивных сайтов на головной группе этер-липида (N- или Y-группа) будет приводить к получению структуры фолата, в которой головная группа представляет собой часть глутаминовой кислоты или ее производную. Типичные структуры фолата основываются на фолатном скелете, то есть птероил-глутаминовой кислоте, соответственно N-[4-[[(2-амино-1,4-дигидро-4-оксо-6-птеридинил)метил]амино]бензоил]-L-глутаминовой кислоте, и ее производных. Такие производные фолата включают фолаты, которые имеют необязательные заместители в реактивных или нереактивных сайтах и/или где выбранные атомы были заменены, например, выбранные гетероатомы, предпочтительно один или два, были заменены атомами углерода (такими как в деаза и дидеаза аналогах). Примеры представляют собой необязательно замещенную фолиевую кислоту, фолиновую кислоту, птерополиглутаминовую кислоту и птеридины, связывающие рецептор, такие как тетрагидроптерины, дигидрофолаты, тетрагидрофолаты и деаза и дидеаза аналоги. Фолиевая кислота, 5-метил-(6S)-тетрагидрофолиевая кислота и 5-формил-(6S)-тетрагидрофолиевая кислота представляют собой предпочтительные базовые структуры, которые используются для соединений в соответствии с изобретением. Термин "деаза" и "дидеаза" аналоги относится к области признанных аналогов, которые имеют атом углерода, замещенный одним или двумя атомами азота в существующей в природе структуре фолиевой кислоты. Например, деаза аналоги включают 1-деаза, 3-деаза, 5-деаза, 8-деаза и 10-деаза аналоги. Дидеаза аналоги включают, например, 1,5-дидеаза, 5,10-дидеаза, 8,10-дидеаза и 5,8-дидеаза аналоги. Предпочтительные соединения деаза аналогов включают N-[4-[2-[(6R)-2-амино-1,4,5,6,7,8-гексагидро-4-оксопиридо[2,3-d]пиримидин-6-ил]этил]бензоил]-L-глутаминовую кислоту (Лометрексол) и N-[4-[1-[(2,4-диамино-6-птеридинил)метил]пропил]бензоил]-L-глутаминовую кислоту (Эдатрексат). В каждой из указанных структур фолата часть глутаминовой кислоты является частью, соответствующей головной группе этер-липида и, таким образом, каждая из указанных выше структур фолата может также включать структуры, которые содержат различные производные глутаминовой кислоты, соответствующие головной группе.
Термин "пептид", как используется в данной заявке, представляет собой олигопептид, который состоит из 1 - 30, предпочтительно 2 - 20, наиболее предпочтительно 3-10 аминокислот. Пептиды типично являются соединенными с помощью своих N-концов, С-концов и/или с помощью своих боковых цепей с реактивными положениями при головной группе (то есть N- и/или Y-группы) этер-липида. Пептиды могут содержать дисульфидные мостики, а также эстерные связи. Кроме того, пептиды могут нести защитные группы на N-конце, С-конце и в боковых цепях. Термин "кислота" включает существующие в природе L-аминокислоты, D-аминокислоты, синтетические аминокислоты, бета аминокислоты и их гомологи.
Предпочтительные пептиды, как определено выше, для применения в настоящей заявке включают, например, специфические для клетки лиганды, такие как RGD-пептид, NGR-пептид, ATWLPPR-пептид, APRPG-пептид, SMSIARL-пептид, TAASGVRSMH-пептид, LTLRWVGLMS-пептид, CDSDSDITWDQLWDLMK-пептид, GPLPLR-пептид, HWGF-пептид и их производные (где обозначение пептида представлено в однобуквенном коде аминокислот), предпочтительно RGD пептид (то есть трипептид с аминокислотной последовательностью аргинин-глицин-аспарагиновая кислота или Arg-Gly-Asp) и его производные. Производные RGD пептида включают любую структурную модификацию пептида, включая пептид, содержащий RGD последовательность, а также непептидные соединения, которые включают RGD пептид.
Термин "аза-пептид", как используется в данной заявке, относится к пептидным аналогам, имеющим атом азота, который замещает один или более атомов углерода в существующей в природе структуре пептида. Аза-пептиды типично состоят из 1-30, предпочтительно 2-20, наиболее предпочтительно 3-10 аминокислот, которые имеют атом азота, который замещает, по крайней мере, один из sp3-гибридизированных атомов углерода, предпочтительно атом углерода в альфа-положении аминокислоты, наиболее предпочтительно атом углерода в альфа-положении аминокислоты на С-конце. Аза-пептиды являются соединенными с помощью своих N-концов, С-концов и/или посредством их боковых цепей с реактивными положениями в головной группе (то есть N-и/или Y-группах) этер-липида. Аза-пептиды могут содержать дисульфидные мостики, а также эстерные связи. Кроме того, аза-пептиды могут нести защитные группы на N-конце, С-конце и на своих боковых цепях. Предпочтительные аза-пептиды представляют собой производные 2-азааспарагина, такие как Cbz-аланилаланил-2-азааспарагин (который является также известным как RR11a) (Ekici и др., 2004, J. Med. Chem. 47, 1889-1892; WO 2012/031175 А9).
В других воплощениях нацеливающий агент или лиганд может также быть представленным или включать, по крайней мере, один блокирующий остаток. Как используется в данной заявке, термин "блокирующий остаток" относится к остаткам, которые маскируют, блокируют, "укрывают", и/или стерически ингибируют активность, самоузнавание и/или самосборку комплементарных связывающих остатков. Например, блокирующий остаток может блокировать способность комплементарных связывающих остатков взаимодействовать друг с другом перед желаемым состоянием или в то время, когда блокирующий остаток удаляется. Блокирующий остаток может включать полимерные соединения, такие как полаксамины; полоксамеры; полиэтиленгликоль (ПЭГ); поли(молочная-со-гликолевая кислота)(PLGA), пептиды; синтетические полимеры и тому подобное.
Как используется в данной заявке, выражение "антиген(ный)", используемый в сочетании с "агент" или "лиганд", относится к соединению, которое вызывает иммунный ответ против него или его частей. Термин "иммунный ответ" относится к узнаванию антигена или его частей иммунной эффекторной клеткой. Такой включает опосредованные Т-клетками и/или В-клетками иммунные ответы, которые подвергаются влиянию с помощью модулирования ко-стимуляции Т-клеток. Термин иммунный ответ также включает иммунные ответы, которые опосредованно подвергаются влиянию с помощью активации Т-клеток, такие как продукция антитела (гуморальные ответы) и активация других иммунных эффекторных клеток, включая, но без ограничения таковыми, моноциты, макрофаги, NK клетки и цитотоксические Т лимфоциты (CTL), например, CTL линии, CTL клоны и CTL из опухолевых, воспалительных или других инфильтратов. Определенная больная ткань экспрессирует специфические антигены, были также идентифицированы CTL для этих антигенов. Например, приблизительно 80% меланом экспрессируют антиген, который является известным как gp-100. Одна из наиболее эффективных и желательных процедур для предотвращения микробных инфекций и патогенных процессов и, таким образом, борьбы с этими заболеваниями, представляет собой вакцины, которые вызывают стимуляцию иммунного ответа в организме хозяина перед актуальной инфекцией или началом заболевания путем введения антигенов или иммуногенов в хозяйский организм.
Квалифицированному специалисту будет понятно, что любая макромолекула, включая практически любую биологическую молекулу (белки, пептиды, липиды, липопротеины, гликаны, гликопротеины, производные нуклеиновых кислот, такие как олигонуклеотиды, полинуклеотиды, геномная или рекомбинантная ДНК) могут служить в качестве антигена. Антиген может быть синтезирован химическим путем или биологическим путем, или может быть получен из рекомбинантной или геномной ДНК, или может быть получен из биологического образца, такого как образец ткани, образец опухоли, клеточная или биологическая жидкость. Антигены могут включать, но без ограничения таковыми, вирусные антигены, бактериальные антигены, грибковые антигены, антигены простейших и других паразитов, опухолевые антигены, антигены, вовлеченные в аутоиммунное заболевание, привыкание, аллергию и отторжение трансплантата, и другие многочисленные антигены. Типичные примеры антигена могут представлять собой белок или пептид бактериального, грибкового, протозойного или вирусного происхождения, или фрагменты, которые получены из этих антигенов, включающие, но без ограничения таковыми, виды Streptococcus, виды Candida, виды Brucella, виды Salmonella, виды Shigella, виды Pseudomonas, виды Bordetella, виды Clostridium, вирус Норуолк, Bacillus anthracis, Mycobacterium tuberculosis, вирус иммунодефицита человека (ВИЧ), виды Chlamydia, папилломавирусы человека, вирус гриппа, виды парамиксовируса, вирус герпеса, цитомегаловирус, вирус ветряной оспы, вирус ветряной оспы, вирус Эпштейна-Барра, вирус гепатита, виды Plasmodium, виды Trichomonas, инфекционные агенты, которые передаются половым путем, агенты вирусного энцефалита, агенты протозойных заболеваний, агенты грибковых заболеваний, агенты бактериальных заболеваний, раковые клетки или их смеси. Иммунизация субъекта может быть улучшена путем использования множественных копий антигена как мультивалентного дисплея и является желательной в случае антигенных лигандов, таких как малые пептиды или углеводы, которые являются сложными для введения и недостаточными для того, чтобы вызвать эффективный иммунный ответ по причине проблем, ассоциированных с размером гаптена. Таким образом, как используется в данной заявке, термин "мультивалентный" относится к дисплею более чем одной копии или типа антигена на системе носителя. Термин "система, которая презентирует антиген" или "система дисплея антигена", как используется в данной заявке, относится к существующей в природе или к синтетической системе, которая (i) может представлять, по крайней мере, один антиген (или его часть) таким образом, что, по крайней мере, один антиген (или его часть) может узнаваться или связываться с молекулой иммунного эффектора, например, рецептором антигена Т-клетки на поверхности Т-клетки, или (и) является способной презентировать, по крайней мере, один антиген (или его часть) в форме комплекса антиген-МНС, который способен распознаваться специфически эффекторными клетками иммунной системы, и таким образом, индуцировать эффективный иммунный ответ против антигена (или его части) который является презентированным. В контексте настоящего изобретения термин "узнаваемый" относится к (i) липидному соединению, конъюгированному, по крайней мере, с одним антигенным лигандом (или его композицией и рецептурой), который узнается и связывается с помощью иммунной эффекторной клетки, где такое связывание является достаточным для эффективного иммунного ответа, или к (ii) липидному соединению, конъюгированному, по крайней мере, с одним нацеливающим лигандом (или его композицией и рецептурой), который узнается и связывается со своим соответствующим рецептором, или к комбинации обоих (а) и (b). Анализы для определения, узнается ли нацеливающий или антигенный лиганд с помощью рецептора или иммунной эффекторной клетки, соответственно, являются известными в области техники и описываются в данной заявке.
Как используется в данной заявке, выражение "терапевтический" используется в сочетании со словом "агент" или "лиганд" и относится к соединению, которое является способным выявлять биологический эффект in vitro и/или in vivo, которое является терапевтическим по своей природе. Терапевтический лиганд может быть нейтральным или позитивно или негативно заряженным. Примеры приемлемых биоактивных агентов включают фармацевтические агенты и лекарственные средства, синтетические органические молекулы, белки, витамины, стероиды, миРНК, микроРНК, адъюванты и генетический материал.
Термин "генетический материал" в общем случает относится к нуклеозидам, нуклеотидам и полинуклеотидам, включая дезоксирибонуклеиновую кислоту (ДНК) и рибонуклеиновую кислоту (РНК). Генетический материал может быть получен с помощью методики химического синтеза, которая является известной среднему специалисту в данной области техники, или при использовании рекомбинантной методики, или при использовании комбинаций этих двух методик. ДНК и РНК могут необязательно включать неприродные нуклеотиды и могут быть одно- или двухцепочечными. "Генетический материал" также относится к смысловой или антисмысловой ДНК и РНК, то есть к нуклеотидной последовательности, которая является комплементарной специфическ