Способ получения силиката висмута bi2sio5
Иллюстрации
Показать всеИзобретение относится к области химии и может быть использовано для катализаторов для получения необходимых в промышленности газов и в синтезе высокопрочной керамики. Способ получения силиката висмута Bi2SiO5 включает предварительное механическое смешивание исходных порошков оксида висмута Bi2О3 и оксида кремния SiO2, нагрев полученной смеси в платиновом тигле до заданной температуры, при этом смешивание исходных порошков Вi2О3 и SiO2 осуществляют непосредственно в тигле не более 1 мин, а нагрев осуществляют при 1020-1200°С, затем осуществляют изотермическую выдержку в расплавленном состоянии в тигле не менее 15 мин с последующим охлаждением в печи вместе с тиглем со скоростью охлаждения не выше 15°С/мин. Технический результат заключается в получении чистого Bi2SiO5 при сокращении затрат на его получение. 4 ил.
Реферат
Способ относится к области химии и может быть использован для катализаторов, как важнейший составляющий для получения необходимых в промышленности газов, кроме того, может найти применение в синтезе высокопрочной керамики.
Известен способ получения фазы Bi2SiO5 [Xiao-Jun Dai, Yong-Song Luo, Shao-Yun Fu, Wen-Quan Chen, Yang Lu. Facile hydrothermal synthesis of 3D hierarchical Bi2SiO5 nanoflowers and their luminescent properties // Journal Solid State Sciences 12 (2010) 637-642]. Его отличие состоит в составе исходных реагентов и способе получения необходимой фазы. Для ее получения 1 моль гидратированного Na2SiO⋅H2O и 1.5 моля гидратированного Вi(NO3)3⋅5Н2O растворяют в 35 мл смешанного растворителя этанол-Н2О (объемное соотношение 5:2), содержащего 4 моля NaOH, с последующим добавлением 1 г поливинилпирролидона (PVP, К30). Полученную смесь перемешивают при помощи магнитной мешалки, чтобы обеспечить полное растворение реагента. После этого смешанный раствор переносят в 40-миллилитровой тефлоновой подкладке в автоклав и нагревают при 180°С в течение 12 ч. Затем автоклав охлаждают до комнатной температуры естественным образом. Осадки отделяют от раствора с помощью центрифуги и промывают абсолютным этанолом несколько раз. Полученные продукты собирают и сушат в течение суток при 70°С.
Предложенный авторами способ, трудно применим в промышленных условиях, состоит из множества последовательно проводимых операций с использованием специальных реактивов и сложного оборудования. Также данный способ требует значительный временных затрат - на 12-часовой синтез, охлаждение с печью, сушку «в течение ночи» и др. технологические операции. Необходимость использования автоклава, магнитной мешалки и центрифуги для отделения осадка, помимо прочего стандартного оборудования, существенно усложняют и удорожают процесс получения Bi2SiOs.
Похожий способ был предложен и в работе [Wei Wei and Jimin Xiea. Synthetic bismuth silicate nanostructures: Photocatalysts grown from silica aerogels precursors // Journal Materials Research Society., Vol. 28, No. 13, Jul 14, (2013), 1658-1668]. Здесь для получения необходимой фазы 1 моль аэрогеля диоксида кремния растворяют в объемном отношении (3:1) в 20 мл смешанного растворителя этанол-Н2О, с последующим добавлением поливинилпирролидона (PVP, K-30). Затем раствор 2 молей Вi(NO3)3⋅5Н2O, растворяют в 2 мл раствора HNO3 (4 моль/л). Полученную смесь перемешивают в течение примерно 20 минут до получения прозрачного раствора. И, наконец, значение рН раствора доводили до 9 с помощью капающей 25%-й по массе NH3⋅3H2O. После перемешивания в течение 30 минут, смесь переносили в тефлоновый автоклав емкостью 25 мл и выдерживали при 180°С в течение 12 ч. Продукт выделяли центрифугованием, промывали деионизированной водой и этанолом несколько раз, а затем сушили в вакууме при 80°С в течение 12 ч.
Способ [Wei Wei and Jimin Xiea. Synthetic bismuth silicate nanostructures: Photocatalysts grown from silica aerogels precursors // Journal Materials Research Society. Vol. 28. No. 13. Jul 14, (2013) 1658-1668], как и рассмотренный выше также требует значительный временных затрат, специальных реактивов и сложного оборудования. Он состоит из множества последовательно проводимых технологических операций, что существенно усложняет производство получаемой фазы.
Еще один способ получения данного соединения был предложен в работе [Jun-que Lu, Xiu-feng Wang, Yuan-ting Wu, Ya-qin Xu. Synthesis of Bi2SiO5 powder by molten salt method // Journal Materials Letters 74 (2012) 200-202]. В нем, в качестве исходных материалов, были использованы Bi2O3 (99,9%), SiO2 (95,55%), NaCl (99,5%) и Na2SO4 (аналитически чистый). Соотношение используемых реагентов Вi2O3/SiO2 было 1:1, а NaCl/Na2SO4 в соотношении эвтектического состава - 0,533:0,467, где температура плавления данного соединения составляет около 625°С. Весовое соотношение соли к реагентам было 2:3. Смеси реагентов и соли смешивались в шаровой мельнице в течение 5 часов в этаноле для равномерного перемешивания. После перемешивания суспензию сушили в течение ночи при 80°С для удаления этанола. Далее смесь нагревалась в алундовом тигле со скоростью 5°С/мин-1 до 625°С, с последующим воздушным охлаждением. Солевые смеси смывали теплой деионизированной водой до тех пор, пока аликвота не станет свободна от солей анионов. Оставшиеся порошки сушили при 80°С в течение ночи.
Однако при использовании данного способа [Jun-que Lu, Xiu-feng Wang, Yuan-ting Wu, Ya-qin Xu. Synthesis of Bi2SiO5 powder by molten salt method // Journal Materials Letters 74 (2012) 200-202] не достигается быстрое получение искомой фазы. Указанный способ является не только более трудоемким, в виду большего количества операций для получения нужной фазы, но еще и более длительным по времени. Введение же в расплав дополнительных компонентов в данном случае, повышает риск их остатка в готовом материале, что негативным образом может сказаться на его чистоте и свойствах.
Общий вывод по аналогам: указанные аналоги в большинстве своем требуют большого количества технологических операций с использованием дополнительных реагентов и оборудования, а также весьма длительны по времени. Это влечет за собой большие затраты, сильно усложняет и удорожает получение искомой фазы Bi2SiO5, а также существенно повышает риск загрязнения получаемого материала.
Наиболее близким по совокупности существенных признаков к предлагаемому способу является способ представлен в работе [H.W. Guo, X.F. Wang, D.N. Gao. A novel method for preparation of pure Bi2SiO5 crystals // Journal Materials Letters 67 (2012) 280-282].
В данном способе [4] аналитически чистые Вi2О3 и SiO2 вместе с абсолютным этиловым спиртом (молярное соотношение Bi2O3/SiO2 - 1:1) размалывают в течение 3 часов при комнатной температуре с использованием шариков оксида алюминия в качестве мелющих частиц (размер частиц составляет 300 mesh и 100 mesh для SiO2 частиц). Далее проводят сушку порошков при помощи инфракрасной сушки мощностью 60 Вт, а затем порошок измельчают в течение 3 часов в сухом состоянии, для достижения однородности. Данные последующего рентгеноструктурного анализа показывали наличие α- Вi2О3 и аморфного SiO2. Далее смесь помещают в платиновый тигель и нагревают в электрической печи от комнатной температуры до 900°С со скоростью нагрева 10°С/мин и выдерживают при данной температуре в течение часа. Под воздействием высокой температуры расплав выдерживают при 805.3°С в течение определенного времени, а затем охлаждают до комнатной температуры со скоростью линейного изменения скорости для получения чистых кристаллов Bi2SiO5.
Однако при использовании данного способа [4] не достигается быстрое получение чистой фазы Bi2SiO5 в виду:
1. большего количества операций, затрачиваемых на получение конечного продукта;
2. больших временных затрат, требуемых на данные операции;
3. использование специализированных мельниц и смачивающих веществ, что в совокупности не только существенно увеличивают время синтеза, но и повышают вероятность загрязнения конечного продукта посторонними веществами.
Основная задача изобретения состоит в повышении эффективности процесса получения чистого силиката висмута с формулой Bi2SiO5, а также снижения временных затрат на его получение.
Для достижения поставленной задачи, заявляемый «Способ получения силиката висмута с формулой Bi2SiO5» содержит следующую совокупность существенных признаков, сходных с прототипом:
1. использование одинаковых по своему химическому составу исходных реагентов (оксидов висмута и кремния в пропорции 50:50 мол. %);
2. проведение процесса плавления в платиновых тиглях.
По отношению к заявляемому способу указанный прототип имеет следующие отличительные признаки и недостатки:
1. способ, указанный в прототипе, отличается тем, что идет в 5 стадий, в то время как заявляемый - позволяет получать готовый материал простым охлаждением из расплава (всего одна стадия) и не требует никаких последующих операций, что существенно снижает время синтеза;
2. в прототипе используется специальное мелющее и сушильное оборудование, в то время как в заявляемом способе этого не требуется. Аморфный оксид кремния великолепно растворяется в расплавленном оксиде висмута, поэтому смысла в длительном смешивании исходных реагентов перед синтезом нет. Для их смешивания вполне достаточно обычной ложки-мешалки, для предварительного перемешивания прямо в тигле. Предварительное смешивание в тигле исключает возможность загрязнения исходных реагентов посторонними веществами, а время перемешивания не более 1 мин является вполне достаточным. Следовательно, и введение специальных растворителей, а также мелющих веществ, облегчающих перемалывание оксидов и несущих опасность их загрязнения, с их последующей сушкой - является нецелесообразным;
3. в прототипе используется низкая температура сплавления исходных реагентов -900°С. Если посмотреть на стабильную диаграмму состояния системы Bi2O3-SiO2, то будет видно, что данная температура лежит между ликвидусом и солидусом, а следовательно, при ней в самом начале синтеза будет плавиться только оксид висмута, который, благодаря своей исключительной растворяющей способности в жидком состоянии будет активно взаимодействовать с твердым оксидом кремния. Именно поэтому авторы и проводят столь долгое механическое смешивание исходных реагентов, обеспечивая тем самым, по сути, их предварительную механоактивацию перед плавлением. В предложенном же способе используется несколько более высокий диапазон температур: 1020-1200°С. Однако его использование позволяет существенно сократить время на подготовительные операции, в заявляемом способе около 10 минут. В прототипе подготовительные операции составляют более 7 часов.
4. финальная выдержка при 805.3°С, время которой авторами не было указано в данной работе, является ничем иным как твердофазным синтезом, т.к. жидкого состояния в данной системе при этой температуре быть не может. Твердофазный синтез, сам по себе, является весьма длительным процессом, что опять же существенно удлиняет и без того длительный процесс получения Bi2SiO5, указанный в прототипе.
Между отличительными признаками и решаемой задачей существует следующая причинно следственная связь:
1. снижение количества операций - существенно снижает временные и экономические затраты на производство данного химического соединения;
2. отказ от применения дополнительного оборудования - также существенно снижает временные и экономические затраты на производство данного химического соединения;
3. более высокие температуры синтеза - существенно снижают временные и энергетические затраты на производство Bi2SiO5, т.к. указанный в заявляемом способе температурный диапазон, хоть немного и превышает заявленный в прототипе, однако дает огромный выигрыш по времени, а следовательно и в затрачиваемых энергетических ресурсах;
4. заявляемый способ не требует никаких дополнительных выдержек после сплавления.
Выбор граничных параметров охлаждения обусловлен тем, что ключевым фактором при получении фазы Bi2SiO5 является именно скорость охлаждения расплава. Диоксид кремния (SiO2) является элементом, обладающим высокими стеклообразующими свойствами и превосходит по этому параметру даже диоксид германия (GeO2). При высоких содержаниях диоксида кремния в Вi2О3 при быстром охлаждении происходит активное стеклование в синтезируемом материале с получением в итоге аморфной структуры. Именно поэтому при синтезе метастабильной фазы состава 50:50 мол. %, главную роль будет играть именно скорость охлаждения расплава. Нами было установлено, что при высоких скоростях охлаждения, например таких, как закалка в воду (450-1000°С/сек), получаемый материал активно стеклуется и становится аморфным. Более медленные режимы охлаждения, как, например, охлаждение на воздухе (15-200°С/мин), приводят лишь к частичному стеклованию, в результате чего, получается смесь из стекла, Bi2SiO5 и других фаз. И только медленное охлаждение с печью (1-15°С/мин) позволяет надежно получить чистое соединение с формулой Bi2SiO5.
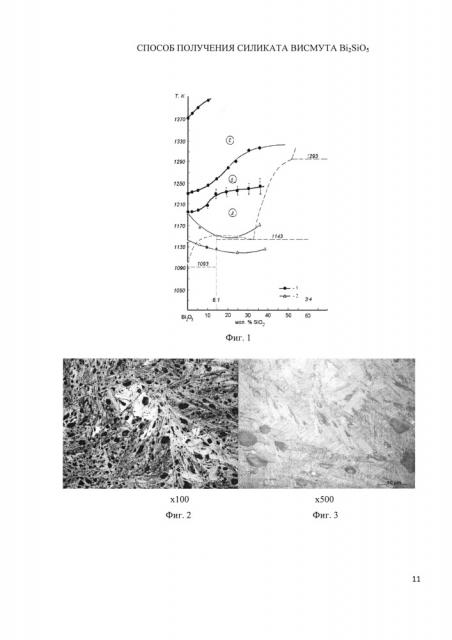
Выбор интервала температур (1020-1200°С) призван показать, что вне зависимости от температурной зоны, из которой ведется охлаждение, соблюдая необходимую скорость охлаждения, мы все равно будет получать требуемую метастабильную фазу - Bi2SiO5. Известно [Каргин В.П. Жереб В.П., Скориков В.М. Стабильное и метастабильное равновесия в системе Вi2O3-SiO2 // Журнал неорганической химии. 1991. Т. 36. №10. С. 2611-2616], что на фазовой диаграмме системы Вi2О3 - SiO2 область расплава может быть разделена на 3 температурные зоны А, В и С (фиг. 1). Исходя из представленной на фиг. 1 фазовой диаграммы [5], для состава 50:50 мол. % актуальными являются только две температурные зоны - В и С. Нами было установлено, что при охлаждении расплава с печью в указанном скоростном диапазоне всегда образуется соединение Bi2SiO5, вне зависимости от температурной зоны из которой ведется охлаждение. Также он демонстрирует и то, что именно при температуре выше ликвидуса стабильной системы, т.е. при плавлении, мы можем быстро получать необходимое нам соединение. Это объясняется тем, что в расплавленном состоянии взаимодействие исходных компонентов идет намного быстрее, чем лишь при частичном плавлении и, тем более, - при твердофазном синтезе.
Выбор граничных параметров выдержки при заданной температуре (не менее 15 минут) должен обеспечивать полное растворение SiO2 в расплаве Вi2О3 с взаимодействием компонентов друг с другом. Расплавленный оксид висмута чрезвычайно химически активное соединение, которое взаимодействует практически со всеми материалами. Поэтому длительное время выдержки для синтеза данной фазы не требуется и ограничивается, в зависимости от массы навески, т.к. на прогрев большего количества вещества требуется более длительное время. Слишком долгое время выдержки, например, нагрев, свыше двух часов и до более высоких температур является нецелесообразным из-за значительных энергозатрат и химической активности расплава.
Способ иллюстрируется графически, где на Фиг.1 - Температурные зоны 1 в области расплава на фазовой диаграмме стабильного равновесия 2 системы Вi2О3 - SiO2.. На фиг. 1 изображена двойная диаграмма стабильного равновесия системы Вi2О3 - SiO2, содержащей температурные зоны расплавов. Известно, что на фазовой диаграмме системы Вi2О3 - SiO2 область расплава может быть разделена на 3 температурные зоны А, В и С.
На Фиг. 2 - Результаты микроструктурного анализа образца, состава 1:1 мол. % (система Вi2О3 - SiO2), полученного заявляемым способом, увеличение - 100 крат;
На Фиг. 3 - Результаты микроструктурного анализа образца, состава 1:1 мол. % (система Вi2О3 - SiO2), полученного заявляемым способом, увеличение - 500 крат;
На Фиг. 4 - Результаты рентгенофазового анализа образца состава 1:1 мол. % (система Вi2О3 - SiO2), полученного заявляемым способом.
Сущность изобретения поясняется диаграммой, а также результатами рентгенофазового и микроструктурного анализа.
Нами было установлено, что при охлаждении расплава с печью в указанном скоростном диапазоне всегда образуется соединение Bi2SiO5, вне зависимости от температурной зоны из которой ведется охлаждение. Также он демонстрирует и то, что именно при температуре выше ликвидуса стабильной системы, т.е. при плавлении, мы можем быстро получать необходимое нам соединение. Это объясняется тем, что в расплавленном состоянии взаимодействие исходных компонентов идет намного быстрее, чем лишь при частичном плавлении и тем более при твердофазном синтезе.
Полученные данные подтверждаются микроструктурным анализом (фиг. 2-3), на котором ясно видно однофазное строение полученного материала в виде длинных, имеющих определенную ориентацию зерен. Существование именно однофазной области с формулой Bi2SiO5 без каких либо посторонних примесей и других фаз подтверждает также рентгенофазовый анализ, приведенный на фиг. 4.
По результатам анализов, представленным в фиг. 2-4, можно сделать вывод о том, что решающую роль при синтезе фазы Bi2SiO5 играет скорость охлаждения расплава. При быстром охлаждении расплава из В и С - температурных зон, происходит активное стеклование из-за большого содержания диоксида кремния, и чем выше будет скорость охлаждения, тем большую массу материала будет занимать аморфное состояние. Поэтому именно медленное охлаждение с печью препятствует аморфизации и обеспечивает надежное получение Bi2SiO5.
Заявляемый способ «Способ получения силиката висмута Bi2SiO5 может быть реализован с помощью следующих материальных объектов:
1. печь - нагревательное устройство с рабочей камерой, обеспечивающее нагревание материала до заданной температуры в интервале (1020-1200°С);
2. платиновый тигель;
Пример конкретного выполнения:
1. в качестве исходных компонентов берем порошки полуторного оксида висмута (Вi2О3) и диоксида кремния (SiO2) в соотношении 50:50 мол. %;
2. исходные реагенты помещаем в платиновый тигель и перемешиваем платиновым шпателем или металлической ложкой;
3. нагреваем полученную смесь до температур, указанных в формуле изобретения, ориентируясь по фазовой диаграмме системы Bi2O3-SiO2 (фиг. 1), например, 1100°С;
4. выдерживаем, например, один час;
5. полученную смесь охлаждаем вместе с печью, не вынимая из тигля; 6. извлекаем полученное чистое вещество Bi2SiO5 из тигля.
Как показали результаты опытной проверки, при использовании заявляемого способа обеспечивается достижение следующих результатов:
1. получен чистый силикат висмута с формулой Bi2SiO5;
2. удалось существенно повысить эффективность процесса получения силиката висмута с формулой Bi2SiO5, а также значительно снизить временные затраты на его получение.
Способ получения силиката висмута Bi2SiO5, включающий предварительное механическое смешивание исходных порошков оксида висмута Bi2O3 и оксида кремния SiO2, нагревание полученной смеси в платиновом тигле до заданной температуры, отличающийся тем, что смешивание исходных порошков оксида висмута Bi2O3 и оксида кремния SiO2 осуществляют непосредственно в тигле не более 1 мин, а нагрев осуществляют при 1020-1200°C, затем изотермическая выдержка в расплавленном состоянии в тигле не менее 15 мин с последующим охлаждением в печи вместе с тиглем со скоростью охлаждения не выше 15°C/мин.