Композиции и способы для лечения злокачественной опухоли
Иллюстрации
Показать всеГруппа изобретений относится к медицине и может быть использована для лечения пациента, у которого диагностирована злокачественная опухоль, ассоциированная с киназой WEE1. Для этого пациенту проводят измерение уровня экспрессии гена PKMYT1 в биологическом образце, содержащем злокачественные клетки, полученном от указанного пациента, и в контрольном образце. После чего определяют, является ли уровень экспрессии гена PKMYT1 в указанном образце от пациента более высоким или более низким, чем уровень экспрессии в указанном контрольном образце. Затем проводят отбор указанного пациента для лечения ингибитором WEE1, если уровень PKMYT1 из образца пациента является более низким, чем в контрольном образце. И выбранному пациенту для лечения злокачественной опухоли вводят ингибитор WEE1. Также предложен способ лечения пациента со злокачественной опухолью, ассоциированной с киназой WEE1, где пациенты характеризуются низкими уровнями экспрессии PKMYT1. Группа изобретений обеспечивает лечение злокачественной опухоли у пациентов с низкими уровнями экспрессии PKMYT1. 3 н. и 10 з.п. ф-лы, 20 ил., 9 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в целом, относится к идентификации биомаркера, уровень экспрессии которого является пригодным для прогнозирования ответа пациента на лечение антипролиферативным средством, в частности, ингибитором WEE1. Уровень экспрессии биомаркера можно использовать для прогнозирования у пациента наличия злокачественного заболевания, которое опосредуется ингибированием апоптоза, и у которого вероятен ответ на лечение ингибитором WEE1.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Многие общепринятые лекарственные средства против злокачественной опухоли неспецифично нацелены на ДНК в делящихся клетках и, в конечном счете, вызывают повреждение ДНК. Это, в свою очередь, запускает активацию точек контроля клеточного цикла, которая останавливает прогрессирование клеточного цикла (в фазы G1, S или G2/M) с целью обеспечения времени для репарации ДНК перед тем, как клетка подвергнется репликации или делению ДНК. С терапевтической точки зрения, ингибирование киназ точки контроля, которые опосредуют остановку клеточного цикла, может вынудить опухолевые клетки продолжить клеточное деление перед репарацией химически вызванного повреждения ДНК, в конечном счете, вызывая апоптоз или нарушение митоза (Medema, R.H. and Macurek, L., Oncogene, 2012, 31(21):2601-2613). Исследования на линиях клеток подтверждают эту гипотезу и демонстрируют хемосенсибилизацию и радиосенсибилизацию при фармакологическом или генетическом прерывании активности киназ точки контроля, включая CHK1, WEE1, ATR и ATM. Ингибиторы этих киназ находятся на различных стадиях доклинической и клинической разработки ввиду их способности сенсибилизировать опухолевые клетки к терапевтическому повреждению ДНК.
Киназа WEE1 точки контроля катализирует ингибиторное фосфорилирование как CDK1 (CDC2), так и CDK2 на тирозине 15 (Parker, L. L. and Piwnica-Worms, H., Science, 1992, 257(5078):1955-1957; Watanabe, N., et al., Embo J., 1995, 14(9):1878-1891). WEE1-зависимое ингибирование CDK1 и CDK2 останавливает клеточный цикл в ответ на вызванное извне повреждение ДНК (Hamer, P.C.D., et al., Clin. Cancer Res., 2011, 17(13):4200-4207). Активность WEE1 также существенна для ненарушенного клеточного цикла (Mcgowan, C.H. and Russell, P., Embo J., 1993, 12(1):75-85; Tominaga, Y., et al., Intl. J. Biol. Sci., 2006, 2(4):161-170). Исследование синхронизации клеток в нормальных фибробластах человека выявило, что сходные количества белка WEE1 выявляются как в S-фазе, и в фазах G2/M, однако наибольшей его активность является в фазе S клеточного цикла (Watanabe, N., 1995). Кроме того, после кондиционального нокаута WEE1 в эмбриональных фибробластах мыши (MEF) клетки демонстрируют признаки геномной нестабильности, нарушения функций точек контроля и преждевременного митоза (Tominaga, et al., 2006). Этот фенотип был частично объяснен последними данными, которые демонстрируют ключевую роль WEE1 в синтезе ДНК. Нокдаун WEE1 в отсутствие агентов, повреждающих ДНК, приводил к быстрому и стабильному обнаружению двунитевых разрывов ДНК, в частности, в клетках в S-фазе, подвергающихся репликации ДНК (Beck, H., et al., J. Cell Biol., 2010, 188(5):629-638; Dominguez-Kelly, R., et al., J. Cell Biol., 2011, 194(4):567-579). Данные свидетельствуют в пользу модели WEE1-зависимой геномной устойчивости, при которой нокдаун или ингибирование WEE1 ведет к аберрантно высокой активности CDK1 и 2, что приводит к несвоевременному запуску избыточных ориджинов репликации ДНК, который быстро истощает количества нуклеотидов и приводит к застреванию репликационных вилок, которые, в отсутствие активности WEE1, являются субстратами для ДНК-эндонуклеаз и вызывают двунитевые разрывы ДНК (Beck, H., et al., 2012).
Полагают, что нарушение регуляции экспрессии или активности WEE1 является отличительным признаком патологии при нескольких типах злокачественной опухоли. WEE1 часто сверхэкспрессируется в глиобластомах, и его активность защищает этот тип опухолей от нарушения митоза, так что высокие уровни WEE1 ассоциируют с неблагоприятным прогнозом (Mir, S.E., et al., Cancer Cell, 2010, 18(3):244-257). Высокая экспрессия WEE1 была обнаружена при злокачественной меланоме, и она коррелировала с низкой выживаемостью без признаков заболевания в этой популяции (Magnussen, G.I., et al., Plos One, 2012, 7(6)). Аберрантная экспрессия WEE1 вовлечена в другие типы опухолей, такие как печеночно-клеточная карционома (Masaki, T., et al., Hepatology, 2003, 37(3):534-543), рак молочной железы (Iorns, E., et al., Plos One, 2009, 4(4)), карцинома ободочной кишки (Backert, S., et al., Intl., J. Cancer, 1999, 82(6):868-874)), карцинома легкого (Yoshida, T., et al., Annals of Oncology, 2004, 15(2):252-256) и плоскоклеточная карцинома головы и шеи (Wu, Z.X., et al., Mol. & Cell. Proteomics, 2011, 10(12)). Для развернутых опухолей с повышенным уровнем геномной нестабильности могут требоваться функциональные точки контроля, чтобы обеспечить возможность репарации такого летального повреждения ДНК. В сущности, WEE1 представляет собой привлекательную мишень при развернутых опухолях, при которых, как полагают, его ингибирование будет приводить к нерепарируемому повреждению ДНК (Sorensen, C.S. and Syljuasen, R.G., Nuc. Acids Res., 2012, 40(2):477-486).
Существует потребность в биомаркерах, которые можно использовать для прогнозирования того, какие пациенты будут поддаваться лечению специфическими способами лечения, в частности, для пациентов, которые не отвечают на лечение или у которых имеется вероятность развития устойчивости к способам терапии первой линии. Поэтому, целью настоящего изобретения является предоставление прогностического биомаркера для отбора пациентов, которые, вероятно, будут отвечать на лечение ингибитором WEE1.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение в целом относится к идентификации прогностического биомаркера, уровень экспрессии которого является пригодным для оценки и классификации пациентов в отношении лечения ингибитором WEE1. В одном варианте осуществления изобретения прогностический биомаркер, PKMYT1, используют для идентификации пациентов с вероятностью ответа на лечение ингибитором WEE1, причем ингибитор WEE1 представляет собой WEE1-1. В другом варианте осуществления изобретение относится к способу лечения пациента, у которого диагностирована злокачественная опухоль, ассоциированная с WEE1, ингибитором WEE1, где злокачественные клетки указанного пациента характеризуются низкой экспрессией PKMYT1. В еще одном варианте осуществления изобретение относится к способу лечения пациента со злокачественной опухолью, который является чувствительным к лечению ингибитором WEE1, где злокачественные клетки указанного пациента характеризуются уровнем экспрессии PKMYT1, который является меньшим, чем эталонная величина. В другом варианте осуществления изобретение относится к способу идентификации ингибиторов WEE1 для применения при лечении злокачественной опухоли, ассоциированной с киназой WEE1. В еще одном варианте осуществления изобретение относится к набору для идентификации пациентов с вероятностью ответа на лечение ингибитором WEE1, содержащему реагенты, взаимодействующие с PKMYT1.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 показано графическое представление прерывания пролиферации клеток в различных опухолевых клеточных линиях ингибитором WEE1. Пролиферацию в течение 96-часового интервала анализировали в трех повторениях для 522 линий злокачественных клеток с обработкой посредством титрования WEE1-1 из 9 точек. Данные ответа клеточных линий разделены с учетом ткани, из которой они происходят, и представлены в виде фракционной жизнеспособности (относительно обработанных DMSO контрольных клеток)) в зависимости от концентрации WEE1-1.
На фиг.2A и 2B представлены иллюстрации повреждения ДНК в S-фазе в результате обработки ингибитором WEE1, где клетки ES-2, A2058, A431, A427, KNS62 и NCI-H460 обрабатывали или DMSO (-), или возрастающими концентрациями WEE1-1 в течение 2 часов. Белковые лизаты анализировали вестерн-блоттингом с антителами против фосфорилированной CHK1S345, фосфорилированной CDK1Y15, фосфорилированной CDK1T14 или актина в качестве нагрузочного контроля (фиг.2A). Клетки TOV-21G обрабатывали DMSO или 150 нМ WEE1-1 в течение периода до 2 или 6 часов (фиг.2B). Клетки импульсно метили за один час до сбора посредством BrdU для мечения клеток в S-фазе, активно подвергающихся репликации ДНК. Клетки анализировали проточной цитометрией для выявления двунитевых разрывов ДНК (γH2AX) относительно общего содержания ДНК (фиг.2B, левые панели) или γH2AX относительно захвата BrdU (фиг.2B, правые панели). Процентная доля клеток с окрашиванием γH2AX отображает клеточную популяцию, содержащую двунитевые разрывы ДНК, и она указана для каждого условия обработки и разделена по статусу BrdU на правых панелях.
На фиг.3A-3C представлены иллюстрации замедления прогрессирования S-фазы в результате обработки ингибитором WEE1. Клетки ES-2 синхронизировали через 36 часов после взятия сыворотки. На фиг.3A и 3B, клетки стимулировали для возобновления цикла посредством 20% FBS в присутствии добавленного либо носителя (DMSO) на дорожках 1-6, либо 500 нМ WEE1-1 на дорожках 7-11. Указано время сбора после стимуляции FBS. За один час до сбора клетки импульсно метили посредством BrdU, и процент клеток с окрашиванием BrdU представлен на верхней панели. Белковые лизаты из параллельно обработанных клеток ES-2 собирали, а затем проводили вестерн-блоттинг с указанными антителами. По сравнению с обработанным носителем контролем, обработка WEE1-1 задерживает прохождение через S-фазу (фиг.3A, верхняя панель, и фиг.3B) и захват BrdU в S-фазе (фиг.3A, верхняя панель), указывая на замедление репликации ДНК. Обработка WEE1-1 задерживает экспрессию циклина A и индуцирует передачу сигналов о повреждении ДНК, о чем свидетельствует pChk1S345 (фиг.3A, нижняя левая панель). На фиг.3B представлены результаты проточно-цитометрического анализа в выбранных образцах (обработки через 4, 12 и 24 часа) из части A, сравнивающий окрашивание BrdU и содержание ДНК. Данные на фиг.3C иллюстрируют лишенные сыворотки клетки ES-2, к которым были добавлены 500 нМ WEE1-1 либо в присутствии, либо в отсутствие 20% FBS. Через двадцать четыре часа содержание ДНК и γH2AX (двунитевые разрывы ДНК) анализировали проточной цитометрией. Процентные доли общей популяции клеток представлены на диаграмме (фиг. 3C), демонстрируя, что WEE1-1 индуцирует двунитевые разрывы ДНК в большем количестве клеток, когда популяцию стимулируют 20% FBS.
Фиг.4A и 4B иллюстрируют, что преждевременный митоз не обязательно индуцирует цитотоксичность при ингибировании WEE1. Клетки A2058, HT-29 и LoVo обрабатывали в течение 24 часов или DMSO (-WE1-1), или WEE1-1 при концентрациях лекарственного средства, представляющих собой EC90. Проточную цитометрию использовали для идентификации популяции клеток, положительных по маркеру митоза - фосфорилированному гистону H3 (pHH3S10, фиг.4A) или маркеру двунитевых разрывов ДНК - γH2AX (фиг.4B). На верхней панели рамка справа указывает ожидаемую митотическую популяцию (содержание ДНК 4N), и окно слева указывает на клетки, положительные в отношении pHH3 с содержанием ДНК менее чем 4N.
Фиг.5A-5D представляют собой иллюстрации эффективности in vivo лечения одним средством WEE1-1, при котором мышам, имеющим ксенотрансплантат A427, вводили либо носитель (0,5% метилцеллюлоза), либо 60 мг/кг WEE1-1. Введение как носителя, так и соединения проводили по схеме BID в течение 28 последовательных суток. Объемы ксенотрансплантатов опухолей определяли дважды в неделю и наносили на график (средний объем -/+ SEM) против количества суток лечения для мышей, которым вводили носитель (n=10) и WEE1-1 (n=10) (фиг.5A). На фиг.5B представлен нанесенный на график конечный объем опухолей индивидуальных ксенотрансплантатов A427 после введения в течение 28 суток либо носителя, либо MK-1775. Средний объем опухоли в начале исследования составлял 164 мм3, и он указан пунктирной линией. На фиг.5C и 5D проиллюстрированы дополнительные исследования эффективности in vivo, проведенные на моделях с ксенотрансплантатами SK-MES-1 (C) и LoVo (D), как описано для фиг. 5A, за исключением того, что введение WEE1-1 прекращали на 13-ые сутки в исследовании ксенотрансплантата LoVo (указано звездочкой), и объемы опухолей измеряли в течение дополнительных 2 недель.
На фиг.6A и 6B проиллюстрировано, что нокдаун PKMYT1 селективно повышал чувствительность к WEE1-1 и снижал ингибиторное фосфорилирование CDK1. На фиг.6A проиллюстрировано, что нокдаун PKMYT1 происходил в двух линиях клеток, которые проявляют относительную устойчивость к WEE1-1: H460 и KNS62. Клетки трансфицировали совокупностями миРНК (siRNA), содержавшими ненацеленные контрольные (CT) последовательности или последовательности PKMYT1. Клетки обрабатывали WEE1-1, карбоплатином, ингибитором MEK (PD0325901) или доксорубицином в течение 72 часов перед анализом для выявления пролиферации с помощью анализа ATP ViaLight. Нокдаун PKMYT1 снижал EC50 пролиферации в случае WEE1-1 отдельно, но не в случае других исследованных соединений. На фиг.6B клетки KNS62 трансфицировали совокупностью ненацеленных контрольных (CT) миРНК или миРНК PKMYT1, и обрабатывали 400 нМ WEE1-1 в течение указанных периодов времени.
На фиг.7A и 7B проиллюстрировано, что низкая экспрессия PKMYT1 повышала чувствительность к WEE1-1. На фиг.7A, относительную экспрессию PKMYT1 (база данных CCLE, Broad-Novartis) наносили на график против ответа на обработку 400 нМ WEE1-1 305 линий клеток, каждая из которых представлена единичной точкой. Ответ на WEE1-1 (ось x) представляет собой величину с внесенной поправкой на основании анализа пролиферации в течение 96 часов, где величина 1 указывает на отсутствие изменений в скорости роста относительно клеток, обработанных DMSO, а величина 0,25 (вертикальная пунктирная линия) или менее указывает на отрицательную скорость роста или гибель клетки. Средняя относительная экспрессия PKMYT1 среди 305 линий клеток составляет 413. На фиг.7B проиллюстрирован пролиферативный ответ на WEE1-1, измеренный в величинах EC50 (мкМ), нанесенных на график против относительной экспрессии мРНК PKMYT1 (левая панель) или белка PKMYT1 (правая панель) для тринадцати линий клеток, не включенных в анализ на фиг.7A, выше.
На фиг.8A и 8B проиллюстрировано, что ингибирование WEE1 посредством WEE1-1 приводит к увеличенной активности CDK1 и 2. Клетки ES-2 обрабатывали в течение 24 часов либо DMSO, или 250 нМ WEE1-1, собирали и лизировали для анализа с использованием вестерн-блоттинга. На фиг.8A лизаты исследовали с помощью индивидуальных антител против субстрата WEE1 (pCDK1Y15), маркера DDR (pCHK1S345) или субстратов CDK1 и 2 (pStathminS38 и pLaminA/CS22, соответственно). На фиг.8B лизаты исследовали с помощью антитела к мотиву общего субстрата CDK.
На фиг.9A и 9B проиллюстрировано, что повреждение ДНК, индуцированное обработкой WEE1-1, требует митогенной стимуляции. Клетки ES-2 лишали сыворотки в течение 36 часов, и в это время их либо оставляли не стимулированными, либо обрабатывали 20% FBS. Клетки, культивированные в обоих условиях, обрабатывали либо DMSO, либо 500 нМ WEE1-1 в течение 24 часов перед сбором для проточно-цитометрического анализа содержания ДНК (7-AAD) и двунитевых разрывов ДНК (γH2AX). На фиг.9A проиллюстрирована гистограмма для распределения клеточного цикла. На фиг.9B проиллюстрирован график разброса данных для окна, которое указывает на популяцию γH2AX. Процентная доля всех клеток указана либо в фазе клеточного цикла, либо в качестве γH2AX-положительных клеток.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Многие способы лечения злокачественной опухоли действуют посредством повреждения ДНК, которое впоследствии инициирует ответ на повреждение ДНК (DDR) и активирует киназы точки контроля для остановки деления, в то время как происходит репарация ДНК. Тирозинкиназа WEE1 активируется посредством DDR, фосфорилируя и ингибируя циклинзависимые киназы (CDK) 1 и 2, и, в сущности, останавливает деление клеток. Ингибирование WEE1 усиливает повреждающие ДНК способы лечения путем предотвращения остановки клеточного цикла и должной репарации ДНК.
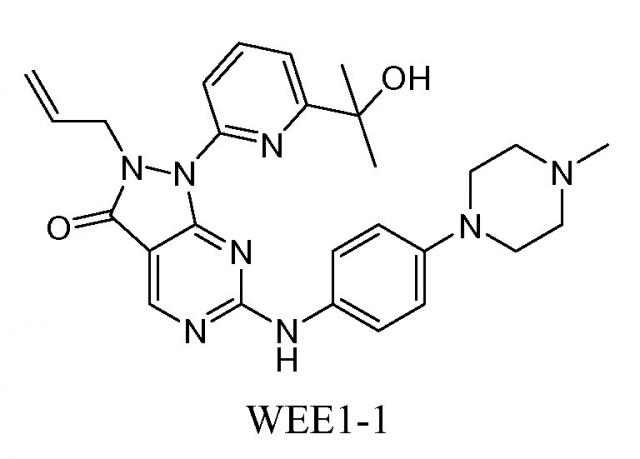
WEE1-1, также известный как 2-аллил-1-[6-(1-гидрокси-1-метилэтил)пиридин-2-ил]-6-{[4-(4-метилпиперазин-1-ил)фенил]амино}-1,2-дигидро-3H-пиразоло[3,4-d]пиримидин-3-он, представляет собой сильнодействующий (IC50=5,2 нМ) и селективный конкурирующий с ATP низкомолекулярный ингибитор WEE1 (Hirai, H., et al., Mol. Cancer Ther., 2009, 8(11):2992-3000), который в настоящее время находится на стадии клинической разработки в качестве противоопухолевого средства в комбинации с химиотерапевтическими средствами, применяемыми в стандарте лечения (SOC) (Stathis, A. and Oza A., Drug News & Perspectives, 2010, 23(7):425-429; Schellens, J.H.M., et al., J. Clin.Oncol., 2011, 29:2011 (suppl; abstr 3068); Mizuarai, S., et al., Mol. Cancer, 2009, 8:34). Предшествующие исследования WEE1-1 продемонстрировали его потенциал в качестве вспомогательного средства или сенсибилизатора для химиотерапевтических средств, применяемых в стандарте лечения (SOC), ввиду его способности принудительно вызывать незапланированный митоз, который, в конечном счете, приводит к апоптозу или нарушению митоза (Hirai, H., et al., Cancer Biol. & Ther., 2010, 9(7):514-522; Aarts, M., et al., Cancer Discovery, 2012, 2(6):524-539; Indovina, P. and Giordano A., Cancer Biol. & Ther., 2010, 9(7);523-525; Wang, Y.L., et al., Cancer Biol. & Ther., 2004, 3(3):305-313). Однако потенциальный терапевтический эффект ингибирования WEE1 в отсутствие химиотерапии SOC является в меньшей степени определенным. Нокдаун WEE1 с помощью РНК-i ингибировал пролиферацию линий клеток злокачественной опухоли (Iorns, E., et al., Cancer Targets, 2009, Plos One, 4(4); Murrow, L.M., et al., Breast Cancer Research and Treatment, 2010, 122(2):347-357), и недавно было продемонстрировано, что WEE1-1 отдельно может индуцировать апоптоз в линиях клеток саркомы, обработанных in vitro (Kreahling, J.M., et al., Mol. Cancer Ther., 2012, 11(1):174-182).
Заявители демонстрируют в настоящем описании, что фармакологическое ингибирование только WEE1 посредством применения WEE1-1 в качестве единственного средства является цитотоксичным для широкого диапазона линий опухолевых клеток и активно индуцирует двунитевые разрывы ДНК. Примечательно, что WEE1-1 индуцировал повреждение ДНК, происходящее в S-фазе, которое было независимым от химиотерапии SOC или лучевой терапии, и в основе которого лежала активная репликация ДНК. При переносимых дозах, монотерапия WEE1-1 приводила к ингибированию или регрессии роста ксенотрансплантата опухоли. Нокдаун PKMYT1 - киназы, функционально связанной с WEE1, селективно сенсибилизровал раковые клетки к WEE1-1, но не сенсибилизровал их к другим цитотоксическим средствам. Как описано в настоящем описании, экспрессия PKMYT1 была ниже средней приблизительно в трех четвертях линий раковых клеток, в наибольшей степени отвечающих на WEE1-1. Выбор линий клеток, которые имели низкую экспрессию PKMYT1, являлся прогностическим для чувствительности этих линий клеток к WEE1-1 in vitro. Взятые вместе, эти данные обеспечивают основание для применения ингибирования WEE1 в качестве сильнодействующего средства терапии против злокачественной опухоли, и использования низкой экспрессии PKMYT1 для идентификации и отбора пациентов, которые с наибольшей вероятностью будут отвечать на монотерапию WEE1-1.
Соответственно, настоящее изобретение относится к способам лечения злокачественной опухоли ингибитором WEE1, где ингибитор WEE1 представляет собой WEE1-1 или его фармацевтически приемлемую соль, или WEE1-2 или его фармацевтически приемлемую соль. В другом варианте осуществления изобретение относится к прогностическому биомаркеру PKMYT1, экспрессия которого чувствительна к ингибированию WEE1 ингибитором WEE1. В еще одном варианте осуществления изобретение относится к способу лечения пациента, у которого диагностирована злокачественная опухоль, ассоциированная с киназой WEE1, нуждающемуся в его лечении, ингибитором WEE1, где злокачественные клетки указанного пациента характеризуются низкой экспрессией PKMYT1, и где указанный ингибитор WEE1 представляет собой WEE1-1 или его фармацевтически приемлемую соль, или WEE1-2 или его фармацевтически приемлемую соль. В еще одном варианте осуществления изобретение относится к способу лечения пациента со злокачественной опухолью, который является чувствительным к лечению ингибитором WEE1, где злокачественные клетки указанного пациента характеризуются уровнем экспрессии PKMYT1, который ниже эталонной величины, и где указанный ингибитор WEE1 представляет собой WEE1-1 или его фармацевтически приемлемую соль, или WEE1-2 или его фармацевтически приемлемую соль. В другом варианте осуществления изобретение относится к способу идентификации ингибиторов PKMYT1 для применения при лечении злокачественной опухоли, ассоциированной с киназой WEE1. В еще одном варианте осуществления изобретение относится к набору для идентификации пациентов, которые, вероятно, будут отвечать на лечение ингибитором WEE1, содержащему реагенты, взаимодействующие с PKMYT1.
В одном варианте осуществления изобретения ингибитор WEE1 представляет собой WEE1-1 или его фармацевтически приемлемую соль.
В другом варианте осуществления изобретения ингибитор WEE1 вводят в дозе от 100 мг в сутки до 200 мг в сутки. В одном варианте осуществления изобретения ингибитор WEE1 можно вводить два раза в сутки (BID) в течение курса из двух с половиной суток (всего 5 доз) или один раз в сутки (QD) в течение курса из двух суток (всего 2 дозы).
Термин «злокачественная опухоль», как используют в настоящем описании, включает различные виды саркомы и карциномы и включает солидную опухоль и гемопоэтическую опухоль. Солидная злокачественная опухоль, как используют в настоящем описании, включают, например, злокачественную опухоль головного мозга, рак головы и шеи, рак пищевода, рак щитовидной железы, мелкоклеточный рак легких, немелкоклеточный рак легких, рак молочной железы, рак эндометрия, рак легких, рак желудка, рак желчного пузыря/желчных протоков, рак печени, рак поджелудочной железы, рак толстой кишки, рак прямой кишки, рак яичников, хориокарциному, рак тела матки, рак шейки матки, рак почечной лоханки/уретры, рак мочевого пузыря, рак предстательной железы, рак полового члена, рак яичек, фетальную злокачественную опухоль, опухоль Вильмса, рак кожи, злокачественную меланому, нейробластому, остеосаркому, опухоль Юинга, саркому мягкой части. С другой стороны, гематопоэтический рак включает, например, острый лейкоз, хронический лимфолейкоз, хронический миелоцитарный лейкоз, истинную полицитемию, злокачественную лимфому, множественную миелому, лимфому Ходжкина, неходжкинскую лимфому.
Термин «злокачественная опухоль, ассоциированная с киназой WEE1», как используют в настоящем описании, обозначает злокачественную опухоль, ассоциированную с активностью или ингибированием киназы WEE1, включая, но не ограничиваясь ими, злокачественную опухоль головного мозга, рак головы и шеи, рак пищевода, рак щитовидной железы, мелкоклеточный рак легких, немелкоклеточный рак легких, рак молочной железы, рак легких, рак желудка, рак желчного пузыря/желчных протоков, рак печени, рак поджелудочной железы, рак толстой кишки, рак прямой кишки, рак яичников, хориокарциному, рак тела матки, рак шейки матки, рак почечной лоханки/уретры, рак мочевого пузыря, рак предстательной железы, рак полового члена, рак яичек, фетальную злокачественную опухоль, опухоль Вильмса, рак кожи, злокачественную меланому, нейробластому, остеосаркому, опухоль Юинга, саркому мягкой части, острый лейкоз, хронический лимфолейкоз, хронический миелоцитарный лейкоз, лимфому Ходжкина, или в качестве сенсибилизаторов для химиотерапии или лучевой терапии этих злокачественных опухолей. В частности, ингибитор WEE1 по настоящему изобретению пригоден в качестве лекарственного средства, например, от рака молочной железы, рака легких, рака поджелудочной железы, рака толстого кишечника, рака яичника, острой лейкемии, хронической лимфатической лейкемии, хронической миелоцитарной лейкемии, лимфомы Ходжкина, или в качестве сенсибилизаторов для химиотерапии или лучевой терапии этих злокачественных опухолей.
Термин «лечение злокачественной опухоли», как используют в настоящем описании, обозначает, что средство против злокачественной опухоли вводят пациенту со злокачественной опухолью, чтобы ингибировать рост злокачественных клеток у пациента. Предпочтительно, лечение приводит к некоторой форме регрессии роста злокачественной опухоли, или лечение задерживает или предотвращает рецидив злокачественной опухоли. Более предпочтительно, лечение приводит к полному исчезновению злокачественной опухоли.
Термин «пациент» или «индивидуум», как используют в настоящем описании, обозначает реципиента, нуждающегося в медицинском вмешательстве или лечении. В него входят пациенты или индивидуумы, являющиеся и не являющиеся млекопитающими.
Термин «прогностический биомаркер», как используют в настоящем описании, обозначает генный маркер, экспрессия которого коррелирует с ответом на данное терапевтическое средство или класс терапевтических средств. Как используют в настоящем описании, этот термин относится к PKMYT1, экспрессия которого коррелирует с терапевтическим эффектом ингибитора WEE1. В одном варианте осуществления настоящего изобретения ингибитор WEE1 представляет собой WEE1-1.
Термин «происходящие из маркера полинуклеотиды» означает РНК, транскрибированную с маркерного гена, любую кДНК или кРНК, продуцированную с него, и любую нуклеиновую кислоту, происходящую из нее, такую как синтетическая нуклеиновая кислота, имеющая последовательность, происходящую из гена, соответствующего маркерному гену.
Термины «контроль», «контрольный уровень», «эталонный уровень» или «заданный эталонный уровень» означает отдельный исходный уровень, измеренный в сравнимой контрольной клетке, которая может иметь или не иметь патологических изменений. Она может представлять собой клетку того же индивидуума или другого индивидуума, который здоров или не имеет того же заболевания, что и у индивидуума, от которого получен патологический или исследуемый образец. Таким образом, «эталонный уровень» может представлять собой абсолютную величину, диапазон величин, усредненную величину, срединную величину, среднюю величину или величину, сравниваемую с конкретной контрольной или исходной величиной. Эталонная величина может быть основана на величине отдельного образца, такой как величина, полученная для образца от индивидуума, страдающего злокачественно опухолью, ассоциированной с киназой WEE1, но в более ранний момент времени или перед лечением, или величина, полученная для образца от пациента, у которого диагностирована злокачественная опухоль, ассоциированная с киназой WEE1, отличного от пациента, подвергаемого исследованию, или «нормального» индивидуума, который является индивидуумом, у которого не диагностирована злокачественная опухоль, ассоциированная с киназой WEE1. Эталонная величина может быть основана на ряде образцов, например, от множества пациентов, у которых диагностирована злокачественная опухоль, опосредуемая киназой WEE1, или здоровых индивидуумов, или она может быть основана на совокупности образцов, включающих или исключающих исследуемый образец.
Термин «PKMYT1», как используют в настоящем описании, обозначает ген, который кодирует ассоциированную с мембраной тирозин- и треонин-специфическую ингибиторную киназу CDK1 - белок, который является членом семейства сериновых/треониновых протеинкиназ (Liu, F., et al., Mol. Cell. Biol., 1997, 17(2):571-583), последовательность которой представлена под номерами эталонных последовательностей NCBI NM_004203 (SEQ ID NO: 1) и NP_004194 (SEQ ID NO: 2).
Термин «низкая экспрессия PKMYT1» или «низкая PKMYT1 экспрессия», как используют в настоящем описании, обозначает клетку, полученную из линии клеток, охарактеризованной как линия злокачественных клеток, или полученную от пациента, у которого диагностирована злокачественная опухоль, имеющая сниженную экспрессию ДНК, мРНК или белка PKMYT1, или уменьшение числа копий гена PKMYT1, по сравнению с клеткой, полученной из линии клеток, охарактеризованной как линия клеток, не являющихся злокачественными, или полученной от пациента, у которого не диагностирована злокачественная опухоль, или с контрольной клеткой.
Как используют в настоящем описании, термины «измерение уровня экспрессии», «измерение уровня экспрессии гена» или «получение уровня экспрессии» и т.п. включают способы, которые количественно определяют уровень экспрессии гена-мишени, например, транскрипта гена, включая микроРНК (miRNA), или белка, кодируемого геном, а также способы, которые определяют, экспрессируется ли вообще представляющий интерес ген. Таким образом, анализ, который обеспечивает результат «да» или «нет» без обязательного обеспечения количественного определения величины экспрессии, представляет собой анализ, который «измеряет экспрессию», как этот термин используют в настоящем описании. Альтернативно, термин может включать количественное определение уровня экспрессии гена-мишени, выражаемого в количественной величине, например, в величине кратного изменения экспрессии, вверх или вниз, относительно контрольного гена или относительно того же гена в другом образце, или логарифмической величине соотношения экспрессии, или в любом его визуальном представлении, например, таком как «тепловая карта», где интенсивность цвета отображает величину выявленной экспрессии гена. Иллюстративные способы выявления уровня экспрессии гена включают, но не ограничиваются ими, норзерн-блоттинг, иммуноанализ с использованием дот-блоттинга или слот-блоттинга, матрицу репортерного гена (см., например, патент США № 5569588), защиту от нуклеаз, ОТ-ПЦР, профилирование на микрочипах, дифференциальный дисплей, SAGE (Velculescu et al., (1995), Science 270:484-87), Digital Gene Expression System (см. WO2007076128; WO2007076129), мультиплексный анализ мРНК (Tian et al., (2004), Nucleic Acids Res. 32:e126), PMAGE (Kim et al., (2007), Science 316:1481-84), анализ с кДНК-опосредуемым отжигом, отбором, удлинением и лигированием (DASL, Bibikova, et al., (2004), AJP 165:1799-807), мультиплексный анализ разветвленной ДНК (Flagella et al., (2006), Anal. Biochem. 352:50-60), 2D гель-электрофорез, SELDI-TOF, ICAT, ферментный анализ, анализ с антителами и т.п.
Ингибиторы WEE1
В одном варианте осуществления изобретения представляющий интерес ингибитор WEE1 по настоящему изобретению представляет собой WEE1-1, структура которого показана ниже.
WEE1-1 представляет собой ингибитор WEE1, который является пригодным для лечения злокачественной опухоли. WEE1-1 также известен как 2-аллил-1-[6-(1-гидрокси-1-метилэтил)пиридин-2-ил]-6-{[4-(4-метилпиперазин-1-ил)фенил]амино}-1,2-дигидро-3H-пиразоло[3,4-d]пиримидин-3-он. WEE1-1 описан в патенте США № 7834019 и в международных публикациях PCT WO2007/126122, WO 2007/126128 и WO2008/153207, которые включены в настоящее описание в качестве ссылок в полном объеме. Кристаллические WEE1-1 описаны в публикации США № US2010-0124544 и в международной публикации PCT WO2011/034743, которые включены в настоящее описание в качестве ссылок в полном объеме.
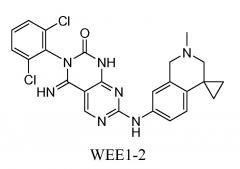
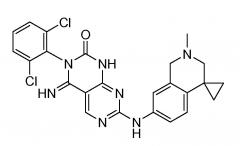
В одном варианте осуществления изобретения ингибитор WEE1 по настоящему изобретению представляет собой WEE1-2, структура которого показана ниже.
WEE1-2 представляет собой ингибитор WEE1, который является пригодным для лечения злокачественной опухоли. WEE1-2 также известен как 3-(2,6-дихлорфенил)-4-имино-7-[(2'-метил-2',3'-дигидро-1'H-спиро[циклопропан-1,4'-изохинолин]-7'-ил)амино]-3,4-дигидропиримидо[4,5-d]пиримидин-2(1H)-он. WEE1-2 был описан в международной публикации PCT № WO2008/153207 и в публикации США US2011-0135601, которые полностью включены в настоящее описание в качестве ссылок в полном объеме. Кристаллические формы WEE1-2 описаны в международной публикации № WO2009/151997 и в публикации США US2011-0092520.
Соединения по настоящему изобретению могут иметь асимметричные центры, хиральные оси и хиральные плоскости (как описано в: E.L. Eliel and S.H. Wilen, Stereochemistry of Carbon Compounds, John Wiley & Sons, New York, 1994, страницы 1119-1190), и встречаются в виде рацематов, рацемических смесей и в виде отдельных диастереомеров, со всеми их возможными изомерами и смесями, включая оптические изомеры, причем все такие стереоизомеры включены в настоящее изобретение. Кроме того, соединения, описанные в настоящем описании, могут существовать в качестве таутомеров, и предполагается, что обе таутомерные формы входят в объем изобретения, даже если изображена только одна таутомерная структура.
В соединениях, описанных в рамках настоящего изобретения, атомы могут проявлять их естественную распространенность, или один или несколько атомов могут быть искусственно обогащены конкретным изотопом, имеющим такое же атомное число, но атомную массу или массовое число, отличающееся от атомной массы или массового числа, преимущественно встречающихся в природе. Предполагается, что настоящее изобретение включает все подходящие изотопные варианты соединений, описанных в настоящем описании. Например, различные изотопные формы водорода (H) включают протий (1H) и дейтерий (2H). Протий представляет собой преобладающий изотоп водорода, встречающийся в природе. Обогащение дейтерием может обеспечить определенные терапевтические преимущества, такие как увеличение времени полужизни in vivo или снижение требуемой дозировки, или может обеспечить соединение, пригодное в качестве стандарта для охарактеризации биологических образцов. Изотопно обогащенные соединения, описанные в настоящем описании, можно получать без излишнего экспериментирования обычными способами, хорошо известными специалистам в данной области, или способами, аналогичными тем, которые описаны в настоящем описании в разделе «Схемы и примеры», с использованием соответствующих изотопно обогащенных реагентов и/или промежуточных соединений.
Ингибиторы WEE1 по настоящему изобретению также могут существовать в виде различных кристаллов, аморфных веществ, фармацевтически приемлемых солей, гидратов и сольватов. Кроме того, ингибиторы WEE1 по настоящему изобретению могут быть предоставлены в форме пролекарств. В целом, такие пролекарства представляют собой функциональные производные ингибиторов WEE1 по настоящему изобретению, которые могут без труда преобразовываться в соединения, которые требуются живым организмам. Соответственно, в способе лечения различных злокачественных опухолей по изобретению термин «введение» включает не только введение определенного соединения, но также введение соединения, которое после введения пациенту может преобразовываться в конкретное соединение в живых организмах. Общепринятые способы выбора и получения подходящих пролекарственных производных описаны, например, в «Design of Prodrugs», ed. H. Bundgaard, Elsevier, 1985, которая включена в настоящее описание, как его часть, в качестве ссылки в полном объеме. Метаболиты соединения могут включать активные соединения, которые продуцируются при помещении соединения в биологическую среду, и они входят в объем соединения по изобретению.
Определение уровней экспрессии биомаркера
A. Способ количественного определения биомаркера
В одном варианте осуществления изобретение относится к прогностическому биомаркеру PKMYT1, экспрессия которого чувствительна к ингибированию WEE1 ингибитором WEE1. Уровни экспрессии прогностического биомаркера в образце можно определить с помощью средств, известных в данной области. Уровень экспрессии можно определить путем выделения и определения уровня (т.е. количества) нуклеиновой кислоты, транскрибированной с биомаркера. Альтернативно или дополнительно, можно определять уровень определенных белков, кодируемых биомаркером.
Уровень экспрессии биомаркера можно определить путем определения количества мРНК или полинуклеотидов, происходящих из нее, присутствующих в образце. Можно использовать любой способ определения уровней РНК. Например, РНК выделяют из образца и отделяют на агарозном геле. Затем отделенную РНК переносят на твердую подложку, такую как фильтр. Затем нуклеиновокислотные зонды, соответствующие одному или нескольким маркерам, гибридизируют на фильтре норзерн-гибридизацией, и определяют количество происходящей из маркера РНК. Такое определение может быть визуальным или автоматизированнным, например, с использованием денситометра. Другим способом определения уровней РНК является использование дот-блота или слот-блота. В этом способе осуществляют мечение РНК или происходящей из нее нуклеиновой кислоты из образца. Затем РНК или происходящую из нее нуклеиновую кислоту гибридизуют на фильтре, содержащем олигонуклеотиды, происходящие из одного или нескольких маркерных генов, причем олигонуклеотиды помещают на фильтре в дискретных легко идентифицируемых областях. Гибридизацию, или ее отсутствие, меченой РНК со связанными с фильтром олигонуклеотидами определяют визуально или деситометром. Полинуклеотиды можно метить с использованием радиоактивной метки или флуоресцентной (т.е. видимой) метки.
Экспрессию биомаркерного гена в ряде образцов ткани можно охарактеризовывать с использованием «тканевой матрицы» (Kononen et al., Nat. Med, 1998, 4(7):844-847). В тканевой матрице множество