2-пиридоновое соединение
Иллюстрации
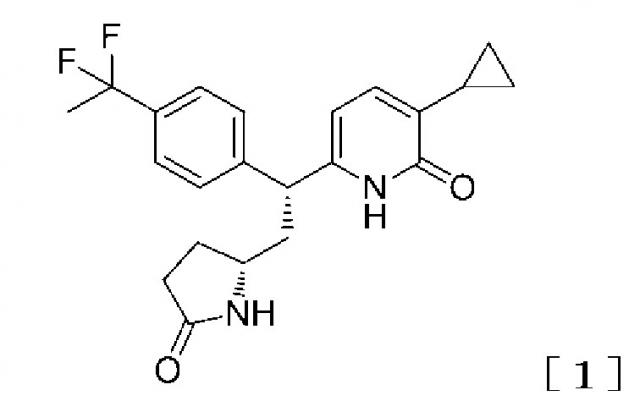
Показать всеИзобретение относится к 2-пиридоновому соединению, представленному формулой [1]:
,
таутомеру данного соединения, его фармацевтически приемлемой соли (далее называется 2-пиридоновое соединение, таутомер данного соединения или его фармацевтически приемлемая соль, называемая термином «2-пиридоновое соединение или родственные соединения»). Изобретение также относится к кристаллическому 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-ону, его способу получения, к лекарственному средству для профилактики или лечения заболевания или состояния, которое может улучшаться посредством эффекта активации глюкокиназы. Технический результат: получено новое 2-пиридоновое соединение, обладающее свойствами активатора глюкокиназы, которое может быть использовано в качестве лекарственного средства для профилактики или лечения диабета. 5 н. и 2 з.п. ф-лы, 3 ил., 2 табл., 3 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение предлагает новые 2-пиридоновые соединения, производящие эффект активации глюкокиназы, и лекарственное средство, содержащее такое соединение в качестве активного ингредиента. Кроме того, настоящее изобретение предлагает кристаллы этих соединений и способ их получения.
Уровень техники
Во всем мире увеличивается число пациентов, страдающих диабетом второго типа, причем прогноз изменения состояния пациентов и развития осложнений является неутешительным; в таких обстоятельствах весьма желательной является разработка нового профилактического или лекарственного средства. Считается, что риск развития диабета второго типа значительно повышается на фоне генетической предрасположенности и старения, предположительно связанного с его развитием, при обычном образе жизни в развитых странах, а именно в состоянии потребления избыточной энергии по сравнению с физическими нагрузками. Кроме того, метаболические расстройства, которые представляют собой предрасполагающие факторы, включают неудовлетворительное усвоение глюкозы в скелетных мышцах и жировых тканях, нарушение секреции инсулина бета-клетками поджелудочной железы и недостаточное регулирование высвобождения глюкозы из печени, и считается, что лекарственное средство, способное устранить эти расстройства, является полезным для профилактики и лечения диабета второго типа.
Для усвоения глюкозы в скелетных мышцах и жировых тканях считается эффективной лекарственная терапия с использованием повышающих чувствительность к инсулину препаратов, представляющих собой производные тиазолидина (например, пиоглитазон); однако было отмечено, что возникают обостряющееся ожирение, задержка жидкости в организме, повышенный риск сердечной недостаточности, повышенная вероятность рака мочевого пузыря и т.д., и, следовательно, требуется всестороннее обследование при использовании этих лекарственных средств. Кроме того, при нарушении секреции инсулина считаются эффективными лекарственные средства на основе сульфонилмочевины (например, глимепирид, глибенкламид, глипизид); однако часто возникает гипогликемия и/или избыточная масса, а также может возникать неудовлетворительное регулирование уровня глюкозы в крови (вторичная резистентность) вследствие снижения терапевтических эффектов при использовании в течение продолжительного периода времени, и, таким образом, остаются нерешенными вопросы безопасности и эффективности. В случае возникающей после приема пищи гипергликемии используются ингибиторы α-глюкозидазы (например, акарбоза, воглибоза и миглитол) или глинидные лекарственные средства (например, натеглинид, репаглинид и митиглинид), но они производят ограниченные терапевтические эффекты на диабет. Для регулирования высвобождения глюкозы из печени эффективными являются бигуанидные лекарственные средства (например, метформин), но гликемический контроль становится затруднительным по мере прогрессирования состояния, и, кроме того, в некоторых случаях использование лекарственного средства может быть ограниченным вследствие его неблагоприятного воздействия на пищеварительный тракт, риска лактоцидоза и т.д. В результате исследования вышеупомянутых основных лекарственных средств становится очевидным, что существующие лекарственные средства не всегда соответствуют медицинским требованиям. В частности, метформин представляет собой практически единственное лекарственное средство для непосредственного улучшения метаболизма глюкозы в печени, и в таких обстоятельствах становится чрезвычайно важной разработка лекарственного средства, способного улучшать метаболизм глюкозы в печени посредством нового механизма действия.
Глюкокиназа (далее сокращенно называется «GK») принадлежит к семейству гексокиназ и катализирует фосфорилирование глюкозы, содержащейся в клетках, таких как бета-клетки поджелудочной железы или клетки печени. Глюкокиназы, содержащиеся в клетках печени и бета-клетках поджелудочной железы, отличаются друг от друга в отношении последовательности 15 аминокислот с концевым атомом азота вследствие различного сплайсинга, но являются ферментативно идентичными. GK проявляет высокое сродство к глюкозе (S0,5 составляет приблизительно 10 мМ), и ее не ингибирует продукт, а именно глюкоза-6-фосфат. Таким образом, ее скорость реакции чутко реагирует на физиологические изменения уровня глюкозы в крови. GK в бета-клетках поджелудочной железы модулирует зависимую от глюкозы секрецию инсулина, в то время как GK в печени модулирует путь расщепления глюкозы или образование гликогена, таким образом, что уровень глюкозы в крови поддерживается и регулируется. Таким образом, считается, что GK функционирует как датчик глюкозы, поддерживая гомеостаз уровня глюкозы в крови (см. непатентный документ 1).
Генетически модифицированные мыши и генетические мутации, обнаруженные у человека, подтверждают гипотезу, что GK функционирует как датчик глюкозы в организме. Гомозиготные по GK мыши умирали от гипергликемии немедленно после рождения, а у гетерозиготных мышей наблюдалась гипергликемия и нарушенная переносимость глюкозы (см. непатентный документ 2). С другой стороны, у имеющих повышенную экспрессию GK мышей подтверждено наличие гипогликемии (см. непатентный документ 3). Кроме того, в случае юношеского инсулиннезависимого сахарного диабета второго типа (MODY2) человека, когда наблюдается мутация гена GK, диабет развивается в молодости (см. непатентный документ 4). Было подтверждено, что эти генные мутации снижают активность GK. С другой стороны, были описаны семьи, имеющие генные мутации, повышающие активность GK (см. непатентный документ 5). Согласно наблюдениям, эти генные мутации повышали сродство GK к глюкозе и вызывали симптомы гипогликемии натощак в сочетании с повышением концентрации инсулина в крови.
Таким образом, было показано, что GK функционирует как датчик глюкозы у млекопитающих, включая человека.
Повышающие активность GK вещества (далее называются «активирующие GK вещества») могут улучшать состояние при гипергликемии посредством усиления метаболизма глюкозы и образования гликогена в печени и зависимой от глюкозы секреции инсулина из бета-клеток поджелудочной железы. В частности, вещества, которые повышают активность GK преимущественно в печени, могут улучшать состояние при гипергликемии посредством усиления метаболизма глюкозы в печени независимым от инсулина путем. Можно также предполагать, что улучшение состояние при гипергликемии приведет к лечению и профилактике хронических диабетических осложнений, таких как ретинопатия, нефропатия, невроз, ишемическая болезнь сердца и артериосклероз, а также к лечению и профилактике связанных с диабетом заболеваний, такие как ожирение, гиперлипидемия, повышенное артериальное давление и метаболический синдром. Таким образом, предполагается, что соединения, усиливающие функцию GK, должны представлять собой эффективные средства для лечения диабета.
С другой стороны, была отмечена экспрессия GK не только в поджелудочной железе и печени, но также в пищевом центре, а также ее важная функция в противопищевом эффекте глюкозы (см. непатентный документ 6). Соответственно, активирующие GK вещества могут воздействовать на пищевой центр и производить противопищевой эффект, и можно предполагать, что они должны действовать не только как средства для лечения диабета, но также как лекарственные средства против ожирения.
В связи с этим отмечено, что некоторые соединения, содержащие 2-пиридон, представляют собой активирующие GK вещества, но значительно отличаются по структуре от соединений согласно настоящему изобретению (см. патентные документы 1 и 2). Описаны и другие 2-пиридоновые соединения, имеющие близкое структурное сходство (см. патентные документы 3 и 4), но соединения согласно настоящему изобретению ранее не были описаны определенным образом. Настоящее изобретение отличается от предшествующих сообщений тем, что в них не содержится описание в отношении медицинского применения, и тем, что они сосредоточены на способе синтеза 2-пиридоновых соединений (см. непатентный документ 7). Кроме того, некоторые ацилмочевинные соединения, которые могут иметь псевдоциклическую структуру, были описаны как активирующие GK вещества (см. патентные документы 5 и 6), но они представляют собой нециклические соединения и отличаются от соединений согласно настоящему изобретению.
Список цитируемой литературы
Непатентная литература
Непатентный документ 1: F. M. Matschinsky и M. A. Magnuson, Frontiers in Diabetes (Ограничения при диабете), 2004 г., с. 16
Непатентный документ 2: A. Grupe и др., Cell, 1995 г., т. 83, № 1, с. 69-78
Непатентный документ 3: T. Ferre и др., Proc. Natl. Acad. Sci., 1996 г., т. 93, № 14, с. 7225-7230
Непатентный документ 4: N. Vionnet и др., Nature, 1992 г., т. 356, № 6371, с. 721-722
Непатентный документ 5: B. Glaser и др., N. Engl. J. Med., 1998 г., т. 338, № 4, с. 226-230
Непатентный документ 6: L. Kang и др., Diabetes, 2006 г., т. 55, № 2, с. 412-420
Непатентный документ 7: R. Latif и др., J. Chem. Soc. C. Organic, 1968 г., т. 17, с. 2140-2144,
Патентная литература
Патентный документ 1: международная патентная заявка WO 2008/079787
Патентный документ 2: международная патентная заявка WO 2010/013161
Патентный документ 3: патент США US 4275069
Патентный документ 4: международная патентная заявка WO 2011/068211
Патентный документ 5: международная патентная заявка WO 2000/58293
Патентный документ 6: международная патентная заявка WO 2001/44216
Сущность изобретения
Техническая проблема
Задача настоящего изобретения заключается в том, чтобы предложить соединения, которые производят превосходный эффект активации GK и являются пригодными для использования в качестве лекарственных средств.
Решение проблемы
Принимая во внимание вышеупомянутые обстоятельства, авторы настоящего изобретения провели всесторонние исследования, чтобы найти соединения, производящие эффект активации GK, и в результате этого обнаружили, что данную задачу могут решить 2-пиридоновое соединение, представленное следующей формулой [1] (название соединения: 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-он), таутомер данного соединения, его фармацевтически приемлемая соль (далее 2-пиридоновое соединение, таутомер данного соединение или его фармацевтически приемлемая соль называются термином «2-пиридоновое соединение или родственные соединения»), или сольват 2-пиридонового соединения или родственных соединений, и, таким образом, было выполнено настоящее изобретение.
(I) Вариант осуществления настоящего изобретения предлагает 2-пиридоновое соединение, представленное формулой [1]:
,
таутомер данного соединение или его фармацевтически приемлемая соль, или сольват 2-пиридонового соединения или родственных соединений.
(II) Следующий вариант осуществления настоящего изобретения предлагает кристаллический 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-он по пункту (I), представленный вышеупомянутой формулой [1] и имеющий следующее физическое свойство (a):
(a) рентгеновская порошковая дифрактограмма (Cu-Kα), проявляющая пики при дифракционных углах 2θ, составляющих 8,5, 13,4, 19,1 и 24,5°.
(III) Следующий вариант осуществления настоящего изобретения предлагает кристаллический 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-он по пункту (I), представленный вышеупомянутой формулой [1] и имеющий следующие физические свойства (a)-(c):
(a) рентгеновская порошковая дифрактограмма (Cu-Kα), проявляющая пики при дифракционных углах 2θ, составляющих 8,5, 13,4, 19,1 и 24,5°;
(b) инфракрасный спектр поглощения, проявляющий характеристические полосы поглощения при 916, 1146, 1167, 1295, 1651, 1664, 2909, 2955, 3003 и 3146 см-1; и
(c) температура плавления, составляющая от 199 до 201°C.
(IV) Следующий вариант осуществления настоящего изобретения предлагает способ получения кристаллического 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-она, имеющего следующие физические свойства (a)-(c):
(a) рентгеновская порошковая дифрактограмма (Cu-Kα), проявляющая пики при дифракционных углах 2θ, составляющих 8,5, 13,4, 19,1 и 24,5°;
(b) инфракрасный спектр поглощения, проявляющий характеристические полосы поглощения при 916, 1146, 1167, 1295, 1651, 1664, 2909, 2955, 3003 и 3146 см-1; и
(c) температура плавления, составляющая от 199 до 201°C,
включающий растворение 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-она, представленного вышеупомянутой формулой [1], в спиртовом растворителе при нагревании для получения раствора; последующее добавление воды в качестве растворителя в раствор; охлаждение полученного в результате раствора до температуры 5°C или ниже для получения кристаллов; и высушивание полученных кристаллов при температуре 60°C или ниже.
(V) Следующий вариант осуществления настоящего изобретения предлагает лекарственное средство содержащее, в качестве активного ингредиента, 2-пиридоновое соединение, таутомер данного соединение или его фармацевтически приемлемую соль, или сольват 2-пиридонового соединения или родственных соединений по пункту (I).
(VI) Следующий вариант осуществления настоящего изобретения предлагает лекарственное средство по пункту (V), где данное лекарственное средство используется для профилактики или лечения заболевания или состояния, которое может улучшаться посредством эффекта активации глюкокиназы.
(VII) Следующий вариант осуществления настоящего изобретения предлагает лекарственное средство по пункту (V), которое представляет собой гипогликемическое средство.
(VIII) Следующий вариант осуществления настоящего изобретения предлагает лекарственное средство по пункту (V), где данное лекарственное средство представляет собой средство для профилактики или лечения диабета.
Полезные эффекты изобретения
Согласно настоящему изобретению, предлагаются 2-пиридоновые соединения, производящие превосходный эффект активации GK.
Кроме того, согласно настоящему изобретению, предлагается кристаллический 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-он, который представляет собой новое кристаллическое соединение, пригодное для использования в качестве лекарственного средства. Данное соединение существует в устойчивой кристаллической форме в условиях комнатной температуры и проявляет хорошую устойчивость при хранении.
Кроме того, согласно настоящему изобретению, предлагается новый способ получения, позволяющий получать безопасным и устойчивым путем вышеупомянутое кристаллическое соединение, имеющее однородное качество.
Краткое описание чертежей
Фиг. 1 представляет рентгеновскую порошковую дифрактограмму кристаллического 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-она согласно настоящему изобретению.
Фиг. 2 представляет инфракрасный спектр поглощения (метод нарушенного полного внутреннего отражения (НПВО), алмазный кристалл) кристаллического 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-она согласно настоящему изобретению.
Фиг. 3 представляет кривые дифференциального термического анализа/термогравиметрического анализа кристаллического 3-циклопропил-6-{(1R)-1-[4-(1,1-дифторэтил)фенил]-2-[(2R)-5-оксопирролидин-2-ил]этил}пиридин-2(1H)-она согласно настоящему изобретению.
Описание вариантов осуществления
Далее настоящее изобретение будет описано подробно, но оно не ограничивается определенным образом примерными вариантами осуществления.
Согласно настоящему изобретению, «н» означает «нормальный», «и» означает «изо», «в» и «втор» означают «вторичный», «трет» означает «третичный», «ц» означает «цикло», «o» означает «орто», «м» означает «мета» и «п» означает «пара».
Сначала будут описаны соединения согласно настоящему изобретению.
Примеры фармацевтически приемлемых солей согласно настоящему изобретению включают соли минеральных кислот, такие как гидрохлориды, гидробромиды, гидройодиды, фосфаты, сульфаты и нитраты; сульфонаты, такие как метансульфонаты, этансульфонаты, бензолсульфонаты и п-толуолсульфонаты; карбоксилаты, такие как оксалаты, тартраты, цитраты, малеаты, сукцинаты, ацетаты, бензоаты, манделаты, аскорбаты, лактаты, глюконаты и малаты; соли аминокислот, такие как соли глицина, соли лизина, соли аргинина, соли орнитина, глутаматы и аспартаты; и минеральные соли, такие как соли лития, соли натрия, соли калия, соли кальция и соли магния, и соли органических оснований, такие как соли аммония, соли триэтиламина, соли диизопропиламина и соли циклогексиламина. Предпочтительные примеры включают гидрохлориды, гидробромиды, фосфаты, сульфаты, метансульфонаты, п-толуолсульфонаты, оксалаты, тартраты, цитраты, ацетаты, лактаты, глутаматы, аспартаты, соли натрия, соли калия, соли аммония и соли триэтиламина.
Сольваты согласно настоящему изобретению представляют собой фармацевтически приемлемые сольваты соединений или их соли согласно настоящему изобретению. Соединения и их соли согласно настоящему изобретению могут абсорбировать влагу, содержать адсорбированную воду или образовывать гидраты при воздействии воздуха, перекристаллизации и т.д. Соединения согласно настоящему изобретению также включают такие гидраты.
Соединения согласно настоящему изобретению имеют два центра асимметрии и представляют собой оптически активные соединения, причем оба центра асимметрии в данных соединениях имеют абсолютную конфигурацию (R). Соединения согласно настоящему изобретению можно получать путем разделения оптических изомеров из соответствующего рацемата или смеси диастереомеров. Приемлемые способы разделения оптических изомеров включают способы, хорошо известные специалисту в данной области техники, такие как способ фракционной кристаллизации или хиральная колоночная хроматография. В качестве альтернативы, оптически активные соединения согласно настоящему изобретению можно также получать хорошо известным способом, практически используемым в органической химии для этой цели. Кроме того, геометрические изомеры, такие как изомер (E) и изомер (Z), могут присутствовать как промежуточные соединения в синтезе для получения соединений согласно настоящему изобретению, и соотношение этих изомеров может представлять собой любую пропорцию.
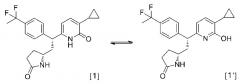
Соединения согласно настоящему изобретению включают таутомеры. Таутомер в настоящем документе означает кето-енольный таутомер соединений, представленных вышеупомянутой формулой [1]. Соединения, представленные вышеупомянутой формулой [1], и соответствующий таутомер [1'] приведены ниже в качестве примера.
2-Пиридоновые соединения согласно настоящему изобретению могут представлять собой соответствующие фармацевтически приемлемые соли или сольваты 2-пиридонового соединения или родственных соединений. Далее 2-пиридоновые соединения, таутомеры соединений, их фармацевтически приемлемые соли или сольваты 2-пиридоновых соединений или родственных соединений в совокупности называются «соединения согласно настоящему изобретению».
Эти «соединения согласно настоящему изобретению» также включают соединения, обычно называемые термином «пролекарства», которые имеют химически или метаболически разлагающуюся группу и образуют фармакологически активные соединения согласно настоящему изобретению в результате сольволиза или в физиологических условиях живого организма.
Соединения согласно настоящему изобретению производят эффект активации GK. Таким образом, соединения согласно настоящему изобретению могут приводить к улучшению при гипергликемии посредством усиления метаболизма глюкозы, главным образом, в печени. Соответственно, данные соединения можно использовать как новые лекарственные средства, которые отличаются по механизму действия от существующих средств для лечения диабета. Диабет включает диабет первого типа, диабет второго типа и диабет других типов, вызванный определенными причинами. Соединения согласно настоящему изобретению также являются эффективными для лечения и профилактики диабетических осложнений, такие как кетоацидоз, микроангиопатия (ретинопатия или нефропатия), артериосклероз (такой как атеросклероз, инфаркт миокарда, церебральный инфаркт или окклюзионная болезнь периферических артерий), нейропатия (такая как сенсорная нейропатия, моторная нейропатия или автономная нейропатия), гангрена ступни и инфекции.
Данные соединения можно также использовать для лечения и профилактики связанных с диабетом заболеваний, таких как ожирение, гиперлипидемия, повышенное артериальное давление, метаболический синдром, отек, гиперурикемия и подагра.
Соединения согласно настоящему изобретению можно также использовать в сочетании с лекарственными средствами, имеющими механизм действия, который представляет собой эффект активации GK, такие как средства для лечения диабета, диабетических осложнений, гиперлипидемии, повышенного артериального давления и т.д. Посредством сочетания соединений согласно настоящему изобретению с такими другими лекарственными средствами можно предполагать аддитивный эффект в лечении вышеупомянутых заболеваний по сравнению с эффектом, достигаемым с помощью каждого из отдельно взятых соответствующих лекарственных средств.
Примеры средств для лечения диабета и средств для лечения диабетических осложнений, которые являются пригодными для использования в сочетании с соединениями согласно настоящему изобретению, включают препараты инсулина, повышающие чувствительность к инсулину вещества, такие как агонисты γ-рецепторов, активируемых пролифератором пероксисом (PPAR), агонисты α/γ-PPAR, агонисты δ-PPAR и агонисты α/γ/δ-PPAR (например, пиоглитазон, росиглитазон, алеглитазар, пнлиглитазар, AVE-0897 и MBX-8025), ингибиторы α-глюкозидазы (например, воглибоза, акарбоза и миглитол), бигуанидные лекарственные средства (например, метформин, буформин и фенформин), усилители секреции инсулина (например, глибенкламид, глимепирид, репаглинид, натеглинид и митиглинид), антагонисты глюкагоновых рецепторов, усилители киназы инсулиновых рецепторов, ингибиторы дипептидилпептидазы IV (например, вилдаглиптин, алоглиптин, ситаглиптин, линаглиптин, саксаглиптин, тенелиглиптин, анаглиптин), ингибиторы натрий-зависимых переносчиков глюкозы (SGLT) (например, дапаглифлозин, лузеоглифлозин, канаглифлозин, эмпаглифлозин, ипраглифлозин, тофоглифлозин), ингибиторы протеинтирозинфосфатазы 1b (PTP1b) (например, ванадат натрия), ингибиторы глюкоза-6-фосфатазы, ингибиторы гликогенфосфорилазы (например, PSN-357 и FR-258900), ингибиторы фруктоза-1,6-бисфосфатазы (FBP) (например, MB-07803), ингибиторы фосфоэнолпируваткарбоксиназы (PEPCK), ингибиторы киназы пируватдегидрогеназы, D-хиро-инозит, ингибиторы киназы гликогенсинтазы-3 (GSK3), агонисты глюкагоноподобного пептида-1 (GLP-1) (например, лираглютид и эксенатид), агонисты амилина (например, прамлинтид), антагонисты глюкокортикоидных рецепторов, ингибиторы 11-β-гидроксистероиддегидрогеназы типа 1 (11βHSD1) (например, INCB-13739, LY-2523199, Ro-5027838, Ro-5093151 и S-707106), ингибиторы протеинкиназы C (например, рубоксистаурин), агонисты адреналиновых рецепторов β3, ингибиторы фосфатидилинозиткиназы, ингибиторы фосфатидилинозитфосфатазы, ингибиторы ацетил-СоА-карбоксилазы (ACC), агонисты рецепторов свободных жирных кислот (GPR40) (например, TAK-875), агонисты протеинсвязанных рецепторов G119 (GPR119) (например, APD-597, PSN-821, MBX-2982 и DS-8500), агонисты протеинсвязанных рецепторов G120 (GPR120), агонисты рецепторов TGR5, активаторы 5'- аденозинмонофосфатпротеинкиназы (AMPK), ингибиторы альдозоредуктазы (например, эпалрестат, ранирестат, фидарестат) и ингибиторы конечных продуктов усиленного гликозилирования (AGE).
Кроме того, примеры средств для лечения связанных с диабетом заболеваний, которые являются пригодными для использования в сочетании с соединениями согласно настоящему изобретению, включают ингибиторы редуктазы 3-гидрокси-3-метилглутарил-СоА (HMG-CoA), ингибиторы синтазы сквалена, адсорбенты желчной кислоты, ингибиторы подвздошного переноса желчной кислоты (IBAT), ингибиторы белка переноса холестерилового эфира (CETP), ингибиторы карнитинпальмитоилтрансферазы (CPT), фибраты, ингибиторы ацил-CoA-холестеринацилтрансферазы (ACAT), ингибиторы моноацилглицеринацилтрансферазы (MGAT), ингибиторы диацилглицеринацилтрансферазы (DGAT), ингибиторы абсорбции холестерина, ингибиторы липазы поджелудочной железы, ингибиторы белка переноса микросомальных триглицеридов (MTP), производные никотиновой кислоты, агонисты печеночных рецепторов X (LXR), усилители рецепторов липопротеинов низкой плотности (LDL), ингибиторы превращающего ангиотензин фермента, антагонисты ангиотензина II, антагонисты рениновых рецепторов, антагонисты альдостерона, диуретики, антагонисты кальция, альфа-блокаторы, бета-блокаторы, ингибиторы превращающего эндотелин фермента, антагонисты эндотелиновых рецепторов, подавляющие аппетит вещества, ингибиторы синтеза мочевой кислоты и способствующие выведению мочевой кислоты средства.
Соединения согласно настоящему изобретению можно вводить в чистом виде или вместе с фармацевтически или фармакологически приемлемыми носителями или разбавителями. Соединения согласно настоящему изобретению, используемые в качестве активирующих GK веществ, можно вводить перорально или парентерально в чистом виде. Соединения согласно настоящему изобретению можно также вводить перорально или парентерально в виде средств, содержащих данные соединения в качестве активных ингредиентов. Примеры парентерального введения включают внутривенное введение, назальное введение, чрескожное введение, подкожное введение, внутримышечное введение и подъязычное введение.
Дозировка соединения согласно настоящему изобретению изменяется в зависимости от пациента, пути введения, рассматриваемого заболевания, симптома и т.д., причем обычно она составляет, например, приблизительно от 0,01 до 1000 мг и предпочтительно от 0,1 до 100 мг в однократной дозе при пероральном введении взрослому пациенту, страдающему диабетом; оказывается желательным введение данной дозы один, два или три раза в сутки.
Далее будет описан способ получения соединения согласно настоящему изобретению.
Соединения согласно настоящему изобретению можно синтезировать, осуществляя способы, представленные ниже. Следующие способы получения представляют общие примеры способов получения и не ограничивают способы получения.
Соединения согласно настоящему изобретению можно также синтезировать, используя способ, общеизвестный в области химии, или способ, включающий один или несколько способов, аналогичных этому способу. Примеры таких способов включают способы, описанные в книгах «Синтезы органических функциональных групп», второе издание, издательство Academic Press, Inc., 1986 г.; «Полное описание превращений органических веществ», издательство VCH Publishers Inc., 1989 г.; и «Основы и эксперименты синтеза пептидов», издательство Maruzen Co., Ltd., 1985 г.
Подходящие способы введения и удаления функциональных защитных групп, содержащихся в исходных материалах, промежуточных продуктах и т.д., при синтезе соединений согласно настоящему изобретению можно осуществлять, используя способы, хорошо известных специалисту в данной области техники, такие как способы, описанные в книге Greene «Защитные группы в органическом синтезе», издательство John Wiley & Sons, 2006 г.
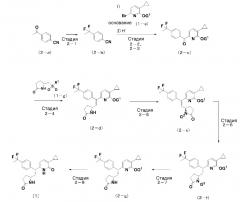
Общие способы получения соединения согласно настоящему изобретению представлены на схемах 1 и 2. Способы получения не ограничиваются следующими способами получения. Соединения согласно настоящему изобретению можно также получать, используя способы, хорошо известные специалисту в данной области техники, например, изменяя последовательность осуществления стадий; используя защитную группу для гидроксильной группы и т.д., осуществляя реакцию и удаление защитной группы на последующей стадии; или добавляя новую стадию в ходе соответствующих стадий.
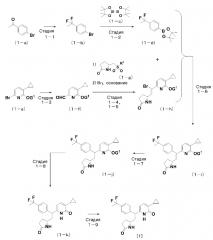
Схема 1: способ синтеза соединения [1] согласно настоящему изобретению из соединения (1-a).
(На данной схеме G1 представляет собой защитную группу для гидроксильной группы в гидроксипиридильной группе, R1 представляет собой 2-бензотиазолильную группу или 1-фенил-1H-тетразол-5-ильную группу.)
Соединение (1-g), используемое на стадии (1-4), можно получать как имеющееся в продаже соединение, общеизвестное соединение или соединение, легко получаемое с использованием разнообразных методик органического синтеза, которые известны специалист в данной области техники.
Стадия (1-1):
Способ получения соединения (1-b): соединение (1-b) можно получить, осуществляя «фторирование» с использованием фторирующего реагента, такого как трифторид N,N-диметоксиэтиламиносеры (трифторид бис(2-метоксиэтил)аминосеры или Deoxo-Fluor (зарегистрированный товарный знак)).
Примеры фторирования включают способ, согласно которому фторирующий реагент, такой как Deoxo-Fluor (зарегистрированный товарный знак) реагирует с соединением (1-a) при отсутствии растворителя или в инертном растворителе при температуре, составляющей от 0°C до 100°C, и образуется соединение (1-b).
Стадия (1-2):
Способ получения соединения (1-d): соединение (1-d) можно получить, вводя в реакцию соединение (1-c) и соединение (1-b) в инертном растворителе в присутствии основания, такого как ацетат калия и палладиевый катализатор.
Стадия (1-3):
Способ получения соединения (1-f): соединение (1-f) можно получить, вводя в реакцию основание, такое как н-бутиллитий или хлорид н-бутилмагния, и соединение (1-e) в инертном растворителе, а затем вводя в реакцию с ними N,N-диметилформамид.
Соединение (1-e) как исходное вещество, можно получать способом, описанным в международной патентной заявке WO 2011/068211, или соответствующим ему способом.
Стадии (1-4, 1-5):
Способ получения соединения (1-h): соединение (1-h) можно получить, вводя в реакцию в инертном растворителе бром и (5R)-5-[2-(5-циклопропил-6-метоксипиридин-2-ил)этенил]пирролидин-2-он (смесь изомеров E и Z), который производит «реакция сочетания», где используются карбонильное соединение (1-f) и соединение (1-g), и после этого в реакцию с ними вводится основание, такое как 1,8-диазабицикло[5,4,0]ундец-7-ен (DBU).
Примерные «реакции сочетания» включают способ получения соединения (1-h) путем образования аниона, где используются соединение (1-g) в качестве матрицы и металлоорганический реагент, такой как н-бутиллитий, втор-бутиллитий или трет-бутиллитий, или основание, такое как гексаметилдисилазид лития или гексаметилдисилазид калия при температуре, составляющей от -78°C до 100°C, в инертном растворителе, и после этого реагируют анион и карбонильное соединение (1-f). Получаемое олефиновое соединение, как правило, получают в форме смеси изомеров E и Z, которые, однако, можно разделять соответствующим образом, используя колоночную хроматографию с силикагелем или высокоэффективную жидкостную хроматографию (ВЭЖХ).
Соединение (1-g), используемое для реакции сочетания, можно получать способом, описанным в международной патентной заявке WO 2011/068211, или соответствующим ему способом.
Стадия (1-6):
Способ получения соединения (1-i): соединение (1-i) можно получить, осуществляя «реакцию сочетания» с фенилборным соединением (1-d), где используется соединение (1-h) в качестве матрицы в присутствии палладиевого катализатора.
Примерные реакции сочетания включают способ, где реагируют соединение (1-h) и фенилборное соединение в инертном растворителе при температуре, составляющей от 20°C до 160°C, в присутствии палладиевого катализатора и основания. Реакцию можно также осуществлять, используя микроволновое излучение.
Примерные палладиевые катализаторы, используемые для реакции сочетания, включают палладиевые катализаторы, известные специалисту в данной области техники, такие как тетракистрифенилфосфинпалладий(0), бис(дибензилиденацетон)палладий(0), трис(дибензилиденацетон)дипалладий(0), дихлорид бис(трифенилфосфин)палладия(II), ацетат бис(трифенилфосфин)палладия(II) и комплекс дихлорида [1,1'-бис(дифенилфосфин)ферроцен]палладия(II) и дихлорметана (1:1). Кроме того, в присутствии основания для реакции можно использовать трис(дибензилиденацетон)дипалладий(0) и три(2-фурил)фосфин.
Стадия (1-7):
Способ получения соединения (1-j): соединение (1-j) можно получить, восстанавливая соединение (1-i) в качестве матрицы посредством реакции каталитического гидрирования, где используется в каталитическом количестве палладий на активированном угле, родий на активированном угле или платина на активированном угле в инертном растворителе в присутствии или при отсутствии кислоты при температуре, составляющей от 0°C до 80°C.
Стадия (1-8):
Способ получения соединения (1-k): соединение (1-k) можно получить, осуществляя «реакцию удаление защитной группы» в отношении защитной группы G1, которую содержит соединение (1-j).
Примерные реакции удаления защитной группы включают (i) реакции удаления защитной группы, где защитная группа G1 представляет собой алкильную группу или аллильную группу, такие как реакции гидролиза для удаления защитной группы в инертном растворителе в присутствии кислоты или сильной кислоты при температуре, составляющей от 0°C до 200°C, реакции с использованием триметилсилилйодида и т.д., и реакции, где используются хлорид алюминия и алкилтиол, и (ii) реакции удаления защитной группы, где в качестве защитной группы G1 присутствуют бензильная группа, 4-метоксибензильная группа, 2,4-диметоксибензильная группа, бензилоксикарбонильная группа, бензгидрильная (дифенилметильная) группа и т.д., такие как реакции удаления защитной группы посредством гидрогенолиза, где в каталитическом количестве используются палладий на активированном угле, родий на активированном угле и т.д., в инертном растворителе в присутствии или при отсутствии кислоты при температуре, составляющей от 0°C до 80°C, или реакции с использованием окислителя, такого как двойной нитрат аммония и церия(IV) или 2,3-дихлор-5,6-дициано-п-бензохинон.
Стадия (1-9):
Способ получения соединения [1] согласно настоящему изобретению: соединение [1] согласно настоящему изобретению можно получить, разделяя диастереомеры соединения (1-k) с использованием, например, высокоэффективной жидкостной хроматографии (ВЭЖХ).
Соединение (1-a) и соединение (1-c), используемые в качестве соединений исходного материала на приведенной выше схеме 1, можно получить, приобретая как товарные продукты или синтезируя известным способом.
Схема 2: способ синтеза соединения [1] согласно настоящему изобретению из соединения (2-a)
(На данной схеме G1 и R1 являются такими, как определено выше. G2 представляет собой защитную группу для атома азота в пирролидинильной группе, замещенной оксогруппой.)
Стадия (2-1):
Способ получения соединения (2-b): соединение (2-b) можно получить способом, описанным в международной патентной заявке WO 2008/103185, или соответствующим ему способом.
Стадии (2-2, 2-3):
Способ получения соединения (2-c): соединение (2-c) можно получить, осуществляя «реакцию присоединения» и используя соединение (2-b) и анион, такой как соединение лития реагент, например, гетероариллитий, реактив Гриньяра (Grignard), например, бромид гетероарилмагния, и обрабатывая полученное соединение кислотой, такой как хлористоводородная кислота.
Примерные «реакции присоединения» включают способ, где реагируют соединение (2-b) и анион, который получают, используя соединение (1-e) в качестве матрицы и металлоорганический реагент, такой как н-бутиллитий, втор-бутиллитий, трет-бутиллитий, или бромид изопропилмагния, металлический реагент, такой как магний, или основание, такое как гексаметилдисилазид лития или гексаметилдисилазид калия, в инертном растворителе при температуре, составляющей от -78°C до 100°C.
Стадия (2-4):
Способ получения соединения (2-d): соединение (2-d) можно получить, осуществляя «реакцию сочетания», где используются карбонильное соединение (2-c) и соединение (1-g).