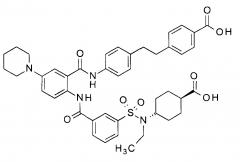
Соединение дикарбоновой кислоты
Иллюстрации
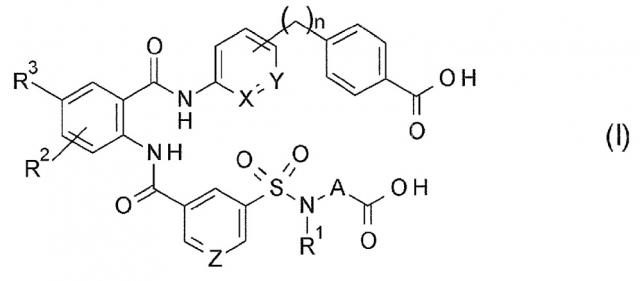
Показать всеИзобретение относится к соединению общей формулы (I):
где R1 представляет собой C1-6алкильную группу, C1-6алкоксиC1-6алкильную группу, C3-6циклоалкильную группу или C3-6циклоалкилC1-6алкильную группу, R2 представляет собой атом водорода или группу галогенов, R3 представляет собой атом водорода, группу галогенов, галогенC1-6алкильную группу, галогенC1-6алкоксигруппу, насыщенную C1-5циклическую аминогруппу, C1-6диалкиламиногруппу, C3-6циклоалкилC1-6алкоксигруппу или C1-6алкоксигруппу, A представляет собой C3-6циклоалкильное кольцо, X представляет собой CH или N, Y представляет собой CH или N, Z представляет собой CH или N и n равен целому числу, выбранному из 1, 2, 3 и 4, или его фармацевтически приемлемой соли или гидрату соединения или его фармацевтически приемлемой соли, которые применяют для предупреждения или лечения гиперфосфатемии. 5 н. и 37 з.п. ф-лы., 17 табл.
Реферат
Область техники
[0001] Настоящее изобретение относится к соединению, которое полезно при предупреждении или лечении гиперфосфатемии или заболевания, связанного с гиперфосфатемией, или его фармакологически приемлемой соли.
Предшествующий уровень техники
[0002] Фосфор присутствует в живом организме в различных формах в виде составных элементов, имеющих важное значение для организма, таких как ДНК, РНК или кости, и играет важную роль в активизации жизнедеятельности.
Фосфорная кислота всасывается, главным образом, из пищи через желудочно-кишечный тракт в форме неорганического фосфора, который затем выводится через почки в виде мочи (непатентная литература 1).
Абсорбция фосфора через пищеварительный тракт, выведение его через почки и поглощение и/или метаболизм в костях находятся под контролем воздействия витамина D, паратиреоидного гормона (PTH) и т.д., и таким образом, уровень фосфора в крови поддерживается постоянным.
В случае почечной недостаточности, гиперфосфатемия, при которой уровень фосфора в крови показывает чрезвычайно высокое значение, развивается во многих случаях вследствие сокращения выведения фосфорной кислоты из почек. Чрезмерное количество фосфорной кислоты связывает кальций крови и вызывает эктопическую кальцификацию в сердечно-сосудистой системе, таким образом, становясь фактором риска для сердечно-сосудистых заболеваний, таких как инфаркт миокарда (непатентная литература 2).
Кроме того, гиперфосфатемия вызывает вторичную гипокальциемию и в качестве компенсации, приводит к развитию гиперпаратиреоза, характеризующегося увеличением уровня PTH в крови. Это также становится главным фактором для развития почечной остеодистрофии. Как указано выше, гиперфосфатемия при хронической почечной недостаточности у пациентов снижает качество жизни (QOL) пациентов из-за перелома кости, боли в костях и т.д., и в то же время, она становится основным фактором, приводящим к смерти пациентов с хронической почечной недостаточностью.
[0003] В настоящее время в качестве терапевтического лекарственного средства против гиперфосфатемии используется фосфатный адсорбент, который адсорбирует фосфорную кислоту в ЖКТ и тем самым подавляет ее всасывание, а также диетические ограничения. В качестве пероральных адсорбентов используются различные лекарственные препараты, такие как препараты на основе кальция (осажденный карбонат кальция и др.), полимерные препараты (гидрохлорид севеламера) и препараты на основе солей металлов (гидроксид алюминия и карбонат лантана). Следует отметить, что отдельные препараты имеют проблемы.
Что касается препаратов на основе кальция, они продемонстрировали, что сосудистая кальцификация активируется благодаря гиперкальциемии (непатентная литература 3) и, что касается полимерных препаратов, они являются проблематичными с точки зрения соблюдения режима приема лекарственного средства, что вызывается введением в дозе нескольких граммов в день и симптомами пищеварения, такими как запор или диарея (непатентная литература 4).
Кроме того, что касается препаратов на основе солей металлов, они указывают на риск накопления в организме (непатентная книжной 5). Таким образом, отвечающее требованиям терапевтическое лекарственное средство против гиперфосфатемии пока еще не разработано.
Сообщалось, что перенос фосфата натрия, выраженный в небольших кишечных эпителиальных клетках, играет важную роль в поглощении неорганического фосфата через пищеварительный тракт (непатентная литература 6). Предполагается, что соединение, которое специально ингибирует активный перенос фосфата, может подавлять абсорбцию фосфора через пищеварительный тракт более эффективно, чем пероральные адсорбенты, и что оно может улучшить соблюдение режима приема лекарственного средства, которое было проблемой при пероральных адсорбентах, и может решить такие проблемы, как симптомы пищеварения и накопления.
В связи с вышеприведенными обстоятельствами, существует потребность в разработке новых препаратов для предупреждения или лечения гиперфосфатемии или заболевания, связанного с гиперфосфатемией.
Соединение, описанное в WO2011/136269, является релевантным соединению настоящего изобретения. Однако это соединение струкурно отличается от соединения настоящего изобретения.
Перечень цитируемой литературы
Патентная литература
[0004] Патентная литература 1: WO2011/136269
Непатентная литература
[0005] Непатентная литература 1: H. Murer et al., Pflugers Arch-Eur J Physiol (2004) 447: 763-767
Непатентная литература 2: F. Verbeke et al., Clinical Journal of the American Society of Nephrology 6, 153 (2011)
Непатентная литература 3: T. Kakuta et al., Am J Kidney Dis. 57(3): 422 (2011)
Непатентная литература 4: T. Maruyama et al., CLINICAL CALCIUM 19, 2, 100(248), (2009)
Непатентная литература 5: M. R. Wills, J. Savory J. Lancet 2, 29 (1983)
Непатентная литература 6: S. C. Schiavi et al., J Am Soc Nephrol 23: 1691, 2012
Сущность изобретения
Техническая проблема
[0006] Задачей настоящего изобретения является обеспечение соединения, которое является полезным в качестве активного ингредиента для предупреждения и лечения гиперфосфатемии, или его фармакологически приемлемой соли.
Решение проблемы
[0007] Настоящие авторы провели интенсивные исследования, направленные на разработку соединения, которое полезно в качестве активного ингредиента для предупреждения и лечения гиперфосфатемии. Как результат, авторы осуществили настоящее изобретение. Более конкретно, настоящее изобретение является таким, как описано ниже.
[0008] [1] Соединение, представленное общей формулой (I), или его фармакологически приемлемая соль:
где каждый заместитель является таким, как определено ниже:
R1 представляет собой C1-6алкильную группу, C1-6алкоксиC1-6алкильную группу, C3-6циклоалкильную группу или C3-6циклоалкилC1-6алкильную группу,
R2 представляет собой атом водорода или группу галогенов,
R3 представляет собой атом водорода, группу галогенов, галогенC1-6алкильную группу, галогенC1-6алкоксигруппу, насыщенную циклическую аминогруппу, диалкиламиногруппу, C3-6циклоалкилC1-6алкоксигруппу или алкоксигруппу,
A представляет собой C3-6циклоалкильное кольцо,
X представляет собой CH или N,
Y представляет собой CH или N,
Z представляет собой CH или N, и
n равен целому числу, выбранному из 1, 2, 3 и 4.
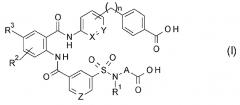
[0009] [2] Соединение согласно пункту [1] выше или его фармакологически приемлемая соль, где соединением, представленным общей формулой (I), является соединение, представленное общей формулой (I'):
[3] Соединение согласно пункту [1] или [2] выше или его фармакологически приемлемая соль, где R1 представляет собой метильную группу, этильную группу, метоксиэтильную группу, циклопропильную группу или циклопропилметильную группу.
[4] Соединение согласно любому из пунктов [1]-[3] выше или его фармакологически приемлемая соль, где R2 представляет собой атом водорода, атом хлора или атом брома.
[5] Соединение согласно любому из пунктов [1]-[4] выше или его фармакологически приемлемая соль, где R3 представляет собой атом водорода, атом фтора, атом хлора, атом брома, трифторметильную группу, 2,2,2-трифторэтоксигруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, диэтиламиногруппу, циклопропилметоксигруппу или метоксигруппу.
[6] Соединение согласно любому из пунктов [1]-[5] выше или его фармакологически приемлемая соль, где A представляет собой циклогексановое кольцо.
[7] Соединение согласно любому из пунктов [1]-[6] выше или его фармакологически приемлемая соль, где X, Y и Z, каждый представляет собой CH.
[8] Соединение согласно любому из пунктов [1]-[7] выше или его фармакологически приемлемая соль, где n равен 2.
[0010] [9] Соединение согласно пункту [1] или [2] выше или его фармакологически приемлемая соль, где каждый заместитель выбран из любого из следующих групп заместителей:
R1 представляет собой метильную группу, этильную группу, метоксиэтильную группу, циклопропильную группу и циклопропилметильную группу,
R2 представляет собой атом водорода, атом хлора и атом брома,
R3 представляет собой атом водорода, атом фтора, атом хлора, атом брома, трифторметильную группу, 2,2,2-трифторэтоксигруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, диэтиламиногруппу, циклопропилметоксигруппу и метоксигруппу,
A представляет собой циклогексановое кольцо,
X представляет собой CH и N,
Y представляет собой CH и N,
Z представляет собой CH и N, и
n равен 2 и 3.
[10] Соединение, выбранное из любого из группы следующих соединений или их фармакологически приемлемой соли:
[0011] [11] Соединение, представленное следующей формулой, или его фармакологически приемлемая соль:
[0012] [12] Соединение, представленное следующей формулой, или его фармакологически приемлемая соль:
[0013] [13] Соединение, представленное следующей формулой, или его фармакологически приемлемая соль:
[0014] [14] Соединение, представленное следующей формулой, или его фармакологически приемлемая соль:
[15] Фармакологически приемлемая соль согласно любому из пунктов [10]-[14] выше, которой является дикалиевая соль.
[16] Фармакологически приемлемая соль согласно любому из пунктов [10]-[14] выше, которой является динатриевая соль.
[17] Фармакологически приемлемая соль согласно пункту [15] или [16] выше, которой является ее гидрат.
[18] Фармацевтическая композиция, содержащая соединение согласно любому из пунктов [1]-[17] выше или его фармакологически приемлемую соль.
[19] Фармацевтическая композиция согласно пункту [18] выше, которая применяется для ингибирования усвоения фосфора.
[20] Фармацевтическая композиция согласно пункту [18] выше, которая применяется при предупреждении или лечении гиперфосфатемии.
[21] Применение соединения согласно любому из пунктов [1]-[17] выше или его фармакологически приемлемой соли для получения фармацевтической композиции для предупреждения или лечения гиперфосфатемии.
[22] Применение соединения согласно любому из пунктов [1]-[17] выше или его фармакологически приемлемой соли для предупреждения или лечения гиперфосфатемии.
[23] Способ предупреждения или лечения гиперфосфатемии, включающий введение эффективного количества соединения согласно любому из пунктов [1]-[17] выше или его фармакологически приемлемой соли.
Преимущество эффектов настоящего изобретения
[0015] Соединение, представленное общей формулой (I) настоящего изобретения, или его фармакологически приемлемая соль, может быть использовано в качестве профилактического и/или терапевтического средства против гиперфосфатемии и подобного.
Описание вариантов осуществления
[0016] В данном описании настоящее изобретение будет описано подробно.
[0017] Термины, такие как заместители, использованные в настоящем описании, имеют следующие значения.
Группа галогенов:
группа галогенов представляет собой атом фтора, атом хлора или атом брома.
C1-6Алкильная группа:
C1-6алкильная группа представляет собой линейную или разветвленную алкильную группу, содержащую 1-6 атомов углерода, и предпочтительные примеры включают
метильную группу, этильную группу, пропильную группу и изопропильную группу.
ГалогенC1-6алкильная группа:
галогенC1-6алкильная группа представляет собой линейную или разветвленную алкильную группу, содержащую 1-6 атомов углерода, которая замещена группой галогенов, и предпочтительные примеры включают трифторметильную группу, дифторметильную группу, 1,1-дифторэтильную группу, 2,2-дифторэтильную группу и 2,2,2-трифторэтильную группу.
ГалогенC1-6алкоксигруппа:
галогенC1-6алкоксигруппа представляет собой линейную или разветвленную алкоксигруппу, содержащую 1-6 атомов углерода, которая замещена группой галогенов, и предпочтительные примеры включают трифторметильную группу, дифторметильную группу, 1,1-дифторэтильную группу, 2,2-дифторэтильную группу и 2,2,2-трифторэтильную группу.
C1-6Акоксигруппа:
C1-6алкоксигруппа представляет собой C1-6алкильную группу, к которой присоединен атом кислорода, и предпочтительные примеры включают метоксигруппу, этоксигруппу, пропоксигруппу и изопропоксигруппу.
Насыщенная C2-5циклическая аминогруппа:
насыщенная C2-5циклическая аминогруппа представляет собой 3-6-членную насыщенную циклическую группу, имеющую атом азота в качестве атома, составляющего кольцо, и предпочтительные примеры включают азетидиновую группу, пирролидиновую группу, пиперидиновую группу, морфолиновую группу и пиперазиновую группу.
C1-6АлкоксиC1-6алкильная группа:
C1-6алкоксиC1-6алкильная группа представляет собой C1-6алкильную группу, замещенную C1-6алкоксигруппой, и предпочтительные примеры включают метоксиметильную группу, метоксиэтильную группу, метоксипропильную группу, этоксиметильную группу и этоксиэтильную группу.
C3-6Циклоалкильная группа:
C3-6циклоалкильная группа представляет собой 3-6-членную циклическую алкильную группу, и предпочтительные примеры включают циклопропильную группу, циклобутильную группу, циклопентильную группу и циклогексильную группу.
C3-6Циклоалкильное кольцо:
C3-6циклоалкильное кольцо представляет собой 3-6-членное циклическое алкильное кольцо. Предпочтительные примеры включают циклопропильное кольцо, циклобутильное кольцо, циклопентильное кольцо и циклогексильное кольцо. Боле предпочтительные примеры включают циклобутильное кольцо, имеющее связь в положении 1,3, циклопентильное кольцо, имеющее связь в положении 1,3, и циклогексильное кольцо, имеющее связь в положении 1,4.
C3-6ЦиклоалкилC1-6алкильная группа:
C3-6циклоалкилC1-6алкильная группа представляет собой C3-6циклоалкильную группу, к которой присоединена C1-6алкильная группа, и предпочтительные примеры включают циклопропилметильную группу, циклобутилметильную группу, циклопентилметильную группу, циклогексилметильную группу, циклопропилэтильную группу, циклобутилэтильную группу, циклопентилэтильную группу и циклогексилэтильную группу.
C3-6ЦиклоалкилC1-6алкоксигруппа:
C3-6циклоалкилC1-6алкоксигруппа представляет собой C3-6циклоалкильную группу, к которой присоединена C1-6алкоксигруппа, и предпочтительные примеры включают циклопропилметоксигруппу, циклобутилметоксигруппу, циклопентилметоксигруппу, циклогексилметоксигруппу, циклопропилэтоксигруппу, циклобутилэтоксигруппу, циклопентилэтоксигруппу и циклогексилэтоксигруппу.
C1-6Диалкиламиногруппа:
C1-6диалкиламиногруппа представляет собой аминогруппу, замещенную двумя C1-6алкильными группами, и предпочтительные примеры включают диметиламиногруппу, метилэтиламиногруппу, диэтиламиногруппу, этилпропиламиногруппу и дипропиламиногруппу.
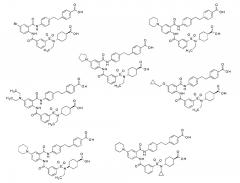
[0018] Предпочтительные примеры соединения, представленного общей формулой (I), включают соединения, описанные в примерах, и более предпочтительные примеры включают следующие соединения:
4-[2-(4-{[5-бром-2-({3-[(транс-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)бензоил]амино}фенил)этил]бензойную кислоту,
4-[2-(4-{[2-({3-[(транс-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)-5-(пирролидин-1-ил)бензоил]амино}фенил)этил]бензойную кислоту,
4-[2-(4-{[2-({3-[(транс-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)-5-(пиперидин-1-ил)бензоил]амино}фенил)этил]бензойную кислоту,
4-[2-(4-{[2-({3-[(транс-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)-5-(диэтиламино)бензоил]амино}фенил)этил]бензойную кислоту,
4-[2-(4-{[2-({3-[(цис-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)-5-(пиперидин-1-ил)бензоил]амино}фенил)этил]бензойную кислоту,
4-[2-(4-{[2-({3-[(транс-4-карбоксициклогексил)(этил)сульфамоил]бензоил}амино)-5-(циклопропилметокси)бензоил]амино}фенил)этил]бензойную кислоту, и
4-[2-(4-{[2-({3-[(транс-4-карбоксициклогексил)(циклопропил)сульфамоил]бензоил}амино)-5-(пиперидин-1-ил)бензоил]амино}фенил)этил]бензойную кислоту.
Структурные формулы этих соединений представляют собой следующие:
[0019] (Фармакологически приемлемая соль)
Термин "его фармакологически приемлемая соль" означает соль, которая может быть использована в качестве лекарственного средства. Когда соединение имеет кислотную группу или основную группу, "соль с основанием" или "кислотно-аддитивная соль" могут быть образованы путем подвергания данного соединения взаимодействию с основанием или кислотой. Термин "его фармакологически приемлемая соль" означает такую образованную соль.
Кроме того, "фармакологически приемлемая соль" также включает ее гидрат.
Предпочтительные примеры фармакологически приемлемой "соли с основанием" данного соединения включают: соли щелочного металла, такие как соль натрия, соль калия или соль лития; соли щелочноземельного металла, такие как соль магния или соль кальция; соли с органическим основанием, такие как соль N-метилморфолина, соль триэтиламина, соль трибутиламина, соль диизопропилэтиламина, соль дициклогексиламина, соль N-метилпиперидина, соль пиридина, соль 4-пирролидинoпиридина или соль пиколина; и соли аминокислоты, такие как соль глицина, соль лизина, соль аргинина, соль орнитина, соль глутамата или аспартата. Предпочтительные примеры включают соли щелочного металла и соли щелочноземельного металла.
[0020] Предпочтительные примеры фармакологически приемлемой "кислотно-аддитивной соли" соединения включают: соли неорганических кислот, включая гидрогалогениды, такие как гидрофторид, гидрохлорид, гидробромид или гидройодид, нитрат, перхлорат, сульфат и фосфат; соли органических кислот, включая низшие алкансульфонаты, такие как метансульфонат, трифторметансульфонат или этансульфонат, арилсульфонаты, такие как бензолсульфонат или п-толуолсульфонат, ацетат, малат, фумарат, сукцинат, цитрат, аскорбат, тартрат, оксалат и малеат; и соли аминокислот, такие как соль глицина, соль лизина, соль аргинина, соль орнитина, и аспартата. Среди других, гидрогалогениды (в частности, гидрохлорид) являются наиболее предпочтительными.
[0021] (Гидрат и т.д.)
Когда соединение настоящего изобретения или его фармакологически приемлемая соль остается на воздухе или подвергается перекристаллизации, имеет место случай, при котором соединение или его соль абсорбирует содержащуюся воду и, таким образом, содержит абсорбированную воду или преобразуется в гидрат. Настоящее изобретение включает различные типы таких гидратов, сольватов и кристаллических полиморфов.
[0022] (Изомер)
Соединение настоящего изобретения включает таутомеры или геометрические изомеры, в зависимости от типа заместителей. В настоящем описании соединение настоящего изобретения описано только как изомерная форма. Однако настоящее изобретение также включает другие изомеры и в дополнение оно включает разделенные изомеры или их смеси.
Существует случай, при котором соединение настоящего изобретения имеет асимметричные атомы углерода или являются аксиальнохиральными и, таким образом, могут присутствовать основанные на этом оптические изомеры. Настоящее изобретение также включает разделенные оптические изомеры или их смесь.
(Изотоп)
Соединение настоящего изобретения включает меченую форму, а именно, соединение, один или два или более атомов которого заменены изотопами (например, 2H, 3H, 13C, 14C, 35S и т.д.).
[0023] (Пролекарство)
Настоящее изобретение включает фармакологически приемлемое пролекарство соединения настоящего изобретения. Фармакологически приемлемое пролекарство представляет собой соединение, имеющее группу, которая может преобразовываться в аминогруппу, гидроксильную группу, карбоксильную группу или подобную при сольволизе или в физиологических условиях. Примерами таких групп, формирующих пролекарство, являются группы, описанные в Prog. Med., 5, 2157-2161 (1985).
Более конкретные примеры пролекарства включают:
когда соединения имеют аминогруппы,
соединения, в которых аминогруппы являются ацилированными, алкилированными или фосфорилированными (например, соединения, у которых аминогруппы являются эйкозаноилированными, аланилированными, пентиламинокарбонилированными, (5-метил-2-оксо-1,3-диоксолен-4-ил)метоксикарбонилированными, тетрагидрофуранилированными, пирролидилметилированными, пивалоилоксиметилированными или трет-бутилированными);
когда соединения имеют гидроксильные группы,
соединения, у которых гидроксильные группы являются ацилированными, алкилированными, фосфорилированными или борированными (например, соединения, у которых гидроксильные группы являются ацетилированными, пальмитоилированными, пропаноилированными, пивалоилированными, сукцинилированными, фумарилированными, аланилированными или диметиламинометилкарбонилированными); и
когда соединения имеют карбоксигруппы,
соединения, у которых карбоксигруппы являются этерифицированными или амидированными (например, соединения, у которых карбоксигруппы являются этил-этерифицированными, фенил-этерифицированными, карбоксиметил-этерифицированными, диметиламинометил-этерифицированными, пивалоилоксиметил-этерифицированными, этоксикарбонилоксиэтил-этерифицированными, амидированными или метиламидированными).
[0024] (Способ получения)
Соединение настоящего изобретения и его фармакологически приемлемая соль могут быть получены различными известными синтетическими способами, используя характеристики, основанные на их базовой структуре или типах заместителей.
При производстве существует вероятность, что эффективная с точки зрения технологии производства функциональная группа замещается подходящей защитной группой (группой, которая может быть легко преобразована в функциональную группу) в ходе проведения стадий от исходных веществ до промежуточных соединений, в зависимости от типа функциональной группы. Примеры таких защитных групп включают защитные группы, описанные в P. G. M. Wuts and T. W. Greene, Greene's Protective Groups in Organic Synthesis (4th edition, 2006). Такие защитные группы могут быть соответствующим образом выбраны и использованы в зависимости от реакционных условий.
В таком способе после введения защитной группы и последующего проведения реакции, требуемое соединение может быть получено удалением защитной группы, при необходимости. Более того, как в случае указанной выше защитной группы, пролекарство соединения настоящего изобретения может быть получено введением специфической группы в ходе проведения стадий от исходных веществ до промежуточного соединения или после дополнительного проведения реакции с использованием полученного соединения. Реакция может быть осуществлена при применении общеизвестных способов, таких как этерификация, амидирование или дегидратация.
[0025] В данном описании способы получения соединения будут описаны. Однако способ получения не ограничивается следующими способами.
[Способ A]
Способ A представляет собой способ получения соединения (A-II) и (A-III) настоящего изобретения.
Способ А
где R1, R2, R3, A, X, Y, Z и n являются такими, как определено выше, R4 и R5, которые являются одинаковыми или различными, каждый представляет собой любую группу, выбранную из C1-6алкильных групп, и M представляет собой металл, который образует соль с карбоксигруппой.
[0026] (Стадия A-1) Стадия гидролиза сложного эфира
Это является стадией гидролиза сложного эфира соединения (A-I) в присутствии основания в растворителе с получением соединения (A-II).
Предпочтительные примеры основания, используемого в данном случае, включают гидроксиды щелочных металлов, такие как гидроксид натрия или гидроксид лития. Предпочтительным примером растворителя, используемого в данном случае, является смешанный с водой растворитель и смесь тетрагидрофуран/метанол.
Температура реакции, как правило, составляет приблизительно от 20°C до 60°C, и время реакции, как правило, составляет приблизительно 1-10 часов.
(Стадия A-2) Стадия преобразования карбоновой кислоты в соль
Это является стадией обработки соединения (A-II) алкоксидом щелочного металла, таким как трет-бутоксид калия, для преобразования его в соль. Таким же способом могут быть получены различные неорганические и органические соли.
Например, соединение (A-II) растворяют в растворителе, таком как тетрагидрофуран, и затем к раствору добавляют трет-бутоксид калия при температуре приблизительно 0°C-40°C, преобразуя, таким образом, соединение в соль, с получением калиевой соли.
[0027] [Способ B]
Способ B представляет собой способ получения соединения (B-III), которое соответствует соединению (A-I), использованному в способе A.
Способ В
где R1, R2, R3, A, X, Y, Z и n являются такими, как определено выше, R4 и R5, которые являются одинаковыми или различными, каждый представляет собой любые группы, выбранные из C1-6алкильных групп.
[0028] (Стадия B-1) Стадия образования амида конденсацией
Это является стадией получения соединения (B-III) (i) путем взаимодействия карбонокислотного соединения (B-II) с оксалилхлоридом для его активации и последующего взаимодействия полученного соединения (B-II) с соединением (B-I) или (ii) путем взаимодействия соединения (B-II) с соединением (B-I) в присутствии конденсирующего агента.
В случае (i), например, оксалилхлорид и небольшое количество диметилформамида добавляют в раствор соединения (B-II) в метиленхлориде при температуре от 0°C до комнатной температуры, и полученную смесь оставляют на некоторое время и после этого соединение (B-I) и основание, такое как пиридин, добавляют в реакционный раствор при температуре от 0°C до комнатной температуры. Как правило, температура реакции составляет приблизительно от комнатной температуры до приблизительно 80°C, и время реакции составляет приблизительно 1-24 часа.
В случае (ii), например, основание и конденсирующий агент добавляют в раствор соединения (B-I) и соединения (B-II) в диметилформамиде или метиленхлориде, и затем осуществляют реакцию. Как правило, температура реакции составляет приблизительно от комнатной температуры до приблизительно 80°C, и время реакции составляет приблизительно 1-24 часа.
В качестве основания, используемого в данном случае, предпочтительным является третичный амин, такой как диизопропилэтиламин.
Примеры конденсирующего агента, используемого в данном случае, включают:
гексафторфосфат 1-[бис(диметиламино)метилен]-1H-бензотриазолий-3-оксида (здесь и далее также называемый, как "HBTU"),
гексафторфосфат 2-(1H-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (здесь и далее также называемый, как "HATU"),
н-гидрат 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолинийхлорида (здесь и далее также называемый, как "DMT-MM") и
гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (здесь и далее также называемый как "WSC" или "EDCI").
[0029] [Способ C]
Способ C представляет собой способ получения соединения (C-IV), которое соответствует соединению (B-I), использованному в способе B.
На стадии C-1, когда реакцию осуществляют с использованием соединения (C-I), в котором нитрогруппу заменяют аминогруппой, соединение (C-IV) может быть получено без проведения стадии C-2.
Способ С
где R2, R3, X, Y и n являются такими, как определено выше, и R4 представляет собой любую группу, выбранную из C1-6алкильных групп.
[0030] (Стадия C-1) Стадия образования амида конденсацией
Это является стадией получения амида в условиях, аналогичных условиям стадии B-2 способа B.
(Стадия C-2) Стадия восстановления нитрогруппы до формы аминогруппы
Это является стадией взаимодействия раствора соединения (C-III) в атмосфере водорода в присутствии металлического катализатора, такого как 10% палладий на углероде.
Предпочтительные примеры растворителя, используемого в данном случае, включают простые эфиры, такие как тетрагидрофуран, спирты, такие как этанол, и смешанный растворитель тетрагидрофуран/этанол.
Как правило, температура реакции составляет приблизительно от комнатной температуры до приблизительно 60°C, и время реакции составляет приблизительно 1-10 часов.
Кроме того, настоящая стадия также может быть осуществлена путем проведения реакции восстановления с использованием порошка железа и аммонийхлорида при нагревании при кипячении с обратным холодильником в смеси растворителей этанол/вода.
[0031] [Способ D]
Способ D представляет собой способ получения соединения (D-IV), которое соответствует соединению (C-III), использованному в способе C. В способе C заместитель, соответствующий R3, уже был введен во время начальной стадии. Когда заместитель, соответствующий R3, представляет собой группу, такую как насыщенная циклическая аминогруппа или диалкиламиногруппа, R3 может быть введен проведением стадий, таких как стадия D-1 и стадия D-2, как в случае способа D. В данном случае, соединение, имеющее пиперидиновую группу, проиллюстрировано группой, такой как насыщенная циклическая аминогруппа или диалкиламиногруппа.
Способ D
где R2, X, Y и n являются такими, как определено выше, и R4 представляет собой любую группу, выбранную из C1-6алкильных групп.
[0032] (Стадия D-1) Стадия образования амида конденсацией
Это является стадией получения амида в условиях, аналогичных условиям на стадии C-1 способа C.
(Стадия D-2) Стадия введения заместителя в бензольное кольцо реакцией замещения
Это является стадией добавления насыщенного циклического амина, такого как пирролидин, пиперидин или диэтиламин или диалкиламин, в раствор соединения (D-III) и последующего проведения реакции.
В качестве растворителя, используемого в данном случае, предпочтительными являются простые эфиры, такие как тетрагидрофуран.
Температура реакции, как правило, составляет от комнатной температуры до 80°C, и время реакции составляет приблизительно 1-24 часа.
[0033] [Способ E]
Как правило, соединение, соответствующее соединению (C-II), использованному в способе C, может быть легко получено согласно известному способу. Так, например, в способе E будет описан способ получения соединения (E-IV), которое соответствует соединению (C-II).
Способ Е
где X и Y являются такими, как определено выше, и R4 представляет собой любую группу, выбранную из C1-6алкильных групп.
[0034] (Стадия E-1) Стадия образования двойной связи реакцией сочетания
Это является стадией обработки соединения (E-I) основанием и последующего подвергания соединения (E-I) взаимодействию с соединением (E-II) с получением соединения (E-III).
В качестве основания, используемого в данном случае, в дополнение к гидриду щелочного металла, такому как гидрид натрия, могут быть использованы основания, которые обычно используются в такой реакции.
В качестве растворителя, используемого в данном случае, предпочтительными являются простые эфиры, такие как тетрагидрофуран.
Температура реакции, как правило, составляет от 0°C до 80°C, и время реакции составляет приблизительно 1-24 часа.
(Стадия E-2) Стадия восстановления двойной связи реакцией гидрирования
Это является стадией получения соединения (E-IV) в условиях, аналогичных условиям на стадии C-2 способа C.
[0035] [Способ F]
Способ F представляет собой способ получения соединения (F-VII), соответствующего соединению (D-IV), использованному в способе D. Способ F отличается тем, что часть, соответствующую соединению (D-II) в способе D, получают на последующей стадии (стадия F-3).
Способ F
где R2, X и Y являются такими, как определено выше, и R4 представляет собой любую группу, выбранную из C1-6алкильных групп.
[0036] (Стадия F-1) Стадия образования амида конденсацией
Это является стадией получения соединения (F-III) в условиях, аналогичных условиям на стадии C-1 способа C.
(Стадия F-2) Стадия введения заместителя в бензольное кольцо реакцией замещения
Это является стадией получения соединения (F-IV) в условиях, аналогичных условиям на стадии D-2 способа D.
(Стадия F-3) Стадия проведения реакции сочетания с использованием катализатора переходного металла
Это является стадией подвергания соединения (F-IV) реакции сочетания с соединением (F-V) с получением соединения (F-VI). Например, соединение (F-IV) растворяют в простом эфире, таком как тетрагидрофуран, и затем добавляют в полученный раствор катализатор, такой как йодид меди(I) или бис(трифенилфосфин)палладий(II)хлорид, и амин, такой как триэтиламин. После этого реакцию осуществляют при температуре приблизительно от комнатной температуры до приблизительно 60°C в течение приблизительно 1-24 часов.
В качестве растворителя, используемого в данном случае, в дополнение к простым эфирам, могут быть использованы различные растворители, такие как диметилформамид, толуол, ацетонитрил или этанол.
В качестве катализатора, используемого в данном случае, в дополнение к бис(трифенилфосфин)палладий(II)хлориду, могут быть использованы катализаторы, содержащие различные переходные металлы и различные лиганды, такие как тетракис(трифенилфосфин)палладий(0).
В качестве амина, используемого в данном случае, в дополнение к триэтиламину, могут быть использованы различные амины, такие как диизопропилэтиламин, диэтиламин или диизопропиламин.
(Стадия F-4) Стадия восстановления тройной связи реакцией гидрирования
Это является стадией получения соединения (F-VII) в условиях, аналогичных условиям на стадии C-2 способа C.
[0037] [Способ G]
Способ G представляет собой способ получения соединения (G-IV), соответствующего соединению (B-II), использованному в способе B.
Способ G
где R1, R5, A и Z являются такими, как определено выше, и Pc представляет собой защитную группу карбоксигрупп, такую как триметилсилилэтильная группа, бензильная группа или трет-бутильная группа.
[0038] (Стадия G-1) Стадии этерификации и сульфонамидирования
(1) Это является стадией подвергания соединения (G-I) взаимодействию с 2-TMS-этанолом, бензиловым спиртом или подобным в присутствии основания для его этерификации (где TMS обозначает триметилсилильную группу).
В качестве основания предпочтительно используют пиридин, диизопропилэтиламин или подобное, и в качестве растворителя, как правило, используют метиленхлорид.
Температура реакции, как правило, составляет от 0°C до комнатной температуры, и время реакции, как правило, составляет приблизительно 2 часа.
(2) Это является стадией подвергания полученного соединения (G-I) дальнейшему взаимодействию с соединением (G-II) в присутствии основания с получением соединения (G-III).
В качестве основания предпочтительно используют пиридин, и в качестве растворителя, как правило, используют метиленхлорид.
Температура реакции, как правило, составляет приблизительно от 0°C до 40°C, и время реакции, как правило, составляет приблизительно 2 часа.
(Стадия G-2) Стадии N-алкилирования и снятия защиты
(1) Это является стадией подвергания соединения (G-III) взаимодействию с R1-I в присутствии основания для его N-алкилирования.
В качестве основания, как правило, используют карбонат калия, и в качестве растворителя используют диметилформамид.
Температура реакции, как правило, составляет приблизительно от комнатной температуры до приблизительно 60°C, и время реакции, как правило, составляет приблизительно от 1 часа до 3 дней.
(2) Это является стадией дополнительного проведения реакции в условиях общеизвестного снятия защиты с карбоксигрупп с получением соединения (G-IV).
Когда защитной группой является TMS-этильная группа, тетрабутиламмонийфторид, как правило, добавляют к раствору тетрагидрофурана и затем осуществляют реакцию.
Температура реакции, как правило, составляет приблизительно комн