Ингибиторы hdac
Иллюстрации
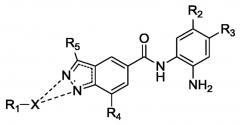
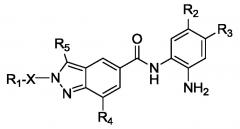
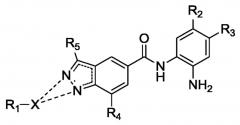
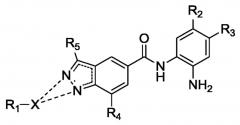
Показать всеИзобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, в которой R1-X присоединен только к одному из кольцевых атомов азота. X представляет собой -Y-[C(Ra)2]a-, где Y представляет собой связь; Ra представляет собой Н; а равен 1, 2 или 3. R1 представляет собой: (i) моноциклический бициклический гетероарил, содержащий 5-6 кольцевых атомов, который необязательно замещен 1-3 Ro; причем 1-2 кольцевых атома представляют собой гетероатом, независимо выбранный из N и N-Ro; (ii) фенил, который необязательно замещен 1-3 Ro; или (iii) C3-C10 циклоалкил. R4 представляет собой H. Каждый вариант Ro независимо выбран из группы, состоящей из галогена; C1-C6 алкила и фтор(C1-C6)алкила. R5 представляет собой водород, R2 представляет собой H и R3 представляет собой H, F или Cl. Соединение формулы (I) ингибирует ферменты гистондеацетилазы (HDAC), например HDAC1, HDAC2 и HDAC3. Изобретение также относится к фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, способам ингибирования указанных ферментов с применением соединения формулы (I) и способам лечения заболеваний, опосредованных указанными ферментами. 10 н. и 30 з.п. ф-лы, 5 табл., 1 пр.
(I).
Реферат
Перекрестная ссылка на родственные заявки
[0001] Настоящая заявка заявляет приоритет предварительной заявки на патент США № 61/800170, поданной 15 марта 2013 года, и предварительной заявки на патент США № 61/863235, поданной 7 августа 2013 года, описания которых включены в данный документ в полном объеме посредством ссылки.
Область техники
[0002] Настоящее изобретение, в общем, направлено на соединения, которые могут ингибировать ферменты гистондеацетилазы (“HDAC”) (например, HDAC1, HDAC2 и HDAC3).
Уровень техники
[0003] До настоящего времени у людей было идентифицировано 18 HDAC, и при этом появляется все больше доказательств, подтверждающих, что у людей 18 гистондеацетилаз (HDAC) не являются избыточными по функции. HDAC классифицируют на три основные группы исходя из их гомологии к дрожжевым белкам. Класс I включает в себя HDAC1, HDAC2, HDAC3 и HDAC8 и характеризуется гомологией к дрожжевому RPD3. HDAC4, HDAC5, HDAC7 и HDAC9 относятся к классу IIa и характеризуются гомологией к дрожжевому HDAC1. HDAC6 и HDAC10 содержат два каталитических участка и классифицируются как класс IIb, при этом HDAC11 содержит консервативные остатки в своем каталитическом центре, которые являются общими для деацетилаз класса I и класса II, и помещается в класс IV. Такие HDAC содержат в своем каталитическом участке цинк и ингибируются соединениями, подобными трихостатину A (TSA) и вориностату [субероиланилид гидроксамовой кислоты (SAHA)]. HDAC класса III известны как сиртуины. Они характеризуются гомологией к дрожжевому Sir2, зависят от NAD+ в качестве кофактора и не содержат цинка в каталитическом участке. В целом ингибиторы HDAC цинк-зависимых HDAC содержат Zn-связывающую группу, а также поверхностный домен распознавания.
[0004] HDAC вовлекаются в регулирование ряда клеточных процессов. Гистонацетилтрансферазы (HAT) и HDAC ацетилируют и деацетилируют лизиновые остатки на N-конце гистоновых белков, посредством чего влияют на транскрипционную активность. Для них также была продемонстрирована регуляция посттрансляционного ацетилирования по меньшей мере 50 негистоновых белков, таких как α-тубулин (смотрите, например, Kahn, N et al Biochem J 409 (2008) 581, Dokmanovic, M et al Mol Cancer Res 5 (2007) 981).
[0005] Изменение экспрессии гена посредством модификации хроматина может сопровождаться ингибированием ферментов гистондеацетилаз (HDAC). Существует доказательство того, что ацетилирование и деацетилирование гистонов представляют собой механизмы, посредством которых достигается транскрипционное регулирование в клетке - главное событие при клеточной дифференциации, пролиферации и апоптозе. Было выдвинуто предположение, что такие эффекты возникают за счет изменений в структуре хроматина из-за изменения сродства гистоновых белков к спиральной ДНК в нуклеосоме. Считается, что гипоацетилирование гистоновых белков повышает взаимодействие гистона с фосфатным остовом ДНК. Более крепкое связывание между гистоновым белком и ДНК может обеспечить недоступность ДНК для транскрипционных регуляторных элементов и механизмов. Для HDAC была продемонстрирована способность катализировать удаление ацетильных групп из ε-аминогрупп лизиновых остатков, присутствующих в N-концевом плече коровых гистонов, что приводит к гипоацетилированию гистонов и блокированию транскрипционного механизма и регуляторных элементов.
[0006] Поэтому ингибирование HDAC может привести к гистондеацетилаза-опосредованной транскрипционной дерепрессии генов-супрессоров опухолевого роста. Например, клетки, обработанные в культуре ингибиторами HDAC, продемонстрировали соответствующую индукцию ингибитора p21 киназы, который играет важную роль в блокировке клеточного цикла. Как полагают, ингибиторы HDAC повышают скорость транскрипции p21 за счет распространения гиперацетилированного состояния гистонов в области гена p21, посредством чего обеспечивается доступность гена для транскрипционного механизма. Дополнительно, негистоновые белки, вовлеченные в регулирование гибели клеток и клеточного цикла, также подвергаются ацетилированию и деацетилированию лизина посредством HDAC и гистонацетилтрансферазы (HAT).
[0007] Данный факт подтверждает применение ингибиторов HDAC при лечении различных типов рака. Например, вориностат (субероиланилид гидроксамовой кислоты (SAHA)) был одобрен FDA для лечения кожной Т-клеточной лимфомы и исследуется в отношении лечения солидных и гематологических опухолей. Дополнительно, другие ингибиторы HDAC находятся на стадии разработки для лечения острого миелоидного лейкоза, болезни Ходжкина, миелодиспластических синдромов и солидных злокачественных опухолей. Избирательные ингибиторы HDAC1/2 могут быть пригодными при лечении острого В-клеточного лимфобластного лейкоза (B-ALL) (Stubbs, et al., Selective Inhibition of HDAC1 and HDAC2 is a Potential Therapeutic Option for B-ALL, Molecular Pharmacology, Drug Resistance: Poster II, Poster Board II-780 (December 5, 2010), и Witter et al., Bioorg. Med. Chem. Lett., 18: 726-731 (2008), а также Fournel et al., Mol. Cancer Ther. 7(4): 759-68 (2008)).
[0008] Для ингибиторов HDAC также было продемонстрировано ингибирование провоспалительных цитокинов, таких как цитокины, вовлеченные в аутоиммунные и воспалительные расстройства (например, TNF-α). Например, для ингибитора HDAC MS275 было продемонстрировано замедление прогрессирования заболевания и деструкции сустава при коллаген-индуцированном артрите в крысиной и мышиной моделях. Для других ингибиторов HDAC было продемонстрировано наличие эффективности при лечении или уменьшении интенсивности воспалительных расстройств или состояний в моделях in vivo или испытаниях в отношении расстройств, таких как болезнь Крона, колит, а также воспаление дыхательных путей и гиперчувствительность. Для ингибиторов HDAC также было продемонстрировано уменьшение интенсивности воспаления спинного мозга, демиелинизации, а также потери нервных клеток и потери аксонов при экспериментальном аутоиммунном энцефаломиелите (смотрите, например, Wanf L. et al., Nat Rev Drug Disc, 8: 969 (2009)).
[0008] Экспансия триплетных повторов в геномной ДНК связана с множеством неврологических состояний (например, нейродегенеративными и нейромышечными заболеваниями), в том числе миотонической дистрофией, спинальной мышечной атрофией, синдромом ломкой X-хромосомы, болезнью Хантингтона, спинально-церебеллярной атаксией, амиотрофическим латеральным склерозом, болезнью Кеннеди, спинальной и бульбарной мышечной атрофией, атаксией Фридрейха и болезнью Альцгеймера. Экспансия триплетных повторов может вызывать заболевание за счет изменения экспрессии гена. Например, при болезни Хантингтона, спинально-церебеллярной атаксии, синдроме ломкой X-хромосомы и миотонической дистрофии увеличенное число повторов приводит к сайленсингу гена. При атаксии Фридрейха отклонение в ДНК, обнаруженное у 98% пациентов с FRDA, представляет собой неустойчивую гиперэкспансию повтора триплета GAA в первом интроне гена фратаксина (смотрите Campuzano et al., Science 271: 1423 (1996)), что приводит к недостаточности фратаксина, приводящей к прогрессирующей спинально-церебеллярной нейродегенерации. Поскольку они могут воздействовать на транскрипцию и потенциально корректировать транскрипционную дисрегуляцию, для ингибиторов HDAC было испытано и продемонстрировано положительное воздействие в отношении нейродегенеративных заболеваний (смотрите Herman D et al, Nat Chem Bio 2: 551 (2006) для атаксии Фридрейха, Thomas EA et al, Proc Natl Acad Sci USA 105: 15564 (2008) для болезни Хантингтона).
[0010] Ингибиторы HDAC также могут играть определенную роль при связанных с когнитивностью состояниях и заболеваниях. Действительно, все более очевидным становится тот факт, что транскрипция, вероятно, представляет собой ключевой элемент для процессов долговременной памяти (Alberini CM, Physiol Rev 89: 121 (2009)), таким образом, выделяя другую роль для проникающих в ЦНС ингибиторов HDAC. Несмотря на то, что исследования продемонстрировали, что лечение с применением неспецифических ингибиторов HDAC, таких как бутират натрия, может привести к формированию долговременной памяти (Stefanko DP et al, Proc Natl Acad Sci USA 106: 9447 (2009)), мало известно о роли конкретных изоформ. Небольшое количество исследований продемонстрировало, что в классе I HDAC, главной мишени бутирата натрия, прототипного ингибитора, применяемого в исследованиях когнитивности, HDAC2 (Guan J-S et al, Nature 459: 55 (2009)) и HDAC3 (McQuown SC et al, J Neurosci 31: 764 (2011)), как было показано, регулируют процессы памяти, и как таковые являются представляющими интерес мишенями для улучшения памяти или уменьшения интенсивности при состояниях с воздействием на память, таких как, но не ограничиваясь этим, болезнь Альцгеймера, посттравматическое стрессовое расстройство или привыкание к лекарственным средствам.
[0011] Ингибиторы HDAC, например, избирательные ингибиторы HDAC1 и/или HDAC2, также могут применяться для лечения серповидноклеточной болезни (SCD) и β-талассемии (bT). Они также могут применяться при лечении аффективных расстройств или расстройств головного мозга с измененной хроматин-опосредованной нейропластичностью (Schoreder, et al., PLoS ONE 8(8): e71323 (2013)).
[0012] Ингибиторы HDAC также могут применяться для лечения инфекционного заболевания, такого как вирусные инфекции. Например, посредством обработки ВИЧ-инфицированных клеток ингибиторами HDAC и антиретровирусными лекарственными препаратами возможно уничтожение вируса в обработанных клетках (Blazkova j et al J Infect Dis. 2012 Sep 1; 206(5): 765-9; Archin NM et al Nature 2012 Jul 25, 487(7408): 482-5).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0013] Настоящее изобретение предлагает соединения формулы (I) или их фармацевтически приемлемую соль:
(I),
композиции (например, фармацевтические композиции), содержащие таковые, а также способы с применением таковых. Для целей ясности формула (I) охватывает обе формулы (Ia) и (Ib) ниже:
(Ia), (Ib).
[0014] Соединения формулы (I), описанные в данном документе, ингибируют ферменты гистондеацетилазы (“HDAC”) (например HDAC1, HDAC2 и HDAC3). Не ограничиваясь какой-либо теорией полагают, что орто-амино(NH2)бензамидная часть соединений формулы (I) взаимодействует с (например, связывается с) цинком в цинк-зависимых HDAC.
[0015] Однако, как будет понятно специалисту в данной области техники, расщепление амидной связи в соединениях формулы (I) (например, во время метаболизма соединений формулы (I), часто изучаемого с применением метаболизма in vitro соединений формулы (I) в присутствии гепатоцитов) потенциально может привести к высвобождению o-фенилендиамина (OPD). OPD представляет собой органическое соединение химической формулы, показанной ниже:
[0016] OPD представляет собой известный канцероген для животных и потенциальный канцероген для человека. Его, главным образом, применяют в качестве промежуточного химического соединения в синтезе красок, пигментов и фунгицидов. OPD представляет собой относительно нестабильную молекулу даже в его твердом состоянии. OPD может вызвать острое отравление у животных, которое может привести к тремору, конвульсиям, слюноотделению и дыхательной недостаточности [1]. Несмотря на то, что OPD относят к канцерогену для животных, исследования по установлению его значимости для людей, а также эффектов однократного и многократного воздействия OPD на людей являются недостаточными [2]. Неблагоприятные эффекты OPD, такие как генотоксичность, репродуктивная токсичность, аллергические реакции и канцерогенность, сообщаются в нескольких исследованиях на животных [1]. Sontag et al (1981) сообщают, что в течении 78 недель пероральное введение OPD приводит к значительному увеличению опухолей печени у самцов крыс - 5 из 16 крыс оказались подверженными воздействию в группе с введением высокой дозы 16000 мг/кг OPD, при этом у 5 из 17 были обнаружены опухоли в группе с низкой дозой при 8000 мг/кг [3, 4]. В статье от NCI описывают образование опухоли на мочевом пузыре и преджелудке как у самцов, так и у самок крыс, а также гепатоцеллюлярную карциному у мышей обоих полов после дозировки OPD [5]. В ней также OPD представлен как безусловный канцероген для крыс Фишера 344 и мышей B6C3FI [5].
[0017] Напротив, в исследованиях Saruta et al (1962) не было отмечено образование опухолей в результате подкожного введения OPD крысам. Группам из 5 крыс вводили низкую дозу 45 мг/кг каждый второй день в течение 11 месяцев и высокую дозу 90 мг/кг каждый второй день в течение 5 месяцев. Ни в одной из двух групп опухоли не обнаруживали [1, 6]. Несмотря на это, OPD был классифицирован как потенциальный канцероген человека ACGIH в 1989 году [2].
[0018] Однако авторы настоящего изобретения обнаружили, что метаболиты соединения формулы (I) практически не содержат OPD, когда соединения формулы (I) подвергаются условиям, предназначенным для имитации метаболических путей in vivo. Применяемый в данном документе термин “практически не содержит OPD” означает, что OPD не обнаруживали с помощью ЖХ-МС/МС после (i) инкубирования соединения формулы (I) в гепатоцитах человека, обезьяны, собаки и крысы и (ii) обработки среды метаболита кислым раствором фенилглиоксаля в органическом растворителе (данное добавление приводит к количественно определяемому образованию 2-фенилхиноксалина, который может быть легко количественно определен при низком нижнем пределе количественного определения (LLOQ)). Смотрите раздел примеров.
[0019] В некоторых вариантах осуществления изобретения, соединения формулы (I), описанные в данном документе, проявляют дополнительные характеристики, например, являются ценными для разработки в качестве фармацевтически применимых соединений, демонстрируя относительно сниженное связывание с белками плазмы (например связывание менее 99%, например связывание от 65% до 95%, например связывание от 75% до 95%, например связывание 75%).
Соответственно, в одном аспекте представлено соединение формулы (I) или его фармацевтически приемлемая соль:
(I),
в которой:
R1-X присоединен только к одному из кольцевых атомов азота;
X представляет собой:
(i) -Y-[C(Ra)2]a-A-[C(Rb)2]b-B-;
(ii) прямую связь; или
(iii) C=O, C(Rj)2-C(=O), C(=O)-C(Rj)2, SO2-NRk, NRk-SO2, C(=O)NRk или NRk-C(=O);
где
Y представляет собой связь, CRc=CRd, O, NRe или S(O)m;
каждый из A и B независимо представляет собой связь, O, NRf или S(O)m;
a равен 1, 2 или 3;
b равен 0, 1, 2 или 3;
m равен 0, 1 или 2;
каждый вариант Ra и Rb независимо выбран из H, F, OH, C1-C6 алкила, C3-C6 циклоалкила, NH2, OCO-(C1-C6 алкила), OCO-(C3-C6 циклоалкила), C1-C6 алкокси, C1-C6 фторалкокси и циано; или
одно или более из следующего может применяться по отношению к Ra и Rb:
любые два Ra вместе с атомами углерода, к которым каждый присоединен, вместе образуют C3-C6 циклоалкил или гетероциклил, содержащий 3-6 атомов в кольце, в котором один из кольцевых атомов гетероциклила выбран из O, S(O)m и NRg; или
один Ra и один Rb вместе с атомами углерода, к которым каждый присоединен, образуют C3-C6 циклоалкил или гетероциклил, содержащий 3-6 атомов в кольце, в котором один из кольцевых атомов гетероциклила выбран из O, S(O)m и NRg; или
любые два Rb вместе с атомами углерода, к которым каждый присоединен, образуют C3-C6 циклоалкил или гетероциклил, содержащий 3-6 атомов в кольце, в котором один из кольцевых атомов выбран из O, S(O)m и NRg;
каждый из Rc и Rd независимо выбран из H, F, OH, C1-C6 алкила, C3-C5 циклоалкила, NH2, OCO-(C1-C6 алкила), OCO-(C3-C5 циклоалкила), C1-C6 алкокси, C1-C6 фторалкокси и циано;
или Rc и Rd вместе с атомами углерода, к которым каждый присоединен, образуют C5-C7 циклоалкил или гетероциклил, содержащий 3-6 атомов в кольце, в котором 1-2 кольцевых атома гетероциклила независимо выбраны из O, S(O)m и NRg';
каждый вариант Re, Rf, Rg и Rg' независимо выбран из H, C1-C6 алкила, -C(=O)H, -C(=O)Rh, C(=O)O(C1-C6 алкила), C(=O)N(Ri)2 и SO2-Rh; где Rh выбран из C1-C6 алкила, CH2-(гетероарила, содержащего 5-10 атомов в кольце), CH2-(C6-C10 арила) и C6-C10 арила; и каждый вариант Ri независимо выбран из H, C1-C6 алкила, CH2-(гетероарила, содержащего 5-10 атомов в кольце), CH2-(C6-C10 арила) и C6-C10 арила;
каждый вариант Rj независимо выбран из H, F, OH, C1-C6 алкила, C3-C6 циклоалкила, NH2, OCO-(C1-C6 алкила), OCO-(C3-C6 циклоалкила), C1-C6 алкокси, C1-C6 фторалкокси и циано;
или Rj-C-Rj вместе образуют C3-C6 циклоалкил или гетероциклил, содержащий 3-6 атомов в кольце, в котором один из кольцевых атомов гетероциклила выбран из O; S(O)m и NRj';
каждый вариант Rj' и Rk независимо выбран из H, C1-C6 алкила, -C(=O)H, -C(=O)Rm, C(=O)O(C1-C6 алкила), C(=O)N(Rn)2 и SO2-Rm, где Rm выбран из C1-C6 алкила, CH2-(гетероарила, содержащего 5-10 атомов в кольце), CH2-(C6-C10 арила) и C6-C10 арила; и каждый вариант Rn независимо выбран из H, C1-C6 алкила, CH2-(гетероарила, содержащего 5-10 атомов в кольце), CH2-(C6-C10 арила) и C6-C10 арила, и где арильная и гетероарильная часть в Rm и Rn могут быть необязательно замещены 1-3 независимо выбранными заместителями из F, C1-C6 алкила, фтор-C1-C6 алкила, C3-C6 циклоалкила, C1-C6 алкокси, C1-C6 фторалкокси или циано;
где дополнительно:
(a) если каждый из A и B представляет собой связь и b равен 0, то X имеет формулу: -Y-[C(Ra)2]a-;
(b) если b равен 0 или 1, то A и B оба не могут представлять собой гетероатомы; и
(c) если A или B служит точкой присоединения X к атомам азота в кольце, то A или B не может представлять собой гетероатом;
R1 представляет собой:
(i) моноциклический или бициклический гетероарил, содержащий 5-10 атомов в кольце, который необязательно замещен 1-3 Ro; причем 1-4 кольцевых атома представляют собой гетероатом, независимо выбранный из O, N, N-H, N-Ro и S;
(ii) C6-C10 арил, который необязательно замещен 1-3 Ro; или
(iii) C3-C10 циклоалкил или C3-C10 циклоалкенил, каждый из которых необязательно замещен 1-6 Ro;
(iv) гетероциклил, содержащий 3-10 атомов в кольце, который необязательно замещен 1-6 Ro; причем 1-4 кольцевых атома представляют собой гетероатом, независимо выбранный из O, N, N-H, N-Ro и S;
(v) водород;
R4 представляет собой H или Ro, и каждый вариант Ro независимо выбран из группы, состоящей из галогена; C1-C6 алкила; фтор(C1-C6)алкила; гидроксила; гидрокси(C1-C4)алкила; C1-C6 алкокси; фтор(C1-C6)алкокси; (C1-C6 алкил)C(O)-; (C1-C6 алкил)NH-; (C1-C6 алкил)2N-; -N*(Ro')2, где Ro'-N*-Ro' вместе образуют насыщенное кольцо, содержащее 5 или 6 кольцевых атомов, в котором 1 или 2 кольцевых атома необязательно представляют собой гетероатом, независимо выбранный из NH, N(C1-C6 алкила), O или S; формила; формил(C1-C4)алкила; циано; циано(C1-C4)алкила; бензила; бензилокси; (гетероциклил)-(C0-C6)алкила, где гетероциклильная часть содержит 5 или 6 кольцевых атомов, в которой 1 или 2 кольцевых атома представляют собой гетероатом, независимо выбранный из NH, N(алкила), O или S, и если указанная алкильная часть присутствует, то указанная алкильная часть служит точкой присоединения к R1, и если алкильная часть отсутствует, то атом углерода в кольце гетероциклила служит точкой присоединения гетероциклила к R1; фенила; гетероарила, содержащего 5-6 кольцевых атомов, причем 1-4 кольцевых атома представляют собой гетероатом, независимо выбранный из O, N, N-H, N-Ro'' и S, каждый из которых необязательно замещен 1-3 Ro''; SO2-(C1-C6)алкила; SO-(C1-C6)алкила и нитро;
каждый вариант Ro'' независимо выбран из группы, состоящей из галогена; C1-C6 алкила; фтор(C1-C6)алкила; гидроксила; гидрокси(C1-C4)алкила; C1-C6 алкокси; фтор(C1-C6)алкокси; (C1-C6 алкил)C(O)-; (C1-C6 алкил)NH-; (C1-C6 алкил)2N-; формила; формил(C1-C4)алкила; циано; циано(C1-C4)алкила; бензила; бензилокси; (гетероциклил)-(C0-C6)алкила, где гетероциклильная часть содержит 5 или 6 кольцевых атомов, в которой 1 или 2 кольцевых атома представляют собой гетероатом, независимо выбранный из NH, N(C1-C6 алкила), O или S, и если указанная алкильная часть присутствует, то указанная алкильная часть служит точкой присоединения к R1; и если алкильная часть отсутствует, то атом углерода в кольце гетероциклила служит точкой присоединения гетероциклила к R1; фенила; гетероарила, содержащего 5-6 кольцевых атомов, причем 1-4 кольцевых атома представляют собой гетероатом, независимо выбранный из O, N, N-H, N-(C1-C6 алкила) и S; SO2-(C1-C6)алкила; SO-(C1-C6)алкила и нитро;
R5 выбран из группы, состоящей из водорода, галогена; C1-C6 алкила; фтор(C1-C6)алкила; гидроксила; гидрокси(C1-C4)алкила; (C1-C6 алкил)C(O)-; формила; формил(C1-C4)алкила; циано; циано(C1-C4)алкила; бензила; (гетероциклил)-(C0-C6)алкила, где гетероциклильная часть содержит 5 или 6 кольцевых атомов, в которой 1 или 2 кольцевых атома представляют собой гетероатом, независимо выбранный из NH, N(C1-C6 алкила), O или S, и если указанная алкильная часть присутствует, то указанная алкильная часть служит точкой присоединения к R1; и если алкильная часть отсутствует, то атом углерода в кольце гетероциклила служит точкой присоединения гетероциклила к R1; фенила; гетероарила, содержащего 5-6 кольцевых атомов, причем 1-4 кольцевых атома представляют собой гетероатом, независимо выбранный из O, N, N-H, N-Rq'' и S, каждый из которых необязательно замещен 1-3 Rq''; SO2-(C1-C6)алкила; SO-(C1-C6)алкила и нитро;
R2 выбран из H, F, Cl, CF3, CF2CF3, CH2CF3, OCF3, OCHF2, фенила или фенила, замещенного 1-3 Ro; и
R3 представляет собой H, F или Cl.
[0020] В другом аспекте представлено соединение формулы (Ia).
[0021] В другом аспекте представлено соединение формулы (Ib).
[0022] В дополнительном аспекте представлены соединения формулы (I), конкретно описанные в данном документе (или соль, например их фармацевтически приемлемая соль) (например соединения A1-A24 или A1-A15, например A1, A2, A3, A4, A5, A6, A7, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A23 или A24).
[0023] В одном аспекте представлена композиция (например фармацевтическая композиция), которая содержит соединение формулы (I) или его соль (например фармацевтически приемлемую соль), определенные где-либо в данном документе, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления изобретения композиция может содержать эффективное количество соединения или его фармацевтически приемлемой соли. В некоторых вариантах осуществления изобретения композиция может дополнительно содержать дополнительное терапевтическое средство.
[0024] В другом аспекте представлена лекарственная форма, которая содержит от около 0,05 миллиграмма до около 2000 миллиграмм (например, от около 0,1 миллиграмма до около 1000 миллиграмм, от около 0,1 миллиграмма до около 500 миллиграмм, от около 0,1 миллиграмма до около 250 миллиграмм, от около 0,1 миллиграмма до около 100 миллиграмм, от около 0,1 миллиграмма до около 50 миллиграмм или от около 0,1 миллиграмма до около 25 миллиграмм) соединения формулы (I) или его соли (например фармацевтически приемлемой соли), определенных где-либо в данном документе. Лекарственная форма может дополнительно содержать фармацевтически приемлемый носитель и/или дополнительное терапевтическое средство.
[0025] В данном документе предлагаются способы ингибирования одной (или более) HDAC (например HDAC1 или HDAC2; например HDAC3) или более чем одной HDAC (например HDAC1 и HDAC2; например HDAC1 и HDAC3; например HDAC2 или HDAC3; например HDAC1, HDAC2 и HDAC3) с помощью соединения формулы (I) или его соли (например фармацевтически приемлемой соли), определенных где-либо в данном документе. В некоторых вариантах осуществления изобретения способы могут включать, например, обеспечение контакта одной (или более) HDAC (например, HDAC1 или HDAC2; например HDAC3) в образце (например, клетке или ткани) с соединением формулы (I) или его солью (например фармацевтически приемлемой солью), определенными где-либо в данном документе. В других вариантах осуществления изобретения способы могут включать введение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту (например, млекопитающему, такому как человек). Соответственно, в еще одном аспекте предлагаются способы скрининга в отношении соединений, которые ингибируют (например, избирательно ингибируют) одну или более HDAC (например, HDAC1 или HDAC2; например HDAC3, например HDAC1 и HDAC2; например HDAC1 и HDAC3; например HDAC2 или HDAC3; например HDAC1, HDAC2 и HDAC3).
[0026] В одном аспекте представлен способ избирательного ингибирования HDAC3, который включает обеспечение контакта HDAC3 в образце (например клетке или ткани) с соединением формулы (I) или его солью (например фармацевтически приемлемой солью), определенными где-либо в данном документе; или введение соединения формулы (I) или его соли (например фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту (например млекопитающему, такому как человек).
[0027] В одном аспекте представлен способ избирательного ингибирования HDAC1 или HDAC2 (например, HDAC1), который включает обеспечение контакта HDAC1 или HDAC2 (например, HDAC1) в образце (например клетке или ткани) с соединением формулы (I) или его солью (например фармацевтически приемлемой солью), определенными где-либо в данном документе; или введение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту (например, млекопитающему, такому как человек).
[0028] В одном аспекте представлен способ избирательного ингибирования HDAC1, HDAC2 и HDAC3, который включает обеспечение контакта HDAC1, HDAC2 и HDAC3 в образце (например, клетке или ткани) с соединением формулы (I) или его солью (например фармацевтически приемлемой солью), определенными где-либо в данном документе; или введение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту (например млекопитающему, такому как человек).
[0029] В одном аспекте представлены способы лечения (например, контроля, облегчения, уменьшения интенсивности, ослабления или замедления прогрессирования) или способы предупреждения (например задерживания дебюта или снижения риска развития) заболевания или расстройства, опосредованных HDAC1 или HDAC2, у субъекта (например млекопитающего, такого как человек), нуждающегося в этом, которые включают введение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту.
[0030] В одном аспекте представлены способы лечения (например, контроля, облегчения, уменьшения интенсивности, ослабления или замедления прогрессирования) или способы предупреждения (например, задерживания дебюта или снижения риска развития) заболевания или расстройства, опосредованных HDAC3, у субъекта (например млекопитающего, такого как человек), нуждающегося в этом, которые включают введение соединения формулы (I) или его соли (например фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту.
[0031] В одном аспекте представлены способы лечения (например контроля, облегчения, уменьшения интенсивности, ослабления или замедления прогрессирования) или способы предупреждения (например задерживания дебюта или снижения риска развития) заболевания или расстройства, опосредованных двумя или более HDAC (например HDAC1 и HDAC2; например HDAC1 и HDAC3; например HDAC2 или HDAC3; например HDAC1, HDAC2 и HDAC3), у субъекта (например млекопитающего, такого как человек), нуждающегося в этом, которые включают введение соединения формулы (I) или его соли (например фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту.
[0032] В одном аспекте представлены способы лечения (например контроля, облегчения, уменьшения интенсивности, ослабления, или замедления прогрессирования) или способы предупреждения (например задерживания дебюта или снижения риска развития) неврологического расстройства, такого как атаксия Фридрейха, миотоническая дистрофия, спинальная мышечная атрофия, синдром ломкой X-хромосомы, болезнь Хантингтона, спинально-церебеллярная атаксия, болезнь Кеннеди, амиотрофический латеральный склероз, спинальная и бульбарная мышечная атрофия и болезнь Альцгеймера; рака (например, кожной Т-клеточной лимфомы, B-клеточных лимфом и колоректального рака, и острого В-клеточного лимфобластного лейкоза); воспалительного заболевания (например, псориаза, ревматоидного артрита и остеоартрита); состояния, связанного с нарушением памяти; аффективного расстройства, нарушения головного мозга, связанного с хроматин-опосредованной нейропластичностью, посттравматического стрессового расстройства; привыкания к лекарственным средствам; серповидноклеточной анемии, β-талассемии (bT), инфекции Plasmodium falciparum (например, малярии), а также других паразитарных инфекций у субъекта (например млекопитающего, такого как человек), нуждающегося в этом, которые включают введение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, субъекту.
[0033] В одном аспекте представлено соединение формулы (I) или его соль (например, фармацевтически приемлемая соль), определенные где-либо в данном документе, для применения в медицине.
[0034] В одном аспекте представлено соединение формулы (I) или его соль (например, фармацевтически приемлемая соль), определенные где-либо в данном документе, для лечения заболевания или расстройства, опосредованных HDAC1 или HDAC2; заболевания или расстройства, опосредованных HDAC3; заболевания или расстройства, опосредованных HDAC3 и HDAC1 или HDAC2; заболевания или расстройства, опосредованных HDAC1 и HDAC2 и HDAC3; неврологического расстройства, такого как атаксия Фридрейха, миотоническая дистрофия, спинальная мышечная атрофия, синдром ломкой X-хромосомы, болезнь Хантингтона, спинально-церебеллярная атаксия, болезнь Кеннеди, амиотрофический латеральный склероз, болезнь Ниманна-Пика, болезнь Питта-Хопкинса, спинальная и бульбарная мышечная атрофия и болезнь Альцгеймера; рака (например кожной Т-клеточной лимфомы, B-клеточных лимфом и колоректального рака); воспалительного заболевания (например, псориаза, ревматоидного артрита и остеоартрита); состояния, связанного с нарушением памяти; посттравматического стрессового расстройства; привыкания к лекарственным средствам; инфекционного заболевания, такого как ВИЧ; инфекции Plasmodium falciparum (например малярии), а также других паразитарных инфекций, B-ALL, bT, серповидноклеточной анемии, аффективных расстройств или нарушений головного мозга, связанных с хроматин-опосредованной нейропластичностью.
[0035] В одном аспекте представлено применение соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе, при получении лекарственного препарата для лечения заболевания или расстройства, опосредованных HDAC1 или HDAC2; заболевания или расстройства, опосредованных HDAC3; заболевания или расстройства, опосредованных HDAC3 и HDAC1 или HDAC2; заболевания или расстройства, опосредованных HDAC1 и HDAC2 и HDAC3; неврологического расстройства, такого как атаксия Фридрейха, миотоническая дистрофия, спинальная мышечная атрофия, синдром ломкой X-хромосомы, болезнь Хантингтона, спинально-церебеллярная атаксия, болезнь Кеннеди, амиотрофический латеральный склероз, болезнь Ниманна-Пика, болезнь Питта-Хопкинса, спинальная и бульбарная мышечная атрофия и болезнь Альцгеймера; рака (например, кожной Т-клеточной лимфомы, B-клеточных лимфом, B-ALL и колоректального рака); воспалительного заболевания (например, псориаза, ревматоидного артрита и остеоартрита); состояния, связанного с нарушением памяти; аффективного расстройства, нарушения головного мозга, связанного с хроматин-опосредованной нейропластичностью, серповидноклеточной анемии, β-талассемии, посттравматического стрессового расстройства; привыкания к лекарственным средствам; инфекционного заболевания, такого как ВИЧ; инфекции Plasmodium falciparum (например малярии), а также других паразитарных инфекций.
[0036] В некоторых вариантах осуществления изобретения субъект может представлять собой субъекта, нуждающегося в этом (например, субъекта, идентифицированного как нуждающегося в таком лечении, такого как субъект, страдающий или подверженный риску заболевания одним или более заболеваний или состояний, описанных в данном документе). Идентификация субъекта, нуждающегося в таком лечении, может заключаться в оценке субъекта или специалиста в области медицины и может быть субъективной (например, заключение) или объективной (например, измеряемой посредством способов испытания или диагностики). В некоторых вариантах осуществления изобретения субъект может представлять собой млекопитающее. В некоторых вариантах осуществления изобретения субъект может представлять собой человека.
[0037] В одном аспекте представлены способы получения соединений, описанных в данном документе. В вариантах осуществления изобретения способы включают взятие любого одного из промежуточных соединений, описанных в данном документе, и приведение его в контакт с одним или более химическими реагентами в одну или более стадий с получением соединения формулы (I) или его соли (например, фармацевтически приемлемой соли), определенных где-либо в данном документе.
[0038] Некоторые соединения формулы (I), описанные в данном документе, характеризуются повышенными (например, увеличенными, например увеличенными на коэффициент около 2 или более, например, по сравнению с другими ингибиторами HDAC на основе o-аминоанилида) значениями устойчивости в кислоте. В некоторых вариантах осуществления изобретения соединения формулы (I) характеризуются повышенными значениями стойкости к разложению, например, менее около 25% разложения (например, менее около 20% разложения, менее около 15% разложения или менее около 10% разложения) при воздействии кислого pH, например кислых условий, предусмотренных для имитации таковых в желудке, например инкубации (например, в виде 10 мкМ раствора) при 50°C и при pH около 2,0 в течение около четырех часов. Стойкость соединений к разложению или метаболизму при кислом pH может быть полезным признаком для фармацевтического средства (например, лекарственного препарата). Увеличенная устойчивость при низком pH может позволить, например, осуществление стадий способа получения, таких как образование соли, без значительного разложения требуемой соли. Кроме того, предпочтительно, чтобы перорально вводимые фармацевтические препараты были устойчивыми к кислому pH желудка. В некоторых вариантах осуществления изобретения соединения проявляют повышенную устойчивость при воздействии кислого pH с устойчивостью периодов полураспада более, например, 12 ч или, например, 18 ч, или, например, 24 ч, при pH 2 и 50°C.
[0039] В некоторых вариантах осуществления изобретения, соединения формулы (I), описанные в данном документе, избирательно ингибируют HDAC3, например избирательно ингибируют HDAC3 относительно HDAC1 и HDAC2 (например проявляют 5-кратную или большую избирательность, например проявляют 25-кратную или большую избирательность). Не ограничиваясь какой-либо теорией, полагают, что HDAC3-избирательные ингибиторы могут повышать экспрессию фратаксина и, вследствие этого, могут применяться при лечении неврологических состояний (например, неврологических состояний, связанных с пониженной экспрессией фратаксина, таких как атаксия Фридрейха). Также полагают, что ингибирование HDAC3 играет важную роль при консолидации памяти (McQuown SC et al, J