Бензотиофеновое соединение
Иллюстрации
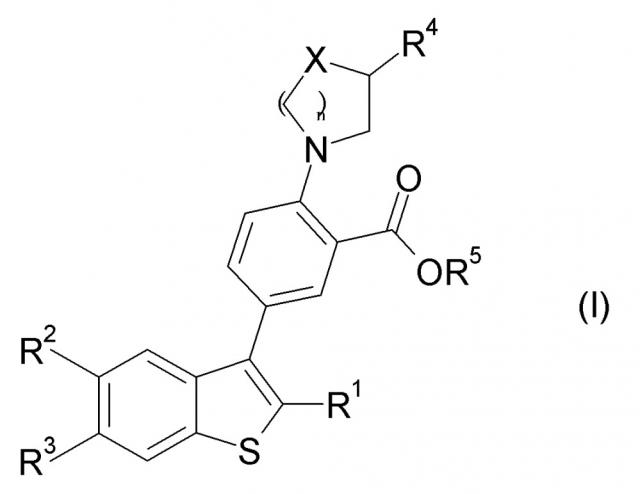
Показать всеИзобретение относится к соединению формулы (I) или к его фармацевтически приемлемой соли, где X представляет собой -O- или -CH2-, n имеет значение от 1 до 3, R1 представляет собой -H, галоген или низший алкил, R2 и R3 являются каждый одинаковыми или отличными друг от друга и представляют собой -H, галоген, низший алкил или галоген-низший алкил, R4 представляет собой -Lk-NH-R0, Lk представляет собой низший алкилен или связь, R0 представляет собой низший алкил, низший алкилен-OH или циклоалкил, и R5 представляет собой -H или низший алкил. Изобретение также относится к фармацевтической композиции, обладающей активностью, направленной на открытие IK1-канала. Технический результат – получены новые соединения, которые могут найти свое применение в медицине для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии. 5 н. и 12 з.п. ф-лы, 26 табл., 31 пр.
Реферат
Область техники
[0001] Настоящее изобретение относится к бензотиофеновому соединению, пригодному в качестве активного ингредиента фармацевтической композиции, в частности, фармацевтической композиции, предназначенной для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии. Кроме того, изобретение относится к средству для предотвращения и/или лечения воспалительной боли, невропатической боли или фибромиалгии, представляющему собой активатор кальций-активируемого калиевого канала с промежуточной проводимостью (в дальнейшем назван как активатор IK1-канала).
Уровень техники
[0002] Калиевый канал, активируемый кальцием, экспрессирован в различных клетках животных, и играет важную роль в регуляции клеточных функций. Это означает, что активируемый кальцием калиевый канал осуществляет выброс калия в результате открытия канала в ответ на увеличение уровня внутриклеточного кальция в возбудимых и не возбудимых клетках, и регулирует мембранные потенциалы путем индуцирования следовой гиперполяризации. Активируемый кальцием калиевый канал подразделяется на канал большой проводимости (BK), канал маленькой проводимости (SK) и канал промежуточной проводимости (IK). Относительно этих каналов было показано, что IK-канал экспрессирован в лимфоцитах, эритроцитах, фибробластах, эндотелиоцитах сосудистой стенки, эпителии дыхательных путей, желудочно-кишечном тракте, периферических нервах, ганглиях задних корешков спинного мозга и тому подобное, и было предположено, что IK-канал участвует в заболеваниях, которые поражают эти клетки (Current Medicinal Chemistry, 2007, vol. 14, p. 1437-1457). Кроме того, исходя из того факта, что открыватель двойного действия IK1/SK улучшает висцеральную гиперчувствительность и атипичную перистальтику кишечника (Gastroenterology, 2008, vol. 134, Issue 4, Supplement 1, p. A-544, T1386), было выдвинуто предположение о возможном лечении синдрома раздраженного кишечника (IBS).
[0003] С другой стороны, имеется сообщение о том, что IK1-канал экспрессирован в сенсорной нервной системе, однако никаких изменений не происходит в уровне экспрессии, наблюдаемой в модели невропатической боли и модели воспалительной боли (Neuroscience, 2005, Vol. 131, стр. 161-175), и что IK1-канал участвует в обезболивающем действии агониста PPAR (The Journal of Pharmacology and Пр.perimental Therapeutics, 2006. vol. 319, p. 1051-1061). Однако достоверный факт не был получен относительно взаимосвязи между каналом IK1 и болевым расстройством. Кроме того, не было сообщения о том, что активатор IK1-канала является эффективным в воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии при использовании модели болезни животных.
Раскрытие сущности изобретения
Проблемы, которые следует решить с помощью изобретения
[0004] Изобретение предоставляет новое соединение, которое пригодно в качестве активного ингредиента лекарственного средства, в частности, фармацевтической композиции, предназначенной для предотвращения и/или лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии.
Кроме того, изобретение относится к средству для предотвращения или лечения воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, представляющему собой активатор IK1-канала.
Средства для решения проблем
[0005] Авторы настоящего изобретения провели интенсивные исследования активаторов IK1-канала, и в результате они обнаружили, что бензотиофеновое соединение согласно настоящему изобретению проявляет превосходные эффекты, тем самым завершили изобретение.
А именно, настоящее изобретение относится к соединению формулы (I) или к его соли, и фармацевтической композиции, содержащей соединение формулы (I) или его соль и фармацевтически приемлемый эксипиент.
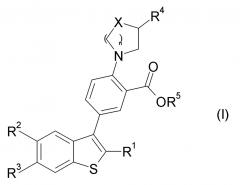
[Химическая формула 1]
(В формуле,
X представляет собой -O-, -CH2-, -NH- или -N(низший алкил)-,
n равно целому числу от 1 до 3,
R1 представляет собой -H, галоген или низший алкил,
R2 и R3 являются каждый одинаковыми или отличными друг от друга и означают -H, галоген, низший алкил или галоген-низший алкил,
R4 представляет собой -H или -Lk-NH-R0,
Lk представляет собой низший алкилен или связь,
R0 представляет собой низший алкил, -низший алкилен-OH или циклоалкил,
при условии, что в случае, когда R4 представляет собой -H, X представляет собой -N(низший алкил)-, и
R5 представляет собой -H или низший алкил.)
[0006] Кроме того, если не указано иное, когда символы в определенной химической формуле в описании настоящего изобретения также использованы в другой химической формуле, тот же символ имеет то же значение.
[0007] Также, с помощью фармакологических тестов при использовании моделей болезни животных было обнаружено, что активатор канала IK1 является эффективным при воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, тем самым завершая изобретение.
А именно, настоящее изобретение относится к средству для предотвращения и/или лечения воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, представляющему собой активатор IK-канала в качестве активного ингредиента.
[0008] Также, настоящее изобретение относится к фармацевтической композиции, предназначенной для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, содержащей соединение формулы (I) или его соль.
Между тем, фармацевтическая композиция содержит средство для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, представляющее собой соединение формулы (I) или его соль.
Кроме того, настоящее изобретение относится к:
(1) применению соединения формулы (I) или его соли для производства фармацевтической композиции, предназначенной для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии;
(2) применению соединения формулы (I) или его соли для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии;
(3) соединению формулы (I) или его соли, предназначенному для лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии; и
(4) способу лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии, включающему в себя введение субъекту эффективного количества соединения формулы (I) или его соли.
Между тем, термин “субъект” представляет собой человека или другого животного, нуждающегося в профилактике или лечении указанным средством, и в соответствии с определенным вариантом осуществления изобретения, человека, нуждающегося в профилактике или лечении указанным средством.
Эффекты изобретения
[0009] Соединение формулы (I) или его соль проявляет активирующее действие на IK1-канал, и может быть использовано в качестве средства, предназначенного для предотвращения и/или лечения висцеральной боли, воспалительной боли, остеоартритной боли, невропатической боли или фибромиалгии.
Варианты для осуществления изобретения
[0010] Далее, настоящее изобретение будет описано более подробно.
В описании настоящего изобретения, “низший алкил” представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода (также названный как С1-6 алкил; далее, число атомов углерода указано таким же образом), и его примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, сек-бутил, трет-бутил, н-пентил, н-гексил и тому подобное. В другом варианте осуществления изобретения, низший алкил представляет собой С1-4 алкил, в еще другом варианте осуществления изобретения, низший алкил представляет собой метил, этил, н-пропил или трет-бутил, в еще одном варианте осуществления изобретения, низший алкил представляет собой метил, в еще другом варианте осуществления изобретения, низший алкил представляет собой линейный или разветвленный алкил, содержащий 4 атома углерода (C4 алкил), и в еще одном варианте осуществления изобретения, низший алкил представляет собой трет-бутил.
[0011] В описании, “галоген-низший алкил” представляет собой низший алкил, замещенный от 1 до 5 атомами галогена. В другом варианте осуществления изобретения, галоген-низший алкил представляет собой низший алкил, замещенный от 1 до 3 атомами галогена, и другом варианте осуществления изобретения, галоген-низший алкил представляет собой -CF3.
[0012] В описании, “низший алкилен” представляет собой линейный или разветвленный C1-6 алкилен, и его примеры включают метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, пропилен, метилметилен, этилэтилен, 1,2-диметилэтилен, 1,1,2,2-тетраметилэтилен и тому подобное. В другом варианте осуществления изобретения, низший алкилен представляет собой C1-4 алкилен, в другом варианте осуществления изобретения, низший алкилен представляет собой C4 алкилен, и в еще одном варианте осуществления изобретения, низший алкилен представляет собой метилен.
[0013] В описании, “галоген” означает F, Cl, Br или I.
[0014] В описании, “циклоалкил” представляет собой насыщенную углеводородную кольцевую группу, содержащую от 3 до 10 атомов углерода(С3-10), и которая может содержать мостиковую связь. Примеры циклоалкила включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, адамантил и тому подобное. В другом варианте осуществления изобретения, циклоалкил представляет собой циклоалкил, содержащий от 3 до 8 атомов углерода (C3-8 циклоалкил), и в другом варианте осуществления изобретения, циклоалкил представляет собой циклобутил.
[0015] Варианты осуществления изобретения представлены ниже.
(1) Соединение формулы (I) и его соль, в которой R1 представляет собой -H, -F или -CH3, в другом варианте осуществления изобретения, R1 представляет собой -H или низший алкил, в еще другом варианте осуществления изобретения, R1 представляет собой -H или -CH3, в еще одном варианте осуществления изобретения, R1 представляет собой -H, в еще одном варианте осуществления изобретения, R1 представляет собой галоген, в еще одном варианте осуществления изобретения, R1 представляет собой -F, в еще одном варианте осуществления изобретения, R1 представляет собой низший алкил, и в еще одном варианте осуществления изобретения, R1 представляет собой -CH3.
(2) Соединение формулы (I) и его соль, в которой R2 представляет собой -H или галоген, в другом варианте осуществления изобретения, R2 представляет собой -H, -F или -Cl, в еще другом варианте осуществления изобретения, R2 представляет собой -H, в еще одном варианте осуществления изобретения, R2 представляет собой галоген, и в еще одном варианте осуществления изобретения, R2 представляет собой -F или -Cl.
(3) Соединение формулы (I) и его соль, в которой R3 представляет собой галоген или галоген-низший алкил, в другом варианте осуществления изобретения, R3 представляет собой -F, -Cl или -CF3, в другом варианте осуществления изобретения, R3 представляет собой галоген, в еще одном варианте осуществления изобретения, R3 представляет собой -F или -Cl, в еще одном варианте осуществления изобретения, R3 представляет собой -Cl, в еще одном варианте осуществления изобретения, R3 представляет собой галоген-низший алкил, и в еще одном варианте осуществления изобретения, R3 представляет собой -CF3.
(4) Соединение формулы (I) и его соль, в которой R4 представляет собой -Lk-NH-R0.
(5) Соединение формулы (I) и его соль, в которой Lk представляет собой низший алкилен, в другом варианте осуществления изобретения, Lk представляет собой C1-4 алкилен, и в еще одном варианте осуществления изобретения, Lk представляет собой -CH2-.
(6) Соединение формулы (I) и его соль, в которой R0 представляет собой C4 алкил, -C4 алкилен-OH или C3-8 циклоалкил, в другом варианте осуществления изобретения, R0 представляет собой C3-8 циклоалкил, в еще одном варианте осуществления изобретения, R0 представляет собой циклобутил, в еще одном варианте осуществления изобретения, R0 представляет собой C4 алкил, и в еще одном варианте осуществления изобретения, R0 представляет собой трет-бутил.
(7) Соединение формулы (I) и его соль, в которой R5 представляет собой -H или -CH3, и в другом варианте осуществления изобретения, R5 представляет собой -H.
(8) Соединение формулы (I) и его соль, в которой X представляет собой -O- или -CH2-, в другом варианте осуществления изобретения, X представляет собой -O-, и в еще одном варианте осуществления изобретения, X представляет собой -CH2-.
(9) Соединение формулы (I) и его соль, в которой n имеет значение 2.
(10) Соединение формулы (I) и его соль, которое представляет собой комбинацию двух или более из вариантов осуществления изобретения, как описано в пунктах от (1) до (9).
[0016] Кроме того, конкретные примеры комбинации в пункте (10) включают следующие варианты осуществления изобретения.
(11) Соединение формулы (I) и его соль, в которой R1 представляет собой низший алкил, R2 представляет собой -H, R3 представляет собой галоген, R4 представляет собой -Lk-NH-R0, Lk представляет собой -CH2-, R0 представляет собой C3-8 циклоалкил, R5 представляет собой -H, X представляет собой -O-, и n имеет значение 2.
(12) Соединение формулы (I) и его соль, в которой R1 представляет собой -H, R2 представляет собой галоген, R3 представляет собой галоген-низший алкил, R4 представляет собой -Lk-NH-R0, Lk представляет собой -CH2-, R0 представляет собой C3-8 циклоалкил, R5 представляет собой -H, X представляет собой -O-, и n имеет значение 2.
(13) Соединение формулы (I) и его соль, в которой R1 представляет собой низший алкил, R2 представляет собой галоген, R3 представляет собой галоген, R4 представляет собой -Lk-NH-R0, Lk представляет собой -CH2-, R0 представляет собой C3-8 циклоалкил, R5 представляет собой -H, X представляет собой -O-, и n имеет значение 2.
[0017] В дополнение, примеры других конкретных вариантов комбинации в пункте (10) включают следующие подпункты от (a) до (f).
(a) Соединение формулы (I) и его соль, в которой R4 представляет собой -Lk-NH-R0.
(b) Соединение (a) и его соль, в формуле которого X представляет собой -O- или -CH2-.
(c) Соединение (b) и его соль, в формуле которого n имеет значение 2.
(d) Соединение (c) и его соль, в формуле которого Lk представляет собой -CH2-.
(e) Соединение (d) и его соль, в формуле которого R5 представляет собой -H.
(f) Соединение (e) и его соль, в формуле которого R0 представляет собой C4 алкил, -C4 алкилен-OH, или C3-8 циклоалкил.
[0018] Примеры вариантов конкретных соединений, представленных в изобретении, включают следующие соединения и их соли:
5-(6-хлор-2-метил-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойную кислоту,
5-(6-хлор-2-фтор-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойную кислоту,
2-{(3R)-3-[(трет-бутиламино)метил)пиперидин-1-ил}-5-[6-(трифторметил)-1-бензотиофен-3-ил]бензойную кислоту,
5-[5-хлор-6-(трифторметил)-1-бензотиофен-3-ил]-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойную кислоту или
5-(6-хлор-5-(фтор-2-метил-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойную кислоту.
[0019] Примеры других вариантов конкретных соединений, представленных в изобретении, включают следующие соединения и их соли:
5-(6-хлор-2-метил-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойной кислоты гидробромид,
5-(6-хлор-2-фтор-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойной кислоты гидрохлорид,
2-{(3R)-3-[(трет-бутиламино)метил]пиперидин-1-ил}-5-[6-(трифторметил)-1-бензотиофен-3-ил]бензойной кислоты гидрохлорид,
5-[5-хлор-6-(трифторметил)-1-бензотиофен-3-ил]-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойной кислоты гидрохлорид или
5-(6-хлор-5-фтор-2-метил-1-бензотиофен-3-ил)-2-{(2R)-2-[(циклобутиламино)метил]морфолин-4-ил}бензойной кислоты гидрохлорид.
[0020] Соединения формулы (I) могут быть представлены в виде геометрических изомеров в зависимости от типов их заместителей. В описании настоящего изобретения, даже в случаях соединений формулы (I), появляющихся только в одной изомерной форме, изобретение охватывает другие изомеры и также охватывает отдельные изомеры или их смеси.
Кроме того, соединение формулы (I) может иметь асимметричные атомы углерода или аксиальную асимметрию, и в результате этого могут присутствовать оптические изомеры. Изобретение также включает отдельный оптический изомер соединения формулы (I) или его смесь.
[0021] Кроме того, изобретение также охватывает фармацевтически приемлемое пролекарство соединения, представленного формулой (I). Фармацевтически приемлемое пролекарство представляет собой соединение, содержащее группу, которая может быть превращена в аминогруппу, гидроксильную группу, карбоксильную группу или тому подобное путем сольволиза или при физиологических условиях. В качестве группы, образующей пролекарство, группы, описанные в публикациях Prog. Med., 1985, vol. 5, p. 2157-2161, и "Pharmaceutical Research and Development, Drug Design" (Hirokawa Publishing Company), 1990, vol. 7, p. 163-198, могут быть представлены в качестве примера.
[0022] В дополнение, соль соединения формулы (I) является фармацевтически приемлемой солью соединения формулы (I), и соединение формулы (I) может образовывать кислотно-аддитивную соль или соль с основанием в зависимости от типов их заместителей. Конкретные примеры соли включают кислотно-аддитивные соли неорганических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и тому подобное, и органических кислот, таких как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, миндальная кислота, винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота, лимонная кислота, метансульфокислота, этансульфокислота, бензолсульфокислота, п-толуолсульфокислота, аспарагиновая кислота, глутаминовая кислота и тому подобное, соли неорганических оснований, такие как натриевые, калиевые, магниевые, кальциевые, алюминиевые и тому подобное, и органических оснований, таких как метиламин, этиламин, этаноламин, лизин, орнитин и тому подобное, соли различных аминокислот, таких как ацетиллейцин, и тому подобное и производные аминокислот, соли аммония и тому подобное.
[0023] Кроме того, изобретение также охватывает различные гидраты или сольваты соединения формулы (I) или его соли, и кристаллические вещества с полиморфизмом. В дополнение, изобретение также охватывает соединения, меченные различными радиоактивными или нерадиоактивными изотопами.
(Способ получения)
[0024] Соединение формулы (I) и его соль могут быть получены при применении различных известных методов синтеза, используя характеристики, основанные на его основной структуре или типах заместителей. При этом, в способе получения может оказаться эффективным, чтобы функциональная группа была замещена подходящей защитной группой (группой, которую можно легко превратить в функциональную группу) на стадии от исходного материала до образования промежуточного в зависимости от типов функциональных групп. В качестве такой защитной группы, защитные группы, описанные в публикации "Greene's Protective Groups in Organic Synthesis (4th edition, 2006)", написанной P. G. M. Wuts и T. W. Greene, могут быть представлены, и они могут быть выбраны подходящим образом и использованы в зависимости от условий реакции. В таком способе, сначала вводят защитную группу, реакцию осуществляют, и затем защитную группу удаляют, при необходимости. Осуществляя это, можно получить желаемое соединение.
В дополнение, пролекарство соединения формулы (I) может быть получено путем дополнительного проведения реакции введением конкретной группы на стадии, осуществляемой от исходного материала до образования промежуточного, таким же образом, как и для описанной выше защитной группы, или с использованием полученного соединения формулы (I). Реакция может быть осуществлена способами, известными специалистам в данной области техники, такими как общая этерификация, амидирование, дегидратация или тому подобное.
Далее, характерные способы получения соединения формулы (I) будут описаны. Каждый из способов получения может также быть осуществлен со ссылкой на ссылки, представленные в описании. Кроме того, способ получения согласно изобретению не ограничивается примерами, описанными ниже.
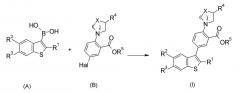
[Химические формулы 2]
(В формуле, Hal представляет собой Cl, Br или I)
[0025] Соединение формулы (I) включает (i) соединение формулы (I), в которой R5 представляет собой низший алкил (далее названо как соединение формулы (I-1)), и (ii) соединение формулы (I), в которой R5 представляет собой -H (далее названо как соединение формулы (I-2)). Каждый общий способ получения будет описан ниже.
[0026] (i) Соединение формулы (I-1) может быть получено из соединений (A) и (B). Реакция представляет собой так называемую реакцию сочетания Сузуки, в которой соединение (I) получают путем взаимодействия соединения (A), содержащего бороновую кислоту, и соединения (B). Реакция может быть осуществлена в отсутствие растворителя, или в растворителе, инертном по отношению к реакции, таком как ароматические углеводороды, включающие толуол, ксилол и тому подобное, простые эфиры, включающие Et2O, ТГФ, DME, диоксан и тому подобное, галогенированные углеводороды, включающие DCM, DCE, хлороформ и тому подобное, и апротонные растворители, включающие ДМФА, ДМСО, EtOAc, CH3CN и тому подобное, и при нагревании с обратным холодильником в диапазоне от комнатной температуры. Реакцию осуществляют в присутствии палладия, фосфинового лиганда и металлосодержащего основания. В качестве палладия, Pd(PPh3)4, Pd(OAc)2, Pd2dba3 и тому подобное могут быть использованы. В качестве фосфинового лиганда, BINAP, DPPF, PPh3, P(But)3 и тому подобное могут быть использованы. В качестве металлосодержащего основания, Na2CO3, K2CO3, Cs2CO3, NaOBut, K3PO4 и тому подобное могут быть использованы.
[0027] (ii) Соединение формулы (I-2) может быть получено деалкилированием R5 соединения формулы (I-1). Например, деалкилирование представляет собой гидролиз и тому подобное. В случае щелочного гидролиза, металлосодержащие основания, такие как NaOH, KOH, Na2CO3, Cs2CO3 и тому подобное, могут быть использованы. В случае гидролиза в кислой среде, хлористоводородная кислота и тому подобное может быть использована. В обоих случаях, температура реакции составляет от температуры при охлаждении льдом до температуры кипячения с обратным холодильником, и можно проводить реакцию в условиях, в которых субстрат не разлагается. В качестве растворителя, спирты, такие как MeOH, EtOH и тому подобное, апротонные растворители, такие как ДМФА, ДМСО и тому подобное, вода или смешанные растворители могут быть использованы.
[0028] (Синтез исходного материала 1)
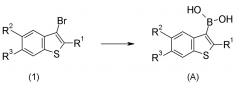
[Химические формулы 3]
[0029] Исходное соединение (A) может быть получено путем взаимодействия соединения (1) и соединений, содержащих борную кислоту, таких как триизопропилборат и тому подобное.
В реакции, соединение (1) и соединение, содержащее борную кислоту, такое как триизопропилборат и тому подобное, смешивают в эквивалентных количествах, или любое из них в избыточном количестве, литийорганический реагент, такой как nBuLi и тому подобное, добавляют к смеси при охлаждении, предпочтительно в диапазоне от -78°С до 0°С, и образованный продукт перемешивают в растворителе, который является инертным по отношению к реакции, или в отсутствие растворителя, обычно от низкой температуры до комнатной температуры, предпочтительно от 0°С до 30°С, в течение от 0,1 часа до 5 дней. Примеры используемого в изобретении растворителя включают, но не ограничиваются ими, углеводороды, такие как гексан и тому подобное, и простые эфиры, такие как Et2O, ТГФ и тому подобное, лишь бы растворитель не препятствовал реакции.
[0030] (Синтез исходного материала 2)
[Химические формулы 4]
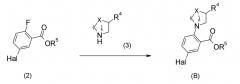
[0031] Исходное соединение (B) может быть получено взаимодействием соединения (2) и соединения (3).
В реакции, соединение (2) и соединение (3) смешивают в эквивалентных количествах, или любое из них в избыточном количестве, и смесь перемешивают в растворителе, инертном по отношению к реакции, или в отсутствие растворителя, обычно в течение от 0,1 часа до 5 дней, при температуре от охлаждения до нагревания с обратным холодильником, предпочтительно от 0°С до 80°С. Примеры используемого в изобретении растворителя включают, но не ограничиваются ими, ароматические углеводороды, простые эфиры, галогенированные углеводороды, ДМФА, ДМСО, EtOAc, CH3CN и смеси этих растворителей. Когда реакцию осуществляют в присутствии органического основания, такого как TEA, DIPEA и тому подобное, или в присутствии неорганического основания, такого как K2CO3, Na2CO3, KOH и тому подобное, этот случай может быть предпочтительным с точки зрения плавности хода реакции.
[References] S. R. Sandler and W. Karo, "Organic Functional Group Preparations", 2nd edition, vol. 1, Academic Press Inc., 1991
"Courses in Пр.perimental Chemistry" (5th edition) edited by The Chemical Society of Japan, vol. 14 (2005) (Maruzen Co., Ltd.)
[0032] (Синтез исходного материала 3)
[Химические формулы 5]
(В формуле, Lv представляет собой галоген, -OMs, -OTs или тому подобное)
Соединение (B-1), которое представляет собой вариант исходного соединения (B), получают путем превращения соединения (4), которое получают взаимодействием соединения (2) и соединения (3-1), в соединение (5), и затем реакцией с соединением (6). Соединение (4) получают из соединения (2) и соединения (3-1) таким же способом, который представлен в описанном выше синтезе исходного материала 2. Соединение (5) получают путем превращения OH-группы соединения (4) в уходящую группу, такую как галоген, -OMs, -OTs или тому подобное, обычными способами ("Courses in Пр.perimental Chemistry" (5th edition) edited by The Chemical Society of Japan, vol. 14 (2005) (Maruzen Co., Ltd.)). На конечной стадии, соединение (B-1) получают путем взаимодействия соединения (5) и соединения (6) с использованием таких же условий, как в описанном выше синтезе исходного материала 2.
[0033] Соединение формулы (I) выделяют и очищают в виде свободного соединения, его соли, гидрата, сольвата или кристаллического вещества с полиморфизмом. Соль соединения формулы (I) может быть получена обычной реакцией образования соли.
Выделение и очистку осуществляют путем применения обычных манипуляций, используемых в области химии, таких как экстракция, фракционная кристаллизация, различные типы фракционной хроматографии и тому подобное.
Различные изомеры могут быть получены путем выбора подходящего исходного соединения, или они могут быть разделены на основе различия в физико-химических свойствах среди изомеров. Например, оптические изомеры получают общими методами разделения на оптические изомеры (например, фракционной кристаллизацией, приводящей к получению диастереомерной соли с оптически активным основанием или кислотой, или хроматографией с использованием хиральной колонки или тому подобное) рацемической смеси, и могут также быть получены из подходящего оптически активного исходного соединения.
[0034] Фармакологическая активность соединения формулы (I) была подтверждена следующими испытаниями.
Кроме того, в примерах испытаний 2-6, 0,5% суспензия метилцеллюлозы была использована в качестве испытуемого лекарственного средства.
[0035] Пример испытаний 1: Испытание по измерению активности, направленной на открывание IK1-канала
Клетки ((1) T84 клетки (которые известны как клетки, экспрессирующие IK1-канал) или (2) человеческие клетки, экспрессирующие IK1-канал (трансген: NM_002250.2, использовали клетки: CHO dhfr-)) высевали в 384-луночном микропланшете так, чтобы было 12000 клеток/лунку. После инкубации в течение ночи, среду удаляли отсасыванием, и 20 мл реактива для анализа трансмембранного потенциала FLIPR (FLIPR набор для анализа трансмембранного потенциала, произведенный компанией Molecular Devices LLC) добавляли к среде с последующей инкубацией при комнатной температуре в течение 1 часа. Интенсивность флуоресценции измеряли при 530 нм/590 нм, которая была установлена в качестве предварительного значения. Затем, 20 мл буферного раствора, содержащего испытуемое лекарственное средство (которое содержит 0,01% плюрониловой кислоты и 20 мМ Hepes-NaOH (pH 7,4); 0,2% CHAPS в HBSS), добавляли с последующей инкубацией при комнатной температуре в течение 1 часа, и конечное значение измеряли. Активность испытуемого лекарственного средства определяли, исходя из относительных значений, где обработка NS-309 (6,7-дихлор-1H-индол-2,3-дион-3-оксим, произведенный компанией Sigma-Aldrich Co., LLC; 0,2 мкМ; раствор ДМСО) была принята за 0%. Значение активности (%) при каждой концентрации откладывали на графике против концентрации испытуемого лекарственного средства, и значение EC50 рассчитывали с помощью метода логистической регрессии.
[0036] Значения EC50 открытия IK1-канала для некоторых характерных примеров соединений согласно изобретению представлены в следующей таблице (в таблице, No. означает номер, и Пр. означает номер примера соединения. То же обозначение будет применяться в дальнейшем). В таблице 1 представлены результаты, полученные при использовании клеток T84, и в таблице 2 представлены результаты, полученные при использовании человеческих клеток, экспрессирующих IK1-канал (трансген: NM_002250.2, использовали клетки: CHO dhfr-). С учетом Р<0,05 в каждом анализе, было установлено, что существует достоверная разница.
| [0037] [Таблица 1] | |||
| № | EC50 | № | EC50 |
| Пр.10 | 3,89 мкМ | Пр.14 | 3,17 мкМ |
| Пр.11 | 3,07 мкМ | Пр.16 | 8,04 мкМ |
| Пр.12 | 1,75 мкМ | Пр.18 | 0,920 мкМ |
| Пр.13 | 3,76 мкМ | Пр.19 | 1,50 мкМ |
| [0038] [Таблица 2] | |||
| No. | EC50 | No. | EC50 |
| Пр.10 | 0,093 мкМ | Пр.14 | 0,028 мкМ |
| Пр.11 | 0,011 мкМ | Пр.16 | 0,033 мкМ |
| Пр.12 | 0,024 мкМ | Пр.18 | 0,048 мкМ |
| Пр.13 | 0,052 мкМ | Пр.19 | 0,0055 мкМ |
[0039] Пример испытаний 2: Влияние на абдоминальную боль, вызванную растяжением толстой кишки у крыс
После того, как самцов крыс линии Wistar (CLEA Japan, Inc.) анестезировали изофлураном, в толстую кишку вводили баллон. После пробуждения, испытуемое лекарственное средство вводили перорально, и через 1 час, абдоминальную боль, вызванную введением баллона, измеряли в качестве показателя характера изменения брюшной полости при сгибании. Каждое раздражение (15, 30, 45, 60 мм Hg) неоднократно выполняли в течение 5 минут при 5-минутных интервалах. Исследование достоверной разницы в группе, обработанной растворителем, и группе, обработанной испытуемым лекарственным средством, осуществляли в сравнении между группами, используя параметрический t-критерий Стьюдента или критерий множественного сравнения Даннетта. С учетом Р<0,05 в каждом анализе, было установлено, что существует достоверная разница.
[0040] Эффективность некоторых характерных примеров соединений согласно изобретению при испытании абдоминальной боли, вызываемой растяжением толстой кишки у крыс, представлена в следующей таблице (в таблице, MED означает минимальную эффективную дозу. То же обозначение будет применяться в дальнейшем). Результаты для каждого примера соединения 10 (Пр.10) или 18 (Пр.18), проявляющего значительную активность в каждой дозе, представлены в следующей таблице.
| [0041] [Таблица 3] | |||
| № | MED | No. | МЭД |
| Пр.10 | 0,3 мг/кг | Пр.18 | 0,3 мг/кг |
[0042] Пример испытаний 3: Ингибирующее действие на распределение массы задней конечности в модели артрита у крыс, вызванного адъювантом
Эта модель представляет собой модель, предоставленную для изучения воспалительной боли. 50 мл убитых микобактерий Mycobacterium tuberculosis H37Ra (производитель Difco Laboratories), суспендированных в жидком парафине, вводили подкожно в подушечку стопы правой задней конечности самки крысы линии Lewis (предоставлена Charles River Laboratories, Japan) так, чтобы концентрация была 10 мг/мл. На следующий день, вводили перорально растворитель или испытуемое лекарственное средство. Через 1 или 2 часа, распределение массы между левой и правой задними конечностями измеряли с помощью тестера Incapacitance (изготовленного Linton Instrumentation). Исследование достоверной разницы в группе, обработанной растворителем, и группе, обработанной испытуемым лекарственным средством, осуществляли в сравнении между группами, используя параметрический t-критерий Стьюдента или критерий множественного сравнения Даннетта. С учетом Р<0,05 в каждом анализе, было установлено, что существует достоверная разница.
[0043] Эффективность некоторых характерных примеров соединений согласно изобретению в модели артрита у крыс, вызванного адъювантом, представлена в следующей таблице. Результаты для каждого примера соединения Пр.10, Пр.11, Пр.14 или Пр.18, проявившего значительную активность в каждой дозе, представлены в следующей таблице.
| [0044] [Таблица 4] | |||
| № | MED | № | MED |
| Пр.10 | 3 мг/кг | Пр.14 | 1 мг/кг |
| Пр.11 | 3 мг/кг | Пр.18 | 3 мг/кг |
[0045] Пример испытаний 4: Ингиб