Стабилизация макролидов
Иллюстрации
Показать всеИзобретение относится к стабилизации рапамицина или производного рапамицина, имеющего иммуносупрессивные свойства и чувствительного к окислению. Способ стабилизации предусматривает добавление антиоксиданта к очищенному рапамицину в малых количествах - до 1% в пересчете на массу рапамицина. Также объектом изобретения является смесь в твердой форме, содержащая рапамицин и антиоксидант в каталитическом количестве. Антиоксидант, предпочтительно, представляет собой 2,6-ди-трет.-бутил-4-метилфенол. Стабилизированный рапамицин обладает высокой стойкостью к окислению, он может храниться в форме без упаковки до его дальнейшей обработки и может применяться в немодифицированной форме для приготовления требуемой галеновой композиции. 2 н. и 12 з.п. ф-лы, 3 ил.
Реферат
Настоящее изобретение относится к стабилизации фармацевтического действующего вещества, чувствительного к окислению, например полиенового макролида, предпочтительно полиенового макролида, обладающего иммуносупрессорными свойствами, прежде всего рапамицинов.
Обработка и хранение, прежде всего бестарное хранение, фармацевтических действующих веществ, чувствительных к окислению, являются затруднительными. В этом случае необходимо применять специальные методы обработки, и часто чувствительный к окислению ингредиент хранят в герметичной упаковке в атмосфере защитного газа. В процессе приготовления композиций на основе таких фармацевтических действующих веществ добавляют значительные количества стабилизаторов.
Полиеновые макролиды обладают удовлетворительными характеристиками стабильности. Однако при создании изобретения было установлено, что их стабильность в отношении кислорода может быть значительно улучшена путем добавления стабилизатора, например антиоксиданта, на стадии их выделения.
Объектом изобретения является:
1. Способ стабилизации полиенового макролида, предусматривающий добавление антиоксиданта к очищенному макролиду, предпочтительно в начале стадии его выделения.
Способ может применяться прежде всего для получения стабилизированного полиенового макролида без упаковки. Количество антиоксиданта обычно может составлять до 1%, более предпочтительно от 0,01 до 0,5% (в пересчете на массу макролида). Далее в настоящем описании такое небольшое количество называется каталитическим количеством.
Кроме того, объектом настоящего изобретения также является:
2. Смесь, например смесь без упаковки, содержащая полиеновый макролид и антиоксидант, предпочтительно в каталитическом количестве, предпочтительно в твердой форме.
Смесь может находиться в форме отдельных частиц, например в кристаллической или аморфной форме. Она может находиться в стерильном или практически стерильном состоянии, например в состоянии, пригодном для фармацевтического применения.
3. Применение смеси, указанной в п.2, для приготовления фармацевтической композиции.
Примерами полиеновых макролидов являются, например, молекулы, содержащие двойные связи, предпочтительно сопряженные двойные связи, например соединения, обладающие антибиотическими и/или иммуносупрессорными свойствами, например макролиды, содержащие лактамовую или лактоновую связь, и их производные, например соединения, обладающие биологической активностью, качественно сходной с активностью встречающихся в естественных условиях макролидов, например замещенные химическим путем макролиды. Соответствующими примерами являются, например, рапамицины и аскомицины. Предпочтительным полиеновым макролидом является макролид, содержащий по крайней мере 2 сопряженные двойные связи, например 3 сопряженные двойные связи.
Рапамицин представляет собой известный лактамовый макролид, который продуцируется, например, Streptomyces hygroscopicus. Строение рапамицина описано у Н. Kessler и др., Helv. Chim. Acta, 76: 117, 1993. Рапамицин обладает антибиотическими и иммуносупрессорными свойствами. Известны производные рапамицина, например, 16-О-замещенные рапамицины, например, описанные в WO 94/01136 и WO 96/41807, 40-О-замещенные рапамицины, например, описанные в WO 94/09010, WO 92/05179, WO 95/14023, WO 94/01136, WO 94/02385 и WO 96/13273, все документы включены в настоящее описание в качестве ссылки. Предпочтительными производными рапамицина являются, например, рапамицины, в которых гидроксигруппа в положении 40 формулы А, приведенной на стр. 1 WO 94/01010, замещена группой -OR, где R обозначает гидроксиалкил, гидроксиалкоксиалкил, ациламиноалкил или аминоалкил, например 40-О-(2-гидрокси)этилрапамицин, 40-О-(3-гидрокси)пропилрапамицин и 40-О-[2-(2-гидрокси)этокси]этилрапамицин.
Аскомицины, среди которых наиболее известными являются FK-506 и аскомицин, представляют собой другой класс лактамовых макролидов, многие из которых обладают выраженной иммуносупрессорной и противовоспалительной активностью. FK-506 представляет собой лактамовый макролид, продуцируемый Streptomyces tsukubaensis. Строение FK-506 приведено в приложении к Меrск Index, 11-е изд. (1989) в пункте А5. Аскомицин описан, например, в USP 3244592. Аскомицин, FK-506 и другие встречающиеся в естественных условиях макролиды, обладающие сходной биологической активностью, и их производные, например синтетические аналоги и производные, в целом называются "аскомицинами". Примерами синтетических аналогов или производных являются, например, галогенированные аскомицины, например 33-эпихлор-33-дезоксиаскомицин, описанный в ЕР-А 427680, тетрагидропирановые производные, которые, например, описаны в ЕР-А 626385.
Наиболее предпочтительными макролидами являются рапамицин и 40-О-(2-гидрокси)этилрапамицин.
Предпочтительными антиоксидантами являются, например, 2,6-ди-трет-бутил-4-метилфенол (далее в настоящем описании называемый ВНТ), витамин Е или С, наиболее предпочтительным является ВНТ.
Наиболее предпочтительной смесью по изобретению является смесь рапамицина или 40-О-(2-гидрокси)этилрапамицина и 0,2% (в пересчете на массу макролида) антиоксиданта, предпочтительно ВНТ.
Антиоксидант может быть добавлен к полиеновому макролиду в начале стадий выделения, предпочтительно на конечной стадии выделения, более предпочтительно непосредственно перед конечной стадией осаждения. Макролид предпочтительно находится в очищенном состоянии. Он может быть растворен в инертном растворителе, и к образовавшемуся раствору добавляют антиоксидант, после чего осуществляют стадию осаждения стабилизированного макролида, например, в аморфной форме или в форме кристаллов. Предпочтительно смесь по изобретению находится в аморфной форме.
Полученный стабилизированный макролид неожиданно обладает более высокой стабильностью к окислению, и его обработка и хранение, например, в форме без упаковки до его дальнейшей обработки, например, для получения галеновой композиции становятся намного легче. Это наиболее важно для макролидов в аморфной форме.
Макролид, стабилизированный согласно изобретению, может применяться в немодифицированной форме для приготовления требуемой галеновой композиции. Такие композиции могут быть приготовлены согласно известным в данной области методам, включающим добавление одного или нескольких фармацевтически приемлемых разбавителей или носителей, в том числе при необходимости добавление дополнительного стабилизатора.
В соответствии с этим еще одним объектом изобретения является:
4. Фармацевтическая композиция, включающая в качестве действующего вещества описанную выше стабилизированную смесь в сочетании с одним или несколькими фармацевтически приемлемыми разбавителями или носителями.
Композиция по изобретению может быть приспособлена для перорального, парентерального, местного (например, на кожу), глазного, назального введения или введения путем ингаляции (например, в легкие). Предпочтительной композицией является композиция для перорального введения, предпочтительно безводная композиция, в которой действующее вещество представляет собой лактоновый макролид.
Фармацевтические композиции по изобретению могут включать другие эксципиенты, например замасливатель, разрыхлитель, поверхностно-активное вещество, носитель, разбавитель, усилитель запаха и т.д. Композиции могут находиться в жидкой форме, например в форме растворов, суспензий или эмульсий, таких как микроэмульсии, например, описанные в USP 5536729, или в твердой форме, например в форме капсул, таблеток, драже, порошков (включая тонкоизмельченные или другим образом уменьшенные частицы), твердые дисперсии, гранулы и т.д., например, описанные в WO 97/03654, содержание обоих документов включено в настоящее описание в качестве ссылки, или в полутвердых формах, таких как мази, гели, кремы и пасты. Предпочтительно их приготавливают в форме, пригодной для перорального введения. Предпочтительно они находятся в твердой форме. Фармацевтические композиции по изобретению могут быть получены согласно известным методам путем смешения макролида, стабилизированного согласно изобретению, с дополнительными ингредиентами; при этом ингредиенты могут быть размолоты или измельчены и при необходимости спрессованы, например, в таблетки.
Настоящее изобретение наиболее предпочтительно касается содержащих рапамицин композиций в жидкой или твердой форме. Наиболее предпочтительной композицией является твердая дисперсия, например, содержащая стабилизированный рапамицин по изобретению и носитель, например, водорастворимый полимер, такой как гидроксипропилметилцеллюлоза, например, как описано в WO 97/03654.
Композиции по изобретению могут применяться при показаниях, известных для макролидов, которые в них содержатся, например, в известных дозах. Например, если макролид обладает иммуносупрессорными свойствами, например представляет собой рапамицин или производное рапамицина, то композиция может применяться, например, для лечения или предупреждения острого или хронического отторжения алло- или ксенотрансплантата органа или ткани, аутоиммунных болезней или воспалительных состояний, астмы, пролиферативных болезней, например опухолей, или гиперпролиферативных сосудистых заболеваний, предпочтительно для предупреждения или лечения отторжения трансплантата.
Количество макролида и композиции, которое требуется ввести, зависит от многочисленных факторов, например от применяемого действующего вещества, состояний, подлежащих лечению, продолжительности лечения и т.д. Например, для рапамицина или 40-О-(2-гидрокси)этилрапамицина пригодная суточная доза при пероральном введении составляет от 0,1 до 10 мг, и она может вводиться однократно или в виде разделенных доз.
Еще одним объектом настоящего изобретения также является 40-О-(2-гидрокси)этилрапамицин в кристаллической форме, прежде всего в практически чистой форме. Предпочтительно кристаллическая форма отличается отсутствием или практически отсутствием любых компонентов растворителя; она находится в несольватированной форме.
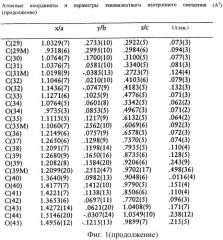
Кристаллическая форма 40-О-(2-гидрокси)этилрапамицина относится к моноциклической системе. Образовавшиеся кристаллы имеют tпл 146-147°С, в основном 146,5°С. Для идентификации новой кристаллической формы был проведен анализ с использованием дифракции ренгеновских лучей. Условия, при которых получали эти данные, были следующими:
40-О-(2-гидрокси)этилрапамицин в кристаллической форме может быть получен путем растворения аморфного соединения в растворителе, например в этилацетате, и добавления алифатического углеводорода СnН2n+2 (n=5, 6 или 7). После добавления углеводорода образовавшаяся смесь может быть нагрета, например, до температуры 25-50°С, например до 30-35°С. Выдерживание образовавшейся смеси обычно производят при низкой температуре, например ниже 25°С, предпочтительно от 0 до 25°С. Кристаллы фильтруют и сушат. В качестве алифатического углеводорода предпочтительно используют гептан. При необходимости процесс образования центров кристаллизации можно инициировать, например, путем облучения ультразвуком или с помощью затравки.
Настоящее изобретение также относится к способу очистки 40-O-(2-гидрокси)этилрапамицина, включающему кристаллизацию 40-O-(2-гидрокси)этилрапамицина из среды для кристаллизации, например из описанной выше среды, и выделения полученных таким образом кристаллов. Среда для кристаллизации может включать один или несколько компонентов в дополнение к перечисленным выше. Было установлено, что наиболее пригодной средой для кристаллизации является среда, содержащая приблизительно 2 части этилацетата и приблизительно 5 частей алифатического углеводорода, например гептана.
Было установлено, что 40-O-(2-гидрокси)этилрапамицин в кристаллической форме обладает in vitro и in vivo иммуносупрессорной активностью, сопоставимой с активностью аморфной формы. В локализованном GvHD максимальное ингибирование (70-80%) набухания лимфатических узлов достигается при использовании дозы 3 мг 40-O-(2-гидрокси)этилрапамицина в кристаллической форме.
40-O-(2-гидрокси)этилрапамицин может применяться для тех же показаний, которые известны для аморфного соединения, например для предупреждения или лечения острого или хронического отторжения алло- или ксенотрансплантата, аутоиммунных болезней или воспалительных состояний, астмы, пролиферативных болезней, например опухолей, или гиперпролиферативных сосудистых заболеваний, например, как описано в WO 94/09010 или в WO 97/35575, содержание которых включено в настоящее описание в качестве ссылки. В целом удовлетворительные результаты получают при пероральном введении в дозах приблизительно от 0,05 до 5 или до 20 мг/кг/день, например приблизительно от 0,1 до 2 или до 7,5 мг/кг/день, которые вводят в виде однократной дозы или в виде разделенных доз 2-4 раза в день. Таким образом, пригодные суточные дозы для пациентов составляют приблизительно до 10 мг, например от 0,1 до 10 мг.
40-O-(2-гидрокси)этилрапамицин в кристаллической форме может вводиться любым пригодным путем, например перорально, например, в виде таблеток или капсул, или назально, или в легкие (путем ингаляции). Он может вводиться в качестве единственного действующего вещества или вместе с другими лекарствами, например иммунодепрессантами, и/или иммуномодуляторами, и/или противовоспалительными агентами, например, как это описано в WO 94/09010.
В соответствии с вышеизложенным объектами настоящего изобретения также являются:
5. Способ предупреждения или лечения острого или хронического отторжения алло- или ксенотрансплантата, аутоиммунных болезней или воспалительных состояний, астмы, пролиферативных болезней или гиперпролиферативных сосудистых заболеваний у пациента, нуждающегося в таком лечении, предусматривающий введение указанному пациенту терапевтически эффективного количества 40-O-(2-гидрокси)этилрапамицина в кристаллической форме;
6. 40-O-(2-гидрокси)этилрапамицин в кристаллической форме, предназначенный для применения в качестве фармацевтического средства; например, согласно описанному выше способу;
7. Фармацевтическая композиция, включающая 40-O-(2-гидрокси)этилрапамицин в кристаллической форме вместе с фармацевтически приемлемым разбавителем или носителем;
8. Набор или упаковка, предназначенные для применения с целью иммуносупрессии или оказания противовоспалительного действия, включающие описанную выше фармацевтическую композицию, и фармацевтическая композиция, включающая иммунодепрессант, или иммуномодулятор, или противовоспалительный агент.
Приведенные ниже примеры служат для иллюстрации изобретения, не ограничивая его объем.
Пример 1: Кристаллизация
0,5 г аморфного 40-O-(2-гидрокси)этилрапамицина растворяют в 2,0 мл этилацетата при 40°С. Добавляют 5,0 мл гептана, после чего раствор становится "мутным". После нагревания до 30°С раствор снова становится прозрачным. После охлаждения до 0°С и поскребывания из раствора выделяется масло. Опытную пробирку закрывают и хранят в течение ночи при 10°С. Затем образовавшееся объемное твердое вещество фильтруют и промывают 0,5 мл смеси этилацетат/гексан (1:2,5) и образовавшиеся кристаллы сушат при 40°С при давлении 5 мбар в течение 16 ч. Таким образом получают 40-O-(2-гидрокси)этилрапамицин в кристаллической форме, имеющий tпл 146,5°С.
Крупномасштабная кристаллизация может быть осуществлена следующим образом.
250 г аморфного 40-О-(2-гидрокси)этилрапамицина растворяют при медленном перемешивании в 1,0 л этилацетата в атмосфере аргона. Раствор выдерживают при 30°С и затем в течение 45 мин по каплям добавляют 1,5 л гептана. В тех же самых условиях добавляют порциями 0,25 г затравочных кристаллов, полученных, как описано выше. Смесь перемешивают при 30°С в течение 2 ч и смесь для кристаллизации охлаждают до 25°С в течение 1 ч, а затем до 10°С в течение 30 мин и фильтруют. Кристаллы промывают 100 мл смеси этилацетат/гексан (2:3). Последующую сушку осуществляют при 50°С и давлении приблизительно 5 мбар. tпл 146,5°С.
ИК (КВr): 3452, 2931, 1746, 1717, 1617, 1453, 1376, 1241, 1191, 1163, 1094, 1072, 1010, 985, 896 см-1.
Элементарное строение, полученное с помощью рентгеновских лучей, с соответствующими координатами, представлено ниже на фиг.1-3.
Пример 2: Получение стабилизированного 40-О-(2-гидрокси)этилрапамицина
100 г 40-О-(2-гидрокси)этилрапамицина растворяют в 600 л абсолютного этанола. После добавления 0,2 г ВНТ образовавшийся раствор по каплям при перемешивании в течение 1 ч добавляют к 3,0 л воды. Образовавшуюся суспензию перемешивают еще в течение 30 мин. После фильтрации с последующей промывкой (3×200 мл смеси вода/этанол в соотношении 5:1 (об./об.)) получают влажный продукт белого цвета, который затем сушат под вакуумом (1 мбар) при 30°С в течение 48 ч. Образовавшийся высушенный продукт содержит 0,2 мас.% ВНТ.
Образовавшийся продукт обладает улучшенной стабильностью при хранении. Сумма побочных продуктов и продуктов разложения в % после хранения в течение 1 недели составляет:
Соединение 50°С в открытой колбе
соединение из примера 2 (0,2% ВНТ) 1,49
без ВНТ >10
Процесс, описанный выше в примере, может быть повторен с использованием рапамицина в качестве действующего вещества.
1. Способ стабилизации рапамицина или производного рапамицина, имеющего иммуносупрессивные свойства, включающий
а. растворение очищенного рапамицина или производного рапамицина в инертном растворителе;
б. добавление антиоксиданта в целевой раствор в количестве до 1% в пересчете на массу рапамицина или производного рапамицина;
в. выделение целевой смеси рапамицина или производного рапамицина и антиоксиданта.
2. Способ по п.1, отличающийся тем, что антиоксидант добавляют в количестве 0,01-0,5% в пересчете на массу рапамицина или производного рапамицина.
3. Способ по п.2, отличающийся тем, что антиоксидант добавляют в количестве 0,2% в пересчете на массу рапамицина или производного рапамицина.
4. Способ по п.1, отличающийся тем, что антиоксидант представляет собой 2,6-ди-трет.-бутил-4-метилфенол.
5. Способ по любому из пп.1-4, отличающийся тем, что производное рапамицина представляет собой 40-O-(2-гидрокси)этилрапамицин.
6. Способ по п.5, отличающийся тем, что на стадии а) используется 40-O-(2-гидрокси)этилрапамицин или рапамицин в кристаллической форме.
7. Способ по любому из пп.1-6, отличающийся тем, что целевая смесь выделяется в виде твердой смеси.
8. Способ по любому из п.1, отличающийся тем, что целевые стабилизированные рапамицин или производное рапамицина затем преобразуются в фармацевтическую композицию.
9. Смесь в твердой форме, включающая рапамицин или производное рапамицина, имеющего иммуносупрессивные свойства, и антиоксидант, причем антиоксидант присутствует в смеси в количестве до 1% в пересчете на массу рапамицина или производного рапамицина.
10. Смесь по п.9, где антиоксидант присутствует в количестве 0,01-0,5% в пересчете на массу рапамицина или производного рапамицина.
11. Смесь по п.10, где антиоксидант присутствует в количестве 0,2% в пересчете на массу рапамицина или производного рапамицина.
12. Смесь по п.9, где антиокисидант представляет собой 2,6-ди-трет.-бутил-4-метилфенол.
13. Смесь по любому из пп.9-12, где производное рапамицина представляет собой 40-О-(2-гидрокси)этилрапамицин.
14. Смесь по п.13, полученная способом по п.1.