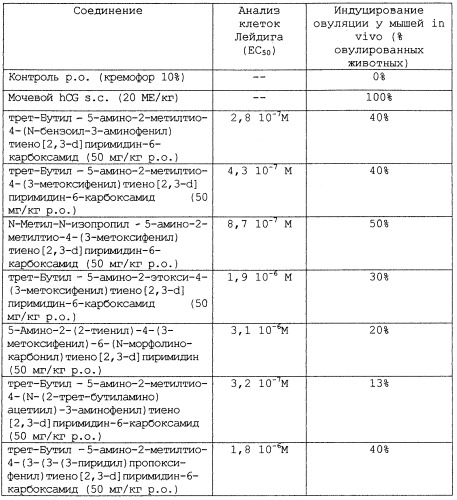
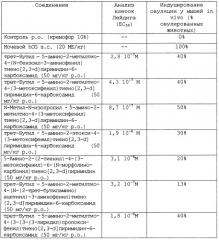
Бициклические гетероароматические соединения в качестве lh агонистов и фармацевтическая композиция
Иллюстрации
Показать всеИзобретение относится к новому производному бициклического гетероароматического соединения общей формулы (I) или его фармацевтически приемлемой соли
обладающему агонистической активностью в отношении лютеинизирующего гормона (LH). Соединения могут быть использованы для получения лекарственных средств для контроля способности к зачатию. В соединениях общей формулы (I) R1 представляет R7; R7 представляет (6-10С)арил, необязательно замещенный в орто- и/или мета-положении атомом галогена; NHR8, OR8, где R8 означает (1-8С)алкил, который может быть замещен атомом галогена, (1-8С)алкилкарбонил, (1-8С)алкилкарбонилокси, фенил, (6-10С)арилкарбониламино, 5-метил-2-фенилимидазол-4-илом, (6С)гетероциклоалкилом, в котором 1-2 гетероатома, выбранных из азота и кислорода, этилоксикарбонилметилтио(1-4С)алкокси, амино, (6-7С)гетероарилом; или (5-6С)гетероарил, содержащий в качестве гетероатома азот, кислород или серу; R2 представляет (1-8С)алкил, либо (6-10С)арил, необязательно замещенный одним или более заместителями, выбранными из (1-8С)алкокси; или (5-6С)гетероарил, содержащий в качестве гетероатома азот, кислород или серу; R3 представляет (1-8C)алкил, возможно замещенный (6-14С)арилом, возможно замещенный галогеном, (1-4С)алкокси, (1-4С)алкоксикарбонилом, моно- или три(6-10С)циклоалкилом, (6-10С)арилом, (5-6C)гетероарилом, содержащим в качестве гетероатома азот, кислород или серу; (5-7С)гетероциклоалкилом, содержащим 2 гетероатома, выбираемых из азота или кислорода; (3-8С)циклоалкил, (2-7С)гетероциклоалкил, содержащий 2 гетероатома, выбираемых из азота или кислорода; либо (6-10С)арил, необязательно замещенный одним или более заместителями, выбранными из (1-8С)алкокси; Х представляет S или N(R4); Y представляет N; R4 представляет Н, (1-8С)алкил, фенил(1-8С)алкил; или Х представляет S, а Y представляет СН; Z представляет NH2 или ОН; А представляет S, О или связь; В представляет N(H), O или связь. Изобретение также относится к фармацевтической композиции. 3 н. и 11 з.п. ф-лы, 1 табл.
Реферат
Изобретение относится к соединениям, обладающим агонистической или ангонистической активностью в отношении гликопротеинового гормона, в частности к соединениям, обладающим агонистической активностью в отношении лютеинизирующего гормона (LH). Кроме того, изобретение относится к производным бициклических гетероароматических соединений, к содержащим их фармацевтическим композициям, а также к применению данных соединений в лечебной терапии, в частности, при использования для контроля зачатия.
Гонадотропины выполняют важные функции во множестве функций тела, включая мегаболизм, регулирование температуры и репродуктивный процесс. Гипофизарный гонадотропин FSH, например, играет стержневую роль в стимулировании развития и созревания фолликула, тогда как LH индуцирует овуляцию (Sharp R.M., Clin. Endocrinol. 33:787-807, 1990; Dorrington и Armstrong, Recent Prog.Horm.Res. 35:301-342, 1979). В настоящее время LH применяют клинически, в сочетании с FSH для стимуляции яичников, то есть гиперстимуляции яичников для оплодотворения in vitro (IVF) и индуцирования овуляции у бесплодных ановулярных женщин (Insler V., Int.J.Fertility 33:85-97, 1988, Navotg и Rosenwaks, J.Vitro Fert.Embryo Transfer 5:3-13, 1988), а также в случае мужского гипогонадизма и мужского бесплодия.
Гонадотропины действуют на специфические клетки половых желез для инициирования дифференцировки и стероидогенеза яичников и семенников. Действие данных гипофизарных и плацентарных гормонов опосредовано специфическими плазматическими мембранными рецепторами, которые являются членами большого семейства G-протеинсвязанных рецепторов. Они состоят из отдельного полипептида с семью трансмембранными доменами и способны взаимодействовать с Gs протеином, приводя к активизации аденилциклаэы.
Гонадотропины, предназначенные для терапевтических целей, могут быть выделены из источника мочи человека и имеют низкую чистоту (Morse et al., Amer.J.Reproduct.Immunol. и Microbiology 17:143, 1988). Альтернативно, они могут быть получены как рекомбинантные гонадотропины.
Как и в случае других терапевтических белков, гонадотропины необходимо вводить или подкожно или внутримышечно. Было бы несомненным преимуществом, однако, активировать рецептор с помощью небольшой молекулы, которую можно было бы вводить посредством, например, перорального или чрескожного пути введения.
В настоящем изобретении описано получение таких низкомолекулярных аналогов гормонов, которые селективно активируют один из гонадотропиновых рецепторов. Это следует рассматривать в качестве одного из главных преимуществ настоящего изобретения.
Таким образом, изобретение относится к бициклическим гетероароматическим производным общей формулы I или их фармацевтически приемлемой соли, или их сольвату
где R1 представляет NR5R6, OR5, SR5 или R7, предпочтительно R1 представляет R7;
R5 и R6 независимо выбраны из Н, (1-8С)алкила, (2-8С)алкенила, (2-8С)алкинила, (3-8С)циклоалкила, (2-7С)гетероциклоалкила, (1-8С)алкилкарбонила, (6-14С)арилкарбонила, (6-14С)арила или (4-13С)гетероарила, или R5 и R6 вместе объединены в (2-7С)гетероциклоалкильное кольцо;
R7 представляет (3-8С)циклоалкил, (2-7С)гетероциклоалкил, (6-14С)арил или (4-13С)гетероарил, предпочтительно R7 представляет (6-14С)арил или (4-13С)гетероарил;
R2 представляет (1-8С)алкил, (2-8С)алкенил, (2-8С)алкинил либо (6-14С)арил или (4-13С)гетероарил, оба необязательно замещенные одним или более заместителями, выбранными из (1-8С)алкила, (1-8С)алкилтио, (1-8С)(ди)алкиламино, (1-8С)алкокси, (2-8С)алкенила или (2-8С)алкинила;
R3 представляет (1-8С)алкил, (2-8С)алкенил, (2-8С)алкинил, (3-8С)циклоалкил,-(2-7С)гетероциклоалкил либо (6-14С)арил или (4-13С)гетероарил, оба необязательно замещенные одним или более заместителями, выбранными из (1-8С)алкила, (1-8С)(ди)алкиламино или (1-8С)алкокси, предпочтительно R3 представляет (1-8С)алкил, более предпочтительно (1-4С)алкил, даже более предпочтительно R3 представляет изопропил или трет-бутил;
Х представляет S, О или N(R4);
R4 представляет Н, (1-8С)алкил, (1-8С)алкилкарбонил, (6-14С)арилкарбонил или (6-14С)арил(1-8С)алкил;
Y представляет СН или N, предпочтительно Y представляет N;
Z представляет NH2 или ОН;
А представляет S, N(H), N(R9), О или связь;
R9 может быть выбран из тех же групп, которые описаны для R2, и В представляет N(Н), О или связь.
Алкильная группа, алкенильная группа или алкинильная группа, если присутствует в R5 и/или R6 в указанной выше формуле, может быть необязательно замещена одним или более заместителями, выбранными из гидроксила, (6-14С)арила, (1-8С)алкокси, (1-8С)алкилкарбонилокси, (6-14С)арилкарбонилокси, (1-8С)алкоксикарбонила, (6-14С)арилоксикарбонила, (1-8C)алкилкарбонила, (6-14С)арилкарбонила, амина, (1-8С)алкиламинокарбонила, (6-14С)ариламинокарбонила, (1-8С) алкилкарбониламино, (6-14С)арилкарбониламино, (6-14С)(ди)ариламино и/или (1-8С)(ди)алкиламино.
Если R7 представляет (6-14С)арил или (4-13С)гетероарил, арил может быть необязательно замещен в орто и/или мета-положении одним или более заместителями, выбранными из R8, (6-14С)арила, (4-13С)гетероарила, (2-7С)гетероциклоалкила, (3-8С)циклоалкила, NHR8, OR8 и/или SR8, где R8 представляет (6-14C)арил, (4-13C)гетероарил, (1-8C)алкилкарбонил, (6-14С) арилкарбонил, (1-8С)алкил, (2-8С)алкенил, (2-8C)алкинил, алкильная группа которых может быть необязательно замещена одним или более заместителями, выбранными из гидроксила, (1-8С)алкокси, (2-7С)гетероциклоалкил((1-8С)алкокси, (3-8)циклоалкил((1-8С)алкокси, (6-14С)арил((1-8С)алкокси, (4-13С)гетероарил((1-8С)алк)окси, (2-7С)гетероциклалкила, (3-8С) циклоалкила, (6-14С)арила, (4-13С)гетероарила, (1-8С) алкоксикарбонила, (6-14С)арилоксикарбонила, (1-8C)алкилкарбонилокси, (1-14С)арилкарбонилокси, (1-8С)алкилкарбонила, (6-14С)арилкарбонила, амино, (1-8С)алкиламинокарбонила, (6-14С)ариламинокарбонила, (1-8С)алкилкарбониламино, (6-14С)арилкарбониламино, (6-14С)(ди)ариламино и/или (1-8C)(ди)алкиламино. Предпочтительно заместители при ариле в R7 выбраны из NHR8 или OR8. R8 предпочтительно представляет (1-8С)алкилкарбонил, (6-14C)арилкарбонил, (1-8С)алкил. Большинство предпочтительных заместителей в алкильной группе представляют (2-7С)гетероциклоалкил, (1-6С)(ди)алкиламино и амин.
Алкильная группа, алкенильная группа или алкилнильная группа, если они присутствуют в R9 или R2 в указанной выше формуле, необязательно могут быть замещены одним или более заместителями, выбранными из (6-14С)арила, (4-13С)гетероарила, (1-8С)алкилкарбонила, (6-14С)арилкарбонила, (1-8C)алкилкарбонилокси, (6-14C)арилкарбонилокси, (6-14С)арилоксикарбонила и/или (1-8С)алкоксикарбонила.
Алкильная группа, алкенильная группа или алкинильная группа, если они присутствуют в R3 в указанной выше формуле, необязательно могут быть замещены одним или более заместителями, выбранными из гидроксила, (1-8С)алкокси, (6-14С)арилокси, (3-8С)циклоалкил((1-8С)алк)окси, (2-7С)гетероциклоалкил((1-8С)алк)окси, (6-14С)арил((1-8С)алк)окси, (4-13С)гетероарил((1-8С)алк)окси, (2-7С)гетероциклоалкила, (6-14С)арила, (4-13С)гетероарила, (1-8С)алкоксикарбонила, (6-14С)арилоксикарбонила, (1-8С)алкилкарбонилокси, (6-14С)арилкарбонилокси, (1-8С)алкилкарбонила, (6-14С)арилкарбонила, амино, (1-8С)алкиламинокарбонила, (6-14С)ариламинокарбонила, (1-8С)алкилкарбониламино, (6-14С)арилкарбониламино, (6-14С)(ди)ариламино или (18С)(ди)алкиламино.
Предпочтительными соединениями согласно изобретению являются соединения общей формулы I, где Х представляет S и/или Z представляет NH2. Среди данных предпочтительных соединений особенно предпочтительными являются те, в которых Х представляет S и Z представляет NH2, даже более предпочтительными соединениями являются те, где в дополнение Y представляет N. Наиболее предпочтительными являются соединения, в которых, в дополнение к указанным выше определениями X, Z и Y, R1 определен как представляющий собой (6-14С)арил и (4-13С)гетероарил. Наиболее предпочтительно А представляет S.
Сверхпредпочтителывами соединениями изобретения являются производные бициклических гетероароматических соединений, имеющие общую формулу I, где
R1 представляет (6-14С)арил или (4-13С)гетероарил,
R2 представляет (1-8С)алкил, (2-8С)алкенил, (2-8С)алкинил либо (6-14С)арил или (4-13С)гетероарил, оба необязательно замещенные одним или более заместителями, выбранными из (1-8С)алкила, (1-8С)алкилтио, (1-8С)алкокси, (2-8С)алкеиила или (2-8С)алкинила,
R3 представляет (1-8С)алкил, (2-8С)алкенил, (2-8С)алкинил, (3-8С)циклоалкил, (2-7С)гетероциклоалкил либо (6-14С)арил или (4-13С)гетероарил, оба необязательно замещенные одним или более заместителями, выбранными из (1-8С)алкила, (1-8С)(ди)алкиламино или (1-8С)алкокси,
Х представляет S, Z представляет NH2, А представляет S и В представляет N(Н), О или связь.
Данные соединения имеют общую структуру
R1 представляет (6-10С)арил, необязательно замещенный одним или более заместителями, выбранными из (1-8С)алкокси, галогена, (1-4С)алкокси, (1-4С)алкоксикарбонила, или (5-6С)гетероарил, содержащий в качестве гетероатома азот, кислород или серу;
R2 представляет (1-8С)алкил, (6-10С) арил, необязательно замещенный одним или более заместителями, выбранными из (1-8С)алкокси, или (5-6С)гетероарил, содержащий в качестве гетероатома азот, кислород или серу,
R3 представляет (1-8С)алкил, возможно замещенный галогеном, (1-4С)алкокси, (1-4С)алкоксикарбонилом моно- или три(6-10С)циклоалкилом, (6-10С)арилом, (5-6С)гетероарилом, (5-7С)гетероциклоалкилом, содержащим в качестве гетероатома азот, кислород или серу; (3-8С)циклоалкип, (2-7С)гетероциклоалкил либо (6-10С)арил, необязательно замещенной одним или более заместителями, выбранными из (1-8С) алкокси;
В представляет N(H), О или связь; Y представляет СН или N.
Наиболее предпочтительными соединениями являются соединения общей формулы I, более предпочтительно общей формулы II, где В представляет N или О, при этом наиболее предпочтительно, когда B представляет N. R2 и/или R3 предпочтительно представляют (1-8С)алкил, более предпочтительно (1-4С)алкил, и Y предпочтительно представляет N.
Особенно предпочтительными соединениями согласно изобретению являются те, в которых R3 представляет изопропил или трет-бутил, при этом трет-бутил является наиболее предпочтительным.
Из изобретения исключены соединения, представляющие собой метил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, этил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, метил-5-амино-4-(4-метоксифенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, этил-5-амино-4-(4-метоксифенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, метил-5-амино-4-(4-хлорфенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат или этил-5-амино-4-(4-хлорфенил)-2-метилтиотиено[2, 3-d]пиримидин-6-карбоксилат.
Исключенные из заявляемого объема притязаний соединения описаны в публикациях Phosph.Sulf.Sil.Rel.Chem: 60, 223-231, 1991; J.Chem.Res., Synop.(6):290-291, 1998, и Sulfur Lett. 9:101-108, 1989.
Термин (1-8С)алкил, как он использован в определении формул I и II, означает разветвленную или неразветвленную алкильную группу, имевшую 1-8 атомов углерода, например метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, гексил и октил (1-6С). Алкильные группы являются предпочтительными, при этом наиболее предпочтительной является (1-3С)алкильная.
Термин (2-8С)алкенил означает разветвленную или неразветвленную алкенильную группу, имеющую 2-8 атомов углерода, такую как этенил, 2-бутенил и т.д.
Термин (2-8С)алкинил означает разветвленную или неразветвленную алкинильную группу, имеющую 2-8 атомов углерода, такую как этинил и пропинил.
Термин (3-8С)циклоалкил означает циклоалкильную группу, имеющую 3-8 атомов углерода, представляющую собой циклопропил, циклобутил, циклогексил, циклогептил или циклооктил.
Термин (2-7С)гетероциклоалкил означает гетероциклоалкильную группу, имеющую 3-8 атомов углерода, предпочтительно 3-5 атомов углерода, и включающую по крайней мере один гетероатом, выбранный из N, О и S. Предпочтительными являются N или О. Наиболее предпочтительны пиперидин, морфолин и пирролидин.
Термин (1-8С)алкокси означает алкоксильную группу, имеющую 1-8 атомов углерода, где алкильный фрагмент имеет такие же значения, как определено выше. (1-6С)Алкоксильные группы являются предпочтительными, наиболее предпочтительной является (1-3С)алкоксигруппа.
Термин (1-8С)алкоксикарбонил означает алкоксикарбонильную группу, в которой алкильная группа содержит 1-8 атомов углерода и имеет такие же значения, как определено выше.
Термин (1-8С)(ди)алкиламино означает (ди)алкиламиногруппу, имеющую 1-8 атомов углерода, где алкильная группа имеет такие же значения, как определено выше.
Термин (6-14С)(ди)ариламино означает (ди)ариламиногруппу, имеющую 6-14С атомов углерода, арильный фрагмент имеет такие же значения, как определено выше.
Термин (1-8С)алкилтио означает алкилтиогруппу, имеющую 1-8 атомов углерода, алкильный фрагмент имеет такие же значения, как определено выше.
Термин (6-14С)арил означает ароматическую углеводородную группу, имеющую 6-14 атомов углерода, такую как фенил, нафтил, тетрагидронафтил, инденил, антрацил, которая необязательно может быть замещена одним или более заместителями, такими как, но не ограничиваясь ими, гидрокси, галоген, нитро, трифторметил, циано, (1-8С) алкилкарбониламино, (1-8С)алкиламинокарбонил или (1-8С)(ди)алкиламино, при этом алкильные фрагменты имеют такие же значения, как определено выше. Предпочтительной ароматической углеводородной группой является фенил.
Термин (6-14С)арилоксикарбонил означает арилоксикарбонильную группу, в которой арильная группа содержит 6-14 атомов углерода и имеет такие же значения, как определено выше.
Термин (6-14С)арил(1-8С)алкил означает арилалкильную группу, имеющую 7-22 атома углерода, где алькильная группа представляет собой (1-8С)алкильную группу, и арильная группа представляет собой (6-14С)арил, как определено ранее. Предпочтительными арилалкильными группами являются фенил(1-8С)алкильные группы, такие как бензил.
Термин (4-13С)гетероарил означает замещенную или незамещенную ароматическую группу, имеющую 3-13 атомов углерода, предпочтительно 4-9, включающую, по крайней мере, один гетероатом, выбранный из N, О и/или S, такую как имидазолил, тиенил, бензтиенил, хинолил, тетрагидрохинолил, изохинолил, тетрагидроизохинолил, индолил, акридинолил, фурил или пиридил. Заместители гетероарильной группы могут быть выбраны из группы заместителей, перечисленных для арильной группы. Предпочтительными гетероарильными группами являются тиенил, фурил и пиридил.
Термин “присоединенный” в (2-7С)гетероциклоалкильном кольце в определении NR5R6, где R5 и R6 вместе с атомом азота, с которым они связаны, представляют кольцо, означает кольцо, содержащее атом азота и дополнительно имеющее вплоть до 2-7 атомов углерода, причем указанное кольцо может содержать ненасыщенные связи или один или более гетероатомов, выбранных из N, О и/или S. Примерами таких колец являются азетидин, пирролидин, пиперидин, пиперазин, морфолин и тиоморфолин.
Термин галоген означает фтор, хлор, бром или иод.
Термин (2-7С)гетероциклоалкил(1-8С)алкокси означает гетероциклоалкильную группу, содержащую 3-8 атомов углерода, как определено выше, присоединенную к (1-8С)алкоксильной группе, где алкоксильный фрагмент имеет значение, определенное выше.
Термин (3-8С)циклоалкил(1-8С)алкокси означает циклоалкильную группу, содержащую 3-8 атомов углерода, как определено выше, присоединенную к (1-8С)алкоксильной группе, где алкоксильный фрагмент имеет значение, определенное выше.
Термин (6-14С)арил(1-8С)алкокси означает арильную группу, содержащую 6-14 атомов углерода, как определено выше, присоединенную к (1-8С)алкоксильной группе, где алкоксильный фрагмент имеет значение, определенное выше.
(4-13С)Гетероарилалкоксигруппы представляют собой аналоги (6-14С)арилалкоксигрупп, включая по крайней мере один гетероатом, выбранный из N, О и S.
Термин (1-8С)алкилкарбонил означает алкилкарбонильную группу, алкильная группа, которой содержит 1-8 атомов углерода и имеет такие же значения, как определено выше.
Термин (6-14С)арилкарбонил означает арилкарбонильную группу, арильная группа которой содержит 6-14 атомов углерода и имеет такое же значение, как определено выше.
Термин (1-8С)алкилкарбонилокси означает алкилкарбонилоксигруппу, алкильная группа которой содержит 1-8 атомов углерода имеет такие же значения, как определено выше.
Термин (6-14С)арилкарбонилокси означает арилкарбонилоксигруппу, арильная группа которой содержит 6-14 атомов углерода и имеет такое же значение, как определено выше.
Термин (1-8С)алкилиминокарбонил означает алкиламинокарбонильную группу, алкильная группа которой содержит 1-8 атомов углерода и имеет такое же значение, как определено выше.
Термин (6-14С)ариламинокарбонил означает ариламинокарбонильную группу, арильная группа которой содержит 6-14 атомов углерода и имеет такое же значение, как определено выше.
Термин (1-8С)алкилкарбониламино означает алкилкарбониламиногруппу, алкильная группа которой содержит 1-8 атомов углерода и имеет такое же значение, как определено выше.
Термин (6-14С)арилкарбониламино означает арилкарбониламиногруппу, арильная группа которой содержит 6-14 атомов углерода и имеет такое же значение, как определено выше.
Термин (2-7С)гетероциклоалкилокси означает гетероциклоалкильную группу, содержащую 3-8 атомов углерода, как определено выше, присоединенную к атому кислорода.
Термин (3-8С)циклоалкилокси означает циклоалкильную группу, содержащую 3-8 атомов углерода, как определено ранее, присоединенную к атому кислорода.
Термин (6-14С)арилокси означает арильную группу, содержащую 6-14 атомов углерода, как определено выше, присоединенную к атому кислорода. (4-13С)Гетероарилоксигруппы представляют собой аналоги (6-14С)арилоксигрупп, включая по крайней мере один гетероатом, выбранный из N, О и S.
Было показано, что соединения указанной выше формулы I способны связываться с LH рецептором и проявляют агонистическую по отношению к LH активность.
Изобретение дополнительно относится к фармацевтической композиции, включающей производное бициклического гетероароматического соединения или его соли, имеющего общую формулу I.
Фармацевтические композиции, которые включают этил-5-амино-4-фенил-2-этоксикарбонилметилтиотиено[2,3-d]пиримидин-6-карбоксилат, метил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат или этил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, подпадают под объем настоящего изобретения. Таким образом, соединения согласно изобретению могут использоваться в терапии. Дополнительный аспект изобретения относится к применению бициклического гетероароматического соединения, имеющего общую формулу I, для получения лекарственного средства для контроля способности к зачатию. Предпочтительно настоящие соединения используют для активации LH рецептора.
Производные бициклических гетероароматических соединений данного изобретения могут обладать одним или более хиральными атомами углерода. Следовательно, соединения могут быть получены в виде хирально чистых соединений или в виде смеси дистереомеров и/или энатиомеров. Способы получения хирально чистых соединений хорошо известны в данной области, например кристаллизация или хроматография.
Для терапевтического применения соли соединений формулы I представляют собой такие соли, в которых противоион является фармацевтически приемлемым. Однако кислотно-аддитивные соли оснований, соответствующих формуле I, могут также найти применение, например, для получения или очистки фармацевтически приемлемого соединения. Все соли независимо от того, являются ли они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения.
Примеры кислотно-аддитивных солей включают соли, полученные из минеральных кислот, таких как хлористоводородная кислота, фосфорная кислота, серная кислота, предпочтительно из хлористоводородной кислоты, и органических кислот, таких как лимонная кислота, винная кислота, уксусная кислота, молочная кислота, малеиновая кислота, малоновая кислота, фумаровая кислота, гликолевая кислота, янтарная кислота и тому подобное.
Подходящие пути введения соединений формулы I или их фармацевтически приемлемых солей, также указанных в данном описании как активный ингредиент, представляют собой внутримышечные инъекции, подкожные инъекции, внутривенные инъекции или внутрибрюшинные инъекции, пероральное или внутриназальное введение. Предпочтительно соединения можно вводить перорально. Точная доза и режим введения активного ингредиента или его фармацевтической композиции необходимым образом будут зависеть от терапевтического действия, которое необходимо достигнуть (лечение бесплодия; контрацепция) и могут изменяться в зависимости от конкретного соединения, пути введения, возраста и состояния индивидуального субъекта, которому следует вводить данное лекарственное средство.
Обычно при парентеральном введении требуются более низкие дозы, чем при других методах введения, которые более зависят от абсорбции. Однако доза для человека предпочтительно составляет 0,0001-25 мг на 1 кг веса тела. Желаемая доза может присутствовать в виде одной дозы или в виде множества поддоз, вводимых через подходящие временные интервалы в течение дня, или, в случае реципиентов женского пола, в виде доз для введения с подходящими суточными интервалами в течение менструального цикла. Дозировка, также как и режим введения, могут различаться для реципиентов женского и мужского пола.
В случае in vitro или ex vivo применений, таких как IVF применения, соединения изобретения следует применять в инкубационной среде в концентрации приблизительно 0,01-5 мкг/мл.
Таким образом, настоящее изобретение также относится к фармацевтическим композициям, содержащим бициклическое гетероароматическое соединение согласно формуле I, включая в том числе фармацевтические композиции, содержащие этил-5-амино-4-фенил-2-этоксикарбонилметилтиотиено[2,3-d]пиримидин-6-карбоксилат, метил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат или этил-5-амино-4-фенил-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат, 6-ацетил-5-амино-4-фенил-2-(2-оксопропилтио)тиено[2,3-d]пиримидин, 5-амино-6-бензоил-4-фенил-2-фенилкарбонилметилтиотиено[2,3-d]пиримидин или 5-амино-6-(4-хлорбензоил)-4-фенил-2-[(4-хлорфенил)карбонилметилтио]тиено[2,3-d]пиримидин в смеси с фармацевтически приемлемыми вспомогательными добавками и, необязательно, другими терапевтическими агентами.
Вспомогательные добавки должны быть “приемлемыми” в смысле совместимости с другими ингредиентами композиции и не должны оказывать вредного воздействия на реципиентов.
Фармацевтические композиции включают подходящие для перорального, ректального назального, местного (включая чрескожное, буккальное и сублингвальное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное и внутрикожное) введения. Композиции могут быть получены любыми способами, хорошо известными в области фармацевтики, например, с использованием таких способов, как описано Gennaro et al., Remington's Pharmaceutical Sciences (18th ed., Mack Publishing company, 1990, в особенности, см. Part 8: Pharmaceutical Preparations и Their Manufacture (Часть 8: Фармацевтические препараты и их получение).
Такие способы включают стадию введения активного ингредиента в состав с любым вспомогательным агентом. Вспомогательный агент(ы), также именуемые вспомогательными ингредиентами, включают общепринятые в данной области (Gennaro, выше), такие как наполнители, связующие вещества, разбавители, дезинтегранты, смазывающие вещества, красители, вкусовые агенты и смачивающие агенты.
Фармацевтические композиции, подходящие для перорального введения, могут присутствовать в виде дискретных препаративных лекарственных форм, таких как пилюли, таблетки или капсулы, или в виде порошка или гранул, или в виде раствора или суспензии. Активный ингредиент также может присутствовать в виде болюса или пасты. Композиции дополнительно могут быть переработаны в суппозитории или клизмы для ректального введения.
Для парентерального введения подходящие композиции включают водные и неводные стерильные инъекции. Композиции могут присутствовать в контейнерах для единичной дозы или для множества доз, например в герметично закрытых сосудах или ампулах, и могут храниться в высушенном вымораживанием (лиофилизованном) виде, требующем только добавления стерильного жидкого носителя, например воды, перед употреблением.
Композиции или составы, подходящие для введения посредством назальной ингаляции, включают мелкоизмельченные порошки или тонкораспыленные жидкости, которые можно генерировать с помощью снабженных дозатором аэрозольных упаковок, распылителей или воздушных инжекторов.
Производные бициклических гетероароматических соединений изобретения также можно вводить в форме имплантируемых фармацевтических устройств, состоящих из ядра активного вещества, заключенного в контролирующую скорость высвобождения мембрану. Такие имплантаты применяют подкожно или местно, и они будут высвобождать активный ингредиент с приблизительно постоянной скоростью на протяжении относительно больших промежутков времени, например от недель до лет. Способы получения имплантируемых фармацевтических устройств как таковые известны в данной области, например описаны в Европейском патенте 0303306 (AKZO N.V.).
Таким образом, соединения согласно настоящему изобретению можно использовать в тех же клинических целях, что и природный LH, с тем преимуществом, что они проявляют измененные свойства стабильности и могут вводиться различными способами.
Соединения настоящего изобретения, где B=NH, представленные формулой (I-a), обычно могут быть получены в соответствии с известной в данной области реакцией конденсации кислоты формулы (III) с амином формулы (IV).
Указанное выше взаимодействие обычно проводят при комнатной температуре в подходящем растворителе, например в апротонном растворителе, таком как N,N-диметилформамид или дихлорметан, с использованием агента сочетания, такого как тетрафторборат O-(бензотриазол-1-ил)-N,N,N’,N’-тетраметилурония (TBTU) или гексафторфосфат бромтрипирролидинфосфония (PyBrOP), и третичного основания, например N,N-диизопропилэтиламина.
Аналогично соединения формулы (I), где В=O, представленные формулой (1-b), могут быть получены таким же способом, как описано выше для соединений формулы (I-a), исходя из кислот общей структуры (III) и спиртов формулы (V).
Соединения формулы (I), где В представляет связь, представленные формулой (I-c), могут быть получены конденсацией пиридилхлоридов (VI), где W = CN или C(O)(OEt), с соединениями общей структуры (VII) в подходящих растворителях, таких как этанол, метанол или тетрагидрофуран, при повышенной температуре (50°С) в присутствии основания, например этоксида натрия, метоксида натрия, карбоната калия или гидроксида калия.
Альтернативно, соединения формулы (I-c), где X = S, представленные формулой (I-d) могут быть получены из тиоамидов структуры (VIII), где W является таким, как определено выше, и соединений формулы (IX), где V = галоген, такой как бромид или хлорид, с использованием указанного выше способа.
Подобные циклизации описаны в литературе, см., например, Ю.А.Шаранин, А.М.Шестопалов и В.К.Промоненков, J.Org.Chem. USSR (Engl.Transl.), 20:1828, 1984, Z.H.Khalil и A.A.Geies, Phosph.Sulf.Silic.Relat.Elem. 60:223, 1991.
Подходящим способом получения промежуточных кислот (III) является известное в данной области омыление под действием оснований этиловых сложных эфиров общей формулы (X). Омыление происходит в присутствии основания, такого как гидроксид лития, гидроксид калия или гидроксид натрия, в смеси водного диоксана при повышенной температуре (от 80°С до температуры кипения с обратным холодильником).
Соединения формулы (X) могут быть получены циклизацией пиридилхлоридов (VI) с HXCH2C(O)OEt, как описано выше при синтезе соединений (I-c). В некоторых случаях можно выделить промежуточный не подвергнутый циклизации продукт, который циклизуется при повторной обработке основанием. Альтернативно, соединения формулы (X), где X=S, также могут быть получены с помощью такого же способа, как описано для синтеза производных (I-d), циклизацией (VIII) с VCH2C(O)OEt (IX), где V такой, как определено выше.
Подобные циклизации существуют в литературе. Например, тиено-циклизации описаны A.A.Santilli, D.H.Kim и S.V.Wanser, J.Heterocycl.Chem., 8:445, 1971; S.Kohra, Y.Tominaga и A.Hosomi, J.Heterocycl.Chem., 25:959, 1988; H.Vieweg, U.Krasselt, N.Bohm, J.Prantz и G.Wagner, Pharmazie 45:731, 1990; H.Vieweg и G.Wagner, Pharmazie 46:51, 1991; G.Wagner. H.Vieweg и S.Leitner, Pharmazie 48:588, 1993. Пирролоциклизации описаны, например, D.H.Kim и A.A.Santiili, J.Heterocycl.Chem., 6:819, 1969.
Соединения формулы (VI), где W такой, как определено выше, могут быть синтезированы в соответствии с литературными способами, например, описанными A.A.Santilli, D.H.Kim и S.V.Wanser, J.Heterocycl.Chem., 8:445, 1971. В типичном варианте осуществления амид общей структуры (XI) обрабатывают РОСl3 при повышенной температуре (от 80°С до температуры кипения с обратным холодильником). Добавление подходящего растворителя, например диоксана, и/или добавление либо PCl5, либо N,N-диметиланилина к реакционной смеси может привести к более короткому времени взаимодействия и более высоким выходам хлоридов (VI).
При другом подходе амиды (XI) могут быть обработаны при повышенной температуре (предпочтительно, температура кипения с обратным холодильником) SOCl2, давая соединения формулы (VI), как описано в литературе D.H.Kim и A.A.Santilii, J.Heterocycl.Chem. 6:819, 1969.
Соединения формулы (VIII), где W является таким, как определено выше, могут быть получены обработкой производных (XI) сульфурирующим агентом, например P2S5, или реагентом Лоуссона (Lawesson), в подходящем растворителе, таком как пиридин, при повышенной температуре (предпочтительно, при температуре кипения с обратным холодильником), см. Z.H.Khalil, Phosph.Sulf.Silic.Relat.Elem. 60:223, 1991.
Кроме того, соединения общей формулы (VIII), где Y=CH и А представляет связь, представленные формулой (VIII-a), могут быть синтезированы циклизацией α,β-ненасыщенных кетонов формулы (XII) и тиоацетамида (XIII).
В типичном эксперименте соединения (XII) и (XIII) подвергают взамодействию в растворителе, таком как этанол, метанол или тетрагидрофуран, при повышенной температуре (предпочтительно, при температуре кипения с обратным холодильником) в присутствии основания, например пиперидина, триэтиламина, метоксида натрия или этоксида натрия. Подобные циклизации известны в литературе: H.Vieweg, V.Hanfeld, S.Leitner и G.Wagner, Pharmazie 44:639, 1989; H.Vieweg и G.Wagner, Pharmazie 46:51, 1991.
Альтернативно, соединения формулы (VIII-a, W=CN) могут быть синтезированы, исходя из α,β-ненасыщенных динитрилов общей структуры (XIV) и тиоацетамидов (XV), как описано G.A.H.Elgemeie, Heterocycles 31:123, 1990.
Соединения формулы (XI), где Y=N, представленные формулой (ХI-a), могут быть получены с помощью нескольких подходов на основе литературных данных.
Например, производные формулы (ХI-a), где R1=(6-14)арил или (4-13С)гетероарил, могут быть синтезированы конденсацией этиловых сложных эфиров (XVI), где W является таким, как определено выше, с альдегидами (XVII) и соединениями (XVIII), которые могут представлять собой изотиомочевину (XVIII-a), изомочевину (XVIII-b), монозамещенные гуанидины (XVIII-c), дизамещенные гуанидины (XVIII-d) или амидины (XVIII-e).
В типичном эксперименте компоненты (XVI), (XVII) и (XVIIIa-e) суспендируют в подходящем растворителе, например этаноле, метаноле, N,N-диметилформамиде, N-метилпирролидиноне, тетрагидрофуране или пиридине, и добавляют основание, такое как карбонат калия, ацетат натрия, метоксид натрия или этоксид натрия. Взаимодействие происходит при повышенной температуре (от 70°С до температуры кипения с обратным холодильником). После фильтрования остаток помещают в воду и подкисляют (pH 2), после чего продукты (ХI-a) выпадают в осадок (S.Kambre, K.Saito и H.Kishi, Synthesis, 287 (1979); A.M.Abd-Alfattah, S.M.Hussain и А.М.El-Reedy, Tetrahedron, 39, 3197 (1983); S.M.Hussain, A.A.El-Barbary и S.A.Mansour, J.Heterocycl.Chem., 22, 169 (1985)). В случае, когда W=C(O)OEt, ароматизация происходит при добавлении окислителя, такого как DDQ или кислород. Подобные циклизации также можно проводить на твердом носителе, таком как смола Меррифилда (Merrifield) с использованием подходящего линкера, см., например, A.L.Mrzinzik и E.R.Felder, J.Org.Chem., 63, 723 (1998); T.Masquelin, D.Sprenger, R.Baer, F.Gerber и Y.Mercadal, Helv.Chim.Acta 81, 646 (1998).
Альтернативно, производные формулы (ХI-a), где R1 не является (6-14С)арилом или (4-13С)гетероарилом, могут быть получены замещением Сl в производных формулы (VI-a) или замещением 4-SMe в соединениях формулы (XI-b).
Подобные реакции замещения известны в литературе, например, S.Kohra, Y.Tominaga и A.Hosomi, J.Heterocycl.Chem. 25:959, 1988; A.A.Santilli, D.H.Kim и S.V.Wanser, J.Heterocycl.Chem., 8:445, 1971; J.Clark, M.S.Shannet, D.Korakas и G.G.Varvounis, J.Heterocycl.Chem., 30:1065, 1993; S.Tumkevicius, Liebigs Ann.Org.Biorg.Chem. 9:1703, 1995.
Пиридины общей формулы (XI), где Y=CH, A=S и W=CN, представленные формулой (XX), получают последовательным алкилированием α,β-ненасыщенных динитрилов общей структуры (XIV) сероуглеродом и иодистым алкилом R2-I, с получением соединения общей формулы (XIX), как описано P.Milart, Tetrahedron 54:15643-156556, 1998. Последующая циклизация соединений формулы (XIX) в кислых условиях, как описано K.Peseke, Z.Chem., 29:442-443 (1989) дает пиридины общей формулы (XX).
Способы определения рецепторного связывания, а также in vitro и in vivo анализы для определения биологической активности гонадотропинов хорошо известны. Обычно экспрессированный рецептор приводят в контакт с исследуемым соединением и измеряют связывание или стимуляцию, либо ингибирование функционального ответа.
Для измерения функционального ответа выделенную ДНК, кодирующую LH-рецепторный ген, предпочтительно рецептор человека, экспрессируют в подходящих клетках-хозяевах. Такая клетка может представлять собой клетку яичника китайского хомяка, но также подходят и другие клетки. Предпочтительно клетки имеют происхождение от млекопитающих (Jia et al., Mol.Endocrin., 5:757-776, 1991).
Способы конструирования клеточных линий, экспрессирующих рекомбинантный LH, хорошо известны в данной области (Sambrook et al., Molecular Cloning: a Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, последнее издание). Экспрессия рецептора достигается экспрессией ДНК, кодирующей желаемый белок. Способы сайт-направленного мутагенеза, лигирования дополнительных последовательностей, ПЦР и конструкции подходящих экспрессирующих систем все, к настоящему времени, хорошо известны в данной области. Части или целиком ДНК, кодирующие желаемый белок, могут быть сконструированы синтетически с использованием стандартных твердофазных способов, предпочтительно для включения сайтов рестрикции для облегчения лигирования. Подходящие контрольные элементы для транскрипции и трансляции включенной кодирующей последовательности могут обеспечиваться ДНК-кодирующими последовательностями. Как хорошо известно, в настоящее время доступны экспрессионные системы, которые совместимы с большим множеством хозяев, в том числе прокариотическими хозяевами, такими как бактерии, и эукариотическими хозяевами, такими как дрожжи, клетки растений, клетки насекомых, клетки млекопитающих, птичьи клетки и тому подобное.
Экспрессирующие рецептор клетки затем приводят в контакт с исследуемым соединением, чтобы наблюдать связывание или стимуляцию, либо ингибирование функционального ответа.
Альтернативно, для измерения связывания соединения можно использовать выделенные клеточные мембраны, содержащие экспрессированный рецептор.
Для измерения связывания можно использовать радиоактивно или флуоресцентно меченные соединения. В качестве ссылочного соединения можно