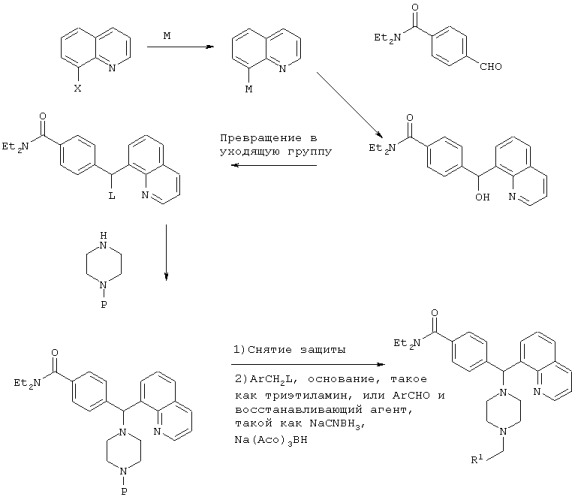
4-(пиперазинил(8-хинолинил)метил)бензамиды, фармацевтическая композиция и способ лечения боли
Иллюстрации
Показать всеНастоящее изобретение относится к новым 4-(пиперазинил(8-хинолинил)метил)бензамидам общей формулы I
где R1 выбран из фенила, пиридинила, тиофенила, фуранила и имидазолила; причем каждое фенильное кольцо и гетероароматическое кольцо возможно и независимо дополнительно замещено 1, 2 или 3 заместителями, выбранными из прямого и разветвленного С1-С6алкила, NO2, CF3, С1-С6алкокси, хлоро, фторо, бромо и йодо, а также их фармацевтически приемлемые соли. Соединения могут быть использованы в терапии, в частности при устранении боли. Описаны также фармацевтическая композиция на основе соединений I и способ лечения боли. 3 н. и 9 з.п. ф-лы, 3 табл.
Реферат
Изобретение относится к новым соединениям, к способу их получения, их применению и фармацевтическим композициям, содержащим эти новые соединения. Эти новые соединения являются полезными в терапии и, в частности, для лечения боли.
Предшествующий уровень техники
δ-Рецептор идентифицирован как рецептор, играющий роль во многих функциях организма, таких как сердечно-сосудистая и лимфатическая и болевая системы. Следовательно, лиганды для δ-рецептора могут находить потенциальное применение в качестве анальгетиков и/или в качестве гипотензивных агентов. Показано также, что лиганды для δ-рецептора обладают иммуномодулирующей активностью.
Идентификация по меньшей мере трех различных групп опиоидных рецепторов (μ, δ и κ) в настоящее время четко установлена, и очевидно, что все три находятся как в центральной, так и в периферической нервных системах многих видов, включая человека. Аналгезию наблюдали в различных животных моделях при активации одного или более чем одного из этих рецепторов.
За редким исключением, имеющиеся в настоящее время селективные δ-опиоидные лиганды являются пептидными по природе и не подходят для введения посредством системных путей. Одним из примеров не пептидного δ-агониста является SNC80 (Bilsky E.J. et al., Journal of Pharmacology and Experimental Therapeutics, 273 (1), pp.359-366 (1995)). Однако все еще существует необходимость в селективных δ-агонистах, обладающих не только повышенной селективностью, но также улучшенным профилем побочных эффектов.
Таким образом, задачей, лежащей в основе настоящего изобретения, являлся поиск новых анальгетиков, обладающих улучшенными болеутоляющими эффектами, но также с улучшенным профилем побочных эффектов по сравнению с современными μ-агонистами, а также обладающих улучшенной системной эффективностью.
Анальгетики, которые идентифицированы и имеются в уровне техники, имеют много недостатков, заключающихся в том, что они обладают неудовлетворительной фармакокинетикой и не оказывают болеутоляющего действия при введении посредством системных путей. Также документально подтверждено, что предпочтительные соединения δ-агонисты, описанные в данном уровне техники, проявляют значительные судорожные эффекты при системном введении.
Авторами изобретения в настоящее время обнаружено, что некоторые соединения, конкретно не раскрытые, но включенные в объем WO 98/28270, демонстрируют неожиданно улучшенные δ-агонистические свойства и эффективность in vivo относительно соединений, раскрытых в WO 98/28270, при системном введении. Соединения по настоящему изобретению демонстрируют значительные и неожиданно повышенные уровни агонизма по отношению к дельта-рецептору и метаболической стабильности.
Краткое изложение сущности изобретения
Новые соединения по настоящему изобретению определены формулой 1
где
R1 выбран из
(1) фенила;
(2) пиридинила
(3) тиофенила
(4) фуранила
(5) имидазолила
(6) триазолила
где каждое фенильное кольцо R1 и гетероароматическое кольцо R1 может быть возможно и независимо дополнительно замещено 1, 2 или 3 заместителями, выбранными из прямого и разветвленного C1-С6алкила, NO2, CF3, C1-С6алкокси, хлоро, фторо, бромо и йодо. Замещения на фенильном кольце и на гетероароматическом кольце могут иметь место в любом положении на указанных кольцевых системах.
В объем настоящего изобретения также входят фармацевтически приемлемые соли соединений формулы I, а также их изомеры.
В предпочтительном воплощении данного изобретения соединения формулы 1 находятся в виде (+)-энантиомера или в виде (-)-энантиомера.
Под «изомерами» авторы изобретения подразумевают соединения формулы I, которые различаются по положению их функциональной группы и/или ориентации. Под «ориентацией» авторы изобретения подразумевают стереоизомеры, диастереоизомеры, региоизомеры и энантиомеры.
Новые соединения по настоящему изобретению являются полезными в терапии, особенно для лечения различных болевых состояний, таких как хроническая боль, невропатическая боль, острая боль, раковая боль, боль, вызванная ревматоидным артритом, мигрень, висцеральная боль и так далее. Этот перечень, однако, не следует интерпретировать как исчерпывающий.
Соединения по настоящему изобретению являются полезными в качестве иммуномодуляторов, особенно при аутоиммунных заболеваниях, таких как артрит, для кожных трансплантатов, трансплантатов органов и подобных хирургических нужд, при коллагенозах, различных аллергиях, для применения в качестве противоопухолевых агентов и противовирусных агентов.
Соединения по настоящему изобретению являются полезными при болезненных состояниях, при которых имеется дегенерация или дисфункция опиоидных рецепторов, либо дегенерация или дисфункция опиоидных рецепторов вовлечена в процесс. В диагностические методики и в применения, связанные с визуализацией, такие как позитронная эмиссионная томография (ПЭТ), может быть также вовлечено использование меченых изотопами вариантов соединений по настоящему изобретению.
Соединения по настоящему изобретению являются полезными для лечения диареи, депрессии, тревоги, недержания мочи, различных психических заболеваний, кашля, отека легких, различных желудочно-кишечных расстройств, повреждения спинного мозга и привыкания к чрезмерному употреблению лекарств, включая лечение злоупотребления алкоголем, никотином, опиоидами и другими лекарствами, а также для лечения расстройств симпатической нервной системы, например гипертензии.
Соединения по настоящему изобретению являются полезными в качестве анальгетического агента для применения во время общей анестезии и контролируемой коррекции анестезии. Комбинации агентов с различными свойствами часто применяют для достижения баланса эффектов, необходимого для поддержания состояния анестезии (например, амнезии, аналгезии, мышечной релаксации и седативного эффекта). В данную комбинацию включены ингаляционные анестетики, снотворные средства, анксиолитики, нейромышечные блокаторы и опиоиды.
В объем настоящего изобретения также входит применение любого из соединений формулы I, указанной выше, для производства лекарства для лечения любого из состояний, обсуждаемых выше.
Следующий аспект настоящего изобретения представляет собой способ лечения субъекта, страдающего от любого из состояний, обсуждаемых выше, при котором пациенту, нуждающемуся в таком лечении, вводят эффективное количество соединения формулы I, указанной выше. Также в объем настоящего изобретения включено любое новое промежуточное соединение, как описано в приведенной ниже Схеме I, полезное в синтезе соединений формулы I, указанной выше.
Способы получения
Соединения по настоящему изобретению можно получить, следуя любой из методик, описанных в Схемах I, II, III и IV. Эти известные методики описаны в J. March, Advanced Organic Chemistry, 4th Edition, John Wiley and sons (1992); Katritsky, A.R., Lan, X. Chem. Soc. Rev., pp.363-373 (1994), которые включены в данное описание изобретения путем ссылки.
СХЕМА I
Р=защитная группа, такая как Bn, Boc, CBz
М=Li, Mg, Zn
Х=Br, I
L=Cl, Br, OMs, OTs, I
R1=как определено в формуле (I), указанной выше.
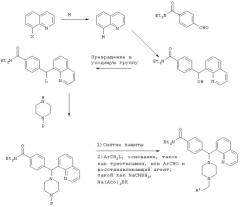
СХЕМА II
Р=защитная группа, такая как Bn, Boc, CBz
М=Li, Mg, Zn
Х=Br, I
L=Cl, Br, OMs, OTs, I
R1=как определено в формуле (I), указанной выше.
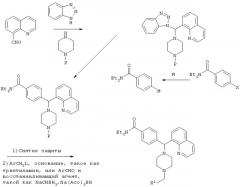
СХЕМА III
Р=защитная группа, такая как Bn, Boc, CBz
М=Li, Mg, Zn
Х=Br, I
L=Cl, Br, OMs, OTs, I
R1=как определено в формуле (I), указанной выше.
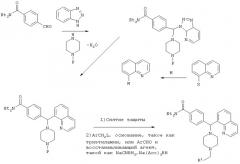
СХЕМА IV
Р=защитная группа, такая как Bn, Boc, CBz
М=Li, Mg, Zn
Х=Br, I
L=Cl, Br, OMs, OTs, I
R1=как определено в формуле (I), указанной выше.
Примеры
Далее изобретение будет описано более подробно с помощью следующих примеров, которые не следует истолковывать как ограничивающие данное изобретение.
Пример 1
Получение 4-[(4-бензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамида дигидрохлорида (соединение 2)
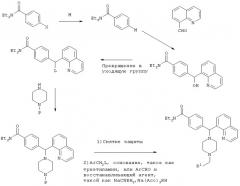
Соединение 2, указанное в заголовке, получили, следуя методике синтеза Схемы 1, приведенной ниже.
Схема 1
(1) Получение N,N-диэтил-4-формилбензамида (соединение I)
4-Формилбензойную кислоту (11,2 г, 74,6 ммоль) и триэтиламин (10,4 мл, 75 ммоль) растворяли в тетрагидрофуране (ТГФ) (100 мл) и охлаждали до -10°С. Добавляли изо-бутилхлорформиат (10,3 мл, 78 ммоль), и перемешивание продолжали в течение 10 минут при -10°С, после чего добавляли диэтиламин (9,7 мл, 94 ммоль), и раствор оставили нагреваться до достижения 25°С. После концентрирования, водной обработки и хроматографии на силикагеле (0-100% ЕЮАс в гептане) получили суммарно 7,4 г (50%) соединения I.
(2) Получение N,N-диэтил-4-[гидрокси(8-хинолинил)метил]бензамида (соединение II)
8-Бромхинолин (3,0 г, 14,4 ммоль) растворяли в безводном ТГФ (150 мл) и охлаждали до -78°С в атмосфере азота. Добавляли по каплям втор-бутиллитий (emop-BuLi) (11,1 мл, 1,3 М в пентане, 14,4 ммоль) в течение 5 мин (Preparation and reactions with 8-lithioquinoline: Suggs, J. Org. Chem. 1980, 45, 1514). Еще через 5 мин добавляли N,N-диэтил-4-формилбензамид (3,5 г, 17,0 ммоль), растворенный в ТГФ (5 мл). Этот раствор перемешивали в течение 1 ч, затем добавляли NH4Cl (водный). После концентрирования, водной обработки и хроматографии на силикагеле (0-100% EtOAc в гептане) получили суммарно 3,5 г (70%) соединения II.
МС: 334, 262, 234, 215, 204, 178, 156, 129.
Альтернативный путь получения соединения II из N,N-диэтил-4-йодбензамида (соединение IV)
Соединение IV (0,67 г, 2,2 ммоль) растворяли в сухом ТГФ (25 мл) и охлаждали до -78°С в атмосфере азота. Добавляли по каплям н-BuLi (1,3 мл, 1,6 М в гексане, 2,2 ммоль) в течение 5 мин. Еще через 10 мин добавляли 8-формилхинолин (0,17 г, 1,1 ммоль) (8-формилхинолин получили из 8-метилхинолина путем окисления диоксидом селена при 150-155°С в течение 12 ч (Kingsbury, J. Med. Chem. 1993, 3308)), растворенный в ТГФ (1 мл). Этот раствор перемешивали в течение 1 ч, затем добавляли NH4Cl (водный). После концентрирования, водной обработки и хроматографии на силикагеле (0-100% EtOAc в гептане) получили суммарно 0,29 г (78%) соединения II.
(3) Получение 4-[хлор(8-хинолинил)метил]-N,N-диэтилбензамида (соединение III).
Соединение II (2,0 г, 6,6 ммоль) растворяли в безводном СН2Cl2 (25 мл) и добавляли SOCl2 (0,53 мл, 7,3 ммоль). Этот раствор перемешивали при 25°С в течение 30 мин, и растворитель выпаривали в вакууме. Соединение III получили в виде масла (-100%) и использовали в следующей реакции без дальнейшей очистки.
МС: 348, 333, 233, 215, 204, 156.
(4) Получение N,N-диэтил-4-[1-пиперазинил(8-хинолинил)метил]бензамида (соединение 1).
Неочищенный продукт соединение III (˜6,6 ммоль) и пиперазин (2,3 г, 26 ммоль) растворяли в безводном MeCN (50 мл) и нагревали с обратным холодильником в течение 12 ч. Растворитель удаляли в вакууме, остаток растворяли в CH2Cl2 и промывали водой, и органическую фазу высушивали (К2СО3) и выпаривали в вакууме. После хроматографии на силикагеле (0-20% МеОН в CH2Cl2, 1% NH4OH) получили суммарно 1,8 г (68%, 2 стадии) соединения 1. Дальнейшей очистки можно достичь путем обращенно-фазовой хроматографии (LiChroprep RP-18, 10-50% MeCN в воде, 0,1% ТФУ) с получением 1,2 г бесцветного продукта. Соль дигидрохлорид получили путем обработки 2 экв. HCl в эфире.
Т.пл.:180-90°С.
ИК (KBr, νmax) 3297, 2982, 2716, 2474, 1611, 1434, 1380, 1288, 1098 см-1.
МС (амин): 402, 318, 246, 217, 109.
1H ЯМР (амин, CDCl3): δ 1.2, 1.1 (2s, 6H), 2.94, 2.51 (2m, 8H), 3.5-3.1 (m, 5H), 6.05 (s, 1H), 8.94-7.20 (m, 10H).
Анализ (C25H30N4Ox3,2 CF3СО2Н) С, N; Н: вычислено 4,36; обнаружено 3,90.
(5) Получение 4-[(4-бензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамида дигидрохлорида (соединение 2, указанное в заголовке).
Соединение 1 (1,3 г, 3,2 ммоль) и триэтиламин (0,90 мл, 6,4 ммоль) растворяли в MeCN (10 мл). Бензилбромид (0,77 мл, 6,4 ммоль) добавляли при перемешивании при 25°С. Через 4 ч этот раствор концентрировали и очищали путем хроматографии на силикагеле (0-5% МеОН в CH2Cl2) или путем обращенно-фазовой хроматографии (LiChroprep RP-18, 20-80% MeCN в воде, 0,1% ТФУ). Суммарно получили 2,2 г (72%) соединения 2, указанного в заголовке.
Путем обработки 2 экв. HCl (водной) и лиофилизации получили соль дигидрохлорид (3,6 г).
ИК (2Х HCI, KBr): 2388, 1606, 1434, 1356, 1287 см-1.
1H ЯМР (свободный амин, CDCl3): δ=1.05 (m, 6H), 2.5 (m, 8H), 3.1-3.6 (m, 6H), 6.04 (s, 1H), 7.18-8.98 (m, 15H).
Анализ (С32Н38Cl2N4O) С, Н, N. Альтернативная методика получения соединения 2, указанного в заголовке, из соединения III
Неочищенный продукт соединение III (˜13,2 ммоль), триэтиламин (2,0 мл, 14,5 ммоль) и N-бензил-пиперазин (2,6 г, 14,5 ммоль) растворяли в безводном MeCN (50 мл) и нагревали с обратным холодильником в течение 12 ч. Добавляли дополнительное количество N-бензил-пиперазина (0,5 г, 2,8 ммоль) и нагревание продолжали в течение 12 ч. Растворитель удаляли в вакууме, остаток растворяли в CH2Cl2 и промывали водой; и органическую фазу высушивали (К2СО3) и выпаривали в вакууме. После хроматографии на силикагеле (0-10% МеОН в СН2Cl2 суммарно получили 3,5 г (53%) соединения 2, указанного в заголовке.
Примеры 2 и 3
Разделение энантиомеров соединения 2 (соединения 3 и 4)
Препаративное разделение данного соединения проводили на колонке Chiralcel OD (50 мм × 50 см), используя смесь гексан/EtOH/диэтиламин в соотношении 85:15:0,1 в качестве подвижной фазы. Обнаружили, что на колонке Chiralcel OD (+)-изомер элюируется первым.
Пример 2 (-)4-[(4-бензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамид (соединение 3)
[α]D 25: -130° (с 0,78, МеОН)
1H ЯМР: (CD3OD): δ=1.05 (m, 6H), 3.0-3.6 (m, 14H), 5.90 (s, 1H), 7.22-8.20 (m, 13H), 8.78 (m, 1H), 9.50 (m, 1H).
АНАЛИЗ: Вычисленная масса 3,1 Н2O, С: 61.85, Н: 7.17, N: 9.02. Обнаружено С: 61.84, Н: 6.60, N: 8.89.
Пример 3
(+)4-[(4-бензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамид (соединение 4)
[α]D 25: +130° (c 0,69, MeOH)
1H ЯМР: (CD3OD): δ=1.05 (m, 6Н), 3.0-3.6 (m, 14H), 5.90 (s, 1H), 7.22-8.20 (m, 13H), 8.78 (m, 1H), 9.50 (m, 1H).
АНАЛИЗ: Вычисленная масса 3,2 Н2O, С: 61.67, Н: 7.18, N: 8.99. Обнаружено С: 61.70, Н: 6.46, N: 8.84.
Пример 4
Получение N,N-диэтил-4-[[4-(4-метилбензил)-1-пиперазинил](8-хинолинил)метил]бензамида (соединение 5)
Соединение 5, указанное в заголовке, получили, следуя методике синтеза Схемы 2, приведенной ниже.
Схема 2
К раствору соединения 1 (0,80 г, 1,99 ммоль) в СН2Cl2 (20 мл) добавляли Et3N (0,83 мл, 5,97 ммоль), затем пара-метилбензилбромид (773 мг, 4,18 ммоль). Эту реакционную смесь перемешивали в течение ночи, а затем концентрировали при пониженном давлении. Очистка путем обращенно-фазовой хроматографии, используя 10%-30% СН3CN/N2О.
(М+1) вычисленная: 507,70, (М+1) наблюдаемая: 507,20.
ИК (NaCl, свободный амин) 2969, 2807, 2360, 1628, 1455, 1425, 1286, 1134, 1095 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.1 (2m, 6H, амид-Ме), 2.31 (s, 3H, Ar-Me), 2.5 (m, 8H, пиперазин-Н), 3.2, 3.5 (2m, амид-СН2), 3.49 (s, 2H, ArCH2N), 6.03 (s, 1H, Ar2CH), 7.06-7.68 (m, 11H, Ar-Н), 8.01-8.12 (m, 2H, Ar-H), 8.93 (m, 1H, Ar-H).
Анализ (C32H38Cl2N4O) С, Н, N.
Примеры 5 и 6
Разделение энантиомеров соединения 5 с получением соединений 6 и 7
Препаративное разделение данного соединения проводили на полупрепаративной колонке Chiralcel AD (21 мм × 25 см), используя смесь гексан/EtOH/диэтиламин в соотношении 80:20:0,1 в качестве подвижной фазы. Обнаружили, что на колонке Chiralcel AD (-)-изомер элюируется первым.
Пример 5
(-)4-[(4-метилбензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамид (соединение 6)
[α]D 25: -131o (c 1,0, MeOH)
Пример 6
(+)4-[(4-метилбензил-1-пиперазинил)(8-хинолинил)метил]-N,N-диэтилбензамид (соединение 7)
[α]D 25: +124o (c 1,4, МеОН)
Пример 7
Получение 4-[{4-[4-(трет-бутил)бензил]-1-пиперазинил}(8-хинолинил)метил]-N,N-диэтилбензамида дигидрохлорида (соединение 8)
С помощью методики, аналогичной методике получения соединения 2, получили соединение 8, указанное в заголовке. Алкилирование осуществляли 4-трет-бутилбензилбромидом.
(МС) (ES): 549,53 (МН+).
ИК (NaCl, свободный амин) 2963, 2807, 2360, 1631, 1456, 1425, 1285, 1135, 1094, 1001 (см-1).
1H ЯМР; (CDCl3, свободный амин): δ=1.0, 1.2 (2m, 6H), 1.29 (s, 9H), 2.50 (m, 8H), 3.2, 3.5 (2m), 3.50 (s, 2H), 6.04 (s, 1H), 7.16-7.68 (m, 11H), 7.98-8.10 (m, 2H), 8.92 (m, 1H).
Анализ (С36Н46Cl2N4O) С, Н, N.
Пример 8
Получение N,N-диэтил-4-[[4-(4-нитробензил)1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 9)
С помощью методики, аналогичной методике получения соединения 2, описанной выше, получили соединение 9, указанное в заголовке. Алкилирование осуществляли 4-нитробензилбромидом.
(МС) (ES): 538,04 (МН+).
ИК (NaCl, свободный амин) 2969, 2809, 2360, 1626, 1518, 1456, 1426, 1343, 1286, 1134, 1095, 1001 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.2 (2m, 6H), 2.50 (m, 8H), 3.2, 3.5 (2m), 3.60 (s, 2H), 6.05 (s, 1H), 7.18-8.16 (m, 13H), 8.94 (m, 1H).
Анализ (С32Н37Cl2N5O3) С, Н, N.
Пример 9
Получение 4-[{4-[2,4-бис(трифторметил)бензил]1-1-пиперазинил}(8-хинолинил)метил]-N,N-диэтилбензамида дигидрохлорида (соединение 10)
Соединение 10
Следуя методике, аналогичной методике получения соединения 2, описанной выше, получили соединение 10, указанное в заголовке. Алкилирование осуществляли 2,4-бис(трифторметил)бензилбромидом.
(МС) (ES): 629,08 (МН+).
ИК (NaCl, свободный амин) 2970, 2811, 2360, 1628, 1456, 1426, 1346, 1275, 1170, 1128 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.2 (2m, 6H), 2.48 (m, 8H), 3.2, 3.5 (2m), 3.71 (s, 2H), 6.06 (s, 1H), 7.20-8.14 (m, 12H), 8.95 (m, 1H).
Анализ (C34H36Cl2F6N4O) С, Н, N.
Пример 10
Получение N,N-диэтил-4-[[4-(4-метоксибензил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 11)
С помощью методики, аналогичной методике получения соединения 2, описанной выше, получили соединение 11, указанное в заголовке. Алкилирование осуществляли 4-метоксибензилхлоридом.
(МС) (ES): 523,45 (МН+).
ИК (NaCl, свободный амин) 2966, 2806, 2360, 1627, 1510, 1456, 1426, 1286,1246, 1134, 1095 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.2 (2m, 6H), 2.48 (m, 8H), 3.2, 3.5 (2m), 3.47 (s, 2H), 3.78 (s, 3Н), 6.03 (s, 1H), 6.80-7.68 (m, 11H), 8.01-8.12 (m, 2H), 8.93 (m, 1H).
Анализ (С33Н40Cl2N4O2) С, Н, N.
Пример 11
Получение 4-[[4-(2,4-дихлорбензил)-1-пиперазинил](8-хинолинил)метил]-N,N-диэтилбензамида дигидрохлорида (соединение 12)
Следуя методике, аналогичной методике получения соединения 2, описанной выше, получили соединение 12, указанное в заголовке. Алкилирование осуществляли 2,4-дихлорбензилбромидом.
(МС) (ES): 562,45 (МН+).
ИК (NaCl, свободный амин) 2968, 2810, 2360, 2341, 1627, 1470, 1426, 1285, 1134, 1095 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.1 (2m, 6H), 2.5 (m, 8H), 3.2, 3.5 (2m), 3.58 (s, 2H), 6.05 (s, 1H), 7.14-7.70 (m, 10H), 8.06 (m, 2H), 8.94 (m, 1H).
Анализ (С32Н36Cl4N4O) С, Н, N.
Пример 12
Получение N,N-диэтил-4-[[4-(2-пиридинилметил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 13)
Соединение 1 (80 мг, 0,20 ммоль) растворяли в МеОН (2 мл) с 2-пиридилкарбоксальдегидом (39 мкл, 0,40 ммоль) и НОАс (1 мкл, 0,02 ммоль). Добавляли цианоборгидрид натрия (26 мг, 0,40 ммоль), и перемешивание продолжали в течение 48 ч. Растворитель выпаривали и остаток очищали путем хроматографии на силикагеле (0-10% МеОН в СН2Cl2). Получили 38 мг (39%) продукта.
(MC)(ES):494,19(MH+).
ИК (NaCl, свободный амин) 2968, 2809, 2360, 1626, 1455, 1428, 1286. 1134, 1094, 1001 (см-1).
1H ЯМР: (CDCl3, свободный амин): δ=1.0, 1.2 (2m, 6H), 2.50 (m, 8H), 3.2, 3.5 (2m), 3.69 (s, 2H), 6.05 (s, 1H), 7.12-7.70 (m, 10Н), 8.08 (m, 2H), 8.54 (m, 1H),8.94(m, 1H).
Анализ (С31Н37Cl2N5O) С, Н, N.
Пример 13
Получение N,N-диэтил-4-[[4-(3-тиенилметил)-1-пиперазинил](8-хинолинил)метил]бензамида (соединение 14)
Соединение 14, указанное в заголовке, получили, следуя методике синтеза Схемы 3, приведенной ниже.
Схема 3
К раствору соединения 1 (500 мг, 0,99 ммоль) в метаноле (10 мл) добавляли тиофен-3-карбоксальдегид (104 мкл, 1,19 ммоль), а затем уксусную кислоту (0,1 мл, 1%) и цианоборгидрид натрия (186,6 мг, 2,97 ммоль). Эту реакционную смесь перемешивали в течение ночи, затем добавляли 2 н гидроксид натрия и эту смесь экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 10%-30% СН3CN/Н2О (ТФУ в качестве буфера), получили 258 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ: >99% (215 нм); >95% (254 нм)
(М+1) вычисленная: 499,25, (М+1) наблюдаемая: 499,46.
Анализ: вычислено для (С30Н34N4OS × 2.80 С2HO2F3 × 1.80 Н2O): С: 50,28%; Н: 4,79%; N: 6,59%; О: 15,80%; S: 3,77%; F: 18,77%. Обнаружено: С: 50,28%; Н: 4,83%; N: 6,53%.
1H ЯМР: 8.95 (dd, 1H, J=4.4, 2.0 Гц), 8.38 (dd, 1H, J=8.0, 2.0 Гц), 8.00 (dd, 1H, J=7.2, 1.6 Гц), 7.84 (dd, 1H, J=8.0, 1.6 Гц), 7.52-7.62 (m, 5H), 7.45 (dd, 1H, J=4.8, 2.8 Гц), 7.20 (dd, 2H, J=8.8, 2.2 Гц), 7.11 (dd, 1H, J=4.8, 1.6 Гц), 5.96 (s, 1H), 4.27 (s, 2H), 3.34-3.44 (m, 2H), 3.22-3.28 (m, 4H), 3.04-3.14 (m, 2H), 2.66-2.88 (m, 4H), 1.04-1.14 (m, 3Н), 0.88-0.98 (m, 3H).
Пример 14
Получение N,N-диэтил-4-[[4-(2-фуранилметил)-1-пиперазинил](8-хинолинил)метил]бензамида (соединение 15)
Соединение 15, указанное в заголовке, получили, следуя методике синтеза Схемы 4, приведенной ниже.
Схема 4
К раствору фурфурилового спирта (0,19 мл, 2,24 ммоль) и триэтиламина (0,52 мл, 3,73 ммоль) в метиленхлориде (4 мл) при 0°С добавляли метансульфонилхлорид (0,17 мл, 2,24 ммоль). Эту смесь перемешивали в течение 1 ч при 0°С, затем добавляли соединение 1 (300 мг, 0,75 ммоль). Эту реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи, затем нагревали до 45°С и перемешивали в течение 1,5 часов. Эту реакционную смесь оставляли охлаждаться до комнатной температуры и добавляли 2 н NaOH, пока рН не стал щелочным. Эту смесь экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 10%-25% СН3CN/H2О (ТФУ в качестве буфера), получили 197 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ: >99% (215 нм, 254 нм и 280 нм)
(М+1) вычисленная: 483,63, (М+1) наблюдаемая: 483,30.
1H ЯМР: 8.89 (dd, 1Н, J=4.4, 1.6 Гц), 8.29 (dd, 1H, J=8.0, 1.6 Гц), 7.97 (dd, 1Н, J=7.2, 1.6 Гц), 7.79 (d, 1H, J=7.2 Гц), 7.61 (d, 2H, J=8.0 Гц), 7.52-7.58 (m, 2H), 7.48 (dd, 1H, J=8.0, 4.4 Гц), 7.19 (d, 2H, J=8.0 Гц), 6.56 (d, 1H, J=3.2 Гц), 6.40 (dd, 1H, J=3.2, 2.4 Гц), 6.02 (s, 1H), 4.26 (s, 2H), 3.34-3.44 (m, 2H), 3.16-3.26 (m, 4H), 3.04-3.14 (m, 2H), 2.68-2.86 (m, 4H), 1.06-1.14 (m, 3Н), 0.90-0.98 (m, 3H).
Пример 15
Получение N,N-диэтил-4-[[4-(3-фуранилметил)-1-пиперазинил](8-хинолинил)метил]бензамида (соединение 16)
Соединение 16, указанное в заголовке, получили, следуя методике синтеза Схемы 5, приведенной ниже.
Схема 5
К раствору 3-фуранметанола (220 мг, 2,24 ммоль) и триэтиламина (0,52 мл, 3,73 ммоль) в метиленхлориде (4 мл) при 0°С добавляли метансульфонилхлорид (0,17 мл, 2,24 ммоль). Эту смесь перемешивали в течение 1 ч при 0°С, затем добавляли соединение 1 (300 мг, 0,75 ммоль). Эту реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи, затем нагревали до 45°С и перемешивали в течение 3,5 часов. Эту реакционную смесь оставляли охлаждаться до комнатной температуры и добавляли 2 н NaOH, пока рН не стал щелочным. Эту смесь экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над HO2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 10%-25% СН3CN/Н2О (ТФУ в качестве буфера), получили 293 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ: >98% (215 нм и 280 нм); >99% (254 нм).
(М+1) вычисленная: 483,63, (М+1) наблюдаемая: 483,34.
Анализ: вычислено для (С30Н34N4О2 × 3.10 С2HO2F3 × 1.70 Н20): С: 50,17%; Н: 4,71%; N: 6,46%; О: 18,27%; F: 20,39%. Обнаружено: С: 50,14%; Н: 4,76%; N; 6,38%.
1H ЯМР: 8.93 (dd, 1H, J=4.4, 2.0 Гц), 8.36 (dd, 1H, J=8.6, 2.0 Гц), 8.00 (dd, 1H, J=7.4, 1.2 Гц), 7.82 (dd, 1H, J=7.6, 1.2 Гц), 7.48-7.66 (m, 6H), 7.19 (d, 2H, J=8.0 Гц), 6.46 (s, 1H), 5.97 (s, 1H), 4.13 (s, 2H), 3.32-3.44 (m, 2H), 3.20-3.28 (m, 4H), 3.04-3.14 (m, 2H), 2.66-2.86 (m, 4H), 1.04-1.14 (m, 3H), 0.88-0.98 (m, 3H).
Пример 16
Получение N,N-диэтил-4-[[4-(2-тиофенилметил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 17)
Соединение 17, указанное в заголовке, получили, следуя методике синтеза Схемы 6, приведенной ниже.
Схема 6
К раствору соединения 1 (0,99 ммоль) в метиленхлориде (10 мл) добавляли 2-тиофенкарбоксальдегид (190 мкл, 1,98 ммоль), а затем уксусную кислоту (0,1 мл, 1%). Эту смесь перемешивали в течение 30 минут, затем добавляли триацетоксиборгидрид натрия (0,63 г, 2,97 ммоль), и эту реакционную смесь перемешивали в течение ночи. Эту реакционную смесь нейтрализовали 2 н гидроксидом натрия и экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 10%-30% CH3CN/H2O (ТФУ в качестве буфера), получили 115 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ; >99% (215 нм); >96% (254 нм).
(М+1) вычисленная: 499,25, (М+1) наблюдаемая: 499,33.
Анализ: вычислено для (C30H34N4OS × 2.50 С2HO2F3 × 0.10 H2O): С: 53,51%; Н: 4,71%; N: 7,13%; О: 12,42%; S: 4,08%; F: 18,14%. Обнаружено: С: 53,49%; Н: 4,63%; N: 7,49%.
1H ЯМР: 8.91 (dd, 1H, J=4.0, 1.6 Гц), 8.30 (dd, 1H, J=8.8, 1.6 Гц), 7.96 (dd, 1H, J=7.4, 1.4 Гц), 7.81 (d, 1H, J=7.2 Гц), 7.62 (d, 2H, J=8.0 Гц), 7.46-7.58 (m, 3H), 7.20 (d, 2H, J=8.0 Гц), 7.14-7.22 (m, 1H), 7.00 (dd, 1H, J=5.2, 3.6 Гц), 6.03 (s, 1H), 4.38 (s, 2H), 3.34-3.44 (m, 2H), 3.14-3.22 (m, 4H), 3.06-3.12 (m, 2H), 2.74-2.88 (m, 4H), 1.04-1.14 (m, 3H), 0.88-0.98 (m, 3H).
Пример 17
Получение N,N-диэтил-4-[[4-(2-имидазолилметил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 18)
Соединение 18, указанное в заголовке, получили, следуя методике синтеза Схемы 7, приведенной ниже.
Схема 7
К раствору соединения 1 (0,99 ммоль) в метаноле (10 мл) добавляли 2-имидазолкарбоксальдегид (114 мг, 1,19 ммоль), а затем уксусную кислоту (0,5 мл, 5%). Эту смесь перемешивали в течение 3 часов, затем добавляли цианоборгидрид натрия (186,6 мг, 2,97 ммоль), и эту реакционную смесь перемешивали в течение ночи. Эту реакционную смесь нейтрализовали 2 н гидроксидом натрия и экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 10%-30% CH3CN/H2O (ТФУ в качестве буфера), получили соль ТФУ. Соль HCl получили, используя HCl/эфир. Выход: 60,3 мг желаемого продукта (соль HCl).
Степень очистки по ВЭЖХ: >95% (215 нм); >93% (254 нм).
(М+1) вычисленная: 483,29, (М+1) наблюдаемая: 483,19.
1H ЯМР: 9.12-9.22 (m, 1Н), 8.54-8.62 (m, 1H), 8.08-8.16 (m, 1H), 7.98-8.04 (m, 1H), 7.60-7.86 (m, 4H), 7.38-7.46 (m, 2H), 7.22-7.32 (m, 2H), 6.32 (s, 1H), 4.11 (s, 2H), 2.94-3.40 (m, 12H), 0.88-1.12 (m, 6H).
Пример 18
Получение N,N-диэтил-4-[[4-(4-имидазолилметил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 19)
Соединение 19, указанное в заголовке, получили, следуя методике синтеза Схемы 8, приведенной ниже.
Схема 8
К раствору 434 (400 мг, 0,99 ммоль) и 4-имидазолкарбоксальдегида (95,5 мг, 0,99 ммоль) в метиленхлориде (10 мл) при комнатной температуре добавляли уксусную кислоту (0,1 мл). Эту смесь перемешивали в течение 5 часов, затем добавляли триацетоксиборгидрид натрия (632 мг, 2,98 ммоль). Эту реакционную смесь перемешивали в течение ночи и нейтрализовали 2 н гидроксидом натрия. Эту смесь экстрагировали метиленхлоридом (3х). Объединенные метиленхлоридные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 15% СН3CN/H2О (ТФУ в качестве буфера), получили 103 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ: >99% (215 нм, 254 нм и 280 нм).
(М+1) вычисленная: 483,28, (М+1) наблюдаемая: 482,96.
Анализ: вычислено для (C29H34N6O × 3.80 С2HO2F3 × 0.80 H2O): С: 47,25%; Н: 4,27%; N: 9,03%; О: 16,17%; F: 23,28%. Обнаружено: С: 47,31%; Н: 4,40%; N: 8,87%.
1H ЯМР: 8.99 (dd, 1H, J=4.4, 1.2 Гц), 8.76 (d, 1H, J=1.2 Гц), 8.39 (dd, 1H, J=8.8, 1.2 Гц), 7.93 (dd, 1H, J=7.2, 1.6 Гц), 7.86 (dd, 1H, J=8.0, 1.6 Гц), 7.71 (d, 2H, J=8.8 Гц), 7.60 (dd, 1H, J=8.8, 4.4 Гц), 7.56 (dd, 1H, J=8.0, 7.2 Гц), 7.40 (s, 1H), 7.27 (d, 2H, J=8.8 Гц), 6.12 (s, 1H), 3.74 (s, 2H), 3.38 (q, 2H, J=6.4 Гц), 3.10-3.25 (m, 6H), 3.06 (q, 2H, J=7.2 Гц), 2.75-2.90 (m, 2H), 1.08 (t, 3H, J=6.4 Гц), 0.92 (t, 3H, J=7.2 Гц).
Пример 19
Получение N,N-диэтил-4-[[4-(3-триазолилметил)-1-пиперазинил](8-хинолинил)метил]бензамида дигидрохлорида (соединение 20)
Соединение 20, указанное в заголовке, получили, следуя методике синтеза Схемы 9, приведенной ниже.
Схема 9
К раствору 434 (200 мг, 0,50 ммоль) в диметилформамиде (10 мл) при комнатной температуре добавляли карбонат калия (275 мг, 1,99 ммоль), а затем N-формамидо-2-(хлорметил)ацетамидин (170 мг, 1,24 ммоль). Эту реакционную смесь нагревали до 60°С и перемешивали в течение 2 суток, затем температуру повышали до 140°С и перемешивали в течение 3 часов. Эту реакционную смесь оставляли охлаждаться до комнатной температуры и добавляли воду. Эту смесь экстрагировали этилацетатом (3х). Объединенные этилацетатные экстракты высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. С помощью очистки путем обращенно-фазовой хроматографии, используя 20% CH3CN/H2O (ТФУ в качестве буфера), получили 21 мг желаемого продукта (соль ТФУ).
Степень очистки по ВЭЖХ: >99% (215 нм, 254 нм и 280 нм).
(М+1) вычисленная: 484,28, (М+1) наблюдаемая: 483,92.
Анализ: вычислено для (С28Н33N7О × 3.30 С2HO2F3 × 3.30 Н2O): С: 45,20%; Н: 4,70%; N: 10,66%; О: 18,97%; F: 20,46%. Обнаружено: С: 45,12%; Н: 4,60%; N: 10,84.
1H ЯМР: 8.94 (dd, 1H, J=4.4, 1.6 Гц), 8.38 (s, 1H), 8.33 (dd, 1H, J=8.0, 1.2 Гц), 7.93 (d, 1H, J=7.2 Гц), 7.85 (d, 1H, J=7.2 Гц), 7.65 (d, 2H, J=8.8 Гц), 7.51-7.58 (m, 2H), 7.23 (d, 2H, J=8.8 Гц), 6.15 (s, 1H), 4.21 (s, 2H), 3.40-3.50 (m, 2H), 3.10-3.30 (m, 8H), 2.90-3.10 (m, 2H), 0.90-1.30 (m, 6H).
Фармацевтические композиции
Новые соединения по настоящему изобретению можно вводить перорально, внутримышечно, подкожно, местно, интраназально, внутрибрюшинно, интраторакально, внутривенно, эпидурально, внутриоболочечно, интрацеребровентрикулярно и путем инъекции в суставы.
Предпочтительным путем введения является пероральный, внутривенный или внутримышечный.
Дозировка будет зависеть от пути введения, тяжести заболевания, возраста и массы пациента и других факторов, обычно учитываемых лечащим врачом при определении индивидуального режима и уровня дозировки как наиболее подходящих для конкретного пациента.
Для изготовления фармацевтических композиций из соединений по данному изобретению инертные фармацевтически приемлемые носители могут быть либо твердыми, либо жидкими. Препараты в виде твердых форм включают в себя порошки, таблетки, диспергируемые гранулы, капсулы, крахмальные капсулы и суппозитории.
Твердым носителем может быть одно или более чем одно вещество, которые могут также служить в качестве разбавителей, корригентов, солюбилизирующих агентов, смазывающих веществ, суспендирующих агентов, связывающих веществ или разрыхляющих агентов для таблеток; он также может являться инкапсулирующим материалом.
В порошках носитель представляет собой тонко измельченное твердое вещество, которое находится в смеси с тонко измельченным активным компонентом. В таблетках активный компонент смешан с носителем, обладающим необходимыми связующими свойствами, в подходящих пропорциях и спрессован в желаемую форму желаемого размера.
Для приготовления композиций в виде суппозиториев сначала плавят легкоплавкий воск, такой как смесь глицеридов жирных кислот и масла какао, и диспергируют в нем активный ингредиент путем, например, перемешивания. Затем эту расплавленную однородную смесь заливают в формы подходящего размера и оставляют охлаждаться и затвердевать.
Подходящими носителями являются карбонат магния, стеарат магния, тальк, лактоза, сахар, пектин, декстрин, крахмал, трагакант, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, легкоплавкий воск, масло какао и тому подобное.
Фармацевтически приемлемыми солями являются ацетат, бензолсульфонат, бензоат, бикарбонат, битартрат, бромид, ацетат кальция, камсилат, карбонат, хлорид, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эзилат, фумарат, глюкаптат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изэтионат, лактат, лактобионат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, памоат (эмбонат), пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, субацетат, сукцинат, сульфат, таннат, тартрат, теоклат, триэтиодид, соли бензатина, хлорпрокаина, холина, диэтаноламина, этилендиамина, меглумина, прокаина, алюминия, кальция, лития, магния, калия, натрия и цинка. Предпочтительными фармацевтически приемлемыми солями являются гидрохлориды и битартраты. Соли гидрохлориды являются особенно предпочтительными.
В термин «композиция» следует включать препарат активного компонента с инкапсулирующим материалом в качестве носителя, образующим капсулу, в которой активный компонент (с другими носителями или без них) окружен носителем, который, таким образом, находится в связи с ним. Подобным образом включены крахмальные капсулы.
Таблетки, порошки, крахмальные капсулы и капсулы можно применять в качестве твердых лекарственных форм, подходящих для перорального введения.
Композиции в виде жидких форм включают в себя растворы, суспензии и эмульсии. Растворы активных соединений в стерильной воде или в воде-пропиленгликоле можно упомянуть в качестве примера жидких препаратов, подходящих для парентерального введения. Жидкие композиции можно также изготавливать в виде раствора препарата в растворе водного полиэтиленгликоля.
Водные растворы для перорального введения можно изготавливать путем растворения активного компонента в воде и добавления подходящих красителей, корригентов, стабилизаторов и загущающих агентов по желанию. Водные суспензии для перорального применения можно изготавливать путем диспергирования тонко измельченного активного компонента в воде вместе с вязким материалом, таким как природные и синтетические смолы, камеди, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и другие суспендирующие агенты, известные в области фармацевтических препаратов.
Предпочтительно фармацевтические композиции находятся в стандартной лекарственной форме. В такой форме композиция разделена на стандартные дозы, содержащие подходящие количества активного компонента. Стандартная лекарственная форма может представлять собой упакованный препарат, причем упаковка содержит дискретные количества препаратов, например упакованных таблеток, капсул и порошков во флаконах или в ампулах. Стандартная лекарственная форма может также представлять собой капсулу, крахмальную капсулу или таблетку саму по себе, либо может представлять собой подходящее количество любых из этих упакованных форм.
БИОЛОГИЧЕСКАЯ ОЦЕНКА
Модель in vitro
Культура клеток
Клетки человека 293S, экспрессирующие клонированные μ-, δ- и κ-рецепторы человека и устойчивость к неомицину, выращивали в суспензии при 37°С и 5% CO2 в качалочных колбах, содержащих свободную от кальция модифицированную Дульбекко среду Игла (DMEM), 10% FBS, 5% BCS, 0,1% плюроник (Pluronic) F-68 и 600 мкг/мл генетицина.
Препарат мембран
Клетки осаждали и ресуспендировали в буфере для лизиса (50 мМ Трис, рН 7,0, 2,5 мМ ЭДТА с фенилметилсульфонилфторидом (PMSF), добавленным непосредственно перед использованием до 0,1 мМ из 0,1 М исходного раствора в этаноле), инкубировали на льду в течение 15 мин, затем гомогенизировали, используя Polytron, в течение 30 сек. Суспензию центрифугировали при 1000 g (максимум) в течение 10 мин при 4°С. Супернатант хранили на льду, а осадки ресуспендир