Способ получения производного хинолинкарбоксальдегида и промежуточных соединений
Иллюстрации
Показать всеПроизводное хинолинкарбоксальдегида-2-циклопропил-4-(4'-фторфенил) хинолин-3-карбоксальдегид получают путем взаимодействия 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном с получением 2-циклопропил-4-(4'-фторфенил) хинолин-3-карбонитрила и его восстановлением. Технический результат - повышение выхода конечного продукта, упрощение процесса. 4 н. и 4 з.п. ф-лы.
Реферат
Область техники
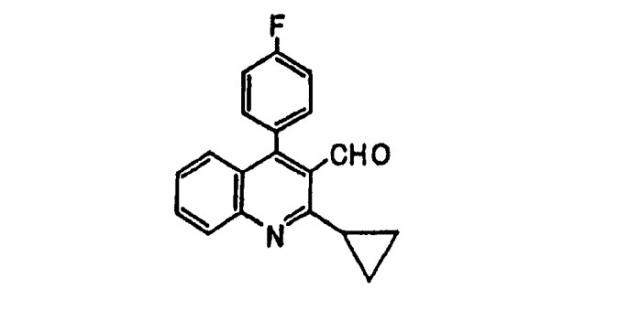
Данное изобретение относится к способу получения производного хинолинкарбоксальдегида, особенно полезного в качестве промежуточного соединения для агентов, снижающих уровень холестерина (ингибиторов HMG-CoA редуктазы). В частности, оно относится к получению 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида.
Уровень техники
В качестве способа получения производного хинолинкарбоксальдегида в JP-A-1-279866, ЕР-А-604063 и патенте США 5011930 описан способ, который включает взаимодействие 2-амино-4'-фторбензофенона с этилизобутирилацетатом с получением производного хинолинкарбоксилата, восстановление его гидридом диизобутилалюминия с получением производного хинолинметанола и дальнейшее окисление его хлорхроматом пиридиния с получением целевого производного хинолинкарбоксальдегида. Однако данный способ получения включает большое количество стадий и не является преимущественным для промышленного производства.
В данном изобретении представлен способ, который делает возможным получение 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида следующей формулы промышленно применимым простым способом.
Описание изобретения
Данное изобретение относится к способу получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида, который включает взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном с получением 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила, и восстановление его, предпочтительно в присутствии кислоты. В данном способе в качестве кислоты предпочтительно применять органическую сульфокислоту.
Данное изобретение также включает способ получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида, который включает восстановление 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Указанный выше 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрил является новым соединением и может быть получен, например, с применением способа, включающего взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном предпочтительно в присутствии кислоты.
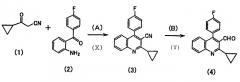
Способ получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида в соответствии с данным изобретением происходит в соответствии со следующей схемой реакции:
(Х): циклизация, (Y): восстановление
Далее описана каждая реакция, входящая в указанную выше схему.
(А) Стадия реакции циклизации
Стадия реакции циклизации в соответствии с данным изобретением представляет собой стадию взаимодействия 3-циклопропил-3-оксопропаннитрила формулы (1) с 2-амино-4'-фторбензофеноном формулы (2), предпочтительно в присутствии кислоты, с получением производного хинолинкарбонитрила [2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила] формулы (3).
Примеры кислоты, предпочтительно применяемой в указанной выше стадии реакции циклизации, включают органические сульфокислоты, такие как метансульфокислота, этансульфокислота, бензолсульфокислота, п-бромбензолсульфокислота и п-толуолсульфокислота; неорганические кислоты, такие как фосфорная кислота, пирофосфорная кислота, полифосфорная кислота, серная кислота и хлористоводородная кислота; и галогенированные органические карбоновые кислоты, такие как монохлоруксусная кислота, дихлоруксусная кислота и трифторуксусная кислота. Особенно предпочтительна органическая сульфокислота.
Количество кислоты, применяемой на стадии циклизации, предпочтительно от 0,1 до 5,0 молей, более предпочтительно от 0,5 до 4,0 молей, особенно предпочтительно от 1,0 до 3,0 молей, на 1 моль 2-амино-4'-фторбензофенона.
Количество применяемого 3-циклопропил-3-оксопропаннитрила предпочтительно составляет от 0,8 до 2,0 молей, более предпочтительно от 1,0 до 1,5 молей на 1 моль 2-амино-4'-фторбензофенона.
Стадию реакции циклизации в соответствии с данным изобретением проводят в присутствии или отсутствии растворителя. Если применяется растворитель, тип растворителя практические не ограничен до тех пределов, пока он не ингибирует реакцию. Примеры растворителей, которые могут применяться, включают алифатические углеводороды, такие как пентан, гексан, гептан, 2-метилбутан, 2-метилпентан, 2-метилгексан, циклопентан, циклогексан и циклогептан; галогенированные алифатические углеводороды, такие как метиленхлорид, хлороформ и дихлорэтан; ароматические углеводороды, такие как бензол, толуол, ксилол и мезитилен; галогенированные ароматические углеводороды, такие как хлорбензол и дихлорбензол; простые эфиры, такие как диизопропиловый эфир, тетрагидрофуран и диоксан; спирты, такие как метанол, этанол, изопропиловый спирт, 2-бутиловый спирт и трет-бутиловый спирт; и органические карбоновые кислоты, такие как уксусная кислота и пропионовая кислота.
Количество растворителя предпочтительно составляет от 2 до 50 мас. частей, более предпочтительно от 3 до 10 мас. частей на 1 мас. часть 2-амино-4'-фторбензофенона. Эти растворители могут применяться как таковые или в сочетании в виде смеси, по крайней мере, двух из них.
Стадию реакции циклизации в соответствии с данным изобретением предпочтительно проводят взаимодействием 2-амино-4'-фторбензофенона с 3-циклопропил-3-оксопропаннитрилом в жидкой фазе предпочтительно в присутствии кислоты. Например, ее проводят методом смешивания кислоты, 3-циклопропил-3-оксопропаннитрила, 2-амино-4'-фторбензофенона и растворителя, с последующим перемешиванием при нагревании в атмосфере азота, при нормальном давлении, при давлении или при пониженном давлении. В таком случае температура реакции предпочтительно составляет от 50 до 160 °С, более предпочтительно от 70 до 140°С. Далее, реакцию циклизации можно проводить при удалении воды, образующейся во время реакции, при необходимости. 2-Амино-4'-фторбензофенон может быть введен в реакционную систему в таком состоянии, чтобы он образовывал соль с указанной выше кислотой (например, он может быть введен в виде метансульфоната 2-амино-4'-фторбензофенона).
Производное хинолинкарбонитрила [2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрил] указанной выше формулы (3), полученное указанной выше реакцией циклизации, является новым соединением и может быть выделено обычным методом выделения/очистки, например дистилляцией, перекристаллизацией или хроматографией на колонке, после завершения реакции.
(В) Стадия восстановления
Стадия восстановления, применяемая в данном изобретении, представляет собой стадию восстановления производного хинолинкарбонитрила формулы (3) с получением производного хинолинкарбоксальдегида формулы (4).
Указанную выше стадию восстановления проводят обычным методом восстановления, который превращает цианогруппу в формильную группу. Например, может применяться восстановление соединением гидрида алюминия (таким как гидрид диизобутилалюминия), восстановление водородом, муравьиной кислотой или формиатом аммония в присутствии никеля Ренея, восстановление хлоридом двухвалентного олова или восстановление водородом в присутствии палладия. Предпочтительно применяют восстановление гидридом диизобутилалюминия (далее обозначенное как реакция восстановления (а)), восстановление муравьиной кислотой в присутствии никеля Ренея (далее обозначенное как реакция восстановления (b)) или восстановление водородом в присутствии никеля Ренея (далее обозначенное как реакция восстановления (с)).
(1) Реакция восстановления (а): восстановление гидридом диизобутилалюминия.
Количество гидрида диизобутилалюминия, применяемое в реакции восстановления (а), предпочтительно составляет от 0,5 до 5,0 молей, более предпочтительно от 0,9 до 1,5 молей на 1 моль производного хинолинкарбонитрила.
Реакцию восстановления (а) проводят в присутствии или отсутствии растворителя. Применяемый растворитель практически не ограничен до тех пор, пока он не ингибирует реакцию, примеры растворителей включают ароматические углеводороды, такие как бензол, толуол и ксилол; и простые эфиры, такие как диизопропиловый эфир, тетрагидрофуран и диоксан. Предпочтительно применяют ароматический углеводород, более предпочтительно толуол.
Применяемое количество растворителя предпочтительно составляет от 2 до 50 мас. частей, более предпочтительно от 3 до 20 мас. частей на 1 мас. часть производного хинолинкарбонитрила. Эти растворители могут применяться в чистом виде или в комбинации в виде смеси, по крайней мере, двух из них.
Реакцию восстановления (а) проводят предпочтительно взаимодействием гидрида диизобутилалюминия с производным хинолинкарбонитрила в жидкой фазе. Например, ее проводят методом смешивания гидрида диизобутилалюминия, производного хинолинкарбонитрила и растворителя, предпочтительно при охлаждении, и их взаимодействием в атмосфере инертного газа, при нормальном давлении или при давлении. В таком случае температура реакции предпочтительно составляет от -50 до 60°С, более предпочтительно от -20 до 40°С.
(2) Реакция восстановления (b): восстановление муравьиной кислотой в присутствии никеля Ренея.
Никель Ренея, применяемый в реакции восстановления (b) представляет собой сплав, содержащий никель и алюминий в качестве основных компонентов, где содержание никеля составляет предпочтительно от 10 до 90 мас.%, более предпочтительно от 40 до 80 мас.%. Обычно применяется разрыхленный никель Ренея, но также может применяться никель Ренея, подвергнутый предварительной обработке различными методами или стабилизированный никель Ренея. Также может применяться никель Ренея, содержащий металлы, такие как кобальт, железо, свинец, хром, титан, молибден, ванадий, марганец, олово или вольфрам.
Применяемое количество никеля Ренея предпочтительно составляет от 0,30 до 2 мас. частей, более предпочтительно от 0,30 до 1,2 мас. частей в расчете на атомы никеля, на 1 мас. часть производного хинолинкарбонитрила.
Муравьиная кислота, применяемая в реакции восстановления (b), может применяться в виде чистой муравьиной кислоты, однако предпочтительно реакцию проводят в присутствии муравьиной кислоты и воды в количестве от 0,25 до 1 об. части на 1 об. часть муравьиной кислоты.
Применяемое количество муравьиной кислоты предпочтительно составляет от 0,25 до 50 мас. частей, более предпочтительно от 1 до 40 мас. частей на 1 мас. часть производного хинолинкарбонитрила.
Реакция восстановления (b) может проводиться в присутствии растворителя, отличного от муравьиной кислоты и воды. Применяемый растворитель практически не ограничен до тех пор, пока он не ингибирует реакцию, примеры растворителей включают амиды, такие как N,N-диметилформамид; спирты, такие как метанол, этанол, изопропиловый спирт и трет-бутиловый спирт; алифатические углеводороды, такие как пентан и циклогексан; ароматические углеводороды, такие как толуол и ксилол; и органические карбоновые кислоты, такие как уксусная кислота и пропионовая кислота.
Применяемое количество растворителя предпочтительно составляет от 0 до 60 мас. частей, более предпочтительно от 0 до 10 мас. частей на 1 часть производного хинолинкарбонитрила. Эти растворители могут применяться как таковые или в сочетании в виде смеси, по крайней мере, двух из них.
Реакцию восстановления (b) проводят предпочтительно взаимодействием муравьиной кислоты и воды с производным хинолинкарбонитрила в жидкой фазе в присутствии никеля Ренея. Например, ее проводят методом смешивания никеля Ренея, производного хинолинкарбонитрила, муравьиной кислоты и воды с последующим перемешиванием при нагревании в атмосфере инертного газа при нормальном давлении или при давлении. В таком случае температура реакции предпочтительно составляет от 20 до 100°С, более предпочтительно от 30 до 80°С.
Далее, при необходимости, в реакционную систему может быть добавлено неорганическое основание, соль платины, соль свинца или соль кадмия для обеспечения реакционноспособности [Teruo Kubomatsu, Shinichiro Komatsu, /Raney catalyst/ (опубликовано Kawaken Fine Chemicals Co., Ltd.), стр. 123-147, HU 45958].
Производное хинолинкарбоксальдегида в качестве конечного продукта выделяют и очищают обычными методами, такими как дистилляция, перекристаллизация или хроматография на колонке после завершения реакции.
(3) Реакция восстановления (с): восстановление водородом в присутствии никеля Ренея.
Никель Ренея, применяемый в реакции восстановления (с) представляет собой сплав, содержащий никель и алюминий в качестве основных компонентов, где содержание никеля составляет предпочтительно от 10 до 90 мас.%, более предпочтительно от 40 до 80 мас.%. Обычно применяется разрыхленный никель Ренея, но также может применяться никель Ренея, подвергнутый предварительной обработке различными методами или стабилизированный никель Ренея. Также может применяться никель Ренея, содержащий металлы, такие как кобальт, железо, свинец, хром, титан, молибден, ванадий, марганец, олово или вольфрам.
Применяемое количество никеля Ренея предпочтительно составляет от 0,001 до 2 мас. частей, более предпочтительно от 0,01 до 1,2 мас. частей в расчете на атомы никеля, на 1 мас. часть производного хинолинкарбонитрила.
Реакцию восстановления (с) проводят предпочтительно в присутствии кислоты, например, может применяться серная кислота, метансульфокислота, уксусная кислота или трифторуксусная кислота. Применяемое количество кислоты предпочтительно составляет от 1 до 10 молей, более предпочтительно от 1,5 до 5 молей на 1 моль производного хинолинкарбонитрила.
Реакцию восстановления (с) проводят в растворителе. Применяемый растворитель практически не ограничен до тех пор, пока он не ингибирует реакцию, примеры растворителей включают воду; спирты, такие как метанол, этанол, изопропиловый спирт и трет-бутиловый спирт; амиды, такие как N,N-диметилформамид; алифатические углеводороды, такие как пентан и циклогексан; ароматические углеводороды, такие как толуол и ксилол; карбоновые кислоты, такие как муравьиная кислота, уксусная кислота и пропионовая кислота; и простые эфиры, такие как диизопропиловый эфир, тетрагидрофуран или диоксан.
Применяемое количество указанного выше растворителя предпочтительно составляет от 1 до 50 мас. частей, более предпочтительно от 2 до 20 мас. частей на 1 мас. часть производного хинолинкарбонитрила. Эти растворители могут применяться в чистом виде или в сочетании в виде смеси, по крайней мере, двух из них.
Реакцию восстановления (с) предпочтительно проводят взаимодействием водорода с производным хинолинкарбонитрила в жидкой фазе в присутствии никеля Ренея. Например, ее проводят методом смешивания никеля Ренея, производного хинолинкарбонитрила и растворителя с последующим перемешиванием при нагревании в атмосфере водорода (который может быть разбавлен инертным газом) при давлении от 0,1 до 5 МПа, в закрытой системе или при циркуляции водорода. В таком случае температура реакции предпочтительно составляет от 10 до 100°С, более предпочтительно от 20 до 70°С.
Далее, при необходимости в реакционную систему может быть добавлено неорганическое основание, органическое основание, соль платины, соль свинца или смоль кадмия для обеспечения реакционноспособности [Teruo Kubomatsu, Shinichiro Komatsu, /Raney catalyst/ (опубликовано Kawaken Fine Chemicals Co., Ltd.), стр. 123-147, HU 45958].
Производное хинолинкарбоксальдегида в качестве конечного продукта выделяют и очищают обычными методами, такими как дистилляция, перекристаллизация или хроматография на колонке после завершения реакции.
Далее данное изобретение иллюстрируется более подробно с помощью примеров.
Пример 1
В стеклянную колбу, имеющую внутренний объем 200 мл, оборудованную мешалкой, термометром, обратным холодильником и насадкой Дина-Старка, помещают 80 мл толуола и 20 мл циклогексана в атмосфере азота и туда при перемешивании добавляют 2,94 г (30,6 ммоль) метансульфокислоты, 3,50 г (32,1 ммоль) 3-циклопропил-3-оксопропаннитрила и 6,59 (30,6 ммоль) 2-амино-4'-фторбензофенона. Затем повышают температуру и реакцию проводят при температуре от 90 до 95°С в течение 4 часов, отгоняя образующуюся воду. После завершения реакции реакционную жидкость охлаждают до комнатной температуры и добавляют 100 мл воды и 5,5 мл (44,0 ммоль) 8 моль/л водного раствора гидроксида натрия для подщелачивания реакционной жидкости. Полученную реакционную жидкость дважды экстрагируют 200 мл этилацетата, затем органический слой отделяют и добавляют 2 г безводного сульфата магния, 2 г силикагеля и 2 г активированного угля с последующим перемешиванием при комнатной температуре в течение 1 часа. После фильтрации фильтрат концентрируют при пониженном давлении с получением 8,45 г 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила в виде бледно-желтого твердого вещества с чистотой 99% (процентная доля площади при высокоэффективной жидкостной хроматографии) (выход: 95%).
Физические свойства полученного 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила следующие:
Температура плавления: 161,0 - 161,5°С.
Элементный анализ: углерод 79,17%, водород 4,54%, азот 9,76%[теоретические значения (С19Н13N2F): углерод 79,15%, водород 4,54%, азот 9,72%]
CI-МС (m/e): 289 (М+1)
ИК(KBr метод, см-1):2225, 1605, 1561, 1514, 1493, 1222, 1162, 846, 769
1H-ЯМР(CDCl3, δ(м.д.)): 1.71-1.24(2Н, м), 1.37-1.43(2Н, м), 2.66-2.72(1Н, м), 7.25-7.32(2Н, м), 7.41-7.49(3Н, м), 7.58(1Н, д, J=6.8 Гц), 7.72-7.79(1Н, м), 7.99(1Н, д, J=8.5 Гц)
Пример 2
В стеклянную колбу, имеющую внутренний объем 10 мл, оборудованную мешалкой, термометром, обратным холодильником и насадкой Дина-Старка, помещают 5 мл диизопропилового эфира в атмосфере азота и туда при перемешивании добавляют 0,82 г (4,6 ммоль) пирофосфорной кислоты, 0,29 г (2,5 ммоль) 3-циклопропил-3-оксопропаннитрила и 0,50 г (2,3 ммоль) 2-амино-4'-фторбензофенона при комнатной температуре. Затем повышают температуру до 70°С и реакцию проводят в течение 3 часов. После завершения реакции реакционную жидкость охлаждают до комнатной температуры и анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 0,60 г (выход: 91%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 3
Реакцию проводят по методике примера 2 за исключением того, что растворитель меняют на дихлорэтан и температуру реакции и время реакции меняют на 70°С в течение 3 часов и 90°С в течение 3 часов. В результате получают 0,54 г (выход: 82%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 4
Реакцию проводят по методике примера 2 за исключением того, что кислоту меняют на 0,66 г (7,0 ммоль) монохлоруксусной кислоты, и время реакции меняют на 9 часов. В результате получают 0,40 г (выход: 60%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 5
Реакцию проводят по методике примера 2 за исключением того, что кислоту меняют на 0,22 г (2,3 ммоль) 96 мас.% серной кислоты и растворитель меняют на 2-бутанол. В результате получают 0,49 г (выход: 75%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 6
В стеклянную колбу, имеющую внутренний объем 50 мл, оборудованную мешалкой, термометром и обратным холодильником, помещают 0,72 г (6,6 ммоль) 3-циклопропил-3-оксопропаннитрила, 1,92 г (6,0 ммоль) метансульфоната 2-амино-4'-фторбензофенона, имеющего чистоту 97,3% и 10 мл толуола в атмосфере азота и реакцию проводят при 80°С в течение 2 часов. После завершения реакции реакционную жидкость охлаждают до комнатной температуры и добавляют 7,0 мл (7,0 ммоль) 1 моль/л водного раствора гидроксида натрия для подщелачивания реакционной жидкости с последующим разделением жидкостей, и полученный органический слой анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 1,70 г (выход: 98%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 7
В стеклянную колбу, имеющую внутренний объем 300 мл, оборудованную мешалкой, термометром, обратным холодильником и насадкой Дина-Старка, помещают 11,6 г (106,6 ммоль) 3-циклопропил-3-оксопропаннитрила, 31,0 г (96,9 ммоль) метансульфоната 2-амино-4'-фторбензофенона, имеющего чистоту 97,3%, и 121 мл толуола в атмосфере азота и реакцию проводят при давлении 0,04 МПа при 80 °С в течение 2 часов, отгоняя образующуюся воду. После завершения реакции реакционную жидкость охлаждают до комнатной температуры и добавляют 60 мл воды и 13,3 мл (106,4 ммоль) 8 моль/л водного раствора гидроксида натрия для подщелачивания реакционной жидкости с последующим разделением жидкостей, и полученный органический слой анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 27,9 г (выход: 99%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 8
В стеклянную колбу, имеющую внутренний объем 50 мл, оборудованную мешалкой, термометром, обратным холодильником и насадкой Дина-Старка, помещают 10,72 г (6,6 ммоль) 3-циклопропил-3-оксопропаннитрила, 1,92 г (6,0 ммоль) метансульфоната 2-амино-4'-фторбензофенона, имеющего чистоту 97,3%, и 10 мл толуола в атмосфере азота и реакцию проводят при 110°С в течение 2 часов, отгоняя образующуюся воду. После завершения реакции реакционную жидкость охлаждают до комнатной температуры и добавляют 7,0 мл (7,0 ммоль) 1 моль/л водного раствора гидроксида натрия для подщелачивания реакционной жидкости с последующим разделением жидкостей, и полученный органический слой анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 1,57 г (выход: 91%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
Пример 9
В стеклянную колбу, имеющую внутренний объем 50 мл, оборудованную мешалкой, термометром и капельной воронкой, помещают 0,29 г (1,0 ммоль) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила, полученного в примере 1, и 2,5 мл толуола в атмосфере аргона, и охлаждают до температуры -10°С на ледяной бане. Затем при поддержании температуры жидкости на уровне от -10 до 0°С постепенно, по каплям добавляют 0,68 мл (1,0 ммоль) 1,5 моль/л раствора гидрида диизобутилалюминия в толуоле. После завершения добавления по каплям температуру повышают до комнатной температуры с последующим перемешиванием в течение 1 часа. После завершения реакции к полученной реакционной жидкости добавляют 1 мл метанола с последующим перемешиванием в течение 10 минут и добавляют 15 мл 1 моль/л хлористоводородной кислоты для нейтрализации. Затем реакционную жидкость концентрируют при пониженном давлении, добавляют 15 мл воды и три раза экстрагируют 30 мл хлороформа. Затем органический слой отделяют, выделяют и сушат над безводным сульфатом магния. После фильтрации фильтрат концентрируют при пониженном давлении с получением 0,30 г 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида в виде желтого твердого вещества с чистотой 99% (процентная доля площади при высокоэффективной жидкостной хроматографии) (выход: 88%).
Физические свойства полученного 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида следующие:
CI-МС (m/e): 292 (М+1)
1Н-ЯМР (CDCl3, δ (м. д.)): 1.07-1.13 (2Н, м), 1.36-1.58 (2Н, м), 3.19-3.24 (1Н, м), 7.23-7.72 (6Н, м), 7.73-7.77 (1Н, м), 7.97 (1Н, д, J=8.7 Гц), 10.07 (1Н, с)
Пример 10
В стеклянную колбу, имеющую внутренний объем 5 мл, оборудованную мешалкой, термометром и капельной воронкой, помещают 500 мг (1,7 ммоль) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила, полученного в примере 1, 5,0 мл (141 ммоль) 95 об.% водного раствора муравьиной кислоты и 750 мг (6,4 ммоль в расчете на атомы никеля) гидрированного разрыхленного никеля Ренея (производства Kawaken Fine Chemicals Co., Ltd., NDHT-90 (содержание никеля: 50 мас.%)) в атмосфере аргона и реакцию проводят при температуре 40оС в течение 7 часов. После завершения реакции реакционную жидкость охлаждают до комнатной температуры, катализатор отфильтровывают через целит и реакционную жидкость концентрируют. Затем к полученному концентрату добавляют 5 мл 1 моль/л хлористоводородной кислоты и дважды экстрагируют 50 мл толуола. Органический слой отделяют и анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 218 мг (выход: 43%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида.
Пример 11
В поликарбонатный автоклав, имеющий внутренний объем 100 мл, оборудованный мешалкой, помещают 300 мг (1,0 ммоль) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила, полученного в примере 1, 1,526 мг (5,2 ммоль) 95 мас.% серной кислоты, 150 мг (1,3 ммоль в расчете на атомы никеля) гидрированного разрыхленного никеля Ренея (производства Kawaken Fine Chemicals Co., Ltd., NDHT-90 (содержание никеля: 50 мас.%)) и 15 мл этанола и реакцию проводят при давлении водорода от 0,2 до 0,4 МПа при комнатной температуре в течение 2 часов. Полученную реакционную жидкость анализируют при помощи высокоэффективной жидкостной хроматографии (абсолютный количественный анализ) с получением 105 мг (выход: 36%) 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида.
Промышленная применимость
Согласно данному изобретению производное хинолинкарбоксальдегида может быть получено с высоким выходом, с использованием легко доступных соединений простым способом. Следовательно, способ получения производного хинолинкарбоксальдегида в соответствии с данным изобретением является промышленно предпочтительным.
1. Способ получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида, который включает взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном с получением 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила и его восстановление.
2. Способ получения по п.1, в котором взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном проводят в присутствии кислоты.
3. Способ получения по п.2, в котором в качестве кислоты применяют органическую сульфокислоту.
4. Способ получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбоксальдегида, который включает восстановление 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила.
5. 2-Циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрил.
6. Способ получения 2-циклопропил-4-(4'-фторфенил)хинолин-3-карбонитрила, который включает взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном.
7. Способ получения по п.6, в котором взаимодействие 3-циклопропил-3-оксопропаннитрила с 2-амино-4'-фторбензофеноном проводят в присутствии кислоты.
8. Способ получения по п.7, в котором в качестве кислоты применяют органическую сульфокислоту.