Замещенные в ортоположении амиды антраниловой кислоты и их применение в качестве лекарственных средств
Иллюстрации
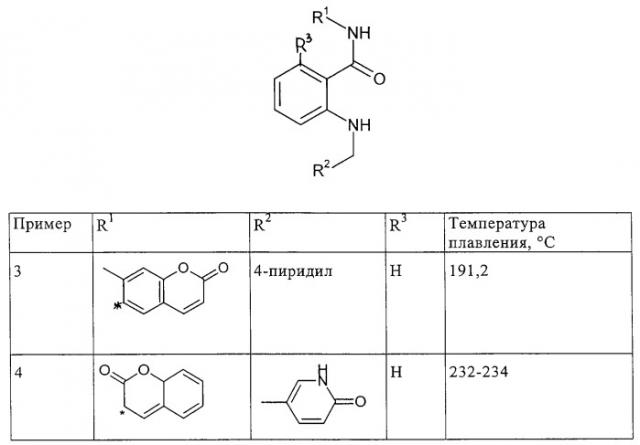
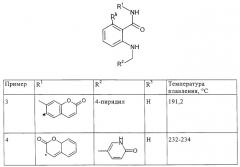
Показать всеИзобретение относится к области органической химии, в частности к соединениям общей формулы I
в которой R1 представляет собой группу
где * обозначает точку присоединения,
R4 обозначает фтор, хлор, бром, -CF3, -N=C, СН3-, -OCF3 или -CH2OH; R5обозначает хлор, бром или ОСН3; R6 обозначает -СН3 или хлор; R7 обозначает СН3 или хлор; R8 обозначает СН3, фтор, хлор или CF3; R2 представляет собой пиридил или группу
и R3 представляет собой водород или фтор, а также их таутомеры, Е-изомеры или Z-изомеры, рацематы, энантиомеры и соли, которые являются ингибиторами тирозинкиназы KDR и FLT. Также описаны лекарственные средства, содержащие заявленные соединения и предназначенные для лечения заболеваний, связанных с ингибированием киназы KDR и FLT. 2 н. и 4 з.п. ф-лы, 2 табл.
Реферат
Настоящее изобретение относится к замещенным в ортоположении амидам антраниловой кислоты и к их применению в качестве лекарственных средств, предназначенных для лечения заболеваний, обусловленных персистирующим ангиогенезом.
Персистирующий ангиогенез может являться причиной различных заболеваний, таких как псориаз, артрит, такой как ревматоидный артрит, гемангиома, ангиофиброма, глазные болезни, такие как диабетическая ретинопатия, неоваскулярная глаукома, заболевания почек, такие как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжения трансплантатов и гломерулопатия, фиброзные заболевания, такие как цирроз печени, заболевания, связанные с пролиферацией мезангиальных клеток, и артериосклероз, или может приводить к прогрессированию этих заболеваний.
Для лечения подобных заболеваний, равно как и других форм патологического ангиогенеза, индуцированного васкулярным эндотолиальным фактором роста (VEGF), и для устранения условий, способствующих проницаемости сосудов, таких как васкуляризация опухолей, можно использовать прямое или косвенное ингибирование VEGF-рецептора. Так, например, известно, что с помощью растворимых рецепторов и антител к VEGF удается подавлять рост опухолей.
Персистирующий ангиогенез индуцируется VEGF-фактором, медиатором чего является его рецептор. Необходимым условием для VEGF проявить это действие является его связывание с рецептором и инициирование фосфорилирования тирозином.
На сегодняшний день известны производные фенилантраниламидов, которые применяются в качестве антагонистов ангиотензина II (см. заявку ЕР 564356), а также в качестве ингибиторов воспалений и в качестве противоязвенных соединений (см. патент US 3409668).
При создании настоящего изобретения было установлено, что соединения общей формулы I
в которой R1 представляет собой группу
где R5 обозначает хлор, бром или ОСН3, или группу
где R7 обозначает СН3 или хлор, или группу
где R8 обозначает СН3, фтор, хлор или CF3, R4 обозначает фтор, хлор, бром, -CF3, -N=C, СН3-, -OCF3 или -CH2OH, a R6 обозначает -СН3 или хлор,
R2 представляет собой пиридил или группу
и R3 представляет собой водород или фтор,
а также их изомеры и соли блокируют фосфорилирование тирозином, соответственно персистирующий ангиогенез и препятствуют тем самым росту и распространению опухолей.
Существуют различные тирозинкиназы (Web-сайт: S. Hauk, A. M. Quinn, Meth. in Enzymol. 200, стр.38-62 (1991), ссылка размещена в разделе (домене), посвященном катализаторам, подгруппа РТК group XIV, Web-страница: http://www.sdsc.edu/K.inases/pkr/pk_catalytic/pk_hanks_seq_align_long.html и Mc Tigue и др., Structure 7, стр. 319-330 (1999)), которые могут подавляться аналогичным образом. Так, например, с помощью соединений, ингибирующих VEGF (васкулярный эндотелиальный фактор роста), удается обычно подавлять в том числе и тирозинкиназу С, присутствующую, в частности, в стволовых клетках. С учетом вышеизложенного понятно стремление получить соединения с избирательным в отношении фактора VEGF ингибирующим действием.
Предлагаемые в изобретении соединения отличаются именно благодаря тому, что обладают такими селективными свойствами и представляют собой тем самым ценные соединения, способные препятствовать росту и распространению опухолей.
Соединения по изобретению общей формулы I содержат также возможные таутомерные формы и включают Е- и Z-изомеры или, при наличии хирального центра, также рацематы и энантиомеры.
Соединения формулы I, равно как и их физиологические приемлемые соли, благодаря их ингибирующей активности по отношению к фосфорилированию VEGF-рецептора могут применяться в качестве лекарственных средств. Механизм их действия позволяет применять предлагаемые соединения для лечения заболеваний, обусловленных персистирующим ангиогенезом.
Поскольку соединения формулы I, как было установлено, являются ингибиторами тирозинкиназы KDR и FLT, они пригодны прежде всего для лечения таких заболеваний, которые обусловлены иницируемым VEGF-рецептором персистирующим ангиогенезом или повышением проницаемости сосудов.
Объектом настоящего изобретения в соответствии с этим является также применение предлагаемых соединений в качестве ингибиторов тирозинкиназы KDR и FLT.
Еще одним объектом настоящего изобретения являются далее лекарственные средства, предназначенные для лечения опухолей, соответственно их применение.
Соединения по изобретению могут применяться индивидуально либо в составе соответствующей композиции в качестве лекарственных средств для лечения псориаза, артрита, такого как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжения трансплантатов и гломерулопатия, фиброзных заболеваний, таких как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза и повреждений нервной ткани.
Соединения по изобретению могут применяться также для подавления повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после использования механических устройств, предназначенных обеспечить проходимость сосудов, таких, например, как стенты.
При лечении повреждений нервной ткани с помощью соединений по изобретению можно предотвратить быстрое образование рубцов в поврежденных местах, т.е. удается предотвратить рубцевание до того момента, когда аксоны снова восстановят связь между собой. Тем самым, как очевидно, создается возможность для восстановления связей между нервными клетками.
Кроме того, с помощью предлагаемых в изобретении соединений можно подавлять образование у пациентов асцита. В равной степени возможно также подавление отеков, обусловленных фактором VEGF.
Лекарственные средства вышеназванного типа, их композиции и их применение также являются объектом настоящего изобретения.
Изобретение относится далее к применению соединений общей формулы I для получения соответствующего лекарственного средства, предназначенного для лечения опухолей, псориаза, артрита, такого как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжения трансплантатов и гломерулопатия, фиброзных заболеваний, таких как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза и повреждений нервной ткани, для подавления повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после использования механических устройств, предназначенных обеспечить проходимость сосудов, таких, например, как стенты.
Для применения соединений формулы I в качестве лекарственных средств из них изготавливают соответствующий фармацевтический препарат, содержащий в своем составе наряду с активным веществом для энтерального или парентерального введения пригодные для этих целей фармацевтические, органические либо неорганические инертные носители, такие, например, как вода, желатин, гуммиарабик, лактоза, крахмал, стеарат магния, тальк, масла растительного происхождения, полиалкиленгликоли и т.п. Фармацевтические препараты могут изготавливаться в твердой форме, например в виде таблеток, драже, суппозиториев, капсул, или в жидкой форме, например в виде растворов, суспензий или эмульсий. При необходимости они содержат, кроме того, вспомогательные вещества, такие как консерванты, стабилизаторы, смачиватели или эмульгаторы, соли для регуляции осмотического давления или буферы.
Для парентерального применения пригодны прежде всего растворы для инъекций или суспензии, в первую очередь водные растворы активных соединений в полигидроксиэтоксилированном касторовом масле.
В качестве систем-носителей можно использовать также поверхностно-активные вспомогательные вещества, такие как соли желчных кислот или фосфолипиды животного либо растительного происхождения, равно как и их смеси, а также липосомы либо их компоненты.
Для перорального применения пригодны прежде всего таблетки, драже или капсулы с тальком и/или углеводородным носителем или связующим, как, например, лактоза, кукурузный или картофельный крахмал. Возможно также применение жидких форм, таких, например, как настойка, необязательно с добавлением подслащивающего вещества.
Дозировку активных веществ можно варьировать в зависимости от методики введения, возраста и веса пациента, типа и степени тяжести соответствующего заболевания и тому подобных факторов. Суточная доза составляет от 0,5 до 2000 мг, предпочтительно от 50 до 1000 мг, причем эту дозу можно назначать в качестве разовой дозы или из расчета на два либо несколько приемов.
Вышеописанные композиции и препаративные формы также являются объектом настоящего изобретения.
Соединения по изобретению можно получать по известным методам. Так, например, соединения формулы I можно получать благодаря тому, что
а) соединение общей формулы II
в которой R4-R7 имеют указанные выше значения, а Т представляет собой Н или защитную группу и А представляет собой галоген или OR13, где R13 обозначает атом водорода, С1-С4алкил либо С1-С4ацил или образует с Т замкнутое кольцо, сначала N-алкилируют, а затем переводят СОА в амид и после этого при необходимости отщепляют защитные группы либо сначала переводят в амид, а затем N-алкилируют, или
б) соединение формулы III,
в которой R4-R7 имеют указанные выше значения, а Т представляет собой Н или защитную группу, металлируют в ортоположении и затем путем захвата электрофилом переводят в амид, после чего защитную группу отщепляют и аминогруппу алкилируют, или
в) соединение формулы IV,
в которой R4-R7 имеют указанные выше значения, а Т представляет собой Н или защитную группу и В обозначает галоген или O-трифлат, O-тозилат либо O-мезилат, переводят в амид, после чего защитную группу отщепляют и аминогруппу алкилируют.
Последовательность проведения вышеописанных операций может во всех случаях варьироваться.
Процесс образования амидов осуществляют по методам, известным из литературы. Так, в частности, для образования амидов можно исходить из соответствующего сложного эфира. Этот эфир подвергают согласно Journ. Org. Chem. стр. 8414 (1995) взаимодействию с триметилалюминием и соответствующим амином в растворителях, таких как толуол, при температурах в интервале от 0°С до температуры кипения используемого растворителя. Данный метод применим также в случае незащищенных эфиров антраниловой кислоты. Если молекула содержит две сложноэфирных группы, то их обе переводят в один и тот же амид.
При использовании вместо сложного эфира нитрилов получают в аналогичных условиях амидины.
Для образования амидов могут использоваться также все методы, известные из химии пептидов. Так, например, соответствующую кислоту можно подвергать в апротонных полярных растворителях, таких, в частности, как диметилформамид, с использованием соответствующего активированного производного кислоты, получаемого, например, с помощью гидроксибензотриазола и карбодиимида, такого как диизопропилкарбодиимид, или же с помощью предварительно образованных реагентов, таких, например, как ГАТУ (Chem. Comm. стр. 201 (1994)) или БТУ, при температурах в интервале от 0°С до температуры кипения растворителя, предпочтительно при 80°С, взаимодействию с амином (при использовании ГАТУ предпочтительно при комнатной температуре). Данные методы применимы и в случае незащищенных антраниловых кислот. Для образования амидов можно применять также метод, где используют смешанный ангидрид кислоты, имидазолид или азид.
Предварительная защита аминогруппы, например в виде амида, не является обязательным условием во всех случаях, однако целесообразнее предусмотреть такую защиту, поскольку это оказывает положительное воздействие на реакцию. Особым исходным материалом являются ангидриды изатовой кислоты, в которых одновременно представлены и защищенная аминогруппа, и активированная кислотная функциональная группа.
Если амин предварительно переводить в БОК-защищенное соединение, то металлирование в ортоположении можно осуществлять взаимодействием с металлоорганическими соединениями, такими, например, как н-бутиллитий, и затем по реакции захвата изоцианатами либо изотиоцианатами превращать в антраниламиды, соответственно антранилтиоамиды. Использование в этом ортоположении такого заместителя, как бром или иод, благодаря обмену галоген-металл позволяет более эффективно осуществлять ортометаллирование. В качестве растворителей для указанных реакций могут использоваться простые эфиры, такие как диэтиловый эфир, или тетрагидрофуран либо углеводороды, такие как гексан, а также их смеси. Целесообразно добавлять при этом комплексообразователи, такие как тетраметилэтилендиамин (ТМЭДА). Температурный режим варьируется в интервале от -78°С до комнатной температуры. Расщепление БОК-амидов осуществляют действием кислот, таких как трифторуксусная кислота, без использования растворителей или в растворителях, таких как метиленхлорид, при температурах в интервале от 0°С до температуры кипения растворителя либо с помощью водной соляной кислоты, предпочтительно 1 н. соляной кислоты, в растворителях, таких как этанол или диоксан, при температурах в интервале от комнатной до температуры кипения растворителя.
Амидную группу можно вводить также путем карбонилирования. С этой целью исходят из соответствующих соединений формулы IV (о-иод-, о-бром- или о-трифлилоксианилинов), которые подвергают взаимодействию с монооксидом углерода при нормальном или же повышенном давлении и с амином в присутствии катализаторов на основе переходных металлов, таких, например, как хлорид палладия(II) либо ацетат палладия(II) или палладийтетракистрифенилфосфин, в растворителях, таких как диметилформамид. Целесообразным может оказаться добавление лиганда, такого как трифенилфосфин, и добавление основания, такого как трибутиламин (см., например, Journ. Org. Chem., стр. 3327 (1974); Journ. Org. Chem., стр. 7482 (1996); Synth. Comm., стр. 367 (1997); Tetr. Lett, стр. 2835 (1998)).
Если предусматривается введение в молекулу различных амидных групп, то необходимо, например, вторую сложноэфирную группу вводить в молекулу после образования первой амидной группы и затем амидировать или в случае молекулы, в которой одна группа представлена в виде сложного эфира, а другая в виде кислоты, обе группы амидируют последовательно с помощью различных методов.
Тиоамиды можно получать из антраниламидов взаимодействием с дифосфадитианами согласно Bull. Soc. Chim. Belg. 87, стр. 229 (1978) или взаимодействием с пентасульфидом фосфора в растворителях, таких как пиридин, либо вообще без использования растворителей при температурах в интервале от 0 до 200°С.
Продукты в виде богатых электронами ароматических соединений могут подвергаться также электрофильному ароматическому замещению. Замещение в этих случаях проводят в орто- либо параположении относительно аминогруппы или одной из аминогрупп. Так, в частности, можно осуществлять ацилирование по Фриделю-Крафтсу с помощью хлорангидридов кислот в присутствии катализаторов Фриделя-Крафтса, таких, например, как трихлорид алюминия, в растворителях, таких как нитрометан, сероуглерод, метиленхлорид или нитробензол, при температурах в интервале от 0°С до температуры кипения используемого растворителя, предпочтительно при комнатной температуре. По известным из литературы методам, например с помощью нитрирующей кислоты, азотной кислоты в различной концентрации без использования растворителей либо с помощью нитратов металлов, таких, например, как нитрат меди(II) или нитрат железа(III), в полярных растворителях, таких как этанол или ледяная уксусная кислота, либо в ацетангидриде можно вводить одну или несколько нитрогрупп.
Галогены вводят по известным из литературы методам, например обменной реакцией с бромом, N-бром- либо N-иодсукцинимидом или гидротрибромидом уротропина в полярных растворителях, таких как тетрагидрофуран, ацетонитрил, метиленхлорид, ледяная уксусная кислота или диметилформамид.
Восстановление нитрогруппы проводят в полярных растворителях при комнатной температуре или при повышенной температуре. В качестве катализаторов восстановления пригодны металлы, такие как никель Ренея, или катализаторы на основе благородных металлов, таких как палладий или платина, а также гидроксид палладия, необязательно нанесенные на носители. Вместо водорода известным образом могут использоваться также, например, формиат аммония, циклогексен или гидразин. В равной степени возможно использование и таких восстановителей, как хлорид олова(II) или хлорид титана(III), а также таких как комплексные гидриды металлов, необязательно в присутствии солей тяжелых металлов. В качестве восстановителя приемлемо также железо. В этих случаях реакцию проводят в присутствии соответствующей кислоты, такой, например, как уксусная кислота, или хлорида аммония, необязательно с добавлением растворителя, такого, например, как вода, метанол, железо/аммиак и т.п. При большей продолжительности реакции в этом варианте может начаться ацилирование аминогруппы.
Если предусматривается алкилирование аминогруппы, то эту группу можно алкилировать по обычным методам, например алкилгалогенидами, или согласно варианту Мицонубо (Mitsonubo) взаимодействием с соответствующим спиртом в присутствии, например, трифенилфосфина и эфира азодикарбоновой кислоты. Возможен и иной подход, а именно: подвергать амин восстановительному алкилированию альдегидами либо кетонами, осуществляя эту реакцию в присутствии восстановителя, такого, например, как цианоборогидрид натрия, в соответствующем инертном растворителе, например этаноле, при температурах в интервале от 0°С до температуры кипения растворителя. Если исходить из первичной аминогруппы, то реакцию можно проводить при необходимости с последовательным использованием двух различных карбонильных соединений, получая при этом смешанные производные [см., например, Verardo и др., Synthesis, стр.121 (1993); Synthesis, стр.447 (1991); Kawaguchi, Synthesis, стр.701 (1985); Micovic и др. Synthesis, стр.1043 (1991)]. Целесообразным может оказаться и вариант, в котором сначала взаимодействием альдегида с амином в растворителях, таких как этанол или метанол, необязательно с добавлением вспомогательных веществ, таких как ледяная уксусная кислота, образуют шиффово основание и лишь после этого добавляют восстановитель, такой, например, как цианоборогидрид натрия.
Гидрирование алкеновых или алкиновых групп в молекуле осуществляют обычным образом, например с помощью каталитически активированного водорода. В качестве катализаторов могут применяться тяжелые металлы, такие как палладий или платина, необязательно нанесенные на соответствующий носитель, или никель Ренея. В качестве растворителей пригодны спирты, такие, например, как этанол. При этом работают при температурах в интервале от 0°С до температуры кипения используемого растворителя и при давлении вплоть до 20 бар, предпочтительно, однако, работать при комнатной температуре и нормальном давлении. Благодаря применению катализаторов, таких, например, как катализатор Линдлара, тройные связи удается частично гидрировать до двойных связей с предпочтительным образованием при этом Z-формы.
Ацилирование аминогруппы осуществляют обычным образом, например соответствующим галогенидом кислоты либо ангидридом кислоты, необязательно в присутствии основания, такого как диметиламинопиридин, в растворителях, таких как метиленхлорид, тетрагидрофуран или пиридин, согласно варианту Шоттена-Баумана в водном растворе при слабощелочном значении рН либо взаимодействием с соответствующим ангидридом в ледяной уксусной кислоте.
Введение галогенов - хлора, брома, иода - или азидной группы с помощью аминогруппы можно также проводить, например, по реакции Зандмейера взаимодействием солей диазония, образованных с помощью нитритов в качестве промежуточных продуктов, с хлоридом меди(I) или бромидом меди(I) в присутствии соответствующей кислоты, такой как соляная кислота или бромистоводородная кислота, или же взаимодействием с иодидом калия.
В случае использования эфира органической азотистой кислоты галогены можно вводить, например, добавлением метилениодида или тетрабромметана в растворителе, таком, например, как диметилформамид. Для удаления аминогруппы есть две возможности: либо взаимодействие с эфиром органической азотистой кислоты в тетрагидрофуране, либо диазотирование и восстановительная варка соли диазония, например, с использованием фосфористой кислоты, при необходимости с добавлением оксида меди(I).
Фтор можно вводить, например, по реакции Бальца-Шимана с использованием тетрафторбората диазония либо согласно Journ. Fluor. Chem. 76 (1996), стр. 59-62, путем диазотирования в присутствии HF х пиридина и последующей варки, необязательно в присутствии источника ионов фторида, такого, например, как фторид тетрабутиламмония.
Введение азидогруппы можно осуществлять после диазотирования взаимодействием с азидом натрия при комнатной температуре.
Отщепление простого эфира осуществляют по известным из литературы методам. При этом и в случае наличия в молекуле нескольких групп может быть достигнуто селективное отщепление. В этих целях эфир обрабатывают, например, трибромидом бора в растворителях, таких как дихлорметан, при температурах в интервале от -100°С до температуры кипения используемого растворителя, предпочтительно при -78°С. Вместе с тем возможен и иной подход, а именно: отщеплять эфир под действием тиометилата натрия в растворителях, таких как диметилформамид. Температура при этом может находиться в интервале от комнатной до температуры кипения растворителя, предпочтительно работать при 150°С.
N- или O-алкилирование амидов, таких как пиридин-2-он, соответственно 2-гидроксипиридин, осуществляют по методам, известным из литературы. Так, в частности, при использовании оснований, таких как гидрид натрия или карбонат калия, в растворителях, таких как диметилформамид, и алкилировании с помощью алкилгалогенидов, таких как метилиодид, обеспечивают N-алкилирование. При использовании же таких оснований, как карбонат серебра, в растворителях, таких как тетрагидрофуран либо толуол или предпочтительно их смесей с алкилгалогенидами, такими как метилиодид, обеспечивают O-алкилирование. O-алкилирование можно обеспечить также взаимодействием с тетрафтороборатом триалкилоксония в инертных растворителях, таких как метиленхлорид. Взаимодействием с диазометаном либо триметилсилилдиазометаном в растворителях, таких как метанол или толуол, предпочтительно в их смесях, при температурах вплоть до температуры кипения растворителя, предпочтительно, однако, при комнатной температуре, получают смеси N- и O-алкилпроизводных. Указанные методы позволяют осуществлять селективное алкилирование пиридона в отличие от амида бензойной кислоты.
Смеси изомеров с помощью обычных методов, например путем кристаллизации, хроматографии или солеобразования, можно разделять на энантиомеры, соответственно на E/Z-изомеры.
Процесс получения солей осуществляют обычным образом, а именно:
раствор соединения формулы I смешивают с эквивалентным количеством или с избытком соответствующего основания либо кислоты, необязательно представленных в растворенном виде, и образовавшийся осадок отделяют либо раствор подвергают обычной переработке.
Ниже на примерах более подробно поясняется получение соединений по изобретению, обладающих избирательным действием.
Пример 1
Амид N-[2-оксо-2Н-1-бензопиран-3-ил]-2-[(4-пиридил)метил]аминобензойной кислоты
1. 484 мг 3-амино-2-оксо-2Н-1-бензопирана предварительно помещают в 20 мл метиленхлорида, после чего при охлаждении льдом добавляют по каплям 0,42 мл триэтиламина и 0,40 мл 2-нитробензоилхлорида. Затем в течение 4 ч перемешивают при комнатной температуре, растворитель отгоняют, остаток растворяют в растворе гидрокарбоната натрия и образовавшийся продукт отделяют вакуум-фильтрацией. В результате получают 0,88 г амида N-[2-оксо-2Н-1-бензопиран-3-ил]-2-нитробензойной кислоты. Вышеуказанный 3-амино-2-оксо-2Н-1-бензопиран получали согласно методу Bonsignore и Loy, описанному в Journ. Heterocyclic Chem. 35, стр.117 (1998), из 2-оксо-2Н-1-бензопиран-3-карбоновой кислоты (Journ. Org. Chem. 64, стр.1033-1035 (1999)).
2. 880 мг амида N-[2-оксо-2Н-1-бензопиран-3-ил]-2-нитробензойной кислоты предварительно помещают в атмосфере азота в 30 мл этанола, после чего смешивают с 11 мл циклогексена и 176 мг гидроксида палладия на активированном угле и в течение 2 ч перемешивают при 110°С. Затем катализатор отфильтровывают, а фильтрат концентрируют практически досуха. Образовавшийся продукт отделяют вакуум-фильтрацией, получая в результате 593 мг амида N-[2-оксо-2Н-1-бензопиран-3-ил]-2-аминобензойной кислоты.
3. 645 мг амида N-[2-оксо-2Н-1-бензопиран-3-ил]-2-аминобензойной кислоты в 50 мл метанола и 170 мл ледяной уксусной кислоты предварительно помещают в реактор при комнатной температуре, после чего смешивают с 0,38 мл 4-пиридинкарбальдегида. Смесь перемешивают в течение 15 ч и затем смешивают с 206 мг цианоборогидрида натрия. Далее продолжают перемешивание в течение 24 ч и образовавшиеся кристаллы отделяют вакуум-фильтрацией. Эти кристаллы смешивают с 70 мл метанола, 40 мл ледяной уксусной кислоты и 95 мкл 4-пиридинкарбальдегида и перемешивают в течение 48 ч. После этого добавляют 57 мг цианоборогидрида натрия и перемешивание продолжают в течение 15 ч. Образовавшийся продукт отделяют вакуум-фильтрацией, промывают метанолом и сушат. В результате получают 521 мг амида N-[2-оксо-2Н-1-бензопиран-3-ил]-2-[(4-пиридил)метил]аминобензойной кислоты с температурой плавления 195-197°С.
Пример 2
Амид N-[6-хлориндазол-5-ил]-2-[(4-пиридил)метил]аминобензойной кислоты
194 мг (0,85 ммоля) 2-(4-пиридилметил)аминобензойной кислоты смешивают в 8 мл диметилформамида с 283 мг (1,69 ммоля) 5-амино-6-хлориндазола. К этому раствору в атмосфере аргона и без доступа влаги добавляют 215 мг (2,13 ммоля) N-метилморфолина и 386 мг (1,02 ммоля) гексафторофосфата O-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония. Эту смесь перемешивают в течение 4 ч при комнатной температуре, после чего разбавляют приблизительно 40 мл воды и трижды экстрагируют этилацетатом порциями по 30 мл. Объединенную органическую фазу промывают водой, сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с использованием в качестве элюента смеси метиленхлорид/этанол в соотношении 10:1. В результате получают 97 мг (30,2% от теории) амида N-[6-хлориндазол-5-ил]-2-[(4-пиридил)метил]аминобензойной кислоты с температурой плавления 222,8°С.
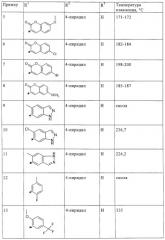
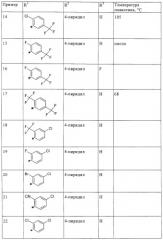
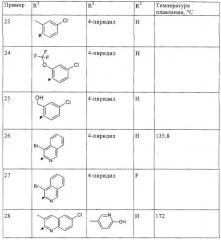
По аналогичной методике получают также следующие соединения формулы
Ниже на примерах по применению более подробно поясняются биологическое действие предлагаемых в изобретении соединений с селективными свойствами и их применение.
Использовавшиеся в опытах растворы
Исходные растворы:
исходный раствор А: 3 мМ АТФ в воде, рН 7,0 (-70°С),
исходный раствор Б: g-33Р-АТФ 1 мКи/100мкл,
исходный раствор В: поли(Glu4Туr) 10 мг/мл в воде.
Раствор для разведений:
растворители субстратов: 10 мМ ДТТ, 10 мМ хлорид марганца, 100 мМ хлорид магния,
раствор фермента: 120 мМ трис/HCl, рН 7,5, 10 мкМ оксид натрийванадия.
Пример по применению 1
Подавление активности киназы KDR и FLT-1 в присутствии соединений по изобретению
В сужающийся по концам титрационный микропланшет (без связывания протеина) добавляют 10 мкл питательной смеси (исходный раствор А объемом 10 мкл АТФ + 25 мкКи g-33Р-АТФ (примерно 2,5 мкл исходного раствора Б) + исходный раствор В: 30 мкл поли(Glu4Туr) + 1,21 мл растворителя субстратов), 10 мкл раствора ингибитора (соединения в соответствии с разведениями, в качестве контроля служит 3%-ный раствор ДМСО в растворителе субстратов) и 10 мкл раствора фермента (11,25 мкг исходного раствора фермента (киназы KDR или FLT-1), разведенного при 4°С в 1,25 мл раствора фермента). Указанные ингредиенты тщательно перемешивают и в течение 10 мин инкубируют при комнатной температуре. Затем добавляют 10 мкл стоп-раствора (250 мМ ЭДТК, рН 7,0), перемешивают и 10 мкл раствора переносят на фосфоцеллюлозный фильтр типа Р 81, после чего несколько раз промывают в 0,1-молярной фосфорной кислоте. Фильтровальную бумагу сушат, покрывают слоем Meltilex и с помощью микросчетчика бета-частиц измеряют радиоактивность.
IC50-значения представляют собой величины, определяемые по концентрации ингибитора, необходимой для подавления встраивания фосфата на 50% от его встраивания в отсутствие ингибитора, за вычетом контрольного значения, полученного в результате слепого опыта (реакция, прекращенная с помощью ЭДТК).
Результаты ингибирования киназы IC50 в мкМ представлены в нижеследующей таблице.
Пример по применению 2
Опыт по определению ингибирования киназной активности выделенного рецептора C-Kit
Исходные растворы:
растворители на 10 порций: 400 мМ трисHCl, рН 7,5; 10 мМ ДТТ, 10 мМ хлорид марганца, 100 мМ хлорид магния, полиэтиленгликоля 20000;
ингибиторы: 2 мМ в диметилсульфоксиде;
исходный раствор субстратов: 3 мг/мл поли(Glu4Туr)n Sigma P275 в воде, замороженные компоненты;
исходный раствор АТФ: 37,5 мМ АТФ в воде с рН, установленным на 7,5, и замороженные компоненты;
100-кратный раствор ванадата: 1 мМ ванадат натрия в воде;
стоп-раствор: 250 мМ этилендиаминтетрауксусная кислота (ЭДТК), рН 7,0;
промывочный раствор для фильтра: 0,5%-ная фосфорная кислота.
Растворы для анализа:
растворы субстратов для 125 анализов:
10 мкл АТФ (37,5 мкМ), 25 мкКи γ33Р-АТФ (˜+2,5 мкл раствора Amersham redivue solution) и 10 мкл поли(glu, tyr) смешивают с 1,23 мл растворителя (однократно);
раствор ингибитора:
соединения растворяют в растворителе (однократно), доводя до требуемой концентрации;
раствор фермента:
соответствующий препарат фермента растворяют с помощью растворителя (однократно) до требуемой концентрации, доводя объем до 1,24 мл, после чего добавляют 12,5 мкл раствора ванадата натрия.
Анализ
Компоненты переносят на титрационный микропланшет с круглыми или мелкоточечными лунками в следующей последовательности: 10 мкл ингибитора в трехкратной конечной концентрации и 10 мкл смеси субстратов, и после их смешения инициируют реакцию добавлением 10 мкл препарата фермента.
Смесь инкубируют в течение 10 мин и затем инкубацию прекращают за счет добавления 10 мкл стоп-раствора. Далее 10 мкл обработанной таким путем смеси переносят на фосфоцеллюлозный фильтр, промывают в фосфорной кислоте, затем сушат, после чего расплавляют в сцинтилляторе mentilex и проводят измерения.
| Пример | KDRIC50 (мкмоль/л) | C-Kit IC50(мкмоль/л) |
| 1 | 0,003 | 6 |
| 2 | 0,2 | >10 |
| 3 | 0,03 | 8 |
| 4 | 0,03 | >10 |
| 5 | 0,01 | >10 |
| 6 | 0,2 | 10 |
| 7 | 0,2 | >10 |
| 9 | 0,04 | 10 |
| 10 | 0,01 | >10 |
| 11 | 1 | >10 |
| 13 | 0,05 | 5 |
| 14 | 0,001 | 5 |
| 15 | 0,002 | 2 |
| 17 | ОИ | >10 |
| 26 | 0,001 | 2 |
| 28 | 0,05 | 0,5 |
| 29 | 0,2 | >10 |
| 30 | 0,02 | 10 |
| Примечание: ОИ означает "отсутствие ингибирования". |
1. Соединения общей формулы I
в которой
R1 представляет собой группу
где * обозначает точку присоединения,
R4 обозначает фтор, хлор, бром, -CF3, -N=C, СН3-, -OCF3 или -CH2OH,
R5 обозначает хлор, бром или ОСН3,
R6 обозначает -СН3 или хлор,
R7 обозначает СН3 или хлор,
R8 обозначает СН3, фтор, хлор или CF3,
R2 представляет собой пиридил или группу
и R3 представляет собой водород или фтор,
а также их таутомеры, Е-изомеры или Z-изомеры, рацематы, энантиомеры и соли.
2. Лекарственное средство, обладающее ингибирующим действием в отношении киназы KDR и FLT, содержащее в своем составе, по меньшей мере, одно соединение по п. 1 и фармацевтически приемлемый носитель.
3. Лекарственное средство по п. 2, обладающее ингибирующим действием в отношении киназы KDR и FLT и предназначенное для лечения опухолей, псориаза, артрита, такого, как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких, как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких, как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжения трансплантатов и гломерулопатия, фиброзных заболеваний, таких, как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза и повреждений нервной ткани, для подавления повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после использования механических устройств, предназначенных обеспечить проходимость сосудов, таких, например, как стенты.
4. Соединения по п. 1 предназначенные для получения лекарственных средств по пп. 2 и 3.
5. Соединения формулы I по п. 1, отличающиеся тем, что они являются ингибиторами тирозинкиназы KDR и FLT.
6. Соединения общей формулы I по п. 1 в качестве активного вещества, ингибирующего тирозинкиназы KDR и FLT, в составе фармацевтического препарата для энтерального, парентерального и перорального введения.