Соединения, способ их получения, применение, фармацевтическая композиция
Иллюстрации
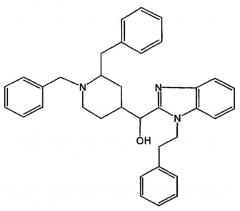
Показать всеИзобретение описывает соединения общей формулы I /значения радикалов см. в формуле изобретения/, являющиеся новыми антагонистами рецептора гистамина. Предпочтительным соединением является 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-он, или его соли, изомеры и N-оксиды. Соединения полезны для предотвращения и лечения повышенного черепного давления (ICP) и/или вторичной ишемии, вызываемых черепно-мозговой травмой. 9 н. и 4 з.п. ф-лы, 5 ил., 13 табл.
Реферат
Данное изобретение относится к новому антагонисту рецептора гистамина и применению антагониста рецептора гистамина для снижения внутричерепного давления (ICP), в частности для предотвращения и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, например, черепно-мозговой травмой, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга.
TBI представляет серьезную проблему в развитых странах. В США каждый год около 500000 человек получают черепно-мозговые травмы, которые являются достаточно тяжелыми и требуют госпитализации. Указанные травмы сопровождаются высокой смертностью, при этом примерно у 80000 человек с травматическим повреждением головного мозга жизненно важные функции не восстанавливаются в течение всей последующей жизни, у 5000 человек возникает эпилепсия и 2000 человек постоянно находятся в вегетативном состоянии. В настоящее время TBI является главной причиной смерти и инвалидности у молодежи, и затраты на лечение таких травм составили в 1989 г. более 25 миллиардов долларов.
Первичное необратимое повреждение после черепно-мозговой травмы включает кровоизлияние, контузию, некроз нервных клеток и диффузное повреждение аксонов. Подобное повреждение в сочетании с возможным угнетением сердечно-сосудистой деятельности и дыхания может вызвать острые вторичные поражения, включающие отек (поражающий кровеносные сосуды и/или клетки), вторичное кровотечение, изменение объема церебральной крови (CBV), нарушение ауторегуляции церебрального кровотока (CBF) и ишемию. Отек, кровотечение и повышение CBV увеличивают общий объем головного мозга и вследствие этого внутричерепное давление (ICP). Это в свою очередь может привести к дальнейшему развитию ишемии, инфаркта и в тяжелых случаях к образованию грыжи ствола мозга с возможным острым угнетением дыхания и летальным исходом. Поэтому лечение в случае TBI должно быть направлено на прерывание последовательности патологических явлений, уменьшение объема головного мозга и снижение внутричерепного давления. Целью лекарственного лечения является также предотвращение опасного для жизни вторичного повышения внутричерепного давления, что часто происходит, например, после острой фазы травмы или восстановления сердечной деятельности.
В настоящее время клинические средства снижения внутричерепного давления весьма ограничены. Стандартные схемы лечения включают хирургическое дренирование желудочков головного мозга, поддержание нормального кровяного давления, вливание маннита, гипервентиляцию легких и введение высоких доз барбитурата. Побочные эффекты нехирургических методов лечения включают ишемию головного мозга, вредное воздействие на внутричерепное давление и повышенный риск бактериальных инфекций и сепсиса. Кроме того, различные соединения, обладающие отличительными механизмами воздействия (например, антагонистическое воздействие на брадикинин и кальций, ингибирование окислительного стресса, блокада рецепторов глутамата и противоэпилептическое воздействие), прошли II и III стадии клинических испытаний или все еще находятся на стадии исследования (причем основное внимание уделяется общему результату, а не ICP). До настоящего времени не было получено разрешение на применение соединения для экстренного лечения внутричерепного давления (K.K. Jain, Chapter 4: Neuroprotection in Acute Trauma, 'Neuroprotection in CNS Disorders: Commercial Opportunities'. A Jain PharmaBiotech Report: 65-73, 2000). Совершенно очевидно, что существует потребность в фармацевтических препаратах и/или методах лечения повышенного внутричерепного давления (ICP) и/или вторичной ишемии, вызываемых, в частности, черепно-мозговой травмой, более конкретно травматическим повреждением головного мозга (TBI).
Авторы настоящего изобретения обнаружили, что производные замещенного тетрациклического имидазола общей формулы (I) обладают антагонистической активностью в отношении Н1- и/или Н2-рецепторов гистамина. Кроме того, установлено, что указанные соединения особенно пригодны для снижения внутричерепного давления (ICP), в частности, для профилактики и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, в частности, черепно-мозговой травмой, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга.
Кроме того, авторы настоящего изобретения обнаружили, что соединения, являющиеся антагонистами Н1- и/или Н2-рецепторов гистамина (обычно называемые антигистаминными средствами), пригодны также для снижения внутричерепного давления (ICP), в частности, для предотвращения и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, в частности, травмой головного мозга, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга.
Отличительной особенностью всех соединений является то, что они способны быстро снижать внутричерепное давление при введение в кровоток млекопитающего, в частности, при внутривенном введении. Весьма полезным и очень важным фактором является то, что, снижая ICP, указанные соединения оказывают незначительное воздействие или вообще не воздействуют на кровяное давление, в частности, такие соединения не снижают кровяное давление, что является наиболее желательным свойством потенциального лекарственного средства.
До настоящего времени не были получены антагонисты Н1- и/или Н2-рецепторов гистамина, предназначенные для снижения ICP, в частности, для снижения ICP после травмы. Mohanty et al., in Journal of the Neurological Sciences, 1989, 90:87-97 установили, что гистамин играет определенную роль в образовании вызванного травмой отека головного мозга. Повышение содержания воды в головном мозге и уровней гистамина в плазме и головном мозге предотвращали путем предварительного введения циметидина, являющегося антагонистом Н2-рецептора гистамина. Однако мейпирамин (антагонист Н1-рецептора гистамина) не вызывал снижения повышенного содержания воды в головном мозге, при этом уровни гистамина в плазме и головном мозге оставались высокими. До сих пор не было исследовано воздействие антагонистов гистамина на ICP, в частности, на экстренное снижение повышенного внутричерепного давления после травмы, а также на кровяное давление.
Не ограничивая себя вышеизложенными теоретическими фактами, авторы настоящего изобретения считают, что с учетом того, что антагонисты рецепторов гистамина способны снижать нормальное внутричерепное давление при отсутствии отека мозга, а также того, что антагонисты рецепторов гистамина не влияют или лишь незначительно влияют на кровяное давление, то есть не вызывают эффект, приписываемый периферической вазодилатации, следует признать, что механизм действия указанных антагонистов не сводится к простому уменьшению отека головного мозга и вазодилатации, в частности, к оказанию таких воздействий, которые, как было известно раньше, присущи антигистаминным средствам.
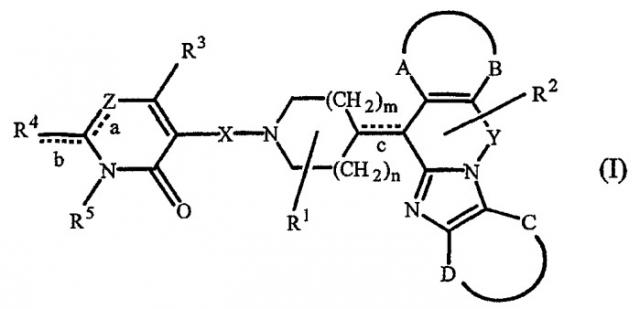
Таким образом, целью настоящего изобретения является создание производных замещенного тетрациклического имидазола общей формулы (I), предназначенных для использования в качестве антагониста гистамина, в частности, в качестве антагониста Н1-рецептора гистамина, более конкретно антагониста Н1- и Н2-рецепторов гистамина,
их фармацевтически приемлемых солей присоединения кислоты или основания, стереохимически изомерных форм и N-оксидов, где
m равно 1 или 2;
n равно 0, 1 или 2;
a, b, c независимо означают простую или двойную связь;
Х означает ковалентную связь или двухвалентный С1-6 алкандиильный радикал, в котором одна или несколько групп -СН2- могут быть необязательно заменены -О-, -S-, -CO- или -NR7-,
где R7 означает водород, алкил, Ar, Ar-алкил, Het, Het-алкил, гидроксиалкил, алкилокси, алкилоксиалкил, алкилоксиалкилоксиалкил, аминоалкил, моно- или диалкиламиноалкил, формил, алкилкарбониламиноалкил, алкилкарбонилоксиалкил, алкилоксикарбонил, алкилоксикарбонилалкил, алкиламинокарбонил, алкиламинокарбонилалкил, гидроксиалкилоксиалкил, аминокарбонил, аминокарбонилалкил, алкилоксикарбонил или алкилкарбонилоксиалкилоксиалкил;
Y означает двухвалентный С1-4 алкандиильный или С2-4 алкендиильный радикал;
Z означает N, когда а означает двойную связь и b означает простую связь, или N-R7, когда а означает простую связь, b означает двойную связь и R7 имеет указанные выше значения;
R1, R2 независимо означают водород, гидрокси, алкил, алкилокси, Ar, Ar-алкил, ди(Ar-)алкил, Het или Het-алкил;
-А-В- независимо означает двухвалентный радикал формулы
| -E-CR8=CR8- | (а-1); |
| -CR8=CR8-E- | (а-2); |
| -CR8=CR8-CR8=CR8- | (а-3); |
где R8 независимо означает водород, галоген, гидрокси, алкил или алкилокси;
Е означает двухвалентный радикал формулы -О-, -S- или -NR7-, где R7 имеет указанные выше значения;
-C-D- независимо означает двухвалентный радикал формулы
| -CR8=CR8-CR8=CR8- | (b-1); |
| -N=CR8-CR8=CR8- | (b-2); |
| -CR8=N-CR8=CR8- | (b-3); |
| -CR8=CR8-N=CR8- | (b-4); |
| -CR8=CR8-CR8=N- | (b-5); |
где R8 имеет указанные выше значения;
R3 означает водород, галоген, гидрокси, алкил, алкилокси, Ar, Ar-алкил, ди(Ar-)алкил, Het или Het-алкил;
R4 означает водород, алкил, амино, алкиламино, Ar-амино, Het-амино, алкилкарбониламино, Ar-карбониламино, Het-карбониламино, алкиламинокарбониламино, Ar-аминокарбониламино, Het-аминокарбониламино, алкилоксиалкиламино, Ar-оксиалкиламино или Het-оксиалкиламино;
R5 означает водород или алкил;
или R4 и R5 вместе могут образовывать двухвалентный радикал формулы
| -M-CR9=CR10- | (с-1); |
| -CR10=CR9-M- | (c-2); |
| -M-CR9R8-CR10R8- | (c-3); |
| -CR10R8-CR9R8-M- | (c-4); |
| -CR8=N-NR7- | (c-5); |
| -NR7-N=CR8- | (c-6); |
| -CR8=CR9-CR10=CR8- | (c-7); |
| -CR8R8-CR9R8-CR10R8-M- | (c-8); |
| -M-CR10R8-CR9R8-CR8R8- | (c-9); |
| -CR8R8-CR8=N-NR7- | (c-10); |
| -NR7-N=CR8-CR8R8- | (c-11); |
где R7 и R8 имеют указанные выше значения;
R9, R10 независимо означают водород, алкил, галоген, галогеналкил;
или R9 и R10 вместе могут образовывать двухвалентный радикал формулы -CR8=CR8-CR8=CR8-, и
М означает двухвалентный радикал формулы -СН2-, -О-, -S- или -NR7-, где R7 имеет указанные выше значения.
В данной заявке Ar означает гомоцикл, выбранный из группы нафтила и фенила, которые, каждый, необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы, включающей гидрокси, галоген, циано, нитро, амино, моно- или диалкиламино, алкил, галогеналкил, алкилокси, галогеналкилокси, карбоксил, алкилоксикарбонил, аминокарбонил и моно- или диалкиламинокарбонил. Ar предпочтительно означает нафтил или фенил, необязательно замещенный 1 заместителем, который независимо выбран из группы, включающей галоген или алкил.
В данной заявке Het означает моноциклический гетероцикл, выбранный из группы, включающей пирролил, пиразолил, имидазолил, фуранил, тиенил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридинил, пиримидинил, пиразинил и пиридазинил, или бициклический гетероцикл, выбранный из группы, включающей хинолинил, хиноксалинил, индолил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензофуранил и бензотиенил; причем каждый моноциклический и бициклический гетероцикл может быть необязательно замещен у атома углерода галогеном, гидрокси, алкилом или алкилокси. Het предпочтительно означает пиридинил, пиразинил или индолил.
В данной заявке алкил означает насыщенный углеводородный радикал с прямой или разветвленной цепью, имеющий 1-6 атомов углерода; циклический насыщенный углеводородный радикал, имеющий 3-6 атомов углерода; циклический насыщенный углеводородный радикал, имеющий 3-6 атомов углерода, присоединенных к насыщенному углеводородному радикалу с прямой или разветвленной цепью, имеющему 1-6 атомов углерода, где каждый атом углерода может быть необязательно замещен галогеном, гидрокси, алкилокси или оксо. Алкил предпочтительно означает метил, этил или циклогексилметил.
В данной заявке галоген является заместителем, выбранным из группы, включающей фтор, хлор, бром и йод; галогеналкил означает насыщенный углеводородный радикал с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, или циклический насыщенный углеводородный радикал, имеющий 3-6 атомов углерода, в котором один или несколько атомов углерода замещены одним или несколькими атомами галогенов. Галоген предпочтительно является фтором или хлором, и галогеналкил предпочтительно является трифторметилом.
Предпочтительную группу соединений составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых -А-В- означает двухвалентный радикал формулы (а-1) или (а-3), где Е означает двухвалентный радикал формулы -О-, -S- или -NR7-, где R7 означает водород, R8 означает водород, -C-D- означает двухвалентный радикал формулы (b-1) или (b-2), где R8 означает водород и Y означает двухвалентный радикал формулы -СН2-, -СН2-СН2- или -СН=СН-.
Другую группу предпочтительных соединений формулы (I) составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых m и n, оба равны 1.
Другую группу предпочтительных соединений формулы (I) составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых R1 и R2 независимо означают водород, алкил, Ar-алкил, Het или Het-алкил.
Еще одну группу предпочтительных соединений формулы (I) составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых Х означает двухвалентный радикал формулы -СН2-СН2- или -СН2-СН2-СН2-.
Еще одну группу предпочтительных соединений формулы (I) составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых R3 означает водород или алкил, Z означает N-R7, где R7 означает водород или алкил, а означает простую связь и b означает двойную связь, и R4 и R5 вместе образуют двухвалентный радикал формулы (с-1), (с-3), (с-5), (с-7), (с-8) или (с-10), где R7 и R8 означают водород.
Еще одну группу предпочтительных соединений формулы (I) составляют соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, в которых R3 означает водород или алкил, Z означает N-R7, где R7 означает водород или алкил, а означает простую связь и b означает двойную связь, R4 и R5 вместе образуют двухвалентный радикал формулы (с-1), (с-3), (с-5), (с-7), (с-8) или (с-10), где R7 и R8 означают водород и R9 и R10 вместе образуют двухвалентный радикал формулы -CR8=CR8-CR8=CR8-, где R8 означает водород.
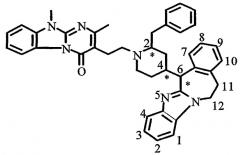
В частности, наиболее предпочтительным является соединение 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-он, его фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды.
Фармацевтически приемлемые кислотно-аддитивные соли включают терапевтически активные нетоксичные кислотно-аддитивные соли, которые могут образовывать соединения формулы (I). Указанные кислотно-аддитивные соли можно получить, обрабатывая основную форму соединений формулы (I) соответствующими кислотами, например, неорганическими кислотами, такими как галогенводородная кислота, в частности, хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота; органическими кислотами, такими как уксусная кислота, гидроксиуксусная кислота, пропановая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, цикламиновая кислота, салициловая кислота, п-аминосалициловая кислота и памовая кислота.
Соединения формулы (I), содержащие кислотные протоны, могут быть также превращены в терапевтически активные нетоксичные основно-аддитивные соли в результате обработки соответствующими органическими и неорганическими основаниями. Соответствующие основные соли включают, например, соли аммония, соли щелочных и щелочноземельных металлов, в частности, соли лития, натрия, калия, магния и кальция, соли с органическими основаниями, такие как соли бензатина, N-метил-D-глюкамина, гибрамина, и соли с аминокислотами, такими как аргинин и лизин.
И наоборот, указанные кислотно- или основно-аддитивные соли могут быть превращены в свободные формы в результате обработки соответствующим основанием или кислотой.
Термин "аддитивная соль" в значении, используемом в данной заявке, означает также сольваты, которые могут образовывать соединения формулы (I), и их соли. Такими сольватами являются, например, гидраты и алкоголяты.
Среди кислотно-аддитивных солей наиболее предпочтительным соединением является гидрат (1:1) (Е)-2-бутендиоата 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-она (2:3), включая все стереоизомерные формы указанного соединения.
Особенно предпочтительными соединениями являются (А)[(2α,4β)(А)]-энантиомер, (В)[(2α,4β)(А)]-энантиомер и смесь указанных энантиомеров соединений 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-β][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-она и гидрата (1:1) (Е)-2-бутендиоата 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-β][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-она (2:3).
N-оксиды соединений формулы (I) являются соединениями формулы (I), в которых один или несколько атомов азота окислены в так называемые N-оксиды, в частности, такие N-оксиды, в которых один или несколько атомов азота пиперидинильного радикала в формуле (I) представляют собой N-окислен.
Термин "стереохимические изомерные формы" в используемом значении означает все возможные изомерные формы, которые могут иметь соединения формулы (I). За исключением особо оговоренных случаев, данное химическое обозначение соединений включает смесь всех возможных стереохимически изомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители двухвалентных циклических (частично) насыщенных радикалов могут иметь цис- или транс-конфигурацию. Соединения, включающие двойные связи, могут иметь Е- или Z-стереохимическую структуру в положении указанной двойной связи. Совершенно очевидно, что стереохимически изомерные формы соединений формулы (I) входят в объем данного изобретения.
В соответствии с условными обозначениями номенклатуры CAS при наличии в молекуле двух стереогенных центров известной абсолютной конфигурации идентификатор R или S присваивается (на основе правила последовательности Кана-Инголда-Прелога) хиральному центру с наименьшим номером, который является центром отсчета. Для обозначения конфигурации второго стереогенного центра используют относительные идентификаторы [R*,R*] или [R*,S*], где R* всегда определяется как центр отсчета, [R*,R*] обозначает центры с одинаковой хиральностью и [R*,S*] обозначает центры с разной хиральностью. Например, если хиральный центр с наименьшим номером в молекуле имеет S-конфигурацию и второй центр имеет R-конфигурацию, идентификатор стереоизомера должен определяться как S-[R*,S*]. При использовании символов "α" и "β": положение заместителя с наивысшим приоритетом в положении асимметричного атома углерода в кольцевой системе, имеющей наименьший номер кольца, всегда условно находится в положении "α" средней плоскости, определяемой кольцевой системой. Положение заместителя с наивысшим приоритетом в положении другого асимметричного атома углерода в кольцевой системе относительно положения заместителя с наивысшим приоритетом в положении атома отсчета обозначается символом "α", если указанный заместитель находится с той же стороны средней плоскости, определяемой кольцевой системой, или символом "β", если указанный заместитель находится с другой стороны средней плоскости, определяемой кольцевой системой.
Когда связь в положении "с" является простой связью, соединения формулы (I) и некоторые промежуточные соединения имеют по крайней мере два стереогенных центра в своей структуре. Когда R1 не является водородом, моноциклическое N-кольцо в формуле (I) имеет еще один стереогенный центр. Таким образом можно получить 8 стереохимически разных структур.
Соединения формулы (I), полученные описанными ниже способами, можно синтезировать в форме рацемических смесей энантиомеров, которые могут быть отделены друг от друга при помощи методов разделения, известных в данной области. Рацемические соединения формулы (I) можно превратить в соответствующие диастереомерные соли, осуществляя взаимодействие с приемлемой хиральной кислотой. Указанные диастереомерные соли затем разделяют, например, селективной или фракционной кристаллизацией и выделяют из них энантиомеры путем щелочной обработки. Альтернативный метод разделения энантиомерных форм соединений формулы (I) включает применение жидкостной хроматографии с использованием хиральной стационарной фазы. Указанные чистые стереохимически изомерные формы можно также получить из соответствующих чистых стереохимически изомерных форм соответствующих исходных веществ при условии выполнения стереоспецифического взаимодействия. Если необходимо получить специфический стереоизомер, указанное соединение предпочтительно синтезируют стереоспецифическими методами получения. При осуществлении указанных методов преимущественно используют энантиомерно чистые исходные вещества.
Соединения формулы (I) могут также существовать в таутомерной форме. Несмотря на то, что такие формы не отражены в полной мере в приведенной выше формуле, они входят в объем настоящего изобретения. Например, соединения формулы (I), в которой R5 означает Н, могут существовать в соответствующей таутомерной форме.
В объем настоящего изобретения входят также производные соединения (обычно именуемые "пролекарствами") фармакологически активных соединений по данному изобретению, которые расщепляются in vivo с образованием соединений по данному изобретению. Пролекарства обычно (но не всегда) оказывают менее сильное воздействие на рецептор-мишень по сравнению с соединениями, в которые они превращаются в результате расщепления. Пролекарства особенно пригодны в тех случаях, когда химические или физические свойства желаемого соединения затрудняют или делают неэффективным процесс его введения. Например, требуемое соединение может плохо растворяться, плохо переноситься через эпителий слизистой оболочки или иметь нежелательно короткий период полувыведения из плазмы. Пролекарства более подробно рассмотрены в статьях Stella, V.J. et al., "Prodrugs", Drug Delivery Systems, 1985, pp. 112-176, and Drugs, 1985, 29, pp. 455-473.
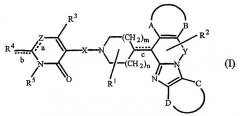
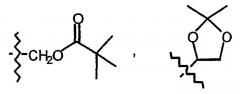
Пролекарственные формы фармакологически активных соединений по данному изобретению обычно представляют собой соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, имеющие кислотную группу, которая этерифицирована или амидирована. К таким этерифицированным кислотным группам относятся группы формулы -COORх, где Rх означает С1-6 алкил, фенил, бензил или одну из нижеследующих групп:
Амидированные группы включают группы формулы -CONRyRz, где Ry означает Н, С1-6 алкил, фенил или бензил и Rz означает -ОН, Н, С1-6 алкил, фенил или бензил.
Соединения по данному изобретению, содержащие аминогруппу, могут быть получены с использованием кетона или альдегида, такого как формальдегид, с образованием основания Манниха. Данное основание гидролизуют при помощи реакционной кинетики первого порядка в водном растворе.
Соединения формулы (I) можно получить, выполняя последовательность стадий, каждая из которых известна специалисту в данной области. Получение указанных соединений описано в одновременно рассматриваемой заявке, которая включена в данное описание изобретения в качестве ссылки.
Помимо снижения внутричерепного давления (ICP) соединения формулы (I) и их производные пригодны также для лечения других заболеваний, обусловленных Н1- и Н2-рецепторами гистамина, в частности, для иммуномодуляции у млекопитающих, подавления повышенной чувствительности и/или воспалительных реакций, лечения и предотвращения аллергических заболеваний, таких как ринит, крапивница, астма, анафилаксия и тому подобные, и лечения заболеваний желудочно-кишечного тракта, таких как язвы, диспепсия, разные рефлюксы и тому подобные. Таким образом, данное изобретение относится также к применению антагониста рецептора гистамина формулы (I) и его производных для получения лекарственных средств для иммуномодуляции у млекопитающих, подавления повышенной чувствительности и/или воспалительных реакций, лечения и профилактики аллергических заболеваний и заболеваний желудочно-кишечного тракта.
Другим объектом данного изобретения является новое применение антагонистов Н1- и/или Н2-рецепторов гистамина для экстренного снижения внутричерепного давления (ICP), в частности, повышенного ICP, более конкретно, критически повышенного ICP и/или предотвращения повышения ICP и вторичной ишемии вследствие травмы головного мозга. При этом особенно важно, что антагонисты Н1- и/или Н2-рецепторов гистамина не влияют на кровяное давление или вызывают незначительное понижение или повышение кровяного давления.
В соответствии с данным изобретением антагонисты Н1- и/или Н2-рецепторов гистамина являются соединениями и их производными формулы (I) или известными антагонистами Н1- и/или Н2-рецепторов гистамина, которые образуют обособленную и ограниченную группу лекарственных средств, уже известных в данной области.
До настоящего времени антагонисты Н1-рецептора гистамина обычно использовались для иммуномодуляции у млекопитающих и подавления повышенной чувствительности и/или воспалительных реакций. В частности, антагонист Н1-рецептора гистамина выбран из группы, включающей акривастин, алимемазин, антазолин, астемизол, азатадин, азеластин, бромфенирамин, буклизин, карбиноксамин, каребастин, цетиризин, хлорциклизин, хлорфенирамин, циннаризин, клемастин, клемизол, клоцинизин, клонидин, циклизин, ципрогептадин, дескарбоэтоксилоратидин, дексхлорфенирамин, дименгидринат, диметинден, диметотиазин, дифенгидрамин, дифенилпиралин, доксиламин, эбастин, эфлетиризин, эпинастин, фексофенадин, гидроксизин, кетотифен, левокабастин, лоратидин, меклизин, меквитазин, метдилазин, миансерин, мизоластин, ниапразин, ноберастин, норастемизол, оксатомид, оксомемазин, фенбензамин, фенирамин, пикумаст, прометазин, пириламин, темеластин, терфенадин, тримепразин, трипеленнамин и трипролидин, их производные и смеси двух или более любых вышеуказанных средств.
До настоящего времени антагонисты Н2-рецептора гистамина обычно использовали для лечения млекопитающих, страдающих некоторыми заболеваниями желудочно-кишечного тракта, такими как язвы, диспепсия, разные рефлюксы и тому подобные. В частности, антагонист Н2-рецептора гистамина выбран из группы, включающей ранитидин, циметидин, фамотидин, низатидин, тиотидин, золантидин, их производные и смеси двух или более любых вышеуказанных средств.
Кроме того, антагонисты рецепторов гистамина могут оказывать антагонистическое действие на Н1- и/или Н2-рецепторы гистамина; к таким антагонистам, в частности, относятся ритансерин или соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды.
Несмотря на то, что все соединения вызывают значительное снижение ICP, установлено, что нижеследующие соединения не влияют на кровяное давление или вызывают незначительное понижение кровяного давления: кетотифен, хлорциклизин, прометазин, пириламин, дифенилгидрамин, хлорфенирамин и золантадин.
Для оценки антагонистического воздействия на гистамин соединений по настоящему изобретению могут быть выполнены исследования in vitro с моделированием соответствующих рецепторов.
Для оценки биологической активности соединений по настоящему изобретению могут быть выполнены исследования in vivo. Для этой цели была создана клинически обоснованная модель травматического повреждения головного мозга у крыс (модель закрытой черепно-мозговой травмы) и использована для испытания соединений по данному изобретению (K. Engelborghs et al., Temporal changes in intracranial pressure in a modified experimental model of closed head injury, J. Neurosurg., 89: 796-806, 1998; K. van Rossem et al., Brain oxygenation after experimental closed head injury, Adv. Exp. Med. Biol., 471: 209-215, 1999; K. Engelborghs et al., Impaired autoregulation of cerebral blood flow in an experimental model of traumatic brain injury, J. Neurotrauma, 17(8):667-677, 2000). В одном исследовании повышенное внутричерепное давление вызывали у кроликов, повреждая холодом кору головного мозга.
Антагонисты рецепторов гистамина по данному изобретению, включающие соединения формулы (I) и известные в настоящее время антагонисты Н1-, Н2- и Н1/Н2-рецепторов гистамина, могут быть использованы для получения разных фармацевтических препаратов. В качестве примеров приемлемых композиций можно привести все композиции, обычно используемые для получения лекарственных средств, предназначенных для системного введения. Для получения фармацевтических композиций по данному изобретению эффективное количество определенного соединения, необязательно в форме аддитивной соли, используемого в качестве активного ингредиента, однородно смешивают с фармацевтически приемлемым носителем, который может иметь разные формы в зависимости от формы требуемого препарата. Указанные фармацевтические композиции предпочтительно получают в виде стандартной дозированной лекарственной формы, пригодной, в частности, для перорального или парентерального введения в виде инъекций. Например, при получении композиции в виде дозированной лекарственной формы для перорального введения можно использовать любые фармацевтические среды, такие как, например, вода, гликоли, масла, спирты и тому подобные, в случае жидких пероральных препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазывающие вещества, связывающие вещества, вещества, улучшающие распадаемость, и тому подобные, в случае порошков, пилюль, капсул и таблеток. Благодаря легкости введения таблетки и капсулы являются наиболее предпочтительными дозированными лекарственными формами для перорального введения, в которых используют твердые фармацевтические носители. При получении композиций для парентерального введения в качестве носителя обычно используют стерильную воду, по крайней мере в значительной степени, хотя для улучшения растворимости в композицию могут быть включены другие ингредиенты. Например, можно получить инъекционные растворы, в которых носителем является физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Кроме того, можно получить инъекционные суспензии, в которых могут быть использованы соответствующие жидкие носители, суспендирующие агенты и тому подобные. В объем настоящего изобретения входят также твердые препараты, которые непосредственно перед применением должны быть превращены в жидкие препараты.
Вышеуказанные фармацевтические композиции предпочтительно получают в виде стандартной дозированной лекарственной формы, которая характеризуется легкостью введения и однородностью доз. Стандартная дозированная лекарственная форма в используемом здесь значении представляет физически раздельные формы, используемые в качестве унифицированных доз, причем каждая форма содержит заранее определенное количество активного ингредиента, необходимое для достижения желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких дозированных лекарственных форм являются таблетки (включая таблетки с насечкой или таблетки с покрытием), капсулы, пилюли, пакетики с порошком, облатки, суппозитории, инъекционные растворы или суспензии и тому подобные, а также несколько вышеуказанных форм в одной упаковке, отделенных друг от друга. Для простого и быстрого введения вышеуказанные фармацевтические композиции наиболее предпочтительно получают в виде раствора или суспензии для инъекций или вливаний.
Приведенные ниже примеры иллюстрируют настоящее изобретение, не ограничивая его объем.
Экспериментальная часть
Для некоторых соединений не была экспериментально определена абсолютная стереохимическая конфигурация одного или нескольких стереогенных атомов углерода. В подобных случаях стереохимически изомерная форма, выделенная первой, обозначена как "А", и выделенная второй, обозначена как "В" без дальнейшей ссылки на действительную стереохимическую конфигурацию. Однако указанные изомерные формы "А" и "В" могут быть точно охарактеризованы специалистом в данной области методами, хорошо известными в данной области, такими как, например, дифракция рентгеновских лучей.
Например, для 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-α]бензимидазол-4(10Н)-она можно определить 8 возможных стереохимически изомерных форм, которые представлены ниже:
| ЦИС-формы | (2α,4α)(A) | (A)[(2α,4α)(A)] |
| (B)[(2α,4α)(A)] | ||
| (2α,4α)(B) | (A)[(2α,4α)(B)] | |
| (B)[(2α,4α)(B)] | ||
| ТРАНС-формы | (2α,4β)(A) | (A)[(2α,4β)(A)] |
| (B)[(2α,4β)(A)] | ||
| (2α,4β)(B) | (A)[(2α,4β)(B)] | |
| (B)[(2α,4β)(B)] |
В данном описании изобретения "DMF" (ДМФА) означает N,N-диметилформамид, "DIPE" означает диизопропиловый эфир, "THF" (ТГФ) означает тетрагидрофуран, "MIBK" означает метилизобутилкетон, "DIPA" означает диизопропиламин.
А. Получение промежуточных соединений
Пример А1
а) Получение промежуточного соединения 1
Использовали сухую стеклянную посуду. Смесь хлорида (метоксиметил)трифенилфосфония (0,35 моль) в ТГФ (чистота для анализа) (молекулярные сита) (2 л) перемешивали при -50°С в потоке N2. Затем по каплям добавляют 2,5 M BuLi/гексан (0,35 моль) и смесь перемешивают при -25°С в течение 30 минут. Раствор 1,2-бис(фенилметил)-4-пиперидинона (0,35 моль) в ТГФ добавляли по каплям при -25°С. Смесь оставляли нагреваться до комнатной температуры, перемешивали при комнатной температуре в течение ночи и разлагали водой. Органический растворитель выпаривали. Водный концентрат экстрагировали CH2Cl2. Органический слой отделяли, сушили (MgSO4), фильтровали и растворитель выпаривали. Остаток очищали хроматографией на колонке с силикагелем (элюент: CH2Cl2/СН3ОН, 97,5/2,5). Чистые фракции собирали и