Фосфатные производные фтороксиндолов и способ лечения с их использованием
Иллюстрации
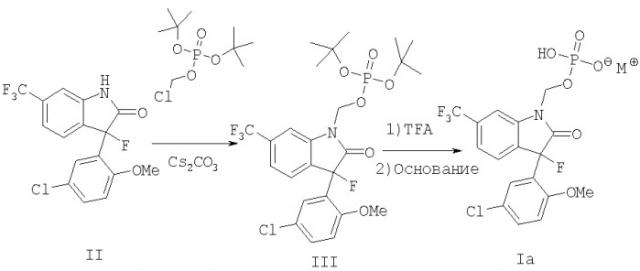
Показать всеИзобретение относится к группе новых соединений формулы (I)
где волнообразная связь обозначает рацемат, (R)-энантиомер или (S)-энантиомер; А представляет собой прямую связь или (С=O); В представляет собой прямую связь, кислород или азот; m имеет значение 0 или 1; n имеет значение 1, 2 или 3; R1 и R2 каждый независимо является водородом или C1-6алкилом, и когда R1 представляет собой водород, R2 может также быть P(O)OR5OR6; R3 и R4 каждый независимо является водородом или C1-4 алкилом; R5 и R6 каждый независимо является водородом, или к их нетоксичным фармацевтически приемлемым солям или сольватам.
Изобретение также относится к способу лечения заболеваний, чувствительных к раскрытию активируемых кальцием калиевых каналов. Технический результат - получение новых биологически активных соединений и способ лечения заболеваний, чувствительных к раскрытию активируемых кальцием калиевых каналов большой проводимости у млекопитающего. 2 н. и 7 з.п. ф-лы, 1 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым фосфатным производным, фтороксиндольным соединениям, которые являются модуляторами активируемых кальцием калиевых каналов (ВК) высокой проводимости и поэтому полезны для защиты нейронных клеток и лечения заболеваний, являющихся результатом дисфункции поляризации клеточной мембраны и проводимости. Настоящее изобретение также обеспечивает способ лечения новыми замещенными производными фтороксиндола, а также их фармацевтические композиции.
УРОВЕНЬ ТЕХНИКИ
В настоящее время инсульт поставлен на третье место при определении причины недееспособности и смертности взрослого населения в США и Европе. За прошедшее десятилетие разрабатывалось несколько терапевтических подходов для снижения связанного с инсультом мозгового повреждения, включая ингибиторы АМРА/кинат, N-метил-D-аспартат (NMDA) и ингибиторы перезахвата аденозина. Целью настоящего изобретения является обеспечение новыми соединениями, которые модулируют калиевые каналы, в частности активируемые кальцием каналы калия (ВК) большой проводимости, которые применимы для ослабления нейронного повреждения при возникновении ишемических состояний во время инсульта.
Калиевые каналы играют ключевую роль в регулировании мембранного потенциала клетки и в модуляции возбудимости клетки. Калиевые каналы непосредственно регулируются напряжением, метаболизмом клетки, ионом кальция и процессами, опосредованными рецептором [Cook, N.S., Trends in Pharmacol. Sciences. - 9, pp.21-28 (1988); and Quast, U. и Cook, N.S., Trends in Pharmacol. Sciences., 10, pp.431-435 (1989)]. Активируемые кальцием каналы (КCa) представляют собой разнообразную группу ионных каналов, которые для активности распределяют зависимость на внутриклеточных ионах кальция. Активность каналов КCa регулируется внутриклеточным [Са2+], мембранным потенциалом и фосфорилированием. На основе проводимости их одиночного канала в симметрических К+ растворах КСа каналы разделяют на три подкласса: большой проводимости (ВК)>150 pS; промежуточной проводимости 50-150 pS; малой проводимости<50 pS (pS обозначает пикосименс, единицу электрической проводимости). Активируемые кальцием каналы калия с большой проводимостью присутствуют во многих легковозбудимых клетках, включая нейроны, кардиальные клетки и различные типы клеток гладкой мышцы [Singer, J.J. and Walsh, J.V., Pflugers Archiv., 408. pp.98-111 (1987); Baro, L, and Escande, D., Pflugers Archiv., 414 (Suppl. 1), pp.S168-S170 (1989); and Ahmed, F. et al, Br. J. Pharmacol, 83, pp.227-233 (1984)].
Ионы калия играют доминирующую роль в контролировании постоянного мембранного потенциала в большинстве легковозбудимых клеток и в поддержании трансмембранного напряжения около K+ потенциала равновесия (Ek), приблизительно равного 90 мВ. Показано, что открытие калиевых каналов изменяет мембранный потенциал клетки к мембранному потенциалу равновесия (Ek) калия, приводя к гиперполяризации клетки. [Cook, N.S., Trends in Phannacol Sciences. 9, pp.21-28 (1988)]. Гиперполяризованные клетки демонстрируют пониженную реакцию на потенциальное повреждение стимулов деполяризации. Каналы BK, которые регулируются и напряжением и внутриклеточным Са2+, действуют так, что ограничивают деполяризацию и проникновение кальция и могут быть особенно эффективны для блокирования разрушительных стимулов. Поэтому гиперполяризация клетки через вскрытие каналов BK может привести к защите нейронных клеток при состоянии ишемии.
Роль калиевых каналов на действие гладкой мышцы человеческого мочевого пузыря описана у S.Trivedi et al. in Biochemical and Biophysical Research Communications (1995), 213. No.2, pp.404-409.
Было сообщено о ряде синтетических и встречающихся в природе соединений с BK открывающей активностью. Avena пирон, извлеченный из avena sativa обыкновенного овса, был идентифицирован как активирующий канал BK, использующий технику двойного слоя липида [РСТ WO 93/08800, опубликованная 13 мая 1993]. Было обнаружено, что плоретин, Флаванойд воздействуют на открытие Са2+-активируемых калиевых каналов в миелинизированных волокнах нерва Xenopus laevis (гладкой шпорцевой лягушки), используемого вне участка тела [Koh, D-S., et ai., Neuroscience Lett., 165. pp.167-170(1994)].
Varia, SA, et al., раскрыл использование фосфонометоксипроизводных (i) в качестве пролекарств гидантоина Фенитоина [J. Pharm. Sci. 73, pp.1068-1073 (1984)].
В РСТ WO 99/33846, опубликованной 8 июля 1999, раскрыты четвертичные аминофосфаты (ii) в качестве пролекарств для аминосодержащих лекарств.
В патенте США 5187173, опубликованном 16 февраля 1993, показано, что фосфонометилсахариновые производные (iii) являются полезными в качестве протеолитических ферментных ингибиторов.
В патенте США 5939405, опубликованном 17 августа 1999, раскрыты фосфатные производные (iv), как полезные пролекарства диарил-1,3,4-оксадиазолонов, которые являются модуляторами активируемых кальцием калиевых каналов (ВК) большой проводимости.
В патенте США 5602169, опубликованном 11 февраля 1997, продемонстрировано, что (3S)-(+)-(5-хлор-2-метоксифенил)-1,3-дигидро-3-фтор-6-(трифторметил)-2Н-индол-2-он (соединение формулы (S)-II) представляет собой модулятор активируемых кальцием калиевых каналов большой проводимости и является полезным для лечения ишемии.
Синтез соединения формулы (S)-II и ее применимость для лечения нарушений, чувствительных к раскрытию калиевого канала, включая мозговую ишемию и травматическое мозговое повреждение, описан в патенте США 5602169. Вследствие низкой растворимости в воде соединения формулы (S)-II, добавки, например, такие как диметилсульфоксид и пропиленгликоль, должны быть применены, чтобы получить растворы соединения формулы (S)-II, пригодные для внутривенной инъекции (Gribkoff, et al., Nature Medicine. 2001, 7, 471-477).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Объектом настоящего изобретения являются новые фосфатные производные 3-фтороксиндолов, имеющие общую формулу
где волнообразная связь означает рацемат, (R)-энантиомер или (S)-энантиомер и А, В, R1, R2, R3, R4, m и n имеют значения, как определено ниже, или их нетоксичную фармацевтически приемлемую соль или его сольват.
Данные фосфаты повышают растворимость в воде 3-фтороксиндолов и, таким образом, уменьшают количество добавок, которые должны быть применены для доставки внутривенной дозы оксиндола. При систематическом введении производные оксиндола преобразуются в свободные системные уровни фтороксиндола. Настоящее изобретение также охватывает фармацевтические композиции, содержащие указанные фосфатные производные и способ лечения нарушений, чувствительных к активности при раскрытии калиевого канала, таких как ишемия, инсульт, конвульсии, астма, эпилепсия, синдром раздражительного кишечника, мигрень, травматическое повреждение мозга, повышенное внутричерепное давление, повреждение спинного мозга, половая дисфункция, отравление монооксидом углерода и недержание мочи.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение охватывает новые фосфатные производные в виде рацемата, (R)-энантиомера и (S)-энантиомера 3-(5-хлор-2-метоксифенил)-1,3-дигидро-3-фтор-6-(трифторметил)-2Н-индол-2-она (соединение формулы II), которые являются мощным вскрывателем активируемых кальцием K+-каналов (BK каналы) большой проводимости и новые соединения, имеющие общую формулу I
где волнообразная связь обозначает рацемат, (R)-энантиомер или (S)-энантиомер;
А представляет собой прямую связь или (С=O);
В представляет собой прямую связь, кислород или азот;
m имеет значение 0 или 1;
n имеет значение 1, 2 или 3;
R1 и R2 каждый независимо являются водородом или C1-6 алкилом, и когда R1 представляет собой водород, R2 может также быть P(O)OR5OR6;
R3 и R4 каждый независимо является водородом или C1-4 алкилом;
R5 и R6 каждый независимо является водородом,
или нетоксичную фармацевтически приемлемую соль или сольват.
Настоящее изобретение также раскрывает способ лечения или профилактики заболеваний, которые опосредуются активируемых кальцием K+ каналов (ВК каналов) большой проводимости у млекопитающего, нуждающегося в этом, включающий введение указанному млекопитающему терапевтически эффективного количества соединения формулы I или его нетоксичной фармацевтически приемлемой соли.
Предпочтительно соединения формулы I являются полезными при лечении ишемии, инсульта, травматического мозгового повреждения и повышенного внутричерепного давления.
Термины "C1-4 алкил" и " C1-6 алкил", как использовано в описании настоящего изобретения и в его формуле (если контекст не указывает иначе), означает прямые или разветвленные цепи алкильных групп, таких как метильная, этильная, пропильная, изопропильная, бутильная, пентильная, гексильная. Предпочтительно эти группы содержат от 1 до 2 атомов углерода. Термин "гетероарил" предназначен, чтобы включать пиридинил, тиофенил, пиримидинил, тиазоил, оксазоил, изоксазоил и им подобные.
Если иначе не определено, термин " гидролизуемой группой сложного эфира" предназначен, чтобы включать группу сложного эфира, которая является физиологически приемлемой и гидролизуемой, такие как C1-6 алкил, бензил, 4-метоксибензил, (низший)-алканоилокси(низший)алкил, например, ацетоксиметил, пропионилоксиметил или пивалоилоксиметил, (низший) алкоксикарбонилокси(низший)алкил, например метоксикарбонилоксиметил или этоксикарбонилоксиметил, (низший)-алкоксикарбонил(низший)алкил, например метоксикарбонилметил или трет-бутоксикарбонилметил, 2-метоксикарбонилоксиэтил, (5-метил-2-оксо-1,3-диоксол-4-ил)метил, дигидроксипропил и им подобные.
Термин "нетоксичная фармацевтически приемлемая соль" предназначен, чтобы включать нетоксичные аддитивно-основные соли с неорганическими и органическими основаниями. Соль соединения I, которая может быть представлена в настоящем изобретении с помощью включает моноанионные, дианионные и трианионные соли, например соли мононатрия, динатрия и тринатрия. Подходящие неорганические основания, такие как основания щелочных и щелочноземельных металлов, включают катионы металлов, таких как натрий, калий, литий, магний, кальций и т.п. Подходящие органические основания включают амины, такие аммонийн, алкиламин, диалкиламин, триалкиламины, тетраалкиламмонийн, пиридин, дибензиламин, этаноламин, N-метилглюкамин, пиперидин, N-метилпиперидин, N-метилморфолин, пролин, глицин, лизин, аргинин, трис(гидроксиметил)аминометан и другие амины, которые могут быть использованы, чтобы образовать соли карбоновой кислоты и фосфорной кислоты.
Вообще, фармацевтически приемлемыми солями по изобретению являются те, в которых противоположный ион не вносит значительный вклад в токсичность или фармакологическую активность соли. В некоторых образцах они имеют физические свойства, которые делают их более желательными для фармацевтических композиций, такие как растворимость, отсутствие гигроскопичности, возможность прессования при формировании таблетки и совместимость с другими ингредиентами, с которыми вещество может использоваться для фармацевтических целей. Соли обычно готовят путем смешивания соединения формулы I, где R1 и R2 представляют собой водород с подобранным основанием, предпочтительно с помощью контакта в растворе, используя избыток обычно применяемых инертных растворителей, таких как вода, эфир, ацетонитрил, диоксан, метиленхлорид, изопропиловый спирт, метанол, этиловый спирт, этилацетат и ацетонитрил. Они могут также быть получены путем обмена на ионообменной смоле в условиях, при которых соответствующий ион соли вещества формулы I заменяется другим ионом в условиях, которые позволяют провести разделение соединений, таких как осаждение из раствора или экстракция в растворитель или элюирование или удержание на ионообменной смоле.
Конкретные соединения по данному изобретению, включая их фармацевтически приемлемые соли, могут существовать как сольватные формы, включая гидратные формы, такие как моногидрат, дигидрат, полугидрат, тригидрат, тетрагидрат и т.п. Продукты могут быть настоящими сольватами, в то время как в других случаях продукты могут просто удерживать дополнительное количество растворителя или быть смесью сольвата плюс некоторого количества добавочного растворителя. Среднему специалисту должно быть понятно, что сольватные формы эквивалентны формам несольватным и предназначены, чтобы быть включенными в границы настоящего изобретения.
Термин "терапевтически эффективное количество" означает общую сумму каждого активного ингредиента композиции, которая является достаточной, чтобы оказать значимое воздействие на пациента, то есть произвести исцеление острых состояний, характеризующихся раскрытием активируемых кальцием K+ каналов большой проводимости или повышением степени исцеления таких состояний. Когда определение применяют к индивидуальному активному ингредиенту, вводимому самому по себе, термин относится к указанному одному ингредиенту. Когда определение применяют к комбинации, термин относится к объединенным количествам активных ингредиентов, которые приводят к терапевтическому эффекту, вводимому ли в комбинации, последовательно или одновременно. Термины "лечат, лечение, обработка" означают профилактику или уменьшение симптомов болезней, повреждения ткани и/или симптомов, связанных с дисфункцией поляризации клеточной мембраны и проводимости. В другом аспекте настоящее изобретение обеспечивает получение растворимого в воде пролекарства соединения, которое находится в виде рацемата, (R)-энантиомера и (S)-энантиомера 3-(5-хлор-2-метоксифенил)-1,3-дигидро-3-фтор-6-(трифторметил)-2Н-индол-2-она, который описан в патенте США 5602169.
Термин пролекарство означает производное активного лекарства, которое превращается после введения в активное лекарственное средство. В особенности, это относится к фосфатным производным лекарственных средств на основе 3-фтороксиндола, которые являются способными к осуществлению гидролиза эфирного остатка или к окислительному расщеплению сложного эфира, так, чтобы перевести лекарственное средство в свободное состояние. Например, фосфат может быть гидролизован ферментами фосфатазы в клетке-хозяине, чтобы получить более активную форму желательного 3-фтороксиндола. Физиологически гидролизуемые группы также служат пролекарствами, которые могут подвергаться гидролизу в организме, чтобы получить на выходе по существу исходное лекарственное средство и, таким образом, растворимые в воде пролекарства предпочтельны для введения исходного лекарственного средства.
В еще одном аспекте настоящее изобретение включает в себя способ лечения или профилактики заболеваний, которые опосредованы раскрытием активируемых кальцием K+ каналов (каналы ВК) большой проводимости у млекопитающего, нуждающегося в этом, включающий введение указанному млекопитающему терапевтически эффективного количества соединения формулы I или его нетоксичной фармацевтически приемлемой соли, сольвата или гидрата. Предпочтительно соединения формулы I являются полезными при лечении ишемии, инсульта, травматического мозгового повреждения и повышенного внутричерепного давления.
Соединения формулы I могут быть приготовлены в соответствии с различными методиками, такими как иллюстрированные в настоящем описании примерами, схемами реакций и их вариациями, которые очевиды среднему специалисту. Различные пролекарственные соединения формулы I могут быть успешно приготовлены из активного вещества лекарственного средства формулы II, которое в свою очередь получают в соответствии с общей методикой, описанной в патенте США 5602169 и используют как исходный материал в способах, иллюстрированных на реакционных схемах 1-9.
РЕАКЦИОННАЯ СХЕМА 1
Получение 3-фтороксидолов формулы Ia иллюстрируется на реакционной схеме 1, где определен в настоящем изобретении. Среднему специалисту должно быть ясно, что если желательно, введение двух молей основания будет давать соединение формулы Ia в виде дианионной соли. Соединение формулы II обрабатывают хлорметилфосфатом и основанием, таким как карбонат цезия в растворителе, таком как ацетонитрил, чтобы получить соответствующее фосфатное промежуточное соединение формулы III. Удаление защитных трет-бутильных групп эффективно осуществляют обработкой кислотой, такой как трифторуксусная кислота, и обработкой полученного фосфата основанием, что дает соединение формулы Ia.
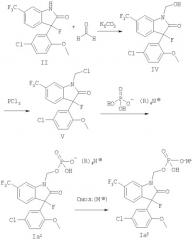
РЕАКЦИОННАЯ СХЕМА 2
Альтернативный путь синтеза соединений формулы Ia, в котором противоположный ион может быть заменен простым способом, изображен на реакционной схеме 2, где R представляет собой C1-4 алкил и имеют значения, как определено в настоящем изобретении. Ацилирование соединения формулы II агентом ацилирования, таким как формальдегид, дает гидроксиметильный аддукт формулы IV. Замена гидроксильной группы галоидирующим агентом, таким как трихлорид фосфора, обеспечивает получение хлорметильного лактама формулы V. Фосфорилирование фосфатом аммония дает фосфат аммония формулы Ia1. Использование ионообменной смолы, которая была предварительно заряжена желаемым противоположным ионом, обеспечивает получение соединения формулы Ia2, где является предпочтительно катионом натрия или калия.
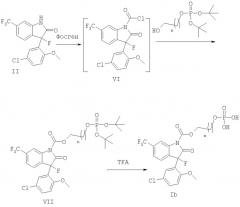
РЕАКЦИОННАЯ СХЕМА 3
Когда имеется необходимость получить соединения формулы Ib, как иллюстрируется на реакционной схеме 3, соединение формулы II ацилируют агентом, таким как фосген, чтобы обеспечить получение хлорформиата формулы VI. Замена уходящей группы в виде хлора гидроксиалкилфосфатом, дает в результате соединения формулы VII, где n имеет значение, как определено в настоящем изобретении. Удаление трет-бутильных групп обработкой кислотой, такой как трифторуксусная кислота, дает на выходе соединения формулы Ib.
РЕАКЦИОННАЯ СХЕМА 4
Получение соединений формулы Ic приведено на реакционной схеме 4, где n имеет значение, как определено в настоящем изобретении. Ацилирование соединения формулы IV хлорформиата обеспечивает получение карбоната формулы VIII. Замена уходящей группы в виде нитрофенола аминоалкильным спиртом дает карбаматы формулы IX, которые могут быть фосфорилированны фосфорамидированием, с последующим окислением фосфора, чтобы обеспечить получение фосфатов формулы X. Удаление трет-бутильных групп обработкой кислотой, такой как трифторуксусная кислота, дает на выходе соединения формулы Ic.
РЕАКЦИОННАЯ СХЕМА 5
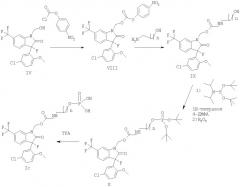
Сложные эфиры формулы Id могут быть получены, как показано на реакционной схеме 5, где n имеет значение, как определено в настоящем изобретении. Замена уходящей группы в виде хлора в соединениях формулы V гидроксиалкильными кислотами, обеспечивает получение сложных эфиров формулы XI, которые могут быть фосфорилированы фосфорамидированием с последующим окислением фосфора, что дает фосфаты формулы XII. Фосфаты формулы Id могут быть получены путем снятия защиты соединений формулы XII обработкой кислотой, такой как трифторуксусная кислота.
РЕАКЦИОННАЯ СХЕМА 6
Получение карбаматов формулы Ie иллюстрируется на реакционной схеме 6. Ацилирование соединений формулы II агентом ацилирования, таким как хлорметилхлорформиат, обеспечивает получение галогенметилкарбаматов формулы XIII. Замена хлора с помощью иодида натрия дает карбаматы иодметила формулы XIV. Замена иода фосфатами дает защищенные фосфаты формулы XV, с которых может быть снята защита обработкой кислотой, такой как трифторуксусная кислота, что дает карбаматы формулы Ie.
РЕАКЦИОННАЯ СХЕМА 7
Фосфоноалкильные эфиры формулы If могут быть получены как иллюстрируется на реакционной схеме 7, где n имеет значения, определенные в настоящем изобретении. Замена уходящей группы в виде хлора в соединении формулы V гидроксиалкилом кислоты обеспечивает получение гидроксиалкильных сложных эфиров формулы XVI. Фосфорилирование спирта фосфорамидированием с последующем окислением фосфора дает соединения формулы XVII, с которых может быть снята защита обработкой кислотой, такой как трифторуксусная кислота, что дает на выходе фосфаты формулы If.
РЕАКЦИОННАЯ СХЕМА 8
Реакционная схема 8 демонстрирует получение пирофосфатов формулы Ig, где R и имеют значения, как определено в настоящем изобретении. Замена уходящей группы в виде хлора в соединениях формулы V пирофосфатом аммония, дает пирофосфаты аммония формулы Ig1, которые могут быть обработаны ионообменной смолой, чтобы обеспечить получение пирофосфатов формулы Ig2.
РЕАКЦИОННАЯ СХЕМА 9
Замена группы хлора в соединениях формулы V фосфатами обеспечивает получение фосфатов алкиламмония формулы Ih1, как изображено на реакционной схеме 9, где R, R1 и М+ имеют значения, как определено в настоящем изобретении. Обработка фосфатов аммония ионообменной смолой дает алкилфосфаты формулы Ih2.
В предпочтительном воплощении изобретения соединения имеют формулу I'
где волнообразная связь означает рацемат, (R)-энантиомер или (S)-энантиомер;
А представляет собой прямую связь или (С=O);
В представляет собой прямую связь или кислород;
m имеет значение 0 или 1;
n имеет значение 1, 2 или 3;
R1 и R2 каждый независимо является водородом или гидролизуемой группой сложного эфира и когда R1 представляет собой водород, R2 может также быть -P(O)OR5OR6;
R3 и R4 каждый независимо является водородом или C1-4 алкилом и
R5 и R6 каждый независимо является водородом или гидролизуемой группой сложного эфира;
или его нетоксичная фармацевтически приемлемая соль или его сольват.
В более предпочтительном воплощении изобретения волнообразная связь означает (S)-энантиомер в соединениях формулы I'.
В другом предпочтительный воплощении изобретения соединения формулы I выбраны из группы, содержащей:
(S)-фосфорной кислоты моно-[3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый] эфир;
(R)-фосфорной кислоты моно-[3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый]эфир;
(S)-3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-карбоновой кислоты 2-фосфоноксипропиловый эфир;
(S)-3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-карбоновой кислоты 2-фосфоноксиэтиловый эфир;
(S)-(2-фосфонооксиэтил)карбаминовой кислоты 3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир;
(S)-фосфоноксиуксусной кислоты 3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир;
(S)-3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-карбоновой кислотаы фосфоноксиметиловый эфир;
(S)-3-фосфоноксипропионовой кислоты 3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир;
(S)-пирофосфорной кислоты [3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир;
(S)-фосфорной кислоты [3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир]метиловый эфир и
(S)-фосфорной кислоты-[3-(5-хлор-2-метоксифенил)-3-фтор-2-оксо-6-трифторметил-2,3-дигидроиндол-1-илметиловый эфир]этиловый эфир или
его нетоксичная фармацевтически приемлемая соль или его сольват.
В другом воплощении настоящее изобретение включает фармацевтические композиции, содержащие, по крайней мере, одно соединение формулы I в комбинации с адъювантом, носителем или разбавителем.
В еще другом воплощении настоящее изобретение относится к способу лечения или профилактики заболеваний, чувствительных к раскрытию калиевых каналов у млекопитающего, нуждающегося в этом, включающему введение указанному млекопитающему терапевтически эффективного количества соединения формулы I или его нетоксичной фармацевтически приемлемой соли, сольвата или гидрата.
В еще другом воплощении настоящее изобретение относится к способу лечения ишемии, конвульсии, эпилепсии, астмы, раздражительного синдрома кишечника, мигрени, травматического мозгового повреждения, повышенного внутричерепного давления, травмы спинного мозга, отравления монооксидом углерода, мужской и женской половой дисфункции, недержания мочи и особенно инсульта у млекопитающего, нуждающегося в этом, включающему введение указанному млекопитающему терапевтически эффективного количества соединения Формулы I или его нетоксичной фармацевтически приемлемой соли, сольвата или гидрата.
Биологическая активность
Каналы калия (K+) являются структурно и функционально различными семействами K+-селективных канальных белков, которые присутствуют в клетках, что определяет их центральную роль для регулирования множества ключевых функций клетки [Rudy, В., Neuroscience. 25, pp.729-749 (1988)]. Хотя они широко распространены как класс, K+ каналы по-разному распределены как индивидуальные члены этого класса или как члены семейства [Gehlert, D.R. и др., Neuroscience. 52, pp.191-205 (1993)]. Вообще, активация K+ каналов в клетках, и особенно в легковозбудимых клетках, таких как нейроны и мышечные клетки, приводит к гиперполяризации клеточной мембраны или в случае деполяризованных клеток - к реполяризации. В дополнение к действию в качестве эндогенного мембранного зажима напряжения, K+ каналы могут обусловливать важные клеточные явления, такие как изменения внутриклеточной концентрации АТФ или внутриклеточной концентрации кальция (Са2+). Центральная роль K+ каналов в регулировании многочисленных функций клетки делает их особенно важными мишенями для терапевтических разработок [Cook, N.S., Potassium channels: Structure, classification, function and therapeutic potential. Ellis Horwood, Chinchester (1990)]. Один класс K+ каналов Са2+-активируемых K+ каналов (ВК или ВК каналы) с большой проводимостью регулируется трансмембранным напряжением, внутриклеточным Са+ и другими разнообразными факторами, такими как состояние фосфорилирования канального белка [Latorre, R. и др., Ann. Rev. Physiol. 51, pp.385-399 (1989)]. Большая отдельная канальная проводимость (обычно >150 pS) и высокая степень специфичности для K+ BK каналов показывает, что небольшое число каналов может глубоко затрагивать мембранную проводимость и клеточную возбудимость. Дополнительно, увеличение открытой вероятности с увеличением внутриклеточного Са2+ указывает на причастность BK каналов к модуляции Са2+-зависимого явления, такого как секреция и мускульное сокращение [Asano, М. и др., J. Pharmacol. Exp.Ther. 267. pp.1277-1285 (1993)].
Вещества, раскрывающие ВК каналы, оказывают их клеточное воздействие путем увеличения вероятности раскрытия этих каналов [МсКау, М.С. и др., J. Neurophvsiol. 71. рр.1873-1882 (1994); Olesen, S.-P, exp.Opin.Invest. Drugs 3, pp.1181-1188 (1994)]. Это увеличение раскрытия всех индивидуальных ВК каналов приводит к гиперполяризации клеточных мембран, особенно в деполяризованных клетках, вызванное существенным увеличением BK-опосредованной проводимости в целой клетке.
Способность соединения формулы II открывать BK каналы и увеличивать направленные наружу (K+) BK-опосредованные потоки целой клетки оценивали в условиях зажима напряжения, определяя их способность увеличивать (mSlo или hSlo) направленного наружу ВК-медиированного потока в клонированном млекопитающем, гетерологически экспрессированного в овоцитах Xenopus [Butler, А. и др., Science, 261. pp.221-224 (1993); Dworetzky, S.I. и др., Mol. Brain Res., 27, pp.189-193 (1994)]. Две используемые ВК конструкции представляют почти структурно почти идентичные гомологичные белки и, как оказалось, являются фармакологически идентичными в испытаниях. Для выделения BK потока из нативного (фон, не-BK) потока использовали специфический и мощный блокирующий ВК канал, блокирующий токсин ибериотоксин (IBTX) [Galvez, А. и др., J. Biol. Chem. 265. pp.11083-11090 (1990)] при супрамаксимальной концентрации (50 нМ). Относительный вклад потока ВК каналов в общий, направленный наружу поток определяли вычитанием потока, остающегося в присутствии IBTX (не-BK поток) из профилей потока, полученных во всех других экспериментальных условиях (контроль, лекарственное средство и промывка). Было определено, что при тестируемой концентрации соединение не производит нативных не-BK потоков в ооцитах. Показано, что соединение Формулы II по крайней мере в 5 ооцитах в концентрации 10 мкМ увеличивает ВК на 170% от контроля IBTX-чувствительного потока. Запись проводили с помощью стандартных способов зажима напряжения с двумя электродами [Stuhmer, W. и др., Methods in Enzymology. 207. pp.319-339 (1992)]; протоколы зажима напряжения состояли из стадий деполяризации продолжительностью 500-750 мсек от держащегося потенциала от -60 до +140 мВ с шагом 20 мВ. Экспериментальная среда (модифицированный раствор Барта) состояла из (в мМ): NaCl (88), NaHCO3 (2.4), KCl (1.0), HEPES (10), MgSO4 (0.82), Ca(NO3)2 (0.33), CaCl2 (0.41); pH 7.5.
Соединение формулы (S)-II или пролекарство Формулы I вводили внутривенно болюсами самцам крыс Sprague-Dawley (n=3 крысы/время) в эквиваленте дозы-мишени 1 мг/кг соединения Формулы (S)-II. В Т=0.25, 1 или 2 часа после дозы собирали образцы общей крови и экстрагировали ацетонитрилом. Экстракты крови проанализировали с помощью LC/MS/MS на уровни соединения Формулы (S)-II. Таблица показывает сравнительные оценки стволовых 0.25-2 часа AUC соединения Формулы (S)-Второй после введения соединения Формулы II или пролекарства Формулы I. Например, как показано в таблице, после введения пролекарств Формулы I, соединение Формулы (S)-II было обнаружено в крови этой модели крыс.
| Уровни соединения (S)-II в крови крыс после введения пролекарства | |
| Пример | AUC (0.25-2 ч) (нг*ч/мл) соединения Формулы (S)-II в стволовой крови |
| Соединение Формулы (S)-II | 261 |
| 5 | 106 |
| 2 | 188 |
| 10 | 135 |
Для определения способности соединений настоящего изобретения уменьшать гибель клеток, обусловленную нейронной ишемией, вызывали стандартную центральную мозговую ишемию путем постоянного перекрывания левой средней мозговой артерии (МСА) и общей сонной артерии (ССА) с одночасовым перекрыванием правой ССА в крысах Wistar. Операции выполняли, используя подвременный подход A. Tamura и др., J. Cereb. Blood Flow Metab., 1, pp.53-60, (1981), и его модификации [K.Osbome и др., J. Neurol Neurosurg. Psychiatry, 50, pp.402-410 (1987) и S. Menzies и др., Neurosurgery. 31., pp.100-107, (1992)].
Соединение Формулы II оценивали в модели центрального паралича, включающей постоянное перекрывание левого МСА (МСАО) и ССА (ССАО) и временного перекрывания правой ССА в крысах Wistar [Gribkoff и др., Nature Med. 7, pp.471-477 (2001)]. Эта процедура приводит к устойчиво большим объемам неокортикального инфаркта, которые измеряют посредством исключения жизненного красителя в последовательных пластинах в мозге через 24 часа после МСАО. В настоящем испытании соединения вводились внутривенным или внутрибрюшинным способом через два часа после перекрывания. Например, в этой модели соединение формулы II значительно уменьшило объем коркового инфаркта, примерно до 28%, при введении внутривенно (0.3 мг / кг) в виде отдельного болюса через два часа после перекрывания средней мозговой артерии по сравнению с контролем в виде инертного вещества.
Для определения способности соединений настоящего изобретения уменьшать количество поврежденных нейронов после травмы головного мозга использовали стандартную модель травмы головного мозга. Модель травмы головного мозга крыс (TBI) использовали для оценки соединения на эффективность изменения или предотвращения вредных эффектов подобной травмы сотрясения мозга. Вообще, крыс в этой модели обезболивали, осуществляли краниотомию (хирургическое вскрытие черепа) и затем в разрез вводили соляной раствор для произведения точного потока увеличенного интракраниального давления (обычно называемое жидкой перкуссионной травмой). Животным вводили соединение в указанных дозах через 15 минут после травмы. Животных умерщвляли через 48 часов после TBI.
Умеренную диффузионную мозговую травму (определенная Mclntosh и др. Neuroscience. 28:233-44 (1989)) вызывали устройством для жидкой перкуссии. Аппарат производит контузию быстрым введением потока соляного раствора [давление ˜от 2.1 до 2.7 атмосфер (атм)] в постоянной продолжительности (21-23 миллисекунды) в закрытую черепную полость. Поток соляного раствора приводит к краткому смещению и деформации основной коры головного мозга. Эта модель, как полагают, имитирует клиническую ситуацию, в которой пациент испытывает подобное сотрясение мозга, характеризующееся краткими неврологическими и системными физиологическими изменениями без серьезного структурного повреждения. Устройство для жидкого вливания производит мозговую травму без непосредственно воздействия на мозг. Распространение мозговой травмы достигается выпуском взвешенного (4.8 кг) металлического маятника с предопределенной высоты (Mclntosh и др., 1989), который ударяет закрытый в конце пробкой поршень Plexiglass цилиндрической емкости, заполненной изотоническим соляным раствором. Различные объемы соляного раствора вводят в закрытую черепную полость, производя поток увеличенного интракраниального давления (ICP). Изменение высоты маятника влияет на величину травмы.
В этом эксперименте пульсацию давления измеряли экстракраниально преобразователем, расположенным в травмирующем устройстве. После анестезии, травмирующий винт сильно связывали с устройством жидкого вливания и вызывали травму умеренной серьезности [от -2.1 до 2.7 атм], основываясь на шкале, установленной Mclntosh и др., 1989. Пульсацию регистрировали на осциллографе, запускаемом фотоэлектрически пуском маятника. После жидкого вливания крышка, созданная винтом травмы, стальной винт и краниопластический цемент были удалены и рану закрывали непроницаемым швом (3-0). Животные, остающиеся под анестезией в течение более 60 секунд после травмы, были немедленно умерщвлены. Крыс оставляли на водной рециркулирующей электрогрелке до нормализации дыхания и они двигались. Животных также умерщвляли и мозг удаляли для оценки отека через 48 часов измерением содержания воды, как описано ранее (Mclntosh и др., 1989).
Ранее было показано, что соединение формулы (S)-II производит существенные сокращения отека в нескольких областях, смежных с зоной воздействия [Cheney и др. J. Cer. Blood Flow & Metab.21:396-403 (2001)]. Соединения Формулы Ia согласно настоящему изобретению производят существенные сокращения отека в смежной коре головного мозга по сравнению с сокращением соединением Формулы (S)-II, когда обоих вводят в эквивалентных молярных дозах в той же самой животной модели травмы головного мозга.
В альтернативном способе серьезность повреждения головного мозга оценивали измерением интракраниального давления (ICP) в различных интервалах после жидкого вливания через 24 часа. Кратко, до вливания жидкости было сделано буровое отверстие 1 мм от стреловидного шва, с центром у правой теменной коры мозга в 5 мм от лямбды, 5 мм от брегмы. После травмы жидким вливанием крышку поверх травмы и краниопластический цемент удаляли. Для достижения адекватных значений ICP, находясь под анастезией, крышку краниотомии ставят в ее первоначальное местоположение после жидкого вливания. Предварительно разрезанную стерильную фольгу также помещают повер