Новые соединения конденсированного имидазола, обладающие свойствами агонистов рецептора св2
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы I или его фармацевтически приемлемым солям, которые обладают свойствами агонистов рецептора СВ2 и могут быть использованы для приготовления лекарственных средств, обладающих аналгезирующим действием, в частности для лечении боли. В соединении формулы I
R1 выбран из группы, состоящей из -(С1-С6)алкила, -(С3-С6)циклоалкила, -(С3-С6)циклоалкил(С1-С6)алкила, -(С2-С6)алкенила, R4 2N(C1-C6)алкила-, R4 2NC(=O)(C1-С6)алкила-, R4O(C1-C6)алкила-, R4OC(=O)(C1-C6)алкила-, R4С(=O)(С1-С6)алкила-, R4C(=O)NR4(C1-C6)алкила-, R4 2NSO2(C1-C6)алкила-, R4 2NC(=O)NR4(C1-C6)алкила-, радикалов фенил(С1-С6)алкил, гетероарил(С1-С6)алкил, гетероциклоалкил(С1-С6)алкил, бициклический гетероарил(С1-С6)алкил; Ar представляет собой фенил или пиридил; R2 представляет собой -(С1-С6)алкил, незамещенный или замещенный по 1-6 атомам углерода одним или более чем одним заместителем фтора, или (С3-С6)циклоалкил; R3 выбран из группы, состоящей из:
, , ,
, , , ,
, ,
и ;
R4 представляет собой группировку, независимо выбранную из группы, состоящей из -H, -(С1-С6)алкила, -(С2-С6)алкенила; группировки R5 независимо выбраны из группы, состоящей из -Н, -(С1-С6)алкила, -(С2-С6)алкенила; группировки R6 независимо выбраны из группы, состоящей из: -Н, -(С1-С6)алкила, -(С3-С6)циклоалкила, -(С2-С6)алкенила, гетероциклила, радикала гетероциклил(С1-С3)алкил, фенила, радикала фенил(С1-С3)алкил, гетероарила, радикалов гетероарил(С1-С3)алкил, бициклический гетероарил и бициклический гетероарил(С1-С3)алкил; R5 и R6 могут объединяться с образованием 5-7-членного гетероцикла; Х выбран из группы, состоящей из -C(R5)2-, -NR5-, С(=O)-, -СН2-СН2-, -СН=СН- и -C(R)(R')-, где R и R' представляют собой (С1-С6)алкил, OR'' или Н, и R'' представляет собой Н; и Y представляет собой СН или азот; при этом гетероциклил или гетероциклоалкил представляет собой насыщенное 5-6-членное кольцо, содержащее от 1 до 2 гетероатомов, выбранных из N и О, которое является незамещенным или замещено -(С1-С6)алкилом; гетероарил представляет собой гетероароматическое 5-6-членное кольцо, содержащее от 1 до 2 гетероатомов, выбранных из N, О и S, которое является незамещенным или замещено группировкой, выбранной из группы, состоящей из -(С1-С6)алкила, нитро, галогена и ацетоксиметила; бициклический гетероарил представляет собой 5-6-членное азотсодержащее кольцо, конденсированное с бензольным кольцом. Изобретение также относится к фармацевтической композиции и способу лечения боли. 4 н. и 5 з.п. ф-лы, 3 табл.
Реферат
Область изобретения
Настоящее изобретение относится к новым соединениям и их солям, представляющим собой агонисты рецептора СВ2. Эти соединения полезны в лечении, в частности для лечения боли. Настоящее изобретение также относится к способам получения новых соединений, содержащим их фармацевтическим композициям и к применению этих соединений в лечении, в частности для лечения боли.
Предшествующий уровень техники
Известны два типа каннабиноидных рецепторов: один экспрессируется преимущественно в центральной нервной системе (СВ1), тогда как другой расположен на периферии и в основном ограничен клетками и тканями, имеющими происхождение от иммунной системы (СВ2) (Abood and Martin Int. Rev. of Neurobio. 39, 197-221 (1996)).
Хотя агонисты рецептора СВ1 и смешанные агонисты высокоэффективны в моделях антиноцицепции у животных, оказалось, что невозможно в какой-либо значительной степени отделить желаемые аналгезирующие действия от нежелательных побочных эффектов в отношении центральной нервной системы (ЦНС). Известно, что эти нежелательные побочные действия в отношении ЦНС опосредованы рецептором СВ1.
Множество сообщений указывают на важную роль СВ2 в патофизиологии. В частности, Munro et. al. f Nature 365 61-65 (1993)] обнаружил, что экспрессия рецептора СВ2 индуцируется в условиях активации клеток иммунной системы. Hanus et. al. [PNAS 96, 14228-14233 (1999)] недавно привел доказательство того, что агонист СВ2 проявляет противовоспалительное и периферическое аналгезирующее действие. Кроме того, Mazzari et. al. [Soc. Neurosci. Abstr. 23 652 (1995)] продемонстрировал, что активация СВ2 ингибирует механическую гипералгезию, ассоциированную с повреждением нервов. Эти результаты указывают на то, рецептор СВ2 представляет собой вызывающую интерес мишень для разработки новых аналгезирующих средств, которые, как можно ожидать, лишены опосредованных СВ1 побочных действий, ассоциированных с обычными каннабиноидными агонистами, например, тетрагидроканнабинолом (ТГК). Кроме того, поскольку расположение рецепторов СВ2 ограничено периферией, можно ожидать, что селективные агонисты СВ2 уменьшают боль без психоактивных побочных действий и обычно осознаваемой возможности злоупотребления, характерных для действующих в отношении центральной нервной системы каннабимиметиков (СВ1) или опиатных лекарств.
Аналгезирующие средства, которые были выявлены и известны из предшествующего уровня техники, обладают множеством недостатков, среди которых можно выделить плохую фармакокинетику и потерю аналгезирующего действия при системном введении.
Подробное описание изобретения
Соединения по данному изобретению определены формулой I, и их фармацевтически приемлемая соль, и диастереоизомеры, и энантиомеры и их смеси:
где
R1 выбран из группы, состоящей из -(С1-С8)алкила, -(С2-С8)алкенила, Р4 2N(C1-C6)алкила-, R4 2NC(=O)(C1-C6)алкила-, R4O(С1-C6)алкила-, R4OC(=O)(C1-C6)алкила-, R4C(=О)(С1-C6)алкила-, R4C(=O)NR4(C1-C6)алкила-, R4 2NSO2(С1-C6)алкила-, R4CSO2NR4(C1-C6)алкила-, R4 2NC(=O)NR4(C1-C6)алкила-, R4 2NSO2NR4(C1-C6)алкила-, арил(С1-С6)алкила-, радикалов ароил(С1-С6)алкил, гетероарил(С1-С6)алкил, гетероароил(С1-С6)алкил, гетероциклоалкил(С1-С6)алкил, бициклический гетероарил(С1-С6)алкил и бициклический гетероароил(С1-С6)алкил;
группировки R1 включают в себя незамещенный -(С2-С8)алкенил и -(С1-С8)алкил, незамещенный или замещенный одной или более чем одной группировкой, независимо выбранной из группы, состоящей из галогена, циано, ацетоксиметила и нитро;
Ar представляет собой возможно замещенную арильную группировку;
R2 представляет собой -(С1-С6)алкил, незамещенный или замещенный (по 1-6 атомам углерода) одним или более чем одним заместителем фтором, или (С3-С6)циклоалкил;
R3 выбран из группы, состоящей из:
и
R4 представляет собой группировку, независимо выбранную из группы, состоящей из -Н, -(С1-С6)алкила, -(С2-С6)алкенила и -(С2-С6)алкинила;
NR4 2 включает в себя соединения, где NR4 2 образует гетероциклильную кольцевую систему, например пиррол, пиперидин, пиперазин или пирролидинон;
группировки R5 независимо выбраны из группы, состоящей из -Н, -(С1-С6)алкила, -(С2-С6)алкенила и гетероциклила;
NR5 2 включает в себя соединения, где NR5 2 образует гетероциклильную кольцевую систему, например пиррол, пиперидин, пиперазин или пирролидинон;
группировки R6 независимо выбраны из группы, состоящей из -Н, -(C1-С6)алкила, -(С2-С6)алкенила и -(С1-С6)алканоила, гетероциклила, радикала гетероциклил(С1-С3)алкил, арила, радикала арил(С1-С3)алкил, гетероарила, радикалов гетероарил(С1-С3)алкил, бициклический гетероарил и бициклический гетероарил(С1-С3)алкил;
R5 и R6 могут объединяться с образованием 5-7-членного гетероцикла, например пиррола, пиперидина, пиперазина, пирролидинона, гомопиперазина или гексаметиленимина;
Х выбран из группы, состоящей из -C(R5)2-, -NR5-, C(=O)-, -CH2-CH2-, -СН=СН-, -О-, -C(R)(R')- и -S(O)n- (где n равно 0, 1 или 2), где R и R' представляют собой (С1-С6)алкил, OR" или Н, и R" представляет собой Н или (С1-С6)алкил; и
Y представляет собой С или N.
Используемый здесь термин "алкил" включает в себя заместители с прямой цепью, с разветвленной цепью и циклические заместители, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, циклопропилметил и циклопентил, и группировки на алкильных цепях могут находиться в любом месте цепи, так что амино(С1-С6)алкил включает в себя 1-аминопропил и 2-аминопропил.
Используемый здесь термин "галоген" включает в себя фтор, хлор, бром и йод.
Термин "арильная группировка" включает в себя ароматические карбоциклы, пятичленные гетероароматические кольцевые системы, шестичленные гетероароматические кольцевые системы и бициклические гетероароматические кольцевые системы.
Ароматический карбоцикл включает в себя фенил и нафтил.
Пятичленная гетероароматическая кольцевая система представляет собой моноциклическую ароматическую кольцевую систему, имеющую пять атомов в кольце, где 1, 2 или 3 атома кольца независимо выбраны из N, О и S.
Предпочтительно пятичленные гетероароматические кольцевые системы выбраны из группы, состоящей из тиенила, фурила, пирролила, имидазолила, тиазолила, оксазолила, пиразолила, изотиазолила, изоксазолила, 1,2,3-триазолила, тетразолила, 1,2,3-тиадиазолила, 1,2,3-оксадиазолила, 1,2,4-триазолила, 1,2,4-тиадиазолила, 1,2,4-оксадиазолила, 1,3,4-триазолила, 1,3,4-тиадиазолила и 1,3,4-оксадиазолила.
Шестичленная гетероароматическая кольцевая система представляет собой моноциклическую ароматическую кольцевую систему, имеющую шесть атомов в кольце, где 1, 2 или 3 атома кольца представляют собой N.
Предпочтительно шестичленные гетероароматические кольцевые системы выбраны из группы, состоящей из пиридила, пиразинила, пиримидинила, триазинила и пиридазинила.
Бициклическая гетероароматическая кольцевая система представляет собой кольцевую систему, имеющую два пяти- или шестичленных гетероароматических кольца, или фенил и пяти- или шестичленное гетероароматическое кольцо, или фенил и гетероциклильное кольцо, или пяти- или шестичленное гетероароматическое кольцо и гетероциклильное кольцо; соединенные посредством слияния колец, причем указанная бициклическая гетероароматическая кольцевая система включает в себя от 8 до 12 атомов в кольце, где 1, 2 или 3 атома кольца независимо выбраны из N, О и S.
Бициклические гетероароматические кольцевые системы предпочтительно выбраны из группы, состоящей из индола, индолина, хинолина, тетрагидрохинолина, изохинолина, тетрагидроизохинолина, 1,4-бензодиоксана, кумарина, дигидрокумарина, бензофурана, 2,3-дигидробензофурана, 1,2-бензизоксазола, бензотиофена, бензоксазола, бензотиазола, бензимидазола, бензотриазола, пирролизидина и хинолизидина.
Гетероциклильная или гетероциклическая группировка представляет собой насыщенную или частично насыщенную кольцевую систему, имеющую от 3 до 7 атомов в кольце, где 1, 2 или 3 атома кольца независимо выбраны из N, О и S.
Гетероциклильные группировки предпочтительно выбраны из группы, состоящей из азиридина, оксирана, тиирана, азетидина, оксетана, тиетана, пирролидина, пирролина, имидазолидина, пиразолидина, диоксолана, сульфолана 2,3-дигидрофуранила, 2,5-дигидрофуранила, тетрагидрофуранила, тиофанила, пиперидина, пиперазина, морфолина, 2,3-дигидропиранила, тетрагидропиранила, 1,4-дигидропиридинила, 1,4-диоксанила, 1,3-диоксанила, диоксанила, гомопиперидинила, гомопиперазинила, 1,3-диоксепана, 4,7-дигидро-1,3-диоксепина и оксида гексаметилена.
Ароматические, гетероароматические, гетероциклильные и бициклические гетероароматические группировки являются незамещенными или замещенными по атомам углерода кольца, предпочтительно группировками, независимо выбранными из группы, состоящей из: галогена, трифторметила, циано, нитро, гидрокси, -NR4 2, -C(=O)OR4, -C(=O)R4, -C(=O)NR4 2, -NR4C(=O)R4, -(С1-С6)алкила, -(С2-С6)алкенила, -(С2-С6)алкинила, -OR4, -SR4, -SO2R4, оксо(=O), имино(=NR4), тио(=S) и оксимино(=N-OR4).
Атомы азота кольца пятичленных гетероароматических, гетероциклильных или бициклических гетероароматических кольцевых систем являются незамещенными или замещенными, если такое замещение химически возможно, без кватернизации указанного атома азота кольца, предпочтительно группировками, независимо выбранными из группы, состоящей из -(С1-С6)алкила и -C(=O)R4.
Заместители -(С1-С6)алкил, -(С2-С6)алкенил и -(С1-С6)алканоил являются незамещенными или замещенными по одному или более чем одному атому углерода группировками, независимо выбранными из группы, состоящей из галогена, гидрокси, -OR4 и -NR4 2.
Понятно, что когда соединения по настоящему изобретению содержат один или более чем один хиральный центр, соединения по данному изобретению могут существовать и могут быть выделены в виде энантиомерных или диастереоизомерных форм или в виде рацемической смеси. Настоящее изобретение включает в себя любые возможные энантиомеры, диастереоизомеры, рацематы или их смеси соединения формулы I, которое действует как агонист СВ2. Синтез оптически активных форм может быть осуществлен с помощью стандартных способов органической химии, хорошо известных из области техники, например путем хирального хроматографического разделения рацемата, путем синтеза из оптически активных исходных веществ или путем асимметрического синтеза.
Также понятно, что некоторые соединения по настоящему изобретению могут существовать в виде геометрических изомеров, например Е- и Z-изомеров алкенов. Настоящее изобретение включает в себя любой геометрический изомер соединения формулы I, которое действует как агонист СВ2. Понятно, что настоящее изобретение охватывает таутомеры соединений формулы I.
Также понятно, что некоторые соединения по настоящему изобретению могут существовать в виде сольватированных, например гидратированных, а также несольватированных форм. Понятно, что настоящее изобретение охватывает все такие сольватированные формы соединений формулы I, которые действуют как агонисты СВ2.
В предпочтительных воплощениях формулы I, если R1 представляет собой R4 2N(C1-C6)алкил-, где оба R4 представляют собой -(С1-С6)алкил, то R3 выбран из группировок (как указано выше) (а), (с), (d), (e), (f), (g), (h) и (k) и возможно (b) и (i) (за исключением того, где R3 представляет собой -(C1-С6)алкил (в особенности, метил, например Рз представляет собой ацетил или ацетамидо)) и (j) (за исключением того, где R5 в обоих случаях представляет собой Н, например R3 представляет собой первичный амин).
Предпочтительные соединения по настоящему изобретению представляют собой соединения формулы I, где:
R1 выбран из группы, состоящей из -(С1-С8)алкила, -(С2-С8)алкенила, радикала арил(С1-С6)алкил, R4 2N(C1-C6)алкила-, R4O(C1-C6)алкила-, радикалов -гетероциклоалкил(С1-С6)алкил (4-8 членного) и гетероарил(С1-С6)алкил;
где арильные и гетероарильные группировки R1 не замещены или замещены -(С1-С6)алкилом, ацетоксиметилом или галогеном;
R2 выбран из группы, состоящей из -СН3, -СН2СН3, -СН(СН3)2, (С3-С5)циклоалкила и CF3;
R3 выбран из группы, состоящей из:
и
Ar представляет собой арильную группировку, незамещенную или замещенную одной или более чем одной группировкой, независимо выбранной из группы, состоящей из (С1-С6)алкила, галогена, трифторметила, циано, нитро, гидрокси и -OR4;
Х выбран из группы, состоящей из -СН2-, -СН2СН2-, -С(=O)-, -S-, -O-, -C(R)(R')- и -N(R)-, где R и R' представляют собой (С1-С6)алкил, OR" или Н, и R" представляет собой Н или (С1-С6)алкил;
когда Ar представляет собой фенил или шестичленную гетероароматическую кольцевую систему, Х расположен на кольце Ar в положении 1, 4 по отношению к группе -O-R2;
когда Ar представляет собой 5-членную гетероароматическую кольцевую систему, Х расположен на кольце Ar в положении 1,3 по отношению к группе -O-R2;
R4 независимо выбран из группы, состоящей из -Н и -(С1-С6)алкила;
R5 независимо выбран из группы, состоящей из -Н, -(С1-С6)алкила и -(С2-С6)алкенила; и
R6 независимо выбран из группы, состоящей из -Н, -(С1-С6)алкила, -(С2-С6)алкенила и гетероарила;
где указанный гетероарил является незамещенным или замещен -(С1-С6)алкилом.
Более предпочтительные соединения по настоящему изобретению представляют собой соединения формулы I, где;
R1 выбран из группы, состоящей из циклопропилметила, этила, пропила, аллила, изопентила, бензила, метоксиэтила, диметиламиноэтила, 4-пиридилметила, 2-пиридилметила, 1-пирролилэтила, 1-морфолиноэтила, циклогексилметила, 2-пирролидилметила, N-метил-2-пирролидилметила, 2-пиперидилметила, N-метил-2-пиперидилметила, 3-тиенилметила, 2-тетрагидрофуранилметила, (2-нитротиофен-5-ил)метила, (1-метил-1Н-имидазол-2-ил)метила, (5-(ацетоксиметил)-2-фуранил)метила, (2,3-дигидро-1 Н-изоиндол-1-ил)метила и 5-(2-метилтиазолила);
R2 выбран из группы, состоящей из -СН3, -СН2СН3, -СН(СН3)2 и CF3;
R4 представляет собой -(С1-С6)алкил;
R5 выбран из группы, состоящей из -Н, -СН3, -СН2СН3, -СН=СН2 и -СН2-СН=СН2;
R6 выбран из группы, состоящей из -СН3, -СН2СН3, -СН=СН2, -CH2-СН=СН2, -СН2-СН2-СН=СН2, -СН2СН(СН3)2 и 5-метил-3-изоксазола;
Ar представляет собой фенил или шестичленную гетероароматическую кольцевую систему, каждый из которых может быть незамещенным или замещенным одной или более чем одной группировкой, независимо выбранной из группы, состоящей из (С1-С6)алкила, галогена, трифторметила, циано, нитро, гидрокси и -OR4;
Х выбран из группы, состоящей из -СН2-, -СН2СН2-, -S-, -O-, -С(=O)-, -C(R)(R')- и -N(R)-, где R и R' представляют собой (С1-С6)алкил, OR" или Н, и R" представляет собой Н или (С1-С6)алкил; и
Х расположен на кольце Ar в положении 1, 4 относительно группы -O-R2.
Наиболее предпочтительные соединения по настоящему изобретению представляют собой соединения формулы I, где:
R2 представляет собой -СН2СН3;
Ar представляет собой незамещенный фенил или пиридил;
Х выбран из группы, состоящей из -СН2-, -СН2СН2-, -S-, -O-, -C(R)(R')- и -N(R)-, где R и R' представляют собой (С1-С6)алкил, OR" или Н, и R" представляет собой Н или (С1-С6)алкил;
Х расположен на кольце Ar в положении 1, 4 относительно группы -O-R2;
и
R4 представляет собой метил.
В некоторых предпочтительных соединениях Х выбран из группы, состоящей из СН(СН3)-, -С(СН3)2-, -СН(ОН)-, -NH- и -N(СН3)-; наиболее предпочтительно СН(СН3).
Авторы изобретения обнаружили, что соединения по настоящему изобретению проявляют избирательное действие в отношении сайта рецептора СВ2 и полезны в облегчении боли, в частности хронической боли, например хронической воспалительной боли, невропатической боли, боли в спине, боли при раке и висцеральной боли. Соединения по настоящему изобретению также полезны в лечении острой боли. В дополнение, соединения по настоящему изобретению полезны при других болезненных состояниях, при которых присутствует или в которые вовлечена дегенерация или дисфункция рецепторов СВ2.
В объем данного изобретения также включены соли соединений формулы I. Как правило, фармацевтически приемлемые соли соединений по настоящему изобретению могут быть получены с использованием стандартных способов, хорошо известных из уровня техники, например путем взаимодействия достаточного количества основного соединения, например алкиламина, с подходящей кислотой, например HCl или уксусной кислотой, с получением физиологически приемлемого аниона. Также возможно получить соответствующую соль щелочного металла (такого как натрий, калий или литий) или щелочноземельного металла (такого как кальций) путем обработки соединения по настоящему изобретению, имеющего подходящий кислотный протон, такого как карбоновая кислота или фенол, одним эквивалентом гидроксида или алкоксида (такого как этоксид или метоксид) щелочного или щелочноземельного металла или подходящего основного органического амина (такого как холин или меглюмин) в водной среде с последующими обычными способами очистки.
Также в объем настоящего изобретения включено применение соединений по настоящему изобретению в лечении.
Новые соединения по настоящему изобретению полезны в лечении, в частности в лечении различных болевых состояний, включающих в себя острую боль, хроническую боль, невропатическую боль, боль в спине, боль при раке и висцеральную боль, но не ограничивающихся ими.
При использовании для лечения у теплокровного животного, такого как человек, агонист СВ2, как правило, вводят в форме обычной фармацевтической композиции, и, как правило, эта композиция может быть в форме, подходящей для перорального или подъязычного введения, например в виде таблетки или капсулы, для парентеральной инъекции (включая внутривенную, подкожную, внутримышечную, внутрисосудистую инъекцию или инфузию), например в виде стерильного раствора, суспензии или эмульсии, для местного введения, например в виде мази или крема, или для ректального введения, например в виде суппозитория. Как правило, вышеописанные композиции могут быть приготовлены обычным образом с использованием обычных носителей. Композиции по настоящему изобретению преимущественно представлены в виде стандартной лекарственной формы.
Терапевтически эффективное количество для практического применения настоящего изобретения может быть определено с использованием известных критериев, включающих в себя возраст, массу и реакцию отдельного пациента, и интерпретировано с учетом заболевания, которое лечат или предотвращают, специалистом в данной области техники.
Также в объем данного изобретения включено применение любого соединения формулы I, указанной выше, для изготовления лекарственного средства для лечения боли.
Дополнительно предложено применение любого соединения формулы I для изготовления лекарственного средства для лечения различных болевых состояний, включающих в себя: острую боль, хроническую боль, невропатическую боль, боль в спине, боль при раке и висцеральную боль, но не ограничивающихся ими
Еще один аспект данного изобретения представляет собой способ лечения субъекта, страдающего от любого из состояний, рассмотренных выше, при котором пациенту, нуждающемуся в таком лечении, вводят эффективное количество соединения формулы I, указанной выше. Кроме того, предложена фармацевтическая композиция, включающая в себя соединение формулы I или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем.
В частности, предложена фармацевтическая композиция, включающая в себя соединение формулы I или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем, для лечения, более конкретно для лечения боли.
Кроме того, предложено применение фармацевтической композиции, включающей в себя соединение формулы I или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем, при любом из состояний, рассмотренных выше. Термин "лечение" в контексте настоящего изобретения означает введение эффективного количества соединения по настоящему изобретению для облегчения или уже существующего болезненного состояния, острого или хронического, или повторяющегося состояния. Это определение также охватывает профилактическое лечение для предотвращения повторяющихся состояний и продолжительное лечение хронических расстройств.
Фармацевтические композиции
Новые соединения по настоящему изобретению можно вводить перорально, подъязычно, внутримышечно, подкожно, местно, интраназально, интраперитонеально, интраторакально, внутривенно, эпидурально, интратекально, интрацеребровентрикулярно и путем инъекции в суставы.
Предпочтительными путями введения являются пероральный, внутривенный или внутримышечный.
Дозировка зависит от пути введения, тяжести заболевания, возраста и массы пациента и других факторов, которые учитываются в норме штатным врачом больницы при определении индивидуального режима и уровня дозировки, наиболее подходящих для отдельного пациента.
Для приготовления фармацевтических композиций из соединений по данному изобретению инертные фармацевтически приемлемые носители могут быть и твердыми и жидкими. Препараты в виде твердой формы включают в себя порошки, таблетки, диспергируемые гранулы, капсулы, крахмальные облатки и суппозитории.
Твердый носитель может представлять собой одно или более чем одно вещество, которое может также действовать в качестве разбавителей, корригентов, солюбилизаторов, смазывающих веществ, суспендирующих агентов, связывающих агентов или разрыхлителей; также это может быть вещество для инкапсуляции.
В порошках носитель представляет собой тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным активным компонентом. В таблетках активный компонент смешан с носителем, обладающим необходимыми связывающими свойствами, в подходящих пропорциях и спрессован в желаемую форму и размер.
Для приготовления композиций суппозиториев легкоплавкий воск, такой как смесь глицеридов жирных кислот и масла какао, сначала плавят и диспергируют в нем активный ингредиент, например, путем перемешивания. Расплавленную гомогенную смесь затем выливают в формы подходящих размеров и оставляют охлаждаться и затвердевать.
Подходящие носители включают в себя карбонат магния, стеарат магния, тальк, лактозу, сахар, пектин, декстрин, крахмал, трагакант, метилцеллюлозу, натрий-карбоксиметилцеллюлозу, легкоплавкий воск, масло какао и тому подобное.
Соли включают в себя фармацевтически приемлемые соли, но не ограничиваются ими. Примеры фармацевтически приемлемых солей в объеме настоящего изобретения включают в себя: ацетат, бензолсульфонат, бензоат, бикарбонат, битартрат, карбонат, цитрат, фумарат, глюконат, глутамат, гидробромид, гидрохлорид, лактат, малеат, манделат, мезилат, фосфат/дифосфат, салицилат, сукцинат, сульфат, тартрат, холин, диэтаноламин, этилендиамин, меглюмин, алюминий, кальций, магний, калий, натрий и цинк.
Примеры фармацевтически неприемлемых солей в объеме настоящего изобретения включают в себя: гидроиодид, перхлорат, тетрафторборат, литий.
Предпочтительные фармацевтически приемлемые соли представляют собой гидрохлориды, сульфаты и битартраты.
Особенно предпочтительными являются соли гидрохлорид и сульфат.
Под термином "композиция" подразумевают препарат активного компонента с веществом для инкапсуляции в качестве носителя, обеспечивающего капсулу, в которой активный компонент (вместе или без других носителей) окружен носителем, который, таким образом, находится с ним в ассоциации. Подобным образом, включены крахмальные облатки.
Таблетки, порошки, крахмальные облатки и капсулы могут быть использованы в виде твердых лекарственных форм, подходящих для перорального введения.
Композиции в виде жидкой формы включают в себя растворы, суспензии и эмульсии. Стерильный водный раствор или раствор вода-пропиленгликоль активных соединений могут быть упомянуты в качестве примера жидких препаратов, подходящих для парентерального введения. Жидкие композиции также могут быть приготовлены в виде раствора в водном растворе полиэтиленгликоля.
Водные растворы для перорального введения могут быть приготовлены путем растворения активного компонента в воде и добавления походящих красителей, корригентов, стабилизаторов и загустителей в соответствии с тем, как требуется. Водные суспензии для перорального применения могут быть приготовлены путем диспергирования тонкоизмельченного активного компонента в воде вместе с вязким веществом, таким как натуральные синтетические смолы, камеди, метилцеллюлоза, натрий-карбоксиметилцеллюлоза и другие суспендирующие агенты, известные из фармацевтической области.
Предпочтительно фармацевтические композиции находятся в виде стандартной лекарственной формы. В такой форме композиция разделена на стандартные дозы, содержащие подходящие количества активного компонента. Стандартная лекарственная форма может представлять собой упакованный препарат, упаковку, содержащую определенные количества препаратов, например упакованные таблетки, капсулы и порошки в пузырьках или ампулах. Стандартная лекарственная форма также может представлять собой капсулу, крахмальную облатку, таблетку саму по себе или может представлять собой подходящее количество любой из этих упакованных форм.
Способы получения
Способ А1
Способ А1 для получения соединений общей формулы I,
при котором осуществляют следующие стадии:
соединения общей формулы II,
где R1, R3 и Y являются такими, как определено для формулы I, можно подвергать взаимодействию с соединениями общей формулы III,
где R2, Ar и Х являются такими, как определено для формулы I, и L представляет собой -ОН или уходящую группу, такую как галогенид, O-тозил или O-мезил. Удобно проводить эту реакцию в инертном растворителе, таком как толуол, при температуре окружающей среды в течение 20 минут. После этого добавляют каталитическое количество концентрированной HCl и смесь нагревают в течение 12 часов при 85°С. Обработку осуществляют посредством водной экстракции, а очистку продукта осуществляют посредством нормальной или обращенно-фазовой хроматографии.
Способ А2
Способ А2 для получения соединений общей формулы II, при котором осуществляют следующие стадии:
соединения общей формулы IV,
где R1, R3 и Y являются такими, как определено для формулы I, можно восстановить до соответствующего анилина (формулы II) путем взаимодействия с водородом при давлении 10-50 ф./кв. дюйм (68,95 кПа -344,75 кПа). Эту реакцию удобно проводить в инертном растворителе, таком как этанол, метанол или тетрагидрофуран, при температуре окружающей среды. Реакцию катализируют с помощью катализатора на основе переходного металла, удобно с помощью 5-10% палладия на тонкоизмельченном углероде.
Способ A3
Способ A3 для получения соединений общей формулы IV, при котором осуществляют следующие стадии:
соединения общей формулы V:
где R1, R3 и Y являются такими, как определено для формулы I, подвергают взаимодействию с первичным амином. Удобно проводить эту реакцию в протонном растворителе, таком как 80% этанол, при температуре 50-100°С. Обработку удобно осуществляют путем водной экстракции, и очистку удобно проводят посредством нормально-фазовой хроматографии.
Способ А4
Способ А4 для получения соединений общей формулы III, при котором осуществляют следующие стадии:
соединения общей формулы VI:
где R2, Ar и Х являются такими, как определено для формулы I, и L представляет собой -ОН или уходящую группу, такую как галогенид, O-тозил или O-мезил, подвергают взаимодействию с галогенирующим агентом, таким как тионилхлорид. Удобно проводить эту реакцию в инертном растворителе, таком как бензол или толуол, при температуре 25-100°С. Обработку удобно осуществляют путем удаления растворителя при пониженном давлении, а очистку удобно производят путем перегонки.
Способ А5
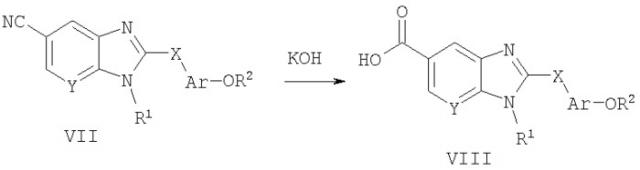
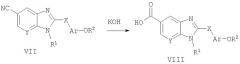
Способ А5 для получения соединений общей формулы VIII, при котором осуществляют следующие стадии:
используя КОН, гидролизуют соединения общей формулы VII (полученные способом А1),
где R1, R2, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше. Эту реакцию легко осуществляют в водной смеси растворителей, такой как 1:1 этанол/вода, при температуре дефлегмации. После нейтрализации продукт удобно выделяют путем фильтрации охлажденной реакционной смеси.
Способ А6
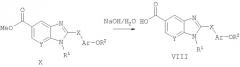
В качестве альтернативы, способ А6 для получения соединений общей формулы VIII, при котором осуществляют следующие стадии:
соединения общей формулы Х (полученные способом А1),
где R1, R2, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше, превращают в соответствующую карбоновую кислоту VIII путем гидролиза эфира Х с использованием водного основания, такого как гидроксид натрия, до соответствующей карбоновой кислоты.
Способ А7
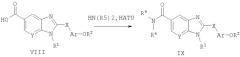
Способ А7 для получения соединений общей формулы IX, при котором осуществляют следующие стадии:
соединения формулы VIII,
где R1, R2, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше, превращают в соответствующий амид путем взаимодействия с первичным или вторичным амином в присутствии кислотного активирующего агента, такого как HATU [гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония], HBTU [гексафторфосфат O-бензотриазол-1-ил)-N,N,N',N'-тетраметилурония] или TBTU [тетрафторборат O-(1Н-бензотриазол-1-ил)-N,N,N',N'-пентаметиленурония]. Эту реакцию легко проводят в полярном апротонном растворителе, таком как диметилформамид (ДМФ), при температуре окружающей среды совместно с третичным амином, таким как триэтиламин или диизопропилэтиламин, который служит в качестве акцептора кислоты. Продукт без труда выделяют путем водной экстракции и очищают путем нормально-фазовой хроматографии.
Способ А8
Способ А8 для получения соединений общей формулы XI, при котором осуществляют следующие стадии:
соединения формулы IX (полученные способом А1 или А7),
где R1, R2, R6, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше, превращают в соответствующий тиоамид (формула XI) путем взаимодействия с P2S5. Эту реакцию легко проводят в пиридине при температуре 100°С. Продукт без труда выделяют путем водной экстракции декантированной части реакционной смеси и очищают путем нормально-фазовой хроматографии.
Способ А9
Способ А9 для получения соединений общей формулы XII, при котором осуществляют следующие стадии:
соединения формулы VII (полученные способом А1),
где R1, R2, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше, каталитически восстанавливают, используя каталитическое количество никеля Ренея в 50% водной муравьиной кислоте. Эту реакцию легко проводят в кислой водной смеси растворителей, такой как 50% водная муравьиная кислота, при 90°С. Продукт удобно выделяют путем фильтрации охлажденной реакционной смеси через подушку из диатомовой земли, концентрирования и очистки посредством нормально-фазовой хроматографии.
Способ А10
Способ А10 для получения соединений общей формулы XIII, при котором осуществляют следующие стадии:
соединения формулы XII,
где R1, R2, R5, Ar, Х и Y являются такими, как определено для формулы I, и полученные общими способами, описанными выше, подвергают восстановительному аминированию с использованием первичного или вторичного амина в присутствии подходящего восстановителя, такого как триацетоксиборогидрид натрия. Эту реакцию удобно проводят в тетрагидрофуране с 1-1,5 эквивалентами уксусной кислоты и 1-1,5 эквивалентами триацетоксиборогидрида натрия при температуре окружающей среды. Продукт удобно выделяют путем разрушения боратного эфирного промежуточного соединения 1н. HCl с последующей водной экстракцией. Концентрирование органического экстракта позволила получить неочищенный продукт, и очистку осуществляют путем нормально-фазовой хроматографии.
Способ А11
Способ А11 для получения соединений общей формулы XIV, при котором осуществляют следующие стадии:
соединения формулы XII,
где R1, R2, R6, Ar и Х являются такими, как определено для формулы I, и полученные общими способами, описанными выше, соединяют с металлоорганическим агентом, таким как реактив Гриньяра, с последующим окислением промежуточного спирта до кетона. Реакцию Гриньяра удобно осуществляют в тетрагидрофуране с шестью эквивалентами магнийорганического галогенида, такого как метилмагнийбромид, при 0°С. Продукт удобно выделяют путем разрушения излишка металлоорганического реактива путем добавления воды с последующей водной экстракцией и концентрированием органического экстракта. Окисление этого промежуточного спирта осуществляют путем взаимодействия с каталитическим количеством (приблизительно 5 мол.%) перрутената тетрапропиламмония (ТРАР) и 1-1,5 эквивалент