Способ прогнозирования прогрессирующего течения хронического гепатита с (развития цирроза печени) путем анализа комбинации полиморфизмов генов цитокинов
Иллюстрации
Показать всеИзобретение относится к области молекулярной биологии и медицинской генетики и может быть использовано в клинической практике при прогнозировании течения хронического гепатита С (ХГС). Предложена предсказательная модель, позволяющая оценить вероятность прогрессирования фиброза печени (развития цирроза) при ХГС. В основу данной модели положено суммирование результатов анализа ДНК пациентов на наличие полиморфизмов генов цитокинов: (-511) С/Т гена IL-1b, (-174) G/C гена IL-6 и (+915) G/C гена TGF-b1. При этом установлено, что генотипы (-511) ТТ гена IL-1b, (-174) СС гена IL-6 и (+915) GC гена TGF-b1 характеризуются выраженным «профибротическим» действием; генотипы (-511) СТ гена IL-1b и (-174) GC гена IL-6 - умеренным «профибротическим» действием; генотипы (-511) СС гена IL-1b, (-174) GG гена IL-6 - протективным действием в отношении развития цирроза печени, а генотип (+915) GC гена TGF-b1 является нейтральным. Применение изобретения позволяет выделить среди больных ХГС группу высокого риска развития цирроза печени, нуждающихся в интенсивной противовирусной, а в перспективе - и в антифибротической терапии. 5 ил., 11 табл.
Реферат
Введение.
Настоящее изобретение относится к области молекулярной биологии и медицинской генетики и может быть использовано при определении прогноза течения хронического гепатита С. Предлагается способ, позволяющий установить предрасположенность к развитию цирроза печени при хроническом гепатите С по результатам тестирования ДНК на носительство определенных полиморфизмов генов цитокинов IL-1b, IL-6 и TGF-b1.
Хронический гепатит С (ХГС) является ведущей формой хронических заболеваний печени с неуклонно прогрессирующим течением и характеризуется значительной межиндивидуальной вариабельностью клинической картины и исходов (Collier J.D., Woodall Т., et al., 2005). Основной причиной морбидности и смертности больных ХГС является цирроз печени (ЦП), скорость формирования которого варьирует от нескольких лет до нескольких десятков лет (Hoofnagle J.H., 2002). Считается, что у 20-30% больных ХГС цирроз печени развивается через 30 лет после инфицирования. Несмотря на то, что к настоящему времени установлено большое число факторов риска прогрессирующего течения ХГС, практикующие специалисты отмечают крайнюю сложность предсказания естественного течения заболевания и его прогноза у конкретного больного. В условиях ограниченной эффективности противовирусной терапии, большого числа нежелательных явлений на фоне лечения и высокой стоимости лекарственных препаратов вопрос об установлении индивидуального риска прогрессирования заболевания до стадии цирроза печени приобретает особую актуальность и диктует необходимость поиска дополнительных предикторов прогрессирования ХГС.
Уровень техники.
К настоящему времени установлен целый ряд факторов риска, ассоциированных с развитием цирроза печени. Условно эти факторы можно подразделить на модифицируемые и немодифицируемые. Среди модифицируемых факторов, влияющих на естественное течение ХГС, наиболее убедительные данные получены в отношении злоупотребления алкоголем, избыточной массы тела, коинфекции вирусами гепатита В и ВИЧ. Из немодифицируемых факторов риска прогрессирования ХГС упоминания заслуживают следующие: большая длительность заболевания, мужской пол и поздний возраст инфицирования. Вместе с тем учет традиционных факторов риска не всегда позволяет надежно предсказать вероятный исход заболевания, что послужило поводом к поиску дополнительных факторов, модифицирующих естественное течение ХГС.
В последние годы особое внимание уделяется изучению генетических факторов риска прогрессирования ХГС. В ряде исследований, посвященных определению клинического и прогностического значения носительства аллельных вариантов гена HFE, установлена взаимосвязь между наличием мутации в этом гене и прогрессирующим течением ХГС (Smith В.С., Gorve J., et al., 1998). Изучалась также взаимосвязь аллельных вариантов генов цитокинов с развитием фиброза при ХГС. Powell E.E. et al. (2000), Gewaltig J. et al. (2002) и Wang H. et al. (2005) установили наличие такой связи между наследуемым полиморфизмом (+915) G/C в гене TGF-bl и прогрессирующим течением ХГС. Показано также, что на естественное течение заболевания может влиять (-511) С/Т полиморфизм в гене IL-1b (Bahr M.J. et al., 2003). Однако исследования, посвященные изучению ассоциации одного полиморфизма с особенностями течения ХГС, имеют ряд недостатков. С одной стороны, результаты работ нередко противоречат друг другу, а с другой - не предоставляют надежных критериев подразделения больных с высоким и низким риском развития цирроза печени. Устранение этих недостатков возможно при исследовании комбинации аллельных вариантов нескольких генов, поскольку при этом происходит суммирование факторов риска, а следовательно, повышается достоверность результатов и предсказательная способность модели.
Наиболее успешной попыткой применения данного подхода для оценки вероятности быстрого развития цирроза при ХГС является работа Richardson M.M. et al. (2005). Авторы исследовали ДНК 149 больных ХГС с медленным и быстрым темпом прогрессирования фиброза по 8 полиморфизмам в 6 различных генах, предположительно ассоциированных с прогрессированием фиброза. Из 6 исследованных генов два гена были связанны с окислительным стрессом (HFE и SOD2), два - с обменом липидов (МТР и АРОЕ) и два имели отношение к иммунному ответу (CCR5 и CTLA4). 6 из 8 исследованных полиморфизмов, для которых была экспериментально подтверждена связь с прогрессирующим развитием фиброза, были использованы в предложенной авторами модели для предсказания вероятного течения ХГС. По данным авторов, 15,2% больных с медленным темпом прогрессирования фиброза и 84,8% больных с быстрым темпом прогрессирования фиброза имели 5 и более из числа аллелей, включенных в предлагаемую модель. Способ прогнозирования быстрого развития фиброза при ХГС, предложенный Richardson et al., является наиболее близким аналогом настоящего изобретения. При всех достоинствах описанной в данной работе модели, она обладает существенным недостатком, который состоит в сложности практического применения, определяемой необходимостью проведения анализа слишком большого числа генов. Очевидно, что это связано со значительными затратами времени и средств. С учетом этого основной задачей настоящего изобретения было создание предсказательной модели прогрессирования фиброза при ХГС, которая, обладая достаточной степенью надежности, основывалась бы на изучении небольшого числа полиморфизмов.
Раскрытие изобретения.
В связи с тем, что ключевую роль в прогрессировании фиброза у больных ХГС играют особенности иммунного ответа организма хозяина на патоген, представлялось целесообразным сосредоточить внимание на полиморфизме генов цитокинов. При этом предполагалось включить в группу полиморфизмов, рекомендуемую для исследования при тестировании ДНК больных ХГС с целью прогнозирования течения заболевания, те из них, которые предварительно будут определены как функционально значимые для быстрого развития фиброза.
Цитокины - группа гормоноподобных белков и пептидов, синтезируемых и секретируемых клетками иммунной системы и другими типами клеток. Основные биологические функции цитокинов связаны с регуляцией развития и гомеостаза иммунной системы, контролем за ростом и дифференцировкой клеток и участием в неспецифических защитных реакциях организма. В свете решаемой задачи особый интерес представляют цитокины, участвующие в таких процессах, как воспаление, регенерация гепатоцитов и фиброгенез, типичными представителями которых, в частности, являются IL-1b, IL-6, IL-10 и TGF-b1. Поскольку считается, что до 50% индивидуальных различий в продукции цитокинов обусловлено наличием полиморфизмов (однонуклеотидных замен в пределах гена), закономерно было ожидать, что полиморфизмы, связанные с изменением продукции названных цитокинов, могут модифицировать естественное течение ХГС и служить маркерами прогрессирующего или доброкачественного течения заболевания.
Известно, что полиморфизм в промоторном участке гена IL-1b в положении (-511) с заменой С на Т приводит к увеличению продукции цитокина в экспериментах in vitro и обусловливает высокую активность воспалительных реакций (Bahr M.J., 2003). В ряде публикаций показана ассоциация данного полиморфизма с формированием цирроза печени у больных ХГС (Bahr M.J., 2003) и развитием гепатоцеллюлярной карциномы (ГЦК) (Tanaka Y., Furuta Т., et al., 2003).
В гене TGF-b1 имеется несколько полиморфных сайтов, наиболее исследованным из которых является однонуклеотидная замена G на С в положении (+915), приводящая к замене Arg на Pro в 25 кодоне и, соответственно, к снижению уровня этого цитокина в сыворотке крови (Wang H., Mengsteab S. et al., 2005). Имеются также данные, что генотип (+915) GG, характеризующийся повышенной продукцией TGF-b1, ассоциирован с развитием фиброза легких и печени (Awad M.R., El-Gamel A., Hasleton P., et al. 1998; Powell Е.Е., Edwards-Smith C.J., et al., 2000). Однако однозначного мнения относительно связи данного полиморфизма с развитием фиброза не существует, поскольку в более поздних работах получены противоположные результаты (Suzuki S., Tanaka Y., Onto E., et al., 2003).
Промоторный регион гена IL-10 содержит три полиморфизма, наиболее изученным из которых является замена G на А в положении (-1082). В ряде исследований было показано, что у лиц с аллелем А в положении (-1082) лимфоциты, стимулированные митогеном, производят меньшее количество противовоспалительного цитокина IL-10 (Lio D., Scola L., Crivello A., et al., 2003), что может приводить к усилению воспалительного процесса и способствовать фиброгенезу (Wang S.C., Ohata M., Schrum L., et al., 1998). До настоящего времени опубликовано очень мало работ по изучению ассоциации данного полиморфизма с прогрессированием фиброза печени, и только в одном исследовании выявлена тенденция к преобладанию (-1082) АА генотипа у больных с быстрым развитием цирроза печени (Knapp S. et al., 2003).
В отношении IL-6 известно, что он является маркером и участником воспалительных процессов, а также регулирует пролиферацию и апоптоз гепатоцитов, однако достоверных данных, свидетельствующих о влиянии данного цитокина или полиморфизмов его гена на течение HCV инфекции, в литературе не имеется. Наиболее изученный полиморфизм в гене IL-6 относится к замене G на С по положению (-174) в промоторном регионе. Известно, что при наличии аллеля G в указанной позиции продукция IL-6 после стимуляции липополисахаридом (ЛПС) увеличивается значительно сильнее по сравнению с начальным уровнем, чем в случае аллеля С (Fishman D., Faulds G. et al., 1998). Кроме того, в некоторых работах приводятся данные, указывающие на то, что (-174) G/C полиморфизм в гене IL-6 коррелирует с индексом массы тела и развитием сахарного диабета 2 типа.
В настоящее время для выявления полиморфных состояний генов используется большое количество разнообразных способов, таких как аллель-специфичная ПЦР, масс-спектрометрия, метод гибридизации, ПЦР в реальном времени. В одном из конкретных воплощений изобретения нами был использован метод полиморфизма длин рестрикционных фрагментов, однако при осуществлении предлагаемого способа может быть применен любой из известных ныне методов, обеспечивающий надежное детектирование точечных замен в последовательности ДНК.
Проведенный нами анализ ДНК у 104 больных ХГС с различными стадиями развития фиброза (примеры 2-5) показал, что
а) в случае полиморфизма (-511) С/Т в гене IL-1b TT генотип примерно в 5 раз чаще выявляется у больных, развивших цирроз печени (15,22%), по сравнению с больными, у которых отмечено медленное прогрессирование фиброза (2,86%), тогда как СС генотип достаточно четко ассоциирован с медленно прогрессирующим течением заболевания;
б) в случае полиморфизма (+915) G/C в гене TGF-b1 гетерозиготный генотип GC в 2 раза чаще выявляется у больных с циррозом печени (19,57%), чем у больных с мягким течением заболевания (8,57%);
в) в случае полиморфизма (-174) G/C в гене IL-6 генотип GG четко ассоциирован с медленной аккумуляцией фиброза и наблюдается у больных с 1 стадией фиброза в 2 раза чаще по сравнению с больными, развившими цирроз печени, а для генотипа СС отмечена явная тенденция к более частому выявлению у больных с циррозом печени (15,21%), чем у больных с благоприятным течением болезни (5,71%);
г) в случае полиморфизма (-1082) G/A в гене IL-10 частота аллелей и генотипов между анализируемыми группами достоверно не различалась.
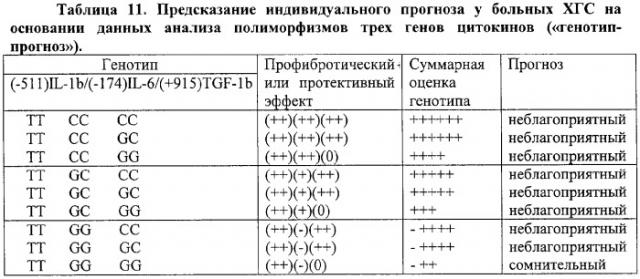
На основании полученных данных как значимые для прогрессирования фиброза при HCV-инфекции были определены полиморфизмы (-511) С/Т гена IL-1b, (+915) G/C гена TGF-b1 и (-174) G/C гена IL-6, анализ комбинации которых и предлагается использовать в новом способе определения предрасположенности больных ХГС к агрессивному течению заболевания. При этом генотипы (-511) ТТ гена IL-1b, (-511) СТ гена IL-1b, (+915) GC гена TGF-b1, (+915) СС гена TGF-b1, (-174) GC гена IL-6 и (-174) СС гена IL-6 рассматриваются как в различной степени "профибротические", генотип (+915) GG гена TGF-b1 рассматривается как нейтральный, а генотипы (-511) СС гена IL-1b и (-174) GG гена IL-6 - как обладающие протективным действием в отношении прогрессирования фиброза. С учетом такого подхода для качественной оценки наследственной предрасположенности к прогрессированию фиброза у больных ХГС по результатам тестирования ДНК на наличие указанных полиморфизмов в генах цитокинов предложена модель, представленная в табл.11.
Таким образом, поставленная задача разработки простого в исполнении и сравнительно недорогого (технический результат) способа прогнозирования предрасположенности к прогрессированию фиброза при HCV-инфекции была решена за счет использования новой комбинации полиморфизмов, определяемых при проведении ДНК-тестирования у пациентов с ХГС. Предложенный метод включает а) получение образца геномной ДНК больного ХГС, б) тестирование указанной ДНК на наличие аллелей, ассоциированных с прогрессированием фиброза, в) оценку результатов и составление заключения о вероятности прогрессирующего течения заболевания, и отличается тем, что ДНК анализируют на наличие полиморфизмов генов цитокинов (-511) С/Т IL-1b, (-174) G/C IL-6 и (+915) G/C TGF-b1, а заключение составляют на основании модели, представленной в табл.11.
Краткое описание чертежей.
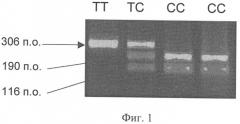
Фиг.1. - Электрофорез в агарозном геле после обработки соответствующего ПЦР-продукта рестриктазой Ava-I ((-511) СС генотип - 2 фрагмента (190 и 116 п.о.); (-511) СТ генотип - 3 фрагмента (306, 190 и 116 п.о.); (-511) ТТ генотип - 1 фрагмента (306 п.о.).
Фиг.2. Электрофорез в агарозном геле после обработки соответствующего ПЦР-продукта рестриктазой Mnl1 ((-1082) GG генотип - 1 фрагмент (141 п.о.); (-1082) GA генотип - 3 фрагмента (141, 92 и 49 п.о.); (-1082) АА генотип - 2 фрагмента (92 и 49 п.о.).
Фиг.3. Электрофорез в агарозном геле после обработки соответствующего ПЦР-продукта рестриктазой SfaN1 ((-174) GG генотип - 2 фрагмента (140 и 58 п.о.); (-174) GC генотип - 3 фрагмента (198,140 и 59 п.о.); (-174) СС генотип - 1 фрагмент (198 п.о.).
Фиг.4. Электрофорез в агарозном геле после обработки соответствующего ПЦР-продукта рестриктазой Bgl1 ((+915) GG генотип - 2 фрагмента (194 и 102 п.о.); (+915) GC генотип - 2 фрагмента (296 и 194); (+915) СС генотип - 1 фрагмент (296 п.о.).
Фиг.5. Частота встречаемости лиц в контрольной группе и среди больных ХГС без (-174) GG и (-511) СС генотипов.
По оси ординат - процент от общего числа индивидуумов данной группы. Незакрашенный столбец - контрольная группа (184 чел.); заштрихованный столбец - больные со стадией фиброза (по Knodell) F1 (35 чел.); столбец с пунктиром - больные со стадией фиброза F4 (46 чел.).
Осуществление изобретения.
Материалы и методы.
1. Критерии отбора больных ХГС для проведения анализа.
В данное исследование были включены больные, имеющие хроническую HCV инфекцию (anti HCV Ab+, HCV RNA+) с гистологически установленной стадией фиброза печени по Knodell. Из общего числа больных с I стадией фиброза печени в данное исследование были включены только те, у которых длительность инфекции составила не менее 10 лет, (считалось, что у этих больных имеет место медленный темп прогрессирования фиброза). В исследование не включались больные с сочетанной патологией печени. Контрольную группу составили здоровые доноры крови (отрицательные анти-HCV и HCV RNA) обоих полов в возрасте 18-45 лет. Все обследованные лица принадлежали к русской этнической группе и не были родственниками.
Диагноз ХГС и ЦПС устанавливался на основании данных анамнеза, клинического обследования, результатов лабораторных методов диагностики, включая вирусологическое исследование (позитивные тесты на антитела к вирусу гепатита С и HCV RNA) и морфологического исследования печени.
2. Выделение ДНК.
Выделение геномной ДНК из образца крови проводили с помощью модифицированного метода с протеиназой К и экстракцией фенол-хлороформом. Для этого в 1,5 мл пробирку (Eppendorf) вносили 700 мкл анализируемого образца крови и 700 мкл ТЕ-буфера (10 мМ Трис-HCl, рН 8,0, 1 мМ ЭДТА) для гемолиза эритроцитов. Процедуру повторяли 2 раза, а затем к клеточному осадку добавляли 400 мкл буфера для протеиназы К, содержащего 200 мкг/мл протеиназы К, после чего инкубировали 4 часа при 60°С на термошейкере с постоянным перемешиванием (850 об/мин). Далее проводили фенол-хлороформную экстрацию ДНК с последующим осаждением 96% этанолом и центрифугированием в течение 10 мин при 10000 об/мин. После серии промывок ДНК элюировали ТЕ буфером (200 мкл). Концентрация выделенной ДНК составляла от 30 до 50 нг/мкл.
3. ПЦР-амплификация и анализ ПЦР-продуктов.
Для определения полиморфизмов в исследуемых генах применялся метод ПДРФ (полиморфизма длины рестрикционных фрагментов). ПЦР проводили в термоциклере Master Cycler (Eppendorf). При этом использовали пробу следующего состава: 100 мМ Tris-HCl, рН 8,3 (25°С), 50 мМ KCl, MgCl2 (концентрация подбиралась индивидуально для каждой пары праймеров), четыре дезоксинуклеозидтрифосфата (по 200 мкМ каждого), Taq-полимераза (0,5 ед./реакцию) и 1-2 мкг геномной ДНК и праймеры (4-8 пмоль/реакцию). Конечный объем реакционной смеси составлял 25 мкл. При постановке ПЦР использовался прием "горячего старта" (Hebert В., Bergeron J., Potworowski E.F., Tijssen P., 1993).
Условия проведения реакции несколько различались в зависимости от определяемого аллеля (см. примеры 2-4).
Рестрикционный анализ продуктов ПЦР проводился с помощью соответствующей рестриктазы в течение 6 часов.
Продукты рестрикции анализировали с помощью электрофореза в агарозном геле, концентрация которого подбиралась в зависимости от длины рестрикционных фрагментов.
4. Статистическая обработка результатов
Данные представляли как среднее арифметическое со стандартным отклонением. Статистическая значимость различий для количественных признаков в случае нормального распределения последних оценивалась с помощью t-критерия. Статистическая значимость различий качественных признаков в сравниваемых группах оценивалась при помощи точного критерия Фишера и критерия χ2. Уровень значимости был принят р<0,05. Для статистической обработки был использован пакет программ Statistica 6.0.
Пример 1. Характеристика группы патентов, отобранных для ДНК-тестирования.
В соответствии с указанными выше критериями было отобрано 104 пациента, из которых 35 имели раннюю (F1) стадию фиброза, а 46 - цирроз печени (F4). Больные с медленным темпом прогрессирования фиброза были статистически достоверно моложе, были инфицированы в более раннем возрасте, имели меньший индекс массы тела и уровень аланиновой аминотрансферазы по сравнению с больными, развившими цирроз печени. В то же время длительность заболевания у них достоверно не отличалась от таковой у больных, развивших цирроз печени (табл.1).
| Таблица 1.Сравнительная характеристика обследованных больных. | |||||||
| Признаки | F1 | F2 | F3 | F4 | всего | ||
| Пол | М | n (%) | 10 (28,57) | 5 (35,71) | 2 (22,22) | 9 (19,57) | 26 (25,0) |
| Ж | n (%) | 25 (71,43) | 9 (64,29) | 7 (77,78) | 37 (80,43) | 78 (75,0) | |
| Возраст | лет | 42±13,6a | 38,6±10,7 | 51,6±11,8 | 57,8±9,5 | ||
| Длительность заболевания | лет | 20,6±7,5b | 13±9 | 20,7±6,0 | 24,6±10,2 | ||
| Возраст инфицирования | лет | 21,7±13,5f | 25,5±15,8 | 30,9±13,0 | 33,0±14,0 | ||
| Индекс массы тела (ИМТ) | кг/м2 | 24,6±4,4c, d | 22,8±2,8 | 27,5±3,4 | 27,6±5,4 | ||
| Аланинамино-трансфераза | U/л | 48,0±34,8e | 95±103,3 | 200±177 | 85,9±59,6 | ||
| а - р=0,004 (между F1 и F2); b - р=0,01 (между F1 и F2); c, d - p=0,01 (между F1 и F4); e - p=0,01 (между F1 и F3); F1, F2, F3, F4 - стадии фиброза по Knodell (I, II, III, IV). |
Пример 2. Определение полиморфизма (-511) С/Т IL-lb.
Геномную ДНК, выделенную из каждого образца крови, подвергали ПЦР-амплификации, как описано в разделе "Материалы и методы".
При проведении ПЦР использовали праймеры 5′-TGG CAT TGA TCT GGT TCA TC-3′ и 5′-GTT TAG GAA TCT TCC CAC TT-3′ и следующие условия: начальная денатурация (94°С, 2 мин) - 1 цикл, денатурация (94°С, 30 сек), отжиг (55°С, 1 мин) и элонгация (74°С, 1 мин) - 32 цикла, заключительная элонгация (70°С, 10 мин) - 1 цикл.
ПЦР-продукт обрабатывали рестриктазой AvaI и анализировали в 2% геле. О наличии в тестируемой ДНК аллеля (-511) С судили по появлению двух фрагментов размером 190 и 116 п.о. (фиг.1). После анализа всех образцов рассчитывали частоту встречаемости аллелей (-511) С и (-511) Т и распространенность генотипов в анализируемых группах. Полученные результаты представлены, соответственно, в табл.2 и табл.3
| Таблица 2.Частота аллелей (-511) С/Т полиморфизма гена IL-1b | ||||||
| Полиморфизм | Аллель | Контроль n=249 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 |
| IL-1b(-511) С/Т | С | 0,647 | 0,814a | 0,714 | 0,722 | 0,685 |
| Т | 0,353 | 0,186 | 0,286 | 0,278 | 0,315 | |
| a - р=0,05 (между F1 и популяцией; критерий Фишера); b - р=0,04 (между F1 и F4; критерий Фишера). | ||||||
| Таблица 3.Распространенность генотипов (-511) С/Т полиморфизма гена IL-1b | ||||||
| Полиморфизм, генотип | Контроль n=249 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 | |
| IL-1b(-511) С/Т) | СС (%) | 101 (40,56) | 23 (65,71)a,b | 7 (50,0) | 4 (44,44) | 24 (52,17) |
| СТ (%) | 120 (48,19) | 11 (31,43) | 6 (42,86) | 5 (55,56) | 15 (32,61) | |
| ТТ (%) | 28 (11,24) | 1 (2,86)c | 1 (7,14) | 0 (0,0) | 7 (15,22) | |
| а - р=0,02 (между F1 и F4; критерий χ2); b - р=0,005 (между F1 и популяцией; критерий χ2); с - р=0,03 (между F1 и F4; критерий Фишера). |
У больных с медленным темпом прогрессирования фиброза аллель С (-511) С/Т полиморфизма выявлялся чаще (0,814), чем во всех других группах, однако различия достигали статистической значимости только в сравнении с контролем (р=0,05). По нашим данным, ТТ генотип более чем в 5 раз чаще выявлялся у больных, развивших цирроз печени (15,22%), по сравнению с больными, у которых отмечено медленное прогрессирование фиброза печени (2,86%) (р=0,05). И наоборот, СС генотип был достаточно четко ассоциирован с медленно прогрессирующим течением заболевания. Низкая встречаемость (-511) ТТ генотипа у больных с медленным темпом прогрессирования фиброза по сравнению с популяционной частотой, а также частотой обнаружения данного генотипа у больных с ЦП свидетельствует о том, что выявление его у больных ХГС является прогностически неблагоприятным.
Пример 3. Определение полиморфизма (-1082) G/A IL-10.
При проведении ПЦР использовали праймеры 5′-ТТС ССС AGG TAG AGC AAC ACT-3′ и 5′-5′-GAT GGG GTG GAA GAA GTT GAA-3′ и следующие условия: начальная денатурация (95°С, 3 мин), 29 циклов: денатурация (95°С, 30 сек), отжиг (64°С, 20 сек) и элонгация (72°С, 30 сек); заключительная элонгация (72°С, 10 мин) - 1 цикл.
ПЦР-продукт обрабатывали рестриктазой MnlI и анализировали в 3% геле. О наличии в тестируемой ДНК аллеля (-1082) А судили по появлению двух фрагментов размером 92 п.о. и 49 п.о. (фиг.2). После анализа всех образцов рассчитывали частоту встречаемости аллелей (-1082) G и (-1082) А и распространенность генотипов в анализируемых группах. Полученные результаты представлены, соответственно, в табл.4 и табл.5.
| Таблица 4.Частота аллелей (-1082) G/A полиморфизма гена IL-10 | ||||||
| Полиморфизм | Аллель | Контроль n=249 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 |
| IL-10(-1082)G/A | G | 0,595 | 0,557 | 0,643 | 0,611 | 0,576 |
| А | 0,405 | 0,443 | 0,357 | 0,389 | 0,424 | |
| Таблица 5.Распространенность генотипов (-1082) G/A полиморфизма гена IL-10 | ||||||
| Полиморфизм, генотип | Контроль n=249 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 | |
| IL-10(-1082) G/A) | СС (%) | 87 (36,10) | 13 (37,14) | 5 (35,71) | 3 (33,33) | 19 (41,30) |
| СТ (%) | 113 (46,89) | 13 (37,14) | 8 (57,14) | 5 (55,56) | 15 (32,61) | |
| ТТ (%) | 41 (17,01) | 9 (25,71) | 1 (7,14) | 1 (11,11) | 12 (21,74) |
Экспериментально определенная распространенность аллелей и генотипов полиморфизма (-1082) G/A гена IL-10 не различалась между всеми исследованными группами. Т.о., по нашим данным, этот полиморфизм явным образом не ассоциирован с изменением скорости прогрессирования фиброза у больных ХГС, поэтому он не был включен в предложенную модель.
Пример 4. Определение полиморфизма (-174) G/C IL-6.
При проведении ПЦР-амплификации участка геномной ДНК, включающего положение (-174) гена IL-6, использовали праймеры 5′-TGA CTT CAG СТТ ТАС ТСТ TTG Т-3′ и 5′-CTG АТТ GGA ААС СТТ АТТ AAG-3′ и следующие условия: начальная денатурация (94°С 10 мин) - 1 цикл, затем 35 циклов: денатурация (94°С, 60 сек), отжиг (55°С, 35 сек) и элонгация (72°С, 60 сек); заключительная элонгация (72°С, 10 мин) - 1 цикл.
ПЦР-продукт анализировали, как описано в примере 2, используя для рестрикции рестриктазу SfaN1. О наличии аллеля (-174) G судили по появлению двух фрагментов 140 п.о. и 48 п.о. (фиг.3).
По результатам анализа всех образцов рассчитывали частоту аллелей (-174) G и С (табл. 6) и распротраненность соответствующих генотипов (табл. 7).
| Таблица 6.Частота аллелей (-174) G/C полиморфизма гена IL-6 | ||||||
| Полиморфизм | Аллель | Контроль n=199 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 |
| IL-6(-174) G/C | G | 0,603 | 0,634а | 0,5 | 0,556 | 0,476 |
| С | 0,397 | 0,366 | 0,5 | 0,444 | 0,524 | |
| a - р=0,04 (между F1 и F4; критерий Фишера). |
| Таблица 7.Распространенность генотипов (-174) G/C полиморфизма гена IL-6 | ||||||
| Полиморфизм, генотип | Контроль n=199 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 | |
| IL-6(-174)G/C | GG (%) | 73 (36,68)a | 19 (54,29)b | 3 (21,43) | 3 (33,33) | 10 (21,74) |
| GC (%) | 94 (47,24) | 14 (40,0) | 8 (57,14) | 4 (44,44) | 29 (63,04) | |
| СС (%) | 32 (16,08) | 2 (5,71) | 3 (21,43) | 2 (22,22) | 7 (15,21) | |
| а - р=0,05 (между F1 и популяцией; критерий χ2); b - р=0,006 (между F1 и F4; критерий χ2). |
Согласно полученным экспериментальным данным, частота встречаемости аллеля (-174) G максимальна у больных с медленно прогрессирующим течением заболевания (0,634), а минимальна - у больных с ЦП (0,476). Результаты анализа встречаемости различных генотипов свидетельствуют о том, что генотип GG четко ассоциирован с медленным формированием фиброза и наблюдается у больных с 1 стадией фиброза в 2 раза чаще по сравнению с больными, развившими цирроз печени (р=0,006). Что касается полиморфизма (-174) СС, то, хотя различия между группами пациентов с различными стадями фиброза не достигали статистической значимости (р=0,16), очевидной была тенденция к более частому выявлению этого полиморфизма у больных с циррозом печени (15,21%) по сравнению с больными, у которых отмечено благоприятное течение болезни (5,71%).
Таким образом, в процессе разработки предлагаемого изобретения впервые показана обратная корреляция между развитием цирроза печени и носительством (-174) GG генотипа гена IL-6, который выявлялся у 54,29% больных с медленным темпом прогрессирования фиброза и только у 21,74% больных с ЦП (р=0,006). Этот результат вкупе с данными о том, что генотип (-174) СС в 3 раза чаще выявляется у больных с ЦП (15,21%) по сравнению с больными, имевшими благоприятное течение ХГС (5,71%), позволил сделать вывод о том, что генотип GG обладает протективным эффектом в отношении прогрессирования фиброза печени у больных ХГС.
Пример 5. Определение полиморфизма (+915 G/C) TGF-β1.
При проведении ПЦР-амплификации участка геномной ДНК, включающего положение (+915) гена TGF-1b, использовали праймеры 5′-TTCCCTCGAGGCCCTCCTA-3′ и 5′-GCCGCAGCTTGGACAGGATC-3′ и следующие условия: начальная денатурация (94°С 10 мин) - 1 цикл, затем 35 циклов: денатурация (94°С, 75 сек), отжиг (62°С, 75 сек) и элонгация (72°С, 75 сек); заключительная элонгация (72°С, 5 мин) - 1 цикл.
ПЦР-продукт анализировали, как описано в примере 2, используя для рестрикции рестриктазу Bgl1. О наличии вариантного аллеля судили по появлению тяжелого фрагмента 296 п.о. вследствие потери сайта рестрикции (фиг.4).
На основании данных по всем исследованным образцам рассчитывали частоту встречаемости аллелей (+915) G и (+915) С и распространенность возможных генотипов в анализируемых группах. Полученные результаты представлены, соответственно, в табл.8 и табл.9.
| Таблица 8.Частота аллелей (+915) G/C полиморфизма гена TGF-b1 | ||||||
| Полиморфизм | Аллель | Контроль n=271 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 |
| TGF-b1(+915) G/C | G | 0,932 | 0,957 | 0,929 | 1,0 | 0,902 |
| С | 0,068 | 0,043a | 0,071 | 0 | 0,098 | |
| а - р=0,15 (между F1 и F4; критерий Фишера). |
| Таблица 9.Распространенность генотипов (+915) G/C полиморфизма ген TGF-b1 | ||||||
| Полиморфизм, генотип | Контроль n=271 | F1 n=35 | F2 n=14 | F3 n=9 | F4 n=46 | |
| TGF-b1(+915) G/C | GG (%) | 235 (86,72) | 32 (91,43) | 12 (85,71) | 9 (100,0) | 37 (80,43) |
| GC (%) | 35 (12,92) | 3 (8,57)a | 2 (14,29) | 0 (0,0) | 9 (19,57) | |
| СС (%) | 1 (0,37) | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0 (0,0) | |
| а - р=0,14 (между F1 и F4; критерий Фишера). |
Несмотря на то, что нами не было получено статистически значимых отличий между группами при сравнении частоты вариантного аллеля С (+915) G/C полиморфизма, тенденция к большей частоте выявления этого аллеля у больных с ЦП (0,098) по сравнению с пациентами с доброкачественным течением заболевания (0,043) была очевидной (р=0,15).
При определении встречаемости генотипов было обнаружено, что гетерозиготный генотип по мутантному аллелю гена TGF-b1 (GC генотип) в 2 раза чаще выявляется у больных с ЦПС (19,57%), чем у больных с мягким течением заболевания (8,57%) (р=0,14). Сделать однозначный вывод относительно (предположительно "профибротического") влияния генотипа СС на прогрессирование фиброза не представлялось возможным, т.к. встречаемость этого генотипа в популяции чрезвычайно низка и составляет всего лишь 0,37%.
Пример 6. Анализ частоты встречаемости комбинации аллелей и прогнозирование возможности агрессивного течения заболевания.
С целью определения зависимости степени надежности прогнозирования течения заболевания от количества определяемых полиморфизмов (из числа трех предлагаемых нами для анализа) было проведено соответствующее суммирование результатов ДНК-тестирования, полученных в примерах 1, 3 и 4 (табл.8).
| Таблица 10.Частота выявления различных сочетаний аллелей, связанных с прогрессирующим течением ХГС | |||
| Количество профибротических аллелей, выявленных в образце ДНК | Популяция n=184 n (%) | F1 n=35 n (%) | F4 n=46 n (%) |
| 0 | 27 (14,67) | 10 (28,57)a | 4 (8,7) |
| 1 | 60 (32,61) | 16 (45,71) | 14 (30,43) |
| 2 | 58 (31,52) | 9 (25,71)b | 20 (43,48) |
| 3 | 39 (21,20) | 0 (0)c,d | 8 (17,39) |
| а - р=0,02 (между F1 и F4, критерий Фишера); b - р=0,08 (между F1 и F4, критерий χ2); с - р=0,008 (между F1 и F4, критерий Фишера); d - р=0,0008 (между F1 и популяцией, критерий Фишера). |
Отсутствие аллелей (первая строка табл.10), ассоциированных с прогрессирующим течением ХГС, отмечено почти у трети (28,57%) больных с медленно прогрессирующим фиброзом и только у 8,7% больных, развивших цирроз печени; при этом различия были статистически значимы (р=0,02).
Результаты, обобщающие случаи выявления в образце ДНК одного из трех ассоциированных с развитием фиброза аллелей (вторая строка табл.10), не позволили обнаружить достоверных различий между анализируемыми группами.
Одновременное присутствие в геноме больных ХГС двух аллелей, ассоциированных с быстрым развитием фиброза (строка 3 табл.10), чаще выявлялось у пациентов с ЦП (43,48%), чем у пациентов с доброкачественным течением заболевания (25,71%), однако различия не достигали статистической значимости (р=0,08). Вместе с тем, после вычета из группы с двумя факторами, больных (3 больных с F1 и 3 больных с F4) с (-174) GG генотипом, который определен нами как "протективный" (см. пример 3), выявленные различия стали достоверными (р=0,05). Наряду с указанным генотипом, определенным "защитным" действием, по нашим данным, обладает и генотип (-511) СС по гену IL-1b, поэтому с целью получить более убедительное доказательство существования протективного действия на естественное течение ХГС у носителей "профибротических" аллелей из анализа нами были исключены все больные, имеющие (-511) СС и (-174) GG генотипы (фиг.5). Как следует из полученных данных, только 8,57% больных из группы с медленным темпом прогрессирования фиброза по сравнению с 34,78% пациентов, развивших цирроз печени, и 41,08% здоровых доноров, не были носителями (-174) GG и (-511) СС генотипов (р=0,005 и р=0,0001, соответственно). Проведенный анализ показывает, что отсутствие указанных генотипов значительно снижает вероятность благоприятного течения ХГС, и определяет необходимость учета их протективного действия при составлении заключения.
Носительство сразу трех "профибротических" аллелей (строка 4 табл.10) не было отмечено ни у одного из 35 больных с медленно прогрессирующим течением заболевания, в то время как в группе больных, развивших цирроз печени, таких пациентов было около 20%.
Таким образом, по нашим данным, полиморфизмы (-511) С/Т в гене IL-1b, (-174) G/C в гене IL-6 и (+915) G/C в гене TGF-b1 влияют на естественное течение хронического гепатита С у пациентов русской этнической принадлежности. При этом генотипы (-511) ТТ гена IL-1b, (-174) СС гена IL-6 и (+915) GC гена TGF-b1 и, по-видимому, (+915) СС гена TGF-b1 ассоциированы с выраженным "профибротическим" ("++") действием, генотипы (-511) СТ гена IL-1b и (-174) GC гена IL-6 характеризуются умеренным "профибротическим" действием ("+"), генотип (+915) GG гена TGF-b1 - нейтральным эффектом ("0"), а генотипы (-511) СС гена IL-1b и (-174) GG гена IL-6 - протективным ("-") эффектом. В таблице 11 представлены возможные варианты генотипов, которые могут быть определены в результате ДНК-тестирования на наличие трех функционально значимых для течения ХГС полиморфизмов, и отмечено влияние каждого из них на развитие фиброза. Использование данной таблицы позволяет дать качественную оценку предрасположенности пациента с определенным генотипом к прогрессированию фиброза.
Предлагаемая модель, основанная на анализе комбинации полиморфизмов генов цитокинов, позволяет выделить среди больных ХГС группу высокого риска развития цирроза печени и с большей уверенностью рекомендовать этим больным интенсивную противовирусную, а в перспективе и антифибротическую терапию.
Способ прогнозирования прогрессирующего течения хронического гепатита С (развития цирроза печени) путем анализа комбинации полиморфизмов генов цитокинов, включающий: а) получение образца геномной ДНК больного ХГС, б) тестирование указанной ДНК на наличие аллелей, ассоциированных с прогрессированием фиброза, в) оценку результатов и составление заключения о вероятности прогрессирующего течения заболевания, отличающийся тем, что ДНК анализируют на наличие полиморфизмов генов цитокинов (-511) С/Т IL-1b, (-174) G/C IL-6 и (+915) G/C TGF-b1, а заключение составляют на основании данных, представленных в табл.11.