Способ лечения опухолей
Иллюстрации
Показать всеИзобретение относится к медицине, онкологии, способам и набору для лечения таких опухолей, как опухоли предстательной железы, молочной железы, неходжкинская лимфома и им подобные. Способ включает последовательные стадии: (а) введения пациенту, по меньшей мере, одной дозы антиангиогенного цикло-(аргинин-глицин-аспарагиновая кислота)-содержащего пентапептида (пентапептида cRGD), такого как цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val); (b) введения пациенту противоопухолевого эффективного количества радиоиммунотерапевтического средства (RIT) не позднее чем 1 час после введения пентапептида cRGD на стадии (а); и (с) введения пациенту, по меньшей мере, двух дополнительных доз пентапептида cRGD, где первую дополнительную дозу вводят в пределах 2 дней после введения RIT и каждую дополнительную дозу пентапептида cRGD вводят с интервалами не более чем примерно 2 дня между дозами. Изобретение, основанное на указанной схеме комбинированного введения пентапептида cRGD и RIT, обеспечивает синергический эффект на апоптоз опухолевых клеток и эндотелиальных клеток сосудов опухоли. 3 н. и 27 з.п. ф-лы, 6 ил., 2 табл.
Реферат
Область изобретения
Изобретение относится к способам лечения опухолей. Конкретнее, изобретение относится к способам лечения опухолей комбинацией радиоиммунотерапии и антагониста рецепторов интегрина.
Перекрестная ссылка на родственные заявки
Данная заявка является частичным продолжением одновременно поданной заявки на патент США под серийным № 09/787374, поданной 9 сентября 1999 г.
Заявление о заинтересованности правительства
Часть описанной в настоящем описании работы была поддержана грантом № РО1 СА-47829 Национального института рака и грантами №№ DEFG01-00NE22944 и DEFG03-84ER60233 Департамента энергетики США. Правительство США может оставить за собой определенные права на данное изобретение.
Предпосылки изобретения
Новые и синергические терапевтические комбинации желательны для лечения метастатического рака молочной железы, рака предстательной железы, лимфомы Ходжкина и других видов рака, многие из которых в настоящее время являются неизлечимыми стандартной терапией с множеством лечебных воздействий. Высокая частота встречаемости мутаций р53 и сверхэкспрессия белка bcl-2 при раке молочной железы увеличивают устойчивость к химиотерапии и лучевой терапии. Системная, нацеленная на опухоль радиоиммунотерапия (RIT) может быть специфически нацелена на ткань, и она способна доставить специфичные для рака цитотоксические антитела к широко распространенным метастатическим очагам. Однако исследования на модели ксенотрансплантата рака молочной железы человека демонстрируют, что RIT в качестве изолированного средства обычно не излечивает указанные опухоли. Проникновение в опухоль антител, меченных радиоактивной меткой, может быть неравномерным и может не быть достаточным во всех областях опухоли для обеспечения излечения. В настоящее время используется комбинация RIT с другими способами лечения, но дополнительная химиотерапия или внешняя лучевая терапия увеличивает риск токсичности для костного мозга, основного ограничивающего дозу фактора при RIT.
Антиангиогенные средства были предложены в качестве средств для лечения опухолей. Указанные средства генетически нацелены на нормальные эндотелиальные клетки, которые пролиферируют с гораздо более высокой скоростью во время ангиогенеза опухоли, по сравнению с очень низкими скоростями обновления эндотелия в нормальных тканях. Было показано, что антиангиогенные средства увеличивают терапевтическую эффективность в сочетании с другими химиотерапевтическими средствами и при применении в комбинации с внешней лучевой терапией. Рецептор интегрина αvβ3, который связывает несколько лигандов посредством аминокислотной последовательности RGD, экспрессирован в нормальной сосудистой системе, но имеет высокую экспрессию в растущей сосудистой системе опухоли, делая ее потенциальной мишенью для антиангиогенных средств. Высокая экспрессия и активация интегрина αvβ3 коррелировались с более метастазирующими и инвазивными опухолями молочной железы. Было показано, что ингибирование активности αvβ3 моноклональным антителом (MAb) и циклическими пентапептидами RGD вызывало апоптоз эндотелия, ингибировало ангиогенез и увеличивало проницаемость эндотелиального монослоя. Ингибирование активности αvβ3 было связано с уменьшенным ростом опухоли в ксенотрансплантатах рака молочной железы и ксенотрансплантатах меланомы. Синергия циклического пентапептида RGD со слитым белком антитела IL-2 привела к возросшей эффективности терапии на мышиных моделях меланомы, рака толстой кишки и нейробластомы. Избирательный захват опухолью был продемонстрирован циклическим пентапептидом RGD, меченным радиоактивной меткой.
Сущность изобретения
Настоящее изобретения предоставляет способ лечения пациента, имеющего опухоль, такую как опухоль предстательной железы, опухоль молочной железы, лимфомы и им подобные. Способ представляет собой схему лечения радиоиммунотерапией с множеством лечебных воздействий (CMRIT), включающий введение пациенту антиангиогенного цикло-(аргинин-глицин-аспарагиновая кислота)пентапептида (пентапептида cRGD) и радиоиммунотерапевтического средства (RIT). Способ включает схему последовательного лечения, включающую первую стадию введения пациенту, по меньшей мере, одной дозы пентапептида cRGD. После данного первоначального лечения пентапептидом cRGD пациенту вводят противоопухолевое, эффективное количество RIT. После лечения RIT пациенту вводят, по меньшей мере, одну дополнительную дозу пентапептида cRGD.
Количество и определение времени введения каждой дозы пентапептида cRGD предпочтительно выбирают так, чтобы она была равной или близкой к максимальной переносимой дозе для пациента, т.е. была на максимальном уровне, при котором токсичность пентапептида cRGD для пациента была терапевтически приемлемой.
Способ CMRIT настоящего изобретения обеспечивает значительно большую противоопухолевую эффективность по сравнению с лечением одним RIT или одним пентапептидом cRGD при тех же уровнях дозировки. Способ CMRIT также обеспечивает больший апоптоз опухолевых клеток и эндотелиальных клеток опухоли по сравнению с лечением одним RIT или одним пентапептидом cRGD при тех же уровнях дозировки.
В одном аспекте настоящее изобретение также предоставляет набор, включающий первый контейнер, включающий, по меньшей мере, одну стандартную дозу RIT и один или несколько дополнительных контейнеров, включающих всего, по меньшей мере, две стандартные дозы пентапептида cRGD. Каждый из контейнеров включает этикетку, описывающую содержимое контейнера, необязательно, последовательность введения и любую другую относящуюся к делу информацию, требуемую правительственными постановлениями, относящимися к фармацевтическим средствам и радиоактивным веществам. Набор может также включать напечатанные инструкции по применению содержимого контейнеров для лечения опухолей, в соответствии с описанными в настоящем описании способами.
Краткое описание чертежей
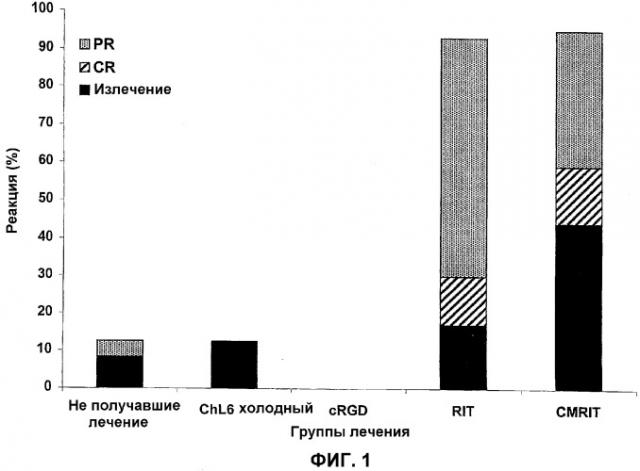
На фиг.1 представлена гистограмма, которая иллюстрирует возросшую частоту излечения опухолей у мышей, получавших лечение способом CMRIT настоящего изобретения, по сравнению со способом лечения одним RIT и одним пентапептидом cRGD, причем PR обозначает частичную регрессию, а CR означает полную регрессию.
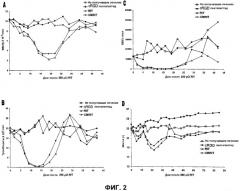
Фиг.2 представляет графические изображения данных токсичности у мышей, получавших лечение способом CMRIT настоящего изобретения, по сравнению со способами лечения одним RIT и одним пентапептидом cRGD.
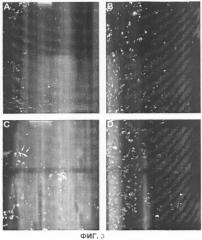
Фиг.3 показывает микрофотографические изображения опухолевых клеток, которые демонстрируют увеличенный апоптоз в опухолях от мышей, получавших лечение способом CMRIT настоящего изобретения.
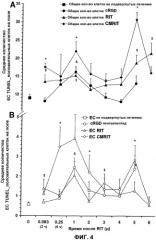
Фиг.4 представляет графические изображения данных, показывающих апоптоз (А) во всех клетках и (В) в эндотелиальных клетках (ЕС) в опухолях от мышей, получавших лечение способом CMRIT настоящего изобретения, по данным метода TUNEL.
Фиг.5 показывает микрофотографические изображения опухолевых клеток, которые демонстрируют уменьшенную пролиферацию клеток в опухолях мышей, получавших лечение способом CMRIT настоящего изобретения, по сравнению со способом лечения одним RIT и одним пентапептидом cRGD.
Фиг.6 показывает микрофотографическое изображение клеток опухоли молочной железы НВТ 3477, которая демонстрирует экспрессию β3 и CD31 на клетках.
Подробное описание предпочтительных вариантов реализации
Настоящее изобретение может быть осуществлено во многих различных формах. Определенные варианты осуществления показаны на чертежах и подробно описаны в описании и формуле изобретения. Настоящее описание представляет собой иллюстрацию принципов изобретения и не ограничивается определенными вариантами реализации, которые иллюстрируются в настоящем описании.
Способ радиоиммунотерапии с множеством лечебных воздействий (CMRIT) для лечения опухолей у пациента включает последовательные стадии:
(а) введения пациенту, по меньшей мере, одной дозы антиангиогенного цикло-(аргинин-глицин-аспарагиновая кислота)пентапептида (пентапептида cRGD);
(b) введения пациенту противоопухолевого эффективного количества радиоиммунотерапевтического средства (RIT) и
(с) введения пациенту, по меньшей мере, одной дополнительной дозы пентапептида cRGD.
Количество и определение времени введения каждой дозы пентапептида cRGD предпочтительно выбирают так, чтобы она была равной или близкой к максимальной переносимой дозе для пациента, т.е. была на максимальном уровне, при котором токсичность пентапептида cRGD для пациента была терапевтически приемлемой. Максимальную переносимую дозу можно легко определить способами, хорошо известными в фармацевтической области. Например, токсичность пентапептида cRGD можно получить в результате клинического исследования. Количество каждой дозировки находится предпочтительно в диапазоне от примерно 0,05 мг до примерно 500 мг, предпочтительнее, от примерно 0,1 до примерно 100 мг, наиболее предпочтительно, от примерно 0,2 до примерно 20 мг. Суточная общая дозировка находится предпочтительно в диапазоне от примерно 0,001 до примерно 2 мг/кг массы тела, предпочтительнее, от примерно 0,002 до примерно 1 мг/кг, наиболее предпочтительно, от примерно 0,002 до примерно 0,2 мг/кг. Однако специфическая доза для каждого предполагаемого пациента зависит от многих факторов, например, от активности определенного используемого соединения пентапептида cRGD, возраста, массы тела, общего состояния здоровья, пола, рациона, времени и пути введения и скорости выведения, фармацевтической комбинации и тяжести конкретного расстройства, по поводу которого применяется лечение. Предпочтительно парентеральное введение, наиболее предпочтительно, внутрибрюшинное (в/б) введение, однако предусматривается также пероральное, в форме суппозиторий или местное введение. При желании, дополнительные дозы пентапептида cRGD можно продолжать вводить в течение периода до нескольких месяцев после проведения RIT.
Пентапептид cRGD можно составлять с фармацевтически приемлемыми эксципиентами и носителями, такими как буферы и подобные вещества, хорошо известные в данной области. Подходящими эксципиентами являются органические или неорганические вещества, которые подходят для энтерального (например, перорального или ректального), парентерального (например, внутривенной инъекции) или локального (например, местного, дермального, глазного или назального) введения или для введения в форме ингаляционного аэрозоля, и которые не взаимодействуют с новыми соединениями, причем их примерами являются вода или водный изотонический солевой раствор, низшие спирты, растительные масла, бензиловые спирты, полиэтиленгликоли, триацетат глицерина и другие глицериды жирных кислот, желатин, лецитин сои, углеводы, такие как лактоза или крахмал, стеарат магния, тальк, целлюлоза и вазелин.
Для перорального применения большой интерес представляют простые таблетки, таблетки, покрытые оболочкой, капсулы, сиропы, соки или капли; особый интерес представляют таблетки, покрытые оболочкой, и капсулы, имеющие энтеросолюбильное покрытие. Суппозитории применяются для ректального введения, растворы, предпочтительно, масляные или водные растворы, а также суспензии, эмульсии или имплантаты применяются для парентерального введения.
Примерами форм, подходящих для местного применения, являются растворы, которые можно применять в форме глазных капель, а также, например, суспензий, эмульсий, кремов, мазей или компрессов. Для введения в форме ингаляционного аэрозоля можно применять аэрозоли, которые содержат активное начало или растворенное, или суспендированное в газе-пропелленте или в смеси газов-пропеллентов (например, двуокиси углерода или фторхромуглеводородных заместителях). В данном случае активное начало надлежащим образом используется в микронизированной форме, причем возможно присутствие одного или нескольких дополнительных, физиологически совместимых растворителей, таких как этанол. Ингаляционные растворы можно вводить с помощью обычных ингаляторов. Пентапептид cRGD можно также лиофилизировать и полученные лиофилизаты использовать, например, для изготовления инъецируемых препаратов. Инъекции можно вводить в виде болюса или в форме непрерывного вливания (например, внутривенного, внутримышечного, подкожного или подоболочечного). Указанные препараты могут стерилизоваться и/или включать вспомогательные ингредиенты, такие как консерванты, стабилизаторы и/или смачивающие агенты, эмульгаторы, соли для воздействия на осмотическое давление, буферные вещества, красители и/или отдушки. При желании, пентапептид cRGD может также содержать один или несколько других активных ингредиентов, включая, например, один или несколько витаминов и им подобных.
Пентапептид cRGD можно использовать как таковой или в виде одной или нескольких из его физиологически приемлемых солей. Пентапептид cRGD может превращаться во внутреннюю соль или в ассоциированную кислотно-аддитивную соль с использованием кислоты. Подходящими кислотами для данной реакции являются, в частности, те, которые дают физиологически приемлемые соли. Можно использовать неорганические кислоты, их примерами являются серная кислота, азотная кислота, галогенводородные кислоты, такие как хлористоводородная кислота или бромистоводородная кислота, фосфорная кислота, такая как ортофосфорная кислота, сульфаминовая кислота, а также органические кислоты, в частности, алифатические, алициклические, аралифатические, ароматические или гетероциклические моно- или многоосновные карбоновые, сульфоновые или серные кислоты, например, муравьиная кислота, уксусная кислота, пропионовая кислота, пиваловая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, молочная кислота, винная кислота, яблочная кислота, бензойная кислота, салициловая кислота, 2- или 3-фенилпропионовая кислота, лимонная кислота, глюконовая кислота, аскорбиновая кислота, никотиновая кислота, изоникотиновая кислота, метан- или этансульфоновая кислота, этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, пара-толуолсульфоновая кислота, нафталин-моно- и -дисульфоновая кислоты, лаурилсульфоновая кислота.
Альтернативно, кислотная форма пентапептида cRGD может превращаться в одну из ее физиологически приемлемых солей металлов или аммония реакцией с основанием. Особенно подходящими солями в данном контексте являются соли натрия, калия, магния, кальция и аммония, а также замещенные соли аммония, например, соли диметил-, диэтил- или диизопропиламмония, соли моноэтанол-, диэтанол- или триэтаноламмония, соли циклогексиламмония, соли дициклогексиламмония, соли дибензилэтилендиаммония, а также, например, соли с N-метил-D-глюкамином или с аргинином или лизином.
Предпочтительно, пентапептид cRGD представляет собой
цикло-(Arg-Gly-Asp-D-Phe-Val) (EMD 66203),
цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) (EMD 121974, циленгитид, имеющийся в продаже от компании Merck KGaA, Darmstadt, Germany) или
цикло-(Arg-Gly-Asp-D-Phe-1-аминоциклогексанкарбоновая кислота) (EMD 270179),
получение которых описано в патентах США № 5866540 и 6001961, выданных Jonczyk et al., релевантные описания которых включены в настоящее описание в качестве ссылки. Наиболее предпочтительно, пентапептид cRGD представляет собой цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val).
Предпочтительно, первую дозировку пентапептида cRGD вводят пациенту не позже чем за 1 час до проведения RIT. Предпочтительно, по меньшей мере, одну дополнительную дозу пентапептида cRGD вводят в пределах примерно двух дней после проведения RIT. В предпочтительном варианте осуществления изобретения, по меньшей мере, примерно 2 дополнительные дозы пентапептида cRGD вводят пациенту после дозы RIT, предпочтительнее, по меньшей мере, примерно 3 дополнительные дозы пентапептида cRGD, наиболее предпочтительно, по меньшей мере, примерно 4 дополнительные дозы. В особенно предпочтительном варианте реализации, по меньшей мере, примерно 5 дополнительных доз пентапептида cRGD последовательно вводят после дозы RIT. Предпочтительно, каждую дополнительную дозу пентапептида cRGD вводят с интервалами не более чем примерно 2 дня между дозами. При желании, введение дополнительных доз RIT можно продолжать в течение нескольких месяцев с частотой примерно 2 дозы в неделю.
Дозировка RIT предпочтительно основана на уровне радиоактивности конкретного средства RIT. Количество используемого RIT предпочтительно обеспечивает радиоактивную дозировку в диапазоне от примерно 20 мКи до примерно 200 мКи на дозу при использовании 90Y в качестве источника излучения. Однако конкретная доза для каждого предполагаемого пациента зависит от многих факторов, например, радиоактивности определенного используемого соединения RIT, определенного используемого радионуклида, возраста, массы тела, общего состояния здоровья, пола, рациона, времени и пути введения и скорости выведения, фармацевтической комбинации и размера и тяжести конкретной опухоли, к которой применяется терапия. Например, при лечении метастатического рака предстательной железы или рака молочной железы моноклональное антитело против MUC-1 (M170), конъюгированное с циклизованным 90Y, обычно вводят при удельной активности примерно 5 мКи/мг антитела для доставки общей дозировки в диапазоне от примерно 20 мКи до примерно 200 мКи, в зависимости от размера опухоли и других факторов, описанных выше. Предпочтительно парентеральное введение RIT, предпочтительнее - внутривенное (в/в) введение.
Радиоиммунотерапевтические средства для лечения опухолей хорошо известны в данной области. Подходящие средства RTI включают любую прицельную радионуклидную терапию любыми терапевтически полезными присоединенными радионуклидами, которые могут присоединяться к опухоли или сосудистой системе опухоли или захватываться ими. Такие полезные средства RIT включают нацеленный на опухоль или нацеленный на сосудистую систему опухоли лиганд или молекулу. Радионуклид может непосредственно присоединяться к нацеленной молекуле или лиганду или присоединяться хелатобразующим веществом, соединенным с лигандом или ассоциированным с ним. Альтернативно, лиганд может включать хелатобразующую или захватывающую радионуклид группу, и его можно вводить пациенту холодным для связывания с опухолью или сосудистой системой опухоли у пациента. При последующем введении радионуклида связанный лиганд может захватывать радионуклид в участке опухоли (предварительно нацеленная радионуклидная терапия). Нацеленные молекулы или лиганды включают антитела, фрагменты антител, рекомбинантные комбинации фрагментов антител, пептидов или другого лиганда, который обладает селективным сродством к опухолям или сосудистой системе опухолей.
Предпочтительно, RIT представляет собой меченный радионуклидом комплекс хелатобразующий агент-лиганд, в котором хелатобразующий агент химически связан с нацеленной на опухоль молекулой. Предпочтительные нацеленные на опухоль молекулы включают антитела, такие как моноклональные антитела или фрагменты антител. Предпочтительнее, нацеленная на опухоль молекула представляет собой противоопухолевое антитело. Можно использовать любое противоопухолевое антитело. Предпочтительно, противоопухолевое антитело нацелено на сосудистую систему опухоли. Альтернативно, антитело может нацеливаться на опухолевые антигены, такие как p185HER2, белок ядра молочного муцина, TAG-72, Lewis a, канцероэмбриональный антиген (СЕА), антигены меланомы с высокой относительной молекулярной массой, распознаваемые антителом 9.2.27, или связанные с яичниками антигены, распознаваемые OV-TL3 или MOV18. Предпочтительными противоопухолевыми антителами являются мноклональные антитела против MUC-1, такие как M170mAb, имеющиеся в продаже от компании Biomira Inc., Edmonton, Canada, химерное противоопухолевое моноклональное антитело L6 (ChL6 Mab) и им подобные.
Любые радионуклиды, подходящие для применения в способах лучевой терапии рака, можно использовать в способе CMRIT настоящего изобретения. Подходящие радионуклиды включают без ограничения 131I, 177Lu, 67Cu, 64Cu, 196Re и 90Y. Предпочтительно, радионуклид представляет собой 90Y.
Подходящие средства RIT и их получение описаны в патенте США № 5958374, выданном Meares et al., релевантное описание которого включено в настоящее описание в качестве ссылки.
Предпочтительно, хелатобразующий агент представляет собой полиазамакроциклическую группу или полиоксамакроциклическую группу. Предпочтительнее, хелатобразующую группу получают из:
1,4,7,10-тетраазациклододекан-N,N′,N″,N′′′-тетрауксусной кислоты;
1,4,7,10-тетраазациклотридекан-N,N′,N″,N′′′-тетрауксусной кислоты;
1,4,8,11-тетраазациклотетрадекан-N,N′,N″,N′′′-тетрауксусной кислоты или
1,5,9,13-тетраазациклогексадекан-N,N′,N″,N′′′-тетрауксусной кислоты.
Предпочтительнее, меченный радионуклидом комплекс хелатобразующий агент-лиганд химически связан с ChL6 mAb или с M170 mAb. Наиболее предпочтительно, RIT представляет собой 90Y-1,4,7,10-тетраазациклододекан-N,N′,N″,N′′′-тетрауксусную кислоту-пептид-ChL6 (далее - 90Y-DOTA-пептид-ChL6) или его анти-MUC-1 mAb аналог.
Радионуклид предпочтительно представляет собой 90Y. 111In может быть включен в RIT для визуализации опухоли. Предпочтительно, меченный радионуклидом комплекс хелатобразующий агент-лиганд химически связан с ChL6 mAb или с M170 mAb.
В предпочтительном варианте реализации хелатобразующий агент представляет собой N-замещенную 1,4,7,10-тетраазациклододекан-N,N′,N″,N′′′-тетрауксусную кислоту, где N-заместитель представляет собой -CH2C(=O)-(Gly)3-L-(пара-изотиоцианат)-Phe-амид (далее - DOTA-пептид) и радионуклид представляет собой 90Y.
RIT может быть составлено с разнообразными фармацевтически приемлемыми эксципиентами, подходящими для жидкой инъецируемой композиции, как описано выше в отношении композиции пентапептидов cRGD.
Способ CMRIT настоящего изобретения можно использовать для лечения различных форм рака. Например, способ CMRIT настоящего изобретения можно использовать для лечения форм рака, которые проявляются солидными опухолями, такие как рак молочных желез, рак толстой кишки, рак легких, рак щитовидной железы, рак яичников и им подобные. Способ CMRIT можно также использовать для лечения форм рака, не являющихся солидными опухолями, таких как неходжкинская лимфома, и им подобные. Способ CMRIT настоящего изобретения предпочтительно используется в качестве лечения рака молочной железы.
Способ CMRIT настоящего изобретения обеспечивает значительно более высокую противоопухолевую эффективность относительно совокупной общей противоопухолевой активности лечения одним RIT или одним пентапептидом cRGD при таких же уровнях дозировки (т.е. наблюдается синергический эффект). Способ CMRIT также обеспечивает больший апоптоз опухолевых клеток и опухолевых эндотелиальных клеток по сравнению с лечением одной RIT или одним пентапептидом cRGD при таких же уровнях дозировки.
Настоящее изобретение в другом аспекте предоставляет набор, включающий первый контейнер, включающий, по меньшей мере, одну стандартную дозу RIT и один или несколько дополнительных контейнеров, включающих всего, по меньшей мере, две стандартные дозы пентапептида cRGD. Каждый из контейнеров включает этикетку, описывающую содержимое контейнера, необязательно, последовательность введения и любую другую относящуюся к делу информацию, требуемую правительственными постановлениями, относящимися к фармацевтическим средствам и радиоактивным веществам. Набор может также включать напечатанные инструкции по применению содержимого контейнеров для лечения опухолей, в соответствии с описанными в настоящем описании способами.
Контейнеры могут представлять собой флаконы, ампулы, бутылки и им подобные. Каждый контейнер предпочтительно включает одну стандартную дозу, однако, можно также использовать контейнеры с множеством доз. Инструкционные материалы также предпочтительно включают информацию по безопасности и эффективности.
Следующие не ограничивающие примеры предоставлены для дополнительной иллюстрации изобретения.
Реагенты. Иттрий-90 (90Y) без носителя (Pacific Northwest National Laboratory, Richland, WA или New England Nuclear, Boston, MA) закупали в виде хлорида в 0,05М HCl. Химерное L6 (ChL6), химера человеческого-мышиного антитела (Bristol-Myers Squibb Pharmaceutical Research Institute, Seattle, WA) взаимодействует с общим мембранным гликопротеидом, проявляющим высокую экспрессию на карциномах молочной железы, толстой кишки, яичников и легких человека. Цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) (EMD 121974) представляет собой антагонист, селективный для интегринов αvβ3 и αvβ5, с величинами IC50 в низком наномолярном диапазоне для клеток меланомы М21, экспрессирующих изолированные интегрины αvβ3, и в низком микромолярном диапазоне для клеток меланомы М21, экспрессирующих αvβ5. Синтез и характеристику пептидов выполняли, как описано ранее Dechantsreiter et al., J. Med. Chem. 42: 3033-40 (1999), релевантное описание которого включено в настоящее описание в качестве ссылки.
Клеточные линии. НВТ 3477, клеточную линию аденокарциномы молочной железы человека, получали из Научно-исследовательского фармацевтического института Bristol-Myers Squibb (Seattle, WA). Более чем 70% клеток НВТ 3477 интенсивно окрашиваются L6. В клетках НВТ 3477 экспрессируется bcl-2, а р53 представляет собой мутант с бессмысленной мутацией в экзоне 10, приводящей к делеции в области белка р53, который функционирует при тетрамеризации и в выявлении разрывов двухнитевой ДНК. Клетки НВТ 3477 экспрессируют функциональный интегрин αvβ5, но не интегрин αvβ3, поскольку соединение с витронектином блокируется специфичным для αvβ5 антителом P1F6, но не блокируется специфичным для αvβ3 антителом LM609. Цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) блокирует соединение клеток НВТ 3477 с витронектином при IC50 примерно 5 мкМ.
90 Y-DOTA-пептид-ChL6. ChL6 конъюгировали с 1,4,7,10-тетраазациклододекан-N,N′,N″,N′′′-тетрауксусной кислотой (DOTA) и метили радиоактивной меткой 90Y, как описано DeNardo, et al. J. Nucl. Med., 36: 829-836, с эффективностью больше 80% или равной ей для получения 90Y-DOTA-пептид-ChL6. 90Y-DOTA-пептид-ChL6 исследовали на структурную и функциональную целостность высокоэффективной жидкостной хроматографией (ВЭЖХ) с просеиванием через молекулярное сито, электрофорезом на пленке из ацетата целлюлозы (САЕ) и радиоиммунореактивным анализом (RIA) связывания с клетками НВТ 3477. ВЭЖХ и САЕ указали на то, что более чем 90% 90Y-DOTA-пептид-ChL6 было в мономерной форме при менее чем 4% видов с высокой молекулярной массой, по данным определения САЕ. Иммунореактивное связывание с живыми клетками указало на реактивность более 92% при введении в виде одной дозы 200, 230 или 260 мкКи 90Y-DOTA-пептид-ChL6.
Мыши. Самок бестимусных мышей Balb/c nu/nu (в возрасте 7-10 недель; Harlan Sprague Dawley, Inc., Frederick, MD) содержали в соответствии с рекомендациями Калифорнийского университета по уходу за животными. Клетки НВТ 3477 (3,0×106), собранные в логарифмической фазе, инъецировали подкожно в одну сторону живота для исследований терапии (за исключением отмеченных случаев) и в обе стороны для исследований иммунопатологии. RIT инъецировали в хвостовую вену, а цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) доставляли внтурибрюшинной (в/б) инъекцией. «0 день» обозначали как время инъекции RIT или первой инъекции пентапептида cRGD для группы с введением только пентапептида cRGD. Мышей умерщвляли смещением шеи для исследований иммунопатологии в указанные точки времени, когда опухолевое поражение превышало допустимые пределы, или через 84 дней для исследований терапии.
Группы контрольного лечения (без RIT). Группы состояли из мышей, не получавших лечение (24 мыши, 14 мышей, имеющих по 2 опухоли каждая, и 10 мышей, имеющих 1 опухоль); получавших немеченое антитело ChL6 (315 мкг) (8 мышей, имеющих по 2 опухоли каждая) и получавших цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val), вводившийся в 6 дозах по 250 мкг в 0, 2, 4, 6, 8 и 10 день (18 мышей с 1 опухолью каждая).
Группы лечения высокой дозой RIT. Группы состояли из мышей, получавших RIT в качестве единственного агента (260 мкКи 90Y-DOTA-пептид-ChL6 (39 мышей, 15 имеющих по 2 опухоли каждая, и 24, имеющие по 1 опухоли)), и RIT (260 мкКи 90Y-DOTA-пептид-ChL6 в комбинации с цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) в 6 дозах по 250 мкг, начиная с 0 дня, за 1 час до RIT c последующим введением еще 5 доз во 2, 4, 6, 8 и 10 день (42 мыши, все имеющие по 1 опухоли каждая).
Группы лечения низкой дозой RIT. Группы состояли из мышей, получавших RIT в качестве единственного агента (200-230 мкКи 90Y-DOTA-пептид-ChL6 (28 мышей, включая 9, имевших по 2 опухоли каждая из предыдущего исследования, которые получали 230 мкКи 90Y-DOTA-пептид-ChL6, и 19 мышей, имевших по 1 опухоли каждая, получавших лечение 200 мкКи 90Y-DOTA-пептид-ChL6)), и группы, получавшей RIT (200 мкКи 90Y-DOTA-пептид-ChL6) в комбинации с 6 дозами (по 250 мкг каждая) цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val). Указанные дозы вводили в 0 день, за 1 час до RIT c последующим введением еще 5 доз во 2, 4, 6, 8 и 10 день (30 мышей, все имеющие по 1 опухоли каждая).
Уничтожающий опухолевые клетки эффект. Опухоли измеряли кронциркулем в 3 ортогональных диаметрах 3 раза/неделю. Объем опухоли рассчитывали с использованием формулы для полуэллипсоидов (DeNardo et al. Clin. Cancer Res., 3: 71-79 (1997)). Исходный объем опухоли определяли как объем в день перед лечением. Опухоли, которые подверглись полной регрессии, считали имеющими нулевой объем. Реакции опухолей классифицировали следующим образом: излечение (С), опухоль исчезла и повторно не росла к концу исследования (84 дня); полная регрессия (CR), опухоль исчезла, по меньшей мере, на 7 день, но позже выросла снова; частичная регрессия (PR), объем опухоли уменьшился на 50% или более по меньшей мере, на 7 день, но позже выросла снова; отсутствие реакции (NR), объем опухоли уменьшился менее чем на 50%. Для мышей, имеющих 2 опухоли с различными реакциями, реакцию опухоли описывали в соответствии с реакциями обеих опухолей. Мыши, умершие перед 30-м днем от токсичности, были исключены из результатов оценки реакции опухоли.
Токсичность. Величины массы и формулу крови измеряли 2-3 раза/неделю в течение 12 недель после инъекции до смерти. Образцы крови брали из хвостовой вены с использованием микрокапиллярных пипеток емкостью 2 мкл. Образцы от мышей в рамках группы дозы объединяли и разбавляли 1:200 в солевом растворе с фосфатным буфером (PBS, 0,9% солевой раствор/10 мМ фосфата натрия, рН 7,6)для количества эритроцитов (RBC); 1:100 в 1% (мас./об.) оксалате аммония для количества тромбоцитов; или 1:20 в 3% (мас./об.) уксусной кислоте для определения лейкоцитарной формулы (WBC).
Группы клеточной иммунопатологии. При отсутствии других указаний, группы состояли из 2 мышей, причем каждая имела по 2 опухоли, при анализе всего 4 опухолей в каждую точку времени. Группы состояли из мышей, не получавших лечение (4 мыши, 7 опухолей); 250 мкг каждая) цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val), вводившихся в виде одной дозы с последующим умерщвлением через 2 часа, 6 часов и 1-5 дней после инъекции пептида; только RIT (260 мкКи 90Y-DOTA-пептид-ChL6) с последующим умерщвлением через 2 часа, 6 часов и 1-6 дней (3 мыши, 5 опухолей на 5-й день); и RIT (260 мкКи 90Y-DOTA-пептид-ChL6) в комбинации с цикло-(Arg-Gly-Asp-D-Phe-[N-Me]-Val) (250 мкг), вводившимся за 1 час до RIT (способ CMRIT) и повторяли через день до 10 дней с последующим умерщвлением через 2 часа, 6 часов и 1-6 дней после RIT. Опухоли удаляли, разрезали пополам, замораживали в среде с оптимальной температурой резания (O.C.T.) и хранили примерно при -70°С до получения срезов (срезы толщиной 10 мкм). Во все точки времени проводили оценку для выявления апоптоза анализом мечения конца однонитевого разрыва dUTP, опосредованного терминальной дезоксинуклеотидилтрансферазой (TUNEL, Carvieli, et al. J. Cell Bio., 119: 493-501 (1992)), и выбранные точки времени (не леченные, 1, 5 и 6 дней) оценивали для выявления различий скорости пролиферации (Ki67) и плотности микрососудов (CD31).
Анализ TUNEL общего апоптоза и эндотелиального апоптоза. Опухоли разрезали на срезы по 10 мкм и помещали на предметные стекла Fisher superplus (Fisher, Pittsbugh, PA), сушили воздухом в течение 1 часа и замораживали примерно при -70°С до анализа TUNEL набором ApopTag Red (родамин, используемый в виде метки, Intergen, Purchase, NY), следуя инструкциям изготовителя после фиксации в течение примерно 10 мин в 1% параформальдегиде. После TUNEL предметные стекла промывали и инкубировали в течение ночи при 4°С с крысиным анти-мышиным антителом Mab против CD31 при разведении 1:100 (Pharmingen, San Diego, CA) для идентификации эндотелиальных клеток. Предметные стекла промывали и инкубировали в течение 1 часа с анти-крысиным антителом, связанным с FITC (разведение 1:50) (Pharmingen). Предметные стекла промывали, кратковременно погружали в 4,6-диамидин-2-фенилиндол (DAPI, 0,2 мкг/мл) для фонового ядерного окрашивания, снова промывали и устанавливали с последующим хранением в темноте примерно при 4°С до количественного анализа.
Количественный анализ общего и эндотелиального апоптоза. Для количественного анализа 6 выбранных методом случайной выборки полей ×600 (150000 мкм2/поле) в лишенных некроза областях каждого среза использовали микроскоп Olympus, оборудованный набором Chroma Pinkle Filter Set (Chroma, Brattleboro, VT) с фильтрами возбуждения для УФ, FITC (флюоресцеин-изоцианата) и родамина и фильтрами с двойной/тройной полосой пропускания для обеспечения возможности одновременной визуализации множества длин волн. Поля выбирали для охвата всей площади осмотра с использованием метки DAPI, которая обычно включала примерно 300-350 клеток. Апоптоз всех клеток определяли по среднему количеству положительных ядер на поле для каждой опухоли, тогда как апоптоз эндотелиальных клеток определяли с использованием тех же полей фильтром с двойной полосой пропускания для подсчета клеток, меченых и FITC (CD31), и родамином (TUNEL). Поля выбирали из явно не некротических областей срезов опухоли, поскольку ксенотрансплантаты НВТ 3477 обычно растут быстро у «голых» мышей, удваивая свои объемы через 6 дней, приводя к центральному некрозу не леченных опухолей. Поскольку TUNEL может метить некротические клетки, хотя менее интенсивно, данная стратегия была выбрана посредством совершенно случайного процесса.
Анализы пролиферации и плотности микрососудов. Срезы толщиной 10 мкм опухолей от не получавших лечение мышей и мышей, получавших лечение пентапептидом cRGD, RIT и способом CMRIT, и умерщвленных через 1, 5 и 6 дней после лечения, фиксировали в течение 10 мин в ледяном ацетоне, споласкивали в PBS и кратковременно инкубировали в метаноле с 0,6% Н2О2 (5 мин). После споласкивания в PBS срезы блокировали в течение 10 мин 10% козлиной сывороткой и 1% бычьим сывороточным альбумином в PBS. Мышиное антитело против Ki67 Mab (Pharmingen, клон В56) вносили в блокирующий раствор (6,25 мкг/мл), и предметные стекла инкубировали при комнатной температуре в течение 2 часов с последующим споласкиванием в PBS. Наносили козье антимышиное, меченное родамином или козье антимышиное, меченное Cy-3 антитело (Jackson ImmunoResearch Laboratories, Inc, West Grove, PA, 1:100), и предметные стекла инкубировали в течение 1 часа при комнатной температуре. После споласкивания в PBS срезы инкубировали в течение 1 часа при комнатной температуре с крысиным антимышиным антителом CD31 (Pharmingen, 1:100) с последующим споласкиванием в PBS и последующей инкубацией в течение 1 часа с козьим антикрысиным антителом, меченым FITC (Pharmingen, 1:50). После споласкивания в PBS предметные стекла подвергали противоокрашиванию DAPI (0,4 мкг/мл), и гистологические препараты заключали в гель Biomeda (Fisher) под покровные стекла. Количественный анализ Ki67 выполняли с использованием микроскопа Olympus при увеличении Х1000 для оценки пролиферации. Среднее общее количество Ki67-положительных клеток/поле в опухоли определяли подсчетами с 6 полей на опухоль, выбранных методом случайной выборки окрашивания DAPI. Плотность микрососудов определяли подсчетом количества сосудов, окрашенных CD31, на случайно выбранное поле при увеличении Х400. Любую эндотелиальную клетку или группу клеток, положительных по CD31, которая была отдельно от соседней группы, считали как один микрососуд. 6 случайно выбранных полей на срез опухоли использовали для установления средней величины для каждой опухоли. Сре