Способ получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов
Иллюстрации
Показать всеИзобретение относится к способу получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов общей формулы (1):
где R=н-C2H5, н-С3Н7, н-C5H11, характеризующемуся тем, что дизамещенный ацетилен общей формулы где R=C2H5, н-С3Н7, н-С5Н11, подвергают взаимодействию с н-BuMgCl в присутствии катализатора цирконацендихлорида Cp2ZrCl2 в мольном соотношении н-BuMgCl:Cp2ZrCl2=10:(22-26):(1.0-1.4) в атмосфере аргона при нормальном давлении в диэтиловом эфире в течение 3 ч с последующим добавлением при 0°С аллилхлорида в количестве 1.1 мольных эквивалента на взятый BuMgCl и CuCl в количестве 0.1 мольный эквивалент на взятый ацетилен с последующим перемешиванием реакционной массы при комнатной температуре в течение 3-5 часов. Полученные замещенные 4,5,6,7-тетраалкил-1,4,6,9-декатетраены могут найти применение в тонком органическом и металлоорганическом синтезе в качестве исходных полупродуктов при получении комплексов на основе переходных металлов, замещенных тиофенов, фуранов, циклопентадиенов и пиридинов, а также в синтезе биологически активных веществ. 1 табл.
Реферат
Предлагаемое изобретение относится к органической химии, в частности, к способу получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов общей формулы (1):
где R=н-С2Н5, н-С3Н7, н -C5H11.
Предлагаемые соединения могут найти применение в тонком органическом синтезе, в производстве пластификаторов, присадок, полимерных материалов, душистых компонентов, а также в синтезе биологически активных препаратов.
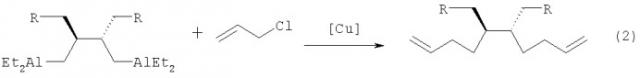
Известен способ (Джемилев У.М., Ибрагимов А.Г., Ажгалиев М.Н., Муслухов P.P. // Изв. АН. Сер. хим., 1995, №8, с.1561) получения трео-5,6-диалкил(арил)-1,9-декадиенов (2) кросс-сочетанием 1,4-диалюминиевых соединений с аллилгалогенидами под действием медных катализаторов по схеме:
Известным способом не могут быть получены 4,5,6,7-тетраалкил-1,4,6,9-декатетраены (1).
Известен способ (Takahashi Т., Kotora M., Kasai К., Suzuki N. // Organometallics, 1994, 13, 4183) получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов (1) взаимодействием цирконациклопентанов с аллилхлоридом в присутствии стехиометрических количеств CuCl по схеме:
Известный способ получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов (1) предполагает использование стехиометрических количеств малостабильного цирконациклопентадиена и однохлористой меди, кроме того, этот процесс энергозатратный, так как при получении цирконациклопентадиена необходимо поддерживать низкую температуру - 78°С.
Предлагается усовершенствованный способ синтеза 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов (1).
Сущность способа заключается во взаимодействии дизамещенных ацетиленов формулы где R=н-С2Н5, н-С3Н7, н-C5H11, с н-BuMgCl в присутствии катализатора цирконацендихлорида Cp2ZrCl2, взятых в мольном соотношении н-BuMgCl: Cp2ZrCl2=10:(22-26):(1.0-1.4), предпочтительно 10:24:1.2, в течение 3 ч с последующим добавлением к реакционной массе при 0°С эфирного раствора аллилхлорида в количестве 1.1 мольных эквивалента по отношению к BuMgCl, затем CuCl в количестве 1 ммоль на 10 ммоль ацетилена, с последующим перемешиванием реакционной массы в атмосфере аргона при комнатной температуре (˜20°С) и атмосферном давлении в течение 3-5 часов. Выход целевых продуктов 52-78%. В качестве растворителя необходимо использовать диэтиловый эфир, в других эфирных растворителях (ТГФ, диоксан) выход целевых продуктов (1) значительно снижается.
Реакция протекает по схеме:
Целевые продукты (1) образуются только лишь с участием дизамещенного ацетилена, н-BuMgCl, аллилхлорида, каталитических количеств Cp2ZrCl2 и CuCl. В присутствии других катализаторов на основе комплексов переходных металлов (например, Zr(acac)4, Ср2TiCl2, Pd(acac)2, Ni(acac)2, Fe(асас)3) целевые продукты (1) не образуются.
Проведение реакции в присутствии катализатора Cp2ZrCl2 больше 1.4 ммоль на 10 ммоль ацетилена не приводит к существенному увеличению выхода целевых продуктов (1). Использование в реакции катализатора Cp2ZrCl2 менее 1 ммоль на 10 ммоль ацетилена снижает выход (1), что связано со снижением каталитически активных центров в реакционной массе. Опыты проводили при комнатной температуре ˜20°С. При более высокой температуре (например, 50°С) увеличивается содержание продуктов уплотнения, при меньшей температуре (например, 0°С) снижается скорость реакции.
Изменение соотношения исходных реагентов в сторону увеличения содержания н-BuMgCl или аллилхлорида не приводит к значительному повышению выхода целевых продуктов (1). Снижение количества н-BuMgCl или аллилхлорида уменьшает выход МОС (1).
Существенные отличия предлагаемого способа.
1. В предлагаемом способе для получения целевого продукта (1) используют в качестве исходных реагентов доступные н-BuMgCl и аллилхлорид, каталитические количества Cp2ZrCl2 и CuCl. В известном способе целевой продукт (1) получают из стехиометрических количеств малостабильного цирконациклопентадиена и стехиометрических количеств CuCl. При этом цирконациклопентадиен предварительно получают из стехиометрических количеств Cp2ZrCl2, крайне пирофорного бутиллития и дизамещенных ацетиленов при температуре -78°С.
Предлагаемый способ обладает следующими преимуществами.
1. Способ позволяет получать 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов (1) с использованием не стехиометрических, а каталитических количеств Cp2ZrCl2 и CuCl.
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 1.2 ммоль Cp2ZrCl2, 10 ммоль гекс-4-ина и при температуре ˜0°С 24 ммоль н-BuMgCl (1.8 М раствор в Et2O). Перемешивают при комнатной температуре 3 часа. Далее реакционную массу охлаждают до 0°С, добавляют 26.4 ммоль аллилхлорида и 1 ммоль CuCl. Температуру доводят до комнатной и перемешивают 4 часа. Получают индивидуальный 4,5,6,7-тетраэтил-1,4,6,9-декатетраен (1) с выходом 63%.
Спектральные характеристики 4,5,6,7-тетраэтил-1,4,6,9-декатетраена (1).
| Спектр ЯМР 13С (δ, м.д.): 12.49, 14.37, 22.11, 22.68, 31.45, 118.29, 128.13, 129.75, 137.47 |
Другие примеры, подтверждающие способ, приведены в таблице 1.
| Таблица 1 | ||||
| №№ п/п | Мольное соотношение :BuMgCl:аллихлорид: CuCl:Cp2ZrCl2, ммоль | Общее время реакции, ч | Выход (1), % | |
| 1 | гекс-3-ин | 10:24:26.4:1:1.2 | 7 | 63 |
| 2 | " | 10:26:28.6:1:1.2 | 7 | 68 |
| 3 | " | 10:22:24.2:1:1.2 | 7 | 57 |
| 4 | " | 10:24:26.4:1:1.4 | 7 | 78 |
| 5 | " | 10:24:26.4:1:1.0 | 7 | 52 |
| 6 | " | 10:24:26.4:1:1.2 | 8 | 65 |
| 7 | " | 10:24:26.4:1:1.2 | 6 | 59 |
| 8 | окт-4-ин | 10:24:26.4:1:1.2 | 7 | 60 |
| 9 | дец-5-ин | 10:24:26.4:1:1.2 | 7 | 58 |
Все опыты проводили при комнатной температуре (˜20°С) в диэтиловом эфире.
Способ получения 4,5,6,7-тетраалкил-1,4,6,9-декатетраенов общей формулы (1):
,
где R=н-C2H5, н-С3Н7, н-С5Н11, характеризующийся тем, что дизамещенный ацетилен общей формулы где R=C2H5, н-C3H7, н-С5Н11, подвергают взаимодействию с H-BuMgCl в присутствии катализатора цирконацендихлорида Cp2ZrCl2 в мольном соотношении н-BuMgCl:Cp2ZrCl2=10:(22-26):(1,0-1,4) в атмосфере аргона при нормальном давлении в диэтиловом эфире в течение 3 ч с последующим добавлением при 0°С аллилхлорида в количестве 1,1 мольных эквивалента на взятый BuMgCl и CuCl в количестве 0,1 мольный эквивалент на взятый ацетилен с последующим перемешиванием реакционной массы при комнатной температуре в течение 3-5 ч.