Производные бензо{b}{1,4}диоксепина
Иллюстрации
Показать всеОбъектом настоящего изобретения являются новые производные бензо{b}{1,4}диоксепина формулы (I)
,
в которых В, X, Y, Z, R1 и R2 принимают значения, указанные в описании изобретения, а также их фармацевтически приемлемые соли. Объектами настоящего изобретения также являются фармацевтические композиции, содержащие эти соединения, для лечения и/или профилактики заболеваний, модулируемых ингибиторами АССβ. 2 н. и 18 з.п. ф-лы, 1 табл.
Реферат
Объектом настоящего изобретения являются новые производные бензо[b][1,4]диоксепина формулы
,
в которых
В является -C≡C- или -CHR3-O-;
R3 является водородом или (С1-С3)алкилом;
X, Y и Z являются C-R4 или азотом, причем хотя бы одна из групп X, Y и Z является C-R4;
R4 является водородом или (С1-С7)алкилом;
R1 и R2 независимо друг от друга выбраны из группы, включающей водород,
(С1-С7)алкил, (С1-С7)алкокси(С1-С7)алкил,
-COOR5 или -COR5, где R5 является водородом или (С1-С7)алкилом,
-OR6, где R6 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
-(СН2)m-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR7, где R7 является водородом или (С1-С7)алкилом, причем m принимает значения 0, 1, 2 или 3, а n принимает значения 1, 2 или 3;
-SR8, где R8 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
или -(CH2)m-гетероциклилом, причем m принимает значения 0, 1, 2 или 3;
-CONR9R10, где R9 и R10 являются водородом или (С1-С7)алкилом, или где NR9R10 может образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл может необязательно включать один или более дополнительных атомов азота или кислорода,
и пятичленный гетероароматический цикл, содержащий от 1 до 4 гетероатомов, выбранных из азота, кислорода или серы, замещенный водородом или (С1-С7)алкилом;
или R1 и R2 совместно с атомами углерода, к которым они присоединены, могут образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл необязательно включает один или более атомов азота или кислорода;
и их фармацевтически приемлемые соли.
Как было обнаружено, соединения формулы I применимы в качестве ингибиторов человеческой ацетилкоэнзим-А-карбоксилазы (АСС), а также стимулируют окисление жирных кислот в печени и мышцах, что делает их пригодными для применения в качестве лекарственных средств в связи с такими заболеваниями, как, например, диабет, ожирение и дислипидемия.
Ацетилкоэнзим-А-карбоксилазы (АСС, ЕС 6.4.1.2) катализируют образование малонилкоэнзима А (малонил-КоА) и регулируют окисление и биосинтез жирных кислот (A.W.Alberts, P.R.Vagelos в Ферменты, под ред. Р.D.Boyer, Academic Press New York 1972, т.6, 37-82). В организме млекопитающих существуют две изоформы АСС. АСС1 или АССα является цитозольным ферментом, и опосредованное им образование малонил-КоА является важной стадией в биосинтезе жирных кислот с длинной цепью. В то же время АСС2 или АССβ является митохондриальным ферментом, и образуемый при ее посредстве малонил-КоА регулирует окисление жирных кислот посредством сильного ингибирования митохондриального фермента карнитинпальмитоилтрансферазы I, который переносит производные ацил-КоА с длинной цепью из цитозоля в митохондрии для окисления (J.D.McGarry и N.F.Brown, Eur.J.Biochem. 1997, 244, 1). Мыши, испытывающие недостаток в АСС2, демонстрируют повышенную по сравнению с нормальной скорость окисления жирных кислот и пониженные содержание жиров в организме и массу тела (L.Abu-Elheiga, M.M.Matzuk, К.А.Н.Abo-Hashema, S.J.Wakil, Science 2001, 291, 2613-2616).
Предполагается, что АССβ регулирует окисление жирных кислот в митохондриях (Ruderman и др., Am.J.Physiol. 276, E1-E18, 1999) и что АССβ также связана с различными заболеваниями (Abu-Elheiga и др., Science 291, 2613-2616, 2001). Ингибиторы АСС, как представляется, пригодны для применения в качестве лекарственных средств, в частности, для лечения и/или профилактики заболеваний, связанных с АССβ. Более того, они могут применяться для лечения и/или профилактики заболеваний, связанных с пониженной скоростью окисления жирных кислот, таких как ожирение, дислипидемии и диабет.
Одно из возможных применений относится к нарушениям обмена веществ, при которых проблемой является низкий уровень окисления жирных кислот в печени, таким как, например, высокие уровни жирных кислот в крови, высокие уровни триглицеридов (TG) в крови, дислипидемии в форме нарушений липопротеидного профиля, дисбаланс липопротеидов очень низкой плотности (VLDL), липопротеидов низкой плотности (LDL) и липопротеидов высокой плотности (HDL), сверхсинтез связанных с VLDL триглицеридов в печени и сосудистые заболевания, связанные с вышеперечисленными метаболическими нарушениями, включая атеросклероз, повышенное давление и сердечно-сосудистые осложнения.
Соответственно ингибиторы АССβ могут быть также применимы в качестве лекарственных средств в связи с метаболическими осложнениями, при которых проблемой является низкий уровень окисления жирных кислот в скелетных мышцах, таких как высокие уровни триглицеридов в мышцах, повышенные уровни реакционноспособных сложных эфиров жирных кислот, таких как ацил-КоА с жирным ацильным радикалом с длинной цепью, карнитин-КоА и диацилглицерин (DAG) в мышцах, низкая чувствительность или нечувствительность мышц к действию инсулина вследствие высоких уровней триглицеридов или повышенных уровней реакционноспособных сложных эфиров жирных кислот в мышцах, нарушенная переносимость глюкозы как следствие пониженной чувствительности к инсулину, прогрессирующие стадии низкой чувствительности к инсулину, приводящие к гиперинсулинемии и резистентности к инсулину, дальнейшие следствия резистентности к инсулину, такие как высокие уровни глюкозы в крови (гипергликемия) и развитие неинсулинзависимого сахарного диабета (NIDDM, диабет типа 2), дальнейшие следствия, вызванные гипергликемией, например, диабетические капиллярные заболевания в форме нефропатии, невропатии, перерождения сетчатки и слепоты.
Ингибиторы АССβ также могут применяться в качестве лекарственных средств в связи с медицинскими показаниями, при которых повышенное окисление жирных кислот считается благотворным, таких как синдромы, связанные с ожирением, например, повышенные запасы эндогенных липидов (жиров), нарушенный контроль аппетита и потребления пищи вследствие низкой усваиваемости липидов и постоянного истощения запаса углеводов, сохранение запаса углеводов, снижение необходимости в восполнении запаса углеводов, потеря аппетита, длительный контроль и поддержание массы тела у всех субъектов с генетической или поведенческой склонностью к пониженному окислению жиров.
Среди вышеупомянутых заболеваний особенный интерес вызывает применение соединений формулы (I) в качестве лекарственных средств в связи с ожирением в качестве средства повышения окисления жирных кислот в митохондриях в мышцах и печени и общего увеличения расходования энергии в периферической (мышечной) ткани в связи с дислипидемией в качестве средства снижения (восстановления равновесия) выработки человеческой печенью связанных с липопротеидами очень низкой плотности триглицеридов (VLDL-TG) и в связи с резистентностью к инсулину и диабетом типа 2 в качестве средства снижения высоких уровней триглицеридов в периферической ткани и снижения повышенных концентраций высокореакционноспособных сложных эфиров жирных кислот, таких как ацил-КоА, карнитин-КоА, диацилглицерин (DAG).
Целью настоящего изобретения является, таким образом, предложить соединения, которые должны отвечать вышеупомянутым критериям. Было обнаружено, что соединения формулы (I) по настоящему изобретению демонстрируют потенциальную способность к селективному ингибированию АССβ. Объектами настоящего изобретения также являются способ получения соединений формулы (I), равно как и применение соединений формулы (I) для опосредованных действием ингибиторов АССβ контроля или профилактики заболеваний и соответственно их применение для изготовления соответствующих лекарственных средств.
Если это не оговорено иначе, нижеследующие определения представлены для иллюстрации и определения значения и границ охвата различных терминов, используемых в контексте для описания изобретения.
Термин «низший алкил» или «(С1-С7)алкил», сам по себе или в сочетании с другими группами, относится к разветвленному или неразветвленному одновалентному алкильному радикалу, содержащему от одного до семи атомов углерода, предпочтительно от одного до четырех атомов углерода. Этот термин может быть далее проиллюстрирован на примере таких радикалов, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, а также тех групп, примеры которых специально приведены в контексте.
Термин «галоид» («галоген») относится к фтору, хлору, брому и иоду.
Термин «алкоксигруппа» относится к группе R'-O-, в которой R' является алкилом. Термин «низшая алкоксигруппа» или «(С1-С7)алкоксигруппа» относится к группе R'-O-, в которой R' является низшим алкилом. Примерами низших алкоксигрупп являются, например, метоксигруппа, этоксигруппа, пропоксигруппа, изопропоксигруппа, бутоксигруппа, изобутоксигруппа и гексилоксигруппа. Предпочтительными являются те низшие алкоксигруппы, примеры которых специально приведены в контексте.
Термин «циклоалкил» или «(С3-С7)циклоалкил» означает насыщенную карбоциклическую группу, содержащую от 3 до 7 атомов углерода, такую как циклопропил, циклобутил, циклопентил, циклогексил или циклогептил.
Термин «гетероциклильный радикал» означает насыщенную гетероциклическую группу, состоящую из одного или более цикла, предпочтительно из одного иди двух циклов, где на каждый цикл приходится от трех до восьми атомов, и включающую один, два или три находящихся в циклах гетероатома (выбранных из азота, кислорода или S(O)0-2), каковая группа может быть необязательно моно- или полизамещенной, в частности, моно- или дизамещенной, галоидом, CF3, низшим алкилом и/или низшей алкоксигруппой. Примерами гетероциклических групп являются оксиранильная, морфолинильная, пиперазинильная, пиперидинильная, пирролидинильная, тетрагидропиранильная, тиоморфолинильная или хинуклидинильная группы. Предпочтительными являются те гетероциклильные группы, примеры которых специально приведены в контексте.
Термин «пятичленный гетероароматический цикл, содержащий от одного до четырех гетероатомов, выбранных из азота, кислорода или серы, замещенный водородом или (С1-С7)алкилом», относится к ароматическому пяти- или шестичленному циклу, который может содержать 1, 2, 3 или 4 атома, выбранных из азота, кислорода и/или серы, охватывая такие радикалы, как фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, триазолил, оксадиазолил, тетразолил, оксатриазолил, пентазолил и их дигидропроизводные. Гетероарильная группа может быть необязательно замещена (С1-С7)алкилом. Предпочтительными являются те гетероарильные группы, примеры которых специально приведены в контексте.
Термин «защитная группа» относится к группам, таким как, например, ацильная, алкоксикарбонильная, арилоксикарбонильная, силильная или иминогруппа, которые используются для того, чтобы временно блокировать реакционную способность функциональных групп. Хорошо известными защитными группами являются, например, сложноэфирные группы с низшим алкильным, β-триметилсилилэтильным и β-трихлорэтильным радикалом, которые могут быть использованы для защиты карбоксигрупп.
Термин «фармацевтически приемлемые соли» охватывает соли соединений формулы (I) с фармацевтически приемлемыми основаниями, такие как соли щелочных металлов, например, натриевые и калиевые соли, соли щелочноземельных металлов, например, кальциевые и магниевые соли, и соли аммония или замещенных аммонийных катионов, такие как, например, соли триметиламмония. Термин «фармацевтически приемлемые соли» также относится к подобным солям.
Соединения формулы (I) также могут быть сольватированы, например, гидратированы. Сольватация может быть осуществлена в ходе процесса получения или может произойти, например, вследствие гигроскопических свойств изначально безводного соединения формулы (I) (гидратация). Термин «фармацевтически приемлемые соли» также включает фармацевтически приемлемые сольваты.
Термин «фармацевтически приемлемые сложные эфиры» относится к сложному эфиру соединения формулы (I), содержащего доступную карбоксигруппу, который может подвергнуться гидролизу in vivo. Более конкретно, в том случае, когда группа (группы) R1 и/или R2 являются группами вида COOR5, R5, может являться не только водородом или низшим алкилом, но может быть подходящим образом преобразована в иные фармацевтически приемлемые и легко гидролизуемые остатки.
Более подробно, объектом настоящего изобретения являются соединения формулы (I)
,
в которых
В является -C≡C- или -CHR3-O-;
R3 является водородом или (С1-С3)алкилом;
X, Y и Z являются C-R4 или азотом, причем хотя бы одна из групп X, Y и Z является C-R4;
R4 является водородом или (С1-С7)алкилом;
R1 и R2 независимо друг от друга выбраны из группы, включающей водород,
(С1-С7)алкил, (С1-С7)алкокси(С1-С7)алкил,
-COOR5 или -COR5, где R5 является водородом или (С1-С7)алкилом,
-OR6, где R6 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
-(СН2)m-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR7, где R7 является водородом или (С1-С7)алкилом, причем m принимает значения 0, 1, 2 или 3, а n принимает значения 1, 2 или 3;
-SR8, где R8 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
или -(СН2)m-гетероциклилом, причем m принимает значения 0, 1, 2 или 3;
-CONR9R10, где R9 и R10 являются водородом или (С1-С7)алкилом, или где
NR9R10 может образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл необязательно включает один или более дополнительных атомов азота или кислорода,
и пятичленный гетероароматический цикл, содержащий от 1 до 4 гетероатомов, выбранных из азота, кислорода или серы, замещенный водородом или (С1-С7)алкилом;
или R1 и R2 совместно с атомами углерода, к которым они присоединены, могут образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл необязательно включает один или более атомов азота или кислорода;
и их фармацевтически приемлемые соли.
Предпочтительными соединениями формулы (I) по настоящему изобретению являются такие соединения формулы (I), в которых какая-либо из групп R1 или R2 является водородом.
Предпочтительными также являются такие соединениями формулы (I), в которых R1 или R2 выбраны из группы, включающей
(С1-С7)алкил, (С1-С7)алкокси(С1-С7)алкил,
-COOR5, где R5 является (С1-С7)алкилом,
-OR6, где R6 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
-(CH2)m-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR7, где R7 является водородом или (С1-С7)алкилом, причем m принимает значения 0, 1, 2 или 3, а n принимает значения 1, 2 или 3;
-SR8, где R8 является (С1-С7)алкилом,
-CONR9R10, где R9 и R10 являются водородом или (С1-С7)алкилом, или где
NR9R10 может образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл необязательно включает один или более дополнительных атомов азота или кислорода,
и пятичленный гетероароматический цикл, содержащий от 1 до 4 гетероатомов, выбранных из азота, кислорода или серы, замещенный водородом или (С1-С7)алкилом.
Особенно предпочтительными являются такие соединения формулы (I), в которых R1 или R2 выбраны из группы, включающей
(С1-С7)алкил, (С1-С7)алкокси(С1-С7)алкил,
-COOR5, где R5 является водородом или (С1-С7)алкилом,
-OR6, где R6 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом,
-(СН2)m-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR7, где R7 является водородом или (С1-С7)алкилом, причем m принимает значения 0, 1, 2 или 3, а n принимает значения 1, 2 или 3;
-SR8, где R8 является (С1-С7)алкилом.
Более предпочтительными являются такие соединения формулы (I) согласно настоящему изобретению, в которых R1 или R2 являются -COOR5, где R5 является водородом или (С1-С7)алкилом.
Кроме того, предпочтительными являются такие соединения формулы (I), в которых R1 или R2 выбраны из группы, включающей (С1-С7)алкокси-(С1-С7)алкил, -OR6, где R6 является водородом, (С1-С7)алкилом, -(СН2)m-циклоалкилом, -(СН2)m-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR7, где R7 является водородом или (С1-С7)алкилом, причем m принимает значения 0, 1, 2 или 3, а n принимает значения 1, 2 или 3; и -SR8, где R8 является (C1-С7)алкилом.
Также предпочтительными являются такие соединения формулы (I), в которых R1 или R2 являются пятичленным гетероароматическим циклом, содержащим от 1 до 4 гетероатомов, выбранных из азота, кислорода или серы, замещенным водородом или (С1-С7)алкилом.
Соединения формулы (I) согласно настоящему изобретению, в которых R1 и R2 совместно с атомами углерода, к которым они присоединены, могут образовывать цикл, содержащий от 3 до 7 атомов, указанный цикл может необязательно включать один или более атомов азота или кислорода, также являются предпочтительными.
Предпочтительными также являются соединения формулы (I), отвечающие формуле
,
в которой X, Y, Z, R1 и R2 принимают указанные в п.1 формулы изобретения значения, а также их фармацевтически приемлемые соли и/или сложные эфиры.
Особенно предпочтительными являются такие соединения формулы (I-A), в которых X, Y и Z являются -CR4, где R4 является водородом.
Примерами подобных соединений являются нижеследующие:
этиловый эфир 4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)бензойной кислоты;
этиловый эфир 3-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)бензойной кислоты;
3,3-диметил-7-(4-метилсульфанилфенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(4-метоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенол;
7-(4-этоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(4-этоксиметилфенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
2-[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенил]-5-метил[1,3,4]оксадиазол;
7-(4-циклопропилметоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
3,3-диметил-7-(4-пропоксифенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин; и
3,3-диметил-7-(4-оксиранилметоксифенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин.
Также являются предпочтительными такие соединения формулы (I-A), в которых какая-либо одна из групп X, Y или Z является азотом, а остальные являются -CR4, где R4 является водородом.
Примерами подобных соединений являются нижеследующие:
этиловый эфир 6-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)никотиновой кислоты; и
этиловый эфир 5-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)пиридин-2-карбоновой кислоты.
Кроме того, также являются предпочтительными соединения формулы (I), отвечающие формуле,
,
в которой X, Y, Z, R1, R2 и R3 принимают указанные в п.1 формулы изобретения значения, а также их фармацевтически приемлемые соли и/или сложные эфиры.
Особенно предпочтительными являются такие соединения формулы (I-Б), в которых X, Y и Z являются -CR4, где R4 является водородом.
Примерами подобных соединений являются нижеследующие:
этиловый эфир 4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-метокси)бензойной кислоты; и
7-(3-этоксифеноксиметил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин.
Кроме того, следующие соединения являются примерами предпочтительных соединений по настоящему изобретению:
этиловый эфир 4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)бензойной кислоты;
этиловый эфир 3-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)бензойной кислоты;
3,3-диметил-7-(4-метилсульфанилфенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
1-[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)фенил]этанон;
7-(4-метоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(3-метоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенол;
7-(4-этоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-бензо[1,3]диоксол-5-илэтинил-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(2,3-дигидробензофуран-5-илэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенил]-морфолин-4-илметанон;
4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)-N,N-диметилбензамид;
этиловый эфир 6-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)никотиновой кислоты;
7-(4-этоксиметилфенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b] [1,4]диоксепин;
2-[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенил]-5-метил[1,3,4]оксадиазол;
этиловый эфир 5-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-этинил)пиридин-2-карбоновой кислоты;
этиловый эфир 4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-ил-метокси)бензойной кислоты;
7-(4-циклопропилметоксифенилэтинил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-[4-(2-метоксиэтоксифенилэтинил]-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенокси]-ацетонитрил;
3,3-диметил-7-(4-пропоксифенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
3,3-диметил-7-(4-оксиранилметоксифенилэтинил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(4-изопропилфеноксиметил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
3,3-диметил-7-(4-метилсульфанилфеноксиметил)-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(3-этоксифеноксиметил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(4-этилфеноксиметил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин;
7-(4-метоксифеноксиметил)-3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин; и
5-[4-(3,3-диметил-3,4-дигидро-2Н-бензо[b][1,4]диоксепин-7-илэтинил)фенил]-2-метил-2Н-тетразол.
Фармацевтически приемлемые соли соединений формулы I также составляют предпочтительный вариант осуществления настоящего изобретения.
Подразумевается, что соединения общей формулы I по настоящему изобретению могут быть преобразованы в производные по функциональным группам с получением производных, которые способны к обратному преобразованию в исходное соединение in vivo. Физиологически приемлемые и метаболически лабильные производные, способные превращаться в исходные соединения общей формулы (I) in vivo, также входят в объем и сущность настоящего изобретения.
В еще одном варианте осуществления настоящего изобретения его объектом является способ получения соединений формулы (I), как они определены выше, включающий
а) взаимодействие соединений формулы
с арильным или гетероарильным галогенпроизводным формулы
,
в котором Hal является бромом или иодом, а X, Y, Z, R1 и R2 принимают указанные выше значения, с получением соединения формулы
в котором X, Y, Z, R1 и R2 принимают указанные выше значения, или, альтернативно,
б) взаимодействие соединения формулы
с алкином формулы
,
в котором X, Y, Z, R1 и R2 принимают указанные выше значения, с получением соединения формулы
,
в котором X, Y, Z, R1 и R2 принимают указанные выше значения, или, альтернативно,
в) взаимодействие соединения формулы
,
в котором R3 является водородом или (С1-С3)алкилом, с соединением формулы
,
в котором X, Y, Z, R1 и R2 принимают указанные выше значения, с получением соединения формулы
,
в котором X, Y, Z, R1, R2 и R3 принимают указанные выше значения.
Как было описано выше, соединения формулы (I) по настоящему изобретению могут применяться в качестве лекарственных средств для лечения и/или профилактики заболеваний, связанных с АССβ и/или окислением жирных кислот, таких как, например, диабет, в частности, инсулинорезистентный сахарный диабет, повышенные уровни липидов и холестерина, в частности, низкие уровни холестерина HDL, высокие уровни холестерина LDL или высокие уровни триглицеридов, атеросклеротические заболевания, метаболический синдром (синдром X), повышенное кровяное давление, эндотелиальная дисфункция, прокоагулянтное состояние и дислипидемия. Предпочтительным является применение в качестве лекарственного средства для лечения и/или профилактики диабета, в особенности неинсулинзависимого сахарного диабета, ожирения и дислипидемии.
Таким образом, объектом настоящего изобретения являются фармацевтические композиции, содержащие соединение, как оно определено выше, и фармацевтически приемлемый носитель и/или адъювант.
Помимо этого, объектом настоящего изобретения являются соединения, как они определены выше, для применения в качестве терапевтически активных веществ, в частности, в качестве терапевтически активных веществ для лечения и/или профилактики заболеваний, модулируемых ингибиторами АССβ. Примерами таких заболеваний являются диабет, в частности, неинсулинзависимый сахарный диабет, повышенные уровни липидов и холестерина, в частности, низкие уровни холестерина HDL, высокие уровни холестерина LDL или высокие уровни триглицеридов, атеросклеротические заболевания, метаболический синдром (синдром X), повышенное кровяное давление, эндотелиальная дисфункция, прокоагулянтное состояние, ожирение и дислипидемия.
Еще в одном варианте осуществления настоящего изобретения его объектом является способ лечения и/или профилактики заболеваний, модулируемых ингибиторами АССβ, включающий введение соединения формулы (I) человеку или животному. Предпочтительными примерами подобных заболеваний являются диабет, в частности, инсулинорезистентный сахарный диабет, повышенные уровни липидов и холестерина, в частности, низкие уровни холестерина HDL, высокие уровни холестерина LDL или высокие уровни триглицеридов, атеросклеротические заболевания, метаболический синдром (синдром X), повышенное кровяное давление, эндотелиальная дисфункция, прокоагулянтное состояние, ожирение и дислипидемия. Предпочтительным способом, как он определен выше, является такой, когда заболевание является диабетом, более предпочтительно, инсулинорезистентным сахарным диабетом, ожирением или дислипидемией.
Объектом настоящего изобретения является также применение соединений, как они определены выше, для лечения и/или профилактики заболеваний, модулируемых ингибиторами АССβ. Предпочтительными примерами таких заболеваний являются диабет, в частности, неинсулинзависимый сахарный диабет, повышенные уровни липидов и холестерина, в частности, низкие уровни холестерина HDL, высокие уровни холестерина LDL или высокие уровни триглицеридов, атеросклеротические заболевания, метаболический синдром (синдром X), повышенное кровяное давление, эндотелиальная дисфункция, прокоагулянтное состояние, ожирение и дислипидемия. В предпочтительном варианте осуществления настоящего изобретения его объектом является применение, как оно определено выше, в том случае, когда заболевание является диабетом, более предпочтительно, инсулинорезистентным сахарным диабетом, ожирением или дислипидемией.
Кроме этого, объектом настоящего изобретения является применение соединений, как они определены выше, для изготовления лекарственных средств для лечения и/или профилактики заболеваний, модулируемых ингибиторами АССβ. Предпочтительными примерами таких заболеваний являются диабет, в частности, неинсулинзависимый сахарный диабет, повышенные уровни липидов и холестерина, в частности, низкие уровни холестерина HDL, высокие уровни: холестерина LDL или высокие уровни триглицеридов, атеросклеротические заболевания, метаболический синдром (синдром X), повышенное кровяное давление, эндотелиальная дисфункция, прокоагулянтное состояние, ожирение и дислипидемия. Подобные лекарственные средства включают соединение, как оно определено выше.
Соединения формулы (I) могут быть получены с помощью способов, приведенных ниже, с помощью способов, приведенных в примерах, или с помощью аналогичных способов. Подходящие условия реакций для индивидуальных стадий известны специалистам в соответствующей области. Исходные вещества либо являются коммерчески доступными, либо могут быть получены с помощью способов, аналогичных приведенным ниже способам, способов, описанных в цитируемых в тексте ссылках или в примерах, или способов, известных специалистам в соответствующей области.
Соединения формулы (I), в которых В является -C≡C- (производные ацетилена), получают с помощью реакции кросс-сочетания по Соногашире подходящего арильного иод- или бромпроизводного с триметилсилилацетиленом, последующего снятия триметилсилильной защитной группы и еще одной реакции по Соногашире (общие условия для стадии кросс-сочетания: [PdCl2(PPh3)2], CuI, диизопропиламин, тетрагидрофуран (ТГФ), нагревание).
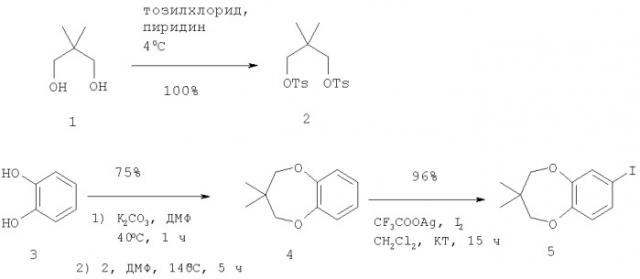
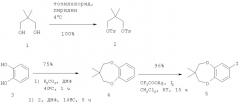
Синтез ключевого арильного иодпроизводного (5) представлен на схеме 1.
7-Иод-3,3-диметил-3,4-дигидро-2H-бензо[b][1,4]диоксепин (5) получают посредством иодирования 3,3-диметил-3,4-дигидро-2H-бензо[b][1,4]диоксепина (4) трифторацетатом серебра в CH2Cl2. 3,3-Диметил-3,4-дигидро-2H-бензо[b][1,4]диоксепин (4) получают согласно М.Klaus, P.Mohr, E. Weiss, заявка на европейский патент ЕР 0350846 А2 (1990).
Схема 1
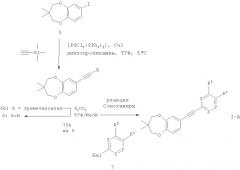
Большинство соединений, рассмотренных в примерах, получают исходя из усовершенствованного ацетиленового промежуточного соединения (6), получаемого исходя из иодпроизводного (5) посредством кросс-сочетания с триметилсилилацетиленом и последующего расщепления триметилсилильного остатка с помощью К2СО3 в смеси ТГФ и метанола (схема 2). В ходе следующей реакции кросс-сочетания по Соногашире соединение (6) вводят в реакцию с подходящим арильным галогенпроизводным или гетероарильным галогенпроизводным вида (7) с целью получения соединения формулы (I-A).
Схема 2
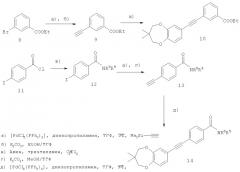
Альтернативно соединения формулы (I) могут быть получены похожим способом посредством обращения порядка реакционных стадий (схема 3). Соединение формулы (9) получают аналогично способу, описанному в Т.Iijima, Y.Endo, M.Tsuji, E.Kawachi, H.Kagechika, К.Shudo, Chem.Pharm.Bull. 1999, 47, 3, 398-404.
Арильные галогенпроизводные или гетероарильные галогенпроизводные (например, 8 и 11), используемые в качестве исходных веществ, являются коммерчески доступными или могут быть получены согласно указанным ниже способам.
Амиды вида (12) получают по реакции хлорангидрида 4-иодбензойной кислоты (11) и соответствующих аминов в СН2Cl2 и триэтиламине.
Схема 3
Бромпроизводное (16) получают исходя из 4-бромбензилбромида (15) в этаноле при кипячении с обратным холодильником (см. схему 4).
Схема 4
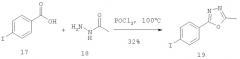
Производное 1,3,4-оксадиазола (19) получают по реакции 4-иодбензойной кислоты (17) и ацетилгидразида (18) в хлорокиси фосфора (POCl3) при температуре 100°С (см. схему 5).
Схема 5
Производное пиридина (22) получают в две стадии исходя из 5-бром-2-метилпиридина (20) путем окисления его до 5-бром-2-пиридинкарбоновой кислоты (21), как это описано в G.M.Sanders, M.van Dijk and Н.С.van der Plas, Heterocycles 1981, 15, 213-223, и хлорирования с помощью SOCl2 с последующей реакцией с EtOH (см. схему 6).
Схема 6
Реакция 4-иодбензонитрила (23) с азидом натрия приводит к производному тетразола (24), которое может быть прометилировано с образованием смеси соединений 25/26. Два региоизомера могут быть легко разделены с помощью флэш-хроматографии (см. схему 7).
Схема 7
Соединения формулы (I) по настоящему изобретению, в которых R1 является -OR5, где R5 является (С1-С7)алкилом, -(СН2)n-циклоалкилом, -(СН2)n-гетероциклилом, -(CH2)n-CN, или -(CH2)n-OR6, где R6 является водородом или (С1-С6)алкилом, могут быть получены путем алкилирования соответствующего производного фенола (27) (см. схему 8).
Схема 8
Соединения формулы (I), в которых В является -СН2О- (производные простых бензиловых эфиров), получают путем алкилирования спирта (31) в условиях по Мицунобу (см. схему 9). Сложный эфир (30) получают исходя из этилового эфира 3,4-дигидроксибензойной кислоты, следуя методике, аналогичной синтезу соединения (4) (М.Klaus, P.Mohr, E.Weiss, заявка на европейский патент ЕР 0350846 А2). Восстановление (30) с помощью диизобутилалюминийгидрида (DIBAL-H) приводит к спирту (31).
Схема 9
Подразумевается, что соединения общей формулы (I) по настоящему изобретению могут быть преобразованы в производные по функциональным группам с целью получения таких производных, которые могут быть преобразованы обратно в исходное соединение in vivo.
Следующие испытания были осуществлены с целью определения активности соединений формулы (I):
Получение и характеристика человеческого фермента АССβ, его применение в анализах активности АСС и исследованиях ингибирования
Клонирование комплементарной ДНК (кДНК) полной длины человеческого АССβ мышечного типа и экспрессию в клетках почек человеческого эмбриона НЕК293 (АТСС, # CRL-1573) осуществляют следующим образом. Амплифицируют кДНК АССβ с помощью полимеразной цепной реакции (PCR) и клонируют ее с помощью стандартных методик для рекомбинантных ДНК. Полимеразную цепную реакцию осуществляют с помощью системы Expand Long Template PCR System (Roche Molecular Biochemicals, # 16818340) и 0,5 нг кДНК из человеческих скелетных мышц в качестве матрицы. Праймеры, используемые для амплификации полимеразной цепной реакции, конструируют на основе опубликованной последовательности человеческой кДНК АССβ, выделенной из библиотеки кДНК человеческой печени (Abul-Elheiga и др. J. Biol Chem. 272, 10669-10677, 1997). Последовательность прямого праймера АССВ1 имеет вид 5'-TTACGCGTGCTAGCCACCATGGTCTTGCTTCTTTGTCTATC-3'; она включает сайт рестрикционного расщепления NheI для субклонирования и консенсусную последовательность Козака инициации трансляции, предшествующую инициирующему кодону ATG. Последовательность обратного праймера АССВ8 имеет вид 5'-TTCTCGAGTCAGGTGGAGGCCGGGCTGTC-3'.
Она включает терминирующий кодон и сайт рестрикционного расщепления XhoI для субклонирования. Амплифицированный фрагмент ДНК размером приблизительно 7,4 тысячи оснований клонируют в экспрессирующий вектор млекопитающих. Получаемые в результате плазмидные изоляты, pRF33A, В, С, D и Е индивидуально трансфецируют в клетки почек человеческого эмбриона 293 (НЕК293), используя стандартный способ трансфекции липидов. Клеточные экстракты трансфецированных клеток получают в буферном растворе для лизиса, содержащем 0,4 мг/мл дигитонина, а ферментативную активность определяют с помощью радиометрического анализа активности АСС, как он описан ниже. Плазмида pRF33D характеризуется наибольшей активност