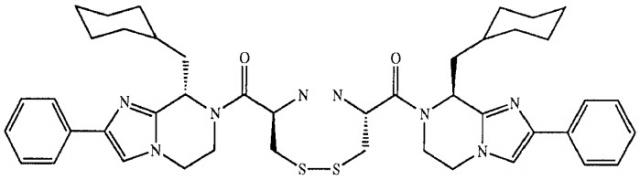
Применение производного дигидроимидазопиразина для лечения или предупреждения боли
Иллюстрации
Показать всеПредложено применение (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8Н)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8Н)-ил]-2-оксоэтиламина или его фармацевтически приемлемых солей для получения лекарственного средства для предупреждения или лечения боли. В частности, боли, спровоцированной нейропатией и/или воспалением, другими хроническими болезнями: раком, радикулопатиями, болезненным ожирением, мигренью, хроническими болезнями, фибромиалгией, алгонейродистрофией или комплексным местным болевым синдромом, сосудистыми поражениями головного мозга, артрозом, артритом, диабетическими нейропатиями или нейропатиями, являющимися следствием ВИЧ, ишиасом, мышечными болезненными сокращениями, интоксикацией, ожогами, постгерпетическими невралгиями, поражениями таламуса или рассеянным склерозом, или пред- и/или послеоперационные боли. Показано снижение порога болевой чувствительности при гиперальгезии и при нейропатии, индуцированной таксолом. 6 з.п. ф-лы, 4 ил.
Реферат
Объектом настоящего изобретения является применение производного дигидроимидазопиразина, а именно (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламина или одной из его фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для предупреждения или лечения боли или болей.
Существуют многочисленные соединения, обладающие анальгетическим эффектом, из которых наиболее известным является морфин.
Однако некоторые больные при лечении такими соединениями могут показывать "толерантность", даже резистентность к вводимой композиции, что проявляется в низкой эффективности соединения. В таком случае необходимо увеличивать вводимые дозы, что может провоцировать вторичные явления.
Для того чтобы отвечать на требования производителей, необходимо находить новые соединения для получения лекарственных средств, предназначенных для предупреждения или лечения боли.
Задача, которую предлагается решить настоящим изобретением, состоит в предоставлении нового соединения, приемлемого для получения лекарственного средства, предназначенного для предупреждения или лечения боли.
Неожиданным образом авторы установили, что возможно использовать (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламин или одну из его фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для предупреждения или лечения боли.
С этой целью в настоящем изобретении предлагается применение (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламина или одной из его фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для предупреждения или лечения боли.
Изобретение обладает определенными преимуществами, в частности применение соединения по настоящему изобретению не вызывает или почти не вызывает седативного эффекта.
Более того, преимущественным образом, поскольку соединение по настоящему изобретению является ингибитором гетеродимерных G-протеинов, его применение по настоящему изобретению позволяет препятствовать действию многих медиаторов, участвующих в механизме боли.
Прочие преимущества и характеристики настоящего изобретения можно выяснить при чтении следующих далее описания и примеров, приведенных только в качестве иллюстрации и не имеющих ограничительного характера.
Настоящее изобретение относится к применению (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламина или одной из его фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для предупреждения или лечения боли.
С целью продолжения описания и облегчения чтения текста (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламин далее упоминается как соединение (I).
Предпочтительно применение по настоящему изобретению позволяет предупреждать или лечить боль, провоцируемую нейропатией и/или воспалением.
Под термином "боль" в смысле настоящего изобретения следует понимать "неприятный эмоциональный и чувственный опыт, ассоциированный с повреждением тканей, имеющийся, или возможный, или описываемый больным подобным образом" (определение согласно International Association for the Study of Pain (IASP)). Далее в настоящей заявке термин "боль" используется независимо для обозначения боли или болевой чувствительности.
Под нейропатией в смысле настоящего изобретения понимают ухудшение функций или патологические изменения, затрагивающие периферическую нервную систему.
Более предпочтительно боль, излечиваемая по настоящему изобретению, провоцируется противораковым лечением, таким как, например, лечение химиотерапией или радиотерапиией.
Еще более предпочтительно применение по настоящему изобретению позволяет предупреждать или лечить боль или боли, провоцируемые раком, в частности боли, связанные с метастазами, такие как, например, боль или боли, связанные с раком простаты, груди, яичников, поджелудочной железы, толстой кишки, легкого или кожи.
Наконец, применение по настоящему изобретению позволяет также предупреждать или лечить боль, связанную с хроническим или острым воспалением, с другими хроническими болезнями, такими как рак, с радикулопатиями, болезненным ожирением, мигренью, хроническими болезнями, фибромиалгией, алгонейродистрофией или комплексным местным болевым синдромом, сосудистыми поражениями головного мозга, артрозом, артритом, диабетическими нейропатиями или нейропатиями, являющимися следствием ВИЧ, ишиасом, мышечными болезненными сокращениями, интоксикацией, ожогами, постгерпетическими невралгиями, поражениями таламуса или рассеянным склерозом.
Наконец, применение по настоящему изобретению позволяет предупреждать или лечить боль или боли, провоцируемые повреждением кожи, или пред- и/или послеоперационные боли, например физические боли при травмах или ампутациях.
Соединение (I) или его соль, используемые по настоящему изобретению, могут быть в форме твердого вещества, например порошков, гранул, таблеток, желатиновых капсул, липосом или суппозиториев. Соответствующими твердыми основами могут быть, например, фосфат кальция, стеарат магния, тальк, сахар, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза натрия, поливинилпирролидин и воск.
Соединение (I) или его соль, используемые по настоящему изобретению, могут находиться также в жидкой форме, например в растворах, эмульсиях, суспензиях или сиропах. Приемлемыми жидкими основами могут быть, например, вода, органические растворители, такие как глицерин или гликоли, а также их смеси с водой в различных пропорциях.
Введение соединения (I) или его соли, используемых по настоящему изобретению, может быть осуществлено топическим, пероральным (р.о.), парентеральным путем внутривенных инъекций (i.v.), внутримышечно (i.m.), подкожно (s.c.) и т.д.
Доза соединения по настоящему изобретению, предусматриваемая для лечения упомянутых ранее болей, варьирует в зависимости от способа введения, возраста и массы тела больного, а также его состояния, и окончательное решение принимает лечащий врач или ветеринар. Такое количество, определенное лечащим врачом или ветеринаром, называется в данном тексте "терапевтически эффективным количеством".
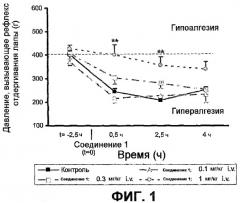
На фиг.1 показан эффект, вызываемый внутривенным введением соединения (I) в модели воспалительной гипералгезии, индуцированной каррагенином.
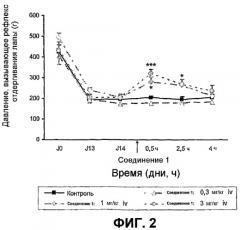
На фиг.2 показан эффект, вызываемый внутривенным введением соединения (I) в модели нейропатии, индуцированной повреждением седалищного нерва.
На фиг. 3 и 4 показан эффект, вызываемый внутривенным или интраперитонеальным введением соединения (I) в модели нейропатии, индуцированной введением противоракового средства.
Настоящее изобретение иллюстрируется следующими далее примерами без ограничения ими его объема.
Фармакологическое исследование соединений по настоящему изобретению
Как было написано ранее, во всем тексте, включая следующие далее примеры, (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8H)-ил]-2-оксоэтиламин упоминается как "соединение (I)".
Соединение (I) соответствует следующей формуле:
Соединение (I)
ПРИМЕР 1
Модель воспалительной гипералгезии, индуцированной каррагенином
Активность соединения (I) или его соли по настоящему изобретению оценивали in vivo В модели воспалительной гипералгезии, индуцированной инъекцией каррагенина в лапу крысы.
Крысы-самцы линии Spraque Dawley (Charles River) массой приблизительно 200 г содержались в клетках от 5 до 8 дней в условиях вивария и не получали на сетке корм в течение 18 ч до эксперимента и во время эксперимента. Были составлены 4 группы не менее чем из 6 животных. Соединения вводили внутривенно (i.v., 1 мл/кг) через 2 ч 30 мин после инъекции каррагенина. Каррагенин с концентрацией 2 мг/0,1 мл вводили путем инъекции в подошву задней правой лапы крысы (каждому животному вводили 0,1 мл). Болевой порог (или ноцицептивный порог) оценивали по рефлексу отдергивания крысой лапы, раздражаемой механическим воздействием с возрастающим давлением (начальное давление 210 г/мм2), прикладываемым посредством аналгезиметра (тест Randall-Selitto). Измерения осуществляли непосредственно перед инъекцией каррагенина (t = -2 ч 30 мин) и затем через 0,5 ч, 2 ч 30 мин и 4 ч после инъекции испытуемого соединения, которую производили при t=0.
Эффективность соединений оценивали по их способности уменьшать в значительной степени гипералгезию, индуцированную каррагенином. Такая эффективность может быть определена статистически в тесте с дисперсионным анализом результатов (первый путь) и/или в тесте Dunnett (второй путь).
Действие соединения (I) на воспалительную гипералгезию, индуцированную каррагенином
Результаты, полученные при использовании разных доз соединения (I) в модели гипералгезии, индуцированной каррагенином в лапе крысы и описанной ранее, представлены на фиг.1.
На фиг.1 результат контрольного опыта показывает значение порога переносимой крысой боли в ее воспаленной лапе при приложении возрастающего давления. На момент введения каррагенина значение этого порога находится в интервале от 370 до 430 г/мм2, затем уменьшается, указывая на то, что чем более воспаленной и болезненной является лапа, тем меньшее приложенное к ней давление переносит крыса.
Действие соединения (I) показывает, что порог переносимой крысой боли в ее воспаленной лапе возрастает по мере увеличения введения соединения (I) до значительных доз. Начиная с дозы 1 мг/кг (i.v.) соединения (I), значение порога боли, вызываемой механическим воздействием, прикладываемым к лапам крысы, значительно увеличивается, достигая приблизительно 400 г/мм2 против 240 г/мм2 в контрольном опыте при времени 0,5 ч. Это позволяет доказать анальгетическую активность, зависящую от дозы соединения (I), в данном испытании с гипералгезией, индуцированной каррагенином.
Была определена эффективная доза (ЕD50) Под ЕD50 понимают дозу, уменьшающую наполовину боль, индуцированную в испытуемой модели.
ED50 составляет 0,42 мг/кг при времени 0,5 ч в модели гипералгезии, индуцированной каррагенином.
ПРИМЕР 2
Модель нейропатии, индуцированной повреждением седалищного нерва (или по-английски "chronic constriction injury")
Активность соединения (I) или его соли по настоящему изобретению оценивали in vivo в модели нейропатии, индуцированной в лапе крысы повреждением седалищного нерва.
Крысы-самцы линии Spraque Dawley (Charles River) массой приблизительно 200 г содержались в клетках в течение 6 дней в условиях вивария. Перед началом эксперимента (нулевой день) болевой порог (или ноцицептивный порог) оценивали по рефлексу отдергивания крысой лапы, раздражаемой механическим воздействием (начальное давление 210 г/мм2), прикладываемым посредством аналгезиметра (тест Randall-Selitto). Это значение представляет собой базовое значение порога боли. Затем, в тот же нулевой день, у крыс вызывали нейропатию повреждением седалищного нерва по методу Bennett и Xies (1988): накладывали 4 лигатуры с промежутками приблизительно 2 мм (монокриловая нить: 5,0) на седалищный нерв правой лапы крысы выше точки трифуркации. Данную операцию проводили под общей анестезией изофлюраном. На 13-й день после хирургической операции из 32 прооперированных крыс отобрали наиболее чувствительных к боли, измеряя давление, вызывающее рефлекс отдергивания крысой лапы, раздражаемой механическим воздействием с возрастающим давлением (начальное давление 210 г/мм2), прикладываемым посредством аналгезиметра (тест Randall-Selitto). По результатам, позволившим отобрать 28 наиболее чувствительных крыс, были составлены 4 группы по 7 животных. На 14-й день после операции порог боли оценивали снова. Затем внутривенно (i.v.) вводили соединение (I) с 3 разными концентрациями. Измерения осуществляли через 0,5, 2,5 и 4 ч после инъекции соединения (I). В контрольной группе производили инъекцию жидкостного наполнителя (раствор NaСl, 0,9%, в г/100 мл) в тех же условиях, что и испытуемое соединение.
Эффективность соединений оценивали по их способности уменьшать в значительной степени боль, индуцированную повреждением седалищного нерва. Такая эффективность может быть определена статистически в тесте с дисперсионным анализом результатов (первый путь) и/или в тесте Dunnett (второй путь).
Действие соединения (I) на нейропатию, индуцированную повреждением седалищного нерва
Результаты, полученные при использовании разных доз соединения (I) в модели нейропатии, индуцированной в лапе крысы повреждением седалищного нерва и описанной ранее, представлены на фиг.2.
На фиг.2 результат контрольного опыта показывает значение порога переносимой крысой боли в ее лапе при приложении к ней возрастающего давления. В нулевой день (до повреждения) это значение составляет 420 г/мм2, затем уменьшается, достигая на 13-й день приблизительно 200 г/мм2. Эти результаты указывают на то, что при повреждении лапа становится болезненной и крыса переносит с большей трудностью приложение давления к лапе.
Введение соединения (I) показывает, что порог переносимой крысой боли в ее поврежденной лапе возрастает пропорционально дозам соединения (I). Начиная с дозы 3 мг/кг (i.v.) соединения (I), значение порога боли, вызываемой механическим воздействием, прикладываемым к лапам крысы, значительно увеличивается, достигая приблизительно 320 г/мм2 против 200 г/мм2 в контрольном опыте при времени 0,5 ч. Это позволяет доказать анальгетическую активность, зависящую от дозы соединения (I), в данном испытании с нейропатией, индуцированной повреждением седалищного нерва.
Была определена эффективная доза (ЕD50). Под ЕD50 понимают дозу, уменьшающую наполовину боль, индуцированную в испытуемой модели.
ЕD50 составляет 2,5 мг/кг при времени 0,5 ч в модели нейропатии, индуцированной повреждением седалищного нерва.
ПРИМЕР 3
Модель нейропатии, индуцированной введением противоракового средства
Активность соединения (I) или его соли по настоящему изобретению оценивали in vivo в модели нейропатии, индуцированной в лапе крысы введением противоракового средства (паклитаксел (таксол)).
Крысы-самцы линии Spraque Dawley (Charles River) массой приблизительно 200 г содержались в клетках в течение 6 дней в условиях вивария. Были составлены 3 группы не менее чем из 10 животных.
Нейропатию индуцировали интраперитонеальной инъекцией (i.p.) 2 мг/кг паклитаксела (экстракт из Taxus Yannanensis) в дни J0, J2, J4 и J7.
Перед первой инъекцией крыс нумеровали и взвешивали, а болевую чувствительность оценивали по приложению механического воздействия с возрастающим давлением: приложение начального давления (210 г/м2) к обеим задним лапам крысы производили посредством аналгезиметра по методу Randall-Selitto. Такие измерения позволяют определять базовые значения до развития нейропатии (J0).
Уменьшение ноцицептивного порога, соответствующего степени нейропатии, является максимальным между 16-м и 24-м днями после первой инъекции паклитаксела. Порог болевой чувствительности обеих задних лап крысы уменьшается похожим образом, позволяя усреднить значения для облегчения расчетов. Таким образом, исследование воздействия на нейропатию следует проводить между 16-м и 24-м днями.
В день проведения эксперимента крыс взвешивали, измеряли болевую чувствительность и животных, не проявлявших развитую нейропатию на этот день (уменьшение болевой чувствительности по сравнению с измерением на день J0), исключали из исследования. Вводили испытуемое соединение и измеряли болевую чувствительность в разное время после его введения.
Действие соединения (I) на нейропатию, индуцированную таксолом
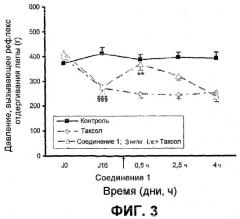
Результаты, полученные при использовании разных доз соединения (I) в модели нейропатии, индуцированной таксолом и описанной ранее, представлены на фиг.3.
На фиг.3 результат контрольного опыта показывает значение порога переносимой крысой боли при приложении возрастающего давления к ее лапам. В нулевой день это значение составляет 400 г/мм2, затем уменьшается, достигая на 16-й день значения приблизительно 270 г/мм2. Эти результаты указывают на то, что после инъекции i.р. паклитаксела чувствительность лап крыс увеличивается при приложении давления к лапам.
Введение соединения (I) показывает, что порог переносимой крысой боли в ее лапах после индуцирования паклитакселом нейропатии увеличивается при введении соединения (I) с дозой 3 мг/кг (i.v.). Значение порога боли, вызываемой механическим воздействием, прикладываемым к лапам крысы, значительно увеличивается, достигая приблизительно 370 г/мм2 против 250 г/мм2 в опыте только с паклитакселом при времени 0,5 ч. Это позволяет доказать анальгетическую активность соединения (I) в данном испытании с нейропатией, индуцированной систематическим хроническим введением паклитаксела.
На фиг.4 результат контрольного опыта показывает значение порога переносимой крысой боли при приложении возрастающего давления к ее лапам. В нулевой день это значение составляет 450 г/мм2, затем уменьшается, достигая на 16-й день значения приблизительно 235 г/мм2. Эти результаты указывают на то, что после инъекции i.р. паклитаксела чувствительность лап крыс увеличивается при приложении давления к лапам.
Введение соединения (I) показывает, что порог переносимой крысой боли в ее лапах после индуцирования паклитакселом нейропатии увеличивается при введении соединения (I) с дозой 100 мг/кг (р.о.). Значение порога боли, вызываемой механическим воздействием, прикладываемым к лапам крысы, значительно увеличивается, достигая приблизительно 400 г/мм2 против 240 г/мм2 в опыте только с паклитакселом при времени 1 ч. Это позволяет доказать анальгетическую активность соединения (I) в данном испытании с нейропатией, индуцированной систематическим хроническим введением паклитаксела.
1. Применение (1R)-1-[({(2R)-2-амино-3-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8Н)-ил]-3-оксопропил}дитио)метил]-2-[(8S)-8-(циклогексилметил)-2-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8Н)-ил]-2-оксоэтиламина или одной из его фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для предупреждения или лечения боли.
2. Применение по п.1, отличающееся тем, что боль спровоцирована нейропатией и/или воспалением.
3. Применение по п.1, отличающееся тем, что боль спровоцирована противораковым лечением.
4. Применение по п.3, отличающееся тем, что противораковое лечение представляет собой лечение химиотерапией или радиотерапией.
5. Применение по п.1, отличающееся тем, что боль спровоцирована раком, как, например, боль, связанная с раком простаты, груди, яичников, поджелудочной железы, толстой кишки, легкого или кожи.
6. Применение по п.1, отличающееся тем, что боль связана с хроническим или острым воспалением, с другими хроническими болезнями, такими как рак, с радикулопатиями, болезненным ожирением, мигренью, хроническими болезнями, фибромиалгией, алгонейродистрофией или комплексным местным болевым синдромом, сосудистыми поражениями головного мозга, артрозом, артритом, диабетическими нейропатиями или нейропатиями, являющимися следствием ВИЧ, ишиасом, мышечными болезненными сокращениями, интоксикацией, ожогами, постгерпетическими невралгиями, поражениями таламуса или рассеянным склерозом.
7. Применение по п.1, отличающееся тем, что боль спровоцирована повреждением кожи или представляет собой пред- и/или послеоперационные боли.