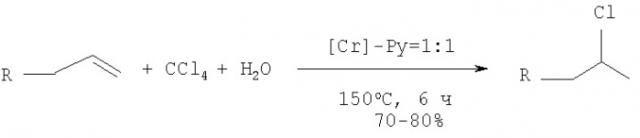Способ получения хлоралканов и хлорциклоалканов гидрохлорированием ненасыщенных соединений
Иллюстрации
Показать всеИзобретение относится к способу получения хлоралканов и хлорциклоалканов путем гидрохлорирования ненасыщенных соединений под действием хромсодержащих катализаторов Cr(асас)3, Cr(НСО2)3 и Cr(СО)6, активированных пиридином, в среде четыреххлористого углерода и воды при температуре 150°С в течение 6 ч, при мольном соотношении [Cr]:[пиридин]:[олефин]:[CCl4]:[H2O]=1:1:100:100:2000. Технический результат - выход монохлоралканов и циклоалканов составляет 70-90%.
Реферат
Изобретение относится к области органической химии, в частности, к способу получения хлоралканов и хлорциклоалканов гидрохлорированием олефинов.
Процессы гидрохлорирования имеют большое теоретическое и практическое значение. Каталитическое присоединение хлористого водорода к ненасыщенным соединениям лежит в основе многотоннажных процессов синтеза хлорорганических продуктов: этилхлорида, винилхлорида, метилхлороформа и др. Полученные при этом хлорпарафины используются в полимерных композициях в качестве пластификаторов, в промышленности синтетических строительных материалов, лаков и красок, искусственных пленок и кож, в резиновой промышленности, а также в качестве огнезамедляющих добавок к различным полимерам.
Как известно, в промышленности и лабораторной практике в качестве катализаторов гидрохлорирования (присоединения к кратной связи), в зависимости от природы олефинового субстрата используются кислоты Льюиса, прежде всего, галогениды алюминия (Houben-Weyl. Methoden der organishen Chemie. V.5. IV Ed., G. Tieme Verloag. Stuttgart, pt 3. s.s. 99, 812 (1960) [1]), олова, титана и цинка (Mousseron М., Manon G., Combes G. Bull. Soc. chim. France. 392-396 (1949) [2]).
В большинстве промышленных процессов катализатором гидрохлорирования служит хлористый алюминий (AlCl3), в частности, он используется в производстве хлористого этила из этилена и хлористого водорода (HCl) (Справочник нефтехимика. В двух томах. Т.2. / Под ред. Огородникова С.Н. - Л.: Химия, 1978. - 592 с.[3]). AlCl3 катализирует присоединение НСl к этилену, начиная с 80°C. Однако из экономических соображений реакцию проводят при 35°C и давлении 8 атм (для обеспечения жидкофазного состояния продуктов реакции). Смесь газов HCl и этилена (1:1) при 35-38°C пропускают через раствор катализатора хлористого алюминия AlCl3 в хлористом этиле или в более высококипящем растворителе. Степень превращения обоих реагентов (HCl и этилен) практически полная, а выход хлористого этила составляет ~90%.
Существенные недостатки метода:
1. Низкая производительность и большой расход катализатора. Оптимальное мольное соотношение [AlCl3]: [этилен] составляет 1:10÷50. Кроме того, хлористый алюминий постоянно выносится из реакционной зоны, разлагается водой и теряется безвозвратно.
2. Образование большого количества отходов в виде сточных вод, которые необходимо утилизировать.
3. Образование НСl при гидролизе катализатора AlCl3 водой
4. Необходимость использования дорогостоящего, коррозионно-стойкого оборудования, рассчитанного для работы под давлением (до 8 атм). Для защиты от коррозии поверхность реактора покрывают платиной или танталом.
Особенностью хлорида цинка как катализатора гидрохлорирования является использование в качестве растворителя бензола [2]:
Хлорид цинка имеет следующие недостатки:
1. Низкая производительность и вследствие этого большой расход катализатора (реакция проводится при мольном соотношении ZnCl2:HCl=1:11).
2. Большой расход токсичного растворителя бензола (для получения 116 г хлорциклооктана необходимо 400 мл растворителя).
3. Образование значительного количества отходов: бензола, непрореагировавшего циклооктена, ZnCl2, воды; утилизация этих отходов требует больших трудо- и энергозатрат.
4. Значительная продолжительность реакции (12.5 ч).
Известные катализаторы гидрохлорирования на основе соединений Ti и вышеупомянутые катализаторы, а также галогениды Sn, В имеют сходные недостатки.
Высокую активность при гидрохлорировании олефинов проявили комплексные соединения родия - Rh(acac)3, Rh(PPh3)3Cl, [Rh(CO)2Cl]2 (Хуснутдинов Р.И., Щаднева Н.А., Джемилев У.М., Толстиков Г.А. Изв. АН СССР. Сер. хим. №6, 1373-1377 (1991) [4]).
Отличительной особенностью родийсодержащих катализаторов является то, что необходимый для реакции HCl генерируется из хлористого метилена (CH2Cl2), т.е., по существу, комплексы родия катализируют два превращения:
1) контролируемое разложение CH2Cl2 с образованием HCl
2) присоединение образовавшегося HCl к кратной связи
Активная форма Rh-содержащего катализатора гидрохлорирования готовится предварительным нагреванием комплекса родия в растворе CH2Cl2 в автоклаве при 200°C в течение 2-3 ч. Реакция гидрохлорирования олефинов (пропилена, гексена, циклогексена) с заведомо приготовленным катализатором проводится при 100°C в течение 3 ч. Выходы хлорсодержащих продуктов достигают 70-91%.
Гидрохлорирование олефинов с помощью CH2Cl2 как источника HCl под действием Rh-содержащих катализаторов можно проводить и без предварительной активации, но в этом случае необходимы более жесткие условия: 200°C, 3-5 ч. Эти условия менее предпочтительны, т.к. способствуют протеканию побочных процессов (теломеризация, изомеризация двойной связи), что приводит к уменьшению селективности гидрохлорирования и снижению выхода целевых продуктов.
Недостатки метода:
1. Дороговизна солей родия.
2. Активность родийсодержащих катализаторов проявляется в жестких условиях (активация проводится при 200°C в течение 3 ч, а реакция - при 200°C в течение 3-5 ч). Общая продолжительность процесса гидрохлорирования с учетом времени подготовки активной формы катализатора составляет 5-8 ч. Таким образом, для проведения реакции требуются большие энерго- и трудозатраты.
Наиболее близким к изобретению является способ гидрохлорирования ненасыщенных соединений, в котором используется катализатор, содержащий соединения двух- или трехвалентного железа и металлического титана (Хуснутдинов Р.И., Латыпов В.Н., Муслимов З.С., Джемилев У.М. Катализатор для гидрохлорирования ненасыщенных соединений. Патент РФ №2152254 (2000) [5]).
Количественный состав катализатора гидрохлорирования: соли железа - 1 моль, титан металлический (порошок, стружки, пластины) - 0.1÷10 молей по отношению к соли железа. В качестве солей железа использовались FeCl2, FeBr2, FeSt3, Fe(acac)3, Fe(нафтенат)3, Fe(OAc)2, Fe(C7H15CO2)3, Fe(C6H5CO2)3 и др. Железо-титановый катализатор так же, как и его Rh- содержащий аналог, способствует разложению хлористого метилена или хлороформа с образованием свободного HCl и последующему его присоединению к кратной связи.
Активную форму катализатора готовят нагреванием смеси солей железа и металлического титана в растворе CH2Cl2 или CHCl3 при 200°C в течение 0.5-1 ч. Приготовленный таким способом катализатор позволяет проводить гидрохлорирование олефинов при 50-70°C в течение 1 ч в соответствующие хлорпроизводные с общим выходом 70-80%.
Прототип имеет следующие недостатки:
1. Дороговизна металлического титана (10 г гранулированного титана по каталогу фирмы "Acros organics" (2004-2005 гг.) стоит ~130 €), а стоимость 25 г титана кристаллического достигает ~86 € (порошок 100 г - 46 €).
2. Необходимость активации катализатора при высокой температуре (200°С) в автоклаве перед проведением основной реакции.
3. Взаимодействие Ti с HCl приводит к образованию TiCl4, дымящего на влажном воздухе с образованием HCl и TiO2.
4. Чувствительность катализатора к воде и кислороду.
5. Проведение реакции в коррозионно-стойких реакторах.
В связи с этим перед авторами стояла задача найти новый катализатор для гидрохлорирования ненасыщенных соединений, который должен быть растворим в органических растворителях, устойчив к воздействию кислорода и воды, дешев и доступен, должен иметь высокую активность и селективность по хлорсодержащим соединениям и обеспечить высокий выход целевых продуктов.
Это достигается тем, что гидрохлорирование ненасыщенных соединений осуществляется под действием хромсодержащих катализаторов - Cr(асас)3, Cr(HCO2)3 и Cr(СО)6 в присутствии пиридина (Ру) в качестве лиганда-активатора в среде четыреххлористого углерода (ССl4) и воды при температуре 150°C в течение 6 часов, при мольном соотношении [Cr]:[Ру]:[олефин]:[CCl4]:[H2O]=1:1:100:100:2000.
В оптимальных условиях выход хлорпроизводных углеводородов составляет 70-90%.
R=C3,C7
[Cr]=Cr(acac)3, Cr(HCO2)3, Cr(CO)6
n=3, 4, 8, 10.
Гидрохлорирующим агентом в реагенте CCl4-H2O-Cr(асас)3 является HCl, который образуется по следующей схеме:
В пользу такой схемы свидетельствуют присутствие в системе хлороформа (метод ГЖХ) и хлорноватистой кислоты (HOCl), обнаруженной методом йодометрического титрования.
Существенные отличия предлагаемого способа от прототипа.
1. Для получения хлорсодержащих соединений гидрохлорированием олефинов используются доступные, устойчивые к действию кислорода и воды хромсодержащие катализаторы.
Преимущества предлагаемого способа.
1. Высокий выход целевых продуктов.
2. Доступность катализаторов, которые стабильны в обычных условиях и могут храниться длительное время без потери активности и не требуют предварительной активации.
3. Доступность гидрохлорирующих агентов: CCl4 и H2O.
4. Способ позволяет решить важную экологическую проблему по утилизации CCl4. В ходе реакции четыреххлористый углерод превращается в хлороформ, на который не распространяется действие Монреальского протокола по защите озонового слоя Земли.
Предлагаемый способ поясняется примерами:
ПРИМЕР 1. В микроавтоклав из нержавеющей стали (V=17 мл) или стеклянную ампулу (V=20 мл) (результаты параллельных опытов не отличаются) помещали 0.1 ммоль Cr(асас)3, 0.1 ммоль пиридина (Ру), 10 ммоль гексена-1, 10 ммоль четыреххлористого углерода (CCl4) и 200 ммоль воды, автоклав закрывали (ампулу запаивали) и нагревали при 150°C в течение 6 ч при перемешивании. После окончания реакции микроавтоклав (ампулу) охлаждали до комнатной температуры, вскрывали, органический слой отделяли, водный экстрагировали хлористым метиленом (5 мл × 3), экстракты объединяли с основным слоем, фильтровали через слой Al2O3 (II степени активности), растворитель отгоняли, остаток перегоняли при атмосферном давлении. Выход 2-хлоргексана 80%, т.кип. 123-123.5°C, nD 20 1.4142 (лит.: т.кип. 123°C - Словарь органических соединений, т.1. Под ред. Хейльброн И. и Бэнбери Г.М. - М., 1949, С.473 [6]. Найдено, %: С 59.66; Н 10.81; Cl 29.53. С6Н13Сl. Вычислено, %: С 59.74; Н 10.86; Cl 29.40.
ПРИМЕР 2. Гидрохлорирование децена-1 и выделение продуктов реакции проводили по методике, описанной выше. Выход 2-хлордекана 72%, т.кип.105°C/10 мм рт.ст. (лит.: т.кип. 233°C [6]). Масс-спектр, m/z (J отн. (%)): [М]+нет, 29 (48), 39 (22), 40 (5), 41 (89), 42 (36), 43 (100), 53 (6), 54 (8), 55 (81), 56 (41), 63 (7), 67 (7), 68 (7), 69 (67), 70 (60), 71 (16), 82 (10), 83 (24), 84 (25), 85 (7), 96 (6), 97 (25), 98 (14), 105 (7), 111 (18), 112 (11), 140 (5). Найдено, %: С 67.48; Н 11.90; Cl 20.62. C10H21Cl. Вычислено, %: С 67.96; Н 11.98; Cl 20.06.
ПРИМЕР 3. Гидрохлорирование циклопентена и выделение продуктов реакции проводили по методике, указанной в примере 1. Выход циклопентилхлорида 90%, т.кип.114°C. Спектр ЯМР 13С δ, м.д.: 61.82 (С-1), 37.30 (С-2, С-5), 23.25 (С-3, С-4). Найдено, %: С 56.98; Н 8.62; Cl 34.40. C5H9Cl. Вычислено, %: С 57.42; Н 8.67; Cl 33.91.
ПРИМЕР 4. В микроавтоклав из нержавеющей стали (V=17 мл) помещали 0.1 ммоль Cr(СО)6, 10 ммоль циклогексена, 10 ммоль CCl4 и 200 ммоля H2O, автоклав закрывали и нагревали при 150°C в течение 6 ч при перемешивании. После окончания реакции реакционную смесь обработали как указано в примере 1. Выход циклогексилхлорида 90%, т.кип. 141°C-141.5°C (лит.: т.кип. 142°C [6]). Спектр ЯМР 13С δ, м.д.: 59.74 (С-1), 36.52 (С-2), 24.69 (С-3), 25.08 (С-4), 24.69 (С-5), 36.59 (С-6). Масс-спектр, m/z (J отн. (%)): 118 [М]+ (2), 83 (24), 82 (62), 81 (11), 68 (6), 67 (100), 66 (9), 56 (9), 55 (45), 54 (36), 53 (11), 51 (5), 42 (7), 41 (51), 40 (7), 39 (28), 38 (5). Найдено, %: С 60.65; Н 9.75; Сl 29.60. C6H11Cl. Вычислено, %: С 60.75; Н 9.35; Cl 29.90.
ПРИМЕР 5. Гидрохлорирование циклооктена и выделение продуктов реакции проводили по методике, указанной в примере 4. Выход циклооктилхлорида 88%, т.кип. 58°C/10 мм рт.ст. Спектр ЯМР 13С δ, м.д.: 62.91 (С-1), 35.60 (С-2, С-8), 24.25 (С-3, С-7), 28.22 (С-4, С-6), 25.67 (С-5). Найдено, %: С 65.43; Н 10.28; С1 24.29. C8H15Cl. Вычислено, %: С 65.51; Н 10.31; Сl 24.18.
ПРИМЕР 6. В стеклянную ампулу (V=20 мл) помещали 0.1 ммоль Cr(HCO2)3, 0.1 ммоль пиридина, 10 ммоль циклододецена, 10 ммоль CCl4 и 200 ммоль H2O, ампулу запаивали и нагревали при 150°C в течение 6 ч. После окончания реакции ампулу вскрывали и реакционную массу обрабатывали как в примере 1. Выход хлорциклододекана 70%, т.кип. 93-94°C/1 мм рт.ст.(лит.: 87-90°C/0.4-0.5 мм рт.ст. (Traynham J.G., Stone D.W., Couvillion J.L. J. Org. Chem. t. 32, 510 (1967)[7])). Спектр ЯМР 13C δ, м.д.: 62.64 (С-1), 30.63 (С-2, С-12), 24.87 (С-3, С-11), 28.29 (С-4, С-10), 26.82 (С-5, С-6, С-7, С-8, С-9). Найдено, %: С 70.95; Н 11.32; Cl 17.73. C12H23Cl. Вычислено, %: С 71.08; Н 11.43; Cl 17.49.
Способ получения монохлоралканов и циклоалканов каталитическим гидрохлорированием ненасыщенных соединений, отличающийся тем, что в качестве катализаторов используют Cr(асас)3, Cr(HCO2)3, Cr(СО)6, активированных пиридином, реакцию проводят в среде четыреххлористого углерода и воды при мольном соотношении [Cr]:[пиридин]:[олефин]:[CCl4]:[H2O]=1:1:100:100:2000 при температуре 150°С в течение 6 ч.