Анетолдитиолтионы и другие дитиолтионы для лечения состояний, связанных с дисфункцией моноаминной нейротрансмиссии
Иллюстрации
Показать всеИзобретение относится к производным дитиолтионов, которые являются ингибиторами моноаминооксидазы, в частности ингибиторами МАО-В. Изобретение также относится к применению указанных соединений в производстве лекарственного средства с полезным эффектом. В вариантах изобретения конкретные соединения используют для получения лекарственного средства для лечения, облегчения или профилактики состояний, связанных с дисфункцией моноаминной нейротрансмиссии. Соединения имеют общую формулу (1)
где
R1 и R2 являются одинаковыми или разными и представляют собой водород, алкил, алкенил, алкинил, арил, тио или алкилтио, или
R1 и R2 могут сами иметь дополнительные заместители, которые выбраны из водорода, алкила, алкенила, алкинила, арила, алкилокси, морфолин-4-илалкокси, пиперидин-1-илалкилокси, алкиламино, диалкиламино, ариламино. 4 н. и 4 з.п. ф-лы, 3 табл.
Реферат
Изобретение относится к производным дитиолтионов в качестве ингибиторов моноаминоксидазы, в частности ингибиторов МАО-В, способам получения таких соединений и к новым промежуточным соединениям, пригодным в синтезе указанных производных дитиолтионов. Изобретение также относится к применению раскрытого здесь соединения в производстве лекарственного средства с полезным эффектом. Полезный эффект раскрыт здесь, или он очевиден специалисту из описания и общего уровня техники. Изобретение также относится к применению соединения изобретения для производства лекарственного средства для лечения или профилактики заболевания или состояния. Более конкретно, изобретение относится к новому применению для лечения заболевания или состояния, раскрытых здесь или очевидных специалисту из описания и общего уровня техники. В вариантах осуществления изобретения конкретные соединения, раскрытые здесь, используются для производства лекарственного средства, применимого для лечения, облегчения состояния или профилактики состояний, связанных с дисфункцией моноаминной нейротрансмиссии.
Ингибиторы митохондриального флавофермента моноаминоксидазы (МАО; ЕС 1.4.3.4) могут повысить уровень норэпинефрина, эпинефрина, допамина, триптамина и серотонина в мозге или других тканях и таким образом вызвать множество фармакологических эффектов, опосредованных их влиянием на эти нейротрансмиттеры.
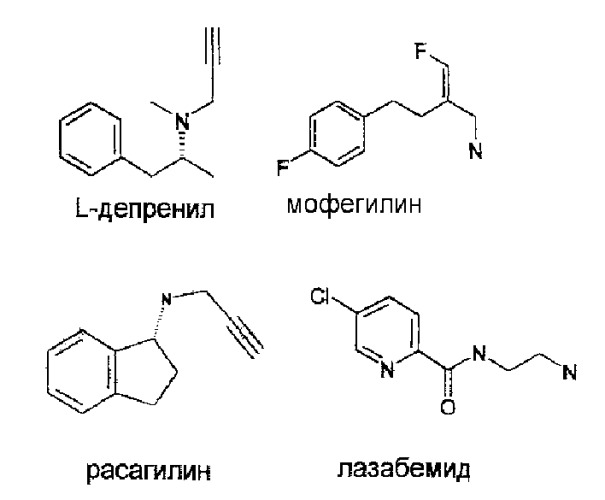
Доступные в настоящее время ингибиторы МАО, такие как L-депренил, мофегилин, расагилин, лазабемид, вызывают широкий набор побочных эффектов, включая психиатрические (делириум, галлюцинации, возбуждение), сердечно-сосудистые (ортостатическую гипертензию, гипертензию) и неврологические (седативное состояние, ненормальные движения).
Целью настоящего изобретения является разработка новых ингибиторов МАО, имеющих другую структуру по сравнению с имеющимися в настоящее время и с меньшими побочными эффектами.
В заявке WO 98/27970 раскрыто применение 1,2-дитиол-3-тионов для лечения заболеваний или профилактики клеточных повреждений, вызванных кислородсодержащими радикалами. В WO 01/091118 раскрыты дитиолтионовые соединения для лечения неврологических заболеваний и улучшения памяти. Было показано, что эти соединения ингибируют оксидазу D-аминокислот (DAAO, E.C. 1.4.3.3) - фермент, который стереоселективно дезаминирует D-аминокислоты с образованием реакционно-способной формы кислорода - пероксида водорода. Ингибирование дитиолтионами совершенно другого фермента - моноаминооксидазы - ранее не было известно.
Неожиданно авторы обнаружили, что дитиолтионы ингибируют активность МАО-В в клеточных экстрактах, полученных из выращенных стриарных астроглиальных клеток крысы, в то время как они не оказывают заметного эффекта на активность МАО-А. Изобретение относится к применению соединений общей формулы (1)
в которой:
- R1 и R2 являются одинаковыми или разными и представляют собой водород, алкил, алкенил, алкинил, арил, фтор, хлор, бром, гидроксил, алкилокси, алкенилокси, арилокси, ацилокси, амино, алкиламино, диалкиламино, ариламино, тиол, алкилтио, арилтио, циано, нитро, ацил, амидо, алкиламидо, диалкиламидо группу, или
- R1 и R2 могут, вместе с атомами углерода, с которыми они связаны, образовывать 5- или 6-членное ароматическое или неароматическое кольцо, содержащее 0, 1 или 2 гетероатома, которые выбирают из азота, кислорода или серы, такие как фуран, тиофен, пиррол, оксазол, тиазол, имидазол, пиразол, изоксазол, изотиазол, 1,2,3-оксадиазол, 1,2,3-триазол, 1,3,4-тиадиазол, пиридин, пиридазин, пиримидин или пиразин,
- R1 и R2 могут сами иметь дополнительные заместители, которые выбирают из водорода, алкила, алкенила, алкинила, арила, фтора, хлора, брома, гидроксила, алкилокси, аминоалкилокси, морфолин-4-илалкокси, пиперидин-1-илалкилокси, алкенилокси, арилокси, ацилокси, амино, алкиламино, диалкиламино, ариламино, тио, алкилтио, арилтио, циано, оксо, нитро, ацила, амидо, алкиламидо или диалкиламидо групп,
и их таутомеров, стереоизомеров и N-оксидов, а также фармакологически приемлемых солей, гидратов и сольватов указанных соединений формулы (1) и их таутомеров, стереоизомеров и N-оксидов для получения фармацевтической композиции для лечения, улучшения состояния или профилактики состояний, связанных с дисфункцией моноаминной нейротрансмиссии.
Изобретение в особенности относится к соединениям общей формулы (1), в которой R1 и R2 являются одинаковыми или разными и представляют собой водород, алкил или арил, необязательно замещенные одним или более атомами или группами, которые выбирают из водорода, алкила, арила, фтора, хлора, брома, гидроксила, алкилокси, арилокси, амино, алкиламино, диалкиламино, тио, оксо или нитро групп.
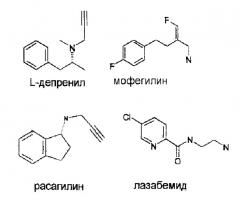
Более конкретно изобретение относится к применению 5-(п-метоксифенил)-3Н-1,2-дитиол-3-тиона (анетолдитиолтион, ADT), 3Н-1,2-дитиол-3-тиона (D3T) и 4-метил-5-(2-пиразинил)-3Н-1,2-дитиол-3-тиона (олтипраз):
Наиболее предпочтительным является применение 5-(п-метоксифенил)-3Н-1,2-дитиол-3-тиона, анетолдитиолтиона (ADT), липофильного замещенного аналога 3Н-1,2-дитиол-3-тиона (D3T), в клинической практике в течение десятилетий в качестве желчегонного и слюновыделяющего средств без каких-либо отмеченных отрицательных реакций (Christen, M-O., Methods Enzymol., 252, 316-323, 1995).
В другом аспекте изобретение относится к соединениям формулы (1):
в которой:
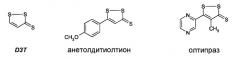
- R1 является необязательно замещенным фенилом и R2 представляет S-CH2-(4-метилфенил) или одну из подгрупп:
в которой n имеет значения 2, 3, 4 или 5 и R3 представляет собой водород или (С1-3)алкил или
- R1 является 4-гексилоксифенилом, и R2 представляет водород, или
- R1 является замещенным фенилом, и R2 представляет SH или подгруппу:
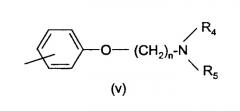
- R1 является водородом, и R2 представляет -СН=СН-4-(диэтиламинофенил), -СН=СН-(2-хинолил) или подгруппу:
в которой n имеет такое же значение, как указано выше, и R4 и R5 независимо представляют собой (С1-3)алкил или вместе с атомом азота, с которым они связаны, образуют насыщенное 5- или 6-членное кольцо, необязательно содержащее один или более гетероатомов, которые выбирают из N, O или S, или
- R1 является (С1-3)алкилом, и R2 представляет 1-(2,3-дигидро-1,4-бензодиоксин-5-ил)пиперазин-4-ил, или
- R1 является цианогруппой, и R2 представляет подгруппу -NH-C(O)-NH-фенил, в которой фенильная группа необязательно замещена или
- R1 является -SO2CH3, и R2 представляет аминогруппу,
и их таутомерам, стереоизомерам и N-оксидам, а также фармакологически приемлемым солям, гидратам и сольватам указанных соединений формулы (1) и их таутомеров, стереоизомеров и N-оксидов.
Изобретение относится к рацематам, смесям диастереомеров, а также к индивидуальным стереоизомерам соединений формулы (1). В описании заместителей аббревиатура «алкил» означает (С1-3)алкил, «алкенил» означает (С1-3)алкенил, «алкинил» означает (С1-3)алкинил, «ацил» означает алкил(С1-3)карбонил, арилкарбонил или арилалкил(С1-3)карбонил и «арил» означает фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, 1,3,5-тиазинил, фенил, индазолил, индолил, индолизинил, изоиндолил, бензо[b]фуранил, бензо[b]тиофенил, (2,3-дигидро-1,4-бензодиоксин-5-ил), бензимидазолил, бензтиазолил, пуринил, хинолинил, изохинолил, хинолил, фталазинил, хиназолинил, хиноксалинил, 1,8-нафтиридинил, птеридинил, нафтил или азуленил, предпочтительно фенил или (2,3-дигидро-1,4-бензодиоксин-5-ил). «(С 1-3 )алкил» означает метил, этил, н-пропил или изопропил, «(С 1-4 )алкил» означает метил, этил, н-пропил, изопропил, н-бутил, 2-бутил, изобутил или 2-метил-н-пропил. «Необязательно замещенный» означает, что группа может быть не замещена или может быть замещена одной или более группами, которые выбирают из алкила, алкенила, алкинила, арила, фтора, хлора, брома, гидроксила, алкилокси, алкенилокси, арилокси, ацилокси, амино, алкиламино, диалкиламино, ариламино, тио, алкилтио, арилтио, циано, оксо, нитро, ацила, амидо, алкиламидо, диалкиламидо, карбоксила, или два необязательных заместителя вместе с атомами углерода, с которыми они связаны, могут образовывать 5- или 6-членное ароматическое или неароматическое кольцо, содержащее 0, 1 или 2 гетероатома, которые выбирают из азота, кислорода или серы. Необязательные заместители могут сами иметь дополнительные необязательные заместители. Предпочтительные необязательные заместители включают (С1-3)алкил, например метил, этил и трифторметил, фтор, хлор, бром, гидроксил, (С1-3)алкокси, например метокси, этокси и трифторметокси и аминогруппу.
Пролекарства указанных выше соединений также входят в настоящее изобретение. Пролекарства являются терапевтическими агентами, которые не активны per se, но превращаются в один или более активных метаболитов. Пролекарства являются биообратимыми производными лекарств, используемых для преодоления некоторых барьеров при использовании исходных молекул лекарств. Эти барьеры включают, но не ограничиваются ими, растворимость, проницаемость, стабильность, пресистемный метаболизм и целевые ограничения (Medicinal Chemistry: Principles and Practice, 1994, ISBN 0-85186-494-5, Ed.: F.D.King, p.215; J.Stella, “Prodrugs as therapeutics”, Expert Opin. Ther. Patents, 14(3), 277-280, 2004; P. Ettmayer et al., “Lessons learned from marketed and investigational prodrugs”, J.Мed.Chem., 47, 2393-2404, 2004). Пролекарства, т.е. соединения, которые при введении людям любым известным способом превращаются в результате метаболизма в соединения формулы (1), входят в изобретение. В частности, это относится к соединениям с первичной или вторичной амино- или гидроксигруппами. Такие соединения могут вступать в реакции с органическими кислотами с образованием соединений формулы (1), где присутствует дополнительная группа, которую легко удалить после введения, например, но не ограничиваясь ими, амидин, енамин, основание Манниха, производное гидроксиметилена, производное О-(ацилоксиметиленкарбамата), карбамат, сложный эфир, амид или енаминон.
N-оксиды указанных выше соединений входят в объем настоящего изобретения. Третичные амины могут привести или не привести к N-оксидам в процессе метаболизма. Доля N-окисления может изменяться от следовых количеств до почти количественной конверсии. N-оксиды могут быть более или менее активны, чем соответствующие третичные амины. В то время как N-оксиды легко химически восстанавливаются в соответствующие третичные амины, в организме человека это происходит в разной степени. Некоторые N-оксиды почти количественно восстанавливаются в соответствующие третичные амины, а в других случаях конверсия является почти следовой или даже полностью отсутствует (M.H. Bickel: “The pharmacology and Biochemistry of N-oxides”, Pharmacological Reviews, 21(4), 325-355, 1969).
Общие принципы синтезов
Выбор конкретного способа синтеза зависит от факторов, известных специалистам в этой области, например от совместимости функциональных групп с использованными реагентами, возможности использования защитных групп, катализаторов, реагентов активации и сочетания и тонких структурных особенностей конечного получаемого соединения.
Фармацевтически приемлемые соли
Фармацевтически приемлемые соли можно получить по хорошо известным стандартным методикам, например смешением соединения настоящего изобретения с подходящей кислотой, например с неорганической кислотой типа хлористоводородной кислоты или с органической кислотой.
Фармацевтические препараты
Соединения данного изобретения могут применяться в подходящих для введения формах с помощью обычных способов с использованием вспомогательных веществ, таких как жидкие или твердые носители. Фармацевтические композиции данного изобретения можно вводить энтерально, перорально, парентерально (внутримышечно или внутривенно), перректально или локально (местно). Их можно вводить в виде растворов, порошков, таблеток, капсул (включая микрокапсулы), мазей (кремов или геля) или суппозиториев. Подходящими эксципиентами для таких препаратов являются обычные фармацевтические жидкие или твердые наполнители и растворители, эмульгаторы, лубриканты, отдушки, красители и/или буферные вещества. Можно назвать такие часто используемые вспомогательные вещества, как карбонат магния, диоксид титана, лактоза, маннит и другие сахара или углеводы, тальк, лактопротеин, желатин, крахмал, целлюлоза и ее производные, животные и растительные масла, такие как рыбий жир, подсолнечное масло, арахисовое или кунжутное масло, полиэтиленгликоль и растворители, такие как, например, стерилизованная вода и моноатомные или многоатомные спирты, такие как глицерин.
Соединения настоящего изобретения обычно вводят в виде фармацевтических композиций, которые представляют собой важные и новые варианты изобретения благодаря присутствию в них таких соединений, более конкретно соединений, раскрытых здесь. Типы фармацевтических композиций, которые можно использовать, включают, но не ограничиваются ими, таблетки, жевательные таблетки, капсулы, растворы, растворы для парентерального введения, суппозитории, суспензии и другие виды, раскрытые здесь или очевидные специалистам из описания и общих знаний уровня техники. В вариантах изобретения предлагается фармацевтическая упаковка или набор из одного или более контейнеров, заполненных одним или более ингредиентами фармацевтической композиции согласно изобретению. К таким контейнерам прилагается письменное сопровождение, такое как инструкции по применению или предписанное правительственным агентством уведомление, регулирующее производство, применение или продажу фармацевтических продуктов, которое содержит аттестацию агентством производства, применения или продажи препарата для введения людям и животным.
Фармакологические методы
Определение МАО активности
В качестве источника активности как МАО-А, так и МАО-В использовали стриарные астроглиальные клетки новорожденной крысы (Carlo et al., Brain Res. 711, 175-183, 1996). Астроглиальные клетки выращивали по известной методике (Langeveld et al., Neurosci. Lett. 192, 13-16, 1995). Через неделю выращивания в культуре в смеси 5% СО2/95% воздух при 37°С клетки были трипсинизированы и обработаны ультразвуком в охлажденном на льду 25 мМ Tris-HCl буфере (pH 7,4), содержащем 1 мМ EDTA. Затем полученные лизаты центрифугировали 5 мин при 10000 g и 4°С и отбирали аликвоты фракции верхнего слоя для определения МАО активности с использованием набора Amplex Red MAO (Molecular Probes, Leiden, The Netherlands) по методике, описанной Zhou and Panchuk-Voloshina (Anal. Biochem. 253, 169-174, 1997). Измерения проводили по инструкциям производителей. Коротко говоря, перед добавлением субстрата образцы инкубировали 30 мин в 96-луночном планшете с лекарствами или растворителем (общий объем 50 мкл). Затем добавили 50 мкл реагента Amplex Red, содержащего 2 мкг/мл пероксидазы хрена (HRP), п-тирамин гидрохлорид (2мМ, субстрат как для МАО А, так и МАО В (Youdim and Finberg, Biochem. Pharmacol., 41, 155-162, 1991) и Amplex Red (10 мМ). В этих условиях благодаря катализируемому МАО окислению тирамина в реакции сочетания с HRP Amplex Red превращается в флуоресцентный резоруфин. Для измерения МАО-активности измеряли зависимое от времени увеличение образования резоруфина через каждые 2 минуты в течение 30 мин при комнатной температуре на микропланшетном флуориметре (BMG Labtechnologies GmbH, Germany), при длине волны возбуждения 544 нм и испускания 595 нм. Было найдено, что в этом временном интервале интенсивность флуоресценции возрастает линейно. Для расчета результатов вносили поправку на интенсивность фона (т.е. в отсутствие субстрата МАО тирамина) и данные выражали в относительных единицах флуоресценции в минуту. Содержание белка определяли по методике Bradford et al. (Anal. Biochem. 72, 248-254, 1976) c использованием BSA в качестве эталона. Статистическое сравнение групп проводили с помощью модели одностороннего дисперсионного анализа ANOVA с последующим тестом Newman-Keuls. Значимыми считали значения Р<0,01.
МАО-В ингибирующую активность соединений A1-D6 определяли в медицинском исследовательском центре CEREP (Париж, Франция) по методике, описанной J.L.Salach, Arch. Biochem. Biophys., 192, 128, 1979.
Анетолдитиолтион и родственные дитиолтионы активны в дозах 0,1-100 мг/кг после перорального введения, и селективное ингибирование моноаминоксидазы-В делает их особенно полезными в лечении психиатрических и/или неврологических заболеваний, вызванных нарушениями основных моноаминергических систем, или эти заболевания можно лечить путем управления этими системами, причем указанные заболевания выбирают из группы, включающей: расстройства настроения, такие как биполярные расстройства I типа, биполярные расстройства II типа и однополярные депрессивные расстройства типа малой депрессии, сезонного аффективного расстройства, послеродовой депрессии, психической депрессии и большой депрессии; тревожные расстройства, включая панические расстройства (с агорафобией или без нее), социальную фобию, обессивно-компульсивные расстройства (с болезненным хроническим тиком или без него и шизофреническое расстройство), посттравматический стресс и генерализированное тревожное расстройство; расстройства, связанные с употреблением наркотиков, включая расстройства, связанные с приемом назначенных лекарственных средств (типа зависимости и злоупотребления), и расстройства, индуцированные употреблением наркотиков (типа синдрома отмены); дефицит внимания и агрессивное поведение, такое как гиперактивность с дефицитом внимания и нарколепсия; расстройства контроля за мотивацией типа патологической игромании; расстройства питания типа нервной анорексии и нервной булимии; тик типа расстройства Tуретта; синдром усталых ног; расстройства, связанные с нарушением познавательной способности и/или памяти, такие как болезнь Альцгеймера, болезнь Паркинсона и слабоумие при СПИДе и/или болезненные психиатрические расстройства и нейрореабилитация (посттравматическое поражение мозга), другие заболевания ЦНС, такие как эпилепсия, синдром Дауна, болезнь Хантингтона, некоторые виды боли, включая головную боль, атипичную лицевую боль, синдром боли и хронической боли; амиотрофический латеральный склероз и сексуальную дисфункцию; расстройства церебральной или периферической сосудистой системы, включая эссенциальную, вазоренальную, легочную или внутриглазную гипертензию, тромбоз, инфаркт миокарда и цереброваскулярный инсульт; расстройства несосудистой гладкой мускулатуры, включая обструкцию дыхательных путей, астму или другие респираторные заболевания, и расстройства сократительной способности желудочно-кишечного тракта, геморрой, спазм сфинктера и гладкой мускулатуры в желудочно-кишечном тракте и дисфункцию мочевого пузыря. Кроме того, ингибиторы МАО могут остановить преждевременные роды и расслабить родовые пути во время родов, они применимы для расслабления мочевых путей при удалении почечных камней и могут быть использованы для снятия контрактуры гладкой мускулатуры и спазм.
Предпочтительно использовать соединения данного изобретения для лечения расстройств настроения, биполярных расстройств I типа, биполярных расстройств II типа, однополярных депрессивных расстройств, малой депрессии, сезонного аффективного расстройства, послеродовой депрессии, психической депрессии, большой депрессии; тревожных расстройств, панического расстройства, социальной фобии, обессивно-компульсивных расстройств, посттравматического стресса, генерализированного тревожного расстройства; расстройств, связанных с употреблением наркотиков; расстройств, связанных с приемом назначенных лекарственных средств; расстройств, индуцированных употреблением наркотиков; синдрома отмены, дефицита внимания и агрессивного поведения, гиперактивности с дефицитом внимания, нарколепсии; расстройства контроля за мотивацией, патологической игромании; расстройства питания, нервной анорексии, нервной булимии; тика, расстройства Tуретта, синдрома усталых ног; боли, головной боли, атипичной лицевой боли, синдрома боли и хронической боли; сексуальной дисфункции; обструкции дыхательных путей, астмы, расстройства сократительной способности желудочно-кишечного тракта, геморроя, спазм сфинктера и гладкой мускулатуры в желудочно-кишечном тракте и дисфункции мочевого пузыря.
Дозировка
Эффективность соединений настоящего изобретения в качестве ингибиторов МАО-В определяли, как описано выше. Из эффективности, определенной для данного соединения формулы (1), можно определить низшую теоретическую эффективную дозу. При концентрации соединения, равной удвоенной измеренной константе ингибирования, фермент вероятно будет ингибироваться соединением на 100%. Переведя эту концентрацию в мг соединения на кг массы пациента, можно определить низшую теоретическую эффективную дозу при условии идеальной биодоступности. С точки зрения фармакокинетики, фармакодинамики и других аспектов можно заменять реально вводимую дозу на более высокую или более низкую. Удобно вводить дозу 0,001-1000 мг/кг, предпочтительно 0,1-100 мг/кг массы тела пациента.
Лечение
Использованный здесь термин «лечение» относится к любому лечению млекопитающих, предпочтительно состояний или заболеваний человека, и включает: (1) профилактику болезни или состояния у пациента, который может быть предрасположен к болезни, но еще не был установлен диагноз, что пациент болен, (2) ингибирование болезни или состояния, т.е. прекращение их развития, (3) облегчение болезни или состояния, т.е. вызов регрессии состояния или (4) облегчение состояний, вызванных болезнью, т.е. прекращение симптомов болезни.
Примеры
Пример 1: вещества и способы
Все реакции с участием соединений, чувствительных к влаге, проводили в атмосфере сухого азота. За ходом реакции следили с помощью тонкослойной хроматографии (ТСХ) на пластиковых пластинках, покрытых силикагелем (Merck silica gel 60 F254) c использованием указанного элюента. Соединения обнаруживали визуально в УФ-свете (254 нм) или с помощью I2. Флэш-хроматографию для очистки соединений проводили на силикагеле Acros (0,030-0,075 мм) с использованием указанного элюента. Спектры ядерного магнитного резонанса (1Н ЯМР и 13С ЯМР, АРТ) записывали в указанном растворителе. Константы взаимодействия J даны в Гц. Формы пиков в спектрах ЯМР обозначены символами «кв» (квартет), «дкв» (двойной квартет), «т» (триплет), «дт» (двойной триплет), «д» (дублет), «дд» (двойной дублет), «с» (синглет), «уш.с» (уширенный синглет) и «м» (мультиплет).
Пример 2: Синтезы конкретных соединений
Конкретные соединения, синтез которых описан ниже, служат для более подробной иллюстрации изобретения и поэтому никоим образом не ограничивают объем изобретения.
| Структура конкретных соединений изобретения | ||
| Соед. | R 1 | R 2 |
| A1 | 4-гексилоксифенил | H |
| A2 | H | |
| A3 | H | |
| B1 | фенил | |
| B2 | 4-метилфенил | |
| B3 | 4-метилфенил | 4-фенилпиперазинил |
| C1 | H | -CH=CH-(4-диэтиламинофенил) |
| C2 | H | -CH=CH-(2-хинолинил) |
| D1 | фенил | -S(CH 2 ) 2 CH(CH 3 )NH-2-пропинил |
| D2 | фенил | -S(CH 2 ) 3 CH(CH 3 )NH-2-пропинил |
| D3 | фенил | -S(CH 2 ) 4 CH(CH 3 )NH-2-пропинил |
| D4 | фенил | -S(CH 2 ) 4 CH(CH 3 )N(CH 3 )-2-пропинил |
| D5 | фенил | -S(CH 2 ) 3 CH(CH 3 )N(CH 3 )-2-пропинил |
| D6 | фенил | -S-CH 2 -(4-метилфенил) |
Другие варианты изобретения будут очевидны специалистам из анализа описания и практики раскрытого здесь изобретения. Описание и примеры следует рассматривать только как иллюстративные, а истинный объем и сущность изобретения определяется формулой изобретения.
Coединение A1
Стадия i cхемы A.1.
32 г (1 моль) серы добавили к 150 мл ДМФА (N,N-диметилформамид) и полученную смесь нагревали при кипении с обратным холодильником до почти полного растворения серы. По каплям добавили 43,6 г (200 ммоль) 2-(4-н-гексилоксифенил)пропена. После этого продолжали перемешивание и нагревание реакционной смеси с последующим анализом методом ТСХ (тонкослойной хроматографии, элюент: толуол), затем в течение 4 ч смеси дали остыть до комнатной температуры. После фильтрации реакционной смеси и упаривания в вакууме получали остаток, который хроматографировали на колонке (SiО2, элюент: толуол). Объединенный продукт, содержащий фракции, концентрировали в вакууме, остаток перекристаллизовывали из циклогексана и получили 5 г (8,1%) нужного соединения A1. Температура плавления: 121°C.
Соединение A2
Стадия i схемы A.2
К раствору 2 экв этилата натрия (NaOEt) в абсолютном этаноле добавили 1 экв 4-гидроксиацетофенона с 1 экв N-(2-хлорэтил)морфолина. После этого реакционную смесь кипятили с обратным холодильником в течение 5 ч, затем нагревание прекратили и перемешивание продолжали 12 ч при комнатной температуре. Растворитель удалили в вакууме, остаток поместили в водный раствор хлористого водорода (~2 н.) и полученный раствор промыли диэтиловым эфиром. Водный слой нейтрализовали раствором гидроксида натрия (~2 н.), после чего экстрагировали диэтиловым эфиром. Объединенные органические вытяжки сушили (Na2SO4). Осушитель удаляли фильтрацией и растворитель удаляли в вакууме и получали простой фенольный эфир в виде оранжево-желтого масла с выходом 91%.
Стадия ii схемы А.2 (согласно Thuiller et al., Bull. Chim. Soc., (1959) 1398)
К холодному абсолютированному толуолу, содержащему 2 экв трет-амилата натрия (NaOC(CH3)2CH2CH3), добавили 1 экв простого фенольного эфира со стадии i и 1 экв раствора дисульфида углерода. Затем реакционную смесь перемешивали 6 ч. После этого добавили 1 экв 1,2-дибромэтана и перемешивание продолжали 12 ч. Реакционную смесь промыли водным раствором гидроксида натрия (~2 н.) и водой до рН 7. Органическую фракцию сушили над Na2SО4. Осушитель удаляли фильтрацией и растворитель удаляли в вакууме и получали чистое производное 1,3-дитиолана в виде оранжевых кристаллов с выходом 70%.
Стадия iii cхемы A.2
Производное дитиолана со стадии ii обработали тетрафосфордекасульфидом (P4S10) в ксилоле при кипячении с обратным холодильником в течение 15 мин. После охлаждения суспензию промыли водным 1 н. раствором гидроксида натрия, затем добавили хлороформ и полученную органическую фракцию сушили над Na2SО4. Осушитель отфильтровали и растворитель удалили в вакууме и получили остаток, который очищали хроматографией на колонке (SiО2, элюент: диэтиловый эфир/толуол 1/1), нужное соединение A2 получили в виде оранжевых кристаллов с выходом 4%. Температура плавления: 102°C. Спектр 1H ЯМР (CDCl3, δ м.д.): 2,59 (т, 4H), 2,83 (т, 2H), 3,73 (т, 4H), 4,17 (т, 2H), 6,98 (д, 2H), 7,60 (д, 2H), 7,36 (с, 1H).
Соединение A3 (красное масло, спектр 1H ЯМР (CDCl3, δ м.д.): 1,49 (кв, 2H), 1,67 (т, 4H), 2,63 (т, 4H), 2,97 (т, 2H), 4,24 (т, 2H), 7,00 (д, 2H), 7,38 (с, 1H), 7,60 (д, 2H)) получали по методике, аналогичной той, которая была описана для соединения A2.
Соединение B1
Стадия i схемы B.1 .
2 экв пиперазина и 1 экв 5-метилсульфанил-4-фенил-[1,2]-дитиол-3-тиона (Grandin, A. et al., Bull.Soc.Chim.Fr., 11(1968)4555) растворили в абсолютном этаноле и реакционную смесь кипятили с обратным холодильником. Через 7 суток растворитель удалили в вакууме и остаток очищали хроматографией (SiО2; элюент 2% этанола в толуоле, об./об.). Собранные фракции сконцентрировали в вакууме, остаток перекристаллизовали из ацетона и получили оранжевые кристаллы с выходом 12%: соединение B1. Температура плавления: 174°C. Спектр 1H ЯМР (CDCl3, δ м.д.): 2,97 (т, 4H), 3,44 (т, 4H), 4,23 (м, 4H), 6,42-6,76 (м, 3H), 7,34-7,49 (м, 5H).
Соединение B2 (желтые кристаллы, температура плавления 108°C, спектр 1H ЯМР (CDCl3, δ м.д.): 2,37 (с, 3H), 2,98 (т, 4H), 3,45 (т, 4H), 4,23 (м, 4H), 6,43-6,76 (м, 3H), 7,22-7,28 (м, 4H)) получали по методике, аналогичной той, которая описана для соединения B1.
Соединение B3 (красные кристаллы, температура плавления 148-150°C с разл.) получали по методике, аналогичной той, которая описана для соединения B1.
Соединение C1
Стадия i схемы C.1.
1 г (6,8 ммоль) 5-метил-[1,2]-дитиол-3-тиона растворили в 50 мл абсолютного этанола. Затем добавили 2,5 г (14,1 ммоль) 4-(диэтиламино)бензальдегида и 1 мл пиперидина, после чего реакционную смесь нагревали на водяной бане в течение 2 ч. Реакционную смесь сконцентрировали в вакууме и остаток поместили в морозильник, где образовались кристаллы. Кристаллы отделили и перекристаллизовали из изопропилового спирта и получили 1,5 г (4,9 ммоль, 35%) нужного соединения C1, температура плавления: 130°C. См. также патент JP1319477.
Соединение C2 (ТСХ (SiО2, элюент толуол), Rf=0,36 в присутствии исходных веществ), получали по методике, аналогичной той, которая описана для соединения C1.
Соединение D1
Стадия i схемы D.1.
17,5 г (87,9 ммоль) 1-бром-2-фенилпропана растворили в 300 мл ДМФА, после чего добавили 14,1 г (441 ммоль) серы. Реакционную смесь кипятили с обратным холодильником в течение ночи, после чего продолжали перемешивание при комнатной температуре еще в течение ночи. Реакционную смесь сконцентрировали в вакууме и затем добавили ~100 мл толуола, образовавшиеся кристаллы собрали и высушили в вакууме. Выход: 13 г (45,3 ммоль, 52%) желтого твердого вещества, содержащего диметиламмониевую соль 4-фенил-5-меркапто-[1,2]-дитиол-3-тиона.
Стадия ii схемы D.1.
3,5 г (10,4 ммоль) иодида (синтез иодида см. ниже) растворили в 40 мл метанола и затем добавили 3 г (10,4 ммоль) диметиламмониевой соли (со стадии i). Реакционную смесь перемешивали в течение ночи, после чего сконцентрировали в вакууме и остаток хроматографировали на колонке (SiО2, элюент: гептан/этилацетат 6/1). После концентрирования фракций, содержащих продукт, получили 700 мг (1,6 ммоль, 15%) в виде красного масла.
Стадия iii схемы D.1.
700 мг (1,6 ммоль) продукта со стадии ii растворили в небольшом количестве дихлорметана, затем добавили некоторое количество 7 н. HCl (в изопропаноле) до конечной концентрации примерно 3 н. Реакционную смесь перемешивали в течение ночи, затем сконцентрировали в вакууме и получили 265 мг оранжевого твердого вещества, содержащего D1.HCl, температура плавления 243°C.
Соединение D2 (температура плавления: 96-101°C с разл.), получали по методике, аналогичной той, которая описана для соединения D1. Используемый иодид можно синтезировать так же, как при получении соединения D1 (см. ниже).
Соединение D3 (температура плавления: 82-87°C) получали по методике, аналогичной той, которая описана для соединения D1. Используемый иодид можно синтезировать так же, как при получении соединения D1.
Соединение D4 (температура плавления: 65-70°C с разл.) получали по методике, аналогичной той, которая описана для соединения D1. Используемый иодид можно синтезировать так же, как при получении соединения D1.
Соединение D5 (температура плавления: 65-72°C), готовили по методике, аналогичной той, которая описана для соединения D1. Используемый иодид можно синтезировать так же, как при получении соединения D1.
Соединение D6 (температура плавления: 134-135°C) получали по методике, аналогичной той, которая описана для соединения D1, исходя из пара-бромметилтолуола в качестве алкилирующего реагента.
Синтез иодида, используемого для получения соединения D1 (схема D.2).
Стадия i схемы D.2.
6,4 г (72,6 ммоль) 4-гидрокси-2-бутанона растворили в 250 мл 1,2-дихлорэтана и добавили 5,5 мл (80 ммоль) пропаргиламина. Реакционную смесь перемешивали 10 мин и затем охладили до 0°C. К реакционной смеси добавили порциями 20 г (94 ммоль) NaBH(OAc)3, перемешивание продолжали 48 ч, после чего смесь вылили в насыщенный водный раствор NaHCО3. После экстракции полученного водного раствора метиленхлоридом и концентрирования в вакууме получили 3 г нужного продукта. Водный слой подщелочили раствором NaOH (33%, водн.), насытили NaCl (тв.) и повторно проэкстрагировали этилацетатом. Комбинированные органические вытяжки сушили (Na2SО4) и после удаления осушителя фильтрацией и удаления растворителя путем концентрирования в вакууме получили 7,6 г (82%) нужного продукта (в виде оранжевого масла). Его использовали на стадии ii без дополнительной очистки.
Стадия ii схемы D.2.
7,6 г (59,8 ммоль) производного аминопропанола (со стадии i) растворили в 200 мл метиленхлорида и добавили 9,2 мл (~65 ммоль) триэтиламина и 14 г (65 ммоль) (Boc)2О (Boc=трет-бутилоксикарбонил). Полученную смесь перемешивали в течение ночи и концентрировали в вакууме и остаток снова растворили в этилацетате. Органическую фракцию промыли насыщенным раствором NaHCО3 (водн.), водой и насыщенным раствором хлорида натрия, затем сушили над Na2SО4. Отфильтровали осушитель, удалили растворитель концентрированием в вакууме и получили 13,7 г (100%) коричневого масла, содержащего аминопропанол с защитной N-Boc группой.
Стадия iii схемы D.2.
33 г (126 ммоль) трифенилфосфина растворили в 600 мл метиленхлорида, добавили 19 г (280 ммоль) имидазола и полученную смесь охладили до 0°C. К реакционной смеси добавили по каплям раствор 35,5 г (140 ммоль) иода в 300 мл метиленхлорида и перемешивали 10 мин. Затем растворили 8 г (35 ммоль) аминопропанола, содержащего защитную группу N-Boc (со стадии ii) в 50 мл метиленхлорида, и перемешивали при 0°C в течение 20 мин. Затем реакционной смеси дали остыть до комнатной температуры и перемешивали 16 ч. Реакционную смесь профильтровали, фильтрат промыли насыщенным раствором хлорида натрия и концентрировали в вакууме. Остаток «отфильтровали» через короткую колонку с SiО2 (элюент: гептан/EtOAc 6/1), элюат сконцентрировали в вакууме и получили 5,1 г (%) соответствующего иодида в виде светло-желтого масла. Этот иодид использовали для получения соединения D1 (см. схему D.1).
Соответствующие иодиды, необходимые для получения соединений D2, D3, D4 и D5, можно получить в условиях, описанных в синтезах иодида, использованного при получении D1 (схема D.2). Для соединений D4 и D5 стадии защиты и снятия защиты (N-Boc) не являются необходимыми из-за присутствия метильной группы при атоме азота.
Пример 3: препарат соединения A1
Для перорального (p.o.) введения: к нужному количеству (0,5-5 мг) твердого соединения А1 в стеклянной трубке добавили несколько стеклянных шариков и твердое вещество размололи, вращая его в течение 2 мин. После добавления 1 мл 1% раствора метилцеллюлозы в воде и 2% (об./об.) Poloxamer 188 (Lutrol F68) соединение суспендировали, перемешивая в течение 10 мин. Установили pH 7 добавлением нескольких капель водного NaOH (0,1 н.). Оставшиеся в суспензии частицы затем суспендировали на ультразвуковой бане.
Для в