Амидное производное и лекарственное средство
Иллюстрации
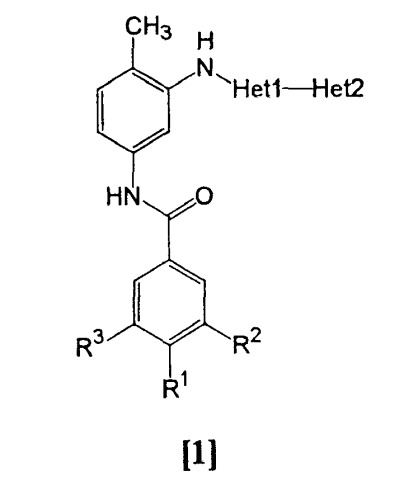
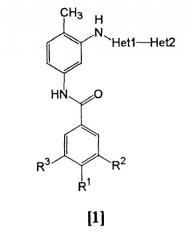
Показать всеИзобретение относится к новым амидным производным общей формулы [1] в любой из версий (А) или (В) или его фармацевтически приемлемой соли, которые обладают свойствами ингибитора тирозинкиназы BCR-ABL и могут найти применение для лечения хронического миелолейкоза, острого лимфобластного лейкоза и острого миелобластного лейкоза. Амидное производное общей формулы [1] представляет собой соединение:
где согласно версии (A) R1 представляет собой любую из следующих групп (1)-(3):
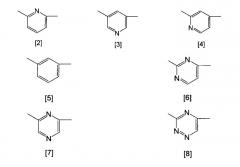
(1) -CH2-R11 [R11 представляет собой насыщенную 4-6-членную азотсодержащую гетероциклическую группу, необязательно содержащую дополнительный атом азота; насыщенную 5-6-членную азотсодержащую гетероциклическую группу, необязательно содержащую дополнительный атом азота, которая замещена группой, выбранной из группы, состоящей из оксо, -СН2-R111 (R111 представляет собой насыщенную 5-членную азотсодержащую гетероциклическую группу), насыщенной 5-членной азотсодержащей гетероциклической группы, аминометила, моноалкиламинометила, диалкиламинометила и (5-метил-2-оксо-1,3-диоксол-4-ил)метила, и, кроме того, может быть замещена 1 или 2 одинаковыми или разными заместителями, выбранными из группы, состоящей из (C1-С4)алкила, (С1-С4)алкоксикарбонила, галогена, галоген(С1-С4)алкила, гидрокси(С1-С4)алкила, амино, карбамоила], (2) -O-R12 [R12 представляет собой насыщенную 4-6-членную азотсодержащую гетероциклическую группу]; и (3) -CH=R13 [R13 представляет собой насыщенную 5-6-членную азотсодержащую гетероциклическую группу, которая может содержать дополнительный атом азота и которая может быть замещена 1-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из оксо, (С1-С4)алкила]; R2 представляет собой (С1-С4)алкил, галоген, галоген(С1-С4)алкил, гидрокси(С1-С4)алкил, (С1-С4)алкокси и карбамоил; R3 представляет собой водород, галоген; Het1 представляет собой любую из групп со следующими химическими формулами [4] и [6]:
Het2 представляет собой пиридил или пиримидинил. Согласно версии (В)
R1 представляет собой -CH2-R14 [R14 представляет собой насыщенную 4-6-членную азотсодержащую гетероциклическую группу, необязательно содержащую дополнительный атом азота; насыщенную 5-6-членную азотсодержащую гетероциклическую группу, которая может быть замещена 1-3 одинаковыми группами, выбранными из (C1-С4)алкила; R2 представляет собой (C1-С4)алкил, галоген, галоген(С1-С4)алкил, гидрокси(С1-С4)алкил, (C1-С4)алкокси, (C1-С4)алкокси(С1-С4)алкил, (C1-С4)алкоксикарбонил, (C1-С4)ацил, амино, моно(C1-С4)алкиламино, ди(С1-С4)алкиламино, нитро, карбамоил, моно(С1-С4)алкилкарбамоил, ди(С1-С4)алкилкарбамоил или циано; R3 представляет собой водород или галоген;
Het1 представляет собой любую из групп со следующими химическими формулами [9] и [10], Het2 представляет собой пиридил. 5 н.п. ф-лы, 3 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к амидному производному или его соли и фармацевтической композиции, включающей амидное производное или его соль в качестве активного ингредиента.
Поскольку тирозинкиназа BCR-ABL (см., например, непатентный документ 1) обусловливает ненормальный рост клеток, ингибирующее ее активность соединение применимо для профилактики или лечения заболеваний, обусловленных активностью тирозинкиназы BCR-ABL, например хронического миелолейкоза, острого лимфобластного лейкоза и острого миелобластного лейкоза (см., например, непатентный документ 2).
Предпосылки создания изобретения
bcr представляет собой ген, содержащийся в 22-й хромосоме человека, ген abl представляет собой ген, содержащийся в 9-й хромосоме человека, а филадельфийская хромосома образуется в результате транслокации 22-й и 9-й хромосом человека. Известно, что продукт гена хромосомы, BCR-ABL, представляет собой белок, обладающий тирозиназной активностью и постоянно генерирующий сигнал к росту, обусловливающий ненормальный рост клеток (см., например, непатентный документ 2).
Поэтому ингибирование активности тирозинкиназы BCR-ABL делает возможным супрессирование обусловленного активностью киназы роста клеток, а соединение, которое ингибирует эту активность, подходит для применения в качестве терапевтического средства для лечения заболеваний, таких как хронический миелолейкоз, острый лимфобластный лейкоз и острый миелобластный лейкоз. Хотя на рынке в качестве лекарства, обладающего тем же действием, уже представлен Гливек® (см., например, патентный документ 1), другие лекарства, обладающие тем же механизмом действия, на рынке не представлены, а потому требуется разработка более эффективных лекарственных средств.
Недавно сообщалось о том, что, кроме примеров бластного криза, при хроническом миелобластном лейкозе рецидивы часто возникают у больных, у которых ремиссия достигается введением Гливек® при BCR-ABL-положительном остром лимфобластном лейкозе (см., например, непатентный документ 3). В результате изучения лейкозных клеток у больных, страдающих от рецидива заболевания, обнаружено появление бластного варианта, такого как E255K (см., например, непатентные документы 4-7). В случае введения Гливек® больным BCR-ABL-положительным острым лимфобластным лейкозом также обнаруживается появление резистентных клеток, которые в основном представляют собой бластный вариант E255K (см., например, непатентный документ 8). В связи с увеличением применения Гливек® дополнительно растет количество резистентных к нему больных, а потому требуется разработка терапии.
Патентный документ 1: нерассмотренная заявка на выдачу патента Японии № 6-87834
Патентный документ 2: брошюрная форма международной публикации WO 02/22597
Непатентный документ 1: Shtivelman E, et al.: Nature, 1985, 315, 550-554
Непатентный документ 2: Daley G Q, et al.: Science, 1990, 247, 824-830
Непатентный документ 3: Druker B J, et al.: N Engl J Med, 2001, 344, 1038-1042
Непатентный документ 4: Weisberg E, et al.: Drug Resist Updat, 2001, 4, 22-28
Непатентный документ 5: Gorre M E, et al.: Science, 2001, 293, 876-880
Непатентный документ 6: Blagosklonny M V: Leukemia, 2002, 16, 570-572
Непатентный документ 7: Hochhaus A, et al.: Leukemia, 2002, 16, 2190-2196
Непатентный документ 8: Hofmann W-K, et al.: blood, 2002, 99, 1860-1862
Непатентный документ 9: Deninger W N, et al.: blood, 2000, 96, 3343-3356
Непатентный документ 10: J. Org. Chem., 1996, 61, 1133-1135
Непатентный документ 11: J. Org. Chem., 2000, 65, 1144-1157
Непатентный документ 12: Recl. Trav. Chim. Pays-Bas., 1950, 69, 673-699
Непатентный документ 13: J. Heterocycl. Chem., 1970, 7, 1137-1141
Непатентный документ 14: J. Am. Chem. Soc., 1999, 121, 4369-4378
Непатентный документ 15: Tetrahedron Lett., 1997, 38, 8005-8008
Непатентный документ 16: J. Med. Chem., 2002, 45, 3406-3417
Непатентный документ 17: J. Med. Chem., 2000, 43, 3895-3905
Непатентный документ 18: J. Med. Chem., 2000, 43, 1508-1518
Непатентный документ 19: J. Med. Chem., 1975, 18, 1077-1088
Непатентный документ 20: Bioorg. Med. Chem. Lett., 2001, 11, 2235-2239
Непатентный документ 21: J. Heterocyclic Chem., 2000, 37, 1457-1462
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Задачи, решаемые настоящим изобретением
Задача, на решение которой направлено настоящее изобретение, состоит в получении нового амидного производного, обладающего отличной ингибирующей активностью в отношении тирозинкиназы BCR-ABL, или его фармацевтически приемлемой соли.
Способы решения задач
Авторы настоящего изобретения активно изучали различные соединения и обнаружили, что указанная выше задача может быть решена при помощи нового амидного производного и его фармацевтически приемлемой соли (здесь и далее в этом документе называемого «соединением по настоящему изобретению»), оформив тем самым настоящее изобретение.
Настоящее изобретение относится к амидному производному, которое представляет собой соединение, представленное следующей общей формулой [1] в любой из последующих версий (A), (B) или (C) или к его фармацевтически приемлемой соли.
Версия (A)
R1 представляет собой любую из следующих групп (1)-(3):
(1) -CH2-R11 [R11 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа замещена группой, выбранной из группы, состоящей из оксо, -CH2-R111 (R111 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси и (5-метил-2-оксо-1,3-диоксол-4-ил)метила, и, кроме того, может быть замещена 1 или 2 одинаковыми или разными заместителями, выбранными из группы, состоящей из алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила],
(2) -O-R12 [R12 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа может быть замещена 1-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из оксо, -CH2-R121 (R121 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси, (5-метил-2-оксо-1,3-диоксол-4-ил)метила, алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила], и
(3) -CH=R13 [R13 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа может быть замещена 1-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из оксо, -CH2-R131 (R131 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси, (5-метил-2-оксо-1,3-диоксол-4-ил)метила, алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила].
R2 представляет собой алкил, галоген, галогеналкил, гидроксиалкил, алкокси, алкоксиалкил, алкоксикарбонил, ацил, амино, моноалкиламино, диалкиламино, нитро, карбамоил, моноалкилкарбамоил, диалкилкарбамоил или циано.
R3 представляет собой водород, галоген или алкокси.
Het1 представляет собой любую из групп со следующими химическими формулами [2]-[8]:
Het2 представляет собой пиридил, пиримидинил, пиразинил, пиридазинил или 1,2-дигидропиридазинил (Het2 может быть замещен 1-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из алкила, галогена и амино).
Исключением является соединение, в котором R11 представляет собой пирролидинил, пиперидинил, пиперазинил или морфолинил (каждый пирролидинил, пиперидинил, пиперазинил или морфолинил замещен группой, выбранной из ряда, состоящего из оксо, -CH2-R111 (R111 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси и (5-метил-2-оксо-1,3-диоксол-4-ил)метила, и, кроме того, может быть замещен 1 или 2 одинаковыми или разными заместителями, выбранными из группы, состоящей из алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила); Het1 представляет собой группу формулы [6]; и Het2 представляет собой пиразинил или пиридил, который может быть замещен алкилом.
Версия (B)
R1 представляет собой -CH2-R14 (R14 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа может быть замещена 1-3 одинаковыми или разными заместителями, выбранными из группы, состоящей из алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила).
R2 представляет собой алкил, галоген, галогеналкил, гидроксиалкил, алкокси, алкоксиалкил, алкоксикарбонил, ацил, амино, моноалкиламино, диалкиламино, нитро, карбамоил, моноалкилкарбамоил, диалкилкарбамоил или циано.
R3 представляет собой водород, галоген или алкокси.
Het1 представляет собой любую из групп со следующими химическими формулами [9] и [10]:
Het2 представляет собой пиридил, пиримидинил, пиразинил, пиридазинил или 1,2-дигидропиридазинил (Het2 может быть замещен 1-3 одинаковыми или разными представителями, выбранными из группы, состоящей из алкила, галогена и амино).
Версия (C)
R1 представляет собой любую из следующих групп (1)-(3):
(1) -CH2-R11 [R11 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа замещена группой, выбранной из группы, состоящей из оксо, -CH2-R111 (R111 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси и (5-метил-2-оксо-1,3-диоксол-4-ил)метила, и, кроме того, может быть замещена 1 или 2 одинаковыми или разными представителями, выбранными из группы, состоящей из алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила],
(2) -O-R12 [R12 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа может быть замещена 1-3 одинаковыми или разными представителями, выбранными из группы, состоящей из оксо, -CH2-R121 (R121 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси, (5-метил-2-оксо-1,3-диоксол-4-ил)метила, алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила], и
(3) -CH=R13 [R13 представляет собой насыщенную азотсодержащую гетероциклическую группу. Насыщенная азотсодержащая гетероциклическая группа может быть замещена 1-3 одинаковыми или разными представителями, выбранными из группы, состоящей из оксо, -CH2-R131 (R131 представляет собой насыщенную азотсодержащую гетероциклическую группу), насыщенной азотсодержащей гетероциклической группы, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкокси, (5-метил-2-оксо-1,3-диоксол-4-ил)метила, алкила, алкоксикарбонила, галогена, галогеналкила, гидроксиалкила, амино, моноалкиламино, диалкиламино, карбамоила, моноалкилкарбамоила и диалкилкарбамоила].
R2 представляет собой алкил, галоген, галогеналкил, гидроксиалкил, алкокси, алкоксиалкил, алкоксикарбонил, ацил, амино, моноалкиламино, диалкиламино, нитро, карбамоил, моноалкилкарбамоил, диалкилкарбамоил или циано.
R3 представляет собой водород, галоген или алкокси.
Het1 представляет собой любую из групп со следующими формулами [9] и [10]:
Het2 представляет собой пиридил, пиримидинил, пиразинил, пиридазинил или 1,2-дигидропиридазинил (Het2 может быть замещен 1-3 одинаковыми или разными представителями, выбранными из группы, состоящей из алкила, галогена и амино).
Примеры предпочтительных соединений среди соединений представленной выше общей формулы [1] включают следующие амидные производные (1)-(14) или их фармацевтически приемлемые соли:
(1) 4-(1-метилпиперидин-4-илиденметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(2) 4-(1-метилпиперидин-4-илокси)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(3) 4-(1-метилпиперазин-4-илметил)-3-трифторметил-N-{4-метил-3-[6-(3-пиридил)пиримидин-4-иламино]фенил}бензамид,
(4) 4-(1-метилпиперазин-4-илметил)-3-трифторметил-N-{4-метил-3-[6-(5-пиримидинил)пиримидин-4-иламино]фенил}бензамид,
(5) (-)-4-((S)-3-амино-2-оксопирролидин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(6) 4-[(S)-2-(1-пирролидинилметил)пирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(7) 4-[3-диметиламинометилазетидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(8) 4-[(S)-3-(1-пирролидинил)пирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(9) 4-{4-[(5-метил-2-оксо-1,3-диоксол-4-ил)метил]пиперазин-1-илметил}-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(10) 4-(4-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(4-пиридил)тиазол-2-иламино]фенил}бензамид,
(11) 4-[3-диметиламиноазетидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(12) 4-[(R)-3-диметиламинометилпирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(13) 4-[(S)-3-диметиламинометилпирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид, и
(14) 4-[(3R,4R)-3-диметиламино-4-метоксипирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид.
Кроме того, в настоящем изобретении представлены следующие примеры амидных производных (1)-(37) или их фармацевтически приемлемые соли:
(1) 3-дифторметил-4-(4-метилпиперазин-1-илметил)-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(2) 3-этил-4-(4-метилпиперазин-1-илметил)-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(3) 4-(1-метилпиперидин-4-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(4) 3,5-дихлор-4-[(S)-3-диметиламинопирролидин-1-илметил]-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(5) 3-метокси-4-(4-метилпиперазин-1-илметил)-N-{3-[4-(5-бромпиридин-3-ил)пиримидин-2-иламино]-4-метилфенил}бензамид,
(6) 4-(4-этилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(7) 4-(4-этилпиперазин-1-илметил)-3-трифторметил-N-{3-[4-(5-бромпиридин-3-ил)пиримидин-2-иламино]-4-метилфенил}бензамид,
(8) 3-хлор-4-(4-метилпиперазин-1-илметил)-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(9) 3-фторметил-4-(1-метилпиперидин-4-илметил)-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(10) 4-(4-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиридин-2-иламино]фенил}бензамид,
(11) 4-(4-этилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиридин-2-иламино]фенил}бензамид,
(12) 4-(4-этилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(3-пиридинил)пиридин-2-иламино]фенил}бензамид,
(13) 4-(4-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(3-пиридинил)пиридин-2-иламино]фенил}бензамид,
(14) 4-[4-(2-фторэтил)пиперазин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(15) 4-[4-(2-гидроксиэтил)пиперазин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(16) 4-[(R)-3-диметиламинопирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(17) 4-(1-пиперазинилметил)-3-трифторметил-N-{3-[4-(5-бромпиридин-3-ил)пиримидин-2-иламино]-4-метилфенил}бензамид,
(18) 4-(1-пиперазинилметил)-3-трифторметил-N-{4-метил-3-[4-(3-пиридинил)пиридин-2-иламино]фенил}бензамид,
(19) 4-(1-пиперазинилметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(20) 4-(3-карбамоилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(21) 4-[(S)-3-диметиламинопирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(22) 4-(3-карбамоил-4-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(23) 4-((S)-3-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(24) 4-((R)-3-метилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(25) 4-[(S)-3-N,N-диэтиламинопирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(26) 4-[(2R,4S)-4-диметиламино-2-метилпирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(27) 4-((S)-3-аминопиперидинометил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(28) 4-[(S)-3-диметиламинопиперидинометил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(29) 4-((3S,4R)-3-амино-4-метилпирролидин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(30) 4-[(3S,4R)-3-диметиламино-4-метилпирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(31) 4-[(S)-3-метиламинопирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(32) 4-((S)-3,4-диметилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(33) 4-((R)-3,4-диметилпиперазин-1-илметил)-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(34) 4-[(3R,4R)-3-диметиламино-4-метоксипирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(5-пиримидинил)пиримидин-2-иламино]фенил}бензамид,
(35) 4-(1-метилпиперидин-4-илокси)-3-трифторметил-N-{4-метил-3-[4-(3-пиридил)пиримидин-2-иламино]фенил}бензамид,
(36) 4-(1-метилпиперидин-4-илиденметил)-3-трифторметил-N-{4-метил-3-[4-(3-пиридил)пиримидин-2-иламино]фенил}бензамид, и
(37) 4-[(R)-3-диметиламинометилпирролидин-1-илметил]-3-трифторметил-N-{4-метил-3-[4-(3-пиридил)пиримидин-2-иламино]фенил}бензамид.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей соединение по настоящему изобретению в качестве активного ингредиента, например ингибитора тирозинкиназы BCR-ABL. Более конкретно, настоящее изобретение относится к фармацевтической композиции, применяемой в качестве терапевтического средства для лечения хронического миелолейкоза, терапевтического средства для лечения острого лимфобластного лейкоза или терапевтического средства для лечения острого миелобластного лейкоза.
Соединение по настоящему изобретению обладает ингибирующей активностью в отношении тирозинкиназы BCR-ABL и применимо в качестве лекарства для профилактики или лечения таких заболеваний, как хронический миелолейкоз, острый лимфобластный лейкоз и острый миелобластный лейкоз (см., например, непатентный документ 9).
Далее настоящее изобретение будет описано подробно.
Выражение «насыщенная азотсодержащая гетероциклическая группа» включает 4-8-членную насыщенную кольцевую группу, представляющую собой насыщенную кольцевую группу, содержащую, по крайней мере, один атом азота в качестве кольцевого атома, которая также может содержать 1-3 одинаковых или разных представителей, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. Если кольцевой атом представляет собой атом азота или атом серы, то атом азота или атом серы могут образовывать оксид. Примеры групп включают пирролидинил, пиперидинил, пиперазинил, азетидинил, морфолинил, тиоморфолинил и гексагидро-1H-1,4-диазепинил. Тем не менее, выражение «насыщенная азотсодержащая гетероциклическая группа» по отношению к R13 ограничивается группами, в которых кольцевой атом, связанный с R13 посредством двойной связи, и соседний с ним кольцевой атом являются атомами углерода, и, например, -CH=R13 включает пиперидин-4-илиденметил.
Термин «алкил» включает неразветвленные или разветвленные алкильные группы, содержащие 1-10 атомов углерода, например метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, н-гексил, изогексил, н-гептил, изогептил, н-октил, н-нонил и н-децил. Особенно предпочтительными являются неразветвленные группы, содержащие 1-3 атома углерода.
Алкильный радикал «диалкиламиноалкила», «алкокси», «алкоксикарбонила», «галогеналкила», «гидроксиалкила», «моноалкиламино», «диалкиламино», «моноалкилкарбамоила», «диалкилкарбамоила», «алкоксиалкила» и «гидроксиалкила» включает упомянутый выше алкил.
Термин «галоген» включает, например, фтор, хлор, бром и йод.
Термин «галогеналкил» включает моногалогеналкил, дигалогеналкил и тригалогеналкил, а галогеновый радикал «галогеналкила» включает упомянутый выше галоген. Термин «галогеналкил» включает, например, фторметил, 2-фторэтил, дифторметил, трифторметил и 2,2,2-трифторэтил.
Термин «ацил» включает ацильные группы, содержащие 1-11 атомов углерода, например формил, ацетил, пропионил, бутирил, изобутирил, бензоил, 1-нафтоил и 2-нафтоил.
Термин «пиридил» включает, например, 2-пиридил, 3-пиридил и 4-пиридил.
Термин «пиримидинил» включает, например, 2-пиримидинил, 4-пиримидинил и 5-пиримидинил.
Термин «пиразинил» включает, например, 2-пиразинил.
Термин «пиридазинил» включает, например, 3-пиридазинил и 4-пиридазинил.
Термин «1,2-дигидропиридазинил» включает, например, 1,2-дигидропиридазин-3-ил и 1,2-дигидропиридазин-4-ил.
Выражение «насыщенная циклическая аминогруппа» включает 4-8-членную насыщенную группу, представляющую собой насыщенную циклическую аминогруппу, содержащую, по крайней мере, один атом азота в качестве кольцевого атома, а также может содержать 1-3 одинаковых или разных представителей, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. Если кольцевой атом представляет собой атом азота или атом серы, то атом азота или атом серы могут образовывать оксид. Примеры групп включают 1-пирролидинил, 1-пиперидинил, 1-пиперазинил, 1-азетидинил, 4-морфолинил, 4-тиоморфолинил, гексагидро-1H-1,4-диазепин-1-ил.
Наиболее предпочтительный вариант осуществления изобретения
Соединение по настоящему изобретению может быть получено из известного per se соединения или промежуточного продукта, который может быть легко получен, например, в соответствии со следующим способом. В получении соединения по настоящему изобретению общеизвестно, что если исходные соединения содержат заместители, влияющие на проведение реакции, то исходные соединения используют в реакции после защиты подходящими защитными группами известными per se способами. После проведения реакции защитные группы могут быть удалены известными per se способами.
Способ получения 1
[где значения R1, R2, R3, Het1 и Het2 определены выше]
Данная реакция представляет собой реакцию конденсации соединения [11] и соединения [12], а потому проводится в соответствии с известными per se способами, применяемыми в реакциях конденсации. Соединение [1] может быть получено путем осуществления взаимодействия карбоновой кислоты в виде соединения [12], или ее реакционно-способного производного, с амином в виде соединения [11]. Примеры реакционно-способных производных соединения [12] включают производные, которые обычно используются в реакции амидной конденсации, например галогенангидрид (например, хлорангидрид, бромангидрид и так далее), смешанный галогенангидрид, имидазол и активный амид. В случае использования карбоновой кислоты [12] используется конденсирующий агент (например, 1,1'-оксалилдиимдазол, 1-этил-3-(3-диметиламинопропил)карбодиимид, дициклогексилкарбодиимид, диэтилцианофосфонат, дифенилфосфорилазид, йодид 2-хлор-1-метилпиридиния, гексафторфосфат 1H-бензотразол-1-илокситрипирролидинофосфония и гексафторфосфат бензотриазол-1-илокситрис(диметиламино)фосфония), а реакцию проводят при температуре от -20ºC до 100ºC в присутствии или в отсутствие основания (например, органического основания, такого как триэтиламин, N,N-диизопропил-N-этиламин, N,N-диметиланилин, пиридин, 4-диметиламинопиридин, 1,8-диазабицикло[5.4.0]ундец-7-ен и так далее). Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают простые эфиры, такие как тетрагидрофуран и диэтиловый эфир; амиды, такие как N,N-диметилформамид и N,N-диметилацетамид; нитрилы, такие как ацетонитрил и пропионитрил; углеводороды, такие как бензол и толуол; галогенированные углеводороды, такие как хлороформ и дихлорметан; и смеси этих растворителей. В этом случае также могут применяться добавки (например, 1-гидроксибензотриазол, N-гидроксисукцинимид и так далее). Продолжительность реакции варьируют в зависимости от видов исходного материала и конденсирующего агента и температуры реакции, но обычно предпочтительно продолжительность реакции составляет от 30 минут до 24 часов. Количество соединения [12] и конденсирующего агента предпочтительно составляет 1-3 моль на моль соединения [11]. В случае использования галогенангидрида в качестве реакционно-способного производного соединения [12] реакцию проводят при температуре от -20ºC до 100ºC с использованием пиридинового растворителя, такого как пиридин или 4-метилпиридин, или того же основания или растворителя, что и описанный выше. В качестве добавки также может быть добавлен 4-диметиламинопиридин. Продолжительность реакции варьируют в зависимости от вида галогенангидрида и температуры реакции, но обычно предпочтительно продолжительность реакции составляет от 30 минут до 24 часов.
Способ получения исходного соединения [11] для применения в способе 1
Применяемое в качестве исходного соединения соединение [11], в котором Het1 представляет собой группу формулы [6], может быть получено, например, таким же образом, как описано в патентном документе 1.
Применяемое в качестве исходного соединения соединение [11], в котором Het1 представляет собой группу формулы [4], [5], [7] или [9], может быть получено следующим образом:
[где значения Het1 и Het2 определены выше; R4 и R5 могут быть одинаковыми или отличаться друг от друга и представляют собой алкил или гидрокси; R6, R7 и R8 представляют собой алкил; и X1 представляет собой галоген]
Стадия 1
Данная реакция представляет собой реакцию кросс-сочетания, в которой используется соединение [13] и борорганическое соединение [14] или оловоорганическое соединение [15], и может проводиться известными per se способами. Например, указанную реакцию проводят при 20ºC-200ºC в подходящем растворителе в присутствии палладиевого катализатора. В качестве палладиевого катализатора обычно используют тетракис(трифенилфосфин)палладий, дихлорбис(трифенилфосфин)палладий и дихлорбис(три-орто-толилфосфин)палладий. Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан; спирты, такие как метанол и этанол; амиды, такие как N,N-диметилформамид и N,N-диметилацетамид; углеводороды, такие как бензол, толуол и ксилол; органические амины, такие как пиридин и триэтиламин; и смеси этих растворителей. При использовании соединения [14] требуется добавление основания (например, гидроксида натрия, карбоната калия, трикалийфосфата и так далее). Продолжительность реакции варьируется в зависимости от природы исходного материала и температуры реакции, но обычно предпочтительно составляет от 1 часа до 48 часов.
Стадия 2
Данная реакция представляет собой реакцию восстановления ароматической нитрогруппы соединения [16] до аминогруппы, а потому проводится в соответствии с известными per se способами, применяемыми в реакциях восстановления. Способ включает, например, способ обработки цинком или оловом в кислых условиях. В соответствии со способом каталитического восстановления, например, может проводиться гидрирование с использованием в качестве катализатора платины, никеля Ренея, платинированного угля (Pt-C), палладированного угля (Pd-C) или комплекса рутения. Кроме того, в качества примера могут быть представлены способ использования сульфида, такого как дитионит натрия, и способ восстановления формиатом аммония или гидразином в присутствии металлического катализатора.
Используемое в качестве исходного материала соединение [13], в котором Het1 представляет собой группу формулы [4], может быть получено, например, путем осуществления взаимодействия 2,4-дихлорпиридина (полученного, например, в соответствии с модификацией способа, описанного в непатентном документе 12) с 2-метил-5-нитроанилином в соответствии со способом по J.P. Wolfe et al. с использованием палладиевого катализатора (см. непатентные документы 10 и 11). Если Het1 представляет собой группу формулы [5], то соединение может быть получено, например, путем осуществления взаимодействия 1-бром-3-йодбензола с 2-метил-5-нитроанилином. Если Het1 представляет собой группу формулы [7], то соединение может быть получено, например, путем осуществления взаимодействия 2,6-дихлорпиразина с 2-метил-5-нитроанилином. Если Het1 представляет собой группу формулы [9], то соединение может быть получено, например, путем осуществления взаимодействия 4,6-дихлорпиримидина с 2-метил-5-нитроанилином. Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и 1,2-диметоксиэтан; углеводороды, такие как бензол, толуол и ксилол; и смеси этих растворителей. Реакцию проводят при 70ºC-100ºC в присутствии основания. Примеры палладиевого катализатора включают трис(дибензилиденацетон)дипалладий(0), ацетат палладия(II) и три(орто-толилфосфин)палладий(0). Обычно количество палладия предпочтительно составляет от 0,5 мол.% до 4 мол.% относительно галогенированного амина. В качестве лиганда палладиевого катализатора может применяться, например, 1,3-бис(дифенилфосфино)пропан, 1,1'-бис(дифенилфосфино)ферроцен и (±)-2,2'-бис(дифенилфосфино)-1,1'-бинафтил [(±)-BINAP]. Примеры основания включают трет-бутоксид натрия, трет-бутоксид калия, карбонат цезия, карбонат калия и карбонат натрия. Продолжительность реакции варьируется в зависимости от природы исходного материала и температуры реакции, но обычно предпочтительно составляет от 1 часа до 36 часов.
Соединение [13] может быть также получено путем осуществления взаимодействия 2,4-дихлорпиридина, например, если Het1 представляет собой группу формулы [4], или путем осуществления взаимодействия 4,6-дихлорпиримидина, например, если Het1 представляет собой группу формулы [9], с 2-метил-5-нитроанилином при 20ºC-200ºC в подходящем растворителе или в отсутствие растворителя в присутствии или в отсутствие основания. Примеры основания включают пиридин, триэтиламин, N,N-диизопропил-N-этиламин, карбонат калия, гидрокарбонат натрия и гидроксид калия. Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают простые эфиры, такие как тетрагидрофуран, дибутиловый эфир и 1,4-диоксан; амиды, такие как N,N-диметилформамид и N,N-диметилацетамид; углеводороды, такие как бензол и толуол; спирты, такие как этиленгликоль и 2-метоксиэтанол; галогенированные углеводороды, такие как хлороформ и дихлорметан; диметилсульфоксид; и смеси этих растворителей. Продолжительность реакции варьируется в зависимости от природы исходного материала и температуры реакции, но обычно предпочтительно составляет от 1 часа до 24 часов.
Используемое в качестве исходного материала соединение [16a] (соединение [16], в котором Het1 представляет собой группу формулы [4]) может быть получено, например, следующим образом:
[где значения R4, R5, R6, R7, R8 и Het2 определены выше и X2 и X3 представляют собой галоген].
Стадия 1
Данная реакция представляет собой реакцию кросс-сочетания, в которой используется соединение [17] и борорганическое соединение [14] или оловоорганическое соединение [15], и может проводиться аналогичным образом, как описано выше.
Стадия 2
Соединение [19] получают путем галогенирования соединения [18]. Поэтому реакцию проводят в соответствии с известными per se способами. Обычно реакцию проводят с использованием хлорангидрида фосфорной кислоты, бромангидрида фосфорной кислоты, пентахлорида фосфора или пентабромида фосфора с использованием или без использования растворителя. Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают простые эфиры, такие как тетрагидрофуран, дибутиловый эфир и 1,4-диоксан; амиды, такие как N,N-диметилформамид и N,N-диметилацетамид; галогенированные углеводороды, такие как хлороформ и дихлорметан; и смеси этих растворителей. Реакцию обычно проводят при температуре от комнатной температуры до 130ºC, а продолжительность реакции обычно предпочтительно составляет от 20 минут до 24 часов.
Стадия 3
Соединение [16a] может быть получено путем осуществления взаимодействия соединения [19] с соединением [20] в соответствии с представленным выше способом с использованием палладиевого катализатора (см., например, непатентные документы 10 и 11).
Соединение [11a] (соединение [11], в котором Het1 представляет собой группу формулы [4]) может быть получено путем осуществления взаимодействия соединения [19] с соединением [21] в соответствии с представленным выше способом с использованием палладиевого катализатора (см., например, непатентные документы 10 и 11) с получением соединения [22] и снятия защитных групп с соединения [22].
[где значения Het2 и X3 определены выше и R9 представляет собой защитную группу].
Стадия 1
Исходное соединение [21] может быть получено путем защиты 2,4-диаминотолуола введением подходящей защитной группы в соответствии с известными per se способами. Примеры защитной группы включают ацилпроизводные, такие как бензоил, ацетил и формил, и производные уретанового типа, такие как бензилоксикарбонил, трет-бутоксикарбонил и 2,2,2-трихлорэтоксикарбонил. Соединение [22] может быть получено путем осуществления взаимодействия соединения [19] с соединением [21] с использованием палладиевого катализатора.
Стадия 2
В реакции снятия защитных групп с соединения [22] защитную группу ацильного типа удаляют путем гидролиза с использованием кислоты или щелочи или удаляют путем добавления аммиачной воды или гидразина. Примеры используемой для гидролиза кислоты включают неорганические кислоты, такие как соляная кислота и серная кислота, а примеры основания включают неорганические основания, такие как гидроксид натрия и гидроксид калия. Выбор растворителя конкретно не ограничен, поскольку он не участвует в реакции, и примеры растворителя включают спирты, такие как метанол и этанол; простые эфиры, такие как тетрагидрофуран и 1,4-диоксан; воду; и смеси этих растворителей. Температура реакции составляет от 0ºC до 100ºC, а продолжительность реакции обычно составляет от нескольких минут до 24 часов. Если защитная группа представляет собой производное уретанового типа, то защитная группа может быть удалена путем гидрирования с использованием палладиевого катализатора или путем добавления соляной кислоты, трифторуксусной кислоты, триметилсилилйодида или трехфтористого бора, в зависимости от природы защитной группы.
Соединение [11b], используемое в качестве исходного соединения [11], в котором Het1 представляет собой группу формулы [10], может быть получено в соответствии со способом, сходным с изложенным, например, в непатентном документе 13, для получения соединения [16b] с после