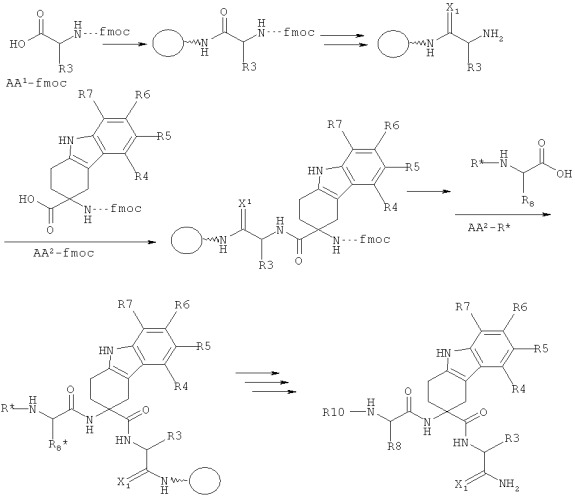
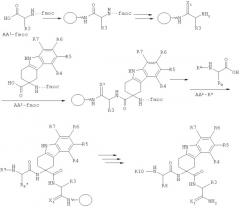
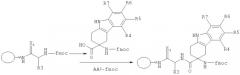
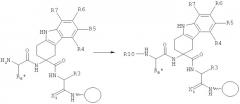
Производные тетрагидрокарбазола и фармацевтическая композиция на их основе
Иллюстрации
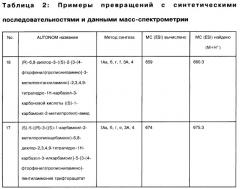
Показать всеНастоящее изобретение относится к новым производным тетрагидрокарбазола, которые обладают улучшенными свойствами и могут быть использованы как ингибиторы рецепторов GPCR. Новые соединения могут быть использованы для лечения патологических состояний, которые имеют строгую зависимость от измененных эффектов рецепторов GPCR. Соединения по настоящему изобретению действуют в особенности через антагонистическое ингибирование LHRH-рецептора. Изобретение также относится к лекарственным средствам, содержащим по меньшей мере одно новое соединение в качестве активного компонента. Лекарственные средства удобны в частности для применения в качестве дозированных пероральных лекарственных форм для млекопитающих, в частности для человека. 3 н. и 20 з.п. ф-лы, 11 ил., 9 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым производным тетрагидрокарбазола, имеющим улучшенное биологическое действие, улучшенную пероральную биодоступность и улучшенную метаболическую стабильность, в качестве лигандов для сопряженных с G-белком рецепторов (GPCR), прежде всего в качестве лигандов для рецептора рилизинг-фактора лютеинизирующего гормона (LHRH-рецептор), к их получению и к их применению в фармацевтических композициях для лечения патологических состояний, опосредованных сопряженными с G-белком рецепторами у млекопитающих и, прежде всего, у человека.
Уровень техники
Содержание всех публикаций или сравнимых источников, процитированных в настоящей заявке для разъяснения обоснования настоящего изобретения, включено в настоящую заявку с целью более полного раскрытия предмета данного изобретения.
Сопряженные с G-белком рецепторы представляют семейство рецепторов, ассоциированных с клеточными мембранами, которые играют важную роль в многочисленных биохимических и патобиохимических процессах у млекопитающих и, в частности, у человека. Все GPCR состоят из семи гидрофобных трансмембранных альфа-спиралей, которые соединены вместе тремя внутриклеточными и тремя внеклеточными петлями и имеют внеклеточный амино-концевой фрагмент и внутриклеточный карбоксиконцевой фрагмент. Один или больше гетеротримерных G-белков вовлечены в перенос клеточных сигналов. Ими опосредуются и контролируются различные физиологические стимулы, такие как фоточувствительность, вкус и запах, а также фундаментальные процессы, такие как метаболизм, репродукция и развитие. Существуют GPCR для экзогенных и эндогенных лигандов. Пептидные гормоны, биогенные амины, аминокислоты, нуклеотиды, липиды, Са2+ а также фотоны, были, среди прочих, идентифицированы как лиганды, к тому же один лиганд может активировать различные рецепторы.
В соответствии с недавним исследованием, 367 последовательностей выявлено в человеческом геноме для сопряженных с G-белком рецепторов (GPCR) с эндогенными лигандами, D.K.Vassilatis et al., PNAS 100(8), 4903-4908 (2003). 284 из них принадлежат к классу А, 50 к классу В, 17 к классу С и 11 к классу F/S. Примеры, принадлежащие к классу А - это бомбезин, допамин и LHRH рецепторы, к классу В - VIP и калцитониновые рецепторы. Естественные лиганды для многочисленных GPCR до сих пор неизвестны.
Вследствие их функции, GPCR являются подходящими мишенями для лекарственных препаратов, предназначенных для терапии и предотвращения большого количества патологических состояний. Предполагается, что около 50% известных в настоящее время мишеней для активных компонентов представляют собой GPCR [Y. Fang et al., DDT 8(16), 755-761 (2003)]. Так, GPCR играют важную роль в патологических процессах, таких как, например, боль (опиоидный рецептор), астма (β2-адренорецептор), мигрень (серотонин 5-НТ1В/1D-рецептор), рак (1-LHRH-рецептор),сердечно-сосудистые нарушения (ангиотензиновый рецептор), нарушения метаболизма (GHS-рецептор) или депрессия (серотонин 5-НТ1а-рецептор), K.L.Pierce et al., Nat. Rev. Mol. Cell Biol. 3, 639-650 (2002).
Общая информация о GPCR находится на http://www.gpcr.org.
Настоящее изобретение описывает новые лиганды с улучшенными свойствами для GPCR в общем, при этом соединения по данному изобретению действуют в особенности как антагонисты LHRH-рецептора.
Естественный лиганд для этого рецептора, пептидный гормон LHRH, синтезируется в клетках гипоталамуса и высвобождается пульсирующим образом из нейронов гипоталамуса в капиллярное сплетение ementia mediana. В передней доле гипофиза, LHRH связывается с LHRH-рецептором гонадотропных клеток и стимулирует определенные тримерные G-белки, которые инициируют разветвленный каскад передачи сигнала. Изначальным событием является активация фосфолипазы С, A2 и/или D. Это ведет к увеличенной выработке вторичных мессенджеров диацилглицерола и IР3, за которыми следует мобилизация Ca2+ из межклеточных бассейнов и активация различных зависимых протеиновых киназ. Наконец, происходит стимулирование выработки и высвобождения гонадотропинов FSH и LH через определенные временные промежутки. Эти два гормона транспортируются посредством кровотока к целевым органам, соответственно яичкам или яичникам. Там они стимулируют выработку и высвобождение соответствующих половых гормонов. Имеет место сложный механизм обратной связи, посредством которого концентрация образующихся половых гормонов, в свою очередь, регулирует выработку LH и FSH.
В мужском организме, LH связывается с мембранными рецепторами клеток Лейдига и стимулирует биосинтез тестостерона. FSH действует через специфические рецепторы на клетках Сертоли и участвует в производстве сперматозоидов. В женском организме LH связывается с LH-рецепторами тека-клеток и активирует формирование андроген-синтезирующих энзимов. FSH стимулирует пролиферацию гранулозных клеток определенных фолликулярных стадий через их FSH рецепторы. Формирующиеся андрогены превращаются в соседних гранулозных клетках в эстрогены эстрон и эстрадиол.
Множество нарушений, отличительными чертами которых являются доброкачественные или злокачественные пролиферации тканей, зависят от стимуляции половыми гормонами, такими как тестостерон или эстрадиол. Типичными нарушениями такого типа являются рак простаты и доброкачественная гиперлазия простаты (ВРН) у мужчин и эндометриоз, фиброзы матки или миомы матки, преждевременное половое созревание, гирсутизм и синдром многокистозного яичника, а также рак молочной железы, рак матки, эндометриальный рак, рак шейки матки и рак яичника у женщин.
С момента их открытия в 1971 году, Serially et al. Science 173, 1036-1038 (1971), было синтезировано и протестировано более 3000 синтетических аналогов природных LHRH. Пептидные агонисты, такие как трипторелин и левпролид, в течение многих лет успешно применялись в терапии гинекологических нарушений и рака. Однако общим недостатком агонистов является то, что они стимулируют LHRH-рецепторы в начальной стадии использования и, таким образом, ведут к побочным эффектам вследствие изначального роста уровня половых гомонов. Только после понижающей регуляции LHRH-рецептора в результате этой перестимуляции суперагонисты могут проявить свой эффект. Это ведет к полному понижению уровня половых гормонов и, таким образом, к фармакологической кастрации со всеми признаками и симптомами. Этот недостаток связан с невозможностью целенаправленной регуляции уровня половых гормонов через дозировку. Таким образом, для заболеваний, которые не требу ют тотального понижения уровня половых гормонов до уровня кастрации, таких как, например, доброкачественные новообразования тканей, терапия с помощью агонистов не является оптимальной для пациента.
Это привело к разработке петидных антагонистов LHRH-рецепторов, из числа которых, например, цетрореликс (Cetrotide™) был успешно применен для котролируемой стимуляции яичников в контексте лечения женского бесплодия. Эти антагонисты ингибируют LHRH-рецепторы немедленно и в зависимости от дозировки, и таким образом приводят к немедленному понижению уровней тестостерона или эстрадиола и прогестерона в плазме. Однако пептидные антагонисты несколько менее активны, чем агонисты, и поэтому должны применяться в более высоких дозировках.
Обзор клинических применений и потенциала LHRH-агонистов и антагонистов был сделан R.P.Millar et al. в British Med. Bull. 56, 761-772 (2000), R.E.Felberbaum et al., Mol. Cell. Endocrinology 166, 9-14 (2000) и F.Haviv et al. в Itegration of Pharmaceutical Discovery and Development Case Studies, Chapter 7, ed. Borchardt et al., Plenum Press, New York (1998). Помимо лечения злокачественных и доброкачественных новообразований, другими возможными применениями являются контролируемая стимуляция яичников в контексте зачатия в пробирке, контроль зачатия (контрацепция), защита от нежелательных побочных эффектов от радио- и хемотерапии, лечение ВИЧ-инфекций (СПИД), а также нейрологических или нейродегенеративных расстройств, таких как болезнь Альцгеймера. Специфические LHRH-рецепторы были найдены не только в клетках гипофиза, но и в клетках различных опухолей, например груди и яичников. Эти рецепторы могут быть посредниками в прямом антипролиферативном эффекте антагонистов LHRH-рецепторов на опухоли.
Пептидные агонисты и антагонисты LHRH-рецепторов в большинстве своем представляют декапептиды, биодоступность которых недостаточна для перорального введения. Они обычно даются как растворы для инъекций или для местного применения, подкожно или внутримышечно. Такое применение связано с неудобствами для пациента, и может вызвать несогласие. К тому же, синтез декапептидов сложный и дорогостоящий.
Поэтому целесообразно искать непептидные антагонисты для LHRH-рецепторов, которые, помимо высокой активности, имеют улучшенную метаболическую стабильность и могут применяться перорально.
В сравнении с пептидными агонистами и антагонистами LHRH-рецептора, до сих пор ни одно непетидное соединение не одобрено и не находится в клиническом использовании для какого-либо из возможных показаний. Современное состояние развития в области агонистов и антагонистов LHRH-рецептора описано в обзорах Y.-F. Zhu et al., Expert Opin. Therap. Patents 14(2), 187-199 (2004), Y.-F. Zhu et al., Ann. Rep. Med. Chem. (39), 99-110 (2004), F.С.Tucci et al., Curr. Opin. Drug Discovery & Development 7(6), 832-847 (2004), R.E.Armer, Curr. Med. Chem. 11, 3017-3028 (2004) и М.V.Chengalvala et al., Curr. Med. Chem.-Anti-Cancer Agents, 3, 399-410 (2003).
Первая из приведенных публикаций содержит всесторонний список изданных патентных спецификаций, описывающих синтез и использование низкомолекулярных антагонистов LHRH-рецептора.
Среди первых примеров непептидных антагонистов LHRH-рецептора присутствует 4-оксотиено[2,3-b]пиридиновая структура, которая была описана N. Cho et al. в работе J. Med. Chem. 41, 4190-4195 (1998). Хотя эти соединения, такие как, например, Т-98745, имеют высокое сродство к рецептору, их растворимость в воде очень мала, и их биодоступность низка. Основываясь на этой активной структуре, были проведены многочисленные дальнейшие исследования, можно упомянуть примеры публикаций в международных заявках WO 95/28405, WO 96/24597, WO 97/14697 и WO 97/41126. Синтез тиено-[2,3-d]-пиримидин-2,4-дионов как пероральнодоступных антагонистов описан S. Sasaki et al., в статье J. Med. Chem. 46, 113-124 (2003).
Новые 1-арилметил-5-арил-6-метилурацилы описаны Z. Guo et al., в статье J. Med. Chem. 47, 1259-1271 (2004). Получение N-[(гетеро)арилметил]бензолсульфонамидов как потенциальных непептидных антагонистов LHRH-рецептора описано в WO 03/078398. Патентная заявка WO 02/11732 описывает трициклические пирролидины как антагонисты LHRH-рецептора. Замещенные пиридин-4-оны как антагонисты LHRH-рецептора описаны в WO 03/13528, а замещенные 1,3,5-триазино-2,4,6-трионы в WO 03/11839.
Синтез и биологическая активность производных эритромицина А, имеющих активность антагонистов LHRH-рецептора, описаны J.Т.Randolph et al. в работе J. Med. Chem. 47(5), 1085-1097 (2004). Отдельные производные показывают пероральную активность на уровне LH в кастрированных моделях на крысах.
Хинолиновые производные как непептидные антагонисты LHRH-рецептора раскрыты, например, в WO 97/14682. Замещенные 2-арилиндолы описаны, среди прочих, в WO 97/21435, WO 97/21703, WO 98/55116, WO 98/55470, WO 98/55479, WO 99/21553, WO 00/04013 как антагонисты LHRH-рецептора. Полезные биологические или биофизические данные для этих соединений не раскрыты.
Патент ЕР 0679642 В1 описывает сопряженные гетероциклические соединения в качестве антагонистов LHRH-рецептора. Основная тетрагидрокарбазольная структура, однако, не является предметом открытия, описанного там.
1,2,3,4-Тетрагидрокарбазолкарбоновые кислоты описаны в патенте ЕР 0239306 В1 в качестве простагландинового антагониста. Антагонистический эффект к LHRH-рецептору не описан и не является очевидным. U.S. Pat. No. 3,970,757 описывает производные тетрагидрокарбазола как желудочные антисекреторные агенты. Однако антагонистический эффект к LHRH-рецептору у этих структур не описан и не является очевидным. ЕР 603432 В1 и U.S. Pat. No. 5,708,187 описывают производные тетрагидрокарбазола в качестве 5-НТ1 агонистов, среди прочего, для лечения мигрени. Однако антагонистический эффект к LHRH-рецептору не описан и не является очевидным. WO 2005/033099 А2 описывает производные тетрагидрокарбазола в качестве дипептидилпептидазных IV ингибиторов. Однако антагонистический эффект к LHRH-рецептору не описан и не является очевидным. Ссылок на антагонистический эффект к LHRH-рецептору нет, и описанные структуры отличаются от соединений по настоящему изобретению. D.J.Davies et al. описывают в статье J. Med. Chem. 41, 451-467 (1998) производные тетрагидрокарбазола, имеющие мелатонин агонистический или антагонистический эффект. Однако антагонистический эффект к LHRH-рецептору не описан и не является очевидным. Производные тетрагидрокарбазола описаны S. J. Shuttleworth et al. в статье Bioorg. Med. Chem. Lett. 14, 3037-3042 (2004) в качестве частичных агонистов рецептора нейромедина В. Однако антагонистический эффект к LHRH-рецептору не описан и не является очевидным. R. Millet et al. описывает в Letters in Peptide Science 6, 221-233 (1999) производные тетрагидрокарбазола в качестве NK1/NK2 лигандов. Приведенные там структуры отличаются от соединений по настоящему изобретению. Более того, антагонистический эффект к LHRH-рецептору не описан и не является очевидным. Описание твердофазного синтеза 3-амино-3'-карбокситетрагидрокарбазолов имеется в работе Koppitz et al., THL 46(6), 911 -914 (2005). Антагонистический эффект к LHRH-рецептору не описан и не является очевидным.
Производные тетрагидрокарбазола в качестве пептидомиметиков антагонистов LHRH-рецептора, имеющие хорошее сродство к рецептору, описаны, например, в патенте WO 03/051837 (DE 10164564 А1). Физикохимические и метаболические свойства этих соединений, однако, не делают их оптимально подходящими для формы пероральной дозировки.
Многие публикации предоставляют обзор состояния развития нейрокининовых антагонистов. G.Giardina et al. в статье IDrugs 6(8), 758-772 (2003) дает обзор текущей патентой литературы. V. Leroy et al., Expert Opinion on Investigational Drugs 9(4), 735-746 (2000), и С. Swain et al., Annual Reports in Medicinal Chemistry 34, 51-60 (1999) описывают состояние развития относительно антагонистов нейрокининовых рецепторов, в то время как, например, R.M.Navari et al. в статье Cancer Investigation 22(4) 569-576 (2004) описывает результаты клинических исследований, в которых антагонисты NK1-рецептора были применены для контроля рвоты, вызываемой хемотерапией. R.G.Hill et al. описывает в работе Pain, 523-530 (2003) антагонисты нейрокининового рецептора в качестве потенциальных анальгетиков, в то время как A. von Sprecher et al. в IDrugs 1(1), 73-91 (1998) описывает антагонисты нейрокининового рецептора как потенциально активные компоненты для терапии воспалений и ревматических артритов. R. Millet et al. описывает в Letters in Peptide Science 6, 221-233 (1999) производные тетрагидрокарбазола как лиганды МK1/NK.2. Приведенные там структуры отличаются от соединений, описанных в настоящем изобретении.
Раскрытие изобретения
Задачей настоящего изобретения является разработка новых соединений с улучшенной пероральной биодоступностью и улучшенной метаболической стабильностью, которые могут быть применены для лечения патологических состояний, опосредованных GPCR, у млекопитающих и, в частности у человека. Новые соединения предпочтительно предназначаются для проявления биологической активности посредством ингибирования LHRH-рецептора. Новые соединения предназначаются для достижения желаемого эффекта в дозировках, которые допустимы к применению и эффект от которых зависит от дозировки при пероральном введении. Для этого требуется, чтобы новые соединения были применимы в качестве фармакологически активных компонентов в лекарственных препаратах для млекопитающих или людей. Цель изобретения достигнута с помощью новых улучшенных производных тетрагидрокарбазола общей формулы (I), приведенной ниже.
Осуществление изобретения
Первый аспект настоящего изобретения относится к новым производным тетрагидрокарбазола общей формулы (I):
в которой:
X1 означает S или О,
X2 и Х3 независимо один от другого означают О или геминально присоединенный Н2,
R1 и R2 независимо один от другого выбираются из группы, состоящей из атома водорода, арил-, алкил- и арилалкил- радикалов, которые могут быть замещены в алкильной или арильной группе заместителями в количестве до 3, независимо выбираемыми из группы, состоящей из атомов галогена, групп -CN и -O-алкил, где R1 и R2 оба прежде всего являются атомами водорода,
R3 означает алкил-, арилалкил-, или гетероарилалкил-радикал, которые необязательно замещены заместителями в количестве до 3, независимо выбираемыми из группы, состоящей из атомов галогена, групп -CN, -СО-O-R12, -CO-NR12R12', -ОН, -O-R13, -OCO-R13, -O-SO2-OR12, -O-SO2-R12, -SO2-OR12, -SO-R12, -OPO(OR12)(OR12'), -O-PO(NR12R12')2, -O-CO-O-R13, -O-СО-NR12R12', -O-CS-NR12R12', -S-R12, -NR12R12', -NH-CO-R13, -NH-SO2-R12, -NH-CO-OR13, -NH-CO-NHR12, -NH-C(NH)-NH2,
R4, R5, R6 и R7 независимо один от другого выбираются из группы, состоящей из атома водорода, атомов галогенов, групп -CN, -СОNН2, -СООН, -СF3, -O-алкил, -ОСF3, -NО2 и алкил-, арилалкил- и гетероарилалкил-радикалов;
R9 означает атом водорода, алкил-, арил-, гетероарил-, арилалкил- или гетероарилалкил-радикал, предпочтительно атом водорода;
R10 означает атом водорода, или радикал -R11, -CO-R11, -CO-OR11, -СО-NHR11, -C(NH)-NHR11, -SO2-R11 или -SO2-NHR11;
R11 означает алкил, арил-, гетероарил-, арилалкил- или гетероарилалкил-радикал, которые могут быть замещены одним или более заместителями, независимо выбираемыми из группы, состоящей из атомов галогена, групп -CN, -алкил, -СF3, -ОСF3, -ОН, -O-алкил и -O-(СН2СН2-O)n-СН3;
R8 означает -C1-C6-алкиларил или -C1-C6-алкилгетероарил, где арильная или гетероарильная группа замещена заместителями в количестве до трех, например одним, двумя, или тремя, но предпочтительно одним, независимо выбираемыми из группы, состоящей из групп -O-(СН2СН2-О)n-СН3, -O-CO-R12, -O-СО-(СН2СН2-O)n-СН3, -O-SO2-OR12, -O-SO2-R12, -O-PO(OR12)(OR12'), -O-PO(NR12R12')2, -O-CO-OR13, -O-CO-NR12R12' и -O-CS-NR12R12', или,
если по меньшей мере
(i) Х1 означает S, или
(ii) R10 не является атомом водорода, и R11 означает арилалкил- или гетероарилалкил-радикал, которые замещены в арильной или гетероарильной группе одним или более заместителем, предпочтительно одним, двумя или тремя заместителями, независимо выбираемыми из группы, состоящей из атомов галогенов, групп -CN, -алкил, -СF3, -OCF3, -ОН, -O-алкил и -O-(СН2СН2-O)n-СН3,
R8 также принимает значения, указанные для R3;
R12 и R12' независимо один от другого означают атом водорода или алкил-, арилалкил-, арил-, гетероарилалкил- или гетероарил-радикал, предпочтительно водород,
R13 выбирается из алкил-, арилалкил-, гетероарилалкил- или гетероарил-радикалов, или группы -(CH2CH2-O)n-CH3, и
n представляет собой любое целое число от 1 до 10, предпочтительно от 1 до 6.
Термины, указанные для толкования соединений, соответствующих общей формуле (I), всегда, если не указано иначе в описании или формуле изобретения, имеют следующие значения:
термин «замещенный» означает, что соответствующий радикал или группа имеет один или более заместителей. Если радикал имеет несколько заместителей, и выборка различных заместителей определена, заместители выбираются независимо друг от друга и не обязательно являются идентичными. Термин «незамещенный» означает, что соответствующая группа не имеет заместителей. Термин «необязательно замещенный» означает, что соответствующая группа или незамещена или замещена одним или более заместителем. Термин «замещенный заместителями в количестве до 3» означает, что соответствующий радикал или группа замещены или одним, или двумя, или тремя заместителями.
Термин «атом галогена» или «галогеновый заместитель» (Hal-) относится к одному, а где применимо, к нескольким атомам фтора (F, фтор-), брома (Вr, бром-), хлора (Сl, хлор-), или иода (I, иод-). Обозначения «дигалоген», «тригалоген» и «пергалоген» относятся соответственно к двум, трем или четырем заместителям, где каждый заместитель может быть выбран независимо из группы, состоящей из фтора, хлора, брома и иода. «Галоген» предпочтительно означает атом фтора или хлора.
Термин «алкил» включает в контексте данного изобретения ациклические насыщенные или частично ненасыщенные углеводороды, имеющие С1-С12 углеродных атомов, которые могут быть линейными или разветвленными. Термин «алкил» предпочтительно означает алкильные цепочки от 1 до 8, в особенности предпочтительно от 1 до 6 атомов углерода. Примеры подходящих алкильных радикалов представляют собой метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, н-пентил, трет-пентил, 2- или 3-метилпентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, пропенил, бутенил, пентенил, гексенил и октадиенил. Термин «алкил» также означает насыщенные или частично ненасыщенные циклоалкильные радикалы, предпочтительно из группы цикло (С3-С8) алкилов. Примеры подходящих циклоалкильных радикалов представляют собой циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклогексенил, циклопентенил, циклооктадиенил и другие. В дополнение, термин «алкил» включает циклоалкилалкильные группы, с предпочтением для цикло(С3-С8)алкил(С1-С4)алкильных радикалов. Их примерами являются циклопропилметил, циклогексилметил, циклопентилэтил, циклогексенилэтил. Таким образом, термин С1-С4-алкил охватывает как минимум следующие группы: метил, этил, н-пропил, изопропил, пропенил, циклопропил, н-бутил, втор-бутил, трет-бутил, циклобутил, циклопропилметил, и бутенил. Наиболее предпочтительными в качестве С1-С4-алкилов являются изопропил, втор-бутил, и циклопропилметил.
Такой алкильный радикал может быть незамещенным, а также моно- или полизамещенным, где заместители могут быть идентичными или различными и быть связанными в каждом или более чем одном желаемом и возможном положении алкила. В случае моно- или полигалоген-замещенных алкильных радикалов, замещение атомами фтора и/или хлора является предпочтительным. Примерами таких радикалов являются фторметил, трифторметил и пентафторэтил.
"Арил" соответствует ароматическим углеводородным системам, имеющим от 3 до 14, предпочтительно от 5 до 14, атомов углерода, которые также могут быть сконденсированы в дальнейшие насыщенные, (частично) ненасыщенные или ароматические циклические системы. Примерами «арилов» являются, среди прочих, фенилы, нафтилы и антраценилы, но также инданилы, инденилы, или 1,2,3,4-тетрагидронафтилы; фенил в особенности предпочтителен для целей данного изобретения. Такой арильный радикал может быть незамещенным или по выбору моно- или полизамещенным, где заместители могут быть одинаковыми или различными и быть связанными в каждом или более чем одном желаемом и возможном положении арила.
«Гетероарил» соответствует 5-, 6- или 7-членным циклическим ароматическим радикалам, которые имеют в своем составе по меньшей мере 1, а где возможно также 2, 3, 4 или 5 гетероатомов, предпочтительно азот, кислород и/или серу, причем гетероатомы одинаковы или различны. Число атомов азота предпочтительно между 0 и 3, а атомов кислорода и серы между 0 и 1. Термин «гетероарил» также включает системы, в которых гетероцикл является частью би- или полициклической системы, а соединение гетероароматического остатка с веществом общей формулы (I) возможно через любой желаемый и возможный член цикла гетероароматического остатка. Примеры «гетероарила» включают пирролил, тиенил, фурил, имидазолил, тиазолил, изотиазолил, оксазолил, изоксазолил, пиразолил, пиридинил, пиримидинил, пиразинил, индолил, хинолинил, и изохинолинил. Такие гетероароматические радикалы могут оставаться незамещенными или моно- или полизамещенными, где заместители могут быть одинаковыми или различными и быть связанными в каждом или более чем одном желаемом и возможном положении гетероарила.
»Арилалкил» или «гетероарилалкил» соответствует радикалам, в которых арильный или гетероарильный радикал соединен через С1-С8-алкильную группу с веществом общей формулы (I), где алкильные, арильные и гетероарильные группы имеют значение определенное выше. Предпочтительными «арилалкильными» группами являются фенил-С1-С4-алкильные радикалы, предпочтительно бензил или фенилэтильные радикалы.
»Циклическая система» соответствует моно- или полициклической системе, имеющей от 3 до 14, предпочтительно от 5 или 5 до 14 атомов в цикле, которые могут быть исключительно атомами углерода. Однако циклическая система может также включать 1, 2, 3, 4 или 5 гетероатомов, в особенности азот, кислород и/или серу. Циклическая система может быть насыщенной, моно- или полиненасыщенной или полностью или частично ароматической, и в случае циклической системы, состоящей как минимум из двух циклов, эти циклы могут быть конденсированными, или спиро-, или как-то иначе соединенными.
Как указано выше в связи с общей формулой (I), вещества по данному изобретению могут, поскольку они имеют по меньшей мере один центр асимметрии, существовать в форме своих рацематов, в форме чистых энантиомеров и/или диастереомеров или в форме смесей этих энантиомеров и/или диастереомеров. Такие смеси могут иметь какое угодно соотношение стереоизомеров.
Предпочтительными соединениями общей формулы (I) являются такие, которые имеют R-конфигурацию у углеродного атома, замещенного заместителями -NН-СХ3- и -CX2-NH-, то есть соответствующие общей формуле (I-а):
Особенно предпочтительными соединениями общей формулы (I) являются такие, которые имеют R-конфигурацию у углеродного атома, замещенного заместителями -NН-СХ3- и -СХ2-NН-, (S)-конфигурацию у углеродного атома, замещенного заместителями -СХ3-NН-, -R8 и -NR9R10, а также (S)-конфигурацию у углеродного атома, замещенного заместителями -NH-CX2-, -R3 и -CX1-NR1R2, то есть имеют природную S-конфигурацию соответствующих аминокислоту этих стереоцентров. Эти соединения имеют общую формулу (I-б):
Где возможно, соединения по настоящему изобретению могут быть в форме таутомеров.
Так, например, соединения по настоящему изобретению, соответствующие общей формуле (I), которые имеют один или более хиральных центров и которые существуют в виде рацематов или как смеси диастереомеров, могут быть разделены известными методами на их чистые оптические изомеры, то есть энантиомеры или диастереомеры. Разделение соединений по настоящему изобретению или их строительных блоков (аминокислот) может осуществляться посредством разделения на колонке на хиральных или нехиральных фазах, или посредством перекристаллизации из необязательно оптически активного растворителя, или с использованием оптически активной кислоты или основания, или посредством модифицирования оптически активным реагентом, таким как, например, оптически активный спирт, и последующего удаления радикала.
Соединения по настоящему изобретению, соответствующие общим формулам (I, Ia и Iб), могут, если они имеют достаточно основные группы, такие как, например, вторичный или третичный амин, быть превращены неорганическими или органическими кислотами в соли. Фармацевтически приемлемые соли сотолуолсульфокислотой, угольной кислотой, муравьиной кислотой, уксусной кислотой, сульфоуксусной кислотой, трифторуксусной кислотой, щавелевой кислотой, малоновой кислотой, малеиновой кислотой, янтарной кислотой, винной кислотой, рацемической кислотой, яблочной кислотой, эмбоновой кислотой, миндальной кислотой, фумаровой кислотой, молочной кислотой, лимонной кислотой, таурохолиевой кислотой, глутаминовой кислотой или аспарагиновой кислотой. Формируемые соли представляют собой, среди прочих, гидрохлориды, гидробромиды, сульфаты, фосфаты, метансульфонаты, тозилаты, карбонаты, бикарбонаты, форматы, ацетаты, сульфоацетаты, трифлаты, оксалаты, малонаты, малеаты, сукцинаты, тартраты, малаты, эмбонаты, манделаты, фумараты, лактаты, цитраты и глутаматы. Стехиометрия формируемых солей соединений по настоящему изобретению может, к тому же, быть составным или несоставным кратным числом единицы.
Соединения по настоящему изобретению, соответствующие общим формулам (I, Ia и Iб), могут, если они содержат достаточно кислую группу, такую как, например, карбоксильную, сульфокислотную, фософорнокислую или фенольную группу, быть превращены неорганическими или орган-гидроксид натрия, гидроксид калия, гидроксид кальция, и органических оснований - этаноламин, диэтаноламин, триэтаноламин, циклогексиламин, дибензилэтилендиамин и лизин. Стехиометрия формируемых солей соединений по настоящему изобретению может, к тому же, быть составным или несоставным кратным числом единицы.
Также возможно для соединений по настоящему изобретению, соответствующих общим формулам (I, Ia и Iб), существовать в форме их сольватов и особенно гидратов, которые получаются, например, при кристаллизации из растворителя или из водного раствора. Также возможно для одной, двух, трех или любого числа молекул растворителя или воды комбинироваться с соединениями по настоящему изобретению с образованием сольватов или гидратов.
Известно, что химические субстанции формируют твердые вещества, которые существуют в различных упорядоченных состояниях, которые обозначаются как полиморфные формы или модификации. Различные модификации полиморфного вещества могут сильно различаться по своим физическим свойствам. Соединения по настоящему изобретению, соответствующие общим формулам (I, Ia и Iб), могут существовать в различных полиморфных формах, и к тому же определенные модификации могут быть метастабильными. Все такие полиморфные формы соединений, соответствующих общим формулам (I, Ia и Iб), должны расцениваться как принадлежащие к данному изобретению.
Также возможно для соединений по настоящему изобретению, соответствующих общим формулам (I, Ia и Iб), существовать в форме любых пролекарств, таких как, например, эфиры, карбонаты или фосфаты, в случае которых истинная биологически активная форма высвобождается только посредством метаболизма.
Известно, что химические вещества превращаются в организме в метаболиты, которые также могут, где возможно, проявлять желаемый биологический эффект - в некоторых обстоятельствах даже в более выраженной форме.
Известно для тиоамидов (Х1=S), например (Casarett & Doull's "Toxicology, the Basic Science of Poisons", Chapter 6: Biotransformation of Xenobiotics, C.D.Klaassen Ed., McGraw-Hill 2001; D.M.Clayton, Biochem. Soc. Trans., 1978, 6(1), 94-96), что они также могут быть метаболизированы до тиоамид-3-оксидов. Эти вещества могут быть также получены синтезом из соответствующих тиоамидов окислением перекисью водорода (Н2О2) (J.R.Cashman et al., J. Org. Chem., 1982, 47 (24), 4645-4650). Так, соединение 68 окисляется, например, в (R)-S-хлор-6-фтор-3-{(S)-2-[2-(2-фторфенил)ацетиламино]-3-метилпентаноиламино}-2,3,4,9-тетрагидро-1Н-карбазол-3-карбоновой кислоты ((S)-2-метил-1-тиокарбамоилбутил)амид-S-оксид, и соединение 76 окисляется до (R)-3-{(S)-2-[2-(2-фторфенил)ацетиламино]-3-метилпентаноиламино}-8-трифторметил-2,3,4,9-тетрагидро-1Н-карбазол-3-карбоновой кислоты ((S)-2-метил-1-тиокарбамоилбутил)амид-S-оксида.
Соответствующие метаболиты соединений соответствующих общим формулам (I, Ia и Iб), особенно с Х1=S+-O-, должны расцениваться как принадлежащие к данному изобретению.
Можно дополнительно заметить в этой связи, что термин «рецепторный лиганд» или «лиганд» в контексте данного изобретения предназначается для обозначения каждого соединения, которое связывается любым образом с рецептором (рецептор в данном изобретении это GPCR-рецептор, предпочтительно LHRH-рецептор) и индуцирует или активацию, или ингибирование и/или другой мыслимый эффект на этом рецепторе. Термин «лиганд», таким образом, охватывает агонисты, антагонисты, частичные агонисты/антагонисты и другие лиганды, которые вызывают эффект на рецепторе, сходный с эффектом агонистов, антагонистов или частичных агонистов/антагонистов. Соединения по настоящему изобретению, соответствующие общим формулам (I, Ia и Iб), являются предпочтительно антагонистами LHRH-рецептора (GnRH-рецептор).
Предпочтительными соединениями, соответствующими общим формулам (I, Ia и Iб) для целей данного изобретения являются такие, где Х означает атом серы или S+-O-, предпочтительно атом серы, и R8 является алкильным, арилалкильным или гетероарилалкильным радикалом, где эти радикалы необязательно замещены заместителями в количестве до 3, выбранными из группы, состоящей из атомов галогена, групп -CN, -СО-O-R12, -CO-NR12R12', -OH, -O-R13, -O-CO-R13, -O-SO2-OR12, -O-SO2-R12, -SO2-OR12, -SO-R12, -O-PO(OR12)(OR12'), -O-PO(NR12R12')2, -O-CO-O-R13, -O-СО-NR12R12', -O-CS-NR12R12', -S-R12, -NR12R12', -NH-CO-R13, -NH-SO2-R12, -NH-CO-O-R13, -NH-CO-NHR12, -NH-C(NH)-NH2, где R12, R12' и R13 имеют значения, обозначенные выше.
Предпочтительными для целей данного изобретения являются также соединения, соответствующие общим формулам (I, Ia и Iб), где
R10 является радикалом -R11, -CO-R11, -CO-OR11, -CO-NHR11, -C(NH)-NHR11, -SO2-R11, или -SO2NHR11,
R11 представляет собой арилалкильный или гетероарилалкильный радикал, который замещен в арильной или гетероарильной группе одним или более заместителями, независимо выбранными из группы, состоящей из атомов галогенов, групп -CN, -алкил, -СF3, -ОСF3, -ОН, -O-алкил и -O-(СН2СН2-O)n, -СН3, и
R8 представляет собой алкильный, арилалкильный или гетероарилалкильный радикал, который по выбору замещен заместителями в количестве до 3, независимо выбранными из группы, состоящей из атомов галогенов, групп -CN, -CO-O-R12, -CO-NR12R12', -ОН, -O-R13, -O-CO-R13, -O-SO2-OR12, -SO2-OR12, -O-SO2-R12, -SO-R12, -O-PO(OR12)(OR12'), -O-PO(NR12R12')2, -O-CO-O-R13, -O-CO-NR12R12', -O-CS-NR12R12', -S-R12, -NR12R12', -NH-CO-R13, -NH-SO2-R12, -NH-CO-O-R13, -NH-CO-NHR12, -NH-C(NH)-NH2, где R12, R12' и R13 имеют значения, обозначенные выше.
Также предпочтительными соединениями, соответствующими общим формулам (I, Ia и Iб), для целей данного изобретения являются такие, где R8 является или -C1-C6-алкиларильным, или -C1-C6-алкилгетероарильным радикалом, где арильная или гетероарильная группа замещена заместителями в количестве от одного до трех, предпочтительно одним, независимо выбранными из группы, состоящей из групп -O-(СН2СН2-O)n-СН3, -O-CO-(CH2CH2-O-)n-CH3, -O-SO2-OR12, -O-SO2-R12, -O-PO(OR12)(OR12'), -O-PO(NR12R12')2, -O-CO-OR13, -O-CO-NR12R12' и -O-CS-NR12R12', где R12, R12' и R13 имеют значения, обозначенные выше.
В предпочтительном варианте данного изобретения, по меньшей мере один, предпочтительно два, из радикалов R4, R5, R6, и R7, предпочтительно R5 и R7, не являются атомами водорода. Радикалы R5 и R7 выбираются независимо один от другого прежде всего из группы, состоящей из атома водорода, атомов галогенов, групп -CN, -СF3, -O-алкил и -ОСF3, и предпочтительно являются атомом водорода, галогена или группой -СF3. Особенно предпочтительны те соединения, в которых R4 и R6 каждый является атомом водорода, R5 - или атомом водорода или атомом галогена, и R7, независимо от R5, является либо атомом галогена, либо группой -СF3.
Также предпочтительными соединениями, соответствующими общим формулам (I, Ia и Iб), для целей данного изобретения являются такие, где X2 и Х3 каждый представляют собой О.
В предпочтительном варианте данного изобретения, R3 представляет собой C1-C6-алкильный радикал, предпочтительно С1-С4-алкильный радикал.
Предпочтительными соединениями для целей данного изобретения являются такие, где R1, R2, R9, и также R12 и R12', если они есть, каждый представляют собой атом водорода.
Также предпочтительными соединениями, соответствующими общим формулам (I, Ia и Iб), являются такие, в которых R13 это фенил-С1-С4-алкильный радикал, или группа -(CH2CH2-O)n-CH3.
В предпочтительных соединениях общей формулы (I, Ia и Iб), R10 означает -CO-R11, -CO-OR11 или R11, где R11 принимает значения, указанные выше.
Также предпочтительными соединениями, соответствующими общим формулам (I, Ia и Iб), являются такие, в которых R11 представляет собой фенил-С1-С4-алкильный радикал, предпочтительно бензильный или фенилэтильный радикал, который замещен в фенильной группе по выбору заместителями в количестве от одного до трех, предпочтительно одним или двумя, независимо выбранными из группы, состоящей из атомов галогенов, -С1-С4-алкил, -СF3, -ОСF3, -ОН, -О-С1-С4-алкил и -O-(CH2CH2-O)n-CH3-.
Ос