Изомеры стевиол-гликозидов
Иллюстрации
Показать всеДанное изобретение относится к соединениям формулы II
где R1 может быть 1-β-D-глюкопиранозилом или 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 может быть водородом, 1-β-D-глюкопиранозилом, 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом или 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. Такие соединения могут быть использованы в качестве подсластителей, не обладающих питательными качествами, в пищевых и питьевых продуктах. Раскрываются также способы получения соединений формулы II. 6 н. и 29 з.п. ф-лы, 23 ил.
Реферат
Заявление об установлении приоритета.
Данная заявка устанавливает приоритет заявки на патент США, серийный №11/856274, зарегистрированной 17 сентября 2007 и озаглавленной "Изомеры стевиол-гликозидов" (№ Реестра патентных поверенных №056943.00381), полное раскрытие которой включено здесь посредством ссылки.
Область техники, к которой относится изобретение.
Данное изобретение относится к некоторым новым изомерам стевиол-гликозидов, пригодным для применения в качестве подсластителей, например, путем включения в пищевые и питьевые продукты.
Предшествующий уровень техники.
Из-за возрастающего внимания к отрицательному влиянию ожирения на здоровье в Соединенных Штатах и во всем мире увеличивается также рыночный спрос на пищевые и питьевые продукты с альтернативными питательными характеристиками, включая, например, сниженное или нулевое содержание калорий. Имеется рыночный спрос на замену высококалорийных подсластителей, обычно применяемых в пищевых и питьевых продуктах, таких как сахароза и кукурузный сироп с высоким содержанием фруктозы (КСВСФ), подсластителями, не обладающими питательными качествами. Например, предложены напитки диетической колы, подслащенные сильными подсластителями, не обладающими питательными качествами, таким как стевиол-гликозиды (стевиозид, ребаудиозид А и т.д.).
Стевиол-гликозиды являются соединениями, обладающими сладким вкусом, экстрагируемыми из растения стевии (Stevia rebaudiana Bertoni). Установлено, что обычно эти соединения включают стевиозид (4-13% от массы сухого вещества), стевиолбиозид (следовое количество), ребаудиозиды, включая ребаудиозид А (1-6%), ребаудиозид В (следовое количество), ребаудиозид С (1-2%), ребаудиозид D (следовое количество), и ребаудиозид Е (следовое количество), и дулькозид А (0,4-0,7%). Многие стевиол-гликозиды являются сильными подсластителями, не обладающими питательными качествами. Стевиол-гликозиды включают дитерпеновую сердцевину (формула I), замещенную в R1 и R2 различными комбинациями водорода, глюкозы, рамнозы и ксилозы.
Например, R1 может быть водородом, 1-β-D-глюкопиранозилом или 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 может быть водородом, 1-β-D-глюкопиранозилом, 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-1-(3-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-3-(1-(β-D-глюкопиранозил)-1-β-D-глюкопиранозилом или 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. Ребаудиозид А (в котором R1=1-β-D-глюкопиранозил, а R2=2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозил) примерно в 200-300 раз слаще сахарозы. Для пищевой промышленности представляют интерес стевиол-гликозиды в качестве альтернативных подсластителей. Однако прямая замена питательных подсластителей известными сильными подсластителями, не имеющими питательных качеств, создает проблемы посторонних привкусов, например, медленного развития, или горького, лакричного или затяжного послевкусия. Эти посторонние привкусы также возникают, когда стевиол-гликозиды применяют в пищевых и питьевых продуктах в качестве подсластителей, не имеющих питательных свойств. Таким образом, имеется потребность в дополнительных альтернативных подсластителях, не обладающих питательными качествами.
Таким образом, задачей по меньшей мере некоторых воплощений настоящего изобретения является обеспечение соединений, пригодных в качестве подсластителей. Задачей по меньшей мере некоторых воплощений изобретения является обеспечение питьевых или пищевых продуктов с альтернативными питательными характеристиками и вкусовыми свойствами. Имеются и другие задачи, черты и преимущества изобретения или конкретных воплощений изобретения, которые будут понятны для специалистов в данной области техники из следующего раскрытия и описания примерных воплощений.
Краткое изложение сущности изобретения.
Раскрывается семейство новых изомеров стевиол-гликозидов. В этих изомерах экзо-циклическая двойная связь формулы I перемещена в эндо-циклическое положение внутри пятичленного кольца (см. формулу II). Эти соединения пригодны в качестве подсластителей, и могут быть включены как таковые в пищевые и питьевые продукты. В соответствии с первым аспектом изобретения обеспечивается соединение, имеющее формулу II
При этом R1 может быть водородом, 1-β-D-глюкопиранозилом или 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 может быть водородом, 1-β-D-глюкопиранозилом, 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом или 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. В некоторых примерных воплощениях соединение формулы II может быть выделено и очищено. Как применяется здесь, «выделено и очищено» означает, что чистота изомера стевиол-гликозида составляет по меньшей мере 90%.
В соответствии с другими аспектами обеспечивается питьевой продукт, включающий водосодержащую жидкость и соединение формулы II.
В соответствии с другими аспектами обеспечивается пищевой продукт, включающий пищевой компонент и соединение формулы II.
В соответствии с другим аспектом изобретения обеспечивается подсластитель, включающий соединение формулы П.
В соответствии с другим аспектом обеспечивается способ для приготовления соединений формулы II, включающий этапы обеспечения кислого водного раствора, включающего соединение формулы I, и нагревания кислого водного раствора до температуры в диапазоне от 30 до 90°C в течение периода времени более двух суток. В некоторых примерных воплощениях кислые водные растворы, включающие ребаудиозид А, нагревают до температуры в диапазоне от 40 до 50°C при pH в диапазоне 1,0-4,0 в течение периода времени более двух суток.
Краткое описание чертежей.
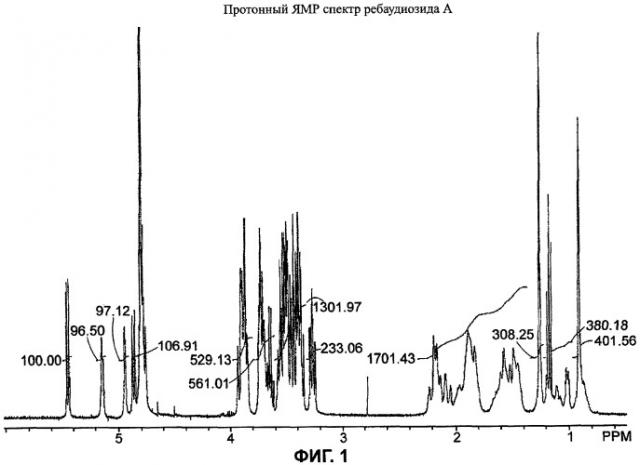
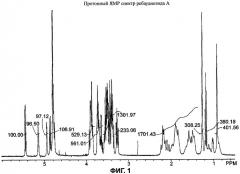
Фиг.1 является протонным ЯМР спектром ребаудиозида А.
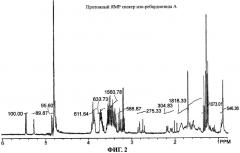
Фиг.2 является протонным ЯМР спектром изо-ребаудиозида А.
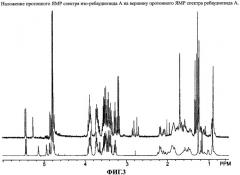
Фиг.3 является наложением спектров из фиг.1 и 2.
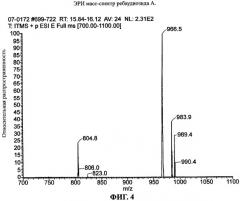
Фиг.4 является ЭРИ масс-спектром ребаудиозида А.
Фиг.5 является ЭРИ масс-спектром изо-ребаудиозида А.
Фиг.6 является ВЭЖХ хроматограммой 10-недельной реакционной смеси, содержащей ребаудиозид А и изо-ребаудиозид А.
Фиг.7 является ЭРИ масс-спектром пика изо-ребаудиозида А из Фиг.6.
Фиг.8 является ВЭЖХ хроматограммой ребаудиозида А.
Фиг.9 является ВЭЖХ хроматограммой изо-ребаудиозида А.
Фиг.10 является ЭРИ масс-спектром пика ребаудиозида А из Фиг.8.
Фиг.11 является ЭРИ масс-спектром пика изо-ребаудиозда из Фиг.9.
Фиг.12 является ВЭЖХ хроматограммой 10-недельной реакционной смеси, обогащенной выделенным изо-ребаудиозидом А.
Фиг.13 является ЭРИ масс-спектром пика изо-ребаудиозида из Фиг.12.
Фиг.14 является изображением рентгеновской структуры кристаллов изо-ребаудиозида А.
Фиг.15 является изображением рентгеновской структуры кристаллов ребаудиозида А.
Фиг.16 является сравнением структур ребаудиозида А и изо-ребаудиозида А.
Фиг.17 и 18 показывают зависимость скорости синтеза изо-ребаудиозида А (Соед.Х) из ребаудиозида А (Реб.А) от рН.
Фиг.19 показывает зависимость скорости синтеза изо-ребаудиозида А (Соед.Х) из ребаудиозида А (Реб.А) от температуры.
Фиг.20 является протонным ЯМР-спектром ребаудиозида В.
Фиг.21 является протонным ЯМР спектром изо-ребаудиозида В.
Фиг.22 является наложением спектров из Фиг.20 и 21.
Фиг.23 является наложением ВЭЖХ хроматограмм ребаудиозида В, изо-ребаудиозида В и 1:1 смеси двух соединений.
Подробное описание некоторых примерных воплощений.
В некоторых примерных воплощениях изомеры стевиол-гликозидов из настоящего изобретения могут быть определены общей формулой II
При этом R1 может быть водородом, 1-β-D-глюкопиранозилом или 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 может быть водородом, 1-β-D-глюкопиранозилом, 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-1-β-D-глюкопиранозилом, 2-(1-α-L-рамнопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом или 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. Некоторые примерные воплощения включают соединения формулы II, в которых R1 является 1-β-D-глюкопиранозилом, а R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозид A), R1 является 1-β-D-глюкопиранозилом, а R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-стевиозид), R1 является водородом, а R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозид В), R1 является водородом, а R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-стевиолбиозид), R1 является 1-β-D-глюкопиранозилом, а R2 является 1-β-D-глюкопиранозилом (изо-рубузозид), R1 является 1-β-D-глюкопиранозилом, а R2 является 2-(1-α-L-рамнопиранозил)-1-β-D-глюкопиранозилом (изо-дулькозид A), R1 является 1-β-D-глюкопиранозилом, а R2 является 2-(1-α-L-рамнопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозой (изо-ребаудиозид С), R1 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, а R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозид D), R1 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, а R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозид Е), R1 является 1-β-D-глюкопиранозилом, а R2 является 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозид F), R1 является водородом, а R2 является 1-β-D- глюкопиранозилом (изо-стевиолмонозид), или R1 является 1-β-D- глюкопиранозилом, а R2 является водородом (изо-стевиол II глюкозил эфир). Одно примерное воплощение включает соединение формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. Это соединение имеет структуру, показанную в Формуле III ниже. Далее это соединение обозначается как изо-ребаудиозид А.
В некоторых примерных воплощениях изомеры стевиол-гликозидов, раскрытые здесь, могут быть приготовлены путем нагревания ребаудиозида А в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, таких как примерно pH 2,0-2,5) в течение достаточного периода времени (например, более двух суток, то есть от двух суток до примерно 11 недель) для получения изо-ребаудиозида А (формула III). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида А превращается в изо-ребаудиозид А. Литературные данные позволяют предположить, что при сильно кислых условиях (pH 2,4-2,6) стевиозид или ребаудиозид А достаточно стабильны при 60°C, но подвергаются резким изменениям при 100°C, с получением побочных продуктов гидролиза, таких как глюкоза, стевиолбиозид (из стевиозида), ребаудиозид В (из ребаудиозида А), и неизвестных соединений, имеющих значительно удаленные от стевиозида или ребаудиозида А факторы удерживания при ТСХ или время удерживания при ВЭЖХ. Когда стевиозид подвергали воздействию высоких температур, также формировался изо-стевиол (формула IV) (S.S.Chang and J.M. Cook, J. Agric. Food Chem., 31, 409-412 (1983)).
В других литературных источниках указано, что кислотно-катализируемый гидролиз стевиозида приводит к образованию изо-стевиола (М.Bridel and R.Lavieille, Journal de Pharmacie et de Chimie, 14, 321-32 и 369-379 (1931); J.R. Hanson and B.H. Oliverira, Natural Product Reports, 10, 301-309 (1993)). Было показано, что изо-стевиол является продуктом перегруппировки Вагнера-Меервейна, включающей инверсию D-кольца стевиола (формула I, в которой каждый из R1 и R2 является водородом). Таким образом, литературные данные свидетельствуют, что стевиол-гликозиды, например ребаудиозид А, подвергаются каждый кислотно-катализируемой изомеризации, с получением продукта, также содержащего изостевиол в качестве агликонового компонента.
Но удивительно, было установлено, что кислотная и тепловая обработка стевиол-гликозидов, например ребаудиозида А, в соответствии с настоящим изобретением, приводит к образованию изомеров стевиол-гликозидов Формулы II, например изо-ребаудиозида А (формула III), имеющих агликоновый компонент, который не является ни стевиолом, ни изо-стевиолом, но скорее новым агликоновым компонентом, имеющим перемещенную двойную связь по сравнению со стевиолом. Неожиданный агликоновый компонент из нового соединения далее называют изо-стевиолом II (см. формулу II). Когда R1 и R2 в Формуле II каждый является водородом, соединение называют изо-стевиолом II (формула V).
В некоторых примерных воплощениях изомеры стевиол-гликозидов, раскрытые здесь, могут быть гидролизованы для удаления глюкозных, рамнозных и/или ксилозных единиц. Таким образом, изомеры стевиол-гликозидов, например изо-ребаудиозиды A-F, изо-стевиозид, изо-дулькозид и т.д., могут быть гидролизованы при дальнейшей обработке нагреванием и кислотой в различные другие изомеры стевиол-гликозидов, например изо-стевиозид, изо-ребаудиозид В, изо-стеволбиозид, изо-рубузозид, изо-стевиолмонозид, изо-стевиол II глюкозил эфир и т.д. Таким образом, в качестве не ограничивающего примера ребаудиозид А может быть изомеризован путем обработки нагреванием и кислотой в изо-ребаудиозид А в качестве промежуточного продукта, который может быть гидролизован в изо-ребаудиозид В. В некоторых примерных воплощениях исходные материалы стевиол-гликозидов могут быть вначале гидролизованы для удаления одной или более глюкозной, рамнозной, и/или ксилозной единиц, а затем изомеризованы до изомеров стевиол-гликозидов. В качестве не ограничивающего примера ребаудиозид A может быть гидролизован путем обработки нагреванием и кислотой до ребаудиозида B в качестве промежуточного продукта, который может быть изомеризован до изо-ребаудиозида В.
В некоторых примерных воплощениях кислый водный раствор, имеющий pH в диапазоне 1,0-4,0 (например, в диапазоне 2,0-2,5) и включающий ребаудиозид А (т.е. соединение формулы I, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом), нагревают до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C или в диапазоне от примерно 40°C до примерно 50°C) в течение достаточного периода времени (например, более двух суток, то есть от двух суток до примерно 11 недель) до получения изо-ребаудиозида В (т.е. соединения формулы II, в котором R1 является водородом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом). В одном примерном воплощении при вышеуказанных условиях ребаудиозид А вначале превращается в изо-ребаудиозид А, который затем превращается в изо-ребаудиозид B. В другом примерном воплощении при вышеуказанных условиях ребаудиозид A превращается в ребаудиозид B, который затем превращается в изо-ребаудиозид B. В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида A превращается в изо-ребаудиозид B.
В других примерных воплощениях каждый из изомеров стевиол-гликозидов, раскрытых здесь, может быть приготовлен путем обработки подходящего стевиол-гликозида, например соответствующего стевиол-гликозида, кислотой и нагреванием в соответствии со способом изобретения. А именно, стевиозид может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-стевиозида). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала стевиозида превращается в изо-стевиозид. Подобным образом, ребаудиозид В может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является водородом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозида В). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида В превращается в изо-ребаудиозид В. Стевиолбиозид может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения из формулы II, в котором R1 является водородом, a R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-стевиолбиозида). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала стевиолбиозида превращается в изо-стевиолбиозид. Рубузозид может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при рН около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 1-β-D-глюкопиранозилом (изо-рубузозида). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала рубузозида превращается в изо-рубузозид. Стевиолмонозид может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при рН около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения из формулы II, в котором R1 является водородом, a R2 является 1-β-D-глюкопиранозой (изо-стевиолмонозида). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала стевиолмонозида превращается в изо-стевиолмонозид. Стевиол глюкозы эфир (Формула I, R1 является 1-β-D-глюкопиранозилом, a R2 является водородом) может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозой, a R2 является водородом (изо-стевиол II глюкозил эфира). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала стевиол глюкозы эфира превращается в изо-стевиол II глюкозил эфир. Дулькозид А может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при рН около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2-(1-α-L-рамнопиранозил)-1-β-D-глюкопиранозилом (изо-дулькозида А). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала дулькозида А превращается в изо-дулькозид А. Ребаудиозид С может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2-(1-α-L-рамнопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозой (изо-ребаудиозида С). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида С превращается в изо-ребаудиозид С. Ребаудиозид D может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозида D). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида D превращается в изо-ребаудиозид D. Ребаудиозид Е может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C) или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения ормулы II, в котором R1 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом, a R2 является 2-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозида Е). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида Е превращается в изо-ребаудиозид Е. Ребаудиозид F может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, 43°C, 65°C, 75°C, 85°C, или в диапазоне от примерно 40°C до примерно 50°C) в сильно кислых условиях (например, при pH около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения соединения формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2-(1-β-D-ксилопиранозил)-3-(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом (изо-ребаудиозида F). В некоторых примерных воплощениях по меньшей мере 1,0% по массе (например, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 25%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 90% по массе) от исходного материала ребаудиозида F превращается в изо-ребаудиозид F. Могут применяться другие способы синтеза, например, ферментативная изомеризация. Изомеры стевиол-гликозидов могут быть выделены и очищены, например, посредством хроматографии, перекристаллизации, и т.д.
Примеры кислот, подходящих для приготовления изомеров стевиол-гликозидов в сильно кислых условиях, включают неорганические кислоты, такие как фосфорная кислота, соляная кислота, азотная кислота, серная кислота и т.д., и/или органические кислоты, такие как лимонная кислота, яблочная кислота, виннокаменная кислота, молочная кислота, аскорбиновая кислота и т.д. Одну или более кислот и факультативно соответствующую соль кислоты (например, лимонную кислоту и цитрат) включают в реакционную смесь в количестве, достаточном, чтобы сделать реакционную смесь сильно кислой (например, чтобы достигнуть значения pH в диапазоне примерно 1,0-4,0, например pH 2,0-2,5). Может также применяться ферментативная изомеризация.
Стевиол-гликозиды формулы I, по одиночке или в виде смеси, могут иметь дополнительное число β-D-глюкопиранозильных единиц, ковалентно связанных 4→1 с существующими β-D-глюкопиранозильными единицами в R1 и/или R2 посредством реакций ферментативного трансглюкозилирования с крахмалом, приводя к получению комплексной смеси продуктов (См. Kazuhiro Ohtani and Kazuo Yamasaki, Chapter 7, "Method to improve the taste of the sweet principles of Stevia rebaudiana", p.145, в книге, озаглавленной "Stevia, The genus Stevia", под редакцией A. Douglas Kinghorn, Taylor & Francis, 2002). Эти ферментативно-модифицированные экстракты стевии коммерчески доступны для применения в качестве подсластителей в пищевых и питьевых продуктах. Изомеры стевиол-гликозидов формулы II могут быть подвергнуты тому же самому виду реакций ферментативного трансглюкозилирования, что приводит к получению комплексной смеси продуктов, пригодных для применения в качестве подсластителей для пищевых и питьевых продуктов. Также предполагается, что продукт ферментативного трансглюкозилирования стевиол-гликозидов формулы I может быть нагрет в водном растворе до температуры в диапазоне от примерно 30°C до примерно 90°C (например, в диапазоне от примерно 40°C до примерно 50°C, такой как 43°C) в сильнокислых условиях (например, при рН около 1,0-4,0, то есть при pH около 2,0-2,5) в течение достаточного периода времени (например, больше двух суток, то есть от двух суток до примерно 11 недель) до получения комплексной смеси продуктов, имеющих агликоновый компонент формулы II. Эти продукты изомеризации могут также быть пригодными в качестве подсластителей в пищевых и питьевых продуктах.
В некоторых примерных воплощениях изомеры стевиол-гликозидов, включающие по меньшей мере одно соединение формулы II, могут применяться в качестве сильного подсластителя, не обладающего питательными свойствами. Подсластители являются съедобными материалами, пригодными для потребления и для применения в пищевых и питьевых продуктах. Как применяется здесь, термин «съедобные материалы» означает пищевой или питьевой продукт, или ингредиент пищевого или питьевого продукта для употребления человеком или животным. Как применяется здесь, «подсластитель, не обладающий питательными качествами» является таким, который не содержит значительного количества калорий в типично применяемых количествах, например, добавляет менее 5 калорий на порцию 8 унций напитка для достижения эквивалента сладости сахара 10 Брикс. Как применяется здесь, «сильный подсластитель» обозначает подсластитель, который слаще сахара (сахарозы) по меньшей мере в два раза, то есть подсластитель, требующий на основе массы не более половины от массы сахара, необходимого для достижения эквивалентной сладости.
Например, сильный подсластитель может требовать менее одной второй от массы сахара для достижения эквивалентной сладости в напитке, подслащенном до уровня 10 градусов по шкале Брикса с сахаром.
В некоторых примерных воплощениях подсластитель может включать по меньшей мере один компонент формулы II, и факультативно уплотнитель, наполнитель, такой как декстроза, мальтодекстрин, эритритол, тагатоза, или смесь эритритола и тагатозы, полидекстроза и/или агент, препятствующий слипанию.
В некоторых примерных воплощениях один или более изомеров стевиол-гликозидов, раскрытых здесь, могут быть представлены в питьевом продукте в качестве подсластителя, не обладающего питательными свойствами. В некоторых примерных воплощениях питьевой продукт включает подсластитель изо-ребаудиозид А (т.е. соединение формулы II, в котором R1 является 1-β-D-глюкопиранозилом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. В некоторых примерных воплощениях питьевой продукт включает по меньшей мере 0,005% по массе (например, по меньшей мере 0,01%, по меньшей мере 0,02%, по меньшей мере 0,03% по массе) изо-ребаудиозида А. В некоторых примерных воплощениях питьевой продукт включает подсластитель изо-ребаудиозид В (т.е. соединение формулы II, в котором R1 является водородом, a R2 является 2,3-бис(1-β-D-глюкопиранозил)-1-β-D-глюкопиранозилом. В некоторых примерных воплощениях питьевой продукт включает по меньшей мере 0,005% по массе (например, по меньшей мере 0,01%, по меньшей мере 0,02%, по меньшей мере 0,03% по массе) изо-ребаудиозида В.
Примерные питьевые продукты включают водосодержащую жидкость и соединение формулы II, и включают напитки, например, такие как готовые к употреблению жидкие рецептуры, концентраты напитков и тому подобное. Напитки включают, например, газированные и негазированные безалкогольные напитки, напитки, приготовляемые автоматами, замороженные готовые к употреблению напитки, замороженные газированные напитки, жидкие концентраты, порошковые концентраты, кофейные напитки, чайные напитки, молочные напитки, ароматизированные воды, обогащенные воды, фруктовые соки, ароматизированные напитки с фруктовым соком, напитки с фруктовым ароматом, спортивные напитки, соевые напитки, овощные напитки, напитки на основе зерна (например, солодовые напитки), ферментированные напитки (например, йогурт и кефир, алкогольные напитки и смеси любых из них. Примеры источников фруктовых соков включают цитрусовые фрукты, например апельсины, грейпфруты, лимоны и лаймы, ягоды, например клюкву, малину, чернику и землянику, яблоки, виноград, ананасы, сливы, груши, персики, вишню, манго и гранат. Питьевые продукты включают бутылки, консервные банки, продукты в картонной упаковке и сироп для газированной воды.
Термины «концентрат для напитков» и «сироп» применяются взаимозаменяемо на протяжении данного описания. По меньшей мере некоторые примерные воплощения предлагаемых концентратов для напитков готовят с исходным объемом воды, к которому добавляют дополнительные ингредиенты. Композиции напитков полной крепости могут быть получены из концентрата для напитков путем добавления дополнительных объемов воды в концентрат. Обычно, например, напитки полной крепости могут быть приготовлены из концентратов путем объединения примерно 1 части концентрата примерно с 3-7 частями воды. В некоторых примерных воплощениях напиток полной крепости готовят путем объединения 1 части концентрата с 5 частями воды. В некоторых примерных воплощениях дополнительная вода, применяемая для получения напитков полной крепости, является газированной водой. В некоторых других воплощениях напиток полной крепости готовят непосредственно без образования концентрата и последующего разбавления.
В некоторых примерных воплощениях один или более изомеров стевиол-гликозидов, раскрытых здесь, могут присутствовать в виде подсластителя, не обладающего питательными качествами, в пищевом продукте. Пищевые продукты включают по меньшей мере один пищевой компонент, т.е. любой съедобный материал, пригодный для потребления человеком или животным, полностью или частично перевариваемый. Не ограничивающие примеры пищевых компонентов включают белки, углеводы, жиры, витамины, минералы и т.д. Пищевые продукты, включающие соединение формулы II, раскрытое здесь, включают, например, толокно, злаки, хлебобулочные изделия (например, булочки, крекеры, пирожные, шоколадные пирожные с орехами, хлеб и т.д.), закусочные пищевые продукты (например, картофельные чипсы, кукурузные чипсы, попкорн, питательные батончики, рисовые оладьи и т.д.), и другие пищевые продукты на основе зерновых. Любые варианты, альтернативы, версии и т.д., обсуждаемые где-либо в этом описании, применяются воплощениям продуктов питания данного изобретения.
Необходимо понять, что пищевые или питьевые продукты в соответствии с данным раскрытием могут иметь любую из многочисленных различных специфических рецептур или структур. Рецептура пищевого или питьевого продукта в соответствии с данным раскрытием может варьировать до определенной степени, в зависимости от таких факторов, как предназначенный для продукта сектор рынка, необходимые питательные характеристики, вкусовой профиль и тому подобное. Например, к рецептуре конкретного воплощения продукта питания или напитка обычно добавляются дополнительные ингредиенты, включая любые рецептуры продуктов питания и напитков, описанные здесь. Могут быть добавлены дополнительные подсластители (т.е. многие и/или другие). Подкислители, ароматизаторы, красители, электролиты, минералы, неминеральные питательные добавки, фруктовые соки или другие фруктовые продукты, вкусовые вещества, вещества, корригирующие вкус и запах, и тому подобные, усилители вкуса, буферные агенты, загустители, эмульгаторы, съедобные частицы, противопенные агенты, консерванты, газирующие агенты, и их смеси обычно могут добавляться к таким рецептурам для изменения вкуса, вкусового впечатления, питательных характеристик, функционального назначения и т.д. пищевого или питьевого продукта. Примеры неминеральных питательных дополнительных ингредиентов известны специалистам в данной области техники и включают, например, антиоксиданты и витамины, включая витамины A, D, Е (токоферол), С (аскорбиновую кислоту), В (тиамин), B2 (рибофлавин), B6, B12, и К, ниацин, фолиевую кислоту, биотин и их комбинации. Факультативные неминеральные питательные добавки обычно присутствуют в количествах, в целом принятых в надлежащей производственной практике. Примерные количества составляют от примерно 1% до примерно 100% РСП (рекомендуемого суточного потребления), если такое РСП установлено. В некоторых примерных воплощениях неминеральный питательный дополнительный ингредиент(ы) присутствует в количестве от примерно 5% до примерно 20% РСП, если установлено. Подходящие дополнительные и альтернативные ингредиенты станут понятны специалисту в данной области техники при оценке преимуществ данного изобретения.
Некоторыми примерными воплощениями газированных напитков, раскрытых здесь, являются газированные напитки с ароматом колы, которые типично включают газированную воду, соединение формулы II, экстракт ореха колы и/или другой ароматизатор колы, карамельный краситель, и подкислитель (например, фосфорную кислоту), и факультативно другие ингредиенты, такие ка