Фармацевтические композиции, содержащие pн-зависимое лекарственное средство, модификатор pн и замедляющий агент
Иллюстрации
Показать всеФармацевтическая композиция представляет минитаблетку или пеллет, покрытые изолирующим слоем и энтеросолюбильным покрытием. Минитаблетка или пеллет содержат рН-зависимое лекарственное средство, предпочтительно дипиридамол, и модификатор рН, выбранный из группы, состоящей из лимонной кислоты, фумаровой кислоты, янтарной кислоты, адипиновой кислоты и малеиновой кислоты. Изолирующий слой включает полимер, пластификатор и агент, уменьшающий липкость, и отделяет минитаблетку или пеллет от энтеросолюбильного покрытия. Соотношение модификатора рН к рН-зависимому лекарственному средству составляет от 0,2:1 до 2:1. Полное высвобождение лекарственного средства из фармацевтической композиции происходит одновременно с высвобождением модификатора рН в течение времени от 1 до 4 часов. Фармацевтические композиции по изобретению характеризуются снижением вариабельности и повышением биодоступности в организме одного пациента или в организмах различных пациентов. 2 н. и 5 з.п. ф-лы, 3 ил., 7 пр.
Реферат
Настоящее изобретение относится к фармацевтическим композициям, содержащим рН-зависимое лекарственное средство, к применению и способам получения таких композиций.
Растворимость рН-зависимых лекарственных средств в существенной степени зависит от рН вдоль всего желудочно-кишечного тракта. Они растворимы при низких значениях рН в желудке здоровых пациентов натощак. Однако они могут осаждаться и/или растворяться неполностью в кишечнике при более высоком значении рН. Кроме того, после приема пищи, медикаментозного лечения и развития патофизиологического состояния рН в желудке повышается и, следовательно, снижается растворимость лекарственного средства. Неполная растворимость приводит к высокой вариабельности биодоступности рН-зависимого лекарственного средства в различных отделах организма одного пациента и в организмах различных пациентов.
Включение модификаторов рН, например органических кислот, в пероральную лекарственную форму модулирует рН микроокружения и тем самым повышает растворимость и растворение лекарственного средства. Кроме того, достигается независимое от рН высвобождение лекарственного средства. Однако, обычно при более высоких рН среды модификаторы рН характеризуются более высокой растворимостью по сравнению с лекарственным соединением, быстрее диффундируют и, следовательно, быстрее отделяются от рН-зависимого лекарственного соединения в составе твердой лекарственной формы. Для замедления быстрой диффузии модификаторов рН применяют полимеры, которые позволяют поддерживать необходимое значение рН внутри твердой лекарственной формы. Однако применение полимеров обычно приводит к модифицированному высвобождению композиции, например высвобождению лекарственного средства в течение длительного периода времени, например в течение 10 ч или более. Полная абсорбция лекарственного соединения из такой композиции с модифицированным высвобождением может в значительной степени зависеть как от физиологических условий, так и от самого лекарственного соединения. Например, лекарственные соединения, которые абсорбируются только в определенных отделах организма, например в верхнем отделе кишечного тракта, например в тонком кишечнике, характеризуются высокой вариабельностью и меньшей биодоступностью в организме одного пациента и в организмах различных пациентов.
Таким образом, существует необходимость в фармацевтических композициях, включающих рН-зависимое лекарственное средство со сниженной вариабельностью компонентов и повышенной биодоступностью в организме одного пациента и в организмах различных пациентов. Неожиданно было установлено, что разработанные авторами улучшенные фармацевтические композиции содержат рН-зависимое лекарственное средство и модификатор рН, который присутствует в составе композиции, например в течение всего периода растворения, и который, например, высвобождается одновременно с лекарственным соединием.
В первом объекте настоящего изобретения предлагается фармацевтическая композиция, включающая рН-зависимое лекарственное соединение, модификатор рН и замедляющий агент, например полимер, например водорастворимый полимер, и лекарственное средство высвобождается из такой фармацевтической композиции полностью через 4 ч, т.е. максимальный период растворения, например в течение периода растворения приблизительно от 1 до 4 ч, например в течение от 1 до 2 ч, или от 1 до 3 ч, или приблизительно от 2 до 4 ч, например от 2 до 3 ч, например, при контактировании с желудочно-кишечным соком.
В другом объекте изобретения предлагается нанесение энтеросолюбильного покрытия, например, для предотвращения любой преждевременной диффузии лекарственного средства и кислоты в желудок и/или для подавления влияния индивидуальных различий рН в желудке на растворение лекарственного средства и кислоты, например, для обеспечения равномерной растворимости лекарственного средства в верхнем отделе кишечного тракта, например в тонком кишечнике.
В еще одном объекте настоящего изобретения предлагается включение изолирующего слоя между кислотным ядром и энтеросолюбильным покрытием, например, для обеспечения растворения энтеросолюбильного покрытия при рН в кишечнике приблизительно ≥5,5.
В другом объекте настоящего изобретения предлагается фармацевтическая композиция в форме многокомпонентной системы, например в форме минитаблеток или пеллетов. Преимущества таких многокомпонентных систем по сравнению с монолитной системой заключаются, например, в улучшенной воспроизводимости прохождения через желудочно-кишечный тракт и/или в более высокой степени дисперсности в желудочно-кишечном тракте, что приводит к снижению вариабельности и улучшению биодоступности в организме одного пациента или в организмах различных пациентов.
Эти и другие признаки, преимущества и объекты настоящего изобретения представляются очевидными для специалистов в данной области техники при ознакомлении с описанием, пунктами формулы изобретения и прилагаемыми фигурами.
Краткое описание фигур
Прилагаемые фигуры предназначены для иллюстрации типичных вариантов осуществления настоящего изобретения и являются частью настоящего описания.
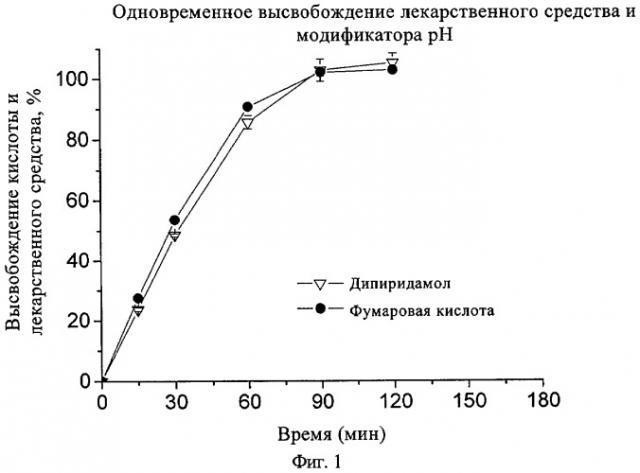
На фиг.1 представлена степень одновременного высвобождения лекарственного средства и модификатора рН.
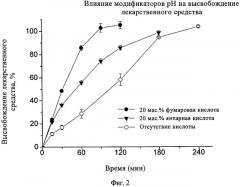
На фиг.2 показано влияние модификаторов рН на высвобождение лекарственного средства.
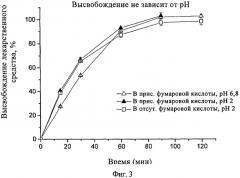
На фиг.3 показано, что высвобождение лекарственного средства не зависит от величины рН в среде растворения.
Композиции по настоящему изобретению обеспечивают модифицированное высвобождение рН-зависимого лекарственного соединения в течение короткого периода времени, прежде всего в верхнем отделе кишечного тракта, например в тонком кишечнике, и характеризуются сниженной вариабельностью и улучшенной биодоступностью в организме одного пациента и в организмах различных пациентов.
Подробное описание вариантов осуществления изобретения
Использованный в данном контексте термин «лекарственное средство» означает любое соединение, вещество, лекарственное средство, препарат или активный ингредиент, оказывающий терапевтическое или фармакологическое действие, пригодный для введения млекопитающему, например человеку. Такие лекарственные средства следует вводить в «терапевтически эффективном количестве».
Использованный в данном контексте термин «терапевтически эффективное количество» означает количество или концентрацию, которые проявляют эффективность при снижении, устранении, лечении и профилактике или контроле симптомов заболевания или его признаков у млекопитающих. Термин «контроль» означает все способы, с помощью которых можно замедлять, прерывать, приостанавливать или останавливать развитие заболеваний или его состояний у млекопитающих. Однако «контроль» необязательно означает полное устранение всех симптомов заболевания и его состояния и включает также профилактическое лечение.
«Терапевтически эффективное количество», известный в данной области техники термин, означает количество, которое изменяется в зависимости от используемого терапевтического соединения и показания, предназначенного для лечения.
Лекарственные средства и его соли, которые прежде всего пригодны для применения по настоящему изобретению, являются рН-зависимыми, прежде всего слабоосновными лекарственными средствами, например любыми лекарственными средствами, различие в растворимости которых при рН в диапазоне 1-6 составляет >100.
Лекарственное средство может присутствовать в количестве приблизительно вплоть до 60 мас.% в рассчете на массу композиции, от приблизительно 1 мас.% до приблизительно 60 мас.% в рассчете на массу композиции. Однако предполагается, что специфический уровень лекарственного средства выбирают в зависимости от известных в фармацевтике факторов, включая способ введения, размер и состояние субъекта.
Пригодные модификаторы рН по настоящему изобретению включают кислоты, например неорганические кислоты, например водорастворимые неорганические кислоты, твердые при температуре окружающей среды, например, сульфаминовую кислоту.
Пригодные органические кислоты содержат одну или более кислотных групп, например карбоксильные и сульфогруппы, прежде всего кислоты, которые являются твердыми при температуре окружающей среды.
Пригодные водорастворимые органические кислоты выбирают из группы, включающей моно, ди- или полиосновные карбоновые кислоты или моно, ди- или трисульфоновые кислоты, например такие кислоты, которые являются твердыми при температуре окружающей среды. Пригодные твердые водорастворимые органические кислоты включают алифатические моно- или поликарбоновые кислоты, например, содержащие от 2 до 8 атомов углерода, прежде всего от 2 до 6 атомов углерода, например, все ди- или трикарбоновые кислоты, содержащие от 4 до 6, например, 4 атома углерода, например, насыщенные или ненасыщенные. Примеры пригодных твердых водорастворимых алифатических монокарбоновых кислот включают сорбиновую кислоту (2,4-гександиеновую кислоту). Примеры пригодных твердых водорастворимых алифатических дикарбоновых кислот включают адипиновую, малоновую, янтарную, глутаровую, малеиновую или фумаровую кислоту. Алифатическая карбоновая кислота необязательно содержит один или более заместителей, например 1, 2 или 3 группы, которые могут быть одинаковыми или различными и которые выбирают из группы, включающей карбокси, амино и гидрокси. Пригодные замещенные твердые водорастворимые алифатические карбоновые кислоты включают, например, гидроксизамещенные алифатические монокарбоновые кислоты, такие как глюконовая кислота, твердые формы молочной, гликолевой или аскорбиновой кислоты; гидроксизамещенные алифатические дикарбоновые кислоты, такие как яблочная, винная, тартроновая (гидроксималоновая) или слизевая (галактаровая) кислота; дигидроксизамещенные алифатические трикарбоновые кислоты, например лимонная кислота, или аминокислоты, содержащие в боковой цепи кислотные группы, такие как глутаминовая кислота или аспарагиновая кислота.
Пригодные ароматические карбоновые кислоты включают водорастворимые арильные карбоновые кислоты, содержащие до 14 атомов углерода. Пригодные арильные карбоновые кислоты включают арильную группу, например фенильную или нафтильную группу, которые содержат одну или более карбоксильных групп, например 1, 2 или 3 карбоксильных групп. Арильная группа необязательно замещена одной или более группами, например 1, 2 или 3 группами, которые являются одинаковыми или различными, выбранными из гидрокси, С1-С4алкокси, например, метокси, и сульфонил. Пригодные арильные карбоксильные кислоты включают бензойную, фталевую, изофталевую, терефталевую или тримеллитовую кислоту (1,2,4-бензолтрикарбоновую кислоту).
Модификатор рН выбирают предпочтительно из группы, включающей лимонную кислоту, фумаровую кислоту, янтарную кислоту, адипиновую кислоту и малеиновую кислоту. Предпочтительно применяют фумаровую кислоту.
В качестве модификаторов рН предпочтительно используют модификаторы по настоящему изобретению, которые изменяют рН микроокружения в более кислотную область, таким образом повышается степень высвобождения лекарственного средства из лекарственной формы при значении рН, при котором лекарственное средство является труднорастворимым, например нерастворимым.
Содержание модификатора рН составляет от приблизительно 1 мас.% до приблизительно 60 мас.% в рассчете на массу композиции, например от приблизительно 10 мас.% до приблизительно 40 мас.% в рассчете на массу композиции. Соотношение модификатора рН к лекарственному соединению в составе композиции по изобретению составляет от приблизительно 0,2:1 до приблизительно 2:1, например 1:1.
В качестве замедляющего агента используют полимеры, например водорастворимые полимеры, например производные целлюлозы, например, вязкость которых составляет более приблизительно 100 сП, например от приблизительно 100 до приблизительно 100000 сП. Предпочтительно используют водорастворимые полимеры.
Пригодные полимеры включают, без ограничения перечисленным, производные целлюлозы, например метилцеллюлозу, гидроксипропилметилцеллюлозу, например гидроксипропилметилцеллюлозу k100LV, K4M или гидроксипропилметилцеллюлозу K15M, гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, этилцеллюлозу, например этилцеллюлозу 100, ацетат целлюлозы, например ацетат целлюлозы СА-398-10 NF, ацетат-фталат целлюлозы, ацетат-пропионат целлюлозы, ацетат-бутират целлюлозы, бутират целлюлозы, нитрат целлюлозы, фталат гидроксипропилметилцеллюлозы, ацетат-сукцинат гидроксипропилметилцеллюлозы, акриловые производные, например полиакрилаты, например сшитые полиакрилаты, сополимеры метакриловой кислоты, виниловые полимеры, например поливинилпирролидоны, поливинилацетаты или поливинилацетат-фталаты и их смеси, которые выпускаются под торговым названием Kollidon SR®, полиэтиленгликоли, полиангидриды, полисахариды, например ксантаны, например ксантановую смолу, галактоманнан, пектин и альгинаты.
Предпочтительные полимеры включают гидроксипропилметилцеллюлозу, например Methocel K100LV, Methocel K4M, Methocel K100M.
Содержание полимеров составляет от приблизительно 10 мас.% до приблизительно 60 мас.% в рассчете на массу композиции, например от приблизительно 30 мас.% до приблизительно 60 мас.% в рассчете на массу композиции.
В некоторых вариантах осуществления настоящего изобретения фармацевтическая композиция включает дополнительные эксципиенты, которые обычно включают в состав фармацевтических композиций, примеры таких эксципиентов включают, без ограничения перечисленным, глиданты, замасливатели, антиоксиданты, антимикробные агенты, ингибиторы ферментов, стабилизаторы, консерванты, ароматизаторы, подсластители и др. компоненты, например, как описано в книге Rowe и др. «Handbook of Pharmaceutical Excipients», 4-e издание, Pharmaceutical Press (2003), которая включена в данное описание в качестве ссылки.
Содержание указанных дополнительных эксципиентов составляет от приблизительно 0,05 до 1 мас.% в рассчете на общую массу фармацевтической композиции, например от приблизительно 0,5 до приблизительно 2 мас.% в рассчете на общую массу композиции. Содержание антиоксидантов, антимикробных агентов, ингибиторов ферментов, стабилизаторов или консервантов обычно составляет от приблизительно 0,05 до 1 мас.% в рассчете на общую массу фармацевтической композиции. Содержание подсластителей или ароматизаторов обычно составляет приблизительно вплоть до 2,5 или 5 мас.% в рассчете на общую массу фармацевтической композиции.
Пригодные замасливатели включают, без ограничения перечисленным, стеарат магния, тальк, гидрированное касторовое масло, глицеринбегенат, моностеарат глицерина, полиэтиленгликоль, полимеры этиленоксида, лаурилсульфат натрия, лаурилсульфат магния, олеат натрия, стеарилфумарат натрия, DL-лейцин, коллоидный гидроксид кремния и т.п. Композиции по изобретению включают от приблизительно 0 до 3 мас.%, например от приблизительно 0,5 до 3 мас.%, например 1 мас.% замасливателя в рассчете на массу композиции.
Пригодные наполнители включают, без ограничения перечисленным, лактозу, например, в безводной или гидратированной форме, сахар, крахмалы, например кукурузный, пшеничный, маисовый или картофельный крахмал, модифицированные крахмалы, гидролизаты крахмала или предварительно желатинизированный крахмал, маннит, сорбит, трегалозу, мальтозу, безводную глюкозу, неорганические соли, например, карбонат кальция, карбонат магния, двухосновный фосфат кальция, трехосновный фосфат кальция или сульфат кальция, микрокристаллическую целлюлозу, производные целлюлозы и т.п. Композиции по изобретению включают от приблизительно 0 до 65 мас.%, например от приблизительно 3 до 65 мас.% наполнителя в рассчете на массу композиции.
Пригодные глиданты включают, без ограничения перечисленным, аэросил 200 или тальк и т.п. Композиции по изобретению включают от приблизительно 0 до 2 мас.% глиданта в рассчете на массу композиции.
Пригодные связующие включают, без ограничения перечисленным, поливинилпирролидон (ПВП), например ПВП K30 или ПВП K12, известные под торговым названием Povidone® фирмы BASF, или гидроксипропилметилцеллюлозу (ГПМЦ), например ГПМЦ с низкой вязкостью, например менее 100 сП, которую определяют при 20°С в виде 2 мас.% водного раствора, например, менее 50 сП, предпочтительно менее 20 сП, например 3 сП, известные под торговым названием Pharmacoat® 603 фирмы Shin-Etsu. Композиции по изобретению включают от приблизительно 0 до 5 мас.%, например от приблизительно 0,5 до 5 мас.% связующего в рассчете на массу композиции.
Пригодные антиоксиданты включают, без ограничения перечисленным, аскорбиновую кислоту и ее производные, токоферол и его производные, бутилгидроксианизол и бутилгидрокситолуол, предпочтительно витамин Е в качестве α-токоферола.
В другом варианте настоящего изобретения предлагается способ получения фармацевтической композиции, например, в форме минитаблеток, как описано в данном контексте, который заключается в том, что смешивают активные ингредиенты, органическую кислоту, полимер и любые дополнительные эксципиенты, которые используют для получения таблеток, и проводят влажную грануляцию смеси с водным или органическим растворителем. Сухие гранулы, например, в форме минитаблеток просеивают через сито с ячейками размером 400 мкм. Затем добавляют внешнюю фазу, включающую диоксид кремния, например, под торговым названием аэросил, добавляют стеарат магния и тщательно перемешивают. Смесь прессуют в минитаблетки диаметром, например, от 1,5 до 4 мм, например от 1,7 до 2 мм. Полученными минитаблетками заполняют капсулы, например твердые желатиновые капсулы или крахмальные капсулы, или минитаблетками заполняют пакетики.
В еще одном варианте настоящего изобретения предлагается способ получения фармацевтической композиции, например, в форме пеллетов, как описано в данном контексте, который заключается в том, что сухую смесь получают при смешивании активного ингредиента, органической кислоты, полимера и, например, микрокристаллической целлюлозы в смесителе планетарного типа. Для получения влажной массы добавляют очищенную воду, затем массу пропускают через экструдер и сито необходимого размера. Экструдат округляют в сферонизаторе, тщательно высушивают и просеивают для отделения необходимого размера и получают, например, пеллеты с модифицированным высвобождением в короткий период времени.
В другом варианте изобретения на минитаблетки или пеллеты наносят энтеросолюбильное покрытие.
Использованный в данном контексте термин «энтеросолюбильное покрытие» означает покрытие, которое защищает лекарственную форму от растворения в желудке, например, при рН от 1-2 до 5.
Энтеросолюбильные покрытия по настоящему изобретению включают следующие компоненты (% содержания определяли в рассчете на общую массу минитаблеток или пеллетов с покрытием):
- 2-40% полимеров для энтеросолюбильного покрытия, например фталат гидроксипропилметилцеллюлозы, например продукт под торговым названием HP50 или HP55 фирмы Shin Etsu, ацетат-сукцинат гидроксипропилметилцеллюлозы, например продукт под торговым названием Aqoat H, М или L фирмы Shin Etsu, сополимер метилакриловой кислоты и этилакриловой кислоты (сополимер метакриловой кислоты, USP), например продукт под торговым названием Eudragit L, S, L100-55 или L30D фирмы Rohm Pharma, Acryl-Eze фирмы Colorcon или Kollicoat МАЕ 30 DP фирмы BASF, ацетат-фталат целлюлозы, например продукт под торговым названием Aquacoat CPD фирмы FMC Biopolymer или Polymer фирмы Eastman Kodak, поливинилацетат-фталат, например продукт под торговым названием Sureteric фирмы Colorcon,
- 0-15% полимеров для промежуточного слоя (изолирующий слой между ядром таблетки и энтеросолюбильным покрытием): гидроксипропилметилцеллюлоза, продукт под торговым названием Pharmacoat 603 или 606, этилцеллюлоза, например продукт под торговым названием Aquacoat ECD фирмы FMC Biopolymer или Surelease фирмы Colorcon, и их смеси при соотношении этилцеллюлоза/НРМС от 1:1 до 1:10, поливиниловый спирт, например продукт под торговым названием Opadry II HP тип 85F фирмы Colorcon),
- 0-10% пластификаторов, например триацетин, триэтилцитрат, ПЭГ 4000, ПЭГ 6000, ПЭГ 8000, диэтилфталат, диэтилсебакат, ацетилтриэтилцитрат и т.п.,
- 0-15% агентов, уменьшающих липкость, например диоксид кремния, например продукт под торговым названием Aerosil 200, Syloid 244 FP, тальк, моностеарат глицерина и т.п.,
- органические растворители или их смеси в отсутствие или в присутствии воды, например этанол, ацетон, изопропанол или вода, необходимые для растворения или диспергирования полимеров, входящих в состав покрытия, и эксципиентов, используемых при получении раствора покрытия,
- 0-0,5% гидроксида натрия для повторного диспергирования полимеров при получении водных суспензий энтеросолюбильного покрытия, например, для диспергирования продукта Eudragit L100-55.
Следующий объект настоящего изобретения относится к способу нанесения покрытия на фармацевтическую композицию, определенную в данном контексте, который включает:
в случае использования энтеросолюбильного покрытия в виде органического раствора:
(1) растворение полимера и пластификатора для энтеросолюбильного покрытия в органическом растворителе и
(2) диспергирование агентов, уменьшающих липкость;
в случае использования энтеросолюбильного покрытия в виде водных дисперсий:
1) растворение или тонкое диспергирование пластификатора в воде,
(2) диспергирование агентов, уменьшающих липкость, и, наконец,
(3) добавление полученной суспензии (например, Aqoat или Eudragit L100-55), или готовой полимерной водной дисперсии (например, Eudragit L 30D, Acryl-Aze, Kollicoat МАЕ 30D).
В изолирующий слой необязательно можно включать, например, водный раствор пригодного полимера, например гидроксипропилметилцеллюлозу (НРМС, 4-8%), пластификатор (0-3%) и агент, уменьшающий липкость (0-3%). Для улучшения эффективности изолирующего слоя в его состав добавляют водную дисперсию этилцеллюлозы, например Aquacoat ECD или Surelease в соотношении от 1:10 до 1:1 (этилцеллюлоза/НРМС). В зависимости от размера минитаблеток/пеллетов общее количество изолирующего слоя составляет 3-15% (более предпочтительно 5-10%). В качестве эффективного изолирующего слоя используют поливиниловый спирт (Opadry II HP) в количестве 2-10% в рассчете на массу ядра.
В другом объекте изолирующий слой НРМС наносят в форме органической суспензии в смеси этанол/ацетон 1:1 (приблизительно 6-10% полимера на один растворитель) в отсутствие других добавок.
Энтеросолюбильное покрытие и/или изолирующий слой наносят с использованием устройства для нанесения покрытия лоткового типа и устройства с псевдоожиженным слоем и с элементом Вурстера или без него. При этом получают слой покрытия, масса которого составляет от 2 до 45 мас.% в рассчете на массу лекарственной формы, например от приблизительно 10 до 25 мас.%, например, для крупных таблеток, например, диаметром от приблизительно 5 до 15 мм, и от приблизительно 20-40%, например, для мелких таблеток, например минитаблеток, например, диаметром от приблизительно 1,5 до 4 мм, например от приблизительно 1,7 до 2 мм. Изолирующий слой включает от приблизительно 2 до 15 мас.% в рассчете на массу лекарственной формы, например от приблизительно 4 до 10 мас.%, например, для крупных таблеток, и от приблизительно 8 до 15 мас.%, например, для мелких таблеток, например минитаблеток или пеллетов. Слой энтеросолюбильного покрытия включает от приблизительно 5 до 40 мас.% в рассчете на массу лекарственной формы, например от приблизительно 8 до 20 мас.%, например, для крупных таблеток, и от приблизительно 15 до 30 мас.%, например, для мелких таблеток, например минитаблеток или пеллетов. Масса слоя зависит от от размера минитаблеток/пеллетов, чтобы обеспечить устойчивость в среде желудка в течение 1-3 ч, например в искусственном желудочном соке или в растворе 0,1 н. НСl (согласно инструкциям Ph.Eur. или USP). Кроме того, следует свести к минимуму набухание ядра таблетки во время испытаний на устойчивость в среде желудка.
В другом объекте настоящего изобретения предлагается фармацевтическая композиция, определенная в данном контексте, обеспечивающая полное высвобождение лекарственного средства, например полное разрушение лекарственной формы в течение 4 ч, например, при контактировании со средой желудочно-кишечного тракта, например в желудке в случае лекарственных форм с неэнтеросолюбильным покрытием или в верхнем отделе кишечного тракта, например в тонкой кишке в случае лекарственных форм с энтеросолюбильным покрытием. Полное высвобождение лекарственного средства обеспечивается, например, в течение приблизительно от 1 до 4 ч, например в течение от 1 до 3 ч или от 1 до 2 ч, или в течение приблизительно от 2 до 4 ч, например от 2 до 3 ч.
Применимость всех фармацевтических композиций по настоящему изобретению оценивают в условиях стандартных клинических испытаний, например, при назначении стандартных доз, обеспечивающих терапевтически эффективный уровень лекарственного средства в крови, например, при введении доз в интервале 2,5-1000 мг лекарственного средства в сут млекопитающему массой 75 кг, например, взрослым пациентам и с использованием стандартных моделей животных. Повышенную биодоступность лекарственного средства, которую обеспечивает композиция, можно наблюдать при испытании на стандартных моделях животных и в условиях клинических испытаний.
Следующие примеры представлены для иллюстрации и не ограничивают объем изобретения, описанный в данном контексте. В примерах описано применение настоящего изобретения на практике. Количество ингредиентов, представленных в мас.% в рассчете на массу фармацевтической композиции, использованных в каждом примере, указано в таблицах и сопровождается соответствующими описаниями.
Примеры
1. Минитаблетки
Лекарственное средство, органическая кислота, полимер и любые дополнительные эксципиенты для таблетирования гранулировали в смеси с водой или органическим растворителем в ступке. После высушивания при 40°С сухие гранулы для получения минитаблеток просеивали через сито с ячейками размером 400 мкм. Затем в смесь добавляли внешнюю фазу, включающую диоксид кремния и стеарат магния, и интенсивно перемешивали. Порошок прессовали и получали минитаблетки диаметром от 1,7 до 2 мм.
| Пример 1 | (%) | мг/капсула |
| Methacel K100LV | 30,00 | 75,00 |
| Дипиридамол | 10,00 | 25,00 |
| Фумаровая кислота | 20,00 | 50,00 |
| Лактоза 200 меш | 34,00 | 85,00 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
| Пример 2 | (%) | мг/капсула |
| Methacel K100LV | 30,00 | 75,00 |
| Дипиридамол | 10,00 | 25,00 |
| Фумаровая кислота | 40,00 | 100,00 |
| Лактоза 200 меш | 14,00 | 35,00 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
| Пример 3 | (%) | мг/капсула |
| Methacel K100LV | 30,00 | 75,00 |
| Лактоза 200 меш | 54,00 | 135,00 |
| Дипиридамол | 10,00 | 25,00 |
| Фумаровая кислота | 0,00 | 0,00 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
| Пример 4 | (%) | мг/капсула |
| Methacel K100LV | 30,00 | 75,00 |
| Дипиридамол | 10,00 | 25,00 |
| Янтарная кислота | 20,00 | 50,00 |
| Лактоза 200 меш | 34,00 | 85,00 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
| Пример 5 | (%) | мг/капсулу |
| Methacel K100LV | 30,00 | 75,00 |
| Дипиридамол | 10,00 | 25,00 |
| Янтарная кислота | 40,00 | 100,00 |
| Лактоза 200 меш | 14,00 | 35,00 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
| Пример 6 | (%) | мг/капсулу |
| Methacel K4M | 30,00 | 75,00 |
| Дипиридамол | 10,00 | 25,00 |
| Фумаровая кислота | 20,00 | 50,00 |
| Лактоза 200 меш | 34,00 | 84,99 |
| НРМС 3 сП | 2,67 | 6,68 |
| Стеарат магния | 1,33 | 3,33 |
| Аэросил 200 | 2,00 | 5,00 |
| 100,00 | 250,00 |
2. Пеллеты:
Сухую смесь получали при смешивании активного ингредиента, органической кислоты, полимера и, например, микрокристаллической целлюлозы в смесителе планетарного типа. Затем добавляли очищенную воду и получали влажную массу, которую пропускали через экструдер с ситом необходимого размера. Экструдат округляли в сферометре, тщательно высушивали и просеивали через соответствующее сито. При этом получали пеллеты с модифицированным высвобождением в течение короткого периода времени.
| Пример 7 | (%) | мг/капсулу |
| Methacel K100V | 30 | 75 |
| Дипиридамол | 10 | 25 |
| Фумаровая кислота | 20 | 50 |
| Моногидрат лактозы 200 меш | 40 | 100 |
3. Нанесение энтеросолюбильного покрытия
Примеры 1-4
Получение изолирующего слоя
Изолирующий слой получали с использованием водного раствора полимера, пластификатора и агента, уменьшающего липкость. Необязательно добавляли водную дисперсию этилцеллюлозы (Aquacoat ECD или Surelease). В другом варианте получали органическую суспензию полимера в воде или смеси этанол/ацетон 1:1.
Получение энтеросолюбильного покрытия
В случае органического раствора для энтеросолюбильного покрытия, после растворения полимера и пластификатора для энтеросолюбильного покрытия в органических растворителях, диспергировали агенты, уменьшающие липкость. В случае водной дисперсии для покрытия растворяли пластификатор или получали его тонкую дисперсию в воде, затем диспергировали агент, уменьшающий липкость, и добавляли предварительно полученную суспензию (т.е. Aqoat или Eudragit L100-55) или добавляли коммерческий продукт, водную дисперсию полимера (Eudragit L30D, Acryl-Aze, Kollicoat МАЕ 30D).
Способ нанесения покрытия.
Покрытие наносили с использованием устройства для нанесения покрытия лоткового типа и устройства с псевдоожиженным слоем и с элементом Вурстера или без него до образования слоя, составляющего 2-45% (приблизительно 10-25% для крупных таблеток и 20-40% для мелких таблеток/минитаблеток). Изолирующий слой составляет 2-15% (4-10% для крупных таблеток, 8-15 мас.% для минитаблеток/пеллетов), а слой энтеросолюбильного покрытия составляет 5-40% (крупные таблетки: 8-20%, минитаблетки/пеллеты: 15-30%). Размер слоя зависит от размера минитаблетки/пеллета, чтобы обеспечить устойчивость в среде желудка в течение 1-3 ч, например в искусственном желудочном соке или в растворе 0,1 н. НСl (согласно инструкциям Ph.Eur. или USP). Кроме того, следует свести к минимуму набухание ядра таблетки во время испытаний на устойчивость в среде желудка.
| Пример 1 | Массовые части | % | мг/250 мг ядра | мг/8 мг ядра |
| Изолирующий слой | ||||
| НРМС 3 сП | 5,0 | 25,0 | 12,50 | 0,80 |
| Триэтилцитрат | 0,5 | 2,5 | 1,25 | 0,08 |
| Тальк | 0,5 | 2,5 | 1,25 | 0,08 |
| Вода q.s. | ||||
| Энтеросолюбильное покрытие | ||||
| Eudragit L30D (сух.) | 10,0 | 50,0 | 25,00 | 1,60 |
| ПЭГ 6000 | 2,0 | 10,0 | 5,00 | 0,32 |
| Syloid 244 FP | 2,0 | 10,0 | 5,00 | 0,32 |
| Вода q.s. | ||||
| Общая масса (сух.) | 20,0 | 100,0 | 50,00 | 3,20 |
| Пример 2 | Массовые части | % | мг/250 мг ядра | мг/8 мг ядра |
| Изолирующий слой | ||||
| НРМС 3 сП | 6,0 | 26,67 | 15,0 | 0,960 |
| Aquacoat ECD (сух.) | 2,0 | 8,89 | 5,0 | 0,320 |
| Триэтилцитрат | 0,6 | 2,67 | 1,5 | 0,096 |
| Моностеарат глицерина | 0,4 | 1,77 | 1,0 | 0,064 |
| Вода q.s. | ||||
| Энтеросолюбильное покрытие | ||||
| НРМС AS (Aqoat) MF | 10,0 | 44,44 | 25,00 | 1,600 |
| Триэтилцитрат | 2,5 | 11,11 | 6,25 | 0,400 |
| Тальк | 1,0 | 4,44 | 2,5 | 0,160 |
| Вода q.s. | ||||
| Общая масса (сух.) | 22,5 | 100,0 | 56,25 | 3,600 |
| Пример 3 | Массовые части | % | мг/250 мг ядра | мг/8 мг ядра |
| Изолирующий слой | ||||
| НРМС 3 сП | 5,0 | 32,5 | 12,5 | 0,80 |
| Этанол/ацетон 1:1 q.s. | ||||
| Энтеросолюбильное покрытие | ||||
| HP 50 | 8,0 | 51,9 | 20,0 | 1,28 |
| Триацетин | 0,8 | 5,2 | 2,0 | 0,13 |
| Аэросил 200 | 1,6 | 10,4 | 4,0 | 0,26 |
| Этанол/ацетон 1:1: q.s. | ||||
| Общая масса (сух.) | 15,4 | 100,0 | 38,5 | 2,47 |
| Пример 3в | Массовые части | % | мг/250 мг основы | мг/250 мг основы |
| Энтеросолюбильное покрытие | ||||
| HP 50 | 10,0 | 71,43 | 25,0 | 1,60 |
| Диэтилсебакат | 1 | 7,14 | 2,5 | 0,16 |
| Тальк | 3 | 21,43 | 7,5 | 0,48 |
| Этанол/ацетон 1:1: q.s. | ||||
| Общая масса (сух.) | 14 | 100,0 | 34,0 | 2,24 |
| Пример 4 | Массовые части | % | мг/250 мг ядра | мг/8 мг ядра |
| Изолирующий слой | ||||
| Opadry II HP | 4,0 | 21,46 | 10,00 | 0,640 |
| Вода q.s. | ||||
| Энтеросолюбильное покрытие | ||||
| Eudragit L100-55 | 10,0 | 53,65 | 25,00 | 1,600 |
| Гидроксид натрия | 0,14 | 0,75 | 0,35 | 0,022 |
| Триэтилцитрат | 2,50 | 13,41 | 6,25 | 0,400 |
| Syloid 244 FP | 2,00 | 10,73 | 5,00 | 0,320 |
| Вода q.s. | ||||
| Общая масса (сух.) | 18,64 | 100,0 | 46,60 | 2,982 |
| Пример 4в | Массовые части | % | мг/250 мг ядра | мг/8 мг ядра |
| Энтеросолюбильное покрытие | ||||
| Eudragit L100-55 | 10,0 | 76,92 | 25,00 | 1,60 |
| Триэтилцитрат | 1 | 7,69 | 2,5 | 0,16 |
| Syloid 244 FP | 2 | 15,38 | 5,0 | 0,32 |
| Изопропанол/вода 97:3 q.s. | ||||
| Общая масса (сух.) | 13 | 100,0 | 32,5 | 2,08 |
4. Оценка растворимости in vitro
Растворимость определяли на приборе USP 1 (100 об/мин, 37°С, 500 мл среды для растворения). Таблетки выдерживали в среде с постоянным рН (фосфатный буферный раствор, рН 6,8) в течение 6 ч. В буферный раствор добавляли 0,1% ДСН для увеличения текучести раствора. Через определенные интервалы времени из среды отбирали образцы и фильтровали их через мембранные фильтры с размером пор 0,45 мкм. Дипиридамол определяли спектрофотометрически при длине волны 410 нм (спектрофотометр УФ/виз. фирмы Perkin Elmer), количество высвобождающейся кислоты определяли методом ЖХВР. Для поддержания постоянного объема среды для растворения добавляли соответствующее количество свежего буферного раствора. Все эксперименты проводили в тройном повторе.
Анализ ЖХВР
Хроматографию проводили в системе Agilent HPLC, HP1100, с использованием программного обеспечения Chromeleon для обработки полученных данных. В течение первых 8 мин колонку промывали раствором следующего состава: 0,1 М NH4H2PO4 буферный раствор, рН которого доводили до 2,7 фосфорной кислотой. Для полного удаления остаточного количества лекарственного агента колонку промывали в градиенте (ацетонитрил/буферный раствор NН4Н2РO4, рН 2,7). Разделение проводили на колонке Inertsil C8 - 3,5 мкм, 4,6×150 мм (Erchatech AG, Швейцария). Скорость потока 1 мл/мин, объем образца 5 мкл (FA) и 10 мкл (СА и SA), время цикл