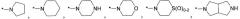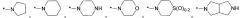Ингибиторы бета-лактамаз
Иллюстрации
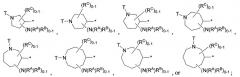
Показать всеВ настоящей заявке описаны замещенные бициклические бета-лактамы формулы I:
которые являются ингибиторами β-лактамаз класса А и класса С, где X, R1 и R2 определены в тексте заявки, а также способ их получения. Соединения формулы I и их фармацевтически приемлемые соли применяют для получения фармацевтической композиции и в производстве лекарственного средства. Заявленные соединения применяются для лечения бактериальных инфекций необязательно в комбинации с β-лактамовым антибиотиком. В частности соединения могут быть использованы с такими β-лактамовыми антибиотиками, как, например, имипенемом, пиперациллином, или цефтазидимом, против микроорганизмов, устойчивых к действию β-лактамовых антибиотиков вследствие присутствия β-лактамаз. 6 н. и 22 з.п. ф-лы, 118 пр., 3 табл., 3 сх., 2 ил.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет предварительной заявки на патент США № 61/011533 (поданной 18 января 2008 г.), содержание которой включено в настоящее описание путем ссылки во всей ее полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к новым ингибиторам бета-лактамаз и их применению против устойчивости бактерий к действию антибиотиков. Более конкретно, изобретение относится к композициям и способам для преодоления устойчивости бактерий к действию антибиотиков.
УРОВЕНЬ ТЕХНИКИ
Устойчивость бактерий к действию антибиотиков стала одной из наиболее серьезных проблем современного здравоохранения. В публикации Cohen, Science 1992, 257: 1051-1055 сообщается, что инфекции, вызванные устойчивыми к действию медицинских препаратов бактериями, часто приводят к более длительному пребыванию в больнице, более высокой смертности и повышенным затратам на лечение. В публикации Neu, Science 1992, 257: 1064-1073 сообщается, что необходимость в новых антибиотиках будет постоянно возрастать в силу того, что бактерии обладают удивительной способностью вырабатывать устойчивость к действию новых лекарственных средств, быстро превращая их в неэффективные. В публикации Anderson, Nature America 1999, 5; 147-149 отмечается, что процесс распространения явления устойчивости к действию антибиотиков носит пандемический характер, и утверждается, что решение растущей серьезной проблемы здравоохранения потребует междисциплинарного подхода.
Данный кризис вызвал проведение различных исследований для выяснения механизмов, лежащих в основе устойчивости бактерий. Так, в публикации Coulton et al., Progress in Medicinal Chemistry 1994, 31: 297-349 заявляется, что широкое применение пенициллинов и цефалоспоринов привело к возникновению β-лактамаз, семейству бактериальных ферментов, которые катализируют гидролиз β-лактамового кольца, которое присутствует в большинстве применяемых в настоящее время антибиотиков. Совсем недавно в публикации Dudley, Pharmacotherapy 1995, 15: 9S-14S было сообщено, что устойчивость, опосредованная β-лактамазами, является главным аспектом причины развития устойчивости бактерий к действию антибиотиков. В настоящее время доступными полусинтетическими или природными ингибиторами β-лактамаз являются клавулановая кислота, которая представляет собой метаболит грибков Streptomyces clavuligerus, и два полусинтетических антибиотика, сульбактам и тазобактам. В патентных документах US 5698577, US 5510343, US 6472406 и публикациях Hubschwerlen et al., J. Med. Chem. 1998, 41: 3961 и Livermore et al., J. Med. Chem. 1997, 40: 335-343 описаны некоторые синтетические ингибиторы β-лактамаз.
Другими источниками информации, относящимися к данному вопросу, являются следующие.
В патентном документе US 2003/0199541 A1 раскрыты несколько азабициклических соединений, включая конкретные 7-оксо-6-диазабицикло[3.2.1]октан-2-карбоксамиды, и их применение в качестве противобактериальных средств.
В патентном документе US 2004/0157826 A1 описаны несколько гетеробициклических соединений, включая конкретные производные диазепинкарбоксамида и диазепинкарбоксилата, и их применение в качестве противобактериальных средств и ингибиторов β-лактамаз.
В патентном документе WO 2008/039420 A2 раскрыты конкретные 7-оксо-2,6-диазабицикло[3.2.0]гептан-6-сульфоокси-2-карбоксамиды и их применение в качестве ингибиторов бета-лактамаз.
В публикации Poole, Cell Mol. Life Set 2004, 61: 2200-2223 приводится обзор устойчивости бактериальных патогенов к β-лактамовым антибиотикам и подходы для преодоления этой устойчивости.
Доступные в настоящее время ингибиторы β-лактамаз неспособны противодействовать постоянно увеличивающемуся разнообразию β-лактамаз. Поэтому существует необходимость в новых ингибиторах β-лактамаз.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к определенным соединениям диазабициклического карбоксамида и карбоксилата, которые являются ингибиторами бета-лактамаз. Соединения и их фармацевтически приемлемые соли применяют в комбинации с бета-лактамовыми антибиотиками при лечении бактериальных инфекций, в частности бактериальных инфекций, устойчивых к действию антибиотиков. Более конкретно, настоящее изобретение включает соединения формулы I:
и их фармацевтически приемлемые соли, где:
связь, обозначенная как "a", является простой связью или двойной связью;
когда связь a является простой связью, X является:
(1) CH2,
(2) CH2CH2,
(3) CH2CH2CH2,
(4) CH-CH,
(5) CH2-CH-CH, или
(6) CH-CH-CH2;
когда связь a является двойной связью, X является:
(1) CH,
(2) CH-CH2, или
(3) CH-CH=CH;
R1 является:
(1) C(O)N(R3)R4,
(2) C(O)OR3, или
(3) C(O)OR5;
R2 является SO3M, OSO3M, SO2NH2, PO3M, OPO3M, CH2CO2M, CF2CO2M, или CF3;
M является H или фармацевтически приемлемым катионом;
R3 является:
(1) C1-8алкилом, замещенным суммарно от 1 до 4 заместителями, выбранными из группы, состоящей из (i) от нуля до 2 N(RA)RB, (ii) от нуля до 2 RC, и (iii) от нуля до 1 из AryA, HetA, или HetB,
(2) CycA,
(3) HetA,
(4) AryA,
(5) HetB, или
(6) AryB;
R4 является H или C1-8алкилом, необязательно замещенным с помощью N(RA)RB;
или, в качестве варианта, когда R1 является C(O)N(R3)R4, R3 и R4 вместе с атомом N, к которому они оба присоединены, образуют насыщенное моноциклическое кольцо с числом членов от 4 до 9, содержащее 1 гетероатом в дополнение к азоту, присоединенному к R3 и R4, выбранному из N, O, и S, где S необязательно окислена до S(O) или S(O)2; где моноциклическое кольцо необязательно конденсировано, соединено мостиком или спиро с насыщенным гетероциклическим кольцом с числом членов от 4 до 7, содержащим от 1 до 3 гетероатомов, независимо выбранных из N, O и S, где S необязательно окислена до S(O) или S(O)2, с образованием бициклической кольцевой системы, где образованная таким образом моноциклическая кольцевая или бициклическая кольцевая система необязательно замещена с помощью 1 или 2 заместителей, каждый из которых независимо является: (1) C1-6алкилом, (2) C1-6фторалкилом, (3) (CH2)1-2G, где G является OH, O-C1-6алкилом, O-C1-6фторалкилом, N(RA)RB, C(O)N(RA)RB, C(O)RA, CO2RA, или SO2RA, (4) O-C1-6алкилом, (5) O-C1-6фторалкилом, (6) OH, (7) оксо, (8) галогеном, (9) N(RA)RB, (10) C(O)N(RA)RB, (11) C(O)RA, (12) C(O)-C1-6фторалкилом, (13) C(O)ORA, или (14) S(O)2RA;
R5 является C1-8алкилом, замещенным 1 или 2 заместителями, каждый из которых независимо является N(RA)C(O)-AryA;
CycA является C4-9циклоалкилом, который необязательно замещен суммарно с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
HetA является насыщенным или мононенасыщенным гетероциклическим кольцом с числом членов от 4 до 9, содержащим от 1 до 3 гетероатомов, независимо выбранных из N, O и S, где любая S в кольце необязательно окислена до S(O) или S(O)2 и либо 1, либо 2 атома углерода в кольце необязательно окислены до C(O); где кольцо необязательно конденсировано с C3-7циклоалкилом; и где необязательно конденсированное, насыщенное или мононенасыщенное кольцо необязательно замещено суммарно с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
AryA является фенилом, который необязательно замещен суммарно с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
HetB является гетероароматическим кольцом с 5 или 6 членами, содержащим от 1 до 4 гетероатомов, выбранных из от 1 до 3 атомов N, из нуля или 1 атома О, и из нуля или 1 атома S; где гетероароматическое кольцо необязательно конденсировано с насыщенным гетероциклическим кольцом с числом членов от 5 до 7, содержащим 1 или 2 гетероатома, независимо выбранных из N, O и S, где любая S в кольце необязательно окислена до S(O) или S(O)2 и либо 1, либо 2 атома углерода в неконденсированном кольце необязательно окислены до C(O); и где необязательно конденсированное гетероароматическое кольцо необязательно замещено суммарно с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
AryB является бициклической кольцевой системой, в которой фенил конденсирован с насыщенным гетероциклическим кольцом с числом членов от 5 до 7, содержащим от 1 до 3 гетероатомов, независимо выбранных из N, O и S, где любая S в кольце необязательно окислена до S(O) или S(O)2, и где бициклическая кольцевая система необязательно замещена суммарно с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
каждое n независимо является целым числом, которое равняется 0, 1, 2, или 3;
каждый RA является независимо H или C1-8алкилом;
каждый RB является независимо H или C1-8алкилом;
каждый RC является независимо C1-6алкилом, OH, O-C1-8алкилом, OC(O)-C1-8алкилом, C(=NH)NH2, NH-C(=NH)NH2, галогеном, CN, C(O)RA, C(O)ORA, C(O)N(RA)RB, SO2RA, SO2N(RA)RB, пиридилом, пирролидинилом, пиперидинилом, пиперазинилом, морфолинилом, или тиоморфолинилом;
и при условии, что:
(A) когда R1 является C(O)OR3 и R3 является AryA, тогда AryA не является (i) незамещенным фенилом, (ii) фенилом, замещенным с помощью NH2, (iii) фенилом, замещенным с помощью OH, (iii) фенилом, замещенным с помощью O-C1-6алкилом, (iv) фенилом, замещенным одним или более галогенами, или (v) фенилом, замещенным с помощью C1-6алкилом;
(B) когда R1 является C(O)OR3 и R3 является C1-6алкилом, замещенным с помощью HetB , тогда HetB не является пиридилом;
(C) когда R1 является C(O)OR3 и R3 является CH2-AryA или CH2CH2-AryA, тогда AryA не является (i) незамещенным фенилом, (ii) фенилом, замещенным с помощью NH2, OH, O-C1-6алкила, или C1-6алкила, или (iii) фенилом, замещенным одним или более галогенами;
(D) когда R1 является C(O)N(R3)R4, R3 является AryA, CH2-AryA или CH2CH2-AryA, и R4 является H или C1-6алкилом, тогда AryA не является незамещенным фенилом, фенилом, замещенным с помощью N(CH3)2, или фенилом, замещенным с помощью C(O)NH2;
(E) когда R1 является C(O)N(R3)R4, R3 является C1-6алкилом, замещенным с помощью HetB, и R4 является H или C1-6алкилом, тогда HetB не является пиридилом; и
(F) когда R1 является C(O)OR3 и R3 является C1-6алкилом, замещенным с помощью RC, тогда RC не является C(O)NH2.
Соединения формулы I ингибируют β-лактамазы и синергитически усиливают противобактериальное действие β-лактамовых антибиотиков (например, имипенема, цефтазидима и пиперациллина) против микроорганизмов, обычно устойчивых к действию β-лактамовых антибиотиков в результате присутствия β-лактамаз. Соединения настоящего изобретения эффективны против β-лактамаз класса A и класса C, и их комбинация с бета-лактамовыми антибиотиками, такими как имипенем, цефтазидим или пиперациллин, может обеспечить эффективное лечение бактериальных инфекций, вызванных β-лактамазами класса A и класса C, продуцируемыми микроорганизмами. Соответственно, настоящее изобретение включает комбинации соединения формулы I с β-лактамовым антибиотиком, подходящим для использования против β-лактамазы класса C, продуцируемой такими бактериями, как Pseudomonas spp., и против β-лактамазы класса A, продуцируемой такими бактериями, как Klebsiella spp. Изобретение также включает композиции, содержащие соединение формулы I или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель. Кроме того, изобретение включает способы лечения бактериальных инфекций и ингибирования бактериального роста путем применения соединения формулы I или его соли, или комбинации, или композиции, содержащей соединение или его соль.
Варианты осуществления, подварианты осуществления, аспекты и характерные черты настоящего изобретения далее либо будут описаны, либо становятся очевидными из последующего описания, примеров и прилагаемых пунктов формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 приведена порошковая рентгенограмма для кристаллического моногидрата, описанного в примере 1D.
На фиг.2 приведена кривая дифференциальной сканирующей калориметрии (DSC) для кристаллического моногидрата, описанного в примере 1D.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как уже было отмечено выше, настоящее изобретение включает соединения формулы I, где соединения являются ингибиторами бета-лактамаз, подходящими для применения в комбинации с бета-лактамовыми антибиотиками для лечения бактериальных инфекций.
Термин "ингибитор β-лактамазы" относится к соединению, которое способно ингибировать активность β-лактамазы. Ингибирование активности β-лактамазы означает ингибирование активности β-лактамазы класса A, C, или D. В случае противомикробных применений предпочтительно, чтобы концентрация, при которой достигается 50% ингибирование, составляла примерно 100 микрограмм/мл или ниже, или примерно 50 микрограмм/мл или ниже, или примерно 25 микрограмм/мл. Термины β-лактамазы "класса A", "класса C", и "класса D" являются хорошо известными терминами для специалистов в этой области, и они описаны в монографии Waley, The Chemistry of β-лактамаза. Page Ed., Chapman & Hall, London, (1992) 198-228.
Термин "β-лактамаза" обозначает белок, способный инактивировать β-лактамовый антибиотик. β-Лактамаза может являться ферментом, который катализирует гидролиз β-лактамового кольца β-лактомового антибиотика. Особый интерес здесь представляют микробные β-лактамазы. β-Лактамаза может являться, например, сериновой β-лактамазой. Представляющий интерес β-лактамазы являются лактамазами, которые описаны, например, в монографии Waley, The Chemistry of β-лактамаза, Page Ed., Chapman & Hall, London, (1992) 198-228. Представляющий здесь особый интерес β-лактамазы включают β-лактамазу класса C из Pseudomonas aeruginosa или Enterobacter cloacae P99 (далее обозначаемую как P99 β-лактамаза) и бета-лактамазу класса A из Klebsiella spp.
Термин "антибиотик" относится к соединению или композиции, которые снижают жизнеспособность микроорганизма, или которые ингибируют рост или пролиферацию микроорганизма. Фраза "ингибирует рост или пролиферацию" означает увеличение времени генерации (то есть времени, требующегося для деления бактериальной клетки или для удвоения популяции), по меньшей мере, примерно в 2 раза. Предпочтительными антибиотиками являются антибиотики, которые могут увеличивать время генерации, по меньшей мере, примерно в 10 раз или более (например, по меньшей мере, примерно в 100 раз или даже до бесконечности, как в случае смерти всех клеток). При использовании в этом описании дополнительно предполагается, что антибиотик включает противомикробное, бактериостатическое, или бактерицидное средство. Примеры антибиотиков, подходящих для применения с точки зрения настоящего изобретения, включают пенициллины, цефалоспорины и карбапенемы.
Термин "β-лактамовый антибиотик" относится к соединению с антибиотическими свойствами, которое содержит β-лактамовую функциональность. Неограничивающие примеры β-лактамовых антибиотиков, подходящих с точки зрения изобретения, включают пенициллины, цефалоспорины, пенемы, карбапенемы, и монобактамы.
Первым вариантом осуществления настоящего изобретения (иначе обозначаемый здесь как "вариант осуществления Е1") является соединение формулы I (иначе обозначаемое здесь как "соединение I"), определяемое выше (то есть определяемое выше в разделе "Сущность изобретения"), или его фармацевтически приемлемая соль; и при условии, что:
(A) когда R1 является C(O)OR3, тогда R3 не является AryA;
(B) когда R1 является C(O)OR3, тогда R3 не является C1-8алкилом, замещенным с помощью HetB;
(C) когда R1 является C(O)OR3, тогда R3 не является C1-8алкилом, замещенным с помощью AryA;
(D) когда R1 является C(O)N(R3)R4; R3 является AryA или C1-8алкилом, замещенным с помощью AryA, и R4 является H или C1-8алкилом, тогда AryA не является незамещенным фенилом, фенилом, замещенным с помощью 1 или 2 N(RA)RB, или фенилом, замещенным с помощью 1 или 2 C(O)N(RA)RB;
(E) когда R1 является C(O)N(R3)R4 и R4 является H или C1-8алкилом, тогда R3 не является C1-8алкилом, замещенным с помощью HetB; и
(F) когда R1 является C(O)OR3 и R3 является C1-8алкилом, замещенным с помощью RC, тогда RC не является C(O)N(RA)RB.
Вторым вариантом осуществления настоящего изобретения (вариант осуществления Е2) является определяемое выше соединение формулы I, или его фармацевтически приемлемая соль; и при условии, что:
(A) когда R1 является C(O)OR3, тогда R3 не является AryA;
(B) когда R1 является C(O)OR3, тогда R3 не является C1-8алкилом, замещенным с помощью HetB;
(C) когда R1 является C(O)OR3, тогда R3 не является C1-8алкилом, замещенным с помощью AryA;
(D) когда R1 является C(O)N(R3)R4, тогда R3 не является AryA или C1-8алкилом, замещенным с помощью AryA;
(E) когда R1 является C(O)N(R3)R4, тогда R3 не является C1-8алкилом, замещенным с помощью HetB; и
(F) когда R1 является C(O)OR3, тогда R3 не является C1-8алкилом, замещенным с помощью RC.
Третьим вариантом осуществления настоящего изобретения (вариант осуществления Е3) является соединение формулы I, или его фармацевтически приемлемая соль; где:
R1 является:
(1) C(O)N(R3)R4, или
(2) C(O)OR3;
R3 является:
(1) C1-8алкилом, замещенным суммарно от 1 до 4 заместителями, выбранными из группы, состоящей из (i) от нуля до 2 N(RA)RB, (ii) от нуля до 2 RC, и (iii) от нуля до 1 из AryA, HetA, или HetB,
(2) CycA,
(3) HetA,
(4) AryA, или
(5) HetB;
R4 является H или C1-8алкилом, необязательно замещенным с помощью N(RA)RB;
HetA является насыщенным гетероциклическим кольцом с числом членов от 4 до 9, содержащим от 1 до 3 гетероатомов, независимо выбранных из N, O и S, где насыщенное гетероциклическое кольцо является необязательно суммарно замещенным с помощью от 1 до 4 заместителей, выбранных из от нуля до 2 (CH2)nN(RA)RB и от нуля до 2 (CH2)nRC;
каждый RC является независимо C1-6алкилом, OH, O-C1-8алкилом, C(=NH)NH2, NH-C(=NH)NH2, галогеном, CN, пиридилом, пирролидинилом, или пиперидинилом; и
все другие переменные определены выше; и при условии, что:
(A) когда R1 является C(O)OR3 и R3 является AryA, тогда AryA не является (i) незамещенным фенилом, (ii) фенилом, замещенным с помощью NH2, (iii) фенилом, замещенным с помощью OH, (iii) фенилом, замещенным с помощью O-C1-6алкила, (iv) фенилом, замещенным одним или более галогенами; или (v) фенилом, замещенным с помощью C1-6алкила;
(B) когда R1 является C(O)OR3 и R3 является C1-6алкилом, замещенным с помощью HetB, тогда HetB не является пиридилом;
(C) когда R1 является C(O)OR3 и R3 является CH2-AryA или CH2CH2-AryA, тогда AryA не является (i) незамещенным фенилом, (ii) фенилом, замещенным с помощью NH2, OH, O-C1-6алкила, или C1-6алкила, или (iii) фенилом, замещенным одним или более галогенами;
(D) когда R1 является C(O)N(R3)R4, R3 является AryA, CH2-AryA или CH2CH2-AryA, и R4 является H или C1-6алкилом, тогда AryA не является ни незамещенным фенилом, ни фенилом, замещенным с помощью N(CH3)2; и
(E) когда R1 является C(O)N(R3)R4, R3 является C1-6алкилом, замещенным с помощью HetB, и R4 является H или C1-6алкилом, тогда HetB не является пиридилом.
Четвертым вариантом осуществления настоящего изобретения (вариант осуществления Е4) является соединение формулы I, определенное в варианте осуществления Е3, или его фармацевтически приемлемая соль; и при условии, что:
(A) когда R1 является C(O)OR3, тогда R3 не является AryA;
(B) когда R1 является C(O)OR3, тогда R3 не является C1-6алкилом, замещенным с помощью HetB;
(C) когда R1 является C(O)OR3, тогда R3 не является C1-6алкилом, замещенным с помощью AryA;
(D) когда R1 является C(O)N(R3)R4, тогда R3 не является AryA или C1-6алкилом, замещенным с помощью AryA; и
(E) когда R1 является C(O)N(R3)R4, тогда R3 не является C1-6алкилом, замещенным с помощью HetB.
Пятым вариантом осуществления настоящего изобретения (вариант осуществления Е5) является соединение формулы I, определенное в варианте осуществления Е3, или его фармацевтически приемлемая соль; и при условии, что:
(A) когда R1 является C(O)OR3, тогда R3 не является AryA;
(B) когда R1 является C(O)OR3, тогда R3 не является C1-6алкилом, замещенным с помощью HetB;
(C) когда R1 является C(O)OR3, тогда R3 не является C1-6алкилом, замещенным с помощью AryA;
(D) когда R1 является C(O)N(R3)R4, тогда R3 не является AryA или C1-6алкилом, замещенным с помощью AryA; и
(E) когда R1 является C(O)N(R3)R4, тогда R3 не является C1-6алкилом, замещенным с помощью HetB.
Шестым вариантом осуществления настоящего изобретения (вариант осуществления Е6) является соединение формулы I, или его фармацевтически приемлемая соль, где связь "a" является простой связью; X является -CH2- или
-CH2CH2-; и все другие переменные определены выше или определены в любом из вышеизложенных вариантов осуществления.
Седьмым вариантом осуществления настоящего изобретения (вариант осуществления Е7) является соединение формулы I, или его фармацевтически приемлемая соль, где связь "a" является простой связью; X является -CH2-, и все другие переменные определены выше или определены в любом из вышеизложенных вариантов осуществления.
Восьмым вариантом осуществления настоящего изобретения (вариант осуществления Е8) является соединение формулы I, или его фармацевтически приемлемая соль, где связь "a" является простой связью; X является -CH2CH2-; и все другие переменные определены выше или определены в любом из вышеизложенных вариантов осуществления.
Девятым вариантом осуществления настоящего изобретения (вариант осуществления Е9) является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; и все другие переменные определены выше или определены в любом одном из предшествующих вариантов осуществления. В аспекте этого варианта осуществления R1 является C(O)NH(R4).
Десятым вариантом осуществления настоящего изобретения (вариант осуществления Е10) является соединение формулы I, или его фармацевтически приемлемая соль, где R2 является OSO3M; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
Одиннадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е11) является соединение формулы I, или его фармацевтически приемлемая соль, где R2 является OSO3H; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
Двенадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е12) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является: (1) C1-4алкилом, замещенным суммарно от 1 до 4 заместителями, выбранными из группы, состоящей из (i) от нуля до 2 N(RA)RB, (ii) от нуля до 2 RC, и (iii) от нуля до 1 из AryA, HetA, или HetB, (2) CycA, (3) HetA, (4) AryA, или (5) HetB; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
Тринадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е13) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является (CH2)2-3N(RA)RB, (CH2)1-3-AryA, (CH2)1-3-HetA, (CH2)1-3-HetB, CycA, HetA, AryA, или HetB; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
Четырнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е14) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA, CH2-HetA, CH2CH2-HetA, CH(CH3)-HetA, или CH(CH2OH)-HetA; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е14 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 определен выше в варианте осуществления Е14; и все другие переменные определены выше в варианте осуществления Е14.
Пятнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е15) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA, CH2-HetA, или CH2CH2-HetA; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е15 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 определен выше в варианте осуществления Е15; и все другие переменные определены выше в варианте осуществления Е15.
Шестнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е16) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA или CH2-HetA; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е16 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 определен выше в варианте осуществления Е16; и все другие переменные определены выше в варианте осуществления Е16.
Семнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е17) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е17 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 определен выше в варианте осуществления Е17; и все другие переменные определены выше в варианте осуществления Е17.
Восемнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е18) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA; HetA является насыщенным гетероциклом, выбранным из группы, состоящей из пирролидинила, пиперидинила, азепанила, и азоканила; где насыщенный гетероцикл необязательно замещен с помощью N(RA)RB и необязательно замещен с помощью 1 или 2 (CH2)nRC; каждый RC является независимо C1-6алкилом, OH, O-C1-8алкилом, C(=NH)NH2, NH-C(=NH)NH2, галогеном, CN, пиридилом, пирролидинилом, или пиперидинилом; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
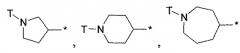
Девятнадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е19) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA; HetA является:
где символ звездочки обозначает место присоединения HetA к остальной части соединения; T является H или RC; RC является C1-6алкилом, OH, O-C1-8алкилом, C(=NH)NH2, NH-C(=NH)NH2, галогеном, CN, пиридилом, пирролидинилом, или пиперидинилом; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления.
Двадцатым вариантом осуществления настоящего изобретения (вариант осуществления Е20) является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA; HetA является:
или
где символ звездочки обозначает место присоединения HetA к остальной части соединения; T является H или RC; RC является С1-6алкилом, OH, O-C1-8алкилом, C(=NH)NH2, NH-C(=NH)NH2, галогеном, CN, пиридилом, пирролидинилом, или пиперидинилом; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. В аспекте этого варианта осуществления T является H.
Двадцать первым вариантом осуществления настоящего изобретения (вариант осуществления Е21) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA является необязательно конденсированным, насыщенным гетероциклическим кольцом, выбранным из группы, состоящей из азетидинила, пирролидинила, оксопирролидинила (например, 2-оксо-пирролидинила), пиперидинила, пиперазинила, тетрагидропиранила, тетрагидротиопиранила, морфолинила, 1,1-диоксидотетрагидро-тиопиранила, азепанила, оксазепанила, азоканила, и азабицикло[3.1.0]циклогексила, где гетероцикл необязательно замещен с помощью 1 или 2 (CH2)nN(RA)RB и необязательно замещен помощью 1 или 2 (CH2)nRC, и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е21 является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA, и HetA и все другие переменные определены выше в варианте осуществления Е21. Вторым подвариантом осуществления варианта осуществления Е21 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 является HetA; и HetA и все другие переменные определены выше в варианте осуществления Е21. В аспекте этого варианта осуществления и его подвариантах осуществления HetA необязательно монозамещен с помощью (CH2)nN(RA)RB и необязательно замещен с помощью 1 или 2 (CH2)nRC.
Двадцать вторым вариантом осуществления настоящего изобретения (вариант осуществления Е22) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA является насыщенным гетероциклическим кольцом, выбранным из группы, состоящей из пирролидинила, пиперидинила, азепанила, и азоканила; где гетероцикл необязательно замещен с помощью 1 или 2 (CH2)nN(RA)RB и необязательно замещен с помощью 1 или 2 (CH2)nRC; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е22 является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA; и HetA и все другие переменные определены выше в варианте осуществления Е22. Вторым подвариантом осуществления варианта осуществления Е22 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)N(R3)R4; R3 является HetA; и HetA и все другие переменные определены выше в варианте осуществления Е22. В аспекте этого варианта осуществления и его подвариантах осуществления HetA необязательно монозамещен с помощью (CH2)nN(RA)RB и необязательно замещен с помощью 1 или 2 (CH2)nRC.
Двадцать третьим вариантом осуществления настоящего изобретения (вариант осуществления Е23) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA определен или в варианте осуществления Е21, или в варианте осуществления E22; каждый RC является независимо OH, O-C1-4алкилом, C(=NH)NH2, NH-C(=NH)NH2, Cl, Br, F, или CN; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. В первом подварианте осуществления R3 является HetA; и HetA определен выше в варианте осуществления Е21. Во втором подварианте осуществления R1 является C(O)N(R3)R4; R3 является HetA; и HetA определен выше в варианте осуществления Е22. В аспекте этого варианта осуществления и его подвариантах осуществления HetA необязательно монозамещен с помощью (CH2)nN(RA)RB и необязательно замещен с помощью 1 или 2 (CH2)nRC.
Двадцать четвертым вариантом осуществления настоящего изобретения (вариант осуществления Е24) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA является гетероциклическим кольцом, определенным или в варианте осуществления Е21 или в варианте осуществления E22; гетероциклическое кольцо в HetA необязательно замещено с помощью галогена, C1-3алкила, O-C1-3алкила, NH2, N(H)-C1-3алкила, N(-C1-3алкила)2, CH2NH2, CH2N(H)-C1-3алкила, CH2N(-C1-3алкила)2, или пиперидинила; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. В первом подварианте осуществления R3 является HetA; и HetA определен выше в варианте осуществления Е24. Во втором подварианте осуществления, R1 является C(O)N(R3)R4; R3 является HetA; и HetA определен выше в варианте осуществления Е24.
Двадцать пятым вариантом осуществления настоящего изобретения (вариант осуществления Е25) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA является гетероциклическим кольцом, определенным или в варианте осуществления Е21 или в варианте осуществления E22; гетероциклическое кольцо в HetA необязательно замещено с помощью F, CH3, OCH3, NH2, N(H)CH3, N(CH3)2, CH2NH2, CH2N(H)CH3, CH2N(CH3)2, или пиперидинила; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. В первом подварианте осуществления R3 является HetA; и HetA определен выше в варианте осуществления Е25. Во втором подварианте осуществления R1 является C(O)N(R3)R4; R3 является HetA; и HetA определен выше в варианте осуществления Е25.
Двадцать шестым вариантом осуществления настоящего изобретения (вариант осуществления Е26) является соединение формулы I, или его фармацевтически приемлемая соль, где HetA является гетероциклическим кольцом, выбранным из группы, состоящей из азетидинила, пирролидинила, пиразолидинила, пиперидинила, пиперазинила, азепанила, оксазепанила, оксазолидинила, изоксазолидинила, морфолинила, и тетрагидропиранила, где гетероциклическое кольцо необязательно замещено с помощью 1 или 2 заместителей, каждый из которых является независимо C1-3алкилом, CH2NH2, CH2N(H)-C1-3алкилом, CH2N(-C1-3алкил)2, O-C1-3алкилом, Cl, Br, F, NH2, N(H)-C1-3алкилом, N(-C1-3алкил)2, C(O)NH2, C(O)N(H)-C1-3алкилом, C(O)N(-C1-3алкил)2, C(O)-C1-3алкилом, C(O)O-C1-3алкилом, OC(O)-C1-3алкилом, S(O)2-C1-3алкилом, S(O)2NH2, S(O)2N(H)-C1-3алкилом, или S(O)2N(-C1-3алкил)2; и все другие переменные определены выше или определены в любом из предшествующих вариантов осуществления. Первым подвариантом осуществления варианта осуществления Е26 является соединение формулы I, или его фармацевтически приемлемая соль, где R3 является HetA, CH2-HetA, CH2CH2-HetA; и HetA и все другие переменные определены выше в варианте осуществления Е26. Вторым подвариантом осуществления варианта осуществления Е26 является соединение формулы I, или его фармацевтически приемлемая соль, где R1 является C(O)OR3; R3 является HetA, CH2-HetA, CH2CH2-HetA; и HetA и все другие переменные определены выше в варианте осуществления Е26. В аспекте этого варианта осуществления и его подвариантах осуществления R2 является OSO3H.
Двадцать седьмым вариантом осущ