Применение и способ профилактики или лечения кариеса, вызванного mutans streptococci, отличных от streptococcus mutans
Иллюстрации
Показать всеИзобретение относится к применению микроорганизма, принадлежащего к роду Lactobacillus, характеризующегося тем, что он способен к специфическому связыванию с бактерией, принадлежащей к группе mutans Streptococci, при котором специфическое связывание характеризуется: (i) стойкостью к тепловой обработке; и/или (ii) стойкостью к протеолитической обработке; и/или (iii) зависимостью от кальция; и/или (iv) формированием при pH в пределах между 4,5 и 8,5; и/или (v) формированием в присутствии слюны, для изготовления противокариозной композиции для лечения или предупреждения кариеса, вызванного mutans Streptococci, отличных от Streptococcus mutans. Специфическое связывание анализируют, осуществляя следующее: (а) выращивание названного микроорганизма до стационарной фазы; (b) смешивание названного микроорганизма с бактерией, принадлежащей к группе mutans Streptococci, которая была выращена до стационарной фазы; (с) инкубирование смеси, полученной на этапе (b) при условиях, позволяющих образование агрегатов названного микроорганизма и бактерии из группы mutans Streptococci; и (d) определение агрегатов по наличию осадка в пробирке. Способ профилактики или лечения кариеса, вызванного mutans Streptococci, отличных от Streptococcus mutans, включает введение пациенту микроорганизма, принадлежащего к роду Lactobacillus, который способен к специфическому связыванию с бактерией, принадлежащей к группе mutans Streptococci, при котором специфическое связывание характеризуется выше обозначенными признаками (i)-(v). Изобретение обеспечивает специфическое связывание вышеупомянутого микроорганизма, принадлежащего к роду Lactobacillus, с такими штаммами mutans Streptococci, отличных от Streptococcus mutans, которые являются кариогенными дентальными патогенами. 2 н. и 22 з.п. ф-лы, 3 ил., 1 табл., 27 пр.
Реферат
Изобретение относится к применению микроорганизма, принадлежащего к группе молочнокислых бактерий или мутанту или его производному, характеризующегося тем, что он способен к специфическому связыванию с бактерией, принадлежащей к группе mutans Streptococci, при котором специфическое связывание характеризуется: (i) стойкостью к тепловой обработке; и/или (ii) стойкостью к протеолитической обработке; и/или (iii) зависимостью от кальция; и/или (iv) формированием при pH в пределах между 4.5 и 8.5; и/или (v) формированием в присутствии слюны, для изготовления противокариозной композиции для лечения или предупреждения кариеса, вызванного mutans Streptococci, другими, чем Streptococcus mutans. Предпочтительно, специфическое связывание может быть проанализировано следующим образом:
(a) выращивание названного микроорганизма до стационарной фазы;
(b) смешивание названного микроорганизма с бактерией, принадлежащей к группе мутантов Streptococci, которая была выращена до стационарной фазы;
(c) инкубирование смеси, полученной на этапе (b) при условиях, позволяющих образование агрегатов названного микроорганизма и бактерии из группы mutans Streptococci; и
(d) определение агрегатов по наличию осадка в пробирке.
Другой объект настоящего изобретения представляет собой способ профилактики или лечения кариеса, вызванного mutans Streptococci, другими, чем Streptococcus mutans, содержащий введение микроорганизма, принадлежащего к группе молочнокислых бактерий, характеризующийся тем, что названный микроорганизм способен к специфическому связыванию с бактерией, принадлежащей к группе mutans Streptococci или мутанта, производного, аналога или фрагмента названного микроорганизма.
Mutans Streptococci поселяются в хозяине после того, как прорежутся первые зубы (Carlson et al., Caries Res. 9 (1975), 333-339). Они локализуются на поверхностях зубов, и их изобилие в зубном камне обусловливает самое большое из первоначальных повреждений (Duchin and van Houte Arch. Biol. Biol. 23 (1978) 779-786). Уровень их заселения внутри зубного камня увеличивается при потреблении сахарозы (Staat et al., J. Dent. Res. 54 (1975) 872-880). Они способны синтезировать некоторые макромолекулы из сахарозы, которые стимулируют их прикрепление к зубам (Tanzer et al., Infect. Immun. 10 (1974) 197-203). Mutans Streptococci являются быстрыми производителями кислоты из простых углеводов, включая сахарозу, и толерантны к низкому pH (Edwardsson, Arch. Biol. 13 (1968) 637-646). Более того, они, по существу, всегда восстанавливаются в местах развившихся первоначальных и упрочившихся кариозных повреждений (Littleton et al., Arch. Oral. Biol. 15 (1979) 461-463). Интерес к ним вырос после демонстрации их возможности вызывать и развивать кариозные повреждения у различных экспериментальных животных, включая моноинфицированных гнотобиотных животных. Их вирулентная экспрессия в значительной степени ассоциируется с потреблением углеводов, особенно сахарозы.
Роль других бактериальных видов, которые связаны с развитием кариеса, подобно молочнокислым бактериям или актиномицетам, не является решающей. Этих бактерий часто находят в кариозных повреждениях, но только в сообществе mutans Streptococci. Согласно современной точке зрения, присутствие mutans Streptococci представляет собой обязательное условие патогенеза кариеса (Tanzer et al., J. Dent. Educ. 65 (2001) 1028-1037). Группа mutans Steptococci образуется как содержащая, по меньшей мере, S. mutans, S. sobrinus, S. cricetus, S. rutti, S. ferus и S. macacae (Loesche et al., Microbio. Rev. 50 (4) (1986) 353-380). Благодаря тому факту, что Streptococcus mutans являются наиболее изобильным представителем из mutans Steptococci у людей, большинство микробиологических исследований кариеса, а также противокариозных мер сосредоточено на этих специфических видах.
Первоначальное присоединение S. mutans к поверхности зубов происходит посредством двух механизмов. Первый механизм представляет собой присоединение S. mutans посредством стрептококкового антигена I/II (SA I/II) - поверхностного белка, также известного под синонимами В, IF, P1, SR, MSL-1 или PAc, - к кутикуле, слою слюнных белков на поверхности зубов. Антитела против этого белка, как было показано, предотвращают адгезию S. mutans in vitro.
Соответственно, стрептококковый антиген I/II (SA I/II) является мишенью для вакцинации. В различных рекомбинантных комбинациях - полный антиген, область присоединения слюны, белок, объединенный с токсином холеры, или экспрессируемый на поверхности авирулентного штамма сальмонеллы - была показана успешная иммунизация животных. Она приводила к высоким титрам IgA и снижению колонизации S. mutans (Huang et al., Infect. Immun. 69 (2001), 2154-2161). Сопоставимые результаты были достигнуты при применении ДНК-вакцины, кодирующей SA I/II (Fan et al., J. Dent. Res. 81 (2002), 784-787).
Пассивный иммунитет достигнут посредством рекомбинантной экспрессии антител анти-SA I/II на поверхности молочнокислых бактерий. Эти молочнокислые бактерии образуют агрегаты с S. mutans, и введение этих бактерий крысам приводило к снижению образования кариеса (Krueger et al., Nature Biotechnology 20 (2002), 702-706).
WO 06/027265 относится к молочнокислым бактериям, способным присоединяться к S. mutans с целью подавить адгезию к зубам.
Наиболее важным партнером по соединению стрептококкового антигена является агглютинин слюны, белок, подобный гликопротеину легкого gp-340 из суперсемейства фагоцитарных цистеин-богатых рецепторов (Prakobphol et al., J. Biol. Chem. 275 (2000) 39860-39866).
Роль агглютинина в патогенезе кариеса до сих пор не полностью понятна. Он может приводить к адгезии S. mutans, когда присутствует в связанном с поверхностью виде, и он может приводить к агрегированию S. mutans, когда присутствует в растворенном состоянии. Последнее может приводить к удалению агрегированных S. mutans изо рта посредством слюны. Высокая концентрация агглютинина в слюне приводит in vitro к увеличению адгезии S. mutans, в то время как in vivo не наблюдается ясной корреляции между концентрацией агглютинина в слюне и риском появления кариеса (Stenudd et al., J. Dent. Res. 80 (2001), 2005-2010).
Моноклональные антитела против агглютинина полностью блокируют присоединение S. mutans к покрытому слюной гидроксиапатиту in vitro и предотвращают зависимое от агглютинина агрегирование (Carlen und Olsson, J. Dent. Res. 74 (1995), 1040-1047; Carlen et al., J. Dent. Res. 77 (1998), 81-90). Brady et al., Infect. Immun. 60 (1992), 1008-1017 показали, что поверхностная адгезия и агрегирование могут независимо друг от друга инициироваться различными антителами. Это показывает, что различные эпитопы агглютинина ответственны за оба эти явления.
Другие белки слюны, часто связываемые с развитием кариеса, представляют собой пролин-богатые белки (PRPs). Однако роль этих белков в адгезии кариесогенных бактерий вызывает дискуссию. Эти белки кодируются двумя генными локусами (PRH-1 и PRH-2) и встречаются в различных вариантах, которые различаются только несколькими аминокислотами (PRP-1, PRP-2, PIF. Db - двойная связь). Эти варианты могут быть протеолитически расщеплены, образуя в результате так называемые маленькие PRPs (PRP-3, PRP-4. Pif-f и Db-f). PRPs опосредуют прочное соединение симбионтов, подобных Actinomyces naeslundii или не-mutans Streptococci. Интересно, что это соединение имеет место только после адгезии белка к поверхности зуба, делая в результате конформационного сдвига сайт связывания доступным. S. mutans связываются только слабо. PRP-вариант Db играет существенную роль в эффективном связывании S. mutans. Высокая концентрация Db коррелирует с высокой адгезией S. mutans и сильным развитием кариеса. Сниженная доля PRP-Db в общей высокой концентрации PRP коррелирует со слабым развитием кариеса (Stenudd et al., J. Dent. Res. 80 (2001), 2005-2010). Присоединяется ли S. mutans непосредственно к PRPs, не известно.
Второй способ присоединения S. mutans к поверхности зуба представляет собой зависимую адгезию посредством сахарозы. S. mutans экспрессируют три различные гликозилтрансферазы (GYFs), которые способны синтезировать полимерный глюкан сахара. Глюканы существуют в водорастворимой форме (1-6 гликозидная связь) и нерастворимой форме, вызванной мутантом (1-3 гликозидная связь). Мутант не может быть разрушен ни ротовыми бактериями, ни ферментами слюны. Он образует клейкую матрицу внутри зубного камня, которая представляет основу для сахарозазависимой адгезии S. mutans. Гликозилтрансферазы GTFB и GTFC, широко распространенные ферменты, ответственные за образование мутанта, размещаются на клеточной поверхности S. mutans. В отличие от них, гликозилтрансфераза GTFD синтезирует растворимый глюкан и секретируется S. mutans. Эксперименты, применяющие GTF дефицитные S. mutans, показывают, что взаимодействие всех трех ферментов необходимо для сахарозазависимой адгезии (Ooshima et al., J. Dent. Res. 80 (2001), 1672-1677).
Гликозилтрансферазы имеют N-терминальный связывающий сайт сахарозы и С-терминальный связывающий сайт глюкана. Антитела против фермента или против связывающего сайта глюкана приводят к ингибированию сахарозазависимой адгезии S. mutans. Невозможно блокировать N-терминальный связывающий сайт сахарозы, применяя антитела (Yu et al., Infect. Immun. 65 (1997), 2292-2298).
Ингибирование гликозилтрансферазы, сопровождаемое снижением адгезии S. mutans, может быть достигнуто посредством некоторых флавоноидов и терпеноидов (US 2004/0057908) или экстрактов прополиса (Duarte et al., Biol. Pharmacol. Bull. 26 (2003), 527-531).
Были найдены молочнокислые бактерии под названием S11, которые снижают образование мутанта и, следовательно, адгезию S. mutans in vitro. Как описано выше, образование мутанта является существенным, для того чтобы S. mutans присоединялись к поверхности зуба. Так, Chung et al. (Oral Microbiol. Immunol. 19 (2004), 214-216) нашли присоединенные клетки S. mutans, когда их инкубировали с молочнокислыми бактериями из штамма S11, которые, как сказано, снижают образование мутанта. Присоединение S. mutans к мутанту происходит посредством присоединения бактериальных белков (белок, присоединяющий глюкан). Точный механизм этого присоединения должен быть определен (Sato et al., Infect. Immun. 65 (1997), 668-675).
Грибы Trichoderma harzianum и Penicillum purpurogenum производят гомолог альфа-1,3-глюконазы (Fuqlsanq et al., J. Biol. Chem. 275 (2000), 2009-2018). Применение видов Enterococcus, Lactobacillus и Lactococcus, эффективных против образования глюкана и образования зубного камня, описано (US 6,036,952). Механизм действия должен быть истолкован.
Другой подход к ингибированию кариеса представляет собой нейтрализацию низкого pH в зубном камне. Мочевина и аргинин являются компонентами слюны. Моча присутствует в концентрации 3-10 ммоль/л, без большого различия между тем, есть у людей кариес или нет. Концентрация свободного аргинина находится в пределах между 4 и 40 µмоль/л. Люди, не имеющие кариеса, в среднем, имеют более высокую концентрацию свободного аргинина в слюне, чем люди, пораженные кариесом (van Wuvckhuvse et al., J. Dent. Res. 74 (1995), 686-690).
Некоторые бактерии зубного камня, подобные Streptococcus sangius и Actinomyces naeslundi, способны расщеплять мочевину или аргинин, образуя в результате аммиак. Щелочной аммоний повышает pH зубного камня и поэтому снижает кариес (Curran et al., Appl. Environm. Microbiol. 61 (1995), 4494-4496; Morou-Bermudez and Burne. Infect. Immun. 68 (2000), 6670-6676). Таким образом, предполагается, что эти бактерии можно применять для лечения кариеса. Другой подход, предложенный для лечения кариеса, состоит в том, что при протеолизе PRP-1 и PRP-3 образуются аргинин-богатые белки, которые могут, после дальнейшего протеолиза посредством оральных бактерий, подобных S. sangius, S. oralis и S. mitis, приводить к более высокому pH в зубном камне. Посредством применения рекомбинантного варианта из этих белков сахарозазависимое снижение pH сдерживается (Li et al., Infect. Immun. 68 (2000), 5425-5429). Более того, описано, что применяя жевательную резинку, содержащую мочевину, после приема сахарозы, можно задержать падение pH, и таким образом, например, S. mutans могут не так сильно повлиять на кариес.
Однако, из сказанного выше очевидно, что специалисты в данной области техники концентрируют свое внимание на противокариозных мерах, направленных против Streptococcus mutans. Никакие меры, которые позволили бы выбрать в качестве цели mutans Streptococci, других, чем Streptococcus mutans, не описываются, несмотря на их возможную роль в патогенезе кариеса. Поэтому необходимо найти средства и способы, которые выполнили бы вышеупомянутые желаемые критерии и которые были бы пригодны для предупреждения и/или лечения кариеса, вызванного бактериями, другими, чем Streptococcus mutans.
Техническая проблема, лежащая в основе настоящего изобретения, такова, чтобы осуществить вышеописанную необходимость. Решение названной технической проблемы достигается посредством обеспечения вариантов выполнения изобретения, как описано в формуле изобретения.
Таким образом, в первом объекте настоящее изобретение относится к применению микроорганизма, принадлежащего к группе молочнокислых бактерий или мутанту или его производного, характеризующегося тем, что он способен к специфическому связыванию с бактерией, принадлежащей к группе mutans Streptococci, при котором специфическое связывание характеризуется: (i) стойкостью к тепловой обработке; и/или (ii) стойкостью к протеолитической обработке; и/или (iii) зависимостью от кальция; и/или (iv) формированием при pH в пределах между 4.5 и 8.5; и/или (v) формированием в присутствии слюны, для изготовления противокариозной композиции для лечения или предупреждения кариеса, вызванного mutans Streptococci, другими, чем Streptococcus mutans. Предпочтительно, при специфическом связывании можно проанализировать следующее:
(a) выращивание названного микроорганизма до стационарной фазы;
(b) смешивание названного микроорганизма с бактерией, принадлежащей к группе mutans Streptococci, которые были выращены до стационарной фазы;
(c) инкубирование смеси, полученной на этапе (b) при условиях, позволяющих образование агрегатов названного микроорганизма и бактерии из группы mutans Streptococci; и
(d) определение агрегатов по наличию осадка в пробирке.
В предпочтительном варианте выполнения изобретения бактерия, принадлежащая к группе mutans Streptococci, использованная в таком анализе, представляет собой Streptococcus mutans.
Специфическое связывание, предпочтительно, оценивается, как описано здесь, в Примере 4 ниже.
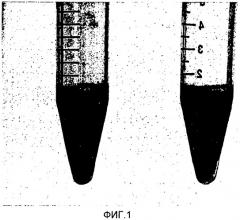
В частности, для определения агрегатов mutans Streptococci по наличию осадка в пробирке, как описано в Примере 4 ниже, микроорганизмы, принадлежащие к группе молочнокислых бактерий, предпочтительно смешаны с mutans Streptococci в объемном отношении от 3:1 до 60:1 (mutans Streptococci:молочнокислые бактерии). Как молочнокислые бактерии, так и mutans Streptococci выращиваются до стационарной фазы, как описано в Примере 1. Предпочтительно, оптическая плотность измеряется способом фотометрии при длине волны 600 нм. Упомянутые отношения соответствуют отношению образующих колонию единиц от 1:50 до 1:2.5. Предпочтительно, OD600=1 в 1 мл соответствует 3×108 образующих колонию единиц mutans Streptococcus. Предпочтительно, OD600=1 в 1 мл соответствует 7×109 образующих колонию единиц молочнокислых бактерий, как здесь описано ниже. Предпочтительно, при определении агрегатов по наличию осадка в пробирке бактерии представлены в объеме 2 мл в пробирках Фалкон емкостью 15 мл. Если необходимо, суспензии культуры разбавляют забуференным фосфатом физиологическим раствором (PBS), чтобы получить упомянутое выше объемное отношение, сохраняя в то же время окончательный объем 2 мл. Предпочтительно, смесь перемешивается в течение около 15 секунд и затем оставляется в покое, по меньшей мере, на 5, 10, 15 минут, и более предпочтительно, по меньшей мере, на 20 минут при комнатной температуре, то есть при любой температуре между 16°С и 25°С. Агрегация наблюдается как немедленное помутнение суспензии, и после, по меньшей мере, 20 минут агрегация наблюдается как скопление агрегатов, которые оседают как видимые гранулы (примерно показано на Фиг.1, левая пробирка Фалкон), в то время как не mutans Streptococcus при агрегации смесей остаются в суспензии (примерно показано на Фиг.1, правая пробирка Фалкон). В качестве контроля само-агрегация соответствующей молочнокислой бактерии и штамма mutans Streptococcus может быть проанализирована в отсутствие либо mutans Streptococcus, либо молочнокислой бактерии.
Агрегация молочнокислой бактерии и mutans Streptococcus согласно описанному выше анализу может быть измерена количественно посредством отделения образовавшихся агрегатов центрифугированием, например, при 500×g в течение 30 секунд. Затем количество агрегатов может быть определено измерением количества не агрегированных клеток, которые остаются в супернатанте. Определение можно выполнить любым подходящим способом, известным специалисту в данной области техники. Предпочтительно, определение выполняется посредством удаления некоторого объема супернатанта, например, 1 мл. Затем оптическая плотность удаленного супернатанта может быть измерена при любой подходящей длине волны, известной специалисту, например, при 600 нм. Измеренное значение после вычитания значения, соответствующего контрольному испытанию без молочнокислой бактерии, представляет количество клеток, которые не были агрегированы.
В качестве альтернативы, чтобы исследовать возможную проблему самоагрегации, можно применить красящее вещество. Таким образом, в более предпочтительном варианте выполнения изобретения специфическое связывание можно проанализировать следующим образом:
(a) выращивание названного микроорганизма до стационарной фазы;
(b) смешивание названного микроорганизма с бактерией, принадлежащей к группе mutans Streptococci, которые были выращены до стационарной фазы и которые были окрашены, используя подходящее красящее вещество, предпочтительно, флюоресцирующее красящее вещество;
(c) инкубирование смеси, полученной на этапе (b), при условиях, позволяющих образование агрегатов названного микроорганизма и бактерии из группы mutans Streptococci; и
(d) определение агрегатов посредством определения красящего вещества, предпочтительно, флюоресцирующего красящего вещества.
Кроме того, в предпочтительном варианте выполнения изобретения бактерия, принадлежащая к группе mutans Streptococci, использованная в таком анализе, представляет собой Streptococcus mutans. Предпочтительно, такой анализ агрегации может быть выполнен, как описано здесь в Примере 5 ниже. В частности, для анализа агрегации mutans Streptococci, как описано в Примере 5 ниже, и молочнокислые бактерии и mutans Streptococci выращиваются до стационарной фазы, как описано в Примере 1. Предпочтительно, оптическая плотность измеряется способом фотометрии при длине волны 600 нм. Предпочтительно, OD600=1 в 1 мл соответствует 3×108 образующих колонию единиц mutans Streptococcus. Предпочтительно, OD600=1 в 1 мл соответствует 7×109 образующих колонию единиц молочнокислых бактерий, как здесь описано ниже. Затем mutans Streptococci окрашиваются. В другом, предпочтительном, варианте выполнения изобретения молочнокислые бактерии окрашиваются, в то время как Streptococci не окрашиваются. Поскольку может применяться любое красящее вещество в качестве красителя, предпочтительно, можно применить флюоресцирующий краситель, известный специалистам в данной области техники. Предпочтительно, специфический или не специфический флюоресцирующий краситель может применяться, например, CFDA-SE. Особым образом клетки собираются, например, центрифугированием, предпочтительно, при 3200×g в течение 5 минут. Затем полученные гранулы могут быть повторно суспендированы в любом подходящем буфере, известном специалисту в данной области техники, предпочтительно, в PBS буфере. Количество буфера можно рассчитать таким образом, чтобы полученная суспензия имела OD600, например, 4.2/мл. Затем суспензия может быть смешана с подходящим красителем, например, с флюоресцирующим красителем, предпочтительно, с 5,6-карбоксифлуоресцеиндиацетатом, сукцинимидиловым эфиром (CFDA-SE), более предпочтительно, с 2µл раствора CFDA-SE (Invitrogen). Затем клетки могут быть инкубированы в течение подходящего периода времени, как известно специалисту в данной области техники, например, в течение 2 часов, при подходящей температуре, как известно специалисту, например, при 37°С. На следующем этапе окрашенные клетки могут быть собраны, например, центрифугированием. Предпочтительно, центрифугирование выполняется при 3200×g в течение 5 минут. Клетки затем могут быть повторно суспендированы в любом подходящем буфере, как известно специалисту, например, в 2 мл PBS буфера. Для агрегирования микроорганизмы, принадлежащие к группе молочнокислых бактерий, предпочтительно, смешиваются с mutans Streptococci в объемном отношении от 3:1 до 1:3 (mutans Streptococci:молочнокислые бактерии). Более предпочтительно, объемное отношение смеси составляет 1:1. Упомянутое отношение соответствует числу единиц, образующих колонию, от 1:50 до 1:150. Для анализа реакции агрегации посредством измерения окрашивания, предпочтительно способом флюоресценции, молочнокислые бактерии и mutans Streptococci применяются в любом соответствующем объеме, как известно специалисту, предпочтительно, в объеме 50 µл. Предпочтительно, смешивание выполняется на пластине микротитратора, например, в 96-ячеечной пластине микротитратора. Затем смесь может быть перемешана, предпочтительно, в течение 12 минут при максимальной скорости. После этого смесь может быть центрифугирована, например, в течение 10 секунд при 500×g. Супернатант затем может быть удален, и гранулы повторно суспендированы в любом подходящем буфере, известном специалисту в данной области техники, предпочтительно, в PBS буфере в любом подходящем объеме, например, в 100 µл. Окрашивание суспензии можно измерить в смеси любым подходящим способом, известным специалисту. Предпочтительно, в случае флюоресценции, флюоресценция может быть определена посредством считывающего устройства, например, при длине волны 495 нм при возбуждении и 525 нм при эмиссии. Для контроля, можно проанализировать только молочнокислые бактерии, и только mutans Streptococci. Исходные данные любого окрашивания, например, флюоресцентного, можно измерить для определения только mutans Streptococci, и можно, предпочтительно, вычесть из значения агрегации с соответствующими молочнокислыми бактериями. Эффект агрегации присутствует, если исходные данные окрашивания, например, флюоресцентного, измеренного как показано здесь выше, вычитаются из измеренного окрашивания, например, флюоресцентного, образца, содержащего молочнокислые бактерии, как описано здесь выше, и испытуемые mutans Streptococci, как описано здесь выше, и полученное значение составляет, по меньшей мере, выше нуля. Более предпочтительно, эффект агрегации присутствует, если полученное значение выше нуля воспроизводится в ряде испытаний, выполненных, как описано здесь выше. "Ряд испытаний" означает, по меньшей мере, 2, предпочтительно 3, более предпочтительно 4, и наиболее предпочтительно 5 испытаний.
Описанное выше специфическое связывание не требует магния. Это свойство может быть испытано, как описано в прилагаемых Примерах.
Как показано в прилагаемых Примерах, неожиданно было найдено, что молочнокислые бактерии, которые первоначально были идентифицированы и выделены посредством вышеупомянутого анализа связывания благодаря их способности связывать Streptococcus mutans, в то же время не связывая другие виды Streptococcus, S. salivarius, S. oralis, S. mitis, и/или S. sanguinis (см. WO 06/27265), показали способность связывать различные другие mutans Streptococci, например, Streptococcus sobrinus, Streptococcus cricetus, Streptococcus ratti, Streptococcus ferus и Streptococcus macacae. Таким образом, идентификация молочнокислых бактерий, которые показали вышеописанные характеристики связывания в отношении Streptococcus mutans, и связывание которых, предпочтительно, оценивается вышеописанными анализами, обеспечивает молочнокислые бактерии, которые не только способны агрегировать Streptococcus mutans, но которые способны также агрегировать другие mutans Streptococci, то есть виды Streptococcus, которые имеют общие характеристики, как описано далее ниже, и которые также вносят свой вклад в развитие кариеса. Таким образом, молочнокислые бактерии, которые показали выше перечисленные характеристики связывания, в отличие от одного типа бактерии, принадлежащей к группе mutans Streptococci (например, Streptococcus mutans), как было найдено, также способны агрегировать другие бактерии, принадлежащие к группе mutans Streptococci, и могут, таким образом, применяться для предупреждения и/или лечения кариеса, вызванного такими другими бактериями. Таким образом, идентифицированные выше анализы для тестирования связывания молочнокислых бактерий с одной бактерией, принадлежащей к группе mutans Streptococci, позволяют идентифицировать молочнокислые бактерии, которые также связываются/агрегируют с другими бактериями из группы mutans Streptococci. Таким образом, настоящее изобретение обеспечивает важное улучшение в обеспечении средств и способов для исследования кариеса, который вызывается mutans Streptococci, другими, чем Streptococcus mutans.
Как очевидно из сказанного выше, все упомянутые выше характеристики относятся к упомянутому выше микроорганизму, принадлежащему к группе молочнокислых бактерий, подходящему агенту для предупреждения и/или лечения кариеса, в частности, кариеса, который вызван mutans Streptococci, другими, чем Streptococcus mutans. Соответственно, вышеупомянутый микроорганизм, принадлежащий к группе молочнокислых бактерий, вызывает противокариозное действие, и таким образом представляет собой подходящий агент для предупреждения и/или лечения кариеса, в частности кариеса, вызванного mutans Streptococci, другими, чем Streptococcus mutans. "Кариес" или "зубной кариес" или "дупло в зубе" являются взаимозаменяемыми терминами для хронической инфекционной болезни, связанной с уязвимой разрушенной областью в зубе, которая постепенно приводит к потере зуба. Она обычно встречается у детей и подростков, но может поразить любого человека. Она является наиболее важной причиной потери зубов у более молодых людей. Кариес можно диагностировать посредством способов, известных специалистам в данной области техники (см., например, Angmar-Mansson and ten Bosch, Adv. Dent. Res. 7 (1993), 70-79).
Термин "mutans Streptococcus" относится к микроорганизму таксономической группы Streptococcus, который находится в зубном камне в ротовой полости и который вызывает ферментацию маннитола и сорбитола. Предпочтительно, это микроорганизм с упомянутыми выше характеристиками, который, кроме того, способен производить внеклеточные глюканы из сахарозы. Предпочтительно, названный микроорганизм является кариесогенным, в частности для людей и/или животных моделей. Более предпочтительно, термин относится к микроорганизму, который показывает все вышеупомянутые характеристики. Ферментация сорбитола и маннитола может быть проверена посредством использования любого подходящего теста, известного специалисту в данной области техники, например, тест API 20 Strep (Biomerieux, France).
Более предпочтительно, термин относится к микроорганизму, принадлежащему к видам Streptococcus mutans, Streptococcus sobrinus, Streptococcus cricetus, Streptococcus ratti, Streptococcus ferus, или Streptococcus macacae. Даже более предпочтительно, термин относится к микроорганизму, принадлежащему Streptococcus mutans серотипа c (DSMZ 20523), Streptococcus mutans серотипа e (NCTC 10923), Streptococcus mutans серотипа f (NCTC 11060), Streptococcus sobrinus DSM 20742, Streptococcus ratti DSM 20564, Streptococcus cricetus DSM 20562, Streptococcus ferus DSM 20646, или Streptococcus macacae DSM 20714. Термин "mutans Streptococci" относится, по меньшей мере, к одному микроорганизму из группы mutans Streptococcus, как описано здесь выше. Предпочтительно, термин относится к какой-либо комбинации и подгруппе микроорганизмов, принадлежащих к группе mutans Streptococcus, как описано здесь выше.
Термин "предупреждение кариеса" включает профилактику кариеса. Таким образом, субъект, который никогда ранее не сталкивался с mutans Streptococci, причинными агентами кариеса, но рискующий встретиться, то есть быть инфицированным mutans Streptococci, извлекает пользу, например, из применений и способов настоящего изобретения до того, как названный субъект будет страдать от кариеса. Следовательно, применения и способы настоящего изобретения можно, например, применять к младенцам, детям или молодым животным для профилактики кариеса, поскольку ротовая полость младенцев или молодых животных обычно свободна от mutans Streptococci. Однако, композиции, применяемые по настоящему изобретению, не ограничиваются введением младенцам, детям или молодым животным.
Термин "лечение кариеса" включает введение композиций, как описано здесь ниже, субъекту, страдающему от кариеса, с целью снижения количества клеток mutans Streptococci и/или для полного очищения рта от mutans Streptococci, в частности ротовой полости, включая зубы. Конечно, после проведенного лечения от mutans Streptococci, представляется возможным, что соответствующий субъект извлекает пользу из применений и способов настоящего изобретения с точки зрения профилактического противокариозного воздействия, направленного на mutans Streptococci.
Если требуется, упомянутый выше микроорганизм, принадлежащий к группе молочнокислых бактерий, представляет собой пробиотический микроорганизм, который, кроме своих противокариозных эффектов, оказывает благоприятное влияние на организм хозяина, которому он вводится. "Пробиотик", по общепринятому определению, представляет собой "пищевую добавку из живых микроорганизмов, которые благоприятно влияют на хозяина-животное, улучшая микробный баланс его кишечника".
Mutans Streptococci встречаются как часть нормальной флоры во рту. Они вовлекаются в случае зубного кариеса у людей и животных, в частности, млекопитающих. Зубной камень пристает к трещинкам и впадинкам зубов, расположенных рядом с деснами. Вначале он состоит из гликопротеина, который осаждается и адсорбируется на зубной эмали. Ротовые бактерии затем начинают объединяться с гликопротеином. Пищевая сахароза является важным участником в развитии кариеса, особенно если сахароза находится в виде клейкой сладкой пищи, часть которой может оставаться во рту в течение некоторого времени. Сахароза, таким образом, более полно метаболизируется mutans Streptococci с образованием кислоты. Напитки, которые содержат сахарозу, проглатываются, и таким образом сахароза проводит во рту меньше времени. Существенно, что наличие зубного камня контролируется регулярным применением зубной щетки, зубочистки и зубной нити. Добавление 1 миллионной доли фторида к питьевой воде оказывается очень эффективным для снижения кариеса. Кроме того, возможность применения вакцины против Streptococcus mutans рассматривалось в научном сообществе. Таким образом, кроме общих схем оральной гигиены, которая воздействует по большей части на бактерии в полости рта, уровень техники почти полностью сфокусирован на специфических мерах против Streptococcus mutans. Однако, согласно удивительной находке настоящего изобретения, такие естественно встречающиеся микроорганизмы, принадлежащие к группе молочнокислых бактерий, предпочтительно, к роду Lactobacillus, которые идентифицированы по их способности связывать Streptococcus mutans, также способны связывать штаммы mutans Streptococci, подобных, например, Streptococcus sobrinus, Streptococcus cricetus, Streptococcus ratti, Streptococcus ferus, или Streptococcus macacae, теперь возможно эффективно предотвратить и/или лечить кариес, вызванный mutans Streptococci, другими, чем Streptococcus mutans, так как вышеупомянутые микроорганизмы, принадлежащие к группе молочнокислых бактерий, способны к агрегированию и смыванию mutans Streptococci, подобных, например, Streptococcus sobrinus, Streptococcus cricetus, Streptococcus ratti, Streptococcus ferus, или Streptococcus macacae. Таким образом, настоящее изобретение обеспечивает применение легко вводимых бактерий, которые представляют собой организмы пищевого класса, которые, в дополнение к их противокариозным свойствам, могут применяться как пробиотики.
В частности, при анализе микроорганизмов, принадлежащих к группе молочнокислых бактерий, предпочтительно, к роду Lactobacillus, которые первоначально были идентифицированы благодаря их способности связывать Streptococcus mutans, но не Streptococcus salivarius, Streptococcus oralis, Streptococcus mitis и Streptococcus sanguinis, с удивлением было обнаружено, что названные микроорганизмы не только способны связываться с Streptococcus mutans, но также присоединять другие виды mutans Streptococci, подобных, например, Streptococcus sobrinus, Streptococcus cricetus, Streptococcus ratti, Streptococcus ferus, или Streptococcus macacae, которые являются причиной кариеса. Посредством связывания с этими mutans Streptococci, микроорганизм, принадлежащий к группе молочнокислых бактерий, предпочтительно, к роду Lactobacillus, как здесь описано, между прочим, присоединяется и агрегирует mutans Streptococcus, и таким образом, в результате вымывает mutans Streptococcus естественным потоком слюны, тем самым предупреждая и/или излечивая кариес. Кроме того, упомянутые выше микроорганизмы, принадлежащие к группе молочнокислых бактерий, действительно, предпочтительно, не связываются с другими микроорганизмами, которые не принадлежат к группе mutans Streptococci, присутствующих в ротовой полости, как описано здесь, и в частности в Примере 6 здесь ниже. Таким образом, микросреда ротовой полости не нарушается, поскольку только mutans Streptococci, как причинные агенты кариеса убывают. Для лучшего понимания, mutans Streptococci не оказывают каких-либо полезных действий в ротовой полости, и таким образом, их потеря не имеет никакого неблагоприятного эффекта для соответствующего хозяина.
Поразительно, что специфическое связывание упомянутого выше микроорганизма, принадлежащего к группе молочнокислых бактерий, в частности, к виду Lactobacillus, описанное здесь, с mutans Streptococci, обладает стойкостью к тепловой обработке и/или обработке протеазой. В дополнение, специфическое связывание зависит от кальция и/или не зависит от магния, и устойчиво при кислотной точке 4.5, и оно совершается в присутствии слюны, что делает, в частности, его подходящим для применения в виде оральных аппликаций или как добавку к пище, фуражу или напиткам, которые могут содержать более высокие концентрации кальция, таким как молоко. Замечательно, что термически инактивированные или лиофилизованные аналоги, производные или фрагмент(ы) названных микроорганизмов, раскрытых здесь, все еще способны к специфическому связыванию с mutans Streptococci. Этот удивительный эффект представляет собой предпочтение для применения названного аналога(ов) или фрагмента(ов) названных микроорганизмов, так же как мутантов, или их производных в композициях для применения у животных, предпочтительно, людей или млекопитающих для предупреждения и/или лечения кариеса. В частности, названные аналоги или фрагменты можно легко добавить к любой композиции, например, к косметической или фармацевтической композиции, пище, или фуражу, или напиткам и подобным. К тому же, производство таких аналогов или фрагментов является дешевым и легким, и они могут храниться продолжительные периоды времени без потери своей способности к специфическому связыванию с mutans Streptococci. Другим преимуществом вышеупомянутого микроорганизма, принадлежащего к группе молочнокислых бактерий, является то, что он сохраняет свою способность к специфическому связыванию с mutans Streptococci, когда он лиофилизован, или высушен, или подвергнут распылительной сушке. Это делает его удобным ингредиентом для применения в описанных здесь композициях.
Другие варианты выполнения и преимущества изобретения частично изложены здесь в описании и частично могут быть очевидными из описания или можно узнать из выполнения изобретения.
До того, как настоящее изобретение будет описано в деталях, следует понимать, что это изобретение не ограничивается отдельной методологией, протоколами, бактериями, векторами, реагентами и т.д., описанными здесь, так как они могут варьироваться. Также следует понимать, что терминология, использованная здесь, применяется только для целей описания конкретных вариантов выполнения и не предназначена ограничить объем настоящего изобретения, который ограничивается только прилагаемой формулой изобретения. Кроме указанного иначе, все технические и научные термины, использованные здесь, имеют те же самые значения, какие обыкновенно подразумеваются обычным специалистом в данной области техники.
Предпочтительно, использованные здесь термины образованы так, как описано в "A multilingual glossary of biotechnological terms: (IUPAC Recommendations)", Leuenberger, H.G.W, Nagel, В and Kölbl, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland).
Во всем описании и формуле изобретения, которая следует, если контекст не требует иначе, слово "содержать", и вариации, такие как "содержат" и "содержащий", понимаются таким образом, чтобы означать включение установленного целого или действия, или группы целых или действий, но без исключения любого другого целого или действия, или группы целых или действий.
В данном описании цитируются некоторые документы. Каждый из документов, цитируемых здесь (включая все патенты, заявки на патент, научные публикации, производственные спецификации, инструкции и т.д.), выше или ниже, введены здесь ссылками во всей полноте. Ничто здесь не должно быть истолковано как признание действительным, что изобретение не озаглавлено, чтобы датировать более ранним числом такое открытие, благодаря предшествующему изобретению.
Следует отметить, что, так как применяется здесь и в прилагаемо