Фармацевтическая композиция для модифицированного высвобождения
Иллюстрации
Показать всеФармацевтическая композиция для модифицированного высвобождения содержит (1) анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты или его фармацевтически приемлемую соль, (2) по меньшей мере, одну добавку, которая обеспечивает проникновение воды в фармацевтическую композицию и которая имеет растворимость, такую что объем воды, требуемой для растворения 1 г добавки, равен 10 мл или меньше, и (3) гидрогель-образующий полимер, имеющий среднюю молекулярную массу приблизительно 100000 или более, или вязкость 12 мПа·с или более в 5% водном растворе при 25°С. Изобретение обеспечивает высвобождение указанного активного агента, не затронутое эффектами пищевого рациона. 2 н. и 21 з.п. ф-лы, 1 ил., 4 табл., 17 пр.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к фармацевтической композиции для модифицированного высвобождения, способного к снижению эффектов пищи, которые наблюдаются с обычными таблетками, комбинацией активного ингредиента с определенными ингредиентами для контроля скорости высвобождения активного ингредиента.
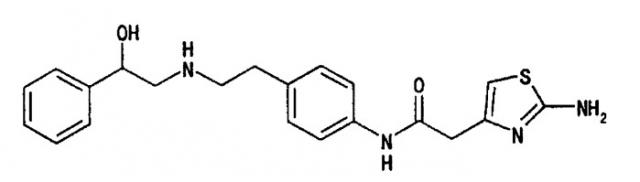
Точнее, данное изобретение относится к фармацевтической композиции, содержащей анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты или его фармацевтически приемлемую соль, добавку, которая обеспечивает проникновение воды в фармацевтическую композицию (иногда называемую в настоящем описании гидрофильной основой), и полимер, который образует гидрогель, в которой изменения в AUC и Cmax, вызываемые потреблением пищи, могут быть снижены контролированием скорости высвобождения активного ингредиента.
Уровень техники
Анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты был разработан фирмой Astellas Pharma Inc., и было опубликовано, что данное соединение обладает не только активностью как по стимулированию секреции инсулина, так и активностью по усилению инсулиновой чувствительности, но также и активностью против ожирения и антигиперлипемической активностью, основанной на активности селективно стимулированного β3-рецептора, и применимо в лечении диабета (см., например, патентную литературу 1).
Кроме того, опубликовано, что данное соединение может быть использовано в качестве терапевтического средства для гиперактивного мочевого пузыря, а именно, гиперактивного мочевого пузыря, сопровождаемого гиперплазией простаты, или гиперактивного мочевого пузыря, сопровождаемого безотлагательностью мочеиспускания, недержанием мочи и частотой мочеиспускания (см., например, патентную литературу 2).
Клиническое испытание анилида (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты в форме обычных композиций выявило недостатки, например, состоящие в том, что фармакокинетические данные неожиданно изменялись согласно наличию или отсутствию потребления пищи (неопубликованные данные). Например, скорость снижения Cmax в состоянии потребления пищи была равна 67%, и скорость уменьшения AUC в состоянии потребления пищи была равна 47% по сравнению с данными показателями в состоянии намеренного голодания. В данном случае Сmax в состоянии намеренного голодания была в три раза больше, чем эта величина в состоянии потребления пищи. Данные проблемы, как полагают, подняты, например, изменениями в фармакокинетике, вызываемыми пищей, и поэтому желательна разработка композиции, способной к предотвращению эффектов от приема пищи.
В качестве методологии приготовления композиции для модифицированного высвобождения, раскрыта гидрогелевая таблетка с пролонгированным высвобождением, содержащая добавку, которая обеспечивает проникновение воды в таблетку, и гидрогель-образующий полимер (см., например, патентную литературу 3).
Однако, патентная литература 3 не относится к анилиду (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты, и требуются дополнительные усовершенствования, чтобы создать фармацевтическую композицию.
Список ссылок
Патентная литература
[Патентная литература 1] International Publication No. WO 99/20607 (пример 41)
[Патентная литература 2] International Publication No. WO 2004/041276
[Патентная литература 3] International Publication No. WO 94/06414
Сущность изобретения
Техническая проблема
Цель данного изобретения состоит в том, чтобы предложить фармацевтическую композицию для модифицированного высвобождения, содержащую анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты или его фармацевтически приемлемую соль, в котором фармацевтическая композиция имеет эффективность, аналогичную или более высокую, чем эффективности обычных препаратов, и не имеет никаких ограничений на прием пищи, и способ изготовления фармацевтической композиции.
Решение проблемы
Период полувыведения (Т1/2) анилида (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты является долгим (приблизительно от 18 до 24 часов), и, следовательно, препарат из него для модифицированного высвобождения не обязательно необходим, чтобы поддерживать его уровень в крови. Принимая в рассмотрение результаты клинического испытания, описанного выше, данные изобретатели провели интенсивные исследования, чтобы создать препарат, с акцентом на контроль скорости высвобождения лекарственного средства из препарата до степени, при которой высвобождение не подвержено воздействию приема пищи или тому подобного, а не на усиление контроля высвобождения.
На основе профилей концентрации в крови (в состоянии намеренного голодания/после потребления пищи) после введения обычного препарата (препарата с быстрым высвобождением) скорость абсорбции лекарственного средства в состоянии потребления пищи вычислена методом деконволюции, чтобы прогнозировать непрерывную абсорбцию в течение примерно 4 часов. Данные изобретатели считали из этого результата, что препарат, способный к непрерывному высвобождению лекарственного средства в течение 4 часов или более, был бы способен снижать эффекты от пищи, потому что высвобождение лекарственного средства из препарата стало бы стадией, ограничивающей скорость для абсорбции.
Данные изобретатели проводили клиническое испытание на человеке, используя три типа препаратов, в которых скорость высвобождения лекарственного средства контролировалась (время, когда процент высвобождения лекарственного средства из стандартного препарата был 80% (Т80%)=4 часа, 6 часов и 10 часов), и нашли, что все препараты могли снижать эффекты от пищи, чтобы завершить данное изобретение.
Общеизвестно, что время удерживания в желудке и скорость высвобождения препаратов для модифицированного высвобождения меняются согласно наличию или отсутствию пищевого рациона, и в результате этого существует возможность того, что профили концентрации в крови изменены. Однако, удивительно, при применении данного препарата, изменение профилей концентрации в крови было небольшим в присутствии или в отсутствие пищевого рациона.
Данное изобретение отличается тем, что предлагает фармацевтическую композицию для модифицированного высвобождения, которое не затронуто эффектами пищевого рациона и проявляет сниженное изменение в AUC и Cmax.
В данном изобретении предлагается:
[1] фармацевтическая композиция для модифицированного высвобождения, содержащая (1) анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты или его фармацевтически приемлемую соль, (2) по меньшей мере, одну добавку, которая обеспечивает проникновение воды в фармацевтическую композицию и которая имеет растворимость, такую что объем воды, требуемой для растворения 1 г добавки, равен 10 мл или меньше, и (3) гидрогель-образующий полимер, имеющий среднюю молекулярную массу приблизительно 100000 или более, или вязкость 12 мПа·с или более в 5% водном растворе при 25°С;
[2] фармацевтическая композиция для модифицированного высвобождения по [1], в которой добавка, которая обеспечивает проникновение воды в фармацевтическую композицию, представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленгликоля, поливинилпирролидона, D-маннита, D-сорбита, ксилита, лактозы, сахарозы, безводной мальтозы, D-фруктозы, декстрана, глюкозы, полиоксиэтилен гидрированного касторового масла, полиоксиэтилен полиоксипропиленгликоля, сложного эфира высшей жирной кислоты и полиоксиэтиленсорбитана, хлорида натрия, хлорида магния, лимонной кислоты, винной кислоты, глицина, β-аланина, гидрохлорида лизина и меглумина;
[3] фармацевтическая композиция для модифицированного высвобождения по [2], в которой добавка, которая обеспечивает проникновение воды в фармацевтическую композицию, представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленгликоля, поливинилпирролидона, D-маннита, лактозы, сахарозы, хлорида натрия и полиоксиэтилен полиоксипропиленгликоля;
[4] фармацевтическая композиция для модифицированного высвобождения по любому одному из [1]-[3], в которой количество добавки, которая обеспечивает проникновение воды в фармацевтическую композицию, составляет от 5% масс. до 75% масс. по отношению к общей массе фармацевтической композиции;
[5] фармацевтическая композиция для модифицированного высвобождения по [4], в которой количество добавки, которая обеспечивает проникновение воды в фармацевтическую композицию, составляет от 5% масс. до 70% масс. по отношению к общей массе фармацевтической композиции;
[6] фармацевтическая композиция для модифицированного высвобождения по любому одному из [1]-[5], в которой гидрогель-образующий полимер представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленоксида, гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, натрий карбоксиметилцеллюлозы, гидроксиэтилцеллюлозы и карбоксивинильного полимера;
[7] фармацевтическая композиция для модифицированного высвобождения по [6], в которой гидрогель-образующий полимер представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленоксида, гидроксипропилметилцеллюлозы и гидроксипропилцеллюлозы;
[8] фармацевтическая композиция для модифицированного высвобождения по любому одному из [1]-[7], в которой количество гидрогель-образующего полимера составляет от 1% масс. до 70% масс. по отношению к общей массе фармацевтической композиции;
[9] фармацевтическая композиция для модифицированного высвобождения по любому одному из [1]-[8], дополнительно содержащая антиоксидант;
[10] фармацевтическая композиция для модифицированного высвобождения по [9], в которой антиоксидант представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из бутилгидрокситолуола, пропилгаллата и аскорбата натрия;
[11] фармацевтическая композиция для модифицированного высвобождения по [10], в которой антиоксидант представляет собой бутилгидрокситолуол;
[12] фармацевтическая композиция для модифицированного высвобождения по любому одному из [9]-[11], в которой количество гидрогель-образующего полимера составляет от 0,025% масс. до 0,25% масс.;
[13] фармацевтическая композиция для модифицированного высвобождения по любому одному из [1]-[12], дополнительно содержащая стабилизатор;
[14] фармацевтическая композиция для модифицированного высвобождения по [13], в которой стабилизатор представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из желтого оксида железа(III), красного оксида железа(III), черного оксида железа;
[15] фармацевтическая композиция для модифицированного высвобождения по [14], в которой стабилизатор представляет собой желтый оксид железа(III) и/или красный оксид железа(III);
[16] фармацевтическая композиция для модифицированного высвобождения по любому одному из [13]-[15], в которой количество стабилизатора составляет от 0,05% масс. до 1% масс.;
[17] способ изготовления фармацевтической композиции для модифицированного высвобождения, отличающийся тем, что включает смешивание (1) анилида (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты или его фармацевтически приемлемой соли с (2), по меньшей мере, одной добавкой, которая обеспечивает проникновение воды в фармацевтическую композицию и которая имеет растворимость, такую что объем воды, требуемой для растворения 1 г добавки, равен 10 мл или меньше, и (3) гидрогель-образующим полимером, имеющим среднюю молекулярную массу приблизительно 100000 или более, или вязкость в 12 мПа·с или более в 5% водном растворе при 25°С, где количество добавки составляет от 5% масс. до 75% масс. по отношению к общей массе фармацевтической композиции, и количество гидрогель-образующего полимера составляет от 1% масс. до 70% масс. по отношению к общей массе фармацевтической композиции;
[18] способ по [17], в котором добавка, которая обеспечивает проникновение воды в фармацевтическую композицию, представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленгликоля, поливинилпирролидона, D-маннита, D-сорбита, ксилита, лактозы, сахарозы, безводной мальтозы, D-фруктозы, декстрана, глюкозы, полиоксиэтилен гидрированного касторового масла, полиоксиэтилен полиоксипропиленгликоля, сложного эфира высшей жирной кислоты и полиоксиэтиленсорбитана, хлорида натрия, хлорида магния, лимонной кислоты, винной кислоты, глицина, β-аланина, гидрохлорида лизина и меглумина; и
[19] способ по [17] или [18], в котором гидрогель-образующий полимер представляет собой одно соединение или два или более соединений, выбираемых из группы, состоящей из полиэтиленоксида, гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, натрий карбоксиметилцеллюлозы, гидроксиэтилцеллюлозы и карбоксивинильного полимера.
В качестве методик приготовления лекарственного средства для снижения или исключения изменений в фармакокинетиках, а именно, AUC и Cmax, сопровождаемых рационом питания, раскрыта методика приготовления, относящаяся к фармацевтической композиции с пролонгированным высвобождением, содержащей гидрохлорид тамсулозина (см. Japanese Unexamined Patent Publication (Kokai) No. 2005-162736 и Japanese Unexamined Patent Publication (Kokai) No. 2005-162737). Данная методика приготовления лекарственного средства ограничена тамсулозином и применена к препарату, содержащему лекарственное средство в малой дозе (0,4 мг на стандартный препарат). Данный препарат создает возможность для контроля высвобождения из него тамсулозина, за счет большого содержания основы для пролонгированного высвобождения. В противоположность этому, фармацевтическая композиция данного изобретения содержит лекарственное средство в высокой дозе (т.е. высокое содержание на стандартный препарат), и, как считают, это затрудняет контроль скорости высвобождения лекарственного средства из препарата, включающего основу для пролонгированного высвобождения при низком содержании, и поэтому данное изобретение методически совершенно отлично от препарата, описанного в данных ссылках.
Полезные эффекты изобретения
Согласно данному изобретению может быть предложена фармацевтическая композиция для модифицированного высвобождения, которая не имеет ограничений на пищевой рацион и является устойчивой (например, снижение изменений в профиле последующего растворения).
Кроме того, может быть предложена фармацевтическая композиция для модифицированного высвобождения, в которой AUC не уменьшена.
Что касается обычного препарата, скорость снижения Сmax в состоянии потребления пищи была равна 67% по сравнению с данным показателем в состоянии намеренного голодания. Напротив, что касается фармацевтической композиции для модифицированного высвобождения по данному изобретению, скорость снижения Сmax в состоянии потребления пищи была равна 42% по сравнению с данным показателем в состоянии намеренного голодания, и данный результат показал, что снижение Сmax, вызываемое пищевым рационом, могло быть значительно уменьшено созданием композиции в виде фармацевтического препарата для модифицированного высвобождения.
Краткое описание чертежей
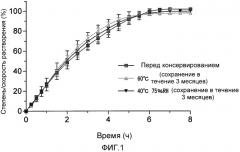
[Фиг. 1] Фигура 1 представляет собой график, показывающий профили растворения фармацевтической композиции для модифицированного высвобождения, приготовленной в примере 11, и их временные продолжительности.
Описание вариантов осуществления
Фармацевтическая композиция для модифицированного высвобождения по данному изобретению будет объяснена в настоящем описании далее.
Термин “препарат для быстрого высвобождения (обычный препарат)”, как он использован в настоящем описании, означает препарат, в котором скорость растворения лекарственного средства из препарата составляет 85% или больше спустя 30 минут от начала теста по растворению, который выполняют в соответствии с тестом по растворению (метод с использованием лопастной мешалки), описанным в фармакопее США, с условиями, что используют 900 мл соответствующей тест-жидкости (такой как USP-буфер, рН 6,8), и скорость вращения лопастной мешалки составляет 100 об/мин. В альтернативном случае, данный термин означает препарат, в котором скорость растворения лекарственного средства из препарата составляет 85% или больше спустя 30 минут от начала теста по растворению, который выполняют в соответствии с тестом по растворению, методом 2, описанным в японской фармакопеи, с условиями, что используют 900 мл соответствующей тест-жидкости (такой как буферный раствор Мак-Илвейна, рН 6,8), и скорость вращения лопастной мешалки составляет 50 об/мин.
Термин “фармацевтическая композиция для модифицированного высвобождения”, как он использован в настоящем описании, означает препарат, в котором скорость растворения лекарственного средства из препарата составляет меньше чем 85% спустя 30 минут от начала теста по растворению в вышеприведенных условиях, и высвобождение лекарственного средства контролируют до степени, при которой эффекты, вызываемые пищей, снижены. Точнее, эта композиция является препаратом, в котором добавка (гидрофильная основа), которая обеспечивает проникновение воды в препарат, объединена с полимером, который образует гидрогель.
Выражение “эффекты, вызываемые пищей, снижены”, как оно использовано в настоящем описании, означает, например, 10% снижение, 20% снижение в другом варианте осуществления и 30% снижение в еще другом варианте осуществления по сравнению с Сmax обычного препарата. В альтернативном случае, данный термин означает, например, 10% снижение относительно скоростей снижения Сmax и AUC при введении после приема пищи по сравнению с Сmax и AUC при введении в состоянии намеренного голодания, 20% снижение в другом варианте осуществления и 30% снижение в еще другом варианте осуществления.
Скорости снижения Сmax и AUC вычислены по следующим уравнениям:
Rd(Cmax)=[Cmax(FS)-Cmax(FI)]×100/Cmax(FS)
Rd(AUC)=[AUC(FS)-AUC(FI)]×100/AUC(FS)
Rd(Cmax):скорость снижения Cmax (%)
Cmax(FS) Cmax при введении в состоянии намеренного голодания
Cmax(FI):Cmax при введении после приема пищи
Rd(AUC):скорость уменьшения AUC (%)
AUC(FS):AUC при введении в состоянии намеренного голодания
AUC(FI):AUC при введении после приема пищи
Выражение “препарат, в котором эффекты, вызываемые пищей, уменьшены”, как оно использовано в настоящем описании, означает препарат, в котором степень растворения лекарственного средства из препарата составляет 75% или меньше спустя 1,5 часа и 100% или меньше спустя 4 часа от начала теста по растворению, который выполняют в вышеприведенных условиях [в соответствии с тестом по растворению (метод с использованием лопастной мешалки), описанным в фармакопее США, с условиями, что используют 900 мл соответствующей тест-жидкости (такой как USP-буфер, рН 6,8), и скорость вращения лопастной мешалки составляет 50-200 об/мин]. В другом варианте осуществления, данный термин означает препарат, в котором степень растворения лекарственного средства из препарата составляет 75% или меньше спустя 1,5 часа и от 75% или больше до 100% или меньше спустя 7 часов.
Термин “устойчивый”, как он использован в настоящем описании, означает устойчивость композиции, например, против нагревания, температуры, влажности или света. Точнее, данный термин означает, что, например, когда пластмассовый сосуд наполняют фармацевтической композицией и герметизируют и затем сосуд хранят в течение трех месяцев в условиях при 40°С и 75% RH/ОВ или при 60°С, изменение в степени растворения в точке, показывающей степень растворения в 50%, принимает значения внутри пределов ±5% или меньше.
Анилид (R)-2-(2-аминотиазол-4-ил)-4'-[2-[(2-гидрокси-2-фенилэтил)амино]этил]уксусной кислоты (далее в настоящем описании иногда называемый как соединение А) представлен следующей структурной формулой.
Химическая структура 1
Соединение А может быть использовано в свободной форме, которая не является солью, и может образовывать соль с кислотой в других вариантах осуществления. Примеры такой соли включают кислотно-аддитивную соль с минеральной кислотой, такой как хлористоводородная кислота, бромистоводородная кислота, иодистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, или тому подобное; и кислотно-аддитивную соль с органической кислотой, такой как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, лимонная кислота, винная кислота, угольная кислота, пикриновая кислота, метансульфоновая кислота, этансульфоновая кислота, глутаминовая кислота, или тому подобное.
Доза соединения А может быть надлежащим образом выбрана в соответствии с симптомом, возрастом, полом и тому подобным для пациента, подлежащего лечению. Суточная доза соединения А для перорального введения во взрослую особь обычно принимает значение в интервале от 0,01 до 100 мг/кг, которую вводят сразу иди делят на две-четыре дозы в сутки.
Содержание соединения А на препарат составляет, например, от 1% масс. до 70% масс., от 5% масс. до 70% масс. в другом варианте осуществления и от 5% масс. до 50% масс. в еще другом варианте осуществления. Содержание соединения А на препарат составляет от 1 мг до 50 мг и от 10 мг до 200 мг в другом варианте осуществления.
Требуется, что гидрогель-образующий полимер, использованный в настоящем изобретении, может контролировать скорость высвобождения лекарственного средства до степени, при которой профиль концентрации в крови лекарственного средства не затронут присутствием или отсутствием приема пищи.
Молекулярная масса гидрогель-образующего полимера равна, например, 100000 или больше, от 100000 до 8000000 в другом варианте осуществления, от 100000 до 5000000 в еще другом варианте осуществления, и от 100000 до 2000000 в еще другом варианте осуществления. Вязкость гидрогель-образующего полимера составляет, например, 12 мПа·с или больше в 5% водном растворе при 25°С; 12 мПа·с или больше в 5% водном растворе при 25°С, и 40000 мПа·с или меньше в 1% водном растворе при 25°С в другом варианте осуществления; 400 мПа·с или больше в 2% водном растворе при 25°С, и 7500 мПа·с или меньше в 1% водном растворе при 25°С в еще другом варианте осуществления; и 400 мПа·с или больше в 2% водном растворе при 25°С, и 5500 мПа·с или меньше в 1% водном растворе при 25°С в еще другом варианте осуществления.
В фармацевтической композиции для модифицированного высвобождения по данному изобретению, период времени высвобождения лекарственного средства из препарата можно произвольно контролировать регулированием вязкости полимера, который использован в качестве гидрогель-образующего полимера.
Гидрогель-образующий полимер, используемый в данном изобретении, особенно не ограничивают, пока высвобождение лекарственного средства можно контролировать до степени, при которой эффекты пищи на соединение А могут быть снижены. Примеры гидрогель-образующего полимера включают полиэтиленоксид, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, натрий карбоксиметилцеллюлозу, гидроксиэтилцеллюлозу и карбоксивинильные полимеры. Примеры гидрогель-образующего полимера в другом варианте осуществления включают полиэтиленоксид, гидроксипропилметилцеллюлозу и гидроксипропилцеллюлозу.
Примеры полиоксиэтиленоксида (далее в настоящем описании называемого иногда как РЕО) включают названия продукта, полиокс WSR-308 [средняя молекулярная масса: 8000000, вязкость: 10000-15000 мПа·с) (1% водный раствор при 25°С)], полиокс WSR-303 [средняя молекулярная масса: 7000000, вязкость: 7500-10000 мПа·с) (1% водный раствор при 25°С)], полиокс WSR коагулятн [средняя молекулярная масса: 5000000, вязкость: 5500-7500 мПа·с) (1% водный раствор при 25°С)], полиокс WSR-301 [средняя молекулярная масса: 4000000, вязкость: 1650-5500 мПа·с) (1% водный раствор при 25°С)], полиокс WSR-N-60K [средняя молекулярная масса: 2000000, вязкость: 2000-4000 мПа·с) (2% водный раствор при 25°С)], полиокс WSR-N-12K [средняя молекулярная масса: 1000000, вязкость: 400-800 мПа·с) (2% водный раствор при 25°С)], полиокс WSR-1105 [средняя молекулярная масса: 900000, вязкость: 8800-17600 мПа·с) (5% водный раствор при 25°С)], полиокс WSR-205 [средняя молекулярная масса: 600000, вязкость: 4500-8800 мПа·с) (5% водный раствор при 25°С)], полиокс WSR-N-750 [средняя молекулярная масса: 300000, вязкость: 600-1200 мПа·с) (5% водный раствор при 25°С)], полиокс WSR-N-80 [средняя молекулярная масса: 200000, вязкость: 55-90 мПа·с) (5% водный раствор при 25°С)] и полиокс WSR-N-10 [средняя молекулярная масса: 100000, вязкость: 12-50 мПа·с) (5% водный раствор при 25°С)] (Dow).
Примеры гидроксипропилметилцеллюлозы (далее в настоящем описании обозначаемой иногда как НРМС) включают название продукта метолоза 90SH50000 [вязкость в 2% водном растворе при 20°С: 2900-3900 мПа·с], метолоза SB-4 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4 мПа·с), TC-5RW (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 6 мПа·с), TC-5S (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 15 мПа·с), TC-5R (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 6 мПа·с), TC-5M (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4 мПа·с), TC-5E (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 3 мПа·с), метолоза 60SH-50 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 50 мПа·с), метолоза 65SH-50 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 50 мПа·с), метолоза 90SH-100 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 100 мПа·с), метолоза 90SH-100SR (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 100 мПа·с), метолоза 65SH-400SR (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 400 мПа·с), метолоза 90SH-400 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 400 мПа·с), метолоза 65SH-1500SR (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 1500 мПа·с), метолоза 60SH-4000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4000 мПа·с), метолоза 65SH-4000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4000 мПа·с), метолоза 90SH-4000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4000 мПа·с), метолоза 90SH-4000SR (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4000 мПа·с), метолоза 90SH-15000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 15000 мПа·с), метолоза 90SH-15000SR (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 15000 мПа·с), метолоза 90SH-30000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 30000 мПа·с).
Примеры гидроксипропилцеллюлозы (далее в настоящем описании обозначаемой иногда как НРС) включают HPC-SSL (название продукта, Nippon Soda Co., Ltd.) (вязкость в 2% водном растворе при 20°С: 2,0-2,9 мПа·с), HPC-SL (название продукта, Nippon Soda Co., Ltd.) (вязкость в 2% водном растворе при 20°С: 3,0-5,9 мПа·с), HPC-L (название продукта, Nippon Soda Co., Ltd.) (вязкость в 2% водном растворе при 20°С: 6,0-10,0 мПа·с), HPC-М (название продукта, Nippon Soda Co., Ltd.) (вязкость в 2% водном растворе при 20°С: 150-400 мПа·с) и HPC-Н (название продукта, Nippon Soda Co., Ltd.) (вязкость в 2% водном растворе при 20°С: 1000-4000 мПа·с).
Примеры метилцеллюлозы (далее в настоящем описании обозначаемой иногда как МС) включают метолозу SM15 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 15 мПа·с), метолозу SM25 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 25 мПа·с), метолозу SM100 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 100 мПа·с), метолозу SM400 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 400 мПа·с), метолозу SM1500 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 1500 мПа·с), метолозу SM4000 (название продукта, Shin-Etsu Chemical Co., Ltd.) (вязкость в 2% водном растворе при 20°С: приблизительно 4000 мПа·с).
Примеры натрий карбоксиметилцеллюлозы (далее в настоящем описании обозначаемой иногда как CMCNa) включают названия продукта, Sunrose F-30MC [вязкость: 250-350 мПа·с (1% водный раствор при 25°С)], Sunrose F-150MC [средняя молекулярная масса: 200000, вязкость: 1200-1800 мПа·с (1% водный раствор при 25°С)], Sunrose F-600MC [вязкость: 6000-8000 мПа·с (1% водный раствор при 25°С)], Sunrose F-1000MC [средняя молекулярная масса: 420000, вязкость: 8000-12000 мПа·с (тот же)], Sunrose F-1400MC [вязкость: 12000-15000 мПа·с (1% водный раствор при 25°С)] и Sunrose F-300MC [средняя молекулярная масса: 300000, вязкость: 2500-3000 мПа·с (тот же)], (Nippon Paper Chemical Co., Ltd.).
Примеры гидроксиэтилцеллюлозы (далее в настоящем описании обозначаемой иногда как НЕС) включают названия продукта, HEC DAICEL SE850 [средняя молекулярная масса: 1480000, вязкость: 2400-3000 мПа·с (1% водный раствор при 25°С)] и HEC DAICEL SE900 [средняя молекулярная масса: 1560000, вязкость: 4000-5000 мПа·с (1% водный раствор при 25°С)] (Daicel Chemical Industries, Ltd.).
Примеры карбоксивинильных полимеров включают карбопол 71G (вязкость: 4000-11000 мПа·с), карбопол 971P (вязкость: 4000-11000 мПа·с), карбопол 981 (вязкость: 4000-10000 мПа·с), карбопол 941 (вязкость: 4000-10000 мПа·с), карбопол 934 (вязкость: 30500-39400 мПа·с) и карбопол 934Р (вязкость: 29400-39400 мПа·с), (B.F. Googrich Chemical).
Данные гидрогель-образующие полимеры могут быть использованы по отдельности или как соответствующая комбинация из двух или более полимеров. Может быть использована комбинация из различных количеств.
Содержание гидрогель-образующего полимера особенно не ограничивают, пока оно представляет собой количество до значения, при котором профиль концентрации лекарственного средства в крови не затронут наличием или отсутствием приема пищи. Содержание гидрогель-образующего полимера составляет, например, от 1% масс. до 70% масс. по отношению к общей массе препарата, и от 3% масс. до 70% масс. в другом варианте осуществления. Содержание гидрогель-образующего полимера составляет от 5% масс. до 70% масс. по отношению к общей массе препарата, от 10% масс. до 60% масс. в другом варианте осуществления и от 10% масс. до 40% масс. в еще другом варианте осуществления. Содержание гидрогель-образующего полимера составляет от 0,1% масс. до 1000% масс. по отношению к общей массе лекарственного средства, от 1% масс. до 500% масс. в другом варианте осуществления и от 5% масс. до 300% масс. в еще другом варианте осуществления.
Полимер, вязкость которого (перед смешиванием) находится за пределами определенного интервала, может быть использован как соответствующая комбинация с одним или несколькими другими полимерами в случае, если смесь, полученная смешиванием данных многих полимеров, имеет вязкость (измеренную перед применением) в рамках определенного интервала.
В добавке, которая обеспечивает проникновение воды в фармацевтическую композицию данного изобретения (гидрофильная основа), количество воды, необходимой для растворения 1 г гидрофильной основы при 20±5°С, равно 10 мл или меньше, 6 мл или меньше в другом варианте осуществления, 5 мл или меньше в еще другом варианте осуществления и 4 мл или меньше в еще другом варианте осуществления. Когда гидрофильная основа имеет высокую растворимость в воде, эффект, который позволяет воде проникать в препарат, является высоким.
Примеры гидрофильной основы включают водорастворимые полимеры, такие как полиэтиленгликоль [PEG: например, названия продуктов PEG 400, PEG 1500, PEG 4000, PEG 6000 и PEG 20000 (NOF Corporation)], поливинилпирролидон (PVP: например, название продукта PVP K30 (BASF)), и тому подобное; спирты сахаров, такие как D-маннит, D-сорбит, ксилит, и тому подобное; сахариды, такие как лактоза, сахароза, безводная мальтоза, D-фруктоза, декстран (например, декстран 40), глюкоза, и тому подобное); сурфактанты, такие как гидрированное полиоксиэтиленкасторовое масло [HCO: например, кремофор RH40 (BASF), HCO-40, HCO-60 (Nikko Chemicals)], полиоксиэтиленполиоксипропиленгликоль [например, плуроник F68 (Asahi Denka и тому подобное)], сложные эфиры высших жирных кислот и полиоксиэтиленсорбитана [твин, например, твин 80 (Kanto Chemical)], и тому подобное; соли, такие как хлорид натрия, хлорид магния, и тому подобное; органические кислоты, такие как лимонная кислота, винная кислота, и тому подобное; аминокислоты, такие как глицин, β-аланин, гидрохлорид лизина, и тому подобное; и аминосахариды, такие как меглумин, и тому подобное.
Как другой вариант осуществления, могут быть использованы PEG, PVP, D-маннит, D-сорбит, ксилит, лактоза, сахароза, безводная мальтоза, D-фруктоза, декстран, глюкоза, полиоксиэтиленполиоксипропиленгликоль, хлорид натрия, хлорид магния, лимонная кислота, винная кислота, глицин, β-аланин, гидрохлорид лизина или меглумин. В качестве еще другого варианта осуществления могут быть использованы PEG, PVP, D-маннит, лактоза, сахароза, хлорид натрия, полиоксиэтиленполиоксипропиленгликоль, или тому подобное.
Данные гидрофильные основы могут быть использованы по отдельности или как соответствующая комбинация из двух или более основ.
Содержание гидрофильной основы особенно не ограничивают, пока оно представляет собой количество, способное контролировать высвобождение лекарственного средства до степени, при которой высвобождение лекарственного средства не затронуто влиянием пищи. Содержание гидрофильной основы составляет, например, от 5% масс. до 75% масс., от 5% масс. до 70% масс. в другом варианте осуществления, и от 20% масс. до 60% масс. в еще другом варианте осуществления.
Фармацевтическая композиция для модифицированного высвобождения по данному изобретению может быть приготовлена в виде разных лекарственных форм, которые включают, например, препараты для перорального введения, такие как таблетки, капсулы (включая микрокапсулы), гранулы и порошок, и препараты для парентерального введения, такие как суппозитории (например, ректальные суппозитории или вагинальные суппозитории). Данные препараты могут быть безопасно введены перорально или парентерально. Препараты для перорального введения, такие как таблетки, капсулы и гранулы, могут быть выбраны в другом варианте осуществления.
Фармацевтическая композиция для модифицированного высвобождения по данному изобретению может быть приготовлена смешиванием лекарственного средства, гидрогель-образующих полимеров и гидрофильной основы и приданием смеси заранее определенной формы. Смешивание и формование может быть выполнено в соответствии с общепринятыми методами, широко применяемыми в технологической области для приготовления лекарственного средства. Если желательно, то может быть использован фармацевтически приемлемый носитель.
В приготовлении фармацевтической композиции для модифицированного высвобождения по данному изобретению могут быть использованы, если желательно, дополнительные различные фармацевтические добавки. Такие фармацевтические добавки на особенно ограничивают, пока они являются фармацевтически приемлемыми. Примеры фармацевтических добавок включают различные органические или неорганические вещества-носители, которые широко используются как продукты для приготовления препаратов, а именно, наполнители, замасливатели, связующие вещества и дезинтеграторы. Если желательно, то могут быть использованы другие добавки для приготовления препаратов, такие как консерванты, антиоксиданты, стабилизаторы, средства для покрытия пленкой, окрашивающие средства и подсластители.
Примеры наполнителей включают лактозу, сахарозу, D-маннит, D-сорбит, крахмал, желатинированный крахмал, декстрин, кристаллическую целлюлозу, малозамещенную гидроксипропилцеллюлозу, карбоксиметилцеллюлозу натрия, аравийскую камедь, пуллулан, слабообезвоженную кремниевую кислоту, синтетический силикат алюминия, алюминатметасиликат магния и тому подобное.
Примеры замасливателей включают стеарат магния, стеарат кальция, тальк