Жидкая композиция, содержащая антитело высокой концентрации
Иллюстрации
Показать всеГруппа изобретений относится к фармацевтике и касается обеспечения жидкой стабильной антителосодержащей композиции и способа ингибирования димеризации молекул антитела в жидкой композиции. Композиция содержит 40-1000 мМ аргинина, 10-200 мМ метионина и антитело в концентрации 50-300 мг/мл. Группа изобретений обеспечивает получение стабильной композиции, подходящей для подкожного введения, при этом предотвращаются димеризация и деамидирование антитела во время долгосрочного хранения. 2 н. и 19 з.п. ф-лы, 8 ил., 3 пр., 7 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к антителосодержащей композиции и, в частности, к стабильной жидкой композиции, содержащей высокую концентрацию антитела.
УРОВЕНЬ ТЕХНИКИ
В недавние годы были разработаны и использованы на практике различные композиции антител. Многие такие композиции антител используются в инъекционных растворах для внутривенного введения. Однако вследствие необходимости клинических служб существует увеличивающаяся потребность в разработке антителосодержащей композиции, которая может вводиться в виде самоинъецируемой подкожной инъекции.
В создании антителосодержащей композиции для подкожной инъекции, поскольку доза антитела на одно введение является большой (приблизительно 100-200 мг) и количество инъекционного раствора обычно ограничивается в подкожной инъекции, необходимо увеличение концентрации антитела во вводимой жидкости. Ввиду этого во многих случаях используют композиции с высокой концентрацией, которые готовят способом лиофилизации-концентрирования, в котором лиофилизированную композицию воссоздают в воде, имеющей объем, меньший, чем объем перед лиофилизацией. Однако существует высокая потребность в жидкой композиции, которая не требует воссоздания и которая поддается легкому манипулированию. Хотя увеличение вязкости композиции вследствие добавления криопротективного агента, такого как сахар, в процессе получения лиофилизированной композиции не является предпочтительным для композиций для подкожной инъекции, предполагается, что эту проблему можно было бы избежать, если бы эта композиция была жидкой композицией.
Растворы, содержащие высокую концентрацию антитела, имеют тенденцию к образованию растворов, имеющих высокую вязкость, вследствие макромолекулярных свойств белков и вследствие межмолекулярных взаимодействий белков. Кроме того, в случаях, когда белок хранят в форме раствора, имеющего высокую концентрацию, имеет место проблематичная деградация, которая включает в себя генерирование нерастворимых и/или растворимых агрегатов; и необходимо предотвратить такую деградацию. В частности, в композициях антител образуются, вероятно, ассоциации, и нерастворимые агрегаты, вероятно, генерируются в жидком состоянии. В случаях, когда жидкую композицию хранят в течение продолжительного времени, существует проблема, заключающаяся в том, что биологическая активность молекул антител теряется вследствие деамидирования аминокислотных остатков, таких как остатки аспарагина.
Были предложены различные идеи в отношении обеспечения стабилизированных композиций, в которых потеря активного компонента является малой даже после хранения этой композиции в течение продолжительного периода времени. Такие композиции готовят растворением активного компонента и различных добавок в буферном растворе. Однако для жидких композиций, содержащих высокую концентрацию антитела, до сих пор не существует способ, который является достаточным для предотвращения димеризации и деамидирования.
Существует потребность в обеспечении композиции, содержащей высокую концентрацию антитела, которая является как стабильной, так и подходящей для применения в подкожном введении.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМА, КОТОРАЯ ДОЛЖНА БЫТЬ РЕШЕНА ИЗОБРЕТЕНИЕМ
Целью данного изобретения является обеспечение жидкой композиции, содержащей высокую концентрацию антитела, в которой ингибируются димеризация и деамидирование во время продолжительного старения и которая пригодна для применения в подкожном введении.
СРЕДСТВА ДЛЯ РЕШЕНИЯ ЭТОЙ ПРОБЛЕМЫ
Авторы этого изобретения проводили интенсивное исследование для достижения вышеуказанной цели и в результате обнаружили, что стабильная жидкая композиция, содержащая антитело высокой концентрации, может быть обеспечена добавлением аминокислоты, аргинина или его соли, в качестве стабилизатора, для выполнения посредством этого данного изобретения.
Таким образом, данное изобретение обеспечивает следующие далее композиции, такие как:
(1) Стабильная антителосодержащая жидкая композиция, характеризующуюся тем, что она содержит аргинин и метионин.
(2) Композиция (1), дополнительно содержащая гистидиновый буферный агент.
(3) Композиция (1) или (2), дополнительно содержащая поверхностно-активное вещество.
(4) Композиция по (1)-(3), содержащая антитело в количестве по меньшей мере 50 мг/мл.
(5) Композиция по (1)-(3), содержащая антитело в количестве по меньшей мере 100 мг/мл.
(6) Композиция по (1)-(3), содержащая антитело в количестве по меньшей мере 120 мг/мл.
(7) Композиция по (1)-(6), где это антитело является антителом против рецептора IL-6.
(8) Стабильная жидкая композиция, содержащая антитело против рецептора IL-6, характеризующаяся тем, что она содержит либо аргинин, либо метионин.
(9) Композиция по (1)-(8), где это антитело является гуманизированным антителом или антителом человека.
(10) Композиция по (1)-(9), дополнительно содержащая триптофан.
(11) Композиция по (1)-(10), имеющая рН в диапазоне от 4 до 8.
(12) Композиция по (1)-(11), где аргинин присутствует в количестве от 50 до 1500 мМ.
(13) Композиция по (1)-(12), имеющая вязкость от 2 до 15 мПа·с.
(14) Композиция по (1)-(13), которая стабильна при 22-28°C в течение по меньшей мере 6 месяцев.
(15) Композиция по (1)-(13), отличающаяся тем, что димеризация молекул антител ингибируется.
(16) Композиция по (1)-(13), отличающаяся тем, что деамидирование молекул антител ингибируется.
(17) Композиция по (1)-(13), которая предназначена для подкожного введения.
(18) Композиция по (1)-(13), которая не подвергалась лиофилизации во время приготовления этой композиции.
(19) Способ ингибирования деамидирования молекул антитела в жидкой композиции, содержащей антитело, предусматривающий добавление аргинина к этой жидкой композиции.
(20) Способ ингибирования димеризации молекул антитела в жидкой композиции, содержащей антитело, предусматривающий добавление аргинина и метионина к этой жидкой композиции.
ПРЕИМУЩЕСТВА ИЗОБРЕТЕНИЯ
Посредством данного изобретения обеспечена жидкая композиция, содержащая высокую концентрацию антитела, с которой повторное приготовление концентрированием при помощи лиофилизации не является необходимым, и, следовательно, она не требует воссоздания. Антителосодержащая жидкая композиция по данному изобретению может храниться в жидком состоянии в течение продолжительного времени. Поскольку антителосодержащая жидкая композиция по данному изобретению может быть получена при помощи процесса, не включающего в себя стадию лиофилизации, добавление сахара или т.п. в качестве криопротективного агента не является необходимым.
КРАТКОЕ ОПИСАНИЕ ФИГУР
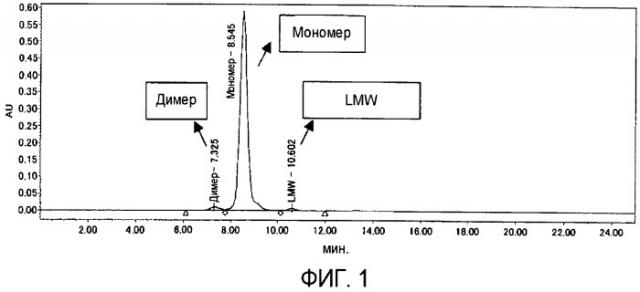
Фиг.1 показывает типичную хроматограмму примера 1.
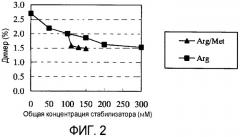
Фиг.2 показывает результаты оценивания гель-проникающей (гель-фильтрационной) хроматографии (SEC) в примере 1.
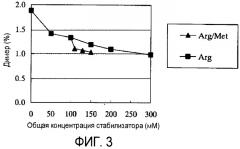
Фиг.3 показывает результаты оценивания гель-проникающей (гель-фильтрационной) хроматографии (SEC) в примере 1.
Фиг.4 показывает типичную хроматограмму примера 2.
Фиг.5 показывает оценивание результатов ионообменной хроматографии (IEC) в примере 2.
Фиг.6 показывает оценивание результатов ионообменной хроматографии (IEC) в примере 2.
Фиг.7 показывает результаты оценивания гель-проникающей (гель-фильтрационной) хроматографии (SEC) в примере 3.
Фиг.8 показывает оценивание результатов ионообменной хроматографии (IEC) в примере 3.
НАИЛУЧШИЙ СПОСОБ ПРОВЕДЕНИЯ ИЗОБРЕТЕНИЯ
Теперь данное изобретение будет описано подробно.
В данном изобретении "антителосодержащая жидкая композиция" обозначает жидкую композицию, содержащую антитело в качестве активного компонента, которую готовят таким образом, что она может вводиться животному, такому как человек, и которую предпочтительно получают при помощи процесса, не включающего в себя стадии лиофилизации.
Эта антителосодержащая жидкая композиция согласно данному изобретению является жидкой фармацевтической композицией, содержащей антитело в высокой концентрации, которая предпочтительно имеет концентрацию антитела не менее 50 мг/мл, более предпочтительно не менее 100 мг/мл, еще более предпочтительно не менее 120 мг/мл и даже более предпочтительно не менее 150 мг/мл. Следует отметить, что жидкая композиция, содержащая антитело в концентрации 120 мг/мл или более или предпочтительно 150 мг/мл или более, не была разработана для коммерческого применения. А именно, авторы этого изобретения впервые предлагают применение жидкой композиции, содержащей антитело в этой высокой концентрации.
Кроме того, с учетом процесса приготовления наивысшая концентрация антител в жидкой композиции согласно данному изобретению может быть обычно равна 300 мг/мл, предпочтительно 250 мг/мл и более предпочтительно 200 мг/мл. Таким образом, антителосодержащая жидкая композиция по данному изобретению предпочтительно имеет концентрацию антитела 50-300 мг/мл, более предпочтительно 100-300 мг/мл, еще более предпочтительно 120-250 мг/мл и еще более предпочтительно 120-250 мг/мл и даже более предпочтительно 150-200 мг/мл.
Антитело для применения в данном изобретении не ограничивается, пока оно связывает желаемый антиген. Это антитело может быть либо поликлональным антителом, либо моноклональным антителом, хотя моноклональное антитело является предпочтительным, так как антитело, имеющее однородные свойства, может продуцироваться стабильно.
Моноклональное антитело, которое может быть использовано в данном изобретении, включает в себя не только моноклональные антитела, происходящие из животного, такого как человек, мышь, крыса, хомяк, кролик, овца, верблюд или обезьяна, но также включает в себя искусственно модифицированные рекомбинантные антитела, такие как химерное антитело, гуманизированное антитело и биспецифическое антитело. Класс иммуноглобулина этого антитела не ограничивается и может быть любым из классов, включающих в себя IgG, такие как IgG1, IgG2, IgG3 и IgG4, IgA, IgD, IgE и IgM. Среди этих классов предпочтительными являются IgG и IgM.
Антитело, которое может быть использовано в данном изобретении, включает в себя не только полные антитела, но также фрагменты антител, такие как Fv, Fab и F(ab)2; и низкомолекулярные антитела, такие как одноцепочечный Fv (scFv, sc(Fv)2, диатела, такие как димер scFv), имеющие одну или несколько специфичностей, получаемых связыванием вариабельных районов антитела через линкер, такой как пептидный линкер.
Вышеописанные антитела, которые могут быть использованы в данном изобретении, могут быть получены способами, хорошо известными квалифицированным в данной области специалистам.
Гибридома, продуцирующая моноклональное антитело, может быть получена следующим образом на основе использования известного способа. То есть гибридома может быть получена иммунизацией животного желаемым антигеном или клетками, экспрессирующими желаемый антиген, в качестве сенсибилизирующего антигена стандартным способом; слиянием полученных иммуноцитов с известными исходными клетками стандартным способом слияния клеток; и скринингом продуцирующей моноклональное антитело клетки (гибридомы) стандартным способом скрининга. Получение гибридомы может проводиться, например, при помощи способа Milstein et al (Kohler. G. and Milstein, C., Methods Enzymol. (1981) 73: 3-46). В случаях, когда иммуногенность этого антигена является низкой, этот антиген может быть связан с антигенной макромолекулой, такой как альбумин, и полученный конъюгат может быть использован в качестве иммуногена.
Могут быть использованы рекомбинантные антитела, которые получают способом генной инженерии, в котором из гибридомы клонируют ген антигена включением этого гена в подходящий вектор, введением этого вектора в хозяина и применением условий, заставляющих этого хозяина продуцировать это антитело (см., например, Carl, A. K. Borrebaeck, James, W. Larrick, THERAPEUTIC MONOCLONAL ANTIBODIES, Published in the United Kingdom by MACMILLAN PUBLISHERS LTD, 1990). Более конкретно, кДНК, кодирующую вариабельную область (V-область) в этом антителе, синтезируют из мРНК гибридомы с использованием обратной транскриптазы. Если получают ДНК, кодирующую V-область желаемого антитела, то эту ДНК затем лигируют с ДНК, кодирующей константную область (C-область) желаемого антитела, и полученную лигированную ДНК вводят в экспрессирующий вектор. Альтернативно, ДНК, кодирующая V-область этого антитела, может быть включена в экспрессирующий вектор, содержащий ДНК, кодирующий С-область этого антитела. Эту ДНК включают в экспрессирующий вектор таким образом, что эта ДНК экспрессируется под контролем регулирующего экспрессию района, такого как энхансер или промотор. Затем клетки-хозяева трансформируют полученным экспрессирующим вектором, и это антитело может экспрессироваться этими клетками-хозяевами.
В данном изобретении могут быть использованы рекомбинантные антитела, искусственно модифицированные для цели уменьшения гетероантигенности в отношении человека, такие как химерные антитела и гуманизированные антитела. Эти модифицированные антитела могут быть получены известными способами. Химерное антитело является антителом, содержащим вариабельные области тяжелой цепи и легкой цепи антитела животного, другого, чем человек, например, мыши, и константные области тяжелой цепи и легкой цепи антитела человека, и могут быть получены легированием ДНК, кодирующей вариабельную область в мышином антителе, с ДНК, кодирующей константную область в антителе человека, включением полученной ДНК в экспрессирующий вектор, введением этого экспрессирующего вектора в хозяина и применением условий, заставляющих этого хозяина продуцировать это антитело.
Гуманизированным антителом называют также реконструированное антитело человека, которое получают трансплантацией CDR (определяющего комплементарность района), например, антитела мыши, с определяющим комплементарность районом антитела человека. Стандартный способ генетической рекомбинации для получения гуманизированного антитела также известен. Конкретно, ДНК, сконструированную таким образом, что CDR антитела мыши и каркасная область (FR) антитела человека являются легированными, синтезируют при помощи ПЦР-способа из нескольких олигонуклеотидов, полученных таким образом, что они имеют перекрывающиеся области на их концах. Полученную ДНК легируют с ДНК, кодирующей константную область антитела человека, и полученную ДНК вводят в экспрессирующий вектор. Этот экспрессирующий вектор вводят в хозяина и этого хозяина заставляют продуцировать это гуманизированное антитело (см. EP 239400 A и WO 96/02576). Поскольку FR антитела человека подлежат легированию через CDR, выбирают антитело, определяющий комплементарность район которого образует хороший антигенсвязывающий сайт. При необходимости аминокислота (аминокислоты) в этом определяющем комплементарность районе могут быть заменены таким образом, что этот определяющий комплементарность район реконструированного антитела человека образует подходящий антигенсвязывающий сайт (Sato, K. et a1., Cancer Res. (1993) 53, 851-856).
Способы получения антитела человека известны в данной области. Например, желаемое антитело человека, имеющее связывающую активность в отношении желаемого антигена, может быть получено сенсибилизацией, in vitro, лимфоцитов человека желаемым антигеном или клетками, экспрессирующими желаемый антиген; слиянием сенсибилизированных лимфоцитов с клетками миеломы человека, например, клетками U266; и получением этого антитела из этих клеток (см. JP 1-59878 B). Желаемое антитело человека может быть также получено иммунизацией трансгенного животного, имеющего все репертуары (спектры) генов антител человека, антигеном (см. WO 93/12227, WO 92/03918, WO 94/02602, WO 94/25585, WO 96/34096 и WO 96/33735). Кроме того, известен также способ, при помощи которого антитело человека получают пэннингом с использованием библиотеки антител человека. Например, вариабельную область антитела из тела человека экспрессируют в форме одноцепочечного антитела (scFv) на поверхности фага с использованием способа фагового дисплея и отбирают фаг, который связывается с этим антигеном. Посредством анализа гена выбранного фага может быть определена ДНК-последовательность, кодирующая вариабельную область антитела человека, которая связывается с этим антигеном. Если ДНК-последовательность scFv, которая связывается с этим антигеном, определена, конструируют подходящий экспрессирующий вектор, содержащий эту последовательность, и может быть получено это гуманизированное антитело. Эти способы хорошо известны, и можно сослаться на WO 92/01047, WO 92/20791, WO 93/06213, WO 93/11236,WO 93/19172, WO 95/01438 и WO 95/15388.
В случаях, когда ген антитела является некогда выделенным и этот ген введен в подходящего хозяина для получения антитела, могут быть использованы подходящие комбинации хозяина и экспрессирующего вектора. В случаях использования эукариотических клеток в качестве хозяина могут быть использованы клетки животных, клетки растений и грибные клетки. Известные клетки животных включают в себя (1) клетки млекопитающих, например, CHO, COS, миеломы, BHK (почек детеныша хомячка), Hela и Vero; (2) клетки земноводных, например, ооциты Xenopus oocytes, и (3) клетки насекомых, например, sf9, sf21 и Tn5. Известные клетки растений включает в себя клетки, происходящие из растений, принадлежащих к роду Nicotiana, например, Nicotiana tabacum, и эти клетки могут быть подвергнуты культивированию в виде каллуса. Известные грибные клетки включают в себя клетки, происходящие из дрожжей, например, клетки, принадлежащие к роду Saccharomyces, например, Saccharomyces cerevisiae; и нитчатые бактерии, например, бактерии, принадлежащие к роду Aspergillus, например, Aspergillus niger. В случаях, когда используют прокариотические клетки, имеются продукционные системы, использующие бактериальные клетки. Известные бактериальные клетки включают в себя клетки E. coli и клетки Bacillus subtilis. Антитело получают введением желаемого гена антитела в эти клетки посредством трансформации и культивированием этих трансформированных клеток in vitro.
Антитела в форме фрагментов антител, низкомолекулярных антител и модифицированных антител могут быть также использованы в качестве антитела данного изобретения. Примеры фрагментов антител и антител с низкой молекулярной массой включают в себя Fab, F(ab')2, Fv и одноцепочечный Fv (scFv, sc(Fv)2 и т.п.), имеющие одну или несколько специфичностей, полученных легированием Fv в Н-цепи и L-цепи через подходящий линкер (Huston, J. S. et a1., Proc. Natl. Acad. Sci. U.S.A. (1988) 85, 5879-5883). Конкретно, антитело обрабатывают папаином или пепсином для генерирования фрагментов антител или конструируют ген, кодирующий эти фрагменты антител, и этот ген экспрессируют в подходящих клетках-хозяевах после введения этого гена в экспрессирующий вектор (см., например, Co, M. S. et a1., T. Immunol. (1994)152, 2968-2976; Better, M. and Horwitz, A. H., Methods Enzymol. (1989) 178, 476-496; Pluckthun, A. and Skerra, A., Methods Enzymol. (1989) 178, 497-515; Lamoyi, E., Methods Enzymol, (1986) 121, 652-663; Rousseaux, J. et a1., Methods Enzymol. (1986)121, 663-669; Bird, R. E. and Walker, B. W., Trends Biotechnol. (1991) 9, 132-137.
Антитела, связанные с различными молекулами, такими как полиэтиленгликоль (ПЭГ), также могут быть использованы в качестве модифицированных антител. Термин "антитело", используемый в данном изобретении, также может включать в себя модифицированные антитела. Эти модифицированные антитела могут быть получены химической модификацией полученного антитела. Способы проведения этих модификаций установлены в данной области.
Примеры антитела, содержащегося в композиции по данному изобретению, включают в себя, но не ограничиваются ими, антитела против тканевого фактора, антитела против рецептора IL-6, антитела к IL-6, моноклональные антитела против антигена HM1.24, антитела против родственного паратереоидному гормону пептида (анти-PTHrP-антитела), анти-глипикан-3-антитела, анти-ганглиозид GM3-антитела, антитела против антагониста рецептора TPO, заменяющие фактор VIII антитела, анти-CD3-антитела, анти-CD20-антитела, анти-GPIIb/IIIa-антитела, анти-TNF-антитела, анти-CD25-антитела, анти-EGFR-антитела, анти-Her2/neu-антитела, анти-RSV-антитела, анти-CD33-антитела, анти-CD52-антитела, анти-IgE-антитела, анти-CD11a-антитела, анти-VEGF-антитела, анти-VLA4-антитела, анти-AXL-антитела и т.д.
Предпочтительные примеры реконструированных антител человека, используемых в данном изобретении, включают в себя гуманизированные антитела против рецептора интерлейкина (IL-6) (hPM-1 или MRA) (см. WO 92-19759), гуманизированные моноклональные антитела против антигена HM1.24 (см. WO 98-14580), гуманизированные антитела против родственного паратиреоидному гормону пептида (анти-PTHrP-антитела) (см. WO 98-13388), гуманизированные антитела против тканевого фактора (см. WO 99-51743) и гуманизированные IgG1κ-антитела против глипикана-3 (см. PCT/JP05/013103). Гуманизированными антителами, особенно предпочтительными в данном изобретении, являются гуманизированные антитела против рецептора IL-6.
В качестве IgM-антител человека предпочтительными являются рекомбинантные IgM-антитела против ганглиозида (см. WO 05-05636) и т.п.
В качестве антител с низкой молекулярной массой предпочтительными являются диатела против антагониста рецептора ТРО (см. WO 02-33072), диатела против агониста CD47 (см. WO 01-66737) и т.п.
Для оценивания стабильности при хранении жидкой композиции, содержащей антитело высокой концентрации, авторы этого изобретения исследовали действия различных добавок проведением тестов теплового ускорения и тестов светового ускорения. В результате было обнаружено, что в растворах, в которых высокую концентрацию антитела растворяют в буферном растворе, содержащем аминокислоту аргинин, количество генерируемого димера было меньшим, чем это количество в растворах, в которые не добавляли аргинин. Из этих результатов было обнаружено, что аргинин является эффективным в качестве стабилизатора для ингибирования димеризации. Кроме того, в растворах, в которых высокую концентрацию антитела растворяли в буферном растворе, содержащем аргинин и метионин, наблюдали ингибирующее действие против димеризации при общей концентрации аргинина и метионина, которая была более низкой, чем концентрация только аргинина, необходимая для получения того же самого ингибирующего действия. На основании этих результатов было обнаружено, что посредством добавления аргинина и метионина вместе получают синергическое действие. Кроме того, было обнаружено, что деамидирование молекул антител ингибируется добавлением аргинина. Эти результаты приводятся в качестве примера тест-результатов, полученных для пробы, содержащей гуманизированное антитело против рецептора IL-6 при концентрации 180 мг/мл.
Таким образом, посредством добавления аргинина в качестве стабилизатора может быть обеспечена стабильная композиция антитела, в которой димеризация этого антитела уменьшается и амидирование этого антитела предотвращается. Таким образом, первый аспект данного изобретения характеризуется добавлением к раствору аргинина, посредством чего димеризация или деамидирование молекул антитела ингибируется в полученной антителосодержащей жидкой композиции. Таким образом, один вариант стабильной антителосодержащей жидкой композиции характеризуется тем, что он содержит антитело и аргинин в буферном растворе. Кроме того, как описано выше, антителосодержащая жидкая композиция данного изобретения может дополнительно содержать метионин в этом растворе, причем посредством применения аргинина и метионина в комбинации получают синергическое действие. Таким образом, второй аспект данного изобретения характеризуется добавлением аргинина и метионина к раствору, посредством чего димеризация, в частности молекул антитела, ингибируется в полученной антителосодержащей жидкой композиции. Таким образом, один вариант стабильной антителосодержащей жидкой композиции характеризуется тем, что он содержит антитело, аргинин и метионин в буферном растворе.
Что касается аргинина, используемого в данном изобретении, может быть использовано любое из соединений аргинина per se, его производных и его солей. Предпочтительными являются L-аргинин и его соли. Что касается метионина, используемого в данном изобретении, может быть использовано любое из соединений метионина per se, его производных и его солей. Предпочтительными являются L-метионин и его соли.
В случаях, когда антителосодержащая жидкая композиция по этому изобретению содержит аргинин и не содержит метионина, концентрация аргинина равна предпочтительно 50-1500 мМ, более предпочтительно 100-1000 мМ, еще более предпочтительно 200-700 мМ. В случаях, когда антителосодержащая жидкая композиция по этому изобретению содержит аргинин и метионин, общая концентрация аргинина и метионина равна предпочтительно 50-1200 мМ, например, предпочтительно концентрация аргинина равна 40-1000 мМ, а концентрация метионина равна 10-200 мМ, более предпочтительно концентрация аргинина равна 50-700 мМ, а концентрация метионина равна 10-100 мМ и еще более предпочтительно концентрация аргинина равна 100-300 мМ, а концентрация метионина равна 10-50 мМ.
Буферный раствор готовят с использованием буферящего агента, который является веществом для поддержания рН раствора. В жидкой композиции, содержащей антитело высокой концентрации согласно данному изобретению, рН этой композиции равен предпочтительно 4-8, более предпочтительно 5,0-7,5, еще более предпочтительно 5,5-7,2 и еще более предпочтительно 6,0-6,5. Буферящим агентом, который может быть использован в данном изобретении, является агент, который может корректировать рН в этом диапазоне и который является фармацевтически приемлемым. Такой буферный агент известен квалифицированным в данной области специалистам, и его примеры включают в себя неорганические соли, такие как соли фосфорной кислоты (натрия или калия), ацетат натрия и сукцинат натрия; и кислоты, такие как фосфорная кислота, угольная кислота, лимонная кислота, янтарная кислота, яблочная кислота и глюконовая кислота. Кроме того, могут быть также использованы трис-буферы, буферы Гуда, такие как MES, MOPS и HEPES, гистидин (например, соль хлористоводородной кислоты и гистидина) и глицин. В жидкой композиции, содержащей антитело высокой концентрации согласно данному изобретению, этим буфером является предпочтительно гистидиновый буфер или глициновый буфер и особенно предпочтительным является гистидиновый буфер. Концентрация этого буферного раствора равна обычно 1-500 мМ, предпочтительно 5-100 мМ, еще более предпочтительно 10-20 мМ. В случаях, когда используют гистидиновый буфер, этот буферный раствор содержит гистидин в концентрации предпочтительно 5-25 мМ, более предпочтительно 10-20 мМ.
Для "стабильной" содержащей антитело высокой концентрации жидкой композиции согласно данному изобретению, значимое изменение не наблюдается при хранении ее при температуре холодильника (2оС-8°C) в течение по меньшей мере 12 месяцев, предпочтительно в течение 2 лет и более предпочтительно в течение 3 лет; или при хранении при комнатной температуре (22оС-28°C) в течение по меньшей мере 3 месяцев, предпочтительно 6 месяцев и более предпочтительно 1 года. Например, суммарное количество димеров и продуктов деградации в этой композиции при ее хранении при 5оС в течение 2 лет составляет 5,0% или менее, предпочтительно 2% или менее и более предпочтительно 1,5% или менее; или суммарное количество димеров и продуктов деградации в этой композиции при ее хранении при 2оС в течение 6 месяцев составляет 5,0% или менее, предпочтительно 2% или менее и более предпочтительно 1,5% или менее.
Композиция согласно данному изобретению может дополнительно содержать поверхностно-активное вещество.
Типичные примеры поверхностно-активного вещества включают в себя неионогенные поверхностно-активные вещества, например, эфиры сорбитана и жирных кислот, такие как монокаприлат сорбитана, монолаурат сорбитана и монопальмитат сорбитана; эфиры глицерина и жирных кислот, такие как монокаприлат глицерина, мономиристат глицерина и моностеарат глицерина; эфиры полиглицерина и жирных кислот, такие как декаглицерилмоностеарат, декаглицерилдистеарат и декаглицерилмонолинолеат; жирные эфиры полиоксиэтиленсорбитана и жирных кислот, такие как монолаурат полиоксиэтиленсорбитана, моноолеат полиоксиэтиленсорбитана, моностеарат полиоксиэтиленсорбитана, монопальмитат полиоксиэтиленсорбитана, триолеат полиоксиэтиленсорбитана и тристеарат полиоксиэтиленсорбитана; эфиры полиоксиэтиленсорбита и жирных кислот, такие как тетрастеарат полиоксиэтиленсорбита и олеат полиоксиэтиленсорбита; эфиры полиоксиэтиленглицерина и жирных кислот, такие как моностеарат полиоксиэтиленглицерина; эфиры полиэтиленгликоля и жирных кислот, такие как дистеарат полиэтиленгликоля; алкиловые эфиры полиоксиэтилена, такие как простой лауриловый эфир полиоксиэтилена; простые алкиловые эфиры полиоксиэтиленполиоксипропилена, такие как простой гликолевый эфир полиоксиэтилена-полиоксипропилена, простой пропиловый эфир полиоксиэтилена-полиоксипропилена и цетиловый эфир полиоксиэтилена-полиоксипропилена; простые фениловые эфиры полиоксиэтилена, такие как простой нонилфениловый эфир полиоксиэтилена; полиоксиэтилированные отвержденные касторовые масла, такие как полиоксиэтилированное отвержденное касторовое масло и полиоксиэтилированное отвержденное касторовое масло (полиоксиэтилированное гидрогенизированное касторовое масло); полиоксиэтилированные производные пчелиного воска, такие как полиоксиэтиленсорбит-пчелиный воск; производные полиоксиэтиленланолина, такие как полиоксиэтиленланолин; поверхностно-активные вещества, имеющие HLB 6-18, такие как амиды полиоксиэтилена и жирных кислот, например, полиоксиэтиленоктадеканамид; анионогенные поверхностно-активные вещества, например, алкилсульфатные соли, имеющие C10-C18 алкильную группу, такие как цетилсульфат натрия, лаурилсульфат натрия и олеилсульфат натрия; алкилсульфатные соли полиоксиэтилена, в которых среднее число молей добавленных этиленоксидных единиц равно 2-4 и число атомов углерода алкильной группы равно 10-18, такие как полиоксиэтиленлаурилсульфат натрия; соли алкилсульфосукцината, имеющие C8-C18 алкильную группу, такие как лаурилсульфосукцинат натрия; природные поверхностно-активные вещества, такие как лецитин и глицерофосфолипиды; сфингофосфолипиды, такие как сфингомиелин; и эфиры сахарозы и C12-C18 жирных кислот. Эти поверхностно-активные вещества могут быть добавлены к композиции данного изобретения по отдельности, или два или более этих поверхностно-активных веществ могут быть добавлены в комбинации.
Предпочтительными поверхностно-активными веществами являются алкиловые эфиры полиоксиэтилена-полиоксипропилена, и особенно предпочтительными являются полисорбаты 20, 21, 40, 60, 65, 80, 81 и 85 и поверхностно-активные вещества Плюроникового типа, и наиболее предпочтительными являются полисорбаты 20 и 80 и Плюроник F-68 (Полоксамер 188).
Количество поверхностно-активного вещества (поверхностно-активных веществ), которое может быть добавлено к композиции антител в соответствии с данным изобретением, обычно равно 0,0001-10% (м/о), предпочтительно 0,001-5%, более предпочтительно 0,005-3%.
В другом аспекте данного изобретения композиция в соответствии с данным изобретением предпочтительно состоит в основном из следующих компонентов:
A) антитела против рецептора IL-6;
B) аргинина и/или метионина и дополнительной другой аминокислоты (дополнительных других аминокислот) (например, триптофана) в качестве необязательного дополнительного компонента (необязательных дополнительных компонентов);
C) буферящего агента (буферящих агентов); и
D) поверхностно-активного вещества (поверхностно-активных веществ).
Термин "состоит в основном из" обозначает здесь, что компонент, другой, чем компоненты, обычно добавляемые к композициям, не содержатся, причем эти компоненты, обычно добавляемые к композициям, являются необязательными дополнительными компонентами, описанными ниже, такими как суспендирующие агенты, солюбилизирующие агенты, изотонические агенты, консерванты, ингибиторы адсорбции, разбавители, носители, корректоры рН, смягчающие (успокаивающие) агенты, серосодержащие восстанавливающие агенты и антиоксиданты.
Вышеописанные "B) аргинин и/или метионин, и дополнительная другая аминокислота (дополнительные другие аминокислоты) (например, триптофан) в качестве необязательного дополнительного компонента (необязательных дополнительных компонентов)" предназначены для включения случаев, в которых эта композиция содержит (b-1) аргинин; (b-2) аргинин и метионин; и (b-3) метионин, соответственно, в качестве аминокислотной добавки (аминокислотных добавок), и дополнительно включает в себя случаи, в которых эта композиция дополнительно содержит другую аминокислоту (другие аминокислоты). Что касается триптофана, могут быть использованы любые соединения триптофана per se, его производные и его соли. Предпочтительными являются L-триптофан и его соли.
При необходимости, к композиции согласно этому изобретению могут быть добавлены суспендирующий агент, солюбилизирующий агент, изотонический агент, консервант, ингибитор адсорбции, разбавитель, носитель, корректор рН, смягчающий (успокаивающий) агент, серосодержащий восстанавливающий агент, антиоксидант и т.п.
Примеры суспендирующего агента включают в себя метилцеллюлозу, полисорбат 80, гидроксиэтилцеллюлозу, аравийскую камедь, порошкообразный трагакант, натрий-карбоксиметилцеллюлозу и монолаурат полиоксиэтиленсорбитана.
Примеры солюбилизирующего агента включают в себя полиоксиэтилированное гидрогенизированное касторовое масло, полисорбат 80, никотинамид, монолаурат полиоксиэтиленсорбитан, макрогол и этиловый эфир жирной кислоты касторового масла.
Примеры изотонического агента включают в себя хлорид натрия, хлорид калия и хлорид кальция.
Примеры консерванта включают в себя метил-п-гидроксибензоат, этил-п-гидроксибензоат, сорбиновую кислоту, фенол, крезол и хлоркрезол.
Примеры ингибитора адсорбции включают в себя сывороточный альбумин человека, лецитин, декстран, сополимер этиленоксида и пропиленоксида, гидроксипропилцеллюлозу, метилцеллюлозу, полиоксиэтилированное гидрогенизированное касторовое масло и полиэтиленгликоль.
Примеры серосодержащего восстанавливающего агента включают в себя соединения, имеющие сульфгидрильную группу (сульфгидрильные группы), такие как N-ацетилцистеин, N-ацетилгомоцистеин, тиоктовую кислоту, тиодигликоль, тиоэтаноламин, тиоглицерин, тиосорбит, тиогликолевую кислоту и их соли, тиосульфат натрия, глутатион и C1-C7 тиоалканы.
Примеры антиоксиданта включают в себя эриторбовую кислоту, дибутилгидрокситолуол, бутилированный гидроксианизол, α-токоферол, L-аскорбиновую кислоту и ее соли, L-аскорбилпальмитат, L-аскорбилстеарат, гидросульфит натрия, сульфит натрия, триамилгаллат, пропилгаллат и хелатообразующие агенты, такие как динатрий-этилендиаминтетраацетат (ЭДТА), пирофосфат натрия и метафосфат натрия.
Антителосодержащую жидкую композицию согласно этому изобретению обычно вводят парентеральным способом, например, инъекцией (подкожной, внутривенной, внутримышечной инъекциями или т.п.), чрескожным, трансмукозным, трансназальным или легочным введением, но она может также вводиться перорально. В случае подкожной инъекции доза антитела на одно введение является большой (приблизительно 100-200 мг), тогда как количество инъекционного раствора является ограниченным, так что композиция по этому изобретению особенно пригодна для подкожной инъекции.
Коэффициент осмотического давления антителосодержащей жидкой композиции согласно этому изобретению равен предпочтительно приблизительно 0,5-4, более предпочтительно приблизительно 0,7-2 и еще более предпочтительно приблизительно 1.
Вязкость антителосодержащей жидкой композиции согласно этому изобретению равна предпочтительно приблизительно 2-15 мПа·с, более предпочтительно приблизительно 4-10 мПа·с. Следует отметить, что описанную здесь вязкость измеряют способом ротационного вискозиметра с использованием плоскоконического вискозиметра в соответствии с 2.53 Viscosity Determination/General Tests, the Japanese Pharmacopoeia, 15th edition.
Как может быть видно из результатов описанных ниже примеров, согласно данному изобретению, может быть получена стабильная жидкая композиция, в ко