Макроциклические индольные производные, применимые в качестве ингибиторов вируса гепатита с
Иллюстрации
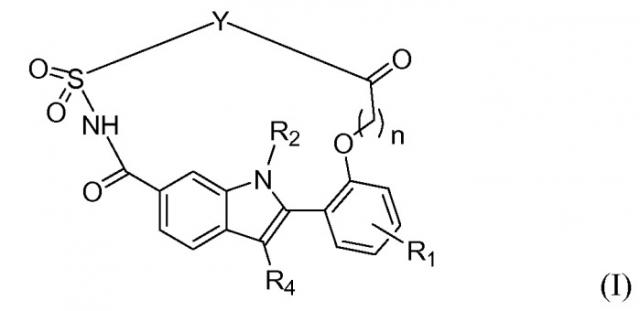
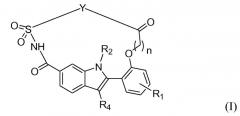
Показать всеИзобретение относится к соединению формулы (I)
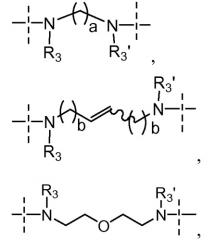
включая его стереохимически изомерные формы, гидраты и сольваты, где R1 выбран из атома водорода, атома галогена и C1-4-алкокси; R2 выбран из C1-4-алкила и C3-6-циклоалкила; R4 представляет собой C3-7-циклоалкил; n равно 1; Y выбран из
И
a равно 4 или 5; R3 и R3' - независимо выбраны из атома водорода и C1-6-алкила. Изобретение также относится к противовирусной фармацевтической композиции на основе указанного соединения формулы (I). Технический результат: получены новые соединения и фармацевтические композиции на их основе, которые могут найти применение в медицине в терапии HCV. 3 н. и 9 з.п. ф-лы, 3 табл., 15 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к макроциклическим индольным производным, обладающим ингибиторной активностью в отношении репликации вируса гепатита C (HCV). Изобретение дополнительно относится к композициям, содержащим такие соединения в качестве активных ингредиентов, а также к способам получения таких соединений и композиций.
Уровень техники
Вирус гепатита C во всем мире является основной причиной хронического заболевания печени и стал центром внимания значительного числа медицинских исследований. HCV является членом семейства вирусов Flaviviridae рода hepacivirus и близко связан с родом flavivirus, который включает ряд вирусов, вовлеченных в заболевания человека, таких как вирус денге и вирус желтой лихорадки, и с семейством пестивирусов (pestivirus) животных, которое включает вирус бычьей вирусной диареи (BVDV). HCV представляет собой положительно-смысловой одноцепочечный РНК-вирус с геномом приблизительно из 9600 оснований. Геном содержит как 5', так и 3' нетранслируемые области, которые принимают вторичные структуры РНК, и центральную открытую рамку считывания, которая кодирует единственный полипротеин, состоящий приблизительно из 3010-3030 аминокислот. Полипротеин кодирует десять генных продуктов, которые генерируются из предшественника полипротеина посредством серии сочетающихся со- и пост-трансляционных эндопротеолитических расщеплений, опосредованных с помощью протеаз как хозяина, так и вируса. Структурные белки вируса включают ядерный нуклеокапсидный белок и два обрамляющих гликопротеина Е1 и Е2. Неструктурные (NS) белки кодируют некоторые неотъемлемые вирусные ферментативные функции (геликаза, полимераза, протеаза), а также белки с неизвестными функциями. Репликация вирусного генома опосредована РНК-зависимой РНК-полимеразой, кодируемой неструктурным белком 5b (NS5B). Было показано, что в дополнение к полимеразе функции как вирусной геликазы, так и протеазы, кодируемые в бифункциональном белке NS3, являются существенными для репликации РНК HCV. Помимо серинпротеазы NS3 HCV также кодирует металлопротеиназу в области NS2.
Репликация HCV предпочтительно протекает в гепатоцитах, но не является непосредственно цитопатической, приводя к персистирующей инфекции. В частности, оказалось, что недостаток сильной ответной реакции Т-лимфоцитов и высокая склонность вируса к мутации промотируют высокую скорость хронической инфекции. Существует 6 основных генотипов HCV и более 50 подтипов, которые географически распределены различным образом. HCV типа 1 является доминирующим генотипом в США и Европе. Например, HCV типа 1 насчитывает от 70 до 75 процентов всех инфекций HCV в США. Большая генетическая гетерогенность HCV имеет важные диагностические и клинические последствия, возможно, объясняя трудности в разработке вакцин и недостаточную ответную реакцию на лечение. Как оценивается, 170 миллионов человек во всем мире инфицировано вирусом гепатита С. После первоначальной острой инфекции у большинства инфицированных индивидуумов развивается хронический гепатит, который может прогрессировать в фиброз печени, приводящий к циррозу - конечной стадии заболевания печени, и HCC (гепатоклеточной карциноме) (National Institutes of Health Consensus Development Conference Statement: Management of Hepatitis C. Hepatology, 36, 5 Suppl. S3-S20, 2002). Цирроз печени, возникший вследствие инфекции HCV, является ответственным приблизительно за 10000 смертей в год только в США и является основной причиной для трансплантаций печени. Передача HCV может происходить за счет контакта с зараженной кровью и продуктами крови, например, после переливания крови или внутривенного применения лекарственных средств (наркотиков). Введение диагностических тестов, применяемых при скрининге крови, привело к нисходящей тенденции случаев HCV после переливания крови. Однако учитывая медленное развитие заболевания печени до конечной стадии, существующие инфекции будут продолжать оставаться серьезной медицинской и экономической проблемой на протяжении десятилетий (Kim W.R., Hepatology, 36, 5 Suppl. S30-S34, 2002).
Существующие в настоящее время способы терапии HCV основаны на (пегилированном) интерфероне-альфа (IFN-α) в сочетании с рибавирином. Такая комбинированная терапия приводит к устойчивому вирусологическому ответу более чем у 40% пациентов, инфицированных вирусами генотипа 1, и приблизительно у 80% пациентов, инфицированных генотипами 2 и 3. Наряду с ограниченной эффективностью в отношении вируса HCV типа 1, комбинированная терапия имеет существенные побочные эффекты и плохо переносится большинством пациентов. Например, в зарегистрированных исследованиях пегилированного интерферона и рибавирина заметные побочные эффекты приводили к приостановке лечения у приблизительно от 10 до 14 процентов пациентов. Основные побочные эффекты при комбинированной терапии включают гриппоподобные симптомы, гематологические аномалии и нейропсихиатрические симптомы. Разработка более эффективных, удобных и легче переносимых способов лечения является важной задачей общественного здравоохранения. Таким образом, лечение данного хронического заболевания является неудовлетворенной клинической потребностью, поскольку существующая в настоящее время терапия является эффективной только частично и ограничена нежелательными побочными эффектами.
Одной из областей особого внимания является поиск ингибиторов NS5b РНК-зависимой РНК-полимеразы (RdRp). В неинфицированной клетке-хозяине не существует близких структурных гомологов данной полимеразы, и обнаружение ингибиторов упомянутой полимеразы могло бы обеспечить более специфический способ воздействия. Ингибиторы, которые в настоящее время находятся на стадии исследования, можно отнести к категории либо нуклеозидных ингибиторов (NI), либо ненуклеозидных ингибиторов (NNI). Ингибиторы NI конкурируют непосредственно с нуклеотидными субстратами за связывание с высококонсервативными активными участками. Более высокой специфичности можно достичь с помощью ингибиторов NNI, которые могут взаимодействовать обычно только со структурно родственными полимеразами за пределами высококонсервативного активного участка на специфическом аллостерическом участке.
Описаны индольные производные с ингибиторной активностью в отношении HCV. В патентной заявке WO 2007/092000 описаны тетрациклические индольные производные в качестве ингибиторов NS5B HCV для лечения и/или профилактики инфицирования вирусом HCV. В заявке США 2008/0146537 описаны циклопропильные конденсированные индолобензазепиновые ингибиторы NS5B HCV. В патентной заявке WO 2008/075103 описаны макроциклические индольные производные, применимые для лечения или профилактики инфицирования вирусом гепатита C.
В настоящее время предварительные клинические исследования закончились высоким количеством неудач, тем самым привлекая внимание к необходимости заниматься поиском новых ингибиторов NS5b. Существует высокая медицинская потребность в надежном и эффективном противовирусном (HCV) лечении. Такие ингибиторы HCV могут преодолевать недостатки существующей в настоящее время терапии HCV, такие как побочные эффекты, ограниченная эффективность, возникновение резистентности и нарушения комплаентности, а также повышать устойчивый вирусологический ответ. В частности, когда терапевтические соединения обладают хорошей биодоступностью и благоприятным фармакокинетическим и метаболическим профилем.
Сущность изобретения
Было обнаружено, что некоторые макроциклические индольные производные проявляют противовирусную активность в отношении субъектов, инфицированных HCV, с полезными свойствами, относящимися к одному или нескольким из следующих параметров: противовирусная эффективность, благоприятный мутантный статус, отсутствие токсичности, благоприятный фармакокинетический и метаболический профиль, легкость получения и введения препарата. Следовательно, такие соединения применимы для лечения инфекций HCV или борьбы с ними.
Настоящее изобретение относится к ингибиторам репликации HCV, которые можно представить в виде формулы (I),
включая стереохимически изомерные формы, и солям, гидратам и сольватам,
где R1 выбран из атома водорода, атома галогена и C1-4-алкокси;
R2 выбран из C1-4-алкила и C3-6-циклоалкила;
R4 представляет собой C3-7-циклоалкил, необязательно замещенный атомом галогена; - n равно 1 или 2;
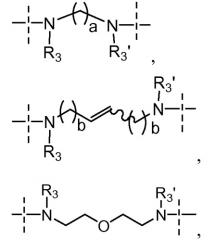
Y выбран из
и
- a равно 2, 3, 4 или 5;
- каждый b независимо равен 1 или 2;
- R3 и R3' независимо выбраны из атома водорода, C1-6-алкила и C3-6-циклоалкила.
Изобретение дополнительно относится к способам получения соединений формулы (I), включая их стереохимически изомерные формы, и солей, гидратов или сольватов, их промежуточных продуктов и применению промежуточных продуктов для получения соединений формулы (I).
Изобретение относится к соединениям формулы (I) как таковым, включая их стереохимически изомерные формы, и солям, гидратам или сольватам для применения в качестве лекарственного препарата. Изобретение относится к соединениям формулы (I) как таковым, включая их стереохимически изомерные формы, и солям, гидратам или сольватам для лечения гепатита C. Изобретение дополнительно относится к фармацевтическим композициям, содержащим носитель и эффективное против вируса количество соединения формулы (I), которое здесь указано. Фармацевтические композиции могут содержать комбинации вышеупомянутых соединений с другими средствами против вируса HCV. Изобретение также относится к вышеупомянутым фармацевтическим композициям для введения субъекту, страдающему от инфекции HCV. Фармацевтические композиции могут дополнительно содержать комбинации вышеупомянутых соединений или фармацевтические композиции со средствами против ВИЧ. Поэтому изобретение также относится к вышеупомянутым фармацевтическим композициям для введения субъекту, страдающему от со-инфекции HCV/ВИЧ.
Изобретение также относится к применению соединения формулы (I), включая его стереохимически изомерные формы, или солей, гидратов или сольватов для получения лекарственного средства для ингибирования репликации HCV. Изобретение также относится к применению соединения формулы (I), включая его стереохимические изомерные формы, или солей, гидратов или сольватов для производства лекарственного препарата для профилактики или лечения состояний, ассоциированных с HCV. Изобретение также относится к способу ингибирования репликации HCV у теплокровного животного; упомянутый способ включает введение эффективного количества соединения формулы (I), включая его стереохимически изомерные формы, или солей, гидратов или сольватов. Изобретение также относится к способу профилактики или лечения состояний теплокровного животного, ассоциированных с HCV; упомянутый способ включает введение эффективного количества соединения формулы (I), включая его стереохимически изомерные формы, или солей, гидратов или сольватов. Изобретение дополнительно относится к способу профилактики или лечения со-инфекции HCV/ВИЧ у теплокровного животного; упомянутый способ включает введение эффективного количества соединения формулы (I), включая его стереохимически изомерные формы или солей, гидратов или сольватов.
Подробное описание изобретения
Теперь настоящее изобретение будет описано дополнительно. Далее более подробно описаны различные аспекты или варианты осуществления изобретения. Каждый аспект или вариант осуществления изобретения, описанный таким образом, может быть объединен с любым другим аспектом (аспектами) или вариантом (вариантами) осуществления изобретения, если ясно не указано обратное. В частности, любой признак, указанный в качестве предпочтительного или благоприятного, может быть объединен с любым другим признаком или признаками, указанными в качестве предпочтительных или благоприятных при формулировке конкретного варианта осуществления изобретения.
Если не указано иначе, употребляются следующие определения, применяемые ранее и в дальнейшем.
Для целей настоящего изобретения термины "субъект" или "инфицированный субъект" или "пациент" относятся к индивидууму, инфицированному HCV, который нуждается в лечении.
Термином "гало" или "галоген" характеризуется фтор, хлор, бром и иод.
Применяемый здесь термин "C1-4-алкил" в виде группы или части группы обозначает насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 4 атомов углерода, например, такие как метил, этил, проп-1-ил, проп-2-ил, бут-1-ил, бут-2-ил, изобутил, 2-метилпроп-1-ил; термин "C1-3-алкил" в виде группы или части группы обозначает насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 3 атомов углерода, например, такие как метил, этил, проп-1-ил, проп-2-ил. Термин "C1-6-алкил" охватывает C1-3-алкильные и C1-4-алкильные радикалы и их более высокие гомологи, содержащие 5 или 6 атомов углерода, например, такие как пент-1-ил, пент-2-ил, пент-3-ил, гекс-1-ил, гекс-2-ил, 2-метилбут-1-ил, 2-метилпент-1-ил, 2-этилбут-1-ил, 3-метилпент-2-ил и т.п. Среди C1-6-алкильных групп интерес представляет C1-4-алкил и C1-3-алкил.
Термин "C1-6-алкилен" в виде группы или части группы относится к C1-6-алкильным группам, которые являются двухвалентными, то есть с двумя одинарными связями для соединения с двумя другими группами. Неограничивающие примеры алкиленовых групп включают метилен, этилен, метилметилен, пропилен, этилэтилен, 1-метилэтилен и 1,2-диметилэтилен.
Термином "C3-7-циклоалкил" характеризуется циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Термином "C3-6-циклоалкил" обозначается циклопропил, циклобутил, циклопентил и циклогексил. Термином "C3-5-циклоалкил" обозначается циклопропил, циклобутил и циклопентил.
Термин "C1-4-алкокси" или "C1-4-алкилокси" в виде группы или части группы относится к радикалу, содержащему формулу -ORa, в которой Ra представляет собой C1-4-алкил, который определен выше. Неограничивающие примеры подходящей C1-4-алкоксигруппы включают метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси.
Следует отметить, что места расположения радикала на любом молекулярном фрагменте, применяемом в определениях, могут находиться на таком фрагменте где угодно, при условии, что он является химически стабильным.
Радикалы, применяемые в определениях переменных, включают все возможные изомеры, если не указано иначе. Например, пиперидинил включает пиперидин-1-ил, пиперидин-2-ил, пиперидин-3-ил и пиперидин-4-ил; пентил включает пент-1-ил, пент-2-ил и пент-3-ил. Когда любая переменная встречается в любом элементе более одного раза, каждое определение является независимым.
Во всех применяемых далее случаях термин "соединения формулы (I)" или "настоящие соединения" или подобные термины означают, что в них включены соединения формулы (I), включая их стереохимически изомерные формы, и соли, гидраты или сольваты. Один из вариантов осуществления изобретения включает соединения формулы (I) или любую указанную здесь подгруппу, включая возможные стереохимически изомерные формы, а также соли, гидраты и сольваты. Еще один вариант осуществления включает соединения формулы (I) или любые указанные здесь подгруппы, включая возможные стереохимически изомерные формы, а также их соли, гидраты и сольваты.
Во всех применяемых далее случаях термин "необязательно замещенный" означает, что в него включены незамещенные, а также замещенные, по меньшей мере, одним из указанных замещающих радикалы. В качестве примера, "C1-4-алкил, необязательно замещенный атомом хлора", означает, что включен незамещенный C1-4-алкил, а также C1-4-алкил, замещенный атомом хлора.
Соединения формулы (I) могут содержать один или несколько центров хиральности и могут существовать в виде стереохимически изомерных форм. Термин "стереохимически изомерные формы" в применяемом здесь значении означает все возможные соединения, состоящие из одинаковых атомов, связанных одинаковой последовательностью связей, но имеющих разные трехмерные структуры, которыми могут обладать соединения формулы (I).
Что касается примеров, где (R) или (S) применяется для обозначения абсолютной конфигурации хирального атома в заместителе, обозначение относится к рассмотрению всего соединения в целом, а не к заместителю в отдельности.
В одном из аспектов настоящее изобретение относится к соединениям формулы (I)
включая стереохимически изомерные формы, и их N-оксидам, солям, гидратам и сольватам, в которой Y, R1, R2, R4 и n имеют такие же значения, которые здесь указаны.
Конкретные подгруппы соединений формулы (I) представляют собой соединения формулы (II), (III), (IV), (V), (VI) и (VII)
и
где Y, R1, R2, R3, R3', R4, a и n имеют те же самые значения, которые указаны для соединений формулы (I) или независимо для любого из вариантов их осуществления, который указан здесь.
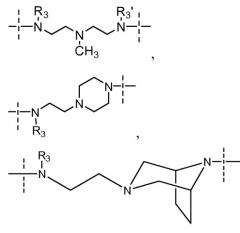
Когда Y соответствует формуле
или ,
понятно, что Y может быть ориентирован в двух направлениях, то есть пиперазинильный или 3,8-диазабицикло[3.2.1]октановый фрагмент может быть соединен с сульфонамидной группой, в то время как алифатический амин соединяется с карбонильной группой, или пиперазинильный или 3,8-диазабицикло[3.2.1]октановый фрагмент соединен с карбонильной группой, а алифатический амин соединен с сульфонамидной группой.
Варианты осуществления настоящего изобретения относятся к соединениям формулы (I) или любой их конкретной подгруппы, которая здесь указана, для которых применяется одно или несколько следующих ограничений:
- Y выбран из -N(R3)-(CH2)4-N(R3)-
и
- Y выбран из -N(R3)-(CH2)а-N(R3)-, где а равно 4 или 5
и
- Y выбран из -N(CH3)-(CH2)4-N(CH3)-
и
- Y выбран из
и
в которой пиперазиновый фрагмент соединен с карбонилом, а алифатический амин - с сульфонилом;
- Y выбран из -N(R3)-(CH2)5-N(R3)- и
- Y представляет собой
- Y представляет собой
в которой пиперазиновый фрагмент соединен с карбонилом, а алифатический амин - с сульфонилом;
- Y содержит цепь длиной в 7 атомов;
- R3 и R3' независимо выбраны из группы, состоящей из атома водорода, метила, этила, изопропила и циклопропила;
- R3 и R3' независимо выбраны из группы, состоящей из атома водорода и метила;
- R3 и R3' представляют собой метил;
- R1 выбран из группы, содержащей атом водорода, атом хлора, атом фтора или метокси;
- R1 представляет собой атом водорода или метокси или атом фтора;
- R1 представляет собой атом водорода;
- R1 расположен на бензольном кольце в мета- или пара-положении относительно связи, соединяющей бензольную группу с индольной группой;
- R1 расположен на бензольном кольце в пара-положении относительно связи, соединяющей бензольную группу с индольной группой;
- R2 выбран из метила, этила, изопропила, циклопентила и циклопропила;
- R2 представляет собой метил или изопропил;
- R2 представляет собой метил;
- R4 выбран из циклопентила, циклогексила и фторциклогексила, в частности 2-фторциклогексила;
- R4 представляет собой циклогексил;
- n равно 1;
- a равно 4 или 5;
В еще одном конкретном варианте осуществления изобретения, когда Y может представлять собой
или
пиперазинильный или 3,8-диазабицикло[3.2.1]октановый фрагмент соединен с карбонильной группой, а алифатический амин соединен с сульфонамидной группой.
В одном из вариантов осуществления изобретение относится к соединениям, независимо, формул (II), (III), (IV), (V), (VI) или (VII), в которых R4 представляет собой циклогексил или 2-фторциклогексил.
В еще одном варианте осуществления изобретение относится к соединениям формул (II), (III), (IV), (V), (VI) или (VII), в которых R1 представляет собой атом водорода, метокси, атом хлора или атом фтора.
В еще одном варианте осуществления изобретение относится к соединениям формул (II), (III), (IV), (V), (VI) или (VII), в которых R2 представляет собой метил, этил или изопропил.
В еще одном варианте осуществления изобретение относится к соединениям формул (II), (III), (IV), (V), (VI) или (VII), в которых n равно 1.
В конкретном варианте осуществления изобретение относится к соединениям формулы (I), выбранным из группы, содержащей:
и
включая стереохимически изомерные формы, и солям, сольватам или гидратам.
Если не упоминается или не указано иначе, химическое обозначение соединения охватывает смесь нескольких или всех возможных стереохимически изомерных форм, которыми упомянутое соединение могло бы обладать. Упомянутая смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры упомянутого соединения. Подразумевается, что в объем настоящего изобретения включены все стереохимически изомерные формы соединений по настоящему изобретению как в чистой форме, так и в смеси друг с другом.
Чистые стереоизомерные формы соединений и промежуточных продуктов, которые упоминаются здесь, определяются как изомеры, по существу не содержащие других энантиомерных или диастереомерных форм той же основной молекулярной структуры упомянутых соединений или промежуточных продуктов. В частности, термин "стереоизомерно чистые" относится к соединениям или промежуточным продуктам, содержащим, по меньшей мере, 80%-ный избыток стереоизомера (то есть с минимальным содержанием 90% одного возможного изомера и максимальным содержанием 10% других возможных изомеров) до 100%-ного избытка (то есть 100% содержание одного изомера и отсутствие других); более предпочтительно - к соединениям или промежуточным продуктам со стереоизомерным избытком в диапазоне от 90% до 100%; еще более предпочтительно - со стереоизомерным избытком в диапазоне от 94% до 100%, и наиболее предпочтительно - со стереоизомерным избытком в диапазоне от 97% до 100%. Термины "энантиомерно чистые" и "диастереомерно чистые" следует понимать аналогичным образом, но в отношении энантиомерного избытка и диастереомерного избытка рассматриваемой смеси соответственно.
Чистые стереоизомерные формы соединений и промежуточных продуктов по данному изобретению можно получать с помощью процедур, известных в данной области техники. Например, энантиомеры могут быть отделены друг от друга с помощью селективной кристаллизации их диастереомерных солей с оптически активными кислотами или основаниями. Примерами таких кислот являются винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота и камфосульфоновая кислота. Альтернативно энантиомеры можно разделять хроматографическими способами с применением хиральных неподвижных фаз. Упомянутые стереохимически чистые изомерные формы также можно получать из соответствующих стереохимически чистых изомерных форм подходящих исходных материалов, при условии, что осуществляется стереоспецифическая реакция. В частности, если требуется конкретный стереоизомер, упомянутое соединение синтезируют с помощью стереоспецифических способов получения. При таких способах преимущественно будут использоваться энантиомерно чистые исходные материалы.
Диастереомерные рацематы соединений формулы (I) или любой их подгруппы можно получать по отдельности с помощью традиционных способов. Подходящие физические способы разделения, которые можно предпочтительно использовать, например, представляют собой селективную кристаллизацию и хроматографию, например, колоночную хроматографию.
Абсолютную стереохимическую конфигурацию некоторых соединений формулы (I), их N-оксидов, солей, гидратов или сольватов и промежуточных продуктов, применяемых при их получении, экспериментально не определяли. Специалист в данной области техники способен определить абсолютную конфигурацию таких соединений с применением способов, известных в данной области техники, например, таких как рентгеновская дифракция.
Однако те соединения формулы (I), в химической структуре которых отсутствует хиральный или стереогенный центр, могут иметь преимущество, связанное с облегчением задачи их синтеза в промышленном масштабе и/или повышением экономической эффективности синтеза.
Конкретными подгруппами соединений формулы (I) являются соединения формулы (IA) и (IB).
Соединения формулы (IA) и (IB) являются изомерами, и в зависимости от длины двухвалентного линкера Y и R2 (например, когда R2 представляет собой изопропил) соединения формулы (IA) и (IB) могут не находиться в равновесии, но находиться в соответствующей "заторможенной" конформации, то есть быть стабильными в своих соответствующих конформациях. Конформация соединений формулы (I), например (IA) или (IB), влияет на характеристики соединений, в том числе на их метаболическую стабильность, фармакокинетическую и биологическую активности.
Конкретными вариантами осуществления соединений формулы (IA) и (IB) являются соединения формулы (IA-I) и (IB-I).
Также подразумевается, что настоящее изобретение включает все изотопы атомов, встречающихся в настоящих соединениях. Изотопы включают такие атомы, имеющие одинаковый атомный номер, но различные масс.вес. В качестве общего примера и без ограничения изотопы водорода включают тритий и дейтерий. Изотопы углерода включают C-13 и C-14.
Соли соединений формулы (I), предназначенные для терапевтического применения, представляют собой те соли, в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые являются фармацевтически неприемлемыми, также могут находить применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, являются ли они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения.
Подразумевается, что упомянутые выше фармацевтически приемлемые соли кислот и оснований содержат терапевтически активные нетоксичные формы аддитивных солей кислот и оснований, которые способны образовывать соединения формулы (I). Фармацевтически приемлемые аддитивные соли кислот можно удобно получать путем обработки основной формы такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например хлористоводородную или бромистоводородную кислоту, серную, азотную, фосфорную и тому подобные кислоты; или органические кислоты, например, такие как уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая (то есть этандионовая), малоновая, янтарная (то есть бутандионовая кислота), малеиновая, фумаровая, яблочная (то есть гидроксибутандионовая кислота), винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и тому подобные кислоты.
С другой стороны, упомянутые солевые формы могут быть превращены в форму свободного основания при обработке подходящим основанием.
Соединения формулы (I) или любой их подгруппы, содержащие кислотный протон, также могут превращаться в форму нетоксичных основно-аддитивных солей металлов или форму аминных солей при обработке подходящими органическими и неорганическими основаниями. Подходящие основные солевые формы включают, например, аммониевые соли, соли щелочных и щелочноземельных металлов, например, соли лития, натрия, калия, магния, кальция и т.п.; соли с органическими основаниями, например, бензатином, N-метил-D-глюкамином, гидрабаминовые соли и соли с аминокислотами, например, такими как аргинин, лизин и т.п.
N-оксидные формы настоящих соединений представляют собой соединения формулы (I) или любой их подгруппы, в которых один или несколько атомов азота окислены до так называемого N-оксида. Обычно такие N-оксиды могут образовываться после введения соединения формулы (I) субъекту и метаболизирования в организме. Альтернативно такие N-оксиды могут быть химически синтезированы с применением способов, известных в данной области техники.
Некоторые из соединений формулы (I) или любой их подгруппы и промежуточные продукты также могут существовать в одной или нескольких таутомерных формах. Хотя в упомянутой выше формуле такие формы не указаны в явной форме, подразумевается, что они включены в объем настоящего изобретения. Соответственно, соединения и промежуточные продукты могут присутствовать в виде смеси таутомеров или в виде индивидуального таутомера.
В изобретении особенное предпочтение отдается соединениям формулы I или любой их подгруппы, которые в описанных ниже анализах ингибирования имеют значение ингибирующей концентрации менее 100 мкМ, в частности менее 50 мкМ, более точно менее 10 мкМ, в частности, менее 5 мкМ, еще более точно менее 1 мкМ, предпочтительно менее 100 нМ, и в частности, менее 50 нМ, как определено данными соответствующего анализа, такого как анализы, применяемые ниже в разделе "Примеры".
Следует понимать, что в настоящем документе подразумевается, что указанные выше подгруппы соединений формулы (I), а также любая другая указанная здесь подгруппа включает стереохимически изомерные формы и любые соли, гидраты и сольваты таких соединений.
Получение соединений формулы (I)
Общие схемы синтеза
Соединения формулы (I) могут быть получены согласно различным способам B, C, D, E, F, описанным ниже, из индольных производных A-6, синтезированных согласно описанному здесь способу A
в которой R1, R2, R4, n имеют значения, указанные для соединений формулы (I) или их подгрупп; Ra выбран из метила и трет-бутила, и Rb выбран из метила или трет-бутила. Синтез A-I описан в патентной заявке WO 2003/010140A2, публикации Journal of Medicinal Chemistry 2005, т. 48(5), стр. 1314-1317 и в патентной заявке WO 2006/029912Al.
Способ A
Схема 1
Соединения формулы A-3 можно получать с помощью реакции кросс-сочетания по Сузуки между соединениями A-I, содержащими заместитель R4 и сложноэфирную метильную или трет-бутильную группу, и производным бороновой кислоты A-2, содержащим заместитель R1 и гидроксил, защищенный подходящей защитной группой PG1, такой как бензильная группа. Кроме того, подходящие защитные группы, которые можно применять, перечислены, например, в публикациях: Greene, "Protective Groups in Organic Chemistry", John Wiley & Sons, New York (1999) и "The Peptides: Analysis, Synthesis, Biology", т. 3, Academic Press, New York (1987). Указанную реакцию можно осуществлять в присутствии палладиевого катализатора, такого как диCl-бис(трифенилфосфино)-Pd(II), и основания, такого как карбонат калия, в подходящем растворителе, таком как смесь диметоксиэтан/вода или толуол/этанол/вода, в инертной атмосфере.
Соединения A-4 можно получать алкилированием соединений A-3, с применением алкилгалогенидного производного, например метилиодида в присутствии основания, такого как гидрид натрия, карбонат калия, карбонат цезия и т.п., в присутствии подходящего растворителя, такого как ДМФА, ТГФ, ацетонитрил и т.п. Соединения A-5 можно получать путем удаления с фенольной группы защитной группы PG1 с помощью способов, известных в данной области техники. Подходящие способы снятия применяемой защиты PG1 описаны в публикациях: Greene, "Protective Groups in Organic Chemistry", John Wiley & Sons, New York (1999) и "The Peptides: Analysis, Synthesis, Biology ", т. 3, Academic Press, New York (1987). Например, бензильную защитную группу можно удалять с помощью каталитического гидрирования с применением палладиевого катализатора в подходящем растворителе, таком как метанол.
Соединения A-6 можно получать с помощью реакции алкилирования фенола с применением, например, галогенацетатного производного формулы X-CH2-CO-O-Rb, в которой X представляет собой галоген. Реакцию алкилирования можно осуществлять в присутствии основания, такого как карбонат калия, карбонат цезия и т.п., в подходящем растворителе, таком как ДМФА, ТГФ, ацетонитрил и т.п. Заместитель Rb может представлять собой метил, когда Ra представляет собой метил или трет-бутил, или трет-бутил, когда Ra представляет собой метил.
Способ B
Схематическое описание синтеза соединений формулы (I) приведено на схеме 2. Способ основывается на соединении формулы A-6.
Соединения формулы B-I можно получать региоселективным гидролизом сложного эфира, содержащего группу Rb. Для тех соединений A-6, в которых Rb представляет собой метильную группу, и Ra представляет собой трет-бутильную группу или метильную группу, региоселективный гидролиз Rb-сложного эфира можно осуществлять в основных условиях с применением гидроксида, такого как LiOH или NaOH, в полярных растворителях, таких как вода, спирт, такой как метанол или этанол, тетрагидрофуран (ТГФ) или в их смеси. Альтернативно, когда Rb представляет собой трет-бутильную группу, региоселективный гидролиз сложного эфира, содержащего группу Rb, можно осуществлять в кислотных условиях с применением, например, TFA в подходящем растворителе типа DCM.
Монозащищенный бифункциональный Y, полученный из реагента формулы PG2-Y-H, в которой Y имеет значение, указанное для формулы (I) или ее подгруппы, затем можно связывать с группой карбоновой кислоты в соединениях B-I для образования амидной связи, приводя к соединениям B-2. "PG2" в применяемом здесь значении представляет собой подходящую аминозащитную группу, выбранную из групп, известных в данной области техники. Подходящие защитные группы, которые можно применять в качестве защитной группы PG2, перечислены, например, в публикации: Greene, "Protective Groups in Organic Chemistry", John Wiley & Sons, New York (1999). В частности, PG2 представляет собой трет-бутилоксикарбонильную (Boc) защитную группу или 2-нитробензолсульфонильную (нозил) группу.
Образование амидных связей можно осуществлять с применением стандартных процедур, таких как процедуры, применяемые для связывания аминокислот в пептидном синтезе. Такое связывание подразумевает дегидратирующее связывание карбоксильной группы одного реагента с аминогруппой другого реагента с образованием соединяющей амидной связи. Образование амидной связи можно осуществлять путем взаимодействия исходных материалов в присутствии конде