N1/n2-лактамные ингибиторы ацетил-коа-карбоксилаз
Иллюстрации
Показать всеИзобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, где G представляет собой группу формулы (II) или (III), R1 представляет собой изопропил или трет-бутил; R2 представляет собой нафтил, хинолинил или изохинолинил, R2 возможно замещен независимо одной-двумя группами метил, метокси или хлоро; R3 представляет собой водород. Также изобретение относится к фармацевтической композиции, содержащей соединение формулы (I). Технический результат - соединения формулы (I) в качестве ингибиторов ацетил-КоА-карбоксилаз(ы). 2 н. и 4 з.п. ф-лы, 10 ил., 7 табл., 125 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к замещенным соединениям пиразолоспирокетонов, действующим в качестве ингибиторов ацетил-КоА-карбоксилаз(ы), и их применению в лечении заболеваний, состояний или расстройств, модулируемых посредством ингибирования фермента(ов) ацетил-КоА-карбоксилаз(ы).
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Ацетил-КоА-карбоксилазы (АСС) представляют собой семейство ферментов, катализирующих получение малонил-КоА из ацетил-КоА, которые обнаружены у большинства видов и ассоциированы с синтезом и метаболизмом жирных кислот. У млекопитающих идентифицированы две изоформы фермента АСС. АСС1, уровни экспрессии которой высоки в липогенных тканях, таких как жировая и печеночная ткани, регулирует первую осуществляемую стадию в биосинтезе длинноцепочечных жирных кислот. Если ацетил-КоА не карбоксилируется с образованием малонил-КоА, он метаболизируется через цикл Кребса. АСС2, минорный компонент АСС в печени, но преобладающая изоформа в сердечной и скелетной мышце, катализирует образование малонил-КоА у цитозольной поверхности митохондрий и посредством этого регулирует утилизацию жирных кислот при β-окислении, ингибируя карнитин-пальмитоил трансферазу. Таким образом, непрерывное введение ингибитора АСС (ACC-I), повышая степень утилизации жирных кислот и предотвращая усиление синтеза жирных кислот de novo, также может опустошить депо триглицеридов (TG) в печеночной и жировой ткани у тучных субъектов посредством потребления пищи с высоким или низким содержанием жиров, что приводит к избирательному уменьшению содержания жира в организме.
Согласно исследованиям, проведенным Abu-Etheiga и др., можно предположить, что АСС2 играет существенную роль в регуляции окисления жирных кислот и, по существу, может представлять собой мишень в терапии ожирения и ассоциированных с ожирением заболеваний, таких как диабет 2 типа. См. Abu-Etheiga L., et al., ″Acetyl-CoA carboxylase 2 mutant mice are protected against obesity and diabetes induced by high-fat/high-carbohydrate diets″, PNAS, 100 (18), 10207-10212 (2003). См. также Choi C.S., et al., ″Continuous fat oxidation in acetyl-CoA carboxylase 2 knockout mice increases total energy expenditure, reduces fat mass, and improves insulin sensitivity″, PNAS, 104 (42), 16480-16485 (2007).
Становится все более очевидно, что накопление липидов в печени вызывает печеночную инсулинорезистентность и вносит вклад в патогенез диабета 2 типа. Salvage и др. продемонстрировали, что оба фермента АСС1 и АСС2 вовлечены в регуляцию окисления жиров в гепатоцитах, в то время как АСС1, доминантная изоформа в печени крыс, представляет собой единственный регулятор синтеза жирных кислот. Кроме того, согласно их модели одновременное уменьшение содержания обеих изоформ необходимо, чтобы существенно снизить уровни малонил-КоА в печени, усилить окисление жиров в состоянии сытости, уменьшить накопление липидов и улучшить действие инсулина in vivo. Таким образом, это указывает на то, что ингибиторы печеночных АСС1 и АСС2 могут быть полезны в лечении неалкогольной жировой болезни печени (NAFLD) и печеночной инсулинорезистентности. См. Savage D.B. et al., ″Reversal of diet-induced hepatic steatosis and hepatic insulin resistance by antisense oligonucleotide inhibitors of acetyl-CoA carboxylases 1 and 2″, J. Clin. Invest. doi: 10.1172/JCI27300. См. также Oh W. et al., ″Glucose and fat metabolism in adipose tissue of acetyl-CoA carboxylase 2 knockout mice″, PNAS, 102 (5), 1384-1389 (2005).
Таким образом, существует необходимость в лекарственных средствах, содержащих ингибиторы АСС1 и/или АСС2, для лечения ожирения и ассоциированных с ожирением заболеваний (таких как NAFLD и диабет 2 типа) посредством ингибирования синтеза жирных кислот и посредством усиления окисления жирных кислот.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям, имеющим структуру формулы (I),
где G представляет собой
или ,
R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил; R2 представляет собой фенил, нафтил, 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси, галогено и CONH2; и R3 представляет собой водород или (С1-С3)алкил; или их фармацевтически приемлемой соли.
Предпочтительным воплощением настоящего изобретения являются соединения формулы (I), где R1 представляет собой изопропил или трет-бутил; или их фармацевтически приемлемые соли.
Другим предпочтительным воплощением настоящего изобретения являются соединения формулы (I), где R2 представляет собой бензоимидазолил, пирролопиридинил, пиразолопиридинил, индазолил, хинолинил или изохинолинил, причем указанный R2 возможно моно- или дизамещен независимо одним-двумя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси и галогено; или их фармацевтически приемлемая соль. Еще одним другим предпочтительным воплощением настоящего изобретения являются соединения формулы (I), где R2 представляет собой индазолил, бензоимидазолил или 1H-пирроло[3,2-b]пиридинил, причем указанный R2 возможно замещен одной-двумя группами метил, метокси или хлоро; или их фармацевтически приемлемые соли.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1'-изопропил-1-(2-метил-1Н-бензо[d]имидазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(2-метил-2Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(1Н-пирроло[2,3-b]пиридин-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1'-изопропил-1-(1Н-пирроло[3,2-b]пиридин-6-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-c]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1'-изопропил-1-(1-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(4,8-диметоксихинолин-2-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(1Н-пирроло[3,2-b]пиридин-2-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1'-изопропил-1-(1Н-пиразоло[4,3-b]пиридин-6-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-c]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1-(3,7-диметил-1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(7-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-трет-бутил-1-(1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-трет-бутил-1-(7-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1'-трет-бутил-1-(3,7-диметил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1-(7-хлор-1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(4-метокси-1Н-индазол-6-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(7-этил-1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3-этил-1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1'-изопропил-1-(3-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1-(1Н-индазол-5-карбонил)-2'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; 2'-трет-бутил-1-(1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; 2'-изопропил-1-(7-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; 1-(3,7-диметил-1Н-индазол-5-карбонил)-2'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; 2'-трет-бутил-1-(7-метил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; 2'-трет-бутил-1-(3,7-диметил-1Н-индазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она и 2'-изопропил-1-(2-метил-1Н-бензо[d]имидазол-5-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(2'Н)-она; или его фармацевтически приемлемая соль.
Другим предпочтительным воплощением настоящего изобретения является соединение, выбранное из 1'-изопропил-1-(хинолин-3-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(хинолин-6-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(изохинолин-6-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1'-изопропил-1-(изохинолин-7-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1'-изопропил-1-(хинолин-7-карбонил)-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другим воплощением настоящего изобретения является соединение формулы (I),
или его фармацевтически приемлемая соль; где
G представляет собой
,,
или ;
R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил; R2 представляет собой фенил; нафтил; 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С6)алкила, (С3-С7)циклоалкила, (С1-С6)алкокси, галогено, циано, CONR4R5, NR4R5 или 3-7-членного гетероциклила, где указанные (С1-С6)алкил, (С3-С7)циклоалкил или (С1-С6)алкокси возможно замещены 1-5 группами фторо; R3 представляет собой водород или (С1-С3)алкил; и R4 и R5 в каждом случае независимо выбраны из водорода, (С1-С6)алкила, (С3-С7)циклоалкила, (С1-С3)алкокси-(С1-С6)алкила или 3-7-членного гетероциклила; где указанные (С1-С6)алкил, (С3-С7)циклоалкил или (С1-С3)алкокси-(С1-С6)алкил возможно замещены 1-5 группами фторо.
Еще одним воплощением настоящего изобретения является соединение формулы (I), где G представляет собой
или ; и
R1 представляет собой изопропил или трет-бутил; или его фармацевтически приемлемая соль.
Другим воплощением настоящего изобретения является соединение формулы (I), где R2 представляет собой бензоимидазолил, бензотриазолил, пирролопиридинил, пиразолопиридинил, индолил, индазолил, хинолинил или изохинолинил, причем указанный R2 возможно замещен одним-двумя заместителями, независимо выбранными из (С1-С6)алкила, (С1-С6)алкокси, галогено или NR4R5, где указанные (С1-С6)алкил или (С1-С6)алкокси возможно замещен 1-5 группами фторо; или его фармацевтически приемлемая соль.
Другим воплощением настоящего изобретения является соединение формулы (I), где R2 представляет собой индазолил, индолил, бензоимидазолил или 1H-пирроло[3,2-b]пиридинил, причем указанный R2 возможно замещен независимо одной-двумя группами метил, метокси, NH2, NHCH3 или хлоро; или его фармацевтически приемлемая соль.
Еще одним воплощением настоящего изобретения является соединение формулы (I), где R2 представляет собой хинолинил или изохинолинил, причем указанный R2 возможно замещен независимо одной-двумя группами метил, метокси, NH2, NHCH3, NHCH2CH3, NHCH2CF3 или хлоро; или его фармацевтически приемлемая соль.
Предпочтительным воплощением настоящего изобретения является соединение, выбранное из группы, состоящей из 1-(3,7-диметил-1Н-индазол-5-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3,7-диметил-1Н-индазол-5-карбонил)-1'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3,7-диметил-1Н-индазол-5-карбонил)-2'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(6-метоксихинолин-3-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(1-метоксиизохинолин-7-карбонил)-2'-трет-бутит-4',6'-дигидро-спиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3-хлор-7-метил-1Н-индазол-5-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(2-метоксихинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(2-аминохинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(5-метоксихинолин-3-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(2-амино-1Н-бензо[d]имидазол-5-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(2-(метиламино)хинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро-[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(1-(метиламино)-изохинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3-хлор-1Н-индол-6-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(3-хлор-1Н-пирроло[3,2-b]пиридин-6-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(2-(метиламино)хинолин-7-карбонил)-1'-изопропил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; 1-(1-(2,2,2-трифторэтиламино)хинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она и 1-(1-(этиламино)изохинолин-7-карбонил)-2'-трет-бутил-4',6'-дигидроспиро[пиперидин-4,5'-пиразоло[3,4-с]пиридин]-7'(1'Н)-она; или его фармацевтически приемлемая соль.
Другой аспект настоящего изобретения относится к фармацевтической композиции, содержащей соединение формулы (I), описанное в любом из воплощений, или его фармацевтически приемлемую соль и фармацевтически приемлемый эксципиент, разбавитель или носитель. Предпочтительно, композиция содержит терапевтически эффективное количество соединения по настоящему изобретению. Композиция также может содержать по меньшей мере один дополнительный фармацевтический агент. Предпочтительные агенты включают антидиабетические средства и/или средства против ожирения.
В другом аспекте настоящее изобретение относится к способу лечения заболевания, состояния или расстройства, опосредованного ингибированием фермента(ов) ацетил-КоА-карбоксилаз(ы), у млекопитающего, включающему стадию введения млекопитающему, предпочтительно человеку, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли либо фармацевтической композиции на их основе.
Заболевания, расстройства или состояния, опосредованные ингибиторами ацетил-КоА-карбоксилаз, включают диабет II типа и диабет-ассоциированные заболевания, такие как неалкогольная жировая болезнь печени (NAFLD), печеночная инсулинорезистентность, гипергликемия, метаболический синдром, нарушенная толерантность к глюкозе, диабетическая нейропатия, диабетическая нефропатия, диабетическая ретинопатия, ожирение, дислипидемия, гипертензия, гиперинсулинемия и синдром инсулинорезистентности. Предпочтительные заболевания, расстройства или состояния включают диабет II типа, неалкогольную жировую болезнь печени (NAFLD), печеночную инсулинорезистентность, гипергликемию, нарушенную толерантность к глюкозе, ожирение и синдром инсулинорезистентности. Более предпочтительными являются диабет II типа, неалкогольная жировая болезнь печени (NAFLD), печеночная инсулинорезистентность, гипергликемия и ожирение. Наиболее предпочтительным заболеванием является диабет II типа.
Одно из предпочтительных воплощений относится к способу лечения (например, замедлению прогрессирования или задержке начала) диабета 2 типа и диабет-ассоциированных расстройств у животных, включающему стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли либо композиции на его основе.
Другое предпочтительное воплощение относится к способу лечения ожирения и ассоциированных с ожирением расстройств у животных, включающему стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли либо композиции на их основе.
Еще одно предпочтительное воплощение относится к способу лечения неалкогольной жировой болезни печени (NAFLD) или печеночной инсулинорезистентности у животных, включающему стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли либо композиции на его основе.
Соединения по настоящему изобретению могут быть введены в комбинации с другими фармацевтическими агентами (в частности, средствами против ожирения и антидиабетическими средствами, изложенными в данном описании ниже). Комбинированную терапию можно назначать с введением в виде (а) единой фармацевтической композиции, содержащей соединение по настоящему изобретению, по меньшей мере один дополнительный фармацевтический агент, изложенный в данном описании, и фармацевтически приемлемый эксципиент, разбавитель или носитель; или (б) двух отдельных фармацевтических композиций, содержащих (1) первую композицию, содержащую соединение по настоящему изобретению и фармацевтически приемлемый эксципиент, разбавитель или носитель, и (2) вторую композицию, содержащую по меньшей мере один дополнительный фармацевтический агент, изложенный в данном описании, и фармацевтически приемлемый эксципиент, разбавитель или носитель. Эти фармацевтические композиции можно вводить одновременно или последовательно и в любом порядке.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Фраза ″терапевтически эффективное количество″ означает количество соединения по настоящему изобретению или его фармацевтически приемлемой соли, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает начало одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании.
Термин ″животное″ относится к людям (мужского или женского пола), домашним животным (например, собакам, кошкам и лошадям), животным-источникам продовольствия, животным зоопарков, морским животным, птицам и другим подобным видам животных. Термин ″годные в пищу животные″ относится к животным-источникам продовольствия, таким как крупный рогатый скот, свиньи, овцы и домашняя птица.
Фраза ″фармацевтически приемлемый″ указывает на то, что данные вещество или композиция должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и/или млекопитающим, которого лечат им.
Термины ″подвергание лечению″, ″лечить″ или ″лечение″ включают как превентивное, т.е. профилактическое, так и паллиативное лечение.
Термин ″модулируемый″, или ″модулирование″, или ″модулируют(ет)″, как использовано в данном описании, если не указано иное, относится к ингибированию фермента(ов) ацетил-КоА-карбоксилаз(ы) (АСС) соединениями по настоящему изобретению.
Термин ″опосредуемый″, или ″опосредующий″, или ″опосредуют(ет)″, как использовано в данном описании, если не указано иное, относится к (1) лечению или предупреждению конкретного заболевания, состояния или расстройства, (2) ослаблению, улучшению или устранению одного или более симптомов конкретного заболевания, состояния или расстройства или (3) предупреждению или задержке начала одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании, посредством ингибирования фермента(ов) ацетил-КоА-карбоксилаз(ы) (АСС).
Термин ″соединения по настоящему изобретению″ (если конкретно не указано иное) относится к соединениям формулы (I) и любым фармацевтически приемлемым солям соединений, а также всем стереоизомерам (включая диастереоизомеры и энантиомеры), таутомерам, конформационным изомерам и меченным изотопами соединениям. Гидраты и сольваты соединений по настоящему изобретению рассматриваются как композиции по настоящему изобретению, в которых соединение ассоциировано с водой или растворителем, соответственно.
Термины ″(С1-С6)алкил″ и ″(С1-С3)алкил″ относятся к алкильным группам, содержащим конкретное количество атомов углерода от одного до шести или от одного до трех атомов углерода, соответственно, которые могут быть либо прямыми, либо разветвленными. Например, термин ″(С1-С3)алкил″ означает группу из одного-трех атомов углерода и включает в себя метил, этил, н-пропил и изопропил.
Термин ″(С3-С7)циклоалкил″ означает циклоалкильную группу из трех-семи атомов углерода и включает в себя циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Термин ″галогено″ означает фторо, хлоро, бромо или иодо. Термин ″(С6-С10)арил″ означает ароматическую карбоциклическую группу, состоящую из шести-десяти атомов углерода, такую как фенил или нафтил.
Термин ″5-12-членный гетероарил″ означает пяти-двенадцатичленную ароматическую группу, содержащую, по меньшей мере, один гетероатом, выбранный из азота, кислорода и серы. Как использовано в данном описании, место присоединения ″5-12-членной гетероарильной″ группы находится на атоме углерода этой группы. Группа ″5-12-членный гетероарил″ может быть бициклической. Предпочтительные воплощения бициклических гетероарилов включают, но не ограничиваются этим, радикалы следующих кольцевых систем:
Термин ″8-12-членный конденсированный гетероциклический арил″ означает 8-12-членную кольцевую систему, в которой неароматическое гетероциклическое кольцо конденсировано с арильным кольцом. Как использовано в данном описании, место присоединения ″8-12-членной конденсированной гетероциклической арильной″ группы находится на атоме углерода этой группы. Термин ″3-7-членный гетероциклил″ означает трех-семи-членное насыщенное кольцо, где от одного до трех атомов являются гетероатомами, независимо выбранными из азота, кислорода и серы. Примеры ″3-7-членных гетероциклических″ групп включают, но не ограничиваются этим, такие группы, как азиридинил, азетидинил, пирролидинил, пиперидинил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидро-2Н-пиранил, тетрагидро-2H-тиопиранил, пиперазинил, морфолинил и тиоморфолинил. Место присоединения ″3-7-членного гетероциклила″ может находиться на атоме углерода или азота, как будет целесообразно для конкретной группы.
В одном из воплощений соединение формулы I представляет собой N1-лактамное АСС-ингибирующее соединение, имеющее следующую структуру:
,
где R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил; R2 представляет собой фенил, нафтил, 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси, галогено и CONH2; и R3 представляет собой водород или (С1-С3)алкил; или его фармацевтически приемлемую соль.
В одном из воплощений соединение формулы I представляет собой N2-лактамное АСС-ингибирующее соединение, имеющее следующую структуру:
,
где R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил; R2 представляет собой фенил; нафтил; 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси, галогено и CONH2; и R3 представляет собой водород или (С1-С3)алкил; или его фармацевтически приемлемую соль.
Соединения по настоящему изобретению могут быть синтезированы с использованием путей синтеза, включающих аналогичные хорошо известным в области химии, в частности, в свете приведенного в данном изобретении описания. Как правило, исходные вещества доступны из коммерческих источников, таких как Aldrich Chemicals (Milwaukee, WI), или их легко получить, используя способы, хорошо известные специалистам в данной области (например, получить способами, в целом описанными в Louis F. Fieser and Mary Fieser, Reagents for Organic Synthesis, v.1-19, Wiley, New York (1967-1999 ed.) или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая приложения (также доступны через онлайн-базу данных Бейльштейна)).
В иллюстративных целях на приведенных ниже реакционных схемах представлены возможные пути синтеза соединений по настоящему изобретению, а также ключевых промежуточных соединений. Для более подробного описания отдельных реакционных стадий см. раздел Примеры, приведенный ниже. Специалистам в данной области техники будет очевидно, что для синтеза соединений по настоящему изобретению можно использовать другие пути синтеза. Несмотря на то, что на схемах приведены и ниже обсуждаются конкретные исходные вещества и реагенты, они легко могут быть заменены на другие исходные вещества и реагенты для обеспечения разнообразия производных и/или реакционных условий. Помимо этого, большинство соединений, полученных описанными ниже способами, могут быть модифицированы далее с учетом данного описания с использованием методов традиционной химии, хорошо известных специалистам в данной области.
При получении соединений по настоящему изобретению может потребоваться введение защиты функциональной группы (например, первичного или вторичного амина) в промежуточных соединениях. Необходимость в такой защите будет варьировать в зависимости от природы такой функциональной группы и условий осуществления способов получения. Подходящие амино-защитные группы (NH-Pg) включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Аналогично, ″гидроксил-защитная группа″ относится к заместителю группы гидрокси, который блокирует или защищает функциональную гидроксигруппу. Подходящие гидроксил-защитные группы (O-Pg) включают, например аллил, ацетил, силил, бензил, пара-метоксибензил, тритил и тому подобные. Необходимость в такой защите легко определяется специалистом в данной области. Для общего описания защитных групп и их использования см. Т.W. Greene, Protective Groups in Organic Synthesis. John Wiley & Sons, New York, 1991.
На следующих далее реакционных схемах, от реакционной схемы I до реакционной схемы V, приведены репрезентативные методики, которые используются для получения соединений формулы (I). Следует понимать, что эти реакционные схемы не должны истолковываться как ограничивающие и что для получения соединений формулы (I) можно использовать разумные варианты представленных способов.
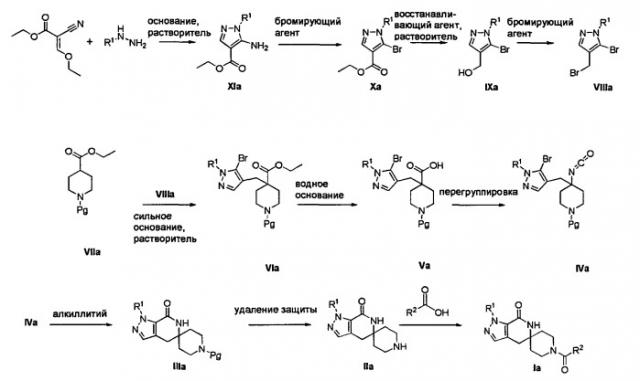
На реакционной схеме I приведены общие методики, которые могут быть использованы для получения N1-лактамных АСС-ингибирующих соединений по настоящему изобретению, имеющих формулу Ia, в которых R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил, и R2 представляет собой фенил, нафтил, 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси, галогено и CONH2.
РЕАКЦИОННАЯ СХЕМА 1
Согласно Схеме I соединение формулы XIa может быть образовано в результате приведения во взаимодействие метил-2-циано-3-этоксиакрилата с соответствующим алкилгидразином (R1NHNH2) в присутствии основания, такого как карбонат калия, и растворителя. Например, соединение формулы XIa может быть образовано в результате приведения во взаимодействие метил-2-циано-3-этоксиакрилата с соответствующим алкилгидразином (R1NHNH2) в присутствии основания, такого как карбонат калия (″К2СО3″), в этаноле с кипячением с обратным холодильником с получением желаемого циклизованного соединения, при температуре от примерно 20°С до примерно 80°С в течение примерно 2-24 часов.
Соединение формулы Xa может быть образовано в результате превращения ариламина формулы XIa в арилбромид с использованием нитрита, такого как изоамилнитрит, нитрит натрия или трет-бутилнитрит, и источника брома, такого как бромид меди(II) в ацетонитриле, с получением соединения формулы Xa, при температуре от примерно 20°С до примерно 80°С в течение от примерно 2 до примерно 18 часов.
Затем можно получить соединение формулы IXa путем обработки сложного эфира формулы Xa восстанавливающим агентом, таким как диизобутилалюминийгидрид (″DIBAL″) или алюмогидрид лития (″LAH″), в апротонном растворителе, таком как тетрагидрофуран (″THF″), толуол или диэтиловый эфир, при температуре от примерно 0°С до примерно 80°С в течение от примерно 1 до примерно 12 часов.
Соединение формулы VIa может быть образовано сначала в результате взаимодействия соединения формулы IXa с бромирующим агентом, таким как трибромид фосфора (″PBr3″) или смесь тетрабромида углерода и трифенилфосфина, при температуре от примерно -20°С до примерно 60°С в течение от примерно 30 до примерно 120 минут с образованием соединения формулы VIIIa. Затем соединение формулы VIIIa приводят во взаимодействие с защищенным производным пиперидина - соединением формулы VIIa в присутствии сильного основания, такого как бис(триметилсилил)амид лития (″LiHMDS″) или диизопропиламин лития (″LDA″), в апротонном растворителе, таком как THF, толуол или диэтиловый эфир, при температуре от примерно -78°С до примерно 20°С в течение от примерно 1 до примерно 18 часов. Группа Pg представляет собой соответствующую защитную группу амина и является предпочтительно N-трет-бутоксикарбонилом (″ВОС″) или карбобензилокси (″Cbz″).
Затем с соединения формулы VIa удаляют защиту путем гидролиза сложноэфирной группы в присутствии сильного водного основания, такого как гидроксид лития или гидроксид натрия, при температуре от примерно 0°С до примерно 100°С в течение от примерно 1 до примерно 18 часов с образованием содержащего группу карбоновой кислоты соединения формулы Va.
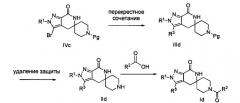
Затем может быть образовано изоцианатное соединение формулы IVa путем приведения во взаимодействие карбоновой кислоты формулы Va с дифенилфосфорилазидом (″DPPA″) в присутствии основания, такого как триэтиламин (″Et3N″) или диизопропилэтиламин, при температуре от примерно 60°С до примерно 120°С в течение от примерно 1 до примерно 12 часов.
Затем может быть образовано лактамное соединение формулы IIIa путем циклизации изоцианата (формула IVa) с использованием алкиллития, такого как н-бутиллитий (″н-BuLi″) или трет-бутиллитий (″f-BuLi″), при температуре от примерно -78°С до примерно 0°С в течение от примерно 5 до примерно 120 минут.
Затем с лактамного соединения формулы (IIIa) можно удалить защиту с получением свободного производного спиропиперидина формулы (IIa), используя стандартные методы в зависимости от того, какая защитная группа Pg была применена. Например, когда Pg представляет собой ВОС, то чтобы удалить группу ВОС, можно использовать стандартные условия удаления защиты с применением сильной кислоты, такой как 4 н соляная кислота в диоксане или трифторуксусная кислота в соответствующем растворителе, таком как дихлорметан. В том случае, когда Pg представляет собой Cbz, для удаления защиты можно использовать гидрирование над палладием на угле в этаноле или обработку с применением источника водорода, такого как формиат аммония или 1-метил-1,4-циклогексадиен в присутствии палладия на угле в этаноле или этилацетате.
Затем, чтобы получить соединение формулы (Ia), производное спиропиперидина формулы (IIa) можно подвергнуть ацилированию путем применения стандартных способов. Например, в таком случае соединение (Ia) может быть образовано с использованием стандартной реакции пептидного сочетания с желаемой карбоновой кислотой (R2CO2H). Например, сочетание промежуточного спиропиперидина (IIa) и карбоновой кислоты (R2CO2H) может быть осуществлено посредством образования активированного сложного эфира карбоновой кислоты, например, путем приведения в контакт карбоновой кислоты (R2CO2H) с реагентом пептидного сочетания, таким как гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (″HATU″) или гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (″EDC·HCl″), в присутствии или в отсутствие активирующего агента, такого как гидроксибензотриазол (″HOBt″), и в присутствии подходящего основания, такого как N,N-диизопропилэтиламин (″DIEA″), триэтиламин или N-метилморфолин (″NMM″), в подходящем растворителе, таком как THF и/или DMF (диметилформамид), диметилацетамид (″DMA″) или дихлорметан, и затем приведения в контакт этого активированного эфира карбоновой кислоты с производным спиропиперидина (IIa) с образованием соединения формулы (Ia).
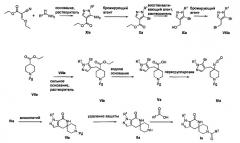
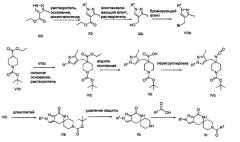
На реакционной схеме II приведены общие методики, которые могут быть использованы для получения N2-лактамных АСС-ингибирующих соединений по настоящему изобретению, имеющих формулу Ib, в которых R1 представляет собой (С1-С6)алкил или (С3-С5)циклоалкил, и R2 представляет собой фенил, нафтил, 5-12-членный гетероарил или 8-12-членный конденсированный гетероциклический арил; где каждая группа R2 возможно замещена одним-тремя заместителями, независимо выбранными из (С1-С3)алкила, (С1-С3)алкокси, галогено и CONH2.
РЕАКЦИОННАЯ СХЕМА II
Согласно Схеме II алкилирование соединения пиразола формулы XIb до соединения формулы Х с использованием первичного или вторичного алкилгалогенида, такого как метилиодид, этилиодид, 1-бромпропан, 1-иодпропан, 2-бромпропан, 2-иодпропан, 1-иодбутан, 2-иодбутан, 1-иод-2-метилпропан или 1-(бромметил)циклопропан, может быть осуществлено в присутствии основания, такого как карбонат цезия (″Cs2CO3″) или карбонат калия (″K2CO3″), и растворителя, такого как диметилформамид (″DMF″), при температуре от примерно 20°С до примерно 100°С в течение от примерно 1 до примерно 12 часов.
Затем можно получить соединение формулы IXb путем обработки соединения формулы Xb восстанавливающим агентом, таким как DIBAL или LAH, в апротонном растворителе, таком как THF, толуол или диэтиловый эфир, при температуре от примерно -78°С до примерно 60°С в течение от примерно 1 до примерно 12 часов.
Соединение формулы VIb может быть образовано сначала в результате взаимодействия соединения формулы IXb с бромирующим агентом, таким как PBr3 или смесь тетрабромида углерода и трифенилфосфина, при температуре от прим