Фосфорамидатные производные нуклеозидов
Иллюстрации
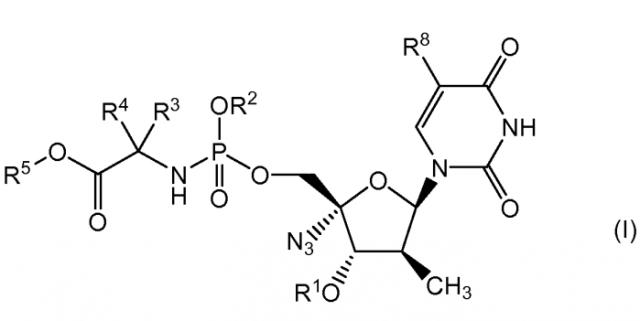
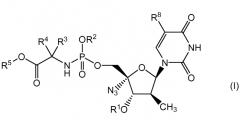
Показать всеИзобретение относится к соединениям для лечения гепатита С формулы I:
его стереоизомерным формам, фармацевтически приемлемым солям или сольватам, где R1 представляет собой водород; R2 представляет собой водород, нафтил или фенил, необязательно замещенный 1, 2 или 3 заместителями, выбранными из галогена и C1-C6алкила; R3 и R4 представляют собой водород или C1-C6алкил; R5 представляет собой C1-C10алкил, необязательно замещенный C1-C6алкоксигруппой, C3-C7циклоалкил или бензил; R8 представляет собой водород. Предложены новые эффективные против гепатита С соединения и композиции на их основе. 4 н. и 8 з.п. ф-лы, 4 пр., 1 табл.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к новым нуклеозидным соединениям, которые являются ингибиторами полимеразы вируса гепатита С (HCV), и к их применению при лечении или при профилактике HCV.
Предпосылки создания изобретения
HCV представляет собой одноцепочечный (+)РНК вирус с геномом, содержащим около 9600 оснований, принадлежащий к вирусному семейству Flaviviridae, к роду гепатовирусов. Фрагмент NS5B полигена РНК кодирует РНК-зависимую РНК-полимеразу (RdRp) с молекулярной массой 65 кДа, которая необходима для репликации вируса. Как последствие первоначальной острой инфекции, у большинства инфицированных пациентов развивается хронический гепатит из-за того, что происходит репликация HCV преимущественно в гепатоцитах, но без явного цитопатического проявления. В частности, недостаток интенсивного ответного действия Т-лимфоцитов и сильная предрасположенность вируса к мутации, по всей видимости, способствуют высокой скорости развития хронического инфекционного процесса. Хронический гепатит может развиваться в фиброз печени, приводящий к циррозу, конечной стадии заболевания печени, и в HCC (гепатоклеточную карциному), что делает его основной причиной необходимости трансплантации печени.
Существует шесть основных генотипов HCV и более 50 подтипов, которые географически по-разному распределены. HCV генотипа 1 представляет собой преобладающий генотип в Европе и США. Экстенсивная генетическая гетерогенность HCV обуславливает существенные осложнения при диагностике и изучении симптомов течения болезни, может служить объяснением трудностей в создании вакцины и недостаточную действенность существующей в настоящее время терапии.
Передача HCV может происходить при контакте с зараженной кровью или препаратами крови, например, вследствие переливания крови или внутривенного применения лекарственного препарата. Внедрение диагностических тестов, применяемых при скрининге крови, приводит к тенденции понижения числа случаев пост-инфузионного HCV. Несмотря на то, что обеспечивается медленное развитие конечной стадии заболевания печени, существующие инфекции будут представлять собой серьезную медицинскую проблему и экономическое бремя на десятилетия.
Существующая в настоящее время терапия HCV основывается на (пегилированном) интерфероне-альфа (IFN-α) в комбинации с рибавирином. Эта комбинированная терапия дает устойчивый вирусологический ответ у более чем 40% пациентов, инфицированных HCV генотипа 1, и, приблизительно, в 80% пациентов, инфицированных HCV генотипов 2 и 3. Кроме ограниченной эффективности против HCV генотипа 1, эта комбинированная терапия имеет существенные побочные эффекты и плохо переносима многими пациентами. Большинство побочных эффектов включают подобные гриппу симптомы, гематологические нарушения и психоневрологические симптомы. Следовательно, существует потребность в более эффективных, удобных и лучше переносимых методах лечения.
Опыт применения лекарственных средств против HIV, в частности ингибиторов HIV протеазы, указывает, что недостаточно оптимальная фармакокинетика и сложный режим дозировки незамедлительно приводят к неумышленным неудачам в соблюдении терапевтических рекомендаций. Это в свою очередь обозначает, что на 24 часу самая низшая точка концентрации (минимум концентрации в плазме) для соответствующих лекарственных средств при HIV состоянии часто опускается ниже IC90 или ED90 пороговой величины для большей части суток. Следует принять во внимание, что на 24 часу самый низший уровень значений, по крайней мере, для IC50, и более реально, для IC90 или ED90, весьма важен для сдерживания проявления «ускользнувших» от лекарственного средства мутантов. Достижение необходимой фармакокинетики и метаболизма лекарственного средства, которые обеспечивают такие самые низшие уровни значений, определяют точные перспективы создания лекарственного средства.
РНК-зависимая полимераза NS5B (RdRp) является существенной для репликации одноцепочечной, положительной смысловой РНК-геномной. Этот фермент вызывает особый интерес у специалистов в области медицинской химии. Известны как нуклеозидные, так и ненуклеозидные ингибиторы NS5B.
Нуклеозидные ингибиторы могут действовать или как терминатор цепи биосинтеза или как конкурентный ингибитор, который мешает связыванию нуклеотида с полимеразой. Чтобы функционировать в качестве терминатора цепи нуклеозидный аналог должен поглощаться клеткой и превращаться in vivo в трифосфат для соответствия сайту связывания нуклеотида с полимеразой. Это превращение в трифосфаты обычно осуществляется посредством клеточных киназ, которые привносят дополнительные структурные требования к потенциальному ингибитору нуклеозидной полимеразы. Кроме того, это ограничивает прямую оценку нуклеозидов в качестве ингибиторов репликации HCV при испытаниях на клетках, способных к фосфорилированию in situ.
Несколькими исследовательскими группами были предприняты усилия для выявления нуклеозидов, являющихся ингибиторами HCV полимеразы, но, несмотря на то, что для небольшого количества соединений начали проводить клинические испытания, ни одно соединение не прошло весь путь до регистрации. В числе проблем, из-за которых нуклеозиды, имеющие своей мишенью HCV, сталкиваются с трудностями их продвижения, представляются следующие: токсичность, мутагенность, отсутствие селективности, низкая эффективность, низкая биодоступность, недостаточно оптимальные режимы дозировки и получающиеся в результате большие масса таблетки и стоимость товара.
Ряд патентов и патентных заявок, а также и научных публикаций раскрывают аналоги нуклеозидов, обладающие ингибирующей активностью по отношению к HCV. WO 2007/020193 раскрывает фосфорамидатные производные определенных нуклеозидов. WO 2008/043704 раскрывает 4-амино-1-((2R,3S,4S,5R)-5-азидо-4-гидрокси-5-гидроксиметил-3-метил-тетрагидрофуран-2-ил)-1H-пиримидин-2-ин и его сложноэфирные производные в качестве ингибиторов полимеразы HCV. WO 2009/067409 раскрывает 2',4'-замещенные нуклеозиды в качестве противовирусных средств.
Существует потребность в ингибиторах HCV, которые могут преодолеть недостатки существующей в настоящее время терапии HCV, такие как побочные эффекты, ограниченная эффективность, возникновение устойчивости и неудачи из-за несоблюдения предписанного режима терапии, а также могут способствовать устойчивому вирусологическому ответу.
Настоящее изобретение касается фосфорамидатных производных 1-((2R,3S,4S,5R)-5-азидо-4-гидрокси-5-гидроксиметил-3-метил-тетрагидрофуран-2-ил)-1H-пиримидин-2,4-диона, которые являются ингибиторами HCV с полезными свойствами, касающимися одного или нескольких следующих параметров: противовирусная эффективность, благоприятный профиль развития устойчивости, отсутствие токсичности и генотоксичности, подходящие фармакокинетика и фармакодинамика, такие как повышенные концентрации моно- или трифосфатных аналогов в печени, повышенная абсорбция, в частности, адсорбция клетками печени, и простота получения препарата и введения.
Описание изобретения
В соответствии с настоящим изобретением, предложены ингибиторы полимеразы HCV, которые могут быть представлены формулой I:
включая любые возможные их стереоизомеры, где:
R1 представляет собой водород, -C(=О)R6 или -C(=О)CHR7-NH2;
R2 представляет собой водород; или C1-C6алкил или фенил, причем последний является необязательно замещенным 1, 2 или 3 заместителями, каждый из которых, независимо друг от друга, выбирают из галогена, C1-C6алкила, C2-C6алкенила, C1-C6алкокси, гидрокси- и аминогруппы; или R2 представляет собой нафтил; или R2 представляет собой индолил;
R3 представляет собой водород, C1-C6алкил, бензил;
R4 представляет собой водород, C1-C6алкил, бензил; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, образуют C3-C7циклоалкил;
R5 представляет собой C1-C10алкил, необязательно замещенный C1-C6алкоксигруппой; или R5 представляет собой C3-C7циклоалкил; бензил; или фенил, необязательно замещенный 1, 2 или 3 заместителями, каждый из которых, независимо друг от друга, выбирают из гидрокси-, C1-C6алкокси-, амино-, моно- и диC1-C6алкиламиногрупп;
R6 представляет собой C1-C6алкил;
R7 представляет собой C1-C6алкил;
R8 представляет собой водород или галоген;
или их фармацевтически приемлемая соль или сольват.
Дополнительная особенность изобретения заключается в предоставлении соединения формулы I или его фармацевтически приемлемой соли, гидрата или сольвата для применения при лечении или профилактике инфекции HCV. Или предлагается применение соединения формулы I или его фармацевтически приемлемой соли, гидрата или сольвата для производства лекарственного средства для лечения или профилактики инфекции HCV. Репрезентативные генотипы HCV в контексте лечения или профилактики, в соответствии с изобретением, включают генотип 1b (распространенный в Европе) или 1a (распространенный в Северной Америке). С другой точки зрения, изобретение предоставляет способ лечения или профилактики инфекции HCV, а именно генотипа 1a или 1b, указанный способ включает введение соединения в количестве, которое является эффективным для лечения HCV или для обеспечения профилактики против HCV.
Дополнительное описание изобретения
Одна подгруппа соединений включает соединения формулы I, или любые подгруппы соединений, указанных в этом документе, в которых R1 представляет собой водород. Другая подгруппа включает соединения формулы I, или любые подгруппы соединений, указанных в этом документе, в которых R1 представляет собой C2-C6 ацильную группу, такую как ацетил, пивалоил или, предпочтительно, изобутирил. Другая подгруппа включает соединения формулы I, или любые подгруппы соединений, указанных в этом документе, в которых R1 представляет собой α-аминоацильную группу, полученную из L-аминокислоты, такой как L-аланин, L-лейцин, L-изолейцин или L-валин.
Другая подгруппа соединений включает такие соединения формулы I или любые подгруппы соединений, указанных в этом документе, в которых R2 представляет собой фенил, необязательно замещенный 1, 2 или 3 заместителями, которые независимо друг от друга выбирают из галогена, C1-C6алкила и C2-C4алкенила, или в которых R2 представляет собой нафтил. Представляют интерес соединения формулы I или любые подгруппы соединений, указанных в этом документе, в которых R2 представляет собой фенил, нафтил или фенил, замещенный метилом, изопропилом и хлором, последний, более конкретно, представляет собой 3-метил-4-хлор-6-изопропилфенил. Другая подгруппа соединений включает соединения формулы I или любые подгруппы соединений, указанных в этом документе, в которых R2 представляет собой водород.
В соединениях формулы I, или в любых подгруппах соединений, указанных в этом документе, группа -NH-C(R3)(R4)-CO- образует аминокислотный остаток, который включает природные и неприродные аминокислотные остатки. Особый интерес представляют такие аминокислотные остатки, в которых R3 представляет собой водород. Если в последнем случае R4 отличается от водорода, тогда конфигурация ассиметрического атома углерода, связанного с R3 и R4, предпочтительно, такая как у L-аминокислоты. Примеры -NH-C(R3)(R4)-CO- представляют собой остатки глицина (Gly), аланина (Ala), 1,1-диметилглицина, валина (Val), изолейцина (Ile) и фенилаланина (Phe), а именно, их L-форму, такую как L-Ala, L-Val, L-Ile и L-Phe. Пример аминокислотного остатка, в котором R3 и R4 вместе с атомом углерода, к которому они присоединены, образуют C3-C7циклоалкил, представляет собой 1,1-циклопропиламинокислоту.
Одна подгруппа соединений включает соединения формулы I или любые подгруппы соединений, указанных в этом документе, в которых R3 представляет собой водород или C1-C6алкил, и R4 представляет собой водород или C1-C6алкил; или в которых R3 представляет собой водород или C1-C4алкил, и R4 представляет собой водород или C1-C4алкил; или в которых R3 представляет собой водород или C1-C4алкил, и R4 представляет собой водород. Конкретная подгруппа из числа вышеуказанных представляет собой такую, в которой R4 представляет собой водород и в которой углерод, связанный с R3 и R4, имеет L-конфигурацию. В одном примере осуществления изобретения, в соединениях формулы I, или в любых подгруппах соединений формулы I, R3 представляет собой метил или разветвленный C1-C6алкил, такой как изопропил или изобутил, и R4 представляет собой водород, или в которых R3 представляет собой метил и R4 представляет собой водород, или в которых R3 представляет собой метил и R4 представляет собой метил. Также представляют интерес соединения формулы I или любые подгруппы соединений, указанных в этом документе, в которых группа -NH-C(R3)(R4)-CO- образует -NH-CH2-CO- (Gly), L-изомер -NH-CH(CH3)-CO- (L-Ala), или -NH-C(CH3)2-CO- (α,α-диметилглицил); а именно L-Ala или α,α-диметилглицил, более конкретно L-Ala.
Один пример осуществления изобретения касается соединений формулы I, или любых подгрупп соединений I, указанных в этом документе, в которых R5 представляет собой C1-C10алкил, необязательно замещенный C1-C4алкокси-группой, или R5 представляет собой C3-C7циклоалкил (а именно, C5-C6циклоалкил), или бензил, а именно, в котором R5 представляет собой метил, этил, н-пропил, 2-бутилпентил, циклопентил, циклогексил или бензил. Представляют интерес такие R5 группы, в которых C1-C6алкильный фрагмент, такой как метил или этил, представляет собой замещенный алкоксигруппой, такой как метокси или этокси, например, R5 представляет собой CH3-О-CH2-CH2-.
Один пример осуществления изобретения касается соединений формулы I, или любых подгрупп соединений I, указанных в этом документе, в которых R6 представляет собой C1-C4алкил, или в которых R6 представляет собой изопропил.
Один пример осуществления изобретения касается соединений формулы I, или любых подгрупп соединений I, указанных в этом документе, в которых R7 представляет собой C1-C4алкил, или в которых R7 представляет собой метил; следующая подгруппа соединений касается таких, в которых R7 представляет собой такой, как указано в этом документе, и -C(=О)CHR7-NH2 имеет L-конфигурацию.
Один пример осуществления изобретения касается соединений формулы I, или любых подгрупп соединений I, указанных в этом документе, в которых R8 представляет собой водород или йод; или R8 представляет собой водород.
Конкретные подгруппы соединений формулы I представляют собой такие, где:
R1 представляет собой водород;
R2 представляет собой фенил, замещенный 1, 2 или 3 заместителями, независимо друг от друга выбираемыми из C1-C6алкила, галогена и C2-C4алкенила; -NH-C(R3)(R4)-CO- образует L-Ala или α,α-диметилглицил;
R5 представляет собой C1-C10алкил, C1-C6алкил, замещенный C1-C6алкоксигруппой; C3-C7циклоалкил или бензил;
R8 представляет собой водород или йод.
Другие конкретные подгруппы соединений формулы I представляют собой такие, где:
R1 представляет собой водород;
R2 представляет собой фенил, фенил, замещенный двумя C1-C4алкилами и галогеном, или нафтил;
-NH-C(R3)(R4)-CO- образует L-Ala или α,α-диметилглицил;
R5 представляет собой C1-C10алкил, C1-C4алкил, замещенный C1-C4алкоксигруппой, C5-C6циклоалкил или бензил.
R8 представляет собой водород.
Конкретные подгруппы соединений формулы I представляют собой такие, где:
R1 представляет собой водород; R2 представляет собой водород; -NH-C(R3)(R4)-CO- образует L-Ala или α,α-диметилглицил; R5 представляет собой C1-C8алкил, C1-C4алкил, замещенный C1-C4алкоксигруппой, циклопентил, циклогексил или бензил; R8 представляет собой водород.
Конкретные подгруппы соединений формулы I представляют собой такие, в которых:
R1 представляет собой водород; R2 представляет собой водород; -NH-C(R3)(R4)-CO- образует L-Ala; R5 представляет собой C1-C8алкил, циклопентил, циклогексил или бензил; R8 представляет собой водород.
Конкретные подгруппы соединений формулы I представляют собой соединения с 1-1 по 1-35, перечисленные в таблице 1 приведенной ниже, включая их фармацевтически приемлемые соли и сольваты.
Соединения формулы I имеют несколько хиральных центров и представлены в этом документе в виде конкретного изомера. Также это относится и к некоторым промежуточным соединениям, применяемым в получении соединений формулы I, где промежуточные соединения могут иметь один или несколько хиральных центров. Однако, соединения формулы I, или какие-либо промежуточные соединения, применяемые в их получении, имеющие, по крайней мере, один хиральный центр, могут содержать небольшие количества других стереоизомеров, т.e. стереоизомеров с различной хиральностью одного или нескольких ассиметрических центров. Общее количество других стереоизомеров, в частности, не должно превышать 25% или 20%, или 10%, или 5%, или 2%, или 1%, или 0,5%, или 0,1 масс.%.
Также хиральность может быть и в заместителях, такая, например, как хиральность, обусловленная заместителями в, например, у атома углерода, имеющего R3 и R4 (где R3 и R4 различны), или у атома фосфора. Фосфорный хиральный центр может быть представлен как Rp или Sp, или смесью таких стереоизомеров, включая рацематы.
Также могут существовать диастереоизомеры, получающиеся как результат существования хирального фосфорного центра и хирального углеродного атома.
Абсолютная конфигурация каждого из хиральных центров может быть определена с использованием известных в данной области техники способов, таких как, например, дифракция рентгеновских лучей или ЯМР, и/или исходя из применения исходных веществ с известной стереохимией. Чистые стереоизомерные формы соединений и промежуточных соединений этого изобретения могут быть получены посредством применения методик, известных в данной области техники. Например, энантиомеры могут быть отделены один от другого путем селективной кристаллизации их диастереомерных солей с оптически активными кислотами или основаниями. Их примеры представляют собой винную кислоту, дибензоилвинную кислоту, дитолилвиннную кислоту и камфорсульфоновую кислоту. Альтернативно, энантиомеры могут быть разделены хроматографическими методами с использованием хиральных неподвижных фаз. Указанные химически чистые стереоизомерные формы также могут быть получены из соответствующих химически чистых стереоизомерных форм подобранных исходных веществ, при условии, что реакция протекает стереоспецифично. Предпочтительно, в том случае, если необходим определенный стереоизомер, синтезировать указанное соединение посредством стереоспецифических способов получения. Для этих способов предпочтительно использовать энантиомерно чистые исходные вещества.
Диастереомерные рацематы соединений формулы I могут быть получены в разделенном виде посредством общепринятых способов. Подходящие физические способы разделения, которые успешно могут быть использованы, представляют собой, например, селективную кристаллизацию и хроматографию, например, колоночную хроматографию.
Фармацевтически приемлемые аддитивные соли включают терапевтически активные кислотно-аддитивные и основно-аддитивные солевые нетоксичные формы соединений формулы I. Фармацевтически приемлемые кислотно-аддитивные соли могут быть стандартно получены посредством обработки основной формы такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например, хлористоводородная или бромистоводородная кислота, серная, азотная, фосфорная и им подобные кислоты; или органические кислоты, такие как, например, уксусная, пропионовая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.e. этандиовая), малоновая, янтарная (т.e. бутандиовая кислота), малеиновая, фумаровая, яблочная (т.e. гидроксибутандиовая кислота), винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и им подобные кислоты. И наоборот, указанные солевые формы при обработке подходящим основанием могут быть превращены в свободные основные формы.
Соединения формулы I, содержащие кислотный протон, могут также быть превращены в их нетоксичные солевые формы присоединения металла или амина при обработке подходящими органическими или неорганическими основаниями. Подходящие основные солевые формы включают, например, аммонийные соли, соли щелочного или щелочноземельного металла, например, литиевые, натриевые, калиевые, магниевые, кальциевые соли и им подобные, соли с органическими основаниями, например, бензатином, N-метил-D-глюкамином, гидрабаминовые соли и соли с аминокислотами, такими как, например, аргинин, лизин и им подобные.
Термин "сольваты" охватывает любые фармацевтически приемлемые сольваты, которые способны образовать соединения формулы I, а также и их соли. Такие сольваты представляют собой, например, гидраты, алкоголяты, например, этаноляты, пропаноляты, включая н-пропаноляты и изопропаноляты, и им подобные.
Некоторые соединения формулы I также могут существовать в виде их таутомерных форм. Уридиновое основание представляет собой пример такой формы. Несмотря на то, что не было подробного указания в вышеприведенной формуле, такие формы предназначены для включения в объем настоящего изобретения.
Как используется в этом документе, "C1-C4алкил" как группа или часть группы, обозначает насыщенные углеводородные радикалы с прямой или разветвленной цепью, имеющие от 1 до 4 атомов углерода, такие как, например, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-l-пропил, 2-метил-2-пропил. "C1-C5алкил" охватывает C1-C4алкильные радикалы и их высшие гомологи, имеющие 5 атомов углерода, такие как, например, 1-пентил, 2-пентил,3-пентил, 2-метил-1-бутил и им подобные. "C1-C6алкил" охватывает C1-C4алкильные радикалы и их высшие гомологи, имеющие 5 или 6 атомов углерода, такие как, например, 1-пентил, 2-пентил, 3-пентил, 1-гексил, 2-гексил, 2-метил-1-бутил, 2-метил-1-пентил, 2-этил-1-бутил, 3-метил-2-пентил и им подобные. Из числа C1-C6алкилов представляет интерес C1-C4алкил.
C1-C10алкил охватывает C1-C6алкильные радикалы и их высшие гомологи, имеющие 7-10 атомов углерода, а именно, разветвленные гомологи, такие как 2-пропилпентил. Среди C1-C10алкилов представляют интерес C1-C8алкилы (которые охватывают C1-C6алкильные радикалы и их высшие гомологи, имеющие 7-8 атомов углерода) или C1-C6алкилы.
"C2-C6алкенил" как группа или часть группы, обозначает насыщенные углеводородные радикалы с прямой или с разветвленной цепью, имеющие от 1 до 6 атомов углерода и одну двойную связь, такие как, например, этенил, 1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-1-пропенил, 2-метил-2-пропенил, 4-пентенил, 3-пентенил, 5-гексенил, 4-гексенил, 3-гексенил и им подобные. Одна из подгрупп C2-C6алкенилов включает C2-C6алкенильные радикалы, в которых углерод, через который группа связана с остальной частью молекулы, является насыщенным. Другую подруппу составляют C2-C4алкенилы, которые представляют собой алкенильные радикалы с атомами углерода в количестве от двух до четырех. Другие подгруппы C2-C6алкенилов включают C2-C6алкенильные или C2-C4алкенильные группы, в которых углерод, через который группа связана с остальной частью молекулы, является насыщенным.
"C1-C4алкокси" обозначает радикал -О-C1-C4алкил, в котором C1-C4алкил является таким, как определено выше. Представляющие интерес C1-C4алкоксильные радикалы включают, но не ограничиваются только перечисленными, метокси, этокси, н-пропокси и изопропокси.
"C3-C7циклoалкил" включает циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Представляют интерес циклопропил, циклопентил и циклогексил.
"C2-C6ацил", как группа или часть группы, обозначает C1-C5алкильную группу, которая присоединена к карбонильной группе одинарной связью, и включает, например, ацетил, пропаноил, бутаноил, изобутаноил, пентаноил, гексаноил, пиваноил и им подобные. Номенклатура C2-C6ацильных фрагментов, перечисленных выше, может быть другой, такой как, например, изобутаноил также может быть обозначен как изобутирил.
Термин "галоген" является общим для фтора, хлора, брома и йода.
Как используется в данном документе, обозначение "(=О)" или "оксo" образует карбонильный фрагмент в случае присоединения к углеродному атому. Следует отметить, что атом только тогда может иметь заместитель в виде оксо-группы, когда валентность атома это допускает.
Следует отметить, что положения радикалов в любом фрагменте молекулы, используемом в определениях могут быть где угодно в таком фрагменте, при условии, что он является химически стабильным. В том случае, когда перемена происходит более чем 1 раз в любом фрагменте, тогда каждое определение является независимым.
Настоящее изобретение также включает изотопномеченные соединения формулы I или любой подгруппы формулы I, где один или несколько атомов заменены изотопом, отличающимся от обычного изотопа(ов), обнаруженного в природе. Примеры таких изотопов включают изотопы водорода, такие как 2H и 3H; углерода, такие как 11C, 13C и 14C; азота, такие как 13N и 15N; кислорода, такие как 15O, 17O и 18O; фосфора, такие как 31P и 32P, серы, такой как 35S; фтора, такой как 18F; хлора, такой как 36Cl; брома, такие как 75Br, 76Br, 77Br и 82Br; и йода, такие как 123I, 124I, 125I и 131I. Изотопномеченные соединения изобретения могут быть получены посредством таких способов, которые аналогичны способам, описанным в этом документе, при использовании соответствующих изотопномеченных реагентов или исходных веществ, или посредством методик, известных в данной области техники. Выбор изотопа, включаемого в изотопномеченное соединение, зависит от конкретного применения этого соединения. Например, для проведения биологических испытаний распределения в тканях используют включение таких радиоактивных изотопов, как 3H или 14C. Для приборов, получающих изображение за счет радиоактивного излучения, будет пригоден позитрон-излучающий изотоп, такой как 11C, 18F, 13N или 15O. Включение дейтерия может обеспечить большую метаболическую стабильность, приводящую в результате, например, к возрастанию in vivo периода полувыведения соединения или к снижению требуемой дозировки.
Всякий раз, когда используются в этом документе, термины "соединения формулы I" или "представленные здесь соединения", или "подгруппы соединений формулы I", или аналогичные термины, подразумевается, что они включают соединения формулы I или их подгруппы, а также их соли и сольваты.
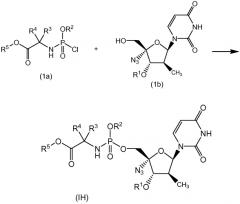
Соединения формулы I могут быть получены посредством взаимодействия производного нуклеозида (1b) с хлорфосфорамидатом (1a), как представлено на схеме 1.
Схема 1
Конденсацию производного нуклеозида (1b) с хлорфосфорамидатом (1a) проводят в реакционно-инертном растворителе, таком как простой эфир, например диэтиловый, тетрагидрофуран (ТГФ) или метилтетрагидрофуран (MeТГФ), или галогенсодержащий углеводород, например дихлорметан, в присутствии основания, такого как N-метилимидазол или ему подобных, получая фосфорамидат формулы (I). Альтернативно реагент Гриньяра, например t-BuMgCl, можно использовать в качестве основания, в этом случае реакцию, как правило, проводят в растворителе, представляющем собой простой эфир, например ТГФ или MeТГФ.
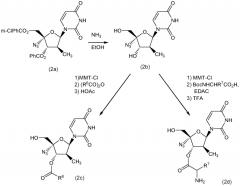
Производные нуклеозидов 1b, где R1 отличен от водорода, могут быть получены, как проиллюстрировано схемой 2.
Схема 2
Производные нуклеозидов (1b), где R1 представляет собой H, могут быть получены посредством гидролиза 3' и 5' сложноэфирных групп в диэфире (2a) (полученном, например, как описано в WO 2008/043704), используя способ гидролиза сложного эфира, например, посредством обработки аммиаком в этаноле. Производные нуклеозидов (1b), имеющие заместитель в положении 3', т.e. когда R1 представляет собой -C(=О)R6 или -C(=О)CR7-NH2, где R6 и R7 являются такими, как определено выше, могут быть получены из диольного нуклеозида (2b) путем последовательных стадий введения защиты - ацилирования - снятия защиты. Например, селективная защита первичной гидрокси-группы с помощью тритильной или монометокситритильной (MMT) группы, или им подобной, посредством обработки тритил-вводящим агентом, например, галогенидом, таким как хлорид, в присутствии основания, такого как пиридин, последующее ацилирование по 3'-гидрокси группе с использованием подходящих для ацилирования условий позволяет получить 3'-ацилированные производные. Нуклеозиды (2c), имеющие сложноэфирную группу в 3'-положении, т.е. R1 в формуле (1a) представляет собой -C(=О)R6, удобно получать посредством реакции 5'-защищенного нуклеозида с алкилангидридом формулы (R6CO)2О в присутствии основания, такого как пиридин или ему подобные. Нуклеозиды (2d), имеющие аминокислоту в 3'-положении, т.e. R1 в формуле (1a) представляет собой -C(=О)CR7-NH2, могут быть получены посредством реакции 5'-защищенного нуклеозида с N-защищенной алифатической аминокислотой в присутствии подходящего пептидосвязующего реагента, такого как 1-этил-3-(3-диметиламинопропил)карбодиимид (EDAC)), или ему подобных. В завершении всего удаление 5'-О-защитной группы и, в случае, когда R1 был введен для получения N-защищенной аминокислоты, N-защитной группы, используя подходящие условия в соответствии примененными защитными группами, такие как кислотная обработка в случае тритильной или монометокситритильной защитной группы, затем обеспечивает получение 3'-ацилированных производных (2c) и (2d). Соединения формулы I, где R1 представляет собой -C(=О)R6 или -C(=О)CR7-NH2, альтернативно могут быть получены посредством проведения, в первую очередь, конденсации хлорфосфорамидата (1a) с дигидроксисоединением (2b) и посредством введения после этого необходимого 3'-заместителя.
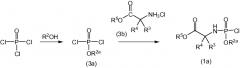
Хлорфосфорамидаты (1a) могут быть получены двумя последовательными стадиями, исходя из фосфороксихлорида, как проиллюстрировано на схеме 3, где R2a обозначает то же самое, что и R2, но не является водородом, и R3, R4 и R5 являются такими, как определено выше.
Схема 3
Конденсация POCl3 со спиртом R2aOH в реакционноинертном растворителе, таком как Et2О, обеспечивает получение алкилокси- или арилокси-фосфордихлоридата (3a). Последующая реакция с аминокислотным производным (3b), в котором R5 является таким, как определено выше, или R5 может быть защитной группой для карбоксильной группы кислоты, которая удаляется и замещается необходимой R5 группой, обеспечивает получение хлорфосфорамидата (1a). Эти реакции проводятся в реакционноинертном растворителе, таком как вышеуказанные растворители в связи с получением соединений формулы I.
В следующем аспекте настоящее изобретение касается фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы I, как указано в этом документе, и фармацевтически приемлемый носитель. Терапевтически эффективное количество в этом контексте представляет собой такое количество, которое является достаточным для воздействия в качестве профилактической меры против инфекции HCV, для стабилизации или ослабления инфекции HCV у инфицированных субъектов или субъектов в состоянии риска заражения. И еще в следующем аспекте это изобретение относится к способу получения фармацевтической композиции, как указано в этом документе, который включает тщательное смешивание фармацевтически приемлемого носителя с терапевтически эффективным количеством соединения формулы I, как указано в этом документе.
Для того, чтобы получить фармацевтические композиции этого изобретения, эффективное количество индивидуального соединения, необязательно в виде аддитивной соли или в виде металлокомплекса, в качестве активного ингредиента объединяют при тщательном смешивании с фармацевтически приемлемым носителем, этот носитель можно использовать в широко разнообразных формах, в зависимости от требуемой для введения формы препарата. Эти фармацевтические композиции необходимы в виде единичной дозированной формы в особенности удобной для перорального введения, для ректального введения, для введения через кожу или для парентеральной инъекции. Например, при получении композиций в пероральной дозированной форме может применяться любая, обычно используемая фармацевтическая среда, такая как, например, вода, гликоли, масла, спирты и им подобные в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, лубриканты, связующие вещества, дезинтегрирующие агенты и им подобные в случае порошков, пилюль, капсул и таблеток. Из-за простоты введения таблетки и капсулы представляют собой преимущественные пероральные единичные дозированные формы, в случае которых конечно же используют твердые фармацевтические носители. Для парентеральных композиций, как правило, носитель будет включать стерильную воду, по крайней мере, в большей его части, однако же могут быть включены и другие ингредиенты, например, способствующие растворимости. Растворы для инъекций, например, могут быть получены таким образом, что носитель включает солевой раствор, раствор глюкозы или смесь солевого и глюкозного растворов. Суспензии для инъекций также могут быть получены таким образом, что в этом случае могут использоваться подходящие жидкие носители, суспендирующие агенты и им подобные. Также охватываются твердые формы препаратов, предназначенные для превращения непосредственно перед применением в жидкие лекарственные формы. В композициях, удобных для введения через кожу, носитель необязательно включает усиливающее проникновение вещество и/или подходящее увлажняющее вещество, необязательно объединенные с подходящими дополнительными компонентами любой природы с меньшим относительным содержанием, причем эти дополнительные компоненты не привносят ощутимого вредного воздействия на кожу.
Соединения настоящего изобретения также могут вводится посредством пероральной ингаляции или инсуффляции с использованием каких-либо способов и композиций, известных из уровня техники для доставки таким путем. Таким образом, в большинстве случаев соединения настоящего изобретения могут быть введены в легкие в форме раствора, суспензии или сухого порошка, предпочтение отдается раствору. Любая система, разработанная для доставки растворов, суспензий или сухих порошков посредством пероральной ингаляции или инсуффляции подходит для введения представленных здесь соединений.
Особо предпочтительной представляется разработка технологии получения препаратов на основе вышеуказанных фар