Способ количественного определения термического стресса, которому подвергался фруктовый сок
Иллюстрации
Показать всеИзобретение относится к способу количественного определения термического стресса, которому подвергается фруктовый сок, а именно при пастеризации или замораживании. Способ включает определение соотношения изолимонина к лимонину, причем пониженное соотношение указывает на меньший термический стресс, а повышенное - на больший термический стресс. Изобретение обеспечивает регулирование вкуса фруктового сока. 3 н. и 4 з.п. ф-лы, 8 ил., 2 табл., 5 пр.
Реферат
Настоящее изобретение имеет приоритет заявки США Сер.№ 60/978515 от 9 октября 2007 года, под названием «Регулирование характеристик аромата и свежести фруктового сока», включенной в данное описание полностью путем ссылки.
Данное изобретение относится к способу количественного определения термического стресса, которому подвергался фруктовый сок, в частности, при пастеризации или замораживании, включающий определение соотношения изолимонина к лимонину во фруктовом соке, таком как цитрусовый сок и, в частности, апельсиновый сок.
Цитрусовые фрукты давно известны как ценный источник важных питательных веществ. Позднее, цитрусовые в качестве источника, полезного для здоровья или пригодного для профилактики и лечения заболеваний, были официально признаны как обладающие благоприятными и полезными свойствами при употреблении в пищу. Соответственно, имеется общее мнение, что увеличение потребления пищи цитрусового происхождения является полезной и важной задачей в общей схеме здоровья человека. Многие потребители получают также удовольствие от цитрусовых фруктов просто потому, что они являются вкусными.
Одним из удобных способов употребления цитрусовых продуктов является употребление в виде их сока. Сок можно легко получать и транспортировать, и он удобен в употреблении. Свежий, или «не из концентрата», сок является лидером по вкусу и качеству. Сок также можно концентрировать и затем восстанавливать его влагосодержание для удобства потребителя. Концентрированный сок также доставляют от источника к потребителю эффективным и недорогим способом. Также сок более легко, по сравнению с фруктами, потребляют те люди, которые имеют проблемы с употреблением твердых фруктов.
Однако, некоторые потребители не любят такие свойства цитрусовых соков, как горечь, кислый вкус, неприятные привкусы, терпкость, золотисто-коричневый цвет и густая консистенция. Все цитрусовые фрукты, включая грейпфруты, апельсины, мандарины, лаймы и лимоны, могут иметь к этому отношение. Некоторые потребители предпочитают соки, имеющие низкий уровень сладости, тогда как другие предпочитают очень сладкий продукт. Кроме того, часто трудно достичь постоянства вкусовых свойств, например, начиная с начала сезона и до его окончания.
Горечь часто представляет собой главный вопрос для потребителя. Низкий уровень горечи может обеспечивать желаемый вклад в органолептические свойства и характеристики сока для многих потребителей. Такие потребители получают удовольствие от пикантной вкусовой ноты на низком уровне горечи. Однако большинство потребителей также соглашается с тем, что избыточная горечь неблагоприятно влияет на органолептические свойства и характеристики сока, делая его неприятным для потребителя. Потребители также часто связывают горечь с недостаточной свежестью, концентрированным соком и/или соком низкого качества.
Соединения, придающие горький вкус, присутствуют в любом виде цитрусовых фруктов в различающихся количествах. Различие в концентрациях соединений, придающих такой вкус, имеется между сортами культурного растения одного и того же фрукта и между фруктами одного и того же культурного растения от начала и до окончания сезона. Следовательно, источник фруктов, время сезона и другие переменные оказывают влияние на концентрации соединений, придающих горький вкус.
Терпкость является характеристикой соков, в частности, цитрусовых соков, которую потребители часто находят нежелательной. В частности, терпкость цитрусового сока часто характеризуется как бархатистое, покрывающее ротовую полость ощущение. Такое ощущение во рту рассматривается как неприятное многими потребителями.
Потребителей также беспокоит кислый вкус фруктового сока. Потребители часто полагают, что цитрусовые соки являются кислыми. Потребители часто связывают кислый вкус не только с неприятно резким вкусом, но также с ощущениями расстройства или дискомфорта в желудке и отрыжкой.
До настоящего времени предпринимались лишь ограниченные попытки для уменьшения горечи, кислого вкуса и других нежелательных органолептических свойств и характеристик, обычно путем удаления некоторых соединений. Одним из таких соединений является лимонин. В других способах из источника сока исключалась часть фруктов, такая как семена и кожура для минимизирования концентрации соединения с горьким вкусом.
Желательной характеристикой для потребителя также является свежесть. Часто сок из концентрата рассматривается как имеющий более низкое качество, чем свежий сок. Известны различные способы обработки замороженных соков и концентратов соков. Однако, до настоящего времени сок из концентрата страдает неблагоприятным действием на вкус, и полностью удовлетворяющий пожеланиям сок, либо свежий, либо замороженный, не стал коммерчески доступным.
Таким образом, существует потребность в соке, горький вкус в котором регулировался бы в границах, которые потребители обычно находят приятными, но не избыточно горькими. Также существует потребность в соке со свежим вкусом.
Существо изобретения
Первый вариант изобретения относится к регулированию горечи фруктового сока, в частности, цитрусового сока.
Второй вариант изобретения относится к регулированию горечи и свежести цитрусового сока путем регулирования концентраций ключевых горьких соединений, придающих вкус.
Третий вариант изобретения относится к регулированию терпкости фруктового сока, в частности, апельсинового сока.
Четвертый вариант изобретения относится к регулированию кислого вкуса фруктового сока, в частности, апельсинового сока.
Пятый вариант изобретения относится к регулированию сладости фруктового сока, в частности, апельсинового сока.
На прилагаемых чертежах
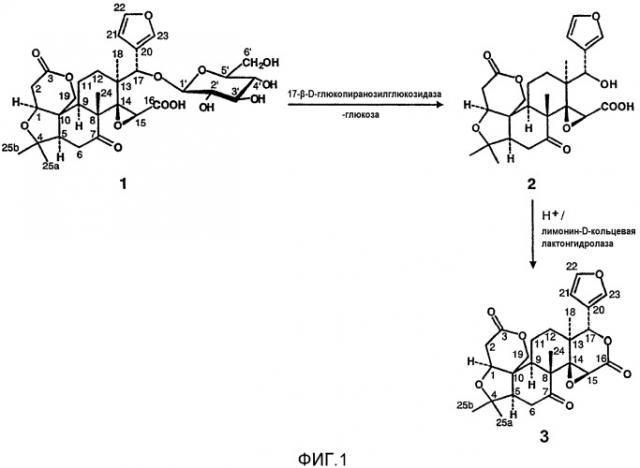
Фиг.1 - схема реакций, демонстрирующая ферментативное разложение лимонин-17-β-D-глюкопиранозида (1) через лимоноат А-кольцевой лактон (2) с получением лимонина (3), имеющего горький вкус.
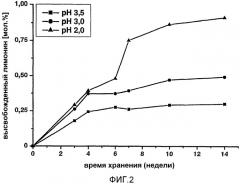
Фиг.2 - график влияния значения рН на время-зависимое образование лимонина (3) в водном растворе лимонин-17-β-D-глюкопиранозида (1), хранящегося при 20ºС.
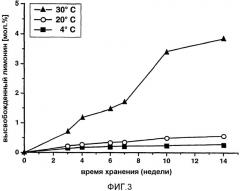
Фиг.3 - график влияния температуры на время-зависимое образование лимонина (3) в водном растворе лимонин-17-β-D-глюкопиранозида (1), при рН 3,0.
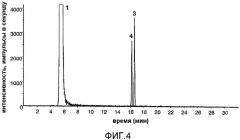
Фиг.4 - RP-ВЭЖХ-МС/МС-хроматограмма, полученная для водного раствора (рН 3,0) лимонин-17-β-D-глюкопиранозида (1), выдержанного в течение десяти недель при 30ºС и демонстрирующего пики лимонина (3) и неизвестного продукта (4) гидролиза.
Фиг.5 - 1Н-ЯМР-спектр (400 МГц) очищенного С17-эпилимонина (4).
Фиг.6 - последовательность реакций, показывающая гидролитическое разложение лимонин-17-β-D-глюкопиранозида (1) с образованием лимонина (3) и С17-эпилимонина (4) через фурфурилиден-карбокатион в качестве ключевого промежуточного соединения.
Фиг.7 - разложение лимонина (А) и С17-эпилимонина (В) при хранении апельсинового сока при 20ºС как функция времени.
Фиг.8 - образование лимонина и С17-эпилимонина (А) и соотношение (В) С17-эпилимонина/лимонина при термической обработке апельсинового сока в зависимости от времени.
Настоящее изобретение относится к регулированию органолептических свойств фруктового сока. В частности, варианты данного изобретения относятся к регулированию горечи в цитрусовом соке посредством регулирования концентраций ключевых соединений, придающих горький вкус, регулирования терпкости посредством регулирования причины ключевых терпких свойств, регулирования кислого вкуса посредством регулирования концентраций и относительных пропорций кислот и регулирования сладости посредством регулирования концентраций и относительных пропорций сахаров.
Изобретение также относится к приданию соку свежего вкуса. В частности, варианты данного изобретения относятся к регулированию компонента во фруктовом соке для получения свежего вкуса сока.
Квалифицированные специалисты отдают себе отчет, что концентрация придающего вкус компонента в пищевом продукте должна превысить пороговый уровень вкуса прежде, чем потребитель будет способен ощутить вкус данного придающего вкус компонента. Пороговые уровни ощущения различных вкусовых характеристик, таких как терпкость и горечь, являются разными. Следовательно, проводимые до настоящего времени работы по идентификации соединений, которые вносят свой вклад во вкусовые характеристики, относились к тем соединениям, которые присутствуют в концентрациях, которые превышают значимый пороговый уровень вкуса.
Авторы настоящего изобретения установили, что горький вкус сока цитрусовых фруктов, в частности, апельсинового сока, вызван, по крайней мере частично, взаимодействием трех групп горьких веществ, и на него оказывает влияние концентрация сахара в соке. Такое открытие синергизма между данными тремя группами горьких веществ и сахаром образует основу возможности регулирования горечи цитрусового сока. До настоящего времени квалифицированным специалистам не было известно, что три группы горьких веществ и сахар регулируют ощущение горечи апельсинового сока.
Лимонин, вещество, которое, как известно квалифицированным специалистам, вызывает горечь в апельсиновом соке, само по себе полностью не несет ответственности за горечь апельсинового сока. Скорее, горечь в апельсиновом соке вызвана взаимодействием следующих трех групп горьких веществ:
(1) лимонин, изолимонин и, в минимальной степени, номилин;
(2) полиметоксилированные флавоны (ПМФ); и
(3) лимоноидные β-D-глюкопиранозиды.
Таким образом, регулирование в соке соответствующих концентраций данных соединений, вместе с регулированием концентрации сахара будет приводить к регулированию чувства горечи в соке.
Концентрации членов данных групп горьких веществ изменяются как функция от сорта культурного растения, времени роста и сезона сбора урожая (т.е. в зависимости от начала, середины или конца сезона) и условий переработки. Например, установлено, что лимонин образуется в большей степени в соке, полученном из апельсинов, собранных в начале и середине сезона, чем в том случае, когда сок получают из апельсинов, собранных в конце сезона. При понимании взаимоотношения между тремя группами горьких веществ и сахара, горечь апельсинового сока и цитрусовых соков, включающих данные компоненты, можно будет регулировать.
Вкусовые пороговые уровни членов данных групп горьких веществ приведены в следующей таблице:
| Компонент | Пороговый уровень горького вкуса, мкмоль/л |
| Лимонин | 4 |
| Номилин | 13 |
| ПМФ | >130 |
| 5,7,8,3',4'-пентаметоксифлавон | 32,3 |
| 3,5,7,8,3',4'-гексаметоксифлавон | >250 |
| 5,6,7,3',4'-пентаметоксифлавон | 56 |
| 3,5,6,7,3',4'-гексаметоксифлавон | 19 |
| 5,7,8,4'-тетраметоксифлавон | >120 |
| 5,6,7,8,3',4'-гексаметоксифлавон | 103 |
| Лимоноид-β-D-глюкопиранозиды | >130 |
| 5,6,7,4'-тетраметоксифлавон | 44 |
| 3,5,6,7,8,3',4'-гептаметоксифлавон | 24-31 |
| 5,6,7,8,4'-пентаметоксифлавон | 93 |
| 4'-гидрокси-3',5,6,7,8-пентаметоксифлавон | 25 |
| 5,6,7,8,3',4'-гексаметоксифлавон-3-O-β-D-глюкопиранозид | 78 |
| 5,6,7,3',4'-пентаметоксифлавон-3-O-β-D-глюкопиранозид | 61 |
| 5,6,7,3',4'-пентаметоксифлавонглюкозид | 61 |
| 5,6,7,8,3',4'-гексаметоксифлавонглюкозид | 78 |
| 5,7,8,3',4'-пентаметоксифлавон | 32 |
| 5,6,7,3',4'-пентаметоксифлавон | 56 |
| 3,5,6,7,3',4'-гексаметоксифлавон | 19 |
| 5,6,7,8,3',4'-гексаметоксифлавон | 103 |
| 5,6,7,4'-тетраметоксифлавон | 150 |
| 7,3',4'-триметоксифлавон | >400 |
| 7,8,3',4'-тетраметоксифлавон | >400 |
| Лимонин-17-β-D-глюкопиранозид | 106 |
| 17-β-D-глюкопиранозид деацетилномилиновой кислоты | 68 |
| 17-β-D-глюкопиранозид эпиизобакуноевой кислоты | 42 |
| β-glpc номилиновой кислоты | >800 |
| Номилин-β-glpc | >700 |
| Обакунон-β-glpc | 49 |
| Деацетилномилин | >106 |
Как можно видеть из структурных формул данных соединений, члены данных групп горьких веществ обладают общими структурными отличительными признаками.
Авторы настоящего изобретения установили, что предпороговые концентрации ПМФ и, в меньшей степени, номилина, усиливают вызванную лимонином горечь в продуктах из апельсинов, таких как сок. Такой эффект является неожиданным, поскольку квалифицированный специалист не мог бы ожидать, что соединение, которое присутствует до содержания ниже вкусового порогового уровня, вносит вклад в ощущение горечи.
Номилин присутствует в концентрации, близкой к пороговой, в апельсиновом соке сорта Хэмлин и может достигать пороговой концентрации в начале сезона. Лимоноидные β-D-глюкопиранозиды присутствуют примерно на пороговом уровне в апельсиновом соке сортов Хэмлин и Валенсия.
Данные члены этих групп горьких веществ являются очень горькими. В частности, они существенно более горькие, чем соединения, обычно находящиеся в газированных безалкогольных напитках и чае. Например, лимонин является примерно в 200 раз более горьким, чем кофеин и в 150 раз более горьким, чем катехин. Номилин является примерно в 150 более горьким, чем кофеин и в 45 раз более горьким, чем катехин.
В то время, как каждый член групп горьких веществ имеет вкусовой порог, горечь не является линейно связанной с концентрацией. Например, удвоение концентрации компонентов не приводит к удвоению горького вкуса. Кроме того, авторы настоящего изобретения установили, что концентрация соединения не должна достигать вкусового порога для того, чтобы соединение вносило свой вклад в горький вкус. Скорее, соединения действуют синергетически, приводя к более горькому вкусу, чем можно было бы ожидать, исходя из суммы индивидуальных частей.
Сахар измеряют в градусах Брикс (Βrix). Авторы настоящего изобретения установили, что ощущаемая (воспринимаемая) горечь снижается по мере увеличения Брикса и, в частности, по мере увеличения соотношения Брикс/кислота.
Таким образом, с использованием приведенных в настоящем описании указаний квалифицированный специалист может регулировать горечь цитрусового сока путем регулирования Брикса, в частности, соотношения Брикс/кислота, и концентраций данных членов этих групп горьких веществ в продукте сока. Например, концентрация данных соединений может быть снижена с использованием подходящей переработки, такой как ионный обмен, перегонка или обратный осмос. Аналогично, различные соки, имеющие разные концентрации каждого из соединений, могут быть смешаны с получением сока, который имеет более низкие концентрации, чем те концентрации, которые приводят к горькому вкусу.
Авторы настоящего изобретения установили, что лимонин образуется различными путями. Обычно лимонин не присутствует в цельном фрукте при концентрации выше порогового уровня вкуса. Однако лимонин образуется посредством лактонизации, ускоряемой ферментами.
На фиг.1 проиллюстрирован данный путь. Лимонин-17-β-D-глюкопиранозид 1 превращается под действием 17-β-D-глюкопиранозилглюкозидазы с образованием лимонат-А-кольцевой лактозы 2. Данная лактоза восстанавливается в присутствии лимонин-D-кольцевой лактонгидролазы в кислых условиях (рН<6,5) с образованием лимонина 3. Поскольку А-кольцевой лактон преобразуется в лимонин-17-β-D-глюкопиранозид по мере созревания фрукта, концентрация глюкозида может достигать примерно 200 вес.ч.н.м.
Также предполагается, что лимонин может образовываться в соке за счет кислотного гидролиза. Такой кислотный гидролиз ускоряется при понижении рН и увеличении температуры и времени. Таким образом, другие способы регулирования лимонина в соке заключаются в отсутствии нагревания, хранении сока в течение ограниченного времени при низкой температуре и/или в увеличении рН сока.
Концентрация каждого члена группы горьких веществ может быть определена с помощью жидкостной хроматографии высокого давления (ЖХВД). Однако более определенное измерение мог бы обеспечить анализ методом жидкостной хроматографии/масс-спектрометрии (ЖХМС) или анализ методом ЖХМС/МС. Квалифицированному специалисту понятны данные и другие методы измерения концентраций членов групп горьких веществ.
Авторы настоящего изобретения установили, что, как и в случае с горечью, множество соединений, присутствующих в апельсиновом соке в концентрации ниже порогового уровня терпкости, вносит свой вклад в вяжущее ощущение во рту. Вкусовые пороговые уровни для данных терпких соединений индивидуально приведены ниже в следующей таблице.
| Компонент | Пороговый уровень терпкого вкуса, мкмоль/л |
| 5,7,8,3',4'-пентаметоксифлавон | 13,3 |
| 3,5,7,8,3',4'-гексаметоксифлавон | 125 |
| 5,6,7,3',4'-пентаметоксифлавон | 24 |
| 3,5,6,7,3',4'-гексаметоксифлавон | 9 |
| 5,7,8,4'-тетраметоксифлавон | 44 |
| 5,6,7,8,3',4'-гексаметоксифлавон | 51 |
| 5,6,7,4'-тетраметоксифлавон | 21 |
| 3,5,6,7,8,3',4'-гептаметоксифлавон | 4-5 |
| 5,6,7,8,4'-пентаметоксифлавон | 19 |
| 4'-гидрокси-3',5,6,7,8-пентаметоксифлавон | 6 |
| 5,6,7,8,3',4'-гексаметоксифлавон-3-О-β-D-глюкопиранозид | 20 |
| 5,6,7,3',4'-пентаметоксифлавон-3-О-β-D-глюкопиранозид | 21 |
| 5,6,7,3',4'-пентаметоксифлавонглюкозид | 21 |
| 5,6,7,8,3',4'-гексаметоксифлавонглюкозид | 20 |
| 5,7,8,3',4'-пентаметоксифлавон | 13 |
| 5,6,7,3',4'-пентаметоксифлавон | 24 |
| 3,5,6,7,3',4'-гексаметоксифлавон | 9 |
| 5,6,7,8,3',4'-гексаметоксифлавон | 51 |
| 5,6,7,4'-тетраметоксифлавон | 31 |
| 7,3',4'-триметоксифлавон | 15 |
| 7,8,3',4'-тетраметоксифлавон | 44 |
| Лимонин-17-β-D-глюкопиранозид | 17 |
| 17-β-D-глюкопиранозид деацетилномилиновой кислоты | 27 |
| 17-β-D-глюкопиранозид эпиизобакуноевой кислоты | 16 |
| Деацетилномилин | 13,2 |
| Лимонин | 4 |
| Изолимонин | 10 мг/л |
Авторы настоящего изобретения установили, что воспринимаемая сладость относится к относительным концентрациям по крайней мере сахаров глюкозы, фруктозы и сахарозы. Концентрации и относительные пропорции данных сахаров влияют на ощущение сладости.
Пороговые уровни сладкого вкуса глюкозы, фруктозы и сахарозы известны в данной области. Относительные пропорции данных сахаров переменны для соков различных сортов культурных растений и времени сезона. Однако с помощью указаний, обеспеченных в данном изобретении, квалифицированный специалист сможет регулировать сладость цитрусового сока путем регулирования концентраций данных сахаров в продукте сока. Например, концентрация данных сахаров может быть уменьшена с помощью подходящей переработки, такой как ионный обмен, перегонка или обратный осмос. Аналогично, различные соки, имеющие разные концентрации каждого из соединений, могут быть смешаны с получением сока, который имеет более низкие концентрации данных соединений, чем концентрации, которые приводят к кислому вкусу.
Авторы настоящего изобретения также установили, что присутствие изолимонина, - соединения, образующегося из одного из данных лимоноидных β-D-глюкопиранозидов, является показателем свежести. Изолимонин также известен как С17-эпилимонин. Изолимонин образуется путем кислотного гидролиза лимонина после пастеризации. Изолимонин также образуется неферментативным путем из лимонин-17-β-D-глюкопиранозида. Концентрация изолимонина в замороженном концентрате апельсинового сока примерно в два раза выше концентрации в свежем апельсиновом соке, указывая на то, что термический стресс при пастеризации или замораживании сока вносит вклад в образование изолимонина. Таким образом, присутствие изолимонина в концентрации, более высокой чем концентрация в свежем продукте, указывает на то, что продукт может быть несвежим (поскольку изолимонин образуется с течением времени) или был заморожен.
Примеры
Следующие примеры иллюстрируют различные аспекты, относящиеся к изобретению. Пример 1 относится к выделению лимонин-17-β-D-глюкопиранозида из апельсиновых косточек. В примере 2 суммированы результаты исследований при различных температурах и значениях рН для определения скорости, с которой лимонин будет образовываться в растворах. Идентификация лимонина и изолимонина методами ЖХВД и ЖХ-МС и ЯМР представлены в примере 3.
Пример 4 относится к количественной оценке содержания лимонина и изолимонина в апельсиновом соке. Пример 5 относится к органолептическому анализу.
Для данных примеров следующие соединения были получены коммерчески: лимонин (Sigma, Steinheim, Германия); муравьиная кислота, метанол и ацетонитрил (Merck, Darmstadt, Германия); дейтерированные растворители (Aldrich, Taufkirchen, Германия); деионизированную воду, использованную для хроматографии, очищали с помощью градиентной систему А10 Milli-Q (Millipore, Βillerica, США). Апельсиновые косточки и апельсиновый сок, полученные из апельсинов (сорт Валенсия, поздний), собранных во Флориде (США) в марте 2006 года, а также замороженный концентрированный апельсиновый сок, приготовленный из той же порции фруктов, получали от промышленных производителей апельсинового сока (США). Свежие апельсины (сорт Валенсия, поздний) получали от местного продавца.
Высокоэффективная жидкостная хроматография
Прибор ВЭЖХ состоял из двух насосов (Sykam, S 1122), градиентного смесителя (Sunchrom, динамический/статистический градиентный смеситель), инжектора Rheodyne (петля 250 мкл), автоматического пробоотборника (Spark, Midas 380), диодного матричного детектора (Sunchrom, SpectraFlow 600, DAD), при регулировании эффлюента в диапазоне длин волн между 200 и 600 нм, модуля расщепления (Upchurch, P-470, градуированный микросплиттер) и испаряющего светорассеивающего детектора (ELSD) (S.E.D.E.R.E., Sedex 85 LT-ELSD, p=2,6 бар, Т=40ºС), оборудованного небулайзером (S.E.D.E.R.E., ВЭЖХ небулайзер 200 мкл/мин-2,5 мл/мин).
Жидкостная хроматография/масс-спектрометрия (ЖХ/МС)
ЖХ-МС/МС анализ проводили с использованием ВЭЖХ системы Agilent 1100, соединенной с ЖХ-МС/МС API 4000 (Applied Βiosystems, Darmstadt, Германия), функционирующей или в режиме отрицательной (ESI-), или положительной (ESI+) ионизации электрораспылением. Напряжение распыления устанавливали при -4500 В, азот служил газом воздушной завесы (20 фт/кв.дюйм), и разгруппировывающий потенциал устанавливали при -65 В. С помощью режима множественного реакционного мониторинга (MRM) соединения 2 и 3 анализировали с использованием описанного выше перехода масс.
Спектроскопия ядерного магнитного резонанса (ЯМР)
Спектроскопические эксперименты 1Н, COSY, HMQC и HMΒC проводили на ЯМР приборе DPX 400 МГц фирмы Βruker (Rheinstetten, Германия). Образцы растворяли в ДМСО-d6 или MeOD-d4 с использованием тетраметилсилана в качестве внутреннего стандарта и помещали в ЯМР-ные ампулы (Schott Professional, 178×5 мм) перед измерением. Обработку данных проводили с использованием программного обеспечения Mestre-C для ЯМР.
Пример 1 - Выделение лимонин-17-β-D-глюкопиранозида из апельсиновых косточек
Апельсиновые косточки (100 г) тщательно промывали водой, затем ацетоном и замораживали в жидком азоте, измельчали в мельнице мелкого помола и затем дважды экстрагировали метанолом (300 мл) в течение 4 часов при 60ºС. После фильтрования из экстракта удаляли растворитель в вакууме, получая экстрагированные в метанол вещества в виде аморфного порошка (28 г).
Аликвоту (2 г) данного неочищенного изолята помещали в воду (10 мл), находящуюся наверху охлаждаемой водой стеклянной колонки (300×35 мм), заполненной суспензией вещества Амберлит XAD-2 (ΒDH Chemicals Ltd, Poole, Англия), уравновешенной водой. Проводили хроматографию при скорости потока 5 мл/мин, начиная с воды (200 мл, фракция I), затем с использованием смесей метанол/вода, содержащих 20% (200 мл, фракция II), 40% (200 мл, фракция III), 60% (200 мл, фракция IV), 80% (200 мл, фракция V) и метанол (200 мл, фракция VI). Индивидуальные фракции собирали по отдельности, растворитель удаляли в вакууме при 30ºС и затем подвергали лиофильной сушке для получения фракций I-VI в виде аморфных порошков.
Фракции II-IV объединяли, растворяли в смеси (20/80, об./об.) метанола и 0,1% водной муравьиной кислоты и, после мембранной фильтрации, аликвоты (250 мкл) фракционировали с помощью полупрепаративной ВЭЖХ на колонке Microsorb-MV, RP-18, 250×10 мм, внутренний диаметр 5 мкм (Varian, Германия). При контроле эффлюента с помощью УФ-детектора при 220 нм, а также ELSD, хроматографию проводили при скорости потока 3,5 мл/мин, начиная со смеси (10/90, об./об.) ацетонитрила и 0,1% водной муравьиной кислоты, повышая содержание ацетонитрила до 20% в течение 15 минут, выдерживая эту концентрацию в течение 5 минут и, наконец, поднимая содержание ацетонитрила до 100% в течение 5 минут. Эффлюент, имеющий пик, обнаруженный при 17 минутах, собирали в охлажденную льдом колбу, органический растворитель удаляли в вакууме, и водный слой наносили на верхнюю часть картриджа Strata C18-E SPE (10 г, 55 мкм, Giga-Tubes, Phenomenex), уравновешенного водой. Картридж наполняли до краев водой (150 мл), затем сушили путем просасывания через него тока азота и, наконец, элюировали метанолом (100 мл). В картридже SPE удаляются следы муравьиной кислоты для предотвращения протон-катализируемого высвобождения агликона. Органический эффлюент избавляли от растворителя в вакууме, остаток суспендировали в воде (5 мл) и подвергали лиофильной сушке, получая лимонин-17-β-D-глюкопиранозид в виде белого аморфного порошка с чистотой более 99%.
Лимонин-17-β-D-глюкопиранозид, 1 на фиг.1 УФ/виз (ацетонитрил/вода; рН 2,5): λмакс.=220 нм; ЖХ/МС (ESI+): m/z 649 ([M-H]-); ЖХ/МС (ESI-): m/z 668 ([M+NH4]+), 673 ([M+Na]+), 689 ([M+K]+); 1H-ЯМР (400 МГц, MeOD-d4, COSY): δ 0,66 [c, 3H, H-C(24)], 0,98 [c, 3H, H-C(25b)], 1,21 [c, 3H, H-C(25a)], 1,40 [c, 3H, H-C(18)], 1,66 [м, 1H, H-C(12)], 1,78 [м, 2H, H-C(11)], 1,99 [м, 1H, H-C(12)], 2,43 [дд, 1H, J=7,4, 22,1 Гц, H-C(6)], 2,55 [дд, 1H, J=5,6, 19,0 Гц, H-C(6)], 2,68 [д, 1H, J=4,3 Гц, H-C(9)], 2,71 [д, 2H, J=4,1 Гц, H-C(2)], 2,79 [дд, 1H, J=5,6, 14,7 Гц, H-C(5)], 2,94 [c, 1H, H-C(15)], 3,11 [м, 2H, H-C(2'), H-C(5')], 3,20 [м, 1H, H-C(4')], 3,27 [м, 1H, H-C(3')], 3,48 [м, 1H, H-C(6')], 4,20 [c, 1H, H-C(1)], 4,29 [д, 1H, J=7,6 Гц, H-C(1')], 4,40 [д, 2H, J=8,1 Гц, H-C(19)], 5,42 [c, 1H, H-C(17)], 6,53 [д, 1H, J=1,3 Гц, H-C(21)], 7,24 [c, 1H, H-C(23)], 7,63 [c, 1H, H-C(22)]; 13C-ЯМР (100 МГц, MeOD-d4, HMQC, HMBC): δ 17,1 [C, C(11)], 18,4 [C, C(24)], 20,8 [C, C(25b)], 24,7 [C, C(18)], 26,8 [C, C(12)], 29,2 [C, C(25a)], 35,2 [C, C(2)], 36,4 [C, C(6)], 44,8 [C, C(13)], 45,1 [C, C(9)], 45,2 [C, C(10)], 50,7 [C, C(8)], 54,8 [C, C(5)], 59,8 [C, C(15)], 61,7 [C, C(6')], 63,8 [C, C(19)], 69,1 [C, C(14)], 70,4 [C, C(4')], 75,4 [C, C(2')], 76,0 [C, C(5')], 76,9 [C, C(3')], 78,1 [C, C(17)], 78,4 [C, C(1)], 80,8 [C, C(4)], 104,3 [C, C(1')], 112,3 [C, C(21)], 125,4 [C, C(20)], 140,3 [C, C(22)], 142,3 [C, C(23)], 173,0 [C, C(3), C(16)], 209,6 [C, C(7)].
Пример 2 - Образование лимонина из лимонин-17-β-D-глюкопиранозида
Для исследования предполагаемого неферментативного высвобождения лимонина из лимонин-17-β-D-глюкопиранозида во время хранения апельсинового сока, водный раствор глюкопиранозида, доведенный до значения рН, соответствующего свежевыжатому апельсиновому соку (рН 3,5), или до значений рН, найденных для концентратов апельсиновых соков (рН 2,0 и 3,0), выдерживали при 20ºС в течение вплоть до 14 недель в темноте. С регулярными временными интервалами из модельных растворов отбирали аликвоты и анализировали в них количество лимонина, высвободившегося из глюкопиранозида, с помощью ВЭЖХ-МС/МС, функционирующего в режиме MRM. Независимо от значения рН модельного раствора лимонин образовывался при увеличении времени хранения, как показано на фиг.2, но пониженные значения рН способствовали образованию горького соединения. Например, 0,85 мол.% лимонина высвободилось из глюкопиранозида при хранении при рН 2,0, тогда как при рН 3,5 образовалось только 0,25% горького соединения.
Для исследования влияния температуры на образование лимонина, водные растворы глюкопиранозида, доведенные до рН 3,0 выдерживали при 4, 20 и 30ºС в течение вплоть до 14 недель в темноте. Через регулярные промежутки времени определяли количество лимонина с помощью ВЭЖХ-МС/МС, функционирующего в режиме MRM. Результаты, представленные на фиг.3, четко показывают, что высвобождение лимонина из лимонин-17-β-D-глюкопиранозида ускорялось при 30ºС по сравнению с модельными растворами, выдерживаемыми при 4 и 20ºС, соответственно. Например, лимонин высвобождался из своего предшественника с выходом около 4,0% при выдерживании при 30ºС, тогда как только 0,2% горького соединения было обнаружено после хранения раствора его предшественника при 4ºС в течение 14 недель.
В частности, водные растворы лимонин-17-β-D-глюкопиранозида (0,35 мг/л), доведенные до значения рН 2,0, 3,0 и 3,5, соответственно, путем добавления следовых количеств соляной кислоты (1 моль/л) выдерживали при разной температуре (4, 20, 30ºС) в течение вплоть до 14 недель в закрытых ампулах в темноте. Через регулярные промежутки времени с помощью шприца отбирали образцы (5 мкл) и анализировали образование лимонина с помощью ЖХ-МС/МС на колонке Synergi Fusion, 150×2 мм, внутренний диаметр 4 мкм (Phenomenex). Для достижения этого, хроматографию проводили при скорости потока 250 мкл/мин, начиная со смеси (80/20, об./об.) 0,1% водной муравьиной кислоты и ацетонитрила, повышая содержание ацетонитрила до 40% в течение 10 минут, затем до 80% в течение 5 минут, выдерживали при этой концентрации в течение 5 минут и, наконец, до 100% в течение 5 минут. С использованием отрицательного режима ионизации электрораспылением лимонин анализировали в режиме множественного реакционного мониторинга (MRM) с использованием перехода массы m/z 469→229. Количественный анализ проводили путем сопоставления площади пиков, полученных для следовых масс с пиками определенных стандартных растворов лимонина в метаноле.
Фиг.4 иллюстрирует, что на хроматограмме ЖХ-МС/МС не проявляются как раз лимонин-17-β-D-глюкопиранозид (1) и лимонин (3), но, неожиданно, на ней имеется третий пик (4), элюированный при 16,59 минуты и демонстрирующий тот же переход массы m/z 469→229, который был выявлен для лимонина, таким образом подразумевая существование стереоизомера лимонина. Поскольку химическая структура данного соединения к этому моменту еще не была с очевидностью подтверждена с помощью ЯМР-спектроскопических экспериментов, дополнительные эксперименты были направлены на получение соединения 4 в подходящих количествах для проведения спектроскопических экспериментов.
Пример 3 - Идентификация лимонина и изолимонина (соединение 4)
Высвобождение из лимонин-17-β-D-глюкопиранозида
Для определения химической структуры соединения 4, выявленного в примере 2 и проиллюстрировано на фиг.4, водный раствор лимонин-17-β-D-глюкопиранозида, доведенный до рН 1,5, выдерживали в течение 4 часов при 60ºС, соединение 4 выделяли и очищали с помощью полупрепаративной ВЭЖХ, и его химическая структура была определена с помощью ЖХ-МС/МС и 1D/2D-ЯМР (одномерный/двумерный ЯМР) экспериментов. В спектре 1Н-ЯМР, показанном на фиг.5, наблюдался 21 сигнал, среди которых 10 сигналов, показавших химические сдвиги при δ 1,44, 1,72, 2,00, 2,25, 2,66, 2,66, 2,73, 2,75, 2,91 и 4,14 м.д., достаточно хорошо соотносились с резонансами алкильных протонов H-C(12a), H-C(11), H-C(12b), H-C(6a), H-C(2a), H-C(5), H-C(2b), H-C(9), H-C(6b) и H-C(1) лимонина. Отнесение данных сигналов было определенно подтверждено с помощью гомо- (COSY) и гетероядерных корреляционных экспериментов (HMQC, HMΒC). Диастереотопные протоны, имеющие резонансные сигналы при 4,51 и 4,78 м.д., хорошо соответствовали метиленовым протонам Н-С(19), указывая таким образом на сохранившееся А-кольцо, какое имеется в лимонине. Также резонансные сигналы, наблюдавшиеся при 6,62, 7,60 и 7,70 м.д. для фурановых протонов Н-С(21), Н-С(22) и Н-С(23), демонстрировали структурное подобие с лимонином. Однако соединение 4 показало бросающееся в глаза различие с лимонином в химических сдвигах протонов Н-С(15), Н-С(17) и Н-С(18). Протон Н-С(17) показал сильнопольный сдвиг от 5,48 м.д. (3) до 5,05 м.д. (4), тогда как для протонов Н-С(15) и Н-С(18) наблюдался слабопольный сдвиг от 4,21 и 1,11 м.д. (3) до 4,50 и 1,48 м.д. (4), соответственно. Кроме того, 2D-ЯМР эксперименты выявили различие в химических сдвигах С(17)/С(18), резонирующих при 77,9/20,0 м.д. для лимонина (3) и 85,1/27,1 м.д. для соединения (4), указывая таким образом на эпимеризацию лимонина в положении С(17) в структуре соединения 4. Принимая во внимание все спектроскопические данные, соединение 4 было впервые однозначно идентифицировано как С17-эпимер лимонина, имеющий фурановое кольцо при С(17) в β-ориентации в отличие от α-ориентации в лимонине. Хотя соединение 4, называемое С17-эпилимонином или изолимонином, ранее предполагалось в качестве метаболита лимонин-17-β-D-глюкопиранозида в плазме крови человека, это является первым подтверждением структуры данного эпимера лимонина на основании спектроскопических данных и демонстрацией его гидролитического высвобождения из глюкопиранозида.
В частности, раствор лимонин-17-β-D-глюкопиранозида (35 мг) в воде (20 мл) доводили до рН 1,5 с использованием следовых количеств соляной кислоты (1 моль/л) и выдерживали в течение 4 часов при 60ºС. После охлаждения раствор наносили на верхнюю часть уравновешенного водой картриджа Strata C18-E SPE (10 г, 55 мкм, Giga Tubes, Phenomex), затем быстро промывали водой (150 мл), затем смесью вода/метанол (50/50, об./об.; 100 мл) и метанолом (150 мл). Из метанольной фракции растворитель удаляли в вакууме, растворяли в смеси метанола и 1% водной муравьиной кислоты и аликвоты (100 мкл) разделяли с помощью полупрепаративной ВЭЖХ на колонке Microsorb-MV, RP-18, 250×10 мм, внутренний диаметр 5 мкм (Varian, Германия). При мониторинге эффлюентов с помощью УФ-детектора при 220 нм, а также ELSD, хроматографию проводили при градиенте растворителя, подающегося со скоростью потока 3,5 мл/мин, начиная со смеси (30/70, об./об.) ацетонитрила и 1% водной муравьиной кислоты, повышая содержание ацетонитрила до 40% в течение 15 минут, затем до 80% в течение 10 минут и, наконец, до 100% в течение 10 минут. Обнаружены два пика; эффлюенты, содержащие каждый из пиков, по отдельности собирали в охлаждаемые на льду колбы, растворитель удаляли в вакууме и затем подвергали лиофильной сушке. Выделенные соединения были идентифицированы с помощью ЖХ-МС и ЯМР экспериментов как лимонин и его ранее неизвестный стереоизомер С17-эпилимонин, также известный как изолимонин.
Лимонин, 3: УФ/виз (ацетонитрил/вода; рН 2,5): λмакс.=220 нм; ЖХ/МС (ESI+): m/z 509 ([M+K]+), 493 ([M+Na]+), 488 ([M+NH4]+); ЖХ/МС (ESI-): m/z 469 ([M-H]-); 1H-ЯМР (400 МГц, ДМСО-d6, COSY): δ 1,00 [c, 3H, H-C(24)], 1,02 [c, 3H, H-C(25b)], 1,11 [c, 3H, H-C(18)], 1,19 [c, 3H, H-C(25a)], 1,23 [м, 1H, H-C(12)], 1,73 [м, 2H, H-C(11)], 1,83 [м, 1H, H-C(12)], 2,27 [дд, 1H, J=3,0, 14,7 Гц, H-C(6)], 2,46 [дд, 1H, J=3,0, 15,7 Гц, H-C(5)], 2,55 [м, 1H, H-C(9)], 2,62 [м, 1H, H-C(2)], 2,77 [д, 1H, J=16,4 Гц, H-C(2)], 3,10 [т, 1H, J=15,5 Гц, H-C(6)], 4,11 [м, 1H, H-C(1)], 4,12 [c, 1H, H-C(15)], 4,48 [д, 1H, J=12,9 Гц, H-C(19)], 4,92 [д, 1H, J=12,9 Гц, H-C(19)], 5,48 [c, 1H, H-C(17)], 6,51 [c, 1H, H-C(22)], 7,66 [c, 1H, H-C(21)], 7,72 [c, 1H, H-C(23)]; 13C-ЯМР (100 МГц, MeOD-d4, HMQC, HMBC): δ 17,4 [C, C(24)], 18,1 [C, C(11)], 20,0 [C, C(18)], 20,4 [C, C(12)], 22,3 [C, C(25b)], 30,1 [C, C(25a)], 35,9 [C, C(2)], 36,5 [C, C(6)], 37,5 [C, C(13)], 45,7 [C, C(10)], 46,9 [C, C(9)], 50,5 [C, C(8)], 54,3 [C, C(15)], 58,2 [C, C(5)], 65,3 [C, C(19)], 67,4 [C, C(14)], 77,9 [C, C(17)], 78,9 [C, C(1)], 80,4 [C, C(4)], 110,9 [C, C(22)], 120,6 [C, C(20)], 141,9 [C, C(23)], 143,9 [C, C(21)], 168,7 [C, C(16)], 170,9 [C, C(3)], 208,5 [C, C(7)].
С17-эпилимонин, 4: УФ/виз (ацетонитрил/вода; рН 2,5): λмакс.=220 нм; ЖХ/МС (ESI+): m/z 509 ([M+K]+), 493 ([M+Na]+), 488 ([M+NH4]+); ЖХ/МС (ESI-): m/z 469 ([M-H]-); 1H-ЯМР (400 МГц, ДМСО-d6, COSY): δ 0,99 [c, 3H, H-C(24)], 0,99 [c, 3H, H-C(25b)], 1,19 [c, 3H, H-C(25a)], 1,44 [м, 1H, H-C(12)], 1,72 [м, 2H, H-C(11)], 2,00 [м, 1H, H-C(12)], 2,25 [дд, 1H, J=3,7, 16,2 Гц, H-C(6)], 2,66 [м, 1H, H-C(2)], 2,66 [м, 1H, H-C(5)], 2,73 [м, 1H, H-C(2)], 2,75 [м, 1H, H-C(9)], 2,91 [т, 1H, J=15,8 Гц, H-C(6)], 4,14 [д, 1H, J=3,68 Гц, H-C(1)], 4,50 [c, 1H, H-C(15)], 4,51 [д, 1H, J=13,2 Гц, H-C(19)], 4,78 [д, 1H, J=13,2 Гц, H-C(19)], 5,05 [c, 1H, H-C(17)], 6,62 [c, 1H, H-C(22)], 7,60 [c, 1H, H-C(21)], 7,70 [c, 1H, H-C(23)]; 13C-ЯМР (100 МГц, MeOD-d4 HMQC, HMBC): δ 18,3 [C, C(11)], 19,3 [C, C(24)], 22,1 [C, C(12)], 22,1 [C, C(25b)], 27,1 [C, C(18)], 30,6 [C, C(25a)], 36,6 [C, C(2)], 36,9 [C, C(6)], 40,3 [C, C(13)], 45,0 [C, C(9)], 45,1 [C, C(10)], 47,6 [C, C(8)], 56,3 [C, C(5)], 56,6 [C, C(15)], 65,4 [C, C(19)], 70,4 [C, C(14)], 79,1 [C, C(1)], 79,9 [C, C(4)], 85,1 [C, C(17)], 112,9 [C, C(22)], 122,4 [C, C(20)], 143,8 [C, C(21)], 144,2 [C, C(23)], 168,8 [C, C(16)], 170,5 [C, C(3)], 208,3 [C, C(7)].
Хотя авторы настоящего изобретения не хотели бы связываться с какой-либо теорией, на фиг.6 проиллюстрирован реакционный путь, показывающий образование лимонина (3) и изолимонина или С17-эпилимоинана (4) из лимонин-17-β-D-глюкопиранозида. Поскольку глюкоза представляет собой хорошую уходящую группу, гексоза отщепляется от α-положения фурфурилиденовой группы 1 в кислотных условиях, таким образом приводя к высвобождению делокализованного фурфурилиденового катиона в качестве основного недолговечного промежуточного соединения. Внутримолекулярная циклизация, индуцированная нуклеофильной атакой карбоксильной функции, затем приводит к образованию лимонина (3), содержащего фурановое кольцо в α-ориентации, а также изолимонин/С17-эпилимонина, для которого фурановое кольцо при С(17) имеет β-ори