Способ получения 1-ацетамидо-3,5-диметиладамантана
Иллюстрации
Показать всеИзобретение относится к области органической химии, в частности к способу получения 1-ацетамидо-3,5-диметиладамантана, который применяется в синтезе ряда труднодоступных производных 1,3-диметиладамантана, например 1-амино-3,5-диметиладамантана - действующего вещества лекарственного препарата «мемантина», уникального фармацевтического средства, эффективного для лечения болезни Паркинсона, дегенеративных заболеваний головного мозга, глаукомы, а также других нарушений ЦНС на ранних стадиях. Способ осуществляют путем взаимодействия 1-бром-3,5-диметиладамантана с ацетамидом в присутствии марганецсодержащих катализаторов, выбранных из ряда MnCl2, MnBr2, Mn(ОАс)2, Mn(асас)3, Mn2(СО)10. Взаимодействие проводят при температуре 120-130°С в течение 3-4 часов при мольном соотношении [1-бром-3,5-диметиладамантан]:[ацетамид]:[катализатор]= 100:150÷200:1÷3. Технический результат - упрощение технологии получения 1-ацетамидо-3,5-диметиладамантана при низком расходе катализатора. 1 табл., 1 пр.
Реферат
Изобретение относится к области органической химии, в частности к способу получения 1-ацетамидо-3,5-диметиладамантана.
1-Ацетамидо-3,5-диметиладамантан (1) находит применение в синтезе ряда труднодоступных производных. Так, из него снятием ацетильной защиты получают 1-амино-3,5-диметиладамантан - действующее вещество известного лекарственного препарата «мемантина». «Мемантин» - уникальный фармацевтический препарат, эффективный для лечения болезни Паркинсона, средство терапии дегенеративных заболеваний головного мозга, глаукомы, а также других нарушений ЦНС на ранних стадиях, способствует нормализации психической активности (улучшает память и способность к концентрации внимания, уменьшает утомляемость, симптомы депрессии и др.) и координирует двигательные нарушения (G.L. Wenk, S.L. Mobley. Eur. J. Pharm. Environ. V. 293, p. 267-270 (1995) [1]; L. Tursi, K.L. Retting, P.A. Loschman, H. Wachtel. Nature, V. 349, p. 414-418 (1991) [2]; К. Gerzon, E.V. Krumkans, R.L. Brindle, F.J. Marshall, M.A. Root. J. Med. Chem. V. 6, p. 760-763 (1963) [3]; P. Kovacic, P.D. Roskos. J. Am. Chem. Soc. V. 91, №23, p.6457-6460 (1969) [4]; A. Scherin, В. Homburg, D. Peteri, H. Markobel. US Patent 4,122,193 (1978) [5]).
Большинство методов получения ацетильного производного 1-аминоадамантана основано на реакции гидрокси- и галогенпроизводного адамантана с ацетонитрилом. Процесс обычно проводят в 5-10-кратном избытке ацетонитрила, который служит и реагентом, и растворителем.
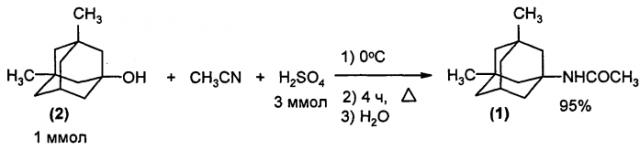
Так, в известном методе смесь 1-гидрокси-3,5-диметиладамантана (2) и ацетонитрила охлаждают до 0°С и добавляют конц. H2SO4. Выдерживают 4 часа при кипении с перемешиванием. После охлаждения реакционной смеси добавляют воду и отгоняют избыток ацетонитрила при пониженном давлении. Водный слой экстрагируют хлороформом, экстракты сушат Na2SO4, отгоняют растворитель и получают 1-ацетамидо-3,5-диметиладамантан (1) с выходом 95% (Т.С. Жук, Е.Ю. Братко, А.Е. Пащенко, П.А. Гунченко, А.Г. Юрченко, П.Р. Шрайнер, А.А. Фокин. Журнал орг.та фарм. хiмii, т. 8, вип. 1 (29), с. 62-66 (2010) [6]).
Недостатки метода:
1. Использование 3-кратного избытка конц. H2SO4.
2. Большое количество неорганических отходов, образующихся при нейтрализации избытка H2SO4.
1-Ацетамидо-3,5-диметиладамантан (1) получают при действии на 1-гидрокси-3,5-диметиладамантан (2) ацетонитрила в растворе трифторуксусной кислоты. Смесь 5 г 1-гидрокси-3,5-диметиладамантана (2), 7.5 мл ацетонитрила и 16 мл CF3CO2H выдерживают при 90-100°С в течение 10 ч и отгоняют CF3CO2H и ацетонитрил. К остатку добавляют 200 мл эфира и 50 мл насыщенного водного раствора поташа. Эфирный экстракт промывают водным раствором поташа, водой и сушат безводным Na2SO4. Эфир упаривают и получают 1-ацетамидо-3,5-диметиладамантан (1) с выходом 88% (В.М. Плахотник, В.Ю. Ковтун, В.Г. Яшунский. ЖОрХ, т. 18, вып. 5, с. 1001-1005 (1982) [7]).
Недостатки метода:
1. Использование большого избытка агрессивной и дорогостоящей трифторуксусной кислоты и необходимость ее нейтрализации.
2. Трудности с выделением целевого продукта из-за сильного разбавления реакционной массы растворителем.
Смесь 1-хлор-3,5-диметиладамантана (3) (150 г), ацетонитрила (275 мл) и ледяной уксусной кислоты (275 мл) помещают в стеклянный реактор при комнатной температуре, затем нагревают до 70±5°С и при этой температуре прибавляют по каплям конц. H2SO4 (166 мл) в течение 4 часов, все время поддерживая температуру реакционной смеси 70±5°С (реакция экзотермична). Смесь охлаждают до 25±5°С (водяная баня), экстрагируют толуолом. Выход соединения (1) составляет 97% (Е. Vigano, E. Landonio, S. Lanfranconi, R. Moltenl. EP 1721888 A1 (15.11.2006), Bulletin 2006/46 [8]).
Недостатки метода:
1. Использование стехиометрического количества конц. H2SO4 и уксусной кислоты.
2. Большое количество неорганических отходов и сточных вод, образующихся при нейтрализации избытка H2SO4 и СН3СООН, которые необходимо утилизировать.
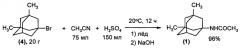
Смесь 20 г 1-бром-3,5-диметиладамантана (4), 75 мл ацетонитрила и 150 мл конц. H2SO4 выдерживают в течение ночи при комнатной температуре. Реакционную смесь выливают на измельченный лед, экстрагируют бензолом, экстракты сушат над NaOH, удаляют в вакууме растворитель и получают 18.2 г продукта (1) (J. Mills, E. Krumkals. US Patent 3,391,142 (02.07.1968) [9]; J.M. Reddy, G. Prasad, V. Raju, M. Ravikumar, V. Himabindu, G.M. Redy. Organic Process Research & Development. V. 11, p. 268-269 (2007) [10]; K. Gerzon, E.V. Krumkalns, R.L. Brindle, F.J. Marshall, M.A. Root. J. Med. Chem. V. 6, p. 760-763 (1963) [3]).
На основании сходства по двум признакам (исходный реагент - 1-бром-3,5-диметиладамантан и образование в результате реакции 1-ацетамидо-3,5-диметиладамантана) за прототип взят способ получения 1-ацетамидо-3,5-диметиладамантана взаимодействием 1-бром-3,5-диметиладамантана с ацетонитрилом в присутствии концентрированной серной кислоты [3, 9, 10].
Прототип имеет следующие недостатки:
1. Использование большого избытка ацетонитрила.
2. Использование 7-кратного избытка конц. серной кислоты.
3. Образование при нейтрализации избытка H2SO4 большого количества неорганических отходов и сточных вод, которые необходимо утилизировать.
Задачей настоящего изобретения является упрощение технологии получения 1-ацетамидо-3,5-диметиладамантана (1).
Авторами предлагается способ получения 1-ацетамидо-3,5-диметиладамантана (1), не имеющий недостатков, присущих прототипу.
Сущность способа заключается во взаимодействии 1-бром-3,5-диметиладамантана с ацетамидом под действием марганецсодержащих катализаторов, таких как MnCl2, или MnBr2, или Mn(ОАс)2, или Mn(асас)3, или Mn2(СО)10 при 120-130°С в течение 3-4 ч при мольном соотношении [1-бром-3,5-диметиладамантан]:[ацетамид]:[катализатор]=100: 150÷200:1÷3 без использования растворителя.
В оптимальных условиях при полной конверсии 1-бром-3,5-диметиладамантана единственным продуктом реакции является 1-ацетамидо-3,5-диметиладамантан (1).
Существенные отличия предлагаемого способа от прототипа:
1. 1-Ацетамидо-3,5-диметиладамантан (1) синтезируют взаимодействием 1-бром-3,5-диметиладамантана (4) с ацетамидом.
2. Для получения 1-ацетамидо-3,5-диметиладамантана (1) из 1-бром-3,5-диметиладамантана (4) и ацетамида используют марганецсодержащие катализаторы.
Преимущества предлагаемого метода:
1. Доступность катализатора.
2. Низкий расход катализатора (1-3%).
3. Уменьшение количества отходов.
4. Удешевление себестоимости и упрощение технологии в целом за счет использования в качестве катализатора доступных и недорогих реагентов - солей и комплексов марганца и уменьшения энерго- и трудозатрат.
Предлагаемый способ поясняется примерами.
Общая методика. В микроавтоклав из нержавеющей стали (V=17 мл) или стеклянную ампулу (V=20 мл) (результаты параллельных опытов практически не отличаются) помещали 0.1-0.3 ммоля марганецсодержащего катализатора [один из таких как MnCl2, MnBr2, Mn(ОАс)2, Mn(асас)2, Mn2(СО)10], 10 ммолей 1-бром-3,5-диметиладамантана и 15-20 ммолей ацетамида (CH3CONH2), автоклав герметично закрывали (ампулу запаивали) и нагревали при 120-130°С в течение 3-4 часов. После окончания реакции микроавтоклав (ампулу) охлаждали до ~20°С, вскрывали, реакционную массу выливали в воду, экстрагировали хлористым метиленом (5 мл × 3 раза), растворитель отгоняли, остаток кристаллизовали из гексана. Выход 1-ацетамидо-3,5-диметиладамантана 82-96%.
ПРИМЕР 1. В микроавтоклав помещали 0.3 ммоля Mn2(СО)10, 10 ммолей 1-бром-3,5-диметиладамантана, 20 ммолей CH3CONH2, автоклав герметично закрывали и нагревали при 120°С в течение 4 часов при перемешивании. После окончания реакции микроавтоклав охлаждали до комнатной температуры, вскрывали, после обработки реакционной массы, как указано выше, был выделен 1-ацетамидо-3,5-диметиладамантан с выходом 96%.
Полученный 1-ацетамидо-3,5-диметиладамантан имел т.пл. 109-110°С (гексан). ИК спектр (v, см-1): 3210 (NH), 1640 (С=O), 1545 (NH). Спектр ЯМР 13С (CDCl3, δ, м.д.): 53.38 (С1), 48.14 (С2,10), 32.35 (С3,5), 50.81 (С4), 42.87 (С6,9), 30.18 (С7), 40.82 (8), 30.35 (СН3), 160.86 (С=O). Найдено, %: С 75.39; Н 10.43; N 6.27. C14H23NO. Вычислено, %: С 75.96; Н 10.47; N 6.33.
Другие примеры, подтверждающие способ, приведены в таблице 1.
| Таблица 1 | |||||
| Результаты опытов по синтезу 1-ацетамидо-3,5-диметиладамантана 1) реакцией 1-бром-3,5-диметиладамантана (4) с ацетамидом под действием марганецсодержащих катализаторов | |||||
| №№ п/п | Катализатор | Мольное соотношение [1-Br-3,5-Me2Ad]:[CH3CONH2]:[Mn] | Температура, °С | Время реакции, ч | Выход 1-ацетамидо-3,5-диме-тиладаман-тана, % |
| 1 | 2 | 3 | 4 | 5 | 6 |
| 1. | MnCl2 | 100:200:3 | 130 | 3 | 82 |
| 2. | MnBr2 | -//- | -//- | -//- | 87 |
| 3. | Mn(ОАс)2 | -//- | -//- | -//- | 92 |
| 4. | Mn(асас)3 | -//- | -//- | -//- | 94 |
| 5. | -//- | 100:150:3 | -//- | -//- | 88 |
| 6. | -//- | 100:200:2 | -//- | -//- | 86 |
| 7. | -//- | 100:200:3 | 120 | 4 | 95 |
| 8. | Mn2(СО)10 | 100:200:3 | 130 | 3 | 96 |
| 9. | -//- | -//- | 120 | 4 | 92 |
| 10. | -//- | 100:150:3 | -//- | -//- | 93 |
| 11. | -//- | 100:300:1 | -//- | -//- | 82 |
| 12. | -//- | 100:300:2 | -//- | -//- | 89 |
Способ получения 1-ацетамидо-3,5-диметиладамантана (1) формулы из 1-бром-3,5-диметиладамантана в присутствии катализатора, отличающийся тем, что 1-бром-3,5-диметиладамантан взаимодействует с ацетамидом под действием марганецсодержащих катализаторов, выбранных из ряда MnCl2, MnBr2, Mn(ОАс)2, Mn(асас)3, Mn2(СО)10 при 120-130°С в течение 3-4 часов при мольном соотношении [1-бром-3,5-диметиладамантан]:[ацетамид]:[катализатор]=100:150÷200:1÷3.