Кристаллическая форма хидамида, способ ее получения и применение
Иллюстрации
Показать всеИзобретение относится к области фармацевтической химии и раскрывает две кристаллические формы хидамида, а именно, кристаллическую форму А хидамида и кристаллическую форму B хидамида, а также способ получения кристаллических форм А и В хидамида, их применение и фармацевтическую композицию на их основе. Технический результат: получены кристаллические формы A и В хидамида, которые обладают низкой токсичностью, стабильностью при хранении и обработке, а также имеют преимущество в отношении перорального всасывания и ингибирования клеточной дифференцировки и пролиферации. 7 н.п. ф-лы, 8 ил., 8 пр.
Реферат
Настоящая заявка испрашивает приоритет китайской патентной заявки №201210489178.8, поданной 27 ноября 2012 года в патентное ведомство Китая, озаглавленной «Кристаллическая форма хидамида, способ ее получения и применение», таким образом, включенной в данный документ путем ссылки полностью.
Техническая область изобретения
Настоящее изобретение относится к области фармацевтической химии, и конкретно к новым кристаллическим формам А и B хидамида, и способу их получения и применения.
Предшествующий уровень техники
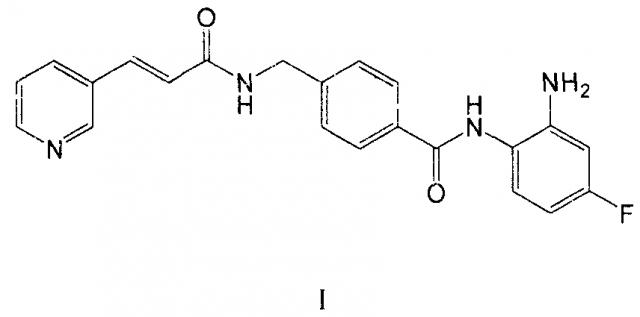
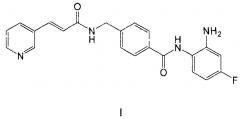
Хидамид является новым противораковым лекарственным средством, которое создано и синтезировано Chipscreen Co. Ltd. (Шенчжэнь, Китай) с полностью новой химической структурой и международными правами на интеллектуальную собственность. Химическим именем хидамида является N-(2-амино-4-фторфенил)-4-(N-(3-пиридилакрилоил)аминометил)бензамид, с химической структурой формулы:
Как описано в патенте ZL 03139760.3 и US 7244751, хидамид обладает ингибирующей активностью в отношении деацетилаз гистонов, и его можно использовать при лечении заболеваний, связанных с дифференцировкой и пролиферацией, таких как злокачественные опухоли и псориаз, и, в частности, он обладает отличной терапевтической эффективностью в отношении лейкоцитемии и солидных опухолей.
Хотя способ получения хидамида описан в патенте ZL 03139760.3 и US 7244751, не было указано, был ли продукт кристаллическим веществом, или для соединения был свойственен полиморфизм. В указанных выше патентах не была произведена оценка активности соединения в твердом состоянии, и таким образом, не было раскрыто описание, связанное с характеристиками кристалла.
Кристаллическая форма является одним из ключевых факторов, который влияет на качество, терапевтическую эффективность и производительность обработки рецептуры лекарственного вещества.
Полиморфизм относится к феномену, когда одно соединение может образовывать два или более молекулярных расположения в пространстве посредством контроля состояний и, таким образом, образовывать различные твердые кристаллы. Полиморфизм является распространенным феноменом при разработке лекарственного вещества, и является ключевым фактором, который влияет на качество лекарственного продукта. Для различных кристаллических форм соединения, хотя они имеют одинаковый химический состав, они обладают различными кристаллическими структурами, что приводит к различиям в их внешней морфологии, физико-химических свойствах и видах биологической активности. Различные кристаллические формы лекарственного вещества имеют тенденцию различаться по растворимости, стабильности хранения, гигроскопичности, плотности и биодоступности. Кристаллическая форма лекарственного вещества напрямую влияет на качество его фармацевтического состава и абсорбцию в организме человека, и таким образом влияет на соотношение терапевтический эффект/побочный эффект в организме человека. Таким образом, очень большое значение имеет исследование полиморфизма лекарственного вещества и способов получения различных кристаллических форм.
Сущность изобретения
Исходя из вышеуказанного, задачей настоящего изобретения является исследование, разработка и предоставление новых кристаллических форм хидамида, способ их получения и применение.
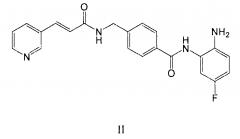
Чистота хидамида, полученного, как описано в примере 2 патента ZL 03139760.3 является низкой (приблизительно 95%). Как продемонстрировано результатами LC/MS на фиг. 1, продукт содержит 4,7% N-(2-амино-5-фторфенил)-4-(N-(3-пиридилакрилоил)аминометил)бензамида формулы II. Как продемонстрировано результатами 1H ЯМР на фиг. 2, продукт содержит 1,80% тетрагидрофурана, что гораздо выше, чем предел остатка растворителя (0,072%) для регистрируемого лекарственного вещества, как предписано Международной Конференцией по гармонизации (ICH). Таким образом, твердая форма не является подходящей для производства лекарственных продуктов.
Посредством кристаллографических способов две кристаллические формы хидамида, т.е. кристаллическая форма A хидамида и кристаллическая форма B хидамида, были исследованы, разработаны и представлены настоящим изобретением.
Новые кристаллические формы хидамида были исследованы и охарактеризованы посредством хорошо известного способа рентгеновской порошковой дифрактометрии (XRPD) в настоящем изобретении. Прибор: рентгеновский порошковый дифрактометр (D/MAX-1200). Условия для детекции: Cu/K-alphal (мишень), 40KV-40 мА (рабочее напряжение и вольт-амперная характеристика), I(max)=2244, 20=5-60° (диапазон сканирования), 0,005/0,06 сек (скорость сканирования) и λ=1,54056.
Кристаллическая форма A по существу чистого хидамида, представленная в настоящем документе, обладает паттерном рентгеновской порошковой дифракции, как представлено на фиг. 3. Она обладает следующими характеристиками: паттерн рентгеновской порошковой дифракции имеет пики при 2θ приблизительно 4,18°, 6,61°, 8,42°, 12,69°, 17,85°, 18,34°, 19,27°, 20,10°, 20,59°, 21,58°, 23,70°, 23,96°, 25,52°, 27,00°, 27,90°, 29,59° и 29,94°.
Настоящее изобретение дополнительно исследует и характеризует новую кристаллическую форму хидамида посредством инфракрасной спектрометрии (ИК). Прибор: FT-IR NICOLET 6700 (US). Измерение: KBr диск, спектральный диапазон: 400 см-1 - 4000 см-1, разрешение: 4 см-1.
Кристаллическая форма A по существу чистого хидамида, представленная в настоящем документе, обладает инфракрасным спектром, как представлено на фиг. 4. Он имеет следующие характеристики: инфракрасный спектр имеет пики характеристического поглощения при приблизительно 3412, 3282, 3199, 3043, 1654, 1615, 1524, 1514, 1497, 1442, 1418, 1332, 1296, 1234, 1198, 1183, 1166 и 1027 см-1.
Другие методы анализа, известные в данной области, также можно использовать, чтобы охарактеризовать кристаллическую форму, такие как дифференциальная сканирующая калориметрия (DSC). Прибор: DSC 204 (Германия), скорость изменения температуры: 10°C/мин, скорость потока азота: 20 мл/мин.
Кристаллическая форма A по существу чистого хидамида, представленная в настоящем документе, имеет паттерн дифференциальной сканирующей калориметрии, как продемонстрировано на фиг. 5, который обладает следующими характеристиками, так, что паттерн имеет эндотермический пик при приблизительно 239,4°C.
Кристаллическая форма В по существу чистого хидамида, представленная в настоящем документе, имеет паттерн рентгеновской порошковой дифракции, как продемонстрировано на фиг. 6. Он имеет следующие характеристики: паттерн рентгеновской порошковой дифракции имеет пики при 2θ приблизительно 4,18°, 8,43°, 12,65°, 16,90°, 17,83°, 19,47°, 20,13°, 20,58°, 21,22°, 21,54°, 21,92°, 23,94°, 25,55°, 26,98°, 27,92°, 29,58° и 29,90°.
Кристаллическая форма В по существу чистого хидамида, представленная в настоящем документе, имеет инфракрасный спектр, как продемонстрировано на фиг. 7. Он обладает следующими характеристиками: инфракрасный спектр имеет пики характеристического поглощения при приблизительно 3412, 3327, 3272, 3196, 3043, 1653, 1619, 1570, 1515, 1496, 1444, 1419, 1331, 1357, 1296, 1278, 1267, 1232, 1198, 1184, 1166 и 1038 см-1.
Кристаллическая форма В по существу чистого хидамида, представленная в настоящем документе, имеет паттерн дифференциальной сканирующей калориметрии, как продемонстрировано на Фиг. 8, который обладает следующими характеристиками, так, что паттерн имеет эндотермические пики при приблизительно 214,1°C и 241,2°C.
Следует отметить, что, в отношении пиков рентгеновской порошковой дифракции кристаллических форм, указанных выше, 2θ паттерна рентгеновской порошковой дифракции может приводить к небольшому изменению от одного прибора к другому, а также между одним образцом и другим. Их численные значения могут отличаться приблизительно на одну единицу, или приблизительно 0,8 единиц, или приблизительно 0,5 единиц, или приблизительно 0,3 единицы, или приблизительно 0,1 единицу. Таким образом, данные численные значения не надо рассматривать как абсолютные.
Экспериментальные результаты демонстрируют, что как кристаллическая форма A хидамида, так и кристаллическая форма В хидамида, описываемые в настоящем документе, имеют благоприятные характеристики в отношении растворимости, и, таким образом, имеют высокую биодоступность.
Настоящее изобретение дополнительно относится к способу получения кристаллической формы A хидамида и кристаллической формы В хидамида с высокой степенью чистоты (>99%) и не содержащих остаток растворителя.
Способ получения кристаллической формы A хидамида, представленный в настоящем документе, включает:
Стадия 1: хидамид добавляют к 2 моль/л разбавленному раствору соляной кислоты, растворяют посредством перемешивания при комнатной температуре и разбавляют водой; к полученному раствору добавляют по каплям 2 моль/л раствор NaOH, перемешивают в течение 30 мин, а затем отфильтровывают; где массовое отношение между хидамидом и разбавленным раствором соляной кислоты на стадии 1 находится в диапазоне от 1:4,2 до 1:4,4, массовое отношение между хидамидом и водой находится в диапазоне от 1:25 до 1:30, и массовое отношение между хидамидом и раствором NaOH находится в диапазоне от 1:2,5 до 1:2,7;
Стадия 2: полученное твердое вещество собирают и добавляют к воде; к смеси добавляют по каплям 2 моль/л раствор NaOH, перемешивают в течение 60 мин, а затем фильтруют; полученное твердое вещество собирают, промывают водой до значения pH от 5 до 7, а затем высушивают; где массовое отношение между хидамидом и водой на стадии 2 находится в диапазоне от 1:15 до 1:25, и массовое отношение между хидамидом и раствором NaOH находится в диапазоне от 1:1,5 до 1:2,0.
Предпочтительно, процесс сушки на стадии 2 представляет сушку в вакууме при 80°C в течение 24 часов.
Способ получения кристаллической формы В хидамида, представленный в настоящем документе, является следующим: кристаллическую форму A хидамида добавляют к диметилсульфоксиду и растворяют посредством перемешивания при комнатной температуре; к полученному раствору добавляют по каплям воду, перемешивают в течение 30 мин, а затем фильтруют; полученное твердое вещество собирают и высушивают с получением указанного соединения; где массовое отношение между кристаллической формой A хидамида и диметилсульфоксидом находится в диапазоне от 1:10 до 1:20, и массовое отношение между кристаллической формой A хидамида и водой находится в диапазоне от 1:100 до 1:200.
Предпочтительно, процесс сушки представляет сушку в вакууме при 80°C в течение 24 часов.
Степень чистоты кристаллической формы A и кристаллической формы В, полученных способами получения кристаллической формы A и кристаллической формы В хидамида, описываемых в настоящем документе, составляла для обеих форм >99,0%.
Стабильность кристаллической формы A хидамида и кристаллической формы В хидамида, описываемых в настоящем документе, тестировали при высокой температуре (60°C), высокой влажности (90%±5%) и воздействии сильного света (4500Lx±500Lx). Результаты показали, что кристаллическая форма A хидамида и кристаллическая форма В хидамида сохраняют исходную кристаллическую форму, и никакого значительного изменения не наблюдали для содержимого и общего количества примеси. Как кристаллическая форма A хидамида, так кристаллическая форма В хидамида являются подходящими для производства лекарственных продуктов и длительного хранения. Кристаллическая форма A хидамида и кристаллическая форма В хидамида, описываемые в настоящем документе, обладают превосходными характеристиками в отношении перорального всасывания и ингибирования клеточной дифференцировки и пролиферации. Дополнительно, обе кристаллические формы обладают низкой токсичностью и благоприятной стабильностью при хранении и обработке, и их можно использовать при получении лекарственного средства для лечения заболеваний, связанных с клеточной дифференцировкой и пролиферацией. Таким образом, настоящее изобретение относится к применению кристаллической формы A хидамида и кристаллической формы В хидамида при получении лекарственного средства для лечения заболеваний, связанных с клеточной дифференцировкой и пролиферацией.
Дополнительно, заболевания, связанные с клеточной дифференцировкой и пролиферацией, выбраны из рака и псориаза, где рак включает лейкоцитемию и солидные опухоли.
Новые кристаллические формы хидамида, описываемые в настоящем документе, могут быть дополнительно получены в различных твердых дозированных формах для перорального введения, таких как таблетка, капсула или гранула.
Фармацевтическая композиция для лечения заболеваний, связанных с клеточной дифференцировкой и пролиферацией, описываемая в настоящем документе, содержит кристаллическую форму A хидамида или/и кристаллическую форму B хидамида, и фармацевтически приемлемые эксципиенты. В некоторых вариантах осуществления фармацевтическая композиция содержит кристаллическую форму A хидамида и фармацевтически приемлемые эксципиенты; и в некоторых вариантах осуществления фармацевтическая композиция содержит кристаллическую форму В хидамида и фармацевтически приемлемые эксципиенты; и в некоторых вариантах осуществления фармацевтическая композиция содержит смесь кристаллической формы А хидамида и кристаллической формы B хидамида и фармацевтически приемлемые эксципиенты.
В некоторых конкретных вариантах осуществления композиция содержит 5-20% кристаллической формы A хидамида или/и кристаллической формы B хидамида, и 80-95% фармацевтически приемлемых эксципиентов. В некоторых дозированных формах активное соединение смешивали с, по меньшей мере, одним из фармацевтически приемлемых инертных эксципиентов или носителей, таких как цитрат натрия, фосфат кальция, наполнитель, адгезив, увлажнитель, дезинтегрант, замедлитель, усилитель всасывания, средство для смачивания, абсорбент или лубрикант и их смесь. Примеры наполнителя включают крахмал, лактозу, сахарозу, глюкозу, маннит и кремниевую кислоту; примеры адгезива включают карбоксиметилцеллюлозу, альгинат, желатин, поливинилпирролидон, сахарозу и гуммиарабик; пример увлажнителя включает глицерин; примеры дезинтегранта включают агар, карбонат кальция, картофельный крахмал или манниоковый крахмал, альгиновую кислоту, некоторые силикаты и карбонаты натрия, низко замещенную гидроксипропилцеллюлозу; пример замедляющего реакцию раствора включает парафин; пример усилителя всасывания включают четвертичные аммониевые соединения; примеры средств для смачивания включают гексадеканол и моностеарат глицерина; примеры абсорбента включают каолин и бентонит; примеры лубриканта включают порошок талька, стеарат кальция, стеарат магния, твердый полиэтиленгликоль и лаурилсульфат натрия.
Краткое описание чертежей
На фиг. 1 продемонстрирована ВЭЖХ хроматограмма твердого вещества, полученного в соответствии с примером 2 патента ZL 03139760.3;
На фиг. 2 продемонстрирован спектр 1H ЯМР твердого вещества, полученного в соответствии с примером 2 патента ZL 03139760.3;
На фиг. 3 продемонстрирован паттерн рентгеновской порошковой дифракции кристаллической формы A хидамида, представленной в примере 1 настоящего изобретения, который получен посредством облучения куперовским Kα лучом. В паттерне рентгеновской порошковой дифракции ордината представляет интенсивность дифракции, выраженную в единицах на секунды (cps), и абсцисса представляет угол дифракции 2θ, выраженный в градусах;
На фиг. 4 продемонстрирован паттерн инфракрасного спектра кристаллической формы A хидамида, представленной в примере 1 настоящего изобретения. Ордината представляет светопропускание (T), выраженное в процентах (%); и абсцисса представляет волновое число, выраженное в см-1;
На фиг. 5 представлен паттерн дифференциальной сканирующей калориметрии (DSC) кристаллической формы A хидамида, представленной в примере 1 настоящего изобретения. Ордината представляет скорость теплового потока, выраженную в калориях/сек, и абсцисса представляет температуру, выраженную в °C;
На фиг. 6 продемонстрирован паттерн рентгеновской порошковой дифракции кристаллической формы В хидамида, представленной в примере 3 настоящего изобретения, который получен посредством облучения куперовским лучом Kα. В паттерне рентгеновской порошковой дифракции ордината представляет интенсивность дифракции, выраженную в единицах в секунду (cps), и абсцисса представляет угол дифракции 2θ, выраженный в градусах;
На фиг. 7 продемонстрирован инфракрасный спектр кристаллической формы В хидамида, представленной в примере 3 настоящего изобретения. Ордината представляет светопропускание (T), выраженное в процентах (%); и абсцисса представляет волновое число, выраженное в см-1.
На фиг. 8 продемонстрирован паттерн дифференциальной сканирующей калориметрии (DSC) кристаллической формы В хидамида, представленной в примере 3 настоящего изобретения. Ордината представляет скорость теплового потока, выраженную в калориях/сек, и абсцисса представляет температуру, выраженную в °C.
ПРИМЕРЫ
Кристаллические формы хидамида и способы их получения и применение описаны в примерах настоящего изобретения. Настоящее изобретение может быть осуществлено посредством надлежащей модификации параметров обработки специалистами в данной области со ссылкой на содержание настоящего документа. Конкретно, следует отметить, что все сходные перестановки и модификации являются очевидными специалистам в данной области, и все из которых предназначены быть включенными в настоящее изобретение. Способ настоящего изобретения описан посредством предпочтительных примеров, и является очевидным, что модификация или надлежащее изменение и их сочетание могут быть произведены способом, описываемым в настоящем документе, специалистами в данной области, без отступления от содержания, существа и объема изобретения, чтобы достичь и применить способы, описанные в настоящем изобретении.
Для лучшего понимания настоящего изобретения оно будет дополнительно описано со ссылкой на конкретные примеры ниже. Процент, описываемый в настоящем документе, относится к массовой доле, если не указано иначе. Все численные диапазоны, такие как единицы измерения, условия реакции, и физические состояния или процентные содержания соединений, описанные в данном описании, представлены для ясной ссылки. Ожидаемые результаты также могут быть достигнуты специалистами в данной области, когда настоящее изобретение практикуется с температурами, концентрациями или количествами и т.д. за пределами диапазона или отличными от индивидуальных значений.
Способы экспериментов:
Условия проведения испытаний для рентгеновской порошковой дифракции: Прибор: D/MAX-1200 (Япония); источник радиации: Cu-Kα (40kV, 40mA).
Условия проведения испытаний для инфракрасного спектра: Прибор: FT-IR NICOLET 6700 (US); KBr диск.
Условия проведения испытаний для дифференциальной сканирующей калориметрии: Прибор: DSC 204 (Германия); скорость изменения температуры: 10°C/мин; скорость потока азота: 20 мл/мин.
Условия проведения испытаний для протонного магнитного резонанса: Прибор: AV-400 (Германия); Растворитель: DMSO-d6.
Пример 1
Получение кристаллической формы А хидамида
4,84 кг хидамида (приблизительно 95% чистоты) добавляли к 20,91 кг 2 моль/л разбавленного раствора соляной кислоты и растворяли посредством перемешивания при комнатной температуре. Затем 137,8 кг воды добавляли и перемешивали в течение 5 мин. К полученному раствору по каплям добавляли 12,35 кг 2 моль/л раствора NaOH, перемешивали в течение 30 мин и фильтровали. Полученное твердое вещество добавляли к 96,70 кг воды, и затем по каплям добавляли 8,39 кг 2 моль/л раствора NaOH. Смесь перемешивали в течение 60 мин, фильтровали, и промывали водой до значения рН 5-7. Полученное твердое вещество сушили в вакууме при 80°С в течение 24 часов с получением 4,32 кг кристаллической формы А хидамида с чистотой 99,2%. Паттерн рентгеновской порошковой дифракции, инфракрасный спектр и паттерн дифференциальной сканирующей калориметрии кристаллической формы представлены на фиг. 3, фиг. 4 и фиг. 5, соответственно.
Пример 2
Получение кристаллической формы В хидамида
1 г кристаллической формы А хидамида добавляли к 10 мл диметилсульфоксида и растворяли посредством перемешивания при комнатной температуре. К полученному раствору по каплям добавляли 100 мл воды, перемешивали в течение 30 мин и фильтровали. Полученное твердое вещество сушили в вакууме при 80°С в течение 24 часов с получением кристаллической формы В хидамида с чистотой 99,2%. Паттерн рентгеновской порошковой дифракции, инфракрасный спектр и паттерн дифференциальной сканирующей калориметрии кристаллической формы продемонстрированы на фиг. 6, фиг. 7 и фиг. 8, соответственно.
Пример 3
Получение таблеток кристаллической формы А хидамида
Рецептура (1000 таблеток):
| Кристаллическая форма А хидамида | 5 г |
| Растворимый крахмал | 50 г |
| Лактоза | 20 г |
| Микрокристаллическая целлюлоза | 20 г |
| Карбоксиметилкрахмал натрия | 8 г |
| Порошок талька | 0,5 г |
Способ получения: кристаллическая форма A хидамида, лактоза, растворимый крахмал, микрокристаллическая целлюлоза и карбоксиметилкрахмал натрия каждый были отвешены в предписанном количестве и смешаны до однородного состояния. Смесь была смочена подходящим количеством воды для получения мягкого теста. Влажные частицы получали с применением 20-меш сита и сушили при 60°C. Частицы просеивали с применением 18-меш сита. Затем порошок талька добавляли в предписанном количестве и смешивали до однородного состояния. Таблетки получали после таблетирования.
Пример 4
Получение капсул кристаллической формы А хидамида
Рецептура (1000 капсул):
| Кристаллическая форма A хидамида | 5 г |
| Микрокристаллическая целлюлоза | 55 г |
| Лактоза | 35 г |
| Карбоксиметилкрахмал натрия | 5 г |
| Стеарат магния | 0,5 г |
Способ получения: кристаллическая форма A хидамида была профильтрована посредством пропускания через 100-меш сито, и микрокристаллическая целлюлоза, лактоза, карбоксиметилкрахмал натрия и стеарат магния были профильтрованы посредством пропускания через 80-меш сито. Микрокристаллическую целлюлозу, лактозу и карбоксиметилкрахмал натрия взвешивали в предписанных количествах и смешивали до однородного состояния. Затем смесь смешивали с кристаллической формой A хидамида до однородного состояния с применением способа равномерного повышения количества. После смешивания с предписанным количеством стеарата магния заполняли капсулы.
Пример 5
Получение гранул кристаллической формы А хидамида
Рецептура (1000 пакетиков):
| Хидамид кристаллическая A форма | 5 г |
| Растворимый крахмал | 500 г |
| Лактоза | 200 г |
| Микрокристаллическая целлюлоза | 175 г |
| Натрий карбоксиметилкрахмал | 100 г |
Способ получения: кристаллическая форма A хидамида, лактоза, растворимый крахмал, микрокристаллическая целлюлоза и карбоксиметилкрахмал натрия каждый были взвешены в предписанных количествах и смешаны до однородного состояния. Смесь смачивали посредством подходящего количества воды для получения мягкого теста. Влажные частицы получали с применением 20-меш сита и сушили при 60°C. Частицы фильтровали с применением 18-меш сита. После заполнения получали гранулы.
Пример 6
Получение таблеток кристаллической формы В хидамида
Рецептура (1000 таблеток):
| Кристаллическая форма В хидамида | 5 г |
| Растворимый крахмал | 50 г |
| Лактоза | 20 г |
| Микрокристаллическая целлюлоза | 20 г |
| Карбоксиметилкрахмал натрия | 8 г |
| Порошок талька | 0,5 г |
Способ получения: кристаллическая форма B хидамида, лактоза, растворимый крахмал, микрокристаллическая целлюлоза и карбоксиметилкрахмал натрия каждый были взвешены в предписанном количестве и смешаны до однородного состояния. Смесь смачивали посредством подходящего количества воды для получения мягкого теста. Влажные частицы фильтровали с применением 20-меш сита и сушили при 60°C. Частицы фильтровали с применением 18-меш сита. Затем порошок талька добавляли в предписанном количестве и смешивали до однородного состояния. Таблетки получали после таблетирования.
Пример 7
Получение капсул кристаллической формы В хидамида
Рецептура (1000 капсул):
| Кристаллическая форма В хидамида | 5 г |
| Микрокристаллическая целлюлоза | 55 г |
| Лактоза | 35 г |
| Карбоксиметилкрахмал натрия | 5 г |
| Стеарат магния | 0,5 г |
Способ получения: кристаллическая форма В хидамида была профильтрована посредством пропускания через 100-меш сито, и микрокристаллическую целлюлозу, лактозу, карбоксиметилкрахмал натрия и стеарат магния просеивали посредством пропускания через 80-меш сито. Микрокристаллическую целлюлозу, лактозу и карбоксиметилкрахмал натрия взвешивали в предписанных количествах и смешивали до однородного состояния. Затем смесь смешивали с кристаллической формой A хидамида до однородного состояния посредством способа равного повышения количеств. После смешивания с предписанным количеством стеарата магния капсулы заполняли.
Пример 8
Получение гранул кристаллической формы В хидамида
Рецептура (1000 пакетиков):
| Кристаллическая форма В хидамида | 5 г |
| Растворимый крахмал | 500 г |
| Лактоза | 200 г |
| Микрокристаллическая целлюлоза | 175 г |
| Карбоксиметилкрахмал натрия | 100 г |
Способ получения: кристаллическую форму B хидамида, лактозу, растворимый крахмал, микрокристаллическую целлюлозу и карбоксиметилкрахмал натрия каждый взвешивали в предписанных количествах и смешивали до однородного состояния. Смесь смачивали подходящим количеством воды для получения мягкого теста. Влажные частицы просеивали с применением 20-меш сита и сушили при 60°C. Частицы просеивали посредством 18-меш сита. После этого гранулы заполняли.
Вышеуказанные примеры описаны только для понимания способов и основных концепций настоящего изобретения. Следует отметить, что некоторые улучшения и модификации могут быть сделаны в настоящем изобретении специалистами в данной области без отклонения от принципов настоящего изобретения. Эти улучшения и модификации также находятся пределах объема формулы изобретения настоящего изобретения.
1. Кристаллическая форма А хидамида, которая характеризуется тем, что ее паттерн рентгеновской порошковой дифракции имеет характеристические пики при 2θ приблизительно 4,18°, 6,61°, 8,42°, 12,69°, 17,85°, 18,34°, 19,27°, 20,10°, 20,59°, 21,58°, 23,70°, 23,96°, 25,52°, 27,00°, 27,90°, 29,59° и 29,94°; ее инфракрасный спектр имеет характеристические пики поглощения при приблизительно 3412, 3282, 3199, 3043, 1654, 1615, 1524, 1514, 1497, 1442, 1418, 1332, 1296, 1234, 1198, 1183, 1166 и 1027 см-1; и ее паттерн дифференциальной сканирующей калориметрии имеет эндотермический пик при приблизительно 239,4°С.
2. Способ получения кристаллической формы А хидамида по п.1, который характеризуется тем, что способ включает:Стадия 1: хидамид добавляют к 2 моль/л разбавленного раствора соляной кислоты, растворяют посредством перемешивания при комнатной температуре и разбавляют водой; к полученному раствору добавляют по каплям 2 моль/л раствор NaOH, перемешивают в течение 30 мин, а затем фильтруют; где массовое отношение между хидамидом и разбавленным раствором соляной кислоты на стадии 1 находится в диапазоне от 1:4,2 до 1:4,4, массовое отношение между хидамидом и водой находится в диапазоне от 1:25 до 1:30, и массовое отношение между хидамидом и раствором NaOH находится в диапазоне от 1:2,5 до 1:2,7;Стадия 2: полученное твердое вещество собирают и добавляют к воде; к смеси добавляют по каплям 2 моль/л раствор NaOH, перемешивают в течение 60 мин, а затем фильтруют; полученное твердое вещество собирают, промывают водой до значения рН от 5 до 7, а затем сушат; где массовое отношение между хидамидом и водой на стадии 2 находится в диапазоне от 1:15 до 1:25, и массовое отношение между хидамидом и раствором NaOH находится в диапазоне от 1:1,5 до 1:2,0.
3. Применение кристаллической формы А хидамида по п.1 при получении лекарственного средства для лечения заболеваний, связанных с клеточной дифференцировкой и пролиферацией.
4. Кристаллическая форма В хидамида, которая характеризуется тем, что ее паттерн рентгеновской порошковой дифракции имеет пики при 2θ приблизительно 4,18°, 8,43°, 12,65°, 16,90°, 17,83°, 19,47°, 20,13°, 20,58°, 21,22°, 21,54°, 21,92°, 23,94°, 25,55°, 26,98°, 27,92°, 29,58° и 29, 90°; ее инфракрасный спектр имеет характеристические пики поглощения при приблизительно 3412, 3327, 3272, 3196, 3043, 1653, 1619, 1570, 1515, 1496, 1444, 1419, 1331, 1357, 1296, 1278, 1267, 1232, 1198, 1184, 1166 и 1038 см-1; и ее паттерн дифференциальной сканирующей калориметрии имеет эндотермические пики при приблизительно 214,1°С и 241,2°С.
5. Способ получения кристаллической формы В хидамида по п.4, который характеризуется тем, что кристаллическую форму А хидамида добавляют к диметилсульфоксиду и растворяют посредством перемешивания при комнатной температуре; к полученному раствору добавляют по каплям воду, перемешивают в течение 30 мин, а затем фильтруют; полученное твердое вещество собирают и сушат с получением указанного соединения; где массовое отношение между кристаллической формой А хидамида и диметилсульфоксидом находится в диапазоне от 1:10 до 1:20, и массовое отношение между кристаллической формой А хидамида и водой находится в диапазоне от 1:100 до 1:200.
6. Применение кристаллической формы В хидамида по п.4 при получении лекарственного средства для лечения заболеваний, связанных с клеточной дифференцировкой и пролиферацией.
7. Фармацевтическая композиция для лечения заболеваний, связанных с клеточной дифференцировкой пролиферацией, которая характеризуется тем, что содержит кристаллическую форму А хидамида по п.1 в эффективном количестве или/и кристаллическую форму В хидамида по п.4 в эффективном количестве, и фармацевтически приемлемые эксципиенты.