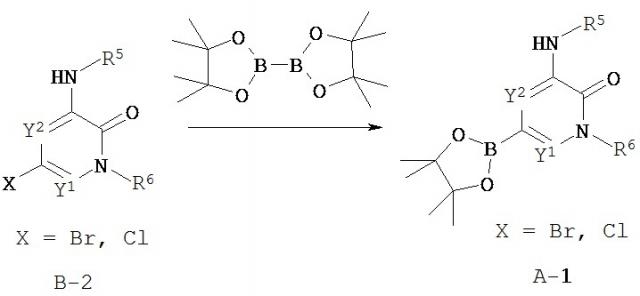
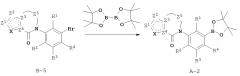
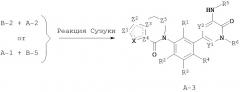
Пиридоновые и азапиридоновые соединения и способы применения
Иллюстрации
Показать всеИзобретение относится к соединению, выбранному из формулы I, или его стереоизомерам, или фармацевтически приемлемым солям, где R1 представляет собой необязательно замещенный C1-С3 алкил; R2, R3 и R4 независимо выбраны из Н, F, Cl; R5 выбран из (i) необязательно замещенного C6-С20 арила, выбранного из фенила; (ii) необязательно замещенного С5-С20 гетероарила, выбранного из пиразолила, пиридинила, пиримидинила, тетрагидроизохинолинила, 4,5,6,7-тетрагидропиразоло[1,5-а]пиразинила, 6,7-дигидро-4Н-пиразоло[5,1-с][1,4]оксазинила, 4,6,7-тригидропиразоло[3,2-с][1,4]оксазинила, 5,6,7,8-тетрагидро-1,6-нафтиридинила, 2,3-дигидро-1Н-изоиндолила, 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинила; (iii) необязательно замещенного -(C6-С20 арил)-(C3-С20 гетероциклила), где гетероциклил выбран из азетидинила, пиперидинила, морфолино, пиперазинила; (iv) необязательно замещенного -(С5-С20 гетероарил)-(C3-С20 гетероциклила), где гетероарил выбран из пиридинила и пиридазинила и гетероциклил выбран из азетидинила, пирролидинила, пиперидинила, пиперазинила, 1,4-диазепанила, 2,6-диазаспиро[3.3]гептанила, 7,9-диазабицикло[3.3.1]нонанила, гексагидропирроло[3,4-с]пирролила, морфолино; (v) необязательно замещенного -(C5-С20 гетероарил)-(C1-С6 алкила), где гетероарил выбран из пиразолила и пиридинила; или (vi) необязательно замещенного -(C5-С20 гетероарил)-С(=O)-(C3-С20 гетероциклила), выбранного из (пиридинил)-С(=O)-(морфолино); R6 представляет собой Н или C1-С3 алкил; Y1 и Y2 независимо выбраны из CR6 и N; где C1-С3 алкил, C3-С20 гетероциклил, C6-С20 арил и C5-С20 гетероарил необязательно замещены от одной до трех групп, независимо выбранных из D, F, Cl, Br, I, -СН3, -СН2СН3, -СН2СН(СН3)2, -СН2ОН, -СН2СН2ОН, -С(СН3)2ОН, -CH2F, -ОС(O)СН3, -СОСН3, -NHCH3, -N(CH3)2, =O, -ОН, -ОСН3, -OCH2CH2N(CH3)2, -ОР(O)(ОН)2, -СН2ОСН3, циклопропила, азетидинила, 1-(метилазетидин-3-ил)окси, N-метил-N-оксетан-3-иламино, азетидин-1-илметила, оксетанила и морфолино; где группа (а), образованная Z1, Z2, Z3, Z4, Z5, X и NC(O), образует структуры, приведенные в формуле изобретения, и при этом волнистая линия указывает на место присоединения. Изобретение относится к фармацевтической композиции для лечения состояния, опосредованного тирозинкиназой Брутона, содержащей соединение формулы (I) и фармацевтически приемлемый носитель, скользящее вещество, разбавитель или наполнитель. Соединения формулы (I) предназначены для применения в качестве лекарственного средства для лечения рака, опосредуемого тирозинкиназой Брутона. Технический результат – пиридоновые и азапиридоновые соединения для лечения нарушений, опосредованных тирозинкиназой Брутона (Btk). 7 н. и 13 з.п. ф-лы, 9 ил., 4 табл., 907 пр.
(а)
Реферат
| ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ |
Настоящая заявка, не являющаяся предварительной, подана в соответствии с параграфом 1.53(b) главы 37 свода федеральных нормативных актов США, испрашивает приоритет в соответствии с параграфом 119(е) главы 35 Свода законов Соединенных Штатов Америки на основании предварительной заявки на патент США 61443952, поданной 17 февраля 2011, и предварительной заявки на патент США 61332353, поданной 7 мая 2010, содержание которых полностью включено в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к соединениям для лечения нарушений, опосредованных тирозинкиназой Брутона (Btk), включая воспаление, иммунологические нарушения и рак, и, в частности, к соединениям, ингибирующим активность Btk. Изобретение также относится к способам применения указанных соединений для in vitro, in situ и in vivo диагностики или лечения клеток млекопитающего или сопутствующих патологических состояний.
УРОВЕНЬ ТЕХНИКИ
Протеинкиназы - самое большое семейство человеческих ферментов - включают более 500 белков. Тирозинкиназа Брутона (Btk) является представителем Тес-семейства тирозинкиназ и регулятором раннего развития В-клеток, а также активации, передачи сигнала и выживаемости зрелых В-клеток.
Передача сигнала В-клеток через В-клеточный рецептор (BCR) может приводить к широкому спектру биологических явлений, которые, в свою очередь, зависят от стадии развития В-клеток. Величина и продолжительность сигналов BCR должна точно регулироваться. Аберрантная BCR-опосредованная передача сигнала может вызывать нарушение регуляции активации В-клеток и/или образование патогенных аутоантител, приводящих к множественным аутоиммунным и/или воспалительным заболеваниям. Мутация Btk у человека приводит к сцепленной с X-хромосомой агаммаглобулинемии (XLA). Указанное заболевание связано с нарушенным созреванием В-клеток, сниженной выработкой иммуноглобулина, аномальным независимым от Т-клеток иммунным ответам и заметному снижению постоянного кальциевого сигнала при стимуляции BCR.
Доказательство роли Btk в аллергических заболевания и/или аутоиммунных заболеваниях и/или воспалительных заболеваниях было получено в моделях на Btk-дефицитных мышах. Например, в стандартных доклинических моделях системной красной волчанки (СКВ) на мышах было показано, что дефицит Btk приводит к заметному ослаблению развития заболевания. Кроме того, мыши с дефицитом Btk также могут быть устойчивы к развитию коллаген-индуцированного артрита и могут быть менее восприимчивы к стафилококк-индуцированному артриту.
Большое количество данных подтверждает роль В-клеток и гуморальной иммунной системы в патогенезе аутоиммунных и/или воспалительных заболеваний. Белковые лекарственные средства (такие как Ритуксан), разработанные для истощения В-клеток, представляют собой один из подходов к лечению ряда аутоиммунных и/или воспалительных заболеваний. Вследствие роли Btk в активации В-клеток ингибиторы Btk могут подходить для применения в качестве ингибиторов патогенной активности, опосредованной В-клетками (такой как выработка аутоантител).
Btk также экспрессируется в остеокластах, тучных клетках и моноцитах, и, как было показано, важна для функционирования данных клеток. Например, дефицит Btk у мышей связан с нарушенной IgE-опосредованной активацией тучных клеток (заметное снижение высвобождения ФНО-альфа и других воспалительных цитокинов), а дефицит Btk у людей связан со значительно сниженной выработкой ФНО-альфа активированными моноцитами.
Таким образом, ингибирование активности Btk может быть полезным для лечения аллергических нарушений и/или аутоиммунных и/или воспалительных заболеваний, таких как: СКВ, ревматоидный артрит, множественные васкулиты, идиопатическая тромбоцитопеническая пурпура (ITP), миастения, аллергический ринит и астма. Кроме того, сообщалось, что Btk вовлечен в апоптоз; таким образом, ингибирование активности Btk может быть полезным при раке, а также для лечения В-клеточной лимфомы и лейкемии. Кроме того, с учетом роли Btk в функции остеокластов, ингибирование активности Btk может быть полезным для лечения костных нарушений, таких как остеопороз.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение в целом относится к соединениям формулы I, обладающим модулирующей активностью по отношению к тирозинкиназе Брутона (Btk).
Соединения формулы I имеют следующие структуры:
включая их стереоизомеры, таутомеры или фармацевтически приемлемые соли. Различные заместители определены в настоящем документе ниже.
Согласно одному аспекту, изобретение представляет собой фармацевтическую композицию, содержащую соединение формулы I и фармацевтически приемлемый носитель, скользящее вещество, разбавитель или наполнитель. Фармацевтическая композиция может дополнительно содержать второй терапевтический агент.
Согласно другому аспекту, изобретение представляет собой способ получения фармацевтической композиции, включающий комбинирование соединения формулы I с фармацевтически приемлемым носителем.
Изобретение включает способ лечения заболевания или нарушения, включающий введение терапевтически эффективного количества соединения формулы I пациенту с заболеванием или нарушением, выбранным из иммунологических нарушений, рака, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, нарушений метаболической/эндокринной функции, неврологических нарушений и опосредованных тирозинкиназой Брутона.
Изобретение включает набор для лечения состояний, опосредованных тирозинкиназой Брутона, содержащий: а) первую фармацевтическую композицию, содержащую соединение формулы I; и b) инструкции по применению.
Изобретение включает соединение формулы I для применения в качестве лекарственного средства и для применения для лечения заболевания или нарушения, выбранного из иммунологических нарушений, рака, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, нарушений метаболической/эндокринной функции, неврологических нарушений и опосредованных тирозинкиназой Брутона.
Изобретение включает применение соединения формулы I для получения лекарственного средства для лечения иммунологических нарушений, рака, сердечно-сосудистого заболевания, вирусной инфекции, воспаления, нарушений метаболической/эндокринной функции и неврологических нарушений, и где указанное лекарственное средство опосредует тирозинкиназу Брутона.
Изобретение включает способы получения соединения формулы I.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фигуре 1 показан типичный способ синтеза для получения 6-хлор,4-амино пиридазиноновых соединений, включая 6-хлор-4-(5-метил-4,5,6,7-тетрагидропиразоло[1,5-a]пиразин-2-иламино)пиридазин-3(2H)-он 101f, из 3-нитропиразол-5-карбоновой кислоты.
На Фигуре 2 показан типичный способ синтеза трициклических амид-фенильных боронатных соединений, включая 2-(2-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)-3,4,6,7,8,9-гексагидропиразино[1,2-а]индол-1(2H)-он 101m, из 4,5,6,7-тетрагидро-1Н-индола.
На Фигуре 3 показан типичный способ синтеза трициклических амид-фенильных бромидных соединений, включая 2-бром-6-(1-оксо-3,4,5,6,7,8-гексагидробензотиено[2,3-с]пиридин-2(1H)-ил)бензилацетат 104h, из 4,5,6,7-тетрагидробензо[b]тиофен-2-карбоновой кислоты.
На Фигуре 4 показан другой типичный способ синтеза трициклических амид-фенильных бромидных соединений, включая 6,б-диметил-3,4,6,7-тетрагидро-5H-циклопента[4,5]тиено[2,3-с]пиридин-1(2H)-он 105i, из 3-метилциклопент-2-енона.
На Фигуре 5 показан типичный способ синтеза трициклических соединений 1,6-дигидропиридин-3-ил)фенил)-3,4,6,7,8,9-гексагидропиридо[3,4-b]индолизин-1(2Н)-она в виде боронатных эфиров, включая 2-(1-оксо-3,4,6,7,8,9-гексагидропиридо[3,4-6]индолизин-2(1H)-ил)-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензилацетат 118f из 5,6,7,8-тетрагидроиндолизин-2-карбоновой кислоты.
На Фигуре 6 показан типичный способ синтеза промежуточного соединения 2-бром-4-фтор-6-(1-оксо-3,4,6,7,8,9-гексагидропиразино[1,2-а]индол-2(1Н)-ил)бензилацетата 198d из 1,3-дибром-5-фтор-2-иодбензола.
На Фигуре 7 показан типичный способ синтеза промежуточного соединения 4-фтор-2-(1 -метил-5-(5-(4-метилпиперазин-1 -ил)пиридин-2-иламино)-6-оксо-1,6-дигидропиридин-3-ил)-6-(1-оксо-3,4,6,7,8,9-гексагидропиразино[1,2-а]индол-2(1Н)-ил)бензилацетата 198g.
На Фигуре 8 показан типичный способ синтеза промежуточного соединения 5-фтор-2-(1-метил-5-(5-(4-(оксетан-3-ил)пиперазин-1-ил)пиридин-2-иламино)-6-оксо-1,6-дигидропиридин-3-ил)-6-(1-оксо-3,4,6,7,8,9-гексагидропиразино[1,2-а]индол-2(1Н)-ил)бензилацетата 210е.
На Фигуре 9 показан типичный способ синтеза промежуточного соединения 5-[5-фтор-2-(ацетоксиметил)-3-(1-метил-5-{[5-(4-метилпиперазин-1-ил)пиридин-2-ил]амино}-6-оксо-1,6-дигидропиридин-3-ил)фенил]-8-тиа-5-азатрицикло[7.4.0.02,7]тридека-1(9),2(7)-диен-6-она 212c.
ПОДРОБНОЕ ОПИСАНИЕ ТИПИЧНЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ
Далее будут подробно описаны некоторые варианты реализации изобретения, примеры которых проиллюстрированы прилагаемыми структурами и формулами. Хотя настоящее изобретение описывается по отношению к приведенным вариантам реализации, следует понимать, что они не предназначены для ограничения изобретения до указанных вариантов реализации. Напротив, настоящее изобретение включает все альтернативы, модификации и эквиваленты, которые могут находиться в рамках настоящего изобретения, определяемых формулой изобретения. Специалистам в данной области техники известны многие способы и вещества, аналогичные или эквивалентные тем, которые описаны в настоящей заявке, которые можно использовать при осуществлении на практике настоящего изобретения. Настоящее изобретение никоим образом не ограничено описанными способами и материалами. В случае, если один или несколько из включенных литературных источников, патентов и подобных материалов отличается от настоящей заявки или противоречит ей, включая, но не ограничиваясь этим, определения терминов, использование терминов, описанные технические приемы или т.п., преимущество имеет настоящая заявка.
ОПРЕДЕЛЕНИЯ
В настоящем документе термин "алкил" относится к насыщенному одновалентному углеводородному радикалу с линейной или разветвленной цепью, содержащей от одного до двенадцати атомов углерода (C1-C12), причем указанный алкильный радикал может быть независимо замещен одним или более заместителями, описанными ниже. Согласно другому варианту реализации, алкильный радикал содержит от одного до восьми атомов углерода (C1-C8) или от одного до шести атомов углерода (C1-С6). Примеры алкильных групп включают, но не ограничиваются ими, метил (Me, -СН3), этил (Et, -СН2СН3), 1-пропил (н-Pr, н-пропил, -CH2CH2CH3), 2-пропил (изо-Pr, изопропил, -СН(СН3)2), 1-бутил (н-Bu, н-бутил, -СН2СН2СН2СН3), 2-метил-1-пропил (изо-Bu, изобутил, -СН2СН(СН3)2), 2-бутил (втор-Bu, втор-бутил, -СН(СН3)СН2СН3), 2-метил-2-припил (трет-Bu, трет-бутил, -С(СН3)3), 1-пентил (н-пентил, -СН2СН2СН2СН2СН3), 2-пентил (-СН(СН3)СН2СН2СН3), 3-пентил (-СН(СН2СН3)2), 2-метил-2-бутил (-С(СН3)2СН2СН3), 3-метил-2-бутил (-СН(СН3)СН(СН3)2), 3-метил-1-бутил (-СН2СН2СН(СН3)2), 2-метил-1-бутил (-СН2СН(СН3)СН2СН3), 1-гексил (-СН2СН2СН2СН2СН2СН3), 2-гексил (-СН(СН3)СН2СН2СН2СН3), 3-гексил (-СН(СН2СН3)(СН2СН2СН3)), 2-метил-2-пентил (-С(СН3)2СН2СН2СН3), 3-метил-2-пентил (-СН(СН3)СН(СН3)СН2СН3), 4-метил-2-пентил (-СН(СН3)СН2СН(СН3)2), 3-метил-3-пентил (-С(СН3)(СН2СН3)2), 2-метил-3-пентил (-СН(СН2СН3)СН(СН3)2), 2,3-диметил-2-бутил (-С(СН3)2СН(СН3)2), 3,3-диметил-2-бутил (-СН(СН3)С(СН3)3, 1-гептил, 1-октил и т.п.
В настоящем документе термин "алкилен" относится к насыщенному двухвалентному углеводородному радикалу с линейной или разветвленной цепью, содержащей от одного до двенадцати атомов углерода (C1-C12), причем указанный алкиленовый радикал может быть независимо замещен одним или более заместителями, описанными ниже. Согласно другому варианту реализации, алкиленовый радикал содержит от одного до восьми атомов углерода (C1-C8), или от одного до шести атомов углерода (C1-С6). Примеры алкиленовых групп включают, но не ограничиваются ими, метилен (-СН2-), этилен (-СН2СН2-), пропилен (-СН2СН2СН2-) и т.п.
Термины "карбоцикл", "карбоциклил", "карбоциклическое кольцо" и "циклоалкил" относятся к одновалентному неароматическому замещенному или частично незамещенному кольцу, содержащему от 3 до 12 атомов углерода (С3-С12) в случае моноциклического кольца или от 7 до 12 атомов углерода в случае бициклического кольца. Бициклические карбоциклы, содержащие от 7 до 12 атомов, могут быть получены, например, в виде бицикло [4,5], [5,5], [5,6] или [6,6] систем и бициклические карбоциклы, содержащие 9 или 10 атомов в кольце, могут быть получены в виде бицикло [5,6] или [6,6] систем, или в виде мостиковых систем, таких как бицикло[2.2.1]гептан, бицикло[2.2.2]октан и бицикло[3.2.2]нонан. Примеры моноциклических карбоциклов включают, но не ограничиваются ими, циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, циклогексадиенил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил, циклододецил и т.п.
"Арил" означает одновалентный ароматический углеводородный радикал с 6-20 атомами углерода (С6-С20), полученный путем удаления одного атома водорода от единого атома углерода исходной системы ароматического кольца. Некоторые арильные группы обозначены в примерах структур как "Ar". Арил включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным или ароматическим карбоциклическим кольцом. Типичные арильные группы включают, но не ограничиваются ими, радикалы, полученные из бензола (фенил), замещенных бензолов, нафталина, антрацена, дифенила, инденила, инданила, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и т.п. Арильные группы возможно независимо замещены одним или несколькими заместителями, описанными к настоящем документе.
"Арилен" означает двухвалентный ароматический углеводородный радикал, содержащий 6-20 атомов углерода (С6-С20), полученный путем удаления двух атомов водорода от двух атомов углерода исходной системы ароматического кольца. Некоторые ариленовые группы обозначены в типичных структурах как "Ar". Арилен включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным или ароматическим карбоциклическим кольцом. Типичные ариленовые группы включают, но не ограничиваются ими, радикалы, полученные из бензола (фенилен), замещенных бензолов, нафталина, антрацена, дифенилена, инденилена, инданилена, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и т.п. Ариленовые группы возможно замещены.
В настоящем документе термины "гетероцикл," "гетероциклил" и "гетероциклическое кольцо" применяют взаимозаменяемо, и они относятся к насыщенному или частично ненасыщенному (то есть, имеющему в кольце одну или более двойную и/или тройную связь) карбоциклическому радикалу, содержащему от 3 до примерно 20 атомов в кольце, в котором по меньшей мере один атом в кольце представляет собой гетероатом, выбранный из азота, кислорода, фосфора, серы и кремния, и оставшиеся атомы в кольце представляют собой С, где один или более атом в кольце возможно независимо замещен одним или более заместителем, описанным ниже. Гетероцикл может представлять собой моноцикл, содержащий от 3 до 7 членов в кольце (от 2 до 6 атомов углерода и от 1 до 4 гетероатомов, выбранных из N, О, Р, и S) или бицикл, содержащий от 7 до 10 членов в кольце (от 4 до 9 атомов углерода и от 1 до 6 гетероатомов, выбранных из N, О, Р, и S), например: бицикло [4,5], [5,5], [5,6] или [6,6] систему. Гетероциклы описаны в Paquette, Leo A.; "Principles of Modem Heterocyclic Chemistry" (W.A. Benjamin, New York, 1968), в частности, Главы 1, 3, 4, 6, 7 и 9; "The Chemistry of Heterocyclic Compounds, A series of Monographs" (John Wiley & Sons, New York, 1950 до настоящего времени), в частности. Тома 13, 14, 16, 19 и 28; и J. Am. Chem. Soc. (I960) 82:5566. "Гетороциклил" также включает радикалы, в которых радикалы гетероциклов сконденсированы с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим или гетероциклическим кольцом. Примеры гетероциклических колец включают, но не ограничиваются ими, морфолин-4-ил, пиперидин-1-ил, пиперидонил, оксопиперазил, пиперазинил, пиперазин-4-ил-2-он, пиперазин-4-ил-3-он, пирролидин-1-ил, тиоморфолин-4-ил, 8-диоксотиоморфолин-4-ил, азокан-1-ил, азетидин-1-ил, октагидропиридо[1,2-а]пиразин-2-ил, [1,4]диазепан-1-ил, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидине, морфолино, тиоморфолино, тиооксанил, пиперазинил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинилимидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, азабицикло[2.2.2]гексанил, 3Н-индолилхинолизинил и N-пиридилмочевины. Спиро фрагменты также включены в объем указанного определения. Примерами гетероциклических групп, в которых 2 атома в кольце замещены оксо (=O) фрагментами, являются пиримидинонил и 1,1-диоксотиоморфолинил. В настоящем документе гетероциклические группы возможно независимо замещены одним или более заместителями, описанными в настоящем документе.
Термин "гетероарил" относится к одновалентному ароматическому радикалу, содержащему 5-, 6- или 7-членные кольца, и включает системы конденсированных колец (по меньшей мере, одно из которых является ароматическим) из 5-20 атомов, содержащих один или более гетероатомов, независимо выбранных их азота, кислорода и серы. Примерами гетероарильных групп являются пиридинил (включая, например, 2-гидроксипиридинил), имидазолил, имидазопиридинил, пиримидинил (включая, например, 4-гидроксипиримидинил), пиразолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксадиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, тетрагидроизохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, триадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензооксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. Гетероарильные группы возможно независимо замещены одним или более заместителями, описанными в настоящем документе.
Гетероциклические или гетероарильные группы могут быть связанными по углероду (углеродсвязанные) или азоту (азотсвязанные), где это возможно. В качестве примера, а не ограничения, гетероциклы и гетероарилы, связанные по углероду, связаны по положению 2, 3, 4, 5 или 6 для пиридина, положению 3, 4, 5 или 6 для пиридазина, положению 2, 4, 5 или 6 для пиримидина, положению 2, 3, 5 или 6 для пиразина, положению 2, 3, 4 или 5 для фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положению 2, 4 или 5 для оксазола, имидазола или тиазола, положению 3, 4 или 5 для изоксазола, пиразола или изотиазола, положению 2 или 3 для азиридина, положению 2, 3 или 4 для азетидина, положению 2, 3, 4, 5, 6, 7 или 8 для хинолина или положению 1, 3, 4, 5, 6, 7 или 8 для изохинолина.
В качестве примера, а не ограничения, гетероциклы и гетероарилы, связанные по азоту, связаны по положению 1 для азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1Н-индазола, положению 2 для изоиндола или изоиндолина, положению 4 для морфилина, и положению 9 для карбазола или β-карболина.
Термины ʺлечитьʺ и ʺлечениеʺ относятся к терапевтическому лечению, причем задачей является замедление (уменьшение) нежелательного физиологического изменения или нарушения, такого как развитие или распространение артрита или рака. Для целей настоящего изобретения, преимущественные или желательные клинические результаты включают, но не ограничиваются ими, смягчение симптомов, уменьшение степени заболевания, стабилизацию (т.е., отсутствие ухудшения) состояния заболевания, отсрочку или замедление развития заболевания, улучшение или временное облегчения состояния заболевания и ремиссию (как частичную, так и полную), как выявленные, так и не выявленные. "Лечение" может также означать продление выживания, по сравнению с ожидаемым выживанием при отсутствии лечения. Нуждающиеся в лечении включают тех, кто обладает указанным состоянием или нарушением.
Выражение "терапевтически эффективное количество" означает количество соединения согласно настоящему изобретению, которое (i) лечит конкретное заболевание, состояние или нарушение, (ii) смягчает, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или нарушения, или (iii) предотвращает или отсрочивает появление одного или более симптомов конкретного заболевания, состояния или нарушения, описанных в настоящем документе. В случае рака, терапевтически эффективное количество лекарственного средства может уменьшать количество раковых клеток, уменьшать размер опухоли, ингибировать (т.е., замедлять до некоторой степени и, предпочтительно, останавливать) инфильтрацию раковых клеток в периферические органы; ингибировать (т.е., замедлять до некоторой степени и, предпочтительно, останавливать) метастазирование опухоли; ингибировать до некоторой степени рост опухоли; и/или облегчать до некоторой степени один или более симптомов, связанных с раком. В той степени, в которой лекарственное средство может предотвращать рост и/или убивать имеющиеся раковые клетки, оно может быть цитостатическим и/или цитотоксическим. Для терапии рака, эффективность можно измерять, например, путем оценки времени прогрессирования заболевания (ТТР) и/или определения частоты ответа (RR).
В настоящем документе "воспалительное нарушение" может относиться к любому заболеванию, нарушению или синдрому, при котором избыточный или нерегулируемый воспалительный ответ приводит к избыточным воспалительным симптомам, повреждению питающей ткани или потере функции ткани. "Воспалительное нарушение" также относится к патологическому состоянию, опосредованному притоком лейкоцитов и/или хемотаксисом нейтрофилов.
В настоящем документе "воспаление" относится к локализованному защитному ответу, вызванному повреждением или разрушением тканей, который способствует разрушению, разжижению или отделению (изолированию) как поражающего агента, так и поврежденной ткани. Воспаление, в частности, связано с притоком лейкоцитов и/или хемотаксисом нейтрофилов. Воспаление может быть результатом инфицирования патогенными организмами и вирусами, а также неинфекционных способов, таких как травма или реперфузия, последующая за инфарктом миокарда или инсульта, иммунного ответа на чужеродный антиген и аутоиммунных ответов. Соответственно, воспалительные нарушения, поддающиеся лечению соединениями формулы I, охватывают нарушения, связанные с реакциями специфической защитной системы, а также с реакциями неспецифической защитной системы.
"Специфическая защитная система" относится к компоненту иммунной системы, который реагирует на присутствие специфических антигенов. Примеры воспаления вследствие ответа специфической защитной системы включают нормальный ответ на чужеродные антигены, аутоиммунные заболевания и ответ гиперчувствительности замедленного типа, опосредованной Т-клетками. Дополнительными примерами воспалительных реакций специфической защитной системы являются хронические воспалительные заболевания, отторжение твердой трансплантированной ткани и органов, например, почки и трансплантата костного мозга, и реакция трансплантат против хозяина (РТПХ).
В настоящем документе термин "неспецифическая защитная система" относится к воспалительным нарушениям, опосредованным лейкоцитами, которые неспособны к иммунологической памяти (например, гранулоциты и макрофаги). Примеры воспаления, в результате, по меньшей мере частично, реакции неспецифической защитной системы, включают воспаление, связанное с состояниями, такими как респираторный дистресс-синдром у взрослых (острый) (ARDS) или синдромы полиорганной недостаточности; реперфузионное повреждение; острый гломерулонефрит; реактивный артрит; дерматоз с острым воспалительным компонентом; острый гнойный менингит или другие воспалительные нарушения центральной нервной системы, такие как инсульт; термическое повреждение; воспалительное заболевание кишечника; синдромы, связанные с трансфузией гранулоцитов; и цитокин-индуцированная токсичность.
В настоящем документе "аутоиммунное заболевание" относится к любой группе нарушений, при которых повреждение ткани связано с гуморальным или клеточно-опосредованным ответами на собственные части тела.
В настоящем документе "аллергическое заболевание" относится к любым симптомам, повреждениям ткани или потере функции ткани в результате аллергии. В настоящем документе "артритное заболевание" относится к любому заболеванию, характеризующемуся воспалительными патологическими изменениями суставов, свойственными различным этиологиям. В настоящем документе "дерматит" относится к любому из большого семейства заболеваний кожи, характеризующихся воспалением кожи, свойственным различным этиологиям. В настоящем документе "отторжение трансплантата" относится к любой иммунной реакции, направленной против трансплантированной ткани, такой как органы или клетки (например, костный мозг), характеризующейся потерей функции трансплантированной и окружающей тканей, болью, опухолью, лейкоцитозом и тромбоцитопенией. Терапевтические способы согласно настоящему изобретению включают способы лечения нарушений, связанных с воспалительной клеточной активацией.
"Воспалительная клеточная активация" относится к индукции посредством стимула (включая, но не ограничиваясь ими, цитокины, антигены или аутоантитела) пролиферативного клеточного ответа, выработку растворимых медиаторов (включая, но не ограничиваясь ими, цитокины, кислородсодержащие радикалы, ферменты, простаноиды или вазоактивные амины) или клеточную поверхностную экспрессию новых или повышенного числа медиаторов (включая, но не ограничиваясь ими, антигены главного комплекса гистосовместимости или молекулы клеточной адгезии) в воспалительных клетках (включая, но не ограничиваясь ими, моноциты, макрофаги, Т лимфоциты, В-лимфоциты, гранулоциты (т.е., полиморфноядерные лейкоциты, такие как нейтрофилы, бозофилы и эозинофилы), тучные клетки, дендритные клетки, клетки Лангерганса и эндотелиальные клетки). Специалистам в данной области будет понятно, что активация одного или комбинации указанных фенотипов в указанных клетках может способствовать возникновению, сохранению или обострению воспалительного нарушения.
Термин "НПВС" является сокращением от "нестероидные противовоспалительные средства" и представляет собой терапевтический агент с анальгетическим, жаропонижающим (понижающий повышенную температуру тела и облегчающий боль без потери сознания) и, в более высоких дозах, противовоспалительным действием (уменьшающий воспаление). Термин "нестероидные " применяют, чтобы отличить указанные лекарственные средства от стероидов, которые (среди широкого спектра других эффектов) обладают аналогичным эйкозаноид-угнетающим, противовоспалительным действием. В качестве анальгетиков, НПВС необычны тем, что являются ненаркотическими. НПВС включают аспирин, ибупрофен и напроксен. НПВС обычно назначают для лечения острых или хронических состояний, в которых присутствует боль и воспаление. НПВС, в целом, назначают для симптоматического облегчения следующих состояний: ревматоидный артрит, остеоартрит, воспалительные артропатии (например, анкилозирующий спондилит, псориатический артрит), синдрома Рейтера, острой подагры, дисменореи, метастатической боли в костях, головной боли и мигрени, послеоперационной боли, боли от легкой до умеренной вследствие воспаления и повреждения ткани, лихорадки, кишечной непроходимости и почечной колики. Большинство НПВС действует в качестве неселективных ингибиторов фермента циклооксигеназы, ингибирующих оба изофермента циклооксигеназу-1 (ЦОГ-1) и циклооксигеназу-2 (ЦОГ-2). Циклооксигеназа катализирует образование простагландинов и тромбоксана из арахидоновой кислоты (которая получена из клеточного фосфолипидного двойного слоя посредством фосфолипазы А2). Простагландины действуют (помимо прочего) в качестве сигнализирующих молекул в процессе воспаления. Ингибиторы ЦОГ-2 включают целекоксиб, эторикоксиб, лумиракоксиб, парекоксиб, рофекоксиб, рофекоксиб и вальдекоксиб.
Термин "рак" относится к или описывает физиологическое состояние у млекопитающего, которое обычно характеризуется неконтролируемым ростом клеток. "Опухоль" содержит одну или более раковых клеток. Примеры рака включают, но не ограничиваются ими, карциному, лимфому, бластому, саркому и лейкемию или лимфолейкоз. В частности, примеры таких раков включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легких, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого ("НМРЛ"), аденокарциному легких и плоскоклеточный рак легкого, рак брюшины, гепатоклеточный рак, рак желудка или рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластома, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатома, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карцинома эндометрия или карцинома матки, карцинома слюнных желез, рак почки или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, карцинома печени, карцинома анального канала, рак полового члена, а также рак головы и шеи.
"Химиотерапевтический агент" представляет собой химическое соединение, подходящее для лечения рака, независимо от механизма действия. Классы химиотерапевтических агентов включают, но не ограничиваются ими: алкилирующие агенты, антиметаболиты, растительные алкалоиды с веретенным ядом, цитотоксичные/противоопухолевые антибиотики, ингибиторы топоизомеразы, антитела, фотосенсибилизаторы и ингибиторы киназы. Химиотерапевтические агенты включают соединения, применяемые в "таргетной терапии" и традиционной химиотерапии. Примеры химиотерапевтических агентов включают: эрлотиниб (Тарцева®, Genentech/OSI Pharm.), доцетаксел (Таксотер®, Sanofi-Aventis), 5-FU (фторурацил, 5-фторурацил, CAS №51-21-8), гемцитабин (Гемзар®, Lilly), PD-0325901 (CAS №391210-10-9, Pfizer), цисплатин (цис-диамин, дихлорплатина (II), CAS №15663-27-1), карбоплатин (CAS №41575-94-4), паклитаксел (Таксол®, Bristol-Myers Squibb Oncology, Princeton, NJ), трастузумаб (Герцептин®, Genentech), темозоломид (4-метил-5-оксо-2,3,4,6,8-пентазабицикло[4.3.0]-нона-2,7,9-триен-9-карбоновая кислота, CAS №85622-93-1, Темодар®, Темодал®, Schering Plough), тамоксифен ((Z)-2-[4-(1,2-дифенилбут-1-енил)фенокси]-N,N-диметилэтанамин, Нолвадекс®, Истубал®, Валодекс®) и доксорубицин (Адриамицин®), Akti-1/2, HPPD (гидроксифенил-пируват диоксигеназа) и рапамицин.
Также примеры химиотерапевтических агентов включают: оксалиплатин (Элоксатин®, Sanofi), бортезомиб (Велкейд®, Millennium Pharm.), сутент (Сунитиниб®, SU11248, Pfizer), летрозол (Фемара®, Novartis), мезилат иматиниба (Гливек®, Novartis), XL-518 (ингибитор МЭК, Exelixis, WO 2007/044515), ARRY-886 (ингибитор МЭК, AZD6244, Array BioPharma, Astra Zeneca), SF-1126 (ингибитор PI3K, Semafore Pharmaceuticals), BEZ-235 (ингибитор PI3K, Novartis), XL-147 (ингибитор PI3K, Exelixis), PTK787/ZK 222584 (Novartis), фулвестрант (Фаслодекс®, AstraZeneca), лейковорин (фолиевой кислоты), рапамицин (сиролимус, Рапамун®, Wyeth), лапатиниб (Тайкерб®, GSK572016, Glaxo Smith Kline), лонафарниб (Сарасар™, SCH 66336, Schering Plough), сорафениб (Нексавар®, BAY43-9006, Bayer Labs), гефитиниб (Иресса®, AstraZeneca), иринотекан (Камптосар®, СРТ-11, Pfizer), типифарниб (ZARNESTRA™, Johnson & Johnson), Абраксан™ (без кремофора), сконструированная на основе альбумина композиция из наночастиц паклитаксела (American Pharmaceutical Partners, Шаумберг, II), вандетаниб (rINN, ZD6474, Зактима®, AstraZeneca), хлорамбуцил, AG1478, AG1571 (SU 5271; Sugen), темсиролимус (Торизел®, Wyeth), пазопаниб (GlaxoSmithKline), санфосфамид (TELCYTA®, Telik), тиотепа и циклофосфамид (Цитоксан®, Неозар®); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбохон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилоломеламин; ацетогенины (в частности, буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекан); бриостатин; каллистатин; СС-1065 (включая его синтетические аналоги адозелезин, карзелезин и безелезин); криптофицины (в частности, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и СВ1-ТМ1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотные иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлоретамин, мехлорэтамин оксид гидрохлорид, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урациловый иприт; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как энедииновые антибиотики (например, калихеамицин, калихеамицин гамма II, калихеамицин омега II (Angew Chem Inti Ed Engi (1994) 33:183-186); динемицин, динемицин А; бисфосфонаты, такие как клодронат; эсперамицин, а также неокарциностатиновый хромофор и родственные хромопротеиновые энедииновые антибиотические хромофоры), аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин и деоксидоксорубицин), эпирубицин, эсорубицин, идарубицин, неморубицин, марцелломицин, митомицины, такие как митомицин С, микофенольная кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флюдарабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидеоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, дромостанолон пропионат, эпитиостанол, мепитиостан, тестолактон; антиадреналиновые средства, такие как аминоглутетимид, митотан, трилостан; вещество, пополняющее запас фолиевой кислоты, такое как фролиновая кислота; ацеглатон; альдофосфамидный гликозид; аминолевулиновая кислота; энилурацил, амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демекольцин; диазиквон; элфорнитин; эллиптиний ацетат; эпотилон; этоглюцид; нитрат галлия; гидроксимочевина; лентинан; лонидамин; мейтансиноиды, такие как мейтансин и ансамитоцины; митогуазон; митоксантрон; мопидамол; нитракрин; пентостатин; фенамет; пирарубицин; подофиллиновая кислота; 2-этилгидразид; прокарбазин; PSK® полисахаридный комплекс (JHS Natural Products, Юджин, Орегон); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазихон; 2,2',2''-трихлортриэтиламин; трихотецены (в частности, Т-2 токсин, верракурин А, роридин А и ангуидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Ara-С"), циклофосфамид; тиотепа; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины,