Фармацевтическая композиция, включающая производное амида, ингибирующее рост раковых клеток, и лубрикант, не являющийся солью металла
Иллюстрации
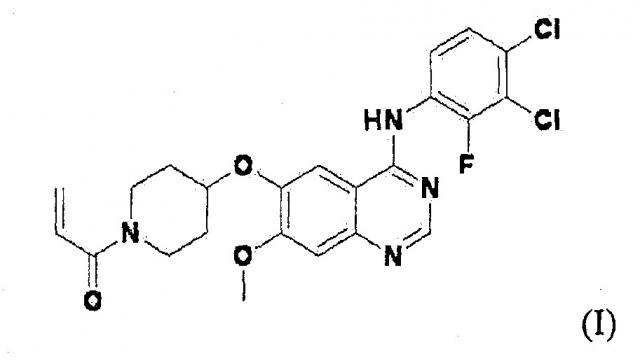
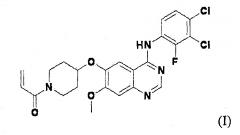
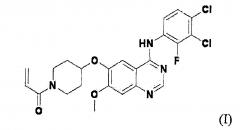
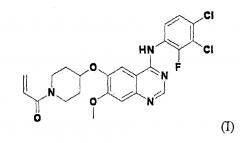
Показать всеИзобретение относится к химико-фармацевтической промышленности и представляет собой фармацевтическую композицию, содержащую вещество формулы (I) или его фармацевтически приемлемую соль и лубрикант, не являющийся солью металла:
,
а также способ получения препарата данной фармацевтической композиции. Изобретение позволяет улучшить стабильность фармацевтической композиции, содержащей производное амида формулы (I) и увеличить срок хранения без качественных изменений в течение долгого времени. 3 н. и 14 з.п. ф-лы, 4 ил., 9 табл., 8 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к фармацевтической композиции, содержащей производное амида или его фармацевтически приемлемую соль, ингибирующие рост раковых клеток, и лубрикант, не являющийся солью металла.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Известно, что рецептор эпидермального фактора роста (EGFR) имеет четыре подтипа рецепторов, т.е. EGFR/ErbB1, Her-2/ErbB2, Her-3/ErbB3 и Her-4/ErbB4. Они аномально сверхэкспрессированы в большинстве клеток солидных опухолей. Кроме того, активация рецептора лигандами приводит к активации клеточного сигнального пути, которая дает повышение роста, дифференцировку, ангиогенезис, метастазирование и резистенцию опухолевых клеток (A. Wells, Int.J. Biochem. Cell. Biol., 1999, 31, 637-643). Таким образом, ожидается, что блокирование сигнального пути раковых клеток, опосредованного рецептором эпидермального фактора роста, произведет антиопухолевые эффекты. Вследствие этого, было сделано много исследовательских работ по разработке противораковых лекарств, направленных на рецептор эпидермального фактора роста.
Такие противораковые лекарства, направленные на рецептор эпидермального фактора роста, делятся по категориям на две группы: моноклональные антитела, специфичные к внеклеточному домену и низкомолекулярные лекарства, направленные на внутриклеточную тирозин киназу. Моноклональные антитела имеют преимущество в высокой фармакологической эффективности с меньшим экстентом побочных эффектов, благодаря их селективному связыванию с рецепторами эпидермального фактора роста. Однако, моноклональные антитела имеют недостатки в том, что они достаточно дороги и должны быть введены путем инъекции. В то же время низкомолекулярные лекарства, направленные на тирозин киназу, являются относительно недорогими и орально принимаемыми, и они также имеют хорошую фармакологическую эффективность за счет селективного или одновременного взаимодействия с подтипами рецептора (например, EGFR, Her-2, Her-3 и Her-4).
Примеры низкомолекулярных лекарств включают селективные ингибиторы EGFR, такие как Iressa® (Гефитиниб, AstraZeneca) и Tarceva® (Эрлотиниб, Roche) и двойные ингибиторы блокирующие одновременно IGFR и Her-2, такие как Tykerb® (Лапатиниб, GlaxoSmithKline). Эти лекарства в настоящее время используются для лечения рака легких и распространенного Her-2 положительного рака груди соответственно. Для них также проводятся клинические испытания для увеличения эффективности против других солидных опухолей.
Недавнее исследование сообщает, что вторая мутация, т.е. замещение треонина на метионин в 790 положении аминокислотной последовательности в участке связывания аденозинтрифосфата (АТФ) с тирозинкиназным доменом EGFR, может уменьшать связывающую способность лекарства, что приводит к радикальному уменьшению показателя эффективности лекарства C.H. Gow, et al., PLos Med., 2005, 2(9), e269). Таким образом, требуется разработка лекарства, имеющего увеличенные ингибирующие активности к EGFR резистентных раковых клеток.
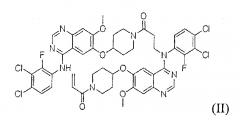
Корейский патент Открытая публикация # 2008-0107294 раскрывает вещество формулы (I), которое селективно и эффективно, без побочных эффектов, ингибирует рост раковых клеток и развитие лекарственной резистенции, индуцируемые EGFR и его мутантами. Однако было обнаружено, что фармацевтическая композиция, содержащая вещество формулы (I) в качестве активного ингредиента и его фармацевтически приемлемые добавки облегчают образование вещества формулы (II) (в дальнейшем именуется, как родственное вещество IV) при определенных условиях хранения, уменьшая, таким образом, количество вещества формулы (I).
Чистота активного ингредиента является важным фактором для приготовления безопасной и эффективной фармацевтической композиции, так как определенные примеси, содержащиеся в лекарственном веществе, могут вызывать побочные эффекты во время лечения. Некоторые примеси могут быть удалены в процессе приготовления лекарства. Но определенные вещества, образованные при деградации лекарства в результате изменений в таких различных условиях как температура, влажность и свет могут оставаться в качестве примесей.
Авторы настоящего изобретения стремились изучить факторы, которые способствуют образованию родственного вещества IV в процессе хранения фармацевтической композиции, содержащей вещество формулы (I) и обнаружили, что фармацевтически приемлемые добавки, в особенности металлические соли, содержащиеся в лубрикантах, вызывают ускорение образования родственного вещества (IV). Вследствие этого, авторы настоящего изобретения разработали фармацевтическую композицию, обладающую повышенной стабильностью за счет использования лубриканта, не являющегося солью металла, которое свободно от компонента соли металла.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является предоставление фармацевтической композиции с улучшенной стабильностью, содержащей производное амида или фармацевтически приемлемую его соль, которое эффективно ингибирует рост раковых клеток.
В соответствии с одной особенностью настоящего изобретения, предоставляется фармацевтическая композиция, содержащая вещество формулы (I) или фармацевтически приемлемую его соль и лубрикант, не являющийся солью металла.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Вышеупомянутые и другие цели и характерные особенности настоящего изобретения станут очевидными из последующего описания изобретения при рассмотрении одновременно с сопровождающими иллюстрациями, которые соответственно демонстрируют:
Фиг. 1: результаты теста на стабильность, показывающие количество родственного вещества IV, образованного после нагревания фармацевтических композиций примеров с 1 по 8 и Сравнительного примера 1 при 60°С;
Фиг. 2: результаты теста на стабильность, показывающие количество родственного вещества IV, образованного после нагревания фармацевтических композиций Сравнительных примеров с 1 по 4 и примера 1 при 60°С;
Фиг. 3: результаты ускоренного теста на стабильность, показывающие количество родственного вещества IV, образованного после выдерживания фармацевтических композиций примеров 1 и 2 и Сравнительных примеров 1 и 3 в ускоренных условиях (40°С и 75% относительной влажности); и
Фиг. 4: результаты ускоренного теста на стабильность в сосуде из ПЭНД, показывающие количество родственного вещества IV, полученного после выдерживания фармацевтических композиций примеров 1 и 2 и Сравнительных Примеров 1 и 3 в ускоренных условиях (40°С и 75% относительной влажности).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение предоставляет фармацевтическую композицию, состоящую из вещества формулы (I) или фармацевтически приемлемой его соли, и лубрикант, не являющийся солью металла.
Каждый ингредиент патентноспособной фармацевтической композиции детально описан нижеуказанным образом.
(a) Фармацевтически активный ингредиент
Фармацевтическая композиция согласно настоящему изобретению содержит вещество формулы (I) или фармацевтически приемлемую его соль в качестве фармацевтически активного ингредиента.
Вещество формулы (I) (в дальнейшем именуется кодовым именем “HM781-36B”), как раскрыто в открытой публикации корейского патента № 2008-0107294, может селективно и эффективно ингибировать рост раковых клеток и развитие лекарственной резистенции, индуцированных EGFR и его мутантами, не вызывая при этом неблагоприятных побочных эффектов.
Фармацевтически приемлемая соль вещества формулы (I), предусматривает, но не ограничивается этим, кислотно-аддитивную соль неорганической или органической кислоты. Примеры неорганической кислотно-аддитивной соли могут включать соли соляной кислоты, серной кислоты, дисульфоновой кислоты, азотной кислоты, фосфорной кислоты, хлорной кислоты или бромноватой кислоты; примеры органической кислотно-аддитивной соли могут включать соли муравьиной кислоты, уксусной кислоты, пропионовой кислоты, щавелевой кислоты, янтарной кислоты, бензойной кислоты, лимонной кислоты, малеиновой кислоты, малоновой кислоты, яблочной кислоты, винной кислоты, глюконовой кислоты, молочной кислоты, жестисиковой кислоты, фумаровой кислоты, лактобионовой кислоты, салициловой кислоты, фталевой кислоты, эмбониковой кислоты, аспартовой кислоты, глутаминовой кислоты, камсиликовой кислоты, бензосульфокислоты или ацетилсалициловой кислоты (аспирин). Фармацевтически приемлемая соль может также включать соли металлов, производные от щелочных металлов, таких как кальций, натрий, магний, стронций, калий и тому подобные.
В настоящем изобретении вещество формулы (I) может применяться в количестве в диапазоне от 0,1 до 50% по весу, предпочтительно от 0,5 до 10% по весу, основанному на тотальном весе композиции.
Лубрикант, не являющийся солью металла
Лубриканты - это ингредиенты, добавленные для улучшения компрессионных процессов гранул, и они рассматриваются как решающий наполнитель, который играет важные роли при производстве твердых прессованных композиций. Преимущества использования лубрикантов включают улучшенное течение порошка или гранулярного материала, что позволяет легче заполнить ими заготовку; уменьшенное трение между порошковыми или гранулярными материалами, а также промежуточными между порошковыми и гранулярными материалами, и компостером или заготовкой; и улучшенную уплотняемость и высвобождаемость таблеток.
Лубриканты могут быть поделены на категории, как показано в Таблице 1.
| Таблица 1 | |
| Категория | Лубрикант |
| Жирная кислотаСоли металлов | стеарат кальция, стеарат кальция, стеарил фумарат натрия, стеарат цинка |
| Эфиры жирных кислот | глицерил бегенат, глицерил пальмитостеарат, глицерил моностеарат, глицерил тримиристат, глицерил тристеарат, эфир сахарозы и жирной кислоты |
| Жирные кислоты и спирты | пальмитиновая кислота, пальмитоиловый спирт, стеариновая кислота, стеариловый спирт |
| Масла | гидрированное касторовое масло, минеральное масло, гидрированное растительное масло |
| Другие | фумаровая кислота, полиэтиленгликоль (ПЭГ 4000 и ПЭГ 6000), политетрафторэтилен, тальк |
Фармацевтическая композиция настоящего изобретения, содержащая вещество формулы (I), характеризуется использованием лубриканта, не являющегося солью металла с целью предотвратить образование родственного вещества (IV), которое может в противном случае образоваться из-за соли металла, если она содержится в композиции.
Термин «лубрикант, не являющийся солью металла» согласно настоящему изобретению, относится к лубриканту, который не содержит металлических материалов, например таких солей металлов, как стеарат кальция, стеарат магния, стеарил фумарат натрия, стеарат цинка и тому подобных. Примеры лубриканта, не являющегося солью металла, согласно настоящему изобретению, могут включать эфиры жирных кислот, жирные кислоты, жирные спирты, масла, фумаровую кислоту, полиэтиленгликоли (ПЭГи), политетрафторэтилены, крахмал, тальк и тому подобные. Улучшенная хранимоспособность разработанной фармацевтической композиции может быть достигнута путем применения таких лубрикантов, не являющихся солью металла.
Как правило, примеры лубриканта, не являющегося солью металла, которые могут быть применены в настоящем изобретении, могут включать, но не лимитируются этим, эфиры жирных кислот (например, глицерил бегенат, глицерил пальмитостеарат, глицерил моностеарат, глицерил тримиристат, глицерил тристеарат, эфир жирной кислоты и сахарозы и им подобные); жирные кислоты и жирные спирты (например, пальмитиновая кислота, пальмитоиловый спирт, стеариновя кислота, стеариловый спирт и им подобные); масла (например, гидрированное касторовое масло, минеральное масло, гидрированное растительное масло и им подобные), фумаровую кислоту; полиэтиленгликоль (например, ПЭГ 4000 или ПЭГ 6000); политетрафторэтилен; крахмал и тальк. Лубриканты, не являющиеся солями металлов, могут быть использованы в единственном виде или в виде их смеси.
Предпочтительно, простейшие лубриканты, не являющиеся солью металла, согласно настоящему изобретению, могут включать эфир сахарозы и жирной кислоты, гидрированное растительное масло, стеариновую кислоту, глицерил бегенат, глицерил пальмитостеарат, тальк, крахмал и ПЭГ 6000, наиболее предпочтительно эфир сахарозы и жирной кислоты и гидрированное растительное масло.
В настоящем изобретении лубрикант, не являющийся солью металла может, быть использован в количестве в диапазоне от 0,1 до 100 весовых частей, предпочтительно от 0,1 до 50 весовых частей, более предпочтительно от 0,25 до 10 весовых частей, по отношению к одной весовой части вещества формулы (I).
Если использовано количество лубриканта, не являющегося солью металла, меньше чем 0,1 весовая часть, то образованная таблетка не будет легко высвобождаться из формовочной матрицы или будет прилипать к формовочной матрице в процессе формования таблетки. С другой стороны, если количество будет больше чем 100 весовых частей, таблетка будет страдать такими проблемами как кэппирование или расслоение. Кроме того, так как лубриканты являются обычно гидрофобными, то если они используются в большом количестве, они могут привести к таким неожиданным проблемам как задержка распада и низкая скорость растворения.
Фармацевтически приемлемые добавки
Фармацевтическая композиция настоящего изобретения может также содержать фармацевтически приемлемые добавки и может быть составлена в различных лекарственных формах, предпочтительно в форме принимаемой орально. Представительные примеры препарата для орального применения могут включать порошок, таблетку, пилюлю, капсулу, жидкость, суспензию, эмульсию, сироп и гранулу, предпочтительно таблетку и капсулу, но не ограничено ими.
В настоящем изобретении фармацевтически приемлемые добавки могут включать, разбавитель, связующее вещество, разрыхлитель и тому подобные.
Примеры разбавителя могут включать микрокристаллическую целлюлозу, лактозу, маннитол, фосфат кальция и тому подобные. Примеры связующего вещества могут включать повидон, гидроксипропилцеллюлозу (HPC), гидроксипропилметилцеллюлозу (HPMC), поливиниловый спирт (PVA), натрий карбоксиметилцеллюлозу и тому подобные; и примеры разрыхлителя могут включать кросповидон, кроскармеллозу натрия, натрий гликолят крахмала и тому подобные.
Разбавитель может быть использован в количестве в диапазоне от 20 до 95% по весу, связующее вещество может быть использовано в количестве в диапазоне от 1 до 10% по весу и разрыхлитель может быть использован в количестве в диапазоне от 1 до 30% по весу, основанному на тотальном весе композиции.
Фармацевтическая композиция настоящего изобретения может быть покрыта покрывающим субстратом для предохранения композиции от прямого контактирования с рукой или кожей пользователя.
Покрывающий субстрат, который может быть использован в настоящем изобретении, может включать быстро высвобождающийся покрывающий субстрат, энтеральный покрывающий субстрат или покрывающий субстрат замедленного высвобождения. Быстро высвобождающийся покрывающий субстрат может быть выбран из группы, состоящей из гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, поливинилового спирта, графт-полимера поливинил алкоголь-полиэтилен гликоля (Kollocoat IR®, BASF), и их смеси. Энтеральный покрывающий субстрат может быть выбран из группы, состоящей из сополимера (мет)акрилата (Eudragit®, EVONIC), фталата гидроксипропилметилцеллюлозы, фталата ацетатцеллюлозы и их смеси. Покрывающий субстрат с замедленным высвобождением может быть выбран из группы, состоящей из ацетатцеллюлозы, этилцеллюлозы, поливинил ацетата и их смеси.
Покрывающий субстрат может быть нанесен на поверхность композиции в количестве в диапазоне от 1 до 50 частей по весу, предпочтительно от 1 до 30 частей по весу, основанному на 100 частях веса непокрытого ядра.
Настоящее изобретение предоставляет также способ приготовления фармацевтической композиции, содержащей вещество формулы (I) или фармацевтически приемлемую его соль и лубрикант, не являющийся солью металла.
Состав фармацевтической композиции, включающей вышеупомянутые ингредиенты, может быть приготовлен следующим способом, который включает этапы:
(1) смешивание вещества формулы (I) или его фармацевтически приемлемой соли с такой фармацевтически приемлемой добавкой как разбавитель и связующее вещество, и гранулирование смеси для получения гранул;
(2) смешивание гранул, приготовленных на этапе (1) с такой фармацевтически приемлемой добавкой как разбавитель и разрыхлитель, и добавление к ним лубриканта, не являющегося солью металла, для получения смешанных гранул, и
(3) использование смешанных гранул, приготовленных на этапе (2) в этапе, составления смеси.
В одном варианте осуществления настоящего изобретения разрабатываемая фармацевтическая композиция может быть приготовлена путем примешивания вещества формулы (I) и маннитола к раствору провидона в очищенной воде, проведения влажной грануляции полученной смеси, и затем высушивания полученных гранул. Приготовленные гранулы могут быть сформированы в таблетку перемешиванием приготовленных гранул с маннитолом и кросповидоном, с добавлением к ним лубриканта, не являющегося солью металла и затем таблетированием смешанных гранул машиной для формирования таблеток.
Разные этапы настоящего изобретения, связанные с приготовлением фармацевтической композиции, могут проводиться согласно общепринятым технологиям, известным в данной области техники. К тому же, способ настоящего изобретения может также включать этап покрытия препарата приготовленного на этапе (3) вышеупомянутыми покрывающими субстратами для подходящего хранения и удобного использования.
Фармацевтическая композиция настоящего изобретения может эффективно ингибировать рост раковых клеток за счет содержания вещества формулы (I), которое селективно и эффективно ингибирует рост раковых клеток и развитие лекарственной устойчивости, индуцированные EGFR и его мутантами. Также, фармацевтическая композиция настоящего изобретения может ингибировать образование примесей (т.е. родственных веществ IV) до менее чем 0,5% по весу при экстремальных условиях (например, выдерживание в герметичном ПЭНД контейнере при 60°С в течение 4 недель) и при ускоренных условиях (например, выдерживание в герметичном ПЭНД контейнере при 40°С/75% относительной влажности в течение 6 месяцев) за счет содержания лубриканта, не являющегося солью метала. Таким образом, фармацевтическая композиция настоящего изобретения может увеличить эффективность и улучшить стабильность вещества формулы (I).
Таким образом, настоящее изобретение предоставляет способ стабилизации фармацевтической композиции, содержащей вещество формулы (I) или фармацевтически приемлемую его соль, содержащей добавку к фармацевтической композиции лубриканта, не являющегося солью металла.
Следующие примеры предназначаются для дополнительной иллюстрации настоящего изобретения без ограничения его границ.
ПРИМЕРЫ
Примеры с 1 по 8: Приготовление фармацевтических композиций, содержащих лубриканты, не являющиеся солями металла
Фармацевтические композиции примеров с 1 по 3 были приготовлены путем использования вещества формулы (I) (далее здесь именуемого как “HM781-36B”, Dongwoo Syntech Co., Ltd., Корея); маннитола (Roquette); Povidone® (BASF); Crospovidone® (BASF); и эфира сахарозы и жирной кислоты (Daiichi Kogyo Seiyaku, Япония), гидрированного растительного масла (Lubritab®, JRSPharma), или стеариновой кислоты (Emery Oleochemicals) в качестве лубриканта, не являющегося металлической солью, в соответствии с композицией и количеством (единицы; мг), описанными в Таблице 2.
Например, HM781-36B и маннитол смешивались, и смесь подвергалась процессу влажной грануляции стандартным способом с использованием связующего раствора провидона, растворенного в очищенной воде. Полученные таким образом влажные гранулы высушивали, смешивали с манитолом и кросповидоном и затем, для приготовления окончательной смеси, объединяли с лубрикантом, который предварительно был просеян через 30 меш сито. Приготовленная таким образом окончательная смесь, соответственно общепринятому способу посредством механизма для таблетирования (Sejong, Корея) формировалась в таблетку, имеющую твердость от около 5 до 10 kp.
| Таблица 2 | |||||
| Пример 1 | Пример 2 | Пример 3 | |||
| Влажнаягранула | Смесь | HM781-36B | 0,5 | 0,5 | 0,5 |
| маннитол | 50 | 50 | 50 | ||
| Связующее вещество | повидон | 1,5 | 1,5 | 1,5 | |
| <очищенная вода> | <10> | <10> | <10> | ||
| Смесь | маннитол | 42 | 42 | 42 | |
| кросповидон | 5 | 5 | 5 | ||
| Окончательная смесь | эфир сахарозы и жирной кислоты | 2 | - | - | |
| растительное гидрированное масло | - | 2 | - | ||
| стеариновая кислота тальк | - | - | 1 | ||
| Суммарный вес | 101 | 101 | 100 |
Фармацевтические композиции примеров с 4 по 8 были приготовлены тем же способом, что и приведенные выше с использованием вещества формулы (I) (HM781-36B, Dongwoo Syntech Co., Ltd., Корея); маннитола (Roquette); Popvidone® (BASF); Crospovidone® (BASF); и глицерил бегената (Compritol 888 ATO® Gattefosse), глицерил пальмитостеарата (Comprotol HD5®, Gattefosse), талька (Nippon Talk Corp., Япония), крахмала (Roquette), или ПЭГ 6000 (Sanyo Chemical, Япония) в качестве лубриканта, не являющегося солью металла, в соответствии с композицией и количеством (единицы, мг), описанными в Таблице 3.
| Таблица 3 | |||||||
| Пример 4 | Пример 5 | Пример 6 | Пример 7 | Пример 8 | |||
| Влажнаягранула | Смесь | HM781-36B | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 |
| маннитол | 50 | 50 | 50 | 50 | 50 | ||
| Связующее вещество | повидон | 1,5 | 1,5 | 1,5 | 1,5 | 1,5 | |
| <очищенная вода> | <10> | <10> | <10> | <10> | <10> | ||
| Смесь | маннитол | 42 | 42 | 42 | 42 | 42 | |
| кросповидон | 5 | 5 | 5 | 5 | 5 | ||
| Окончательная смесь | глицерил бегенат | 2 | - | - | - | - | |
| глицерил пальмитостеарат | - | 2 | - | - | - | ||
| тальк | - | - | 3 | - | - | ||
| крахмал | - | - | - | 5 | - | ||
| ПЭГ 6000 | 3 | ||||||
| Суммарный вес | 101 | 101 | 102 | 104 | 102 |
Фармацевтические композиции примеров с 9 по 15 были приготовлены тем же способом, что и приведенные выше с использованием вещества формулы (I) (HM781-36B, Dongwoo Syntech Co., Ltd., Корея); маннитола (Roquette); Popvidone® (BASF); Crospovidone® (BASF;) и глицерил моностеарата (Capmul GMS-50), пальмитоилового спирта (Landz International Company Ltd., Китай), стеарилового спирта (Lubrizol Advanced Materials, США), гидрированного касторового масла (BASF), минерального масла (Alfa Aesar, США), фумаровой кислоты (Merck) и диоксида кремния (Grace Davison, США)) в качестве лубриканта, не являющегося солью металла, в соответствии с композицией и количеством (единицы, мг), описанными в Таблице 4.
| Таблица 4 | |||||||||
| Пример 9 | Пример 10 | Пример 11 | Пример 12 | Пример 13 | Пример 14 | Пример 15 | |||
| Влажнаягранула | Смесь | HM781-36B | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 |
| маннитол | 50 | 50 | 50 | 50 | 50 | 50 | 50 | ||
| Связующее вещество | повидон | 1,5 | 1,5 | 1,5 | 1,5 | 1,5 | 1,5 | 1,5 | |
| <очищенная вода> | <10> | <10> | <10> | <10> | <10> | <10> | <10> | ||
| Смесь | маннитол | 42 | 42 | 42 | 42 | 42 | 42 | 42 | |
| кросповидон | 5 | 5 | 5 | 5 | 5 | 5 | 5 | ||
| Окончательная смесь | глицерил моностеарат | 5 | - | - | - | - | - | - | |
| Пальмитоиловый спирт | - | 5 | - | - | - | - | - | ||
| стеариловый спирт | - | - | 5 | - | - | - | - | ||
| гидрированное касторовое масло | - | - | - | 5 | - | - | - | ||
| минеральное масло | - | - | - | - | 5 | - | - | ||
| фумаровая кислота | - | - | - | - | - | 5 | - | ||
| диоксид кремния | - | - | - | - | - | - | 2 | ||
| Суммарный вес | 104 | 104 | 104 | 104 | 104 | 104 | 101 |
Процедуры указанных выше примеров были повторены с применением композиции и количества (единицы; мг) описанные в Таблице 5, для приготовления фармацевтических композиций, содержащих лубриканты являющиеся солью металлов, Сравнительных примеров с 1 по 4.
| Таблица 5 | ||||||
| Сравнительный пример 1 | Сравнительный пример 2 | Сравнительный пример 3 | Сравнительный пример 4 | |||
| Влажнаягранула | Смесь | HM781-36B | 0,5 | 0,5 | 0,5 | 0,5 |
| маннитол | 50 | 50 | 50 | 50 | ||
| Связующее вещество | повидон | 1,5 | 1,5 | 1,5 | 1,5 | |
| <очищенная вода> | <10> | <10> | <10> | <10> | ||
| Смесь | маннитол | 42 | 42 | 42 | 42 | |
| Кросповидон | 5 | 5 | 5 | 5 | ||
| Окончательная смесь | стеарат магния | 1 | - | - | - | |
| стеарат кальция | - | 1 | - | - | ||
| стеарилфумарат натрия | - | - | 1 | - | ||
| стеарат цинка | - | - | - | 1 | ||
| Суммарный вес | 100 | 100 | 100 | 100 |
Тестовый пример: Измерение образованного родственного соединения
С целью выяснить хранимоспособность фармацевтических композиций, приготовленных в Примерах с 1 по 8 и в Сравнительных примерах с 1 по 4, каждая из фармацевтических композиций была упакована в сосуды из ПЭНД с 1 г силикагеля и хранилась в камере (60ºС). Через 2 и 4 недели, соответственно, родственное вещество IV, основной продукт деградации HM781-36B, экстрагировали 60% ацетонитрилом в качестве растворителя, и затем были проведены HPLC анализы. Результаты Примеров с 1 по 8 представлены в Таблице 6 и на Фиг. 1, а результаты Сравнительных примеров с 1 по 4 представлены в таблице 7 и на Фиг. 2.
| Таблица 6 | ||||||||
| Пример | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Исходное | 0,05 | 0,04 | 0,04 | 0,05 | 0,05 | 0,04 | 0,04 | 0,05 |
| 2 недели, 60°C | 0,26 | 0,23 | 0,17 | 0,27 | 0,21 | 0,15 | 0,18 | 0,37 |
| 4 недели, 60°C | 0,34 | 0,35 | 0,31 | 0,38 | 0,36 | 0,26 | 0,29 | 0,45 |
| Таблица 7 | ||||
| Сравнительный пример | 1 | 2 | 3 | 4 |
| Исходное | 0,04 | 0,04 | 0,04 | 0,04 |
| 2 недели, 60°C | 1,52 | 0,98 | 1,60 | 1,09 |
| 4 недели, 60°C | 2,46 | 2,25 | 3,41 | 1,98 |
Для того чтобы пронаблюдать изменения стабильности фармацевтических композиций, приготовленных в соответствии с Примерами 1 и 2 и Сравнительными примерами 1 и 3 на фоне температуры и влажности, фармацевтические композиции были подвержены действию 40°С и 75% относительной влажности. Через 1 и 2 недели, соответственно, родственное вещество IV, основной продукт деградации HM781-36B, экстрагировали 60% ацетонитрилом в качестве растворителя и затем были проведены HPLC анализы. Результаты представлены в Таблице 8 и на Фиг. 3.
| Таблица 8 | ||||
| Пример 1 | Пример 2 | Сравнительный пример 1 | Сравнительный пример 3 | |
| Исходное | 0,05 | 0,04 | 0,04 | 0,04 |
| 1 неделя, 40°C/75%RH | 0,12 | 0,10 | 0,73 | 0,32 |
| 2 недели, 40°C/75%RH | 0,16 | 0,15 | 1,18 | 0,51 |
Для того чтобы пронаблюдать изменения стабильности фармацевтических композиций, приготовленных в соответствии с Примерами 1 и 2 и Сравнительными примерами 1 и 3 на фоне температуры и влажности при ускоренных условиях, фармацевтические композиции были подвержены 40°С и 75% относительной влажности в заклеенных контейнерах из ПЭНД в течение 1, 3 и 6 месяцев. Родственное вещество IV каждой композиции было экстрагировано 60% ацетонитрилом в качестве растворителя и затем были проведены HPLC анализы. Результаты представлены в Таблице 9 и на Фиг. 4.
| Таблица 9 | ||||
| Пример 1 | Пример 2 | Сравнительный пример 1 | Сравнительный пример 3 | |
| Исходное | 0,05 | 0,04 | 0,04 | 0,04 |
| 1 месяц ACLTD 40°C | 0,15 | 0,14 | 0,31 | 0,28 |
| 3 месяца ACLTD 40°C | 0,17 | 0,15 | 0,41 | 0,32 |
| 6 месяцев ACLTD 40°C | 0,20 | 0,18 | 0,62 | 0,58 |
Как показано в таблицах 6 и 9 и Фиг. с 1 по 4, образование родственного вещества IV было уменьшено в около от 4 до 10 раз или более в фармацевтических композициях, содержащих любой из лубрикантов, не являющийся солью металла, по сравнению с фармацевтическими композициями, содержащими лубриканты являющиеся солями металла. Таким образом, хранимоспособность фармацевтических композиций, содержащих HM781-36B в качестве активного ингредиента может быть существенно улучшена путем добавления в фармацевтические композиции любого из лубрикантов, не являющегося солью металла.
Согласно рекомендациям Международной конференции по упорядочению технических требований для регистрации фармацевтических препаратов для использования человеком (ICH), ограничения известных и неизвестных