N-алкоксикарбониламиноэтил-n'-арилмочевины, проявляющие рост-регулирующую активность
Иллюстрации
Показать всеИзобретение относится к способу получения N-алкоксикарбониламиноэтил-N'-арилмочевин общей формулы I, где R=втор-С4H9, R1=Н, R2=H, R3=СН3 (Ia), R=втор-С4H9, R1=СН3, R2=H, R3=H (Iб), R=изо-С3H7, R1=СН3, R2=H, R3=CH3 (Iв), R=н-C4H9, R1=CH3, R2=H, R3=H (Iг), R=изо-С3Н7, R1=H, R2=H, R3=CH3 (Iд), R=изо-С3Н7, R1=H, R2=H, R3=COOC2H5 (Ie), R=втор-С4H9, R1=CH3, R2=H, R3=CH3 (Iж), которые могут найти применение в сельском хозяйстве для повышения устойчивости растений к неблагоприятным факторам окружающей среды. Способ включает взаимодействие соответствующих ароматических изоцианатов с алкиловыми эфирами β-аминоэтилкарбаминовой кислоты в инертном растворителе при комнатной температуре с последующим выделением целевых соединений формулы I известными приемами. Изобретение относится также к N-алкоксикарбониламиноэтил-N'-арилмочевинам общей формулы I, где R=втор-С4H9, R1=Н, R2=H, R3=СН3 (Ia), R=втор-С4H9, R1=СН3, R2=H, R3=H (Iб), R=изо-C3H7, R1=СН3, R2=H, R3=CH3 (Iв), R=н-С4Н9, R1=СН3, R2=H, R3=H (Iг), R=изо-C3H7, R1=H, R2=H, R3=CH3 (Iд), R=втор-С4H9, R1=CH3, R2=H, R3=CH3 (Iж), которые могут использоваться в качестве регуляторов роста растений антистрессового типа. 2 н. и 3 з.п. ф-лы, 7 табл., 5 пр.
Реферат
Настоящее изобретение относится к органической химии и агрохимии, в частности к новым замещенным мочевинам, а именно к N-алкоксикарбонил-(3-аминоэтил-N'-арилмочевинам общей формулы I
где
R=втор-C4H9, R1=Н, R2=H, R3=СН3 (Ia),
R=втор-C4H9, R1=CH3, R2=H, R3=H (Iб),
R=изо-C3H7, R1=СН3, R2=H, R3=CH3 (Iв),
R=н-C4H9, R1=СН3, R2=H, R3=H (Iг),
R=изо-C3H7, R1=H, R2=H, R3=СН3 (Iд),
R=изо-C3H7, R1=H, R2=H, R3=COOC2H5 (Ie),
R=втор-C4H9, R1=CH3, R2=H, R3=СН3 (Iж),
обладающим рострегулирующей активностью антистрессового типа, а также к способу их получения. Изобретение наиболее успешно может быть использовано в сельском хозяйстве для повышения устойчивости растений к неблагоприятным факторам среды, а именно для повышения морозоустойчивости и засухоустойчивости сельскохозяйственных культур.
Внедрение высокопродуктивных культур, использование широкого комплекса агротехнических мероприятий и внесение в почву оптимальных по количеству и по составу удобрений позволяет значительно повышать урожайность сельскохозяйственных культур. Однако выращенные в данных условиях растения оказываются очень чувствительными к поражению патогенными микроорганизмами и другими вредителями, а также к воздействию неблагоприятных погодных факторов. Следствием этого становится обязательная обработка вегетирующих растений инсектицидами и контактными фунгицидами. В зонах рискованного земледелия, к которым относится значительная часть посевных площадей России, важную роль в обеспечении стабильности сельскохозяйственного производства играют регуляторы роста растений с антистрессовыми свойствами.
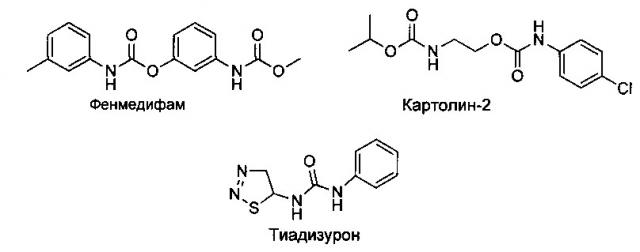
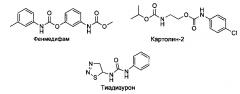
Известно, что фитогормонами с антистрессовыми свойствами являются цитокинины, например зеатин - замещенный по аминогруппе гидроксиизопентенильной группой аденин. Незначительная цитокининовая активность обнаружена у дифенилмочевины. До настоящего времени цитокининовая активность синтетических соединений использовалась преимущественно для получения дефолиантов (тиадиазурон, цитодеф) и гербицидов (фенмедифам и другие соединения с двумя карбаматными группами на основе 3-аминофенола). Переход к бискарбаматам на основе этаноламина привел к появлению регуляторов роста растений антистрессового действия, защищающих их от избытка солей в почвах, недостатка влаги и заморозков (картолин-2) (Авт. свид. СССР №1387946, БИ №14, 1988; Баскаков Ю.А. Новый антистрессовый препарат цитокининового типа действия II Агрохимия. 1988. №4. С. 103-105; Авт. свид. СССР №710545, БИ №3, 1980).
Способы получения синтетических аналогов ауксинов с дефолиантной активностью основаны на реакции аминозамещенных гетероциклов с арилизоцианатами. Образующиеся при этом несимметричные мочевины показывают определенное структурное сходство с естественными цитокининами. Можно предположить, что соединения с карбаматной и мочевинной структурными единицами, получаемые, например, на основе этилендиамина и других диаминных соединений, будут более эффективными регуляторами роста растений, поскольку прочность связывания их с соответствующими биомишенями будет достаточна для проявления у них дополнительных видов активности по сравнению с аналогичными бискарбаматными соединениями.
Задачей настоящего изобретения является создание новых производных арилмочевин, обладающих более высокой рострегулирующей активностью и обеспечивающих повышенную устойчивость растений к неблагоприятным условиям среды.
Поставленная задача решается заявляемыми соединениями общей формулы I
где
R=втор-C4H9, R1=Н, R2=H, R3=СН3 (Ia),
R=втор-C4H9, R1=CH3, R2=H, R3=H (Iб),
R=изо-C3H7, R1=СН3, R2=H, R3=CH3 (Iв),
R=н-C4H9, R1=СН2, R2=H, R3=H (Iг),
R=изо-C3H7, R1=H3, R2=H, R3=СН3 (Iд),
R=изо-C3H7, R1=H, R2=H, R3=COOC2H5 (Ie),
R=втор-C4H9, R1=CH3, R2=H, R3=СН3 (Iж),
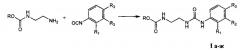
обладающими рострегулирующей активностью антистрессового типа, и способом их получения, который включает взаимодействие ароматических изоцианатов с алкиловыми эфирами β-аминоэтилкарбаминовой кислоты в среде инертного растворителя (схема 1).
Схема 1
Соединения I представляют собой бесцветные кристаллические вещества. Выходы соединений I, полученных заявляемым способом, температуры плавления и данные элементного анализа представлены в таблице 1.
Первичные испытания на выявление биологической активности проводили на культуре клеток табака, выращиваемой в строго контролируемых условиях. Эталоном в данном тесте служил картолин-2.
Как видно из табл. 2, все испытанные соединения оказывают значительное влияние на процессы обмена веществ в растительных клетках. Это выражается в существенной стимуляции роста клеток на фоне значительного подавления или стимуляции интенсивности метаболических процессов, связанных с дыханием.
Дальнейшие испытания, проведенные на целых растениях, иллюстрируют рострегулирующую активность соединений формулы I.
В табл. 3 представлены данные по влиянию соединений Iд, Iе на рост вегетативных органов фасоли и овса.
Из табл. 3 видно, что исследуемые соединения обладают способностью подавлять рост вегетативных органов однодольных и двудольных растений. Эта способность коррелируется с антистрессовой активностью, поскольку остановка роста является защитной реакцией растения на неблагоприятные условия среды.
Испытания действия заявленных соединений на засухоустойчивость проводили на яровой пшенице сорта Московская 35.
Для характеристики засухоустойчивости пшеницы использовали такие показатели, как:
а) водоудерживающая способность тканей проростков, которая определяется по потере воды при высушивании. Чем ниже этот показатель, тем выше водоудерживающая способность тканей и тем выше устойчивость растений к обезвоживанию;
б) количество выживших растений при обезвоживании, одинаковом для всех вариантов;
в) сухая масса растений после регенерации во влажной камере, которая характеризует биохимическую устойчивость к обезвоживанию. Чем выше этот показатель, тем выше устойчивость.
Действие соединений на засухоустойчивость определяли в нескольких опытах. Поскольку чувствительность растений к физиологическим воздействиям в разных опытах неодинакова, для сопоставления активности в каждый опыт вводили эталон - хлорхолинхлорид, который применяют на практике для повышения засухоустойчивости. Данный эталон служил нулевой точкой отсчета активности.
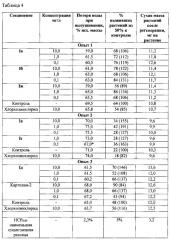
В табл. 4 приведены результаты изучения засухоустойчивости проростков пшеницы, данные по биологической активности представлены в абсолютных единицах. В табл.5 приведены те же данные, но интерпретированные для удобства сравнения по отношению к хлорхолинхлориду.
Из табл. 5 видно, что исследуемые соединения Ia-г превосходят картолин-2 и хлорхолинхлорид по способности повышать засухоустойчивость растений.
Испытания действия соединений формулы I на морозоустойчивость проводили на озимой пшенице сорта Ильичевка. В качестве аналогов для сравнения использовали картолин и хлорхолинхлорид. Результаты опытов на морозоустойчивость в абсолютных величинах представлены в табл. 6.
В табл. 7 приведены результаты сравнения активности заявляемых соединений формулы I с активностью хлорхолинхлорида на основании данных, представленных в табл. 6. Как видно из табл. 7 соединения Iд и Iе превосходят близкое по структуре соединение картолин-2.
Таким образом, было обнаружено, что производные мочевины формулы I, получаемые по реакции N-изопропоксикарбонилэтилендиамина с ароматическими изоцианатами, с разделенными этиленовым мостиком карбаматными и мочевинными функциональными группами оказались регуляторами роста растений с уникальными противострессовыми свойствами, превосходящими известные близкие структурные аналоги, например картолин-2.
Технический результат - получение новых производных мочевины, обладающих рострегулирующей активностью, превышающей активность аналогов, и обеспечивающих повышение устойчивости растений к неблагоприятным условиям среды и разработка способа получения указанных производных.
Пример 1. N'-(4-толил)-N-[2-(изопропоксикарбониламино)этил]мочевина (соединение Iд).
К 1,47 г (0,01 моль) изопропилового эфира β-аминоэтилкарбаминовой кислоты в 15 мл сухого бензола или толуола при перемешивании прибавляют 1,33 г (0,01 моль) 4-толилизоцианата. Образовавшийся осадок отфильтровывают, получают 2,7 г N'-(4-толил)-N-(2-изопропоксикарбониламино)этилмочевины (выход 98%) с т.пл. 183-184 С. Далее полученный осадок перекристаллизовывают из изопропилового спирта, получают 2,4 г (выход 79%) N-(4-толил)-N'-[2-(изопропоксикарбониламино)этил]мочевины Iд с т.пл. 185-186°С.
ИК-спектр (вазелиновое масло): 1691 см-1 и 1635 см-1 (С=0); 1235 см-1 (С-О-С); 1607 см-1 (арил); 1558 см-1 (амид). Приведенные полосы в ИК-спектре являются характеристическими для всех соединений формулы I.
Заявляемые соединения Iа, Iб, Iв, Iг, Iе и Iж получают по методике, приведенной в примере 1, из соответствующих ароматических изоцианатов и алкиловых эфиров β-аминоэтилкарбаминовой кислоты (табл. 1).
Пример 2. Первичные испытания на выявление биологической активности на культуре клеток.
Испытания соединений в качестве регуляторов роста растений проводят на культуре клеток табака, выращиваемой в строго контролируемых условиях (температура 26°С, модифицированная среда по Шнеку и Хильдебрандту). Испытания проводят при концентрации вещества 5⋅10-6 моль/л, показания снимают через 120 ч. Результаты приведены в табл. 2.
Примеры 3-5 иллюстрируют рострегулирующую активность соединений на целых растениях.
Пример 3. Влияние на рост вегетативных органов фасоли и овса.
В бумажные стаканчики емкостью 0,5 л, наполненные перлитом, высевают семена фасоли сорта Белозерная и овса сорта Орел. Растения выращивают на стеллажах с люминесцентными лампами в течение 10 дней. На вариант по два сосуда, на сосуд по 3-4 растения фасоли и по 10 растений овса, растения опрыскивают исследуемыми препаратами из расчета 4 мг действующего вещества на сосуд. Через две недели проводят учет, определяя суммарную массу растений овса и суммарную массу прироста после обработки у фасоли на вариант. Эталоном служит ингибитор роста ГМК (гидразидмалеиновая кислота). Результаты приведены в табл. 3.
Пример 4. Испытания действия заявляемых соединений на засухоустойчивость пшеницы.
Яровую пшеницу сорта Московская 35 выращивают 4 дня на водопроводной воде и 3 дня - на растворе исследуемого соединения. Далее растения пшеницы без корней и зерновки подвергают медленному высушиванию в термостате при 24°С, через сутки растения раскладывают на влажной фильтровальной бумаге во влажной камере и через 7 дней определяют число выживших растений в каждом варианте. Результаты приведены в табл. 4 и 5.
Пример 5. Испытание действия заявляемых соединений на морозоустойчивость пшеницы.
Озимую пшеницу сорта Ильичевка проращивают 3 дня в термостате и 7 дней выращивают в растворах исследуемых препаратов. Десятидневные растения пшеницы без корней, но с зерновками закаливают 7 дней при температуре 2°С, промораживают сутки при минус 5°С, оттаивают при комнатной температуре, заливают дистиллированной водой на 2 ч и определяют выход электролитов из убитых тканей. Отношение выхода электролитов из промороженных тканей к выходу электролитов из убитых тканей есть мера устойчивости тканей к отрицательным температурам. Чем ниже эта величина, тем выше устойчивость. Результаты приведены в табл. 6 и 7.
1. Способ получения N-алкоксикарбониламиноэтил-N'-арилмочевин общей формулы I
где R=втор-С4H9, R1=Н, R2=H, R3=СН3 (Ia), R=втор-С4H9, R1=СН3, R2=H, R3=H (Iб), R=изо-С3H7, R1=СН3, R2=H, R3=CH3 (Iв), R=н-C4H9, R1=CH3, R2=H, R3=H (Iг), R=изо-С3Н7, R1=H, R2=H, R3=CH3 (Iд), R=изо-С3Н7, R1=H, R2=H, R3=COOC2H5 (Ie), R=втор-С4H9, R1=CH3, R2=H, R3=CH3 (Iж), включающий взаимодействие соответствующих ароматических изоцианатов с алкиловыми эфирами β-аминоэтилкарбаминовой кислоты в инертном растворителе при комнатной температуре и выделение соответствующего целевого соединения формулы I известными приемами.
2. Способ по п.1, отличающийся тем, что в качестве растворителя используют бензол.
3. Способ по п.1, отличающийся тем, что в качестве растворителя используют толуол.
4. N-Алкоксикарбониламиноэтил-N'-арилмочевины общей формулы I
где R=втор-С4H9, R1=Н, R2=H, R3=СН3 (Ia), R=втор-С4H9, R1=СН3, R2=H, R3=H (Iб), R=изо-C3H7, R1=СН3, R2=H, R3=CH3 (Iв), R=н-С4Н9, R1=СН3, R2=H, R3=H (Iг), R=изо-C3H7, R1=H, R2=H, R3=CH3 (Iд), R=втор-С4H9, R1=CH3, R2=H, R3=CH3 (Iж).
5. Соединения по п.4 в качестве регуляторов роста растений антистрессового типа.